智能化控释载药骨水泥及其制备方法和应用与流程
本发明涉及生物医用材料技术领域,尤其是涉及一种智能化控释载药骨水泥及其制备方法和应用。
背景技术:
pmma骨水泥(polymethylmethacrylic,聚甲基丙烯酸甲酯)作为生物有机高分子骨水泥材料的典型代表,具有填充骨与假体间隙并具有聚合反应而自发凝固的特性,主要用于人工关节置换手术。向骨水泥中掺入抗生素,使之在植入部位局部形成高浓度抗生素环境,从而可以减少术后感染或治疗人工关节置换术后感染。
目前搭载抗生素的pmma骨水泥还存在以下缺陷:
1、药物释放不够完全,内部抗生素无法很好释放,造成浪费。
2、药物释放不能按需控释。
3、存在“突然释药”现象:现有商用含抗生素骨水泥在植入后,在植入初期会产生抗生素“突释”现象,因此在植入早期即会形成局部抗生素高浓度环境。但不是所有炎症或感染在植入初期产生。对植入后一段时间后才产生的感染或炎症,抗生素的初期大量释放造成了抗生素的浪费,继而无法起到及时的治疗效果,严重者可能面临二次翻修的风险。
此外,目前搭载抗生素的pmma骨水泥的生物活性有待进一步提高。
有鉴于此,特提出本发明。
技术实现要素:
本发明的目的之一在于提供一种智能化控释载药骨水泥,能够解决目前含抗骨水泥产品药物释放不可控问题,以及提高药物总体释放率和骨水泥生物活性。
本发明的目的之二在于提供一种智能化控释载药骨水泥的制备方法。
本发明的目的之三在于提供一种智能化控释载药骨水泥的应用。
为了实现本发明的上述目的,特采用以下技术方案:
第一方面,本发明提供了一种智能化控释载药骨水泥,包括粉剂和液剂;粉剂和液剂的液固比为1(ml):2-2.2(g);
其中,所述粉剂包括质量百分比的如下组分:
进一步的,所述抗生素在空心聚多巴胺纳米粒子/抗生素载药微球中的负载量为23-30%。
进一步的,所述抗生素包括庆大霉素、万古霉素、妥布霉素或克林霉素中的一种或几种,优选为庆大霉素、万古霉素、妥布霉素。
进一步的,所述空心聚多巴胺纳米粒子的粒径为100-300nm。
进一步的,所述液剂包括质量浓度的如下组分:
甲基丙烯酸甲酯单体98±1%;
促进剂2±0.5%;
阻聚剂70±10ppm。
进一步的,所述引发剂为过氧化苯甲酰;
优选地,所述显影剂为硫酸钡和/或二氧化锆;
优选地,所述促进剂为n,n-二甲基对甲苯胺;
优选地,所述阻聚剂为对苯二酚。
第二方面,本发明提供了上述智能化控释载药骨水泥的制备方法,包括以下步骤:
(a)制备空心聚多巴胺纳米粒子/抗生素载药微球;
(b)按配比将聚甲基丙烯酸甲酯、引发剂、空心聚多巴胺纳米粒子/抗生素载药微球和显影剂混合,获得粉剂;
(c)粉剂和液剂组成智能化控释载药骨水泥。
进一步的,步骤(a)包括以下步骤:
将空心聚多巴胺纳米粒子溶于含有抗生素的缓冲液中避光反应,分离后洗涤得到空心聚多巴胺纳米粒子/抗生素载药微球;
优选地,含有抗生素的缓冲液中抗生素浓度为0.1-0.3mg/ml。
进一步的,空心聚多巴胺纳米粒子的制备方法包括:
以sio2微球为模板,在碱性条件下使多巴胺在其表面氧化自聚形成壳层,除去模板后得到空心聚多巴胺纳米粒子;
优选地,空心聚多巴胺纳米粒子的制备方法包括以下步骤:
采用stober法合成sio2纳米粒子,将sio2纳米粒子分散于水中,得到分散液a;将盐酸多巴胺分散于分散液a中,再加入碱溶液,混合液变为黑色,混合反应后分离,产物洗涤、干燥;
将干燥后的产物分散于水中,加入氢氟酸,混合反应后分离,洗涤、干燥,得到空心聚多巴胺纳米粒子。
第三方面,本发明提供了一种上述智能化控释载药骨水泥在骨修复材料中的应用;
优选地,将粉剂和液剂按比例调和,得到待使用的骨水泥。
本发明提供的智能化控释载药骨水泥及其制备方法和应用具有如下有益效果:
1、本发明骨水泥中加入空心聚多巴胺纳米粒子/抗生素载药微球,聚多巴胺微球具有ph敏感性(ph响应),在人体正常环境下(ph=7.4)结构无变化,在酸性环境下(如感染位置局部ph≈5.0)结构失去稳定,易被降解,进而释放包埋在里面的药物,根据ph变化控释药物,达到按需释药。
2、本发明载药方式即包括空心聚多巴胺微球的物理包埋,也包括聚多巴胺和抗生素的化学结合(聚多巴胺上的邻苯二酚基团与上述抗生素的伯氨基极易发生席夫碱反应,以化学键的形式与聚多巴胺结合),因此,聚多巴胺作为载体载药量高且稳定。
3、空心聚多巴胺微球包埋药物且以化学键结合微球表面药物,比较稳定,可以防止药物过早释放,保证药物的有效利用。
4、通过控制加入空心聚多巴胺纳米粒子/抗生素载药微球在粉体中配比,不影响骨水泥本身的力学性能,同时改善了骨水泥的生物活性。
5、本发明的制备方法简单易行,所需原料少,反应步骤少。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
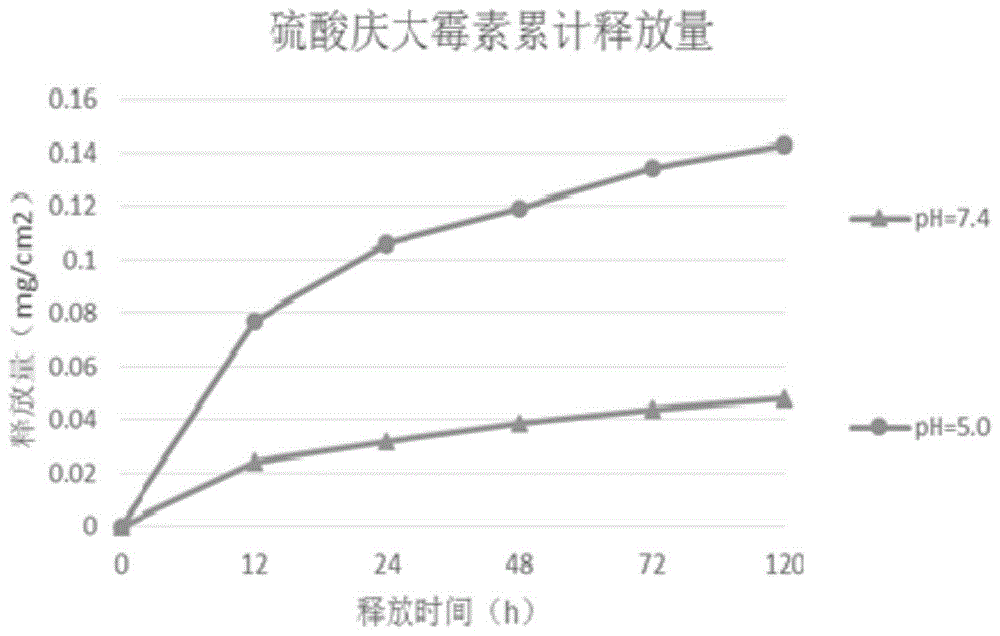
图1为本发明实施例提供的不同ph环境下药物释放测试对比结果图。
具体实施方式
下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
为防止搭载抗生素的pmma骨水泥的药物突释,并得到可控释药物的性能,解决微球类载体包埋药物率不高的问题,以及进一步改善骨水泥生物活性,继而提出本发明。
根据本发明的第一个方面,提供了一种智能化控释载药骨水泥,包括粉剂和液剂;粉剂和液剂的液固比为1(ml):2-2.2(g);
其中,所述粉剂包括质量百分比的如下组分:
pmma骨水泥包括粉体和液体,粉剂和液剂的液固比为1(ml):2-2.2(g),例如1ml:2g、1ml:2.1g、1ml:2.2g。
以粉剂为基准(100%计),聚甲基丙烯酸甲酯(pmma)典型但非限制性的含量例如为78.5%、79%、80%、80.5%。引发剂典型但非限制性的含量例如为0.4%、0.5%或0.6%。空心聚多巴胺纳米粒子/抗生素载药微球典型但非限制性的含量例如为9%、9.5%、10.5%、11%。显影剂典型但非限制性的含量例如为9%、9.5%、10.5%、11%。
[引发剂]
引发剂包括但不限于过氧化苯甲酰(bpo)。
引发剂用于粉剂和液剂混合时,引发聚甲基丙烯酸甲酯与甲基丙烯酸甲酯单体发生聚合反应直至固化。
[空心聚多巴胺纳米粒子/抗生素载药微球]
空心聚多巴胺纳米粒子/抗生素载药微球中“/”表示“和”的意思,是指抗生素包埋于空心聚多巴胺纳米粒子(微球)中,形成的一种载药微球。
微球包埋抗生素,主流抗生素均适用,例如庆大霉素、万古霉素、妥布霉素等市场上应用在骨水泥的主流抗生素。
对空心聚多巴胺纳米粒子不作限定,可以市购获得,也可以自行制备得到。
在一种实施方式中,空心聚多巴胺纳米粒子通过以下方式制备得到:
取100mg的sio2纳米粒子分散于30-50ml去离子水中,称取100-150mg的盐酸多巴胺分散于上述溶液中,再加入200-300μlnaoh(1m)溶液,混合液即变为黑色,室温下磁力搅拌反应10-12h后离心分离,产物用去离子水洗涤三次,冷冻干燥。
最后,将干燥完成的产物分散于30-50ml去离子水中,量取500μl的氢氟酸,充分混合反应2-4h,离心洗涤三次,冷冻干燥,即得空心的聚多巴胺纳米粒子。
其中sio2纳米粒子可以采用现有方法合成,例如采用stober法合成。
该方式以sio2微球为模板,在碱性条件下使多巴胺在其表面氧化自聚形成壳层,除去模板后得到空心聚多巴胺纳米粒子。
在一种优选的实施方式中,空心聚多巴胺纳米粒子的粒径为100-300nm。
对微球的载药方式不作限定。
在一种实施方式中,以庆大霉素为例,负载抗生素的步骤如下:
称取5-15mg硫酸庆大霉素溶于50ml现配的pbs溶液中(ph7.4),配制得0.1-0.3mg/ml溶液,避光存放;
称取3-6mg空心聚多巴胺基纳米粒子溶于5ml上述配制的溶液中避光搅拌6-12h,反应结束后离心保存,再用pbs缓冲溶液离心洗涤一次,除去未负载的抗生素。
在一种优选的实施方式中,抗生素在空心聚多巴胺纳米粒子/抗生素载药微球中的负载量为23-30%,例如23%、24%、25%、26%、27%、28%、29%或30%。
利用空心聚多巴胺纳米粒子微球的物理包埋及化学结合抗生素同时用于载药,除了物理包埋外,聚多巴胺上的邻苯二酚基团与抗生素的伯氨基极易发生席夫碱反应,以化学键的形式与聚多巴胺结合,因此聚多巴胺作为载体载药量高且稳定。药物包埋在聚多巴胺微球内部,且在微球表面上化学结合,包埋完全且化学结合稳定,防止释放过快过多,防止过早释放,保证药物的有效利用。因此可以起到防止初期药物突释,解决微球类载体包埋药物率不高的问题。
空心聚多巴胺纳米粒子/抗生素载药微球具有ph响应性,实现智能化控释。
ph响应原理:
当骨关节及其周围软组织产生感染时,感染部位局部组织由于血管收缩造成血液供应减少,进而引起血氧及营养物质缺乏,导致糖酵解增加,周围乳酸量也随之提高。最终导致感染部位局部ph值降低(可达到ph≈5.0左右),呈微酸性。
聚多巴胺微球,在人体正常环境下(ph=7.4)结构无变化,在酸性环境下(如感染位置局部ph≈5.0)结构失去稳定,易被生物降解,进而释放包埋在微球内部及结合在微球表面的药物,达到控释目的。
骨水泥中药物释放具有ph敏感性,根据局部环境ph值的变化,进而控制药物释放速率,达到按需释放。
[显影剂]
显影剂包括但不限于硫酸钡或氧化锆。
显影剂用于手术中便于观察。
进一步的,液剂包括质量浓度的如下组分:
甲基丙烯酸甲酯单体98±1%;
促进剂2±0.5%;
阻聚剂70±10ppm。
以液剂为基准,甲基丙烯酸甲酯单体典型但非限制性的含量例如为97%、97.5%、98.5%、99%。促进剂典型但非限制性的含量例如为1.5%、2%或2.5%。阻聚剂典型但非限制性的含量例如为60ppm、65ppm、75ppm、80ppm。
促进剂包括但不限于n,n-二甲基对甲苯胺。用于促进骨水泥聚化过程。
阻聚剂包括但不限于对苯二酚。用于阻止液剂中甲基丙烯酸甲酯自聚。
本发明解决了目前搭载抗生素的pmma骨水泥控释、突释问题,提高药物总体释放率。同时,不影响骨水泥本身力学性能的同时改善骨水泥生物活性。控制聚多巴胺载药微球在粉体中的配比,达到力学性能与药物控释性能之间的平衡。
根据本发明的第二个方面,提供了上述智能化控释载药骨水泥的制备方法,包括以下步骤:
(a)制备空心聚多巴胺纳米粒子/抗生素载药微球;
(b)按配比将聚甲基丙烯酸甲酯、引发剂、空心聚多巴胺纳米粒子/抗生素载药微球和显影剂混合,获得粉剂;
(c)粉剂和液剂组成智能化控释载药骨水泥。
进一步的,步骤(a)包括以下步骤:
将空心聚多巴胺纳米粒子溶于含有抗生素的缓冲液中避光反应,分离后洗涤得到空心聚多巴胺纳米粒子/抗生素载药微球;
优选地,含有抗生素的缓冲液中抗生素浓度为0.1-0.3%。
以庆大霉素为例,具体包括:
称取5-15mg硫酸庆大霉素溶于50ml现配的pbs溶液中(ph7.4),配制得0.1-0.3mg/ml溶液,避光存放;
称取3-6mg空心聚多巴胺基纳米粒子溶于5ml上述配制的溶液中避光搅拌6-12h,反应结束后离心保存,再用pbs缓冲溶液离心洗涤一次,除去未负载的抗生素。
进一步的,空心聚多巴胺纳米粒子的制备方法包括:
以sio2微球为模板,在碱性条件下使多巴胺在其表面氧化自聚形成壳层,除去模板后得到空心聚多巴胺纳米粒子,包括以下步骤:
采用stober法合成sio2纳米粒子,将sio2纳米粒子分散于水中,得到分散液a;将盐酸多巴胺分散于分散液a中,再加入碱溶液,混合液变为黑色,混合反应后分离,产物洗涤、干燥;
将干燥后的产物分散于水中,加入氢氟酸,混合反应后分离,洗涤、干燥,得到空心聚多巴胺纳米粒子。
具体包括:取100mg的sio2纳米粒子分散于30-50ml去离子水中,称取100-150mg的盐酸多巴胺分散于上述溶液中,再加入200-300μlnaoh(1m)溶液,混合液即变为黑色,室温下磁力搅拌反应10-12h后离心分离,产物用去离子水洗涤三次,冷冻干燥。
最后,将干燥完成的产物分散于30-50ml去离子水中,量取500μl的氢氟酸,充分混合反应2-4h,离心洗涤三次,冷冻干燥,即得空心的聚多巴胺纳米粒子。
本发明聚多巴胺载药微球制备条件温和,所需原料少、反应步骤少,整个制备方法简单易行。
根据本发明的第三个方面,提供了一种上述智能化控释载药骨水泥在骨修复材料中的应用。
优选地,将粉剂和液剂按比例调和,得到待使用的骨水泥。
需要说明的是,这里的骨水泥的使用方法是指填充入人体前的粉剂和液剂的调和阶段,此时待注射的骨水泥呈牙膏状或面团状,未完全固化,以待使用。因此,不涉及疾病的治疗方法。
下面通过实施例对本发明作进一步说明。如无特别说明,实施例中的材料为根据现有方法制备而得,或直接从市场上购得。
实施例中的抗生素以庆大霉素为例,空心聚多巴胺纳米粒子/抗生素载药微球按照如下方式制备得到:
取100mg的sio2纳米粒子分散于50ml去离子水中,称取135mg的盐酸多巴胺分散于上述溶液中,再加入250μlnaoh(1m)溶液,混合液即变为黑色,室温下磁力搅拌反应10h后离心分离,产物用去离子水洗涤三次,冷冻干燥。最后,将干燥完成的产物分散于50ml去离子水中,量取500μl的氢氟酸,充分混合反应2h,离心洗涤三次,冷冻干燥,即得空心的聚多巴胺纳米粒子。空心聚多巴胺纳米粒子的粒径为178±34nm。
称取15mg硫酸庆大霉素溶于50ml现配的pbs溶液中(ph7.4),配制得0.3mg/ml溶液,避光存放;称取6mg空心聚多巴胺基纳米粒子溶于5ml上述配制的溶液中避光搅拌8h,反应结束后离心保存,再用pbs缓冲溶液离心洗涤一次,除去未负载的抗生素。抗生素在空心聚多巴胺纳米粒子/抗生素载药微球中的负载量为24.7%。
实施例1
一种智能化控释载药骨水泥,包括粉剂和液剂;粉剂和液剂的液固比为1(ml):2.12(g)。
粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯79.5%、过氧化苯甲酰0.5%、空心聚多巴胺纳米粒子/抗生素载药微球10.0%、硫酸钡10.0%。
液剂包括质量浓度的如下组分:甲基丙烯酸甲酯单体98%、n,n-二甲基对甲苯胺2%、对苯二酚70ppm。
实施例2
一种智能化控释载药骨水泥,包括粉剂和液剂;粉剂和液剂的液固比为1(ml):2.15(g)。
粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯78.5%、过氧化苯甲酰0.6%、空心聚多巴胺纳米粒子/抗生素载药微球11%、硫酸钡9.9%。
液剂包括质量浓度的如下组分:甲基丙烯酸甲酯单体97.5%、n,n-二甲基对甲苯胺2.5%、对苯二酚60ppm。
实施例3
一种智能化控释载药骨水泥,包括粉剂和液剂;粉剂和液剂的液固比为1(ml):2.07(g)。
粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯80.5%、过氧化苯甲酰0.4%、空心聚多巴胺纳米粒子/抗生素载药微球9%、硫酸钡10.1%。
液剂包括质量浓度的如下组分:甲基丙烯酸甲酯单体98%、n,n-二甲基对甲苯胺2%、对苯二酚80ppm。
实施例4
一种智能化控释载药骨水泥,包括粉剂和液剂;粉剂和液剂的液固比为1(ml):2.09(g)。
粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯80%、过氧化苯甲酰0.5%、空心聚多巴胺纳米粒子/抗生素载药微球10.5%、硫酸钡9%。
液剂包括质量浓度的如下组分:甲基丙烯酸甲酯单体98.5%、n,n-二甲基对甲苯胺1.5%、对苯二酚75ppm。
实施例5-6
实施例5-6与实施例1的区别在于粉剂中空心聚多巴胺纳米粒子/抗生素载药微球的加入量不同,具体如下表1所示。
表1
对比例1
对比例1与实施例1的区别在于,粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯89.5%、过氧化苯甲酰0.5%、硫酸钡10.0%。
对比例2
对比例2与实施例1的区别在于,粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯74.5%、过氧化苯甲酰0.5%、空心聚多巴胺纳米粒子/抗生素载药微球15.0%、硫酸钡10.0%。
对比例3
对比例3与实施例1的区别在于,粉剂包括质量百分比的如下组分:聚甲基丙烯酸甲酯84.5%、过氧化苯甲酰0.5%、空心聚多巴胺纳米粒子/抗生素载药微球5.0%、硫酸钡10.0%。
试验例1不同ph环境下药物释放测试
试验样本:实施例1的骨水泥;
试验方法:
在(23±1)℃环境条件下混合一套骨水泥的粉体和液体,待混合后的骨水泥呈面团状时,将其仔细地填入75×10×3.3mm模具内,盖上顶板。并用c型夹子将顶板、底板和模具固定。1h后取下样条。
将制备的样品置于不同ph环境下(ph=7.4、ph=5.0)的pbs缓冲液中,密封并于37℃恒温放罝。于不同时间间隔(12h、24h、48h、72h、120h)自每一容器中取样。取出的样品溶液进行衍生化处理后采用hplc进样测量,并计算统计硫酸庆大霉素累计释放量。硫酸庆大霉素释放量结果用mg/cm2来表示。
试验结果:如图1所示。
由图1可以看出,本发明制得的智能化控释载药骨水泥在ph=5.0,即在微酸性环境下抗生素释放量相比在ph=7.4的正常体液环境下的抗生素释放量有了明显提高。显示出非常明显的ph响应药物控释特性。由此可以看出,空心聚多巴胺纳米粒子/抗生素载药微球可以根据感染位置ph变化控释药物。
试验例2骨水泥药物7天释放率测定
试验样本:实施例1-6的骨水泥;
试验方法:
在(23±1)℃环境条件下混合一套骨水泥的粉体和液体,待混合后的骨水泥呈面团状时,将其仔细地填入75×10×3.3mm模具内,盖上顶板。并用c型夹子将顶板、底板和模具固定。1h后取下样条。
将制备的样品置于不同ph环境下(ph=7.4、ph=5.0)的pbs缓冲液中,密封并于37℃恒温放罝。于不同时间间隔(12h、24h、48h、72h、120h)自每一容器中取样。取出的样品溶液进行衍生化处理后采用hplc进样测量,并计算统计骨水泥样品中硫酸庆大霉素7天释放率。硫酸庆大霉素释放率用%表示。
试验结果:如表2所示。
表2
由表2可以看出,与传统商用含抗生素骨水泥相比,本发明制得的智能化控释载药骨水泥在ph=5.0,即在微酸性环境下抗生素释放率有了明显提高,而在ph=7.4的正常体液环境下,抗生素释放率则较低,但普遍比商用含抗生素骨水泥的释放率低。证明本发明制得的智能化控释载药骨水泥显示出非常优异的ph响应性药物控释特性以及防止初期药物突释特性。
商用含抗生素骨水泥为depuy公司生产的smartsetgmvendurance骨水泥产品。
试验例3骨水泥力学性能测定
试验样本:实施例1-6、对比例1-3的骨水泥;
试验方法:对骨水泥的力学性能进行测试,具体测试方法:
抗压强度测试:在(23±1)℃环境条件下混合一套骨水泥的粉体和液体,待混合后的骨水泥呈面团状时,将其仔细地填入特定模具内,制备6×12mm规格的样柱。将测试样条放置于测试设备的静态压缩测试装置上,开动试验机在19.8mm/min–25.6mm/min的范围内用恒定的十字头速率对样品施加负载,当样品破裂或已过上屈服点时停止。
抗弯强度及抗弯模量测试:在(23±1)℃环境条件下混合一套骨水泥的粉体和液体,待混合后的骨水泥呈面团状时,将其仔细地填入特定模具内,制备75×10×3.3mm规格的样条。将测试样条放置于测试设备装置上,用弯曲试验机以5mm/min±1mm/min的十字头速率,从零开始在中央负载柱上加力,记录试条挠度随施力的变化情况,继续加力直至试条断裂。
试验结果:见表3。
表3
由表3可以看出,在粉体中加入空心聚多巴胺纳米粒子/抗生素载药微球后,骨水泥力学性能基本没有太大变化,可以证明空心聚多巴胺/抗生素载药微球的加入不影响骨水泥各项力学性能,测试结果均满足临床使用需求。且由于在粉体中加入的空心聚多巴胺/抗生素载药微球本身具有良好的生物相容性及可降解性,因此可以有效改善骨水泥的生物活性。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
- 还没有人留言评论。精彩留言会获得点赞!