MSC用于调控病毒性感染患者终末分化细胞基因表达的应用的制作方法
本发明涉及生物医药工程技术领域,尤其涉及一种msc用于调控病毒性感染患者终末分化细胞基因表达的应用。
背景技术:
病毒性感染是指能在人体寄生繁殖,并能致病的病毒引起的传染病。主要表现有发热、头痛、全身不适等全身中毒症状及病毒寄主和侵袭组织器官导致炎症损伤而引起的局部症状。病毒性感染患者体内易诱发细胞因子风暴,产生炎症反应,出现各种并发症。且病毒感染(如流感、sars、mers和埃博拉)在人类中快速传播,对人类健康造成了巨大的威胁。尤其是2020年在全世界大爆发的新型冠状病毒(covid-19病毒),对人类健康、经济造成了严重的损失。covid-19的病原已被证实是一种新型冠状病毒,现称为严重急性呼吸综合征冠状病毒2(sars-cov-2)。目前,针对该病毒的特效药及疫苗均未研发成功,sars-cov-2的出现给临床医生带来了一个艰难的治疗困境。大多数感染患者表现出非特异性症状,如发热、干咳和疲劳。多数患者预后良好,部分病情严重者可迅速发展为急性呼吸窘迫综合征、感染性休克、代谢性酸中毒、凝血功能障碍,甚至死亡。病人病情的恶化可能是由于体内的细胞因子风暴,鉴于sars-cov-2是一种引起全球大流行病的新型毒株迫切需要有效的靶向治疗,包括抗病毒和免疫疗法。
目前病毒感染疾病以及病毒性感染的并发症缺乏特异性治疗,以支持和对症治疗为主,抗病毒药物和激素治疗均无法起到有效治疗。通常是通过辅助手段减缓患者的症状,主要还是依靠患者自身的免疫力战胜病毒性感染及其并发症。病毒性感染的重症患者外周血cd4+和cd8+t细胞的数量常显著减少,部分患者免疫异常激活,出现细胞因子风暴综合征(css),进而导致肺脏等器官严重损害和死亡。目前主要应对是使用糖皮质激素。由于病毒性感染患者的免疫过度激活与免疫抑制转化迅速,激素使用有导致病毒清除延缓和继发感染等风险。
鉴于此,本发明提供了一种msc用于调控病毒性感染患者终末分化细胞基因表达的应用,通过msc对患者终末分化细胞亚群抗病毒相关细胞基因表达和终末分化细胞亚群凝血相关细胞基因表达进行调控以实现对病毒性感染患者并发症的有效治疗。
技术实现要素:
本发明的目的是提供一种msc用于调控病毒性感染患者终末分化细胞基因表达的应用,通过将msc制剂纳入到msc治疗组以对病毒性感染患者进行充质干细胞制剂和常规治疗的联合用药,实现对患者终末分化细胞亚群抗病毒相关基因表达和终末分化细胞亚群凝血相关细胞基因表达进行调控,从而达到对病毒性感染所诱发的并发症的有效治疗。
本发明中,一种msc用于调控病毒性感染患者终末分化细胞基因表达的应用,通过将msc应用于调控患者终末分化细胞亚群抗病毒相关基因表达和终末分化细胞亚群凝血相关基因表达,以实现对病毒性感染所诱发的并发症进行有效治疗。其中,所述病毒性感染所诱发的并发症是指急性呼吸窘迫综合症。
优选地,其应用步骤包括:
s1、制备msc制剂;
s2、筛选病毒性感染患者并进行分组,至少包括msc治疗组和常规治疗组;
s3、对常规治疗组中病毒性感染患者进行常规治疗,同时将所制备的msc制剂纳入常规治疗组的常规治疗方案中对msc治疗组中的病毒性感染患者进行联合治疗;
s4、利用单细胞测序技术分别对愈后患者的外周血单个核细胞进行采样分析,获取愈后患者终末分化细胞亚群抗病毒相关基因表达和终末分化细胞亚群凝血相关基因表达的情况。
优选地,所述msc制剂的制备方法包括:
s11、采集脐带并置于培养皿中,然后通过生理盐水对脐带组织进行清洗;
s12、将清洗完毕的脐带组织剪成小组织块并种植于培养皿中培养;
s13、去除培养皿中的培养液,然后通过生理盐水清洗后加入胰酶进行消化,直至培养皿中细胞消化完成后加入终止液终止消化,将细胞悬液转移至离心管中离心并弃上层清液,再用适量培养液重悬细胞并计数,最后根据计数结果将细胞悬液种植于新培养皿进行培养;
s14、去除步骤s13中新培养皿中的培养液,然后通过生理盐水清洗后加入胰酶进行消化,直至培养皿中细胞消化完成后加入终止液终止消化,再用细胞筛过滤并将过滤后的细胞悬液转移至离心管中计数离心弃上层清液,再配置细胞制剂悬液并加入细胞制剂悬液重悬细胞,最后将细胞悬液转移至转移袋中并放入低温环境中待取,从而完成msc制剂的制备;
s15、对步骤s14中制备的msc制剂进行合格检测。
优选地,所述步骤s4中的愈后患者包括msc治疗组治愈后的病毒性感染患者和常规治疗组治愈后的病毒性感染患者。
与现有技术比较,本发明通过对常规治疗组中的病毒性感染患者进行常规治疗的同时,将所制备的msc制剂纳入msc治疗组的病毒性感染患者中进行msc制剂和常规治疗的联合治疗(即将所制备的msc制剂纳入常规治疗方案中作为msc治疗组的联合治疗方案),实现对患者终末分化细胞亚群抗病毒相关基因表达和终末分化细胞亚群凝血相关细胞基因表达的有效调控,从而有效抑制了患者单核细胞的过度激活,实现了对病毒性感染患者并发症的有效治疗。
附图说明
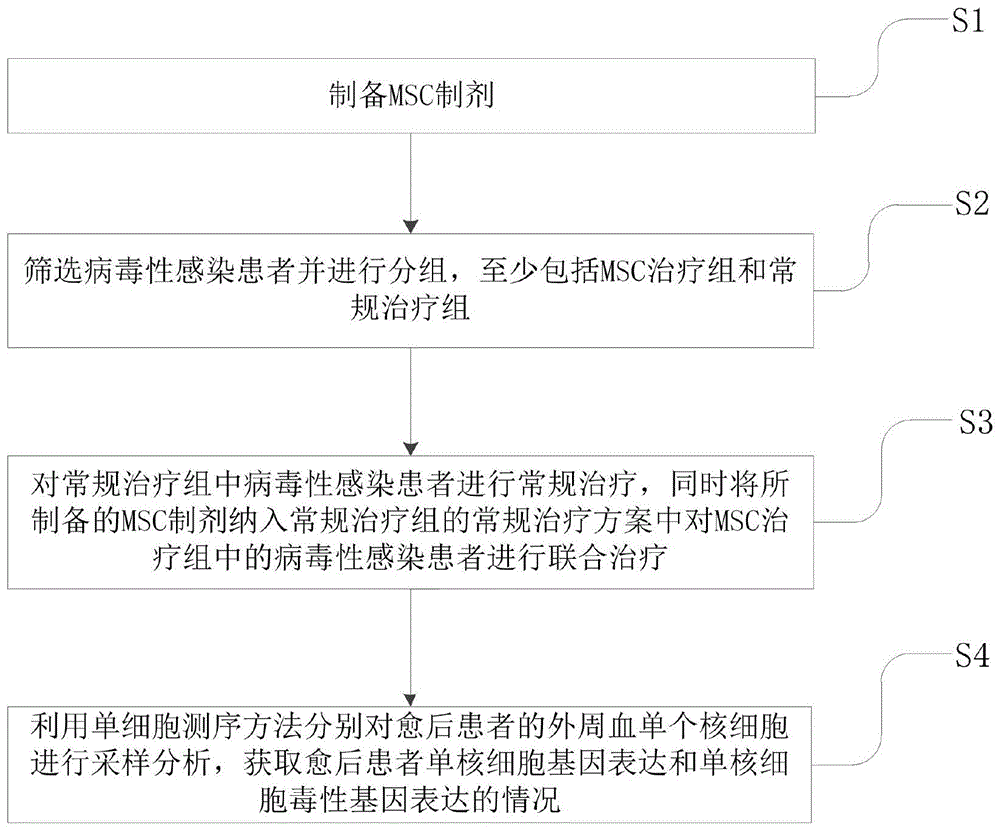
图1是本发明一种msc用于调控病毒性感染患者终末分化细胞基因表达的应用步骤流程图,
图2是本发明中msc制剂的制备方法流程图,
图3是本发明中所述外周血单个核细胞的20个亚群降维分析图,
图4是本发明msc治疗组、常规治疗组和健康组中的病毒性感染并发症患者的两个单核细胞亚群(mono4和mono5)示意图,
图5是本发明中msc治疗组、常规治疗组和健康组的cd14+细胞亚群中各差异基因所占比例的示意图,
具体实施方式
为了使本技术领域的人员更好地理解本发明的技术方案,下面结合附图对本发明作进一步的详细说明。
需要说明的是,本发明中所述原有治疗方案指的是国家卫生健康委员会办公厅和国家中医药管理局办公室印发的新型冠状病毒肺炎诊疗方案中所采取的治疗方案,msc+表示msc治疗组,msc-表示常规治疗组,healthy表示健康组,其中,msc(mesenchymalstemcells)表示间充质干细胞。
如图1所示,msc用于调控病毒性感染患者终末分化细胞基因表达的应用,通过将msc应用于调控患者终末分化细胞亚群抗病毒相关基因表达和终末分化细胞亚群凝血相关基因表达,以实现对病毒性感染所诱发的并发症进行有效治疗。其中,所述病毒性感染所诱发的并发症是指急性呼吸窘迫综合症,其应用的具体步骤包括:
s1、制备msc制剂;
s2、筛选病毒性感染患者并进行分组,至少包括msc治疗组和常规治疗组;
s3、对常规治疗组中病毒性感染患者进行常规治疗,同时将所制备的msc制剂纳入msc治疗组并对msc治疗组中的病毒性感染患者进行联合治疗;
s4、利用单细胞测序技术分别对愈后患者的外周血单个核细胞进行采样分析,获取愈后患者终末分化细胞亚群抗病毒相关基因表达和终末分化细胞亚群凝血相关基因表达的情况。
如图2所示,所述msc制剂的制备方法包括:
s11、采集脐带并置于培养皿中,然后通过生理盐水对脐带组织进行清洗;
s12、将清洗完毕的脐带组织剪成小组织块并种植于培养皿中培养;
s13、去除培养皿中的培养液,然后通过生理盐水清洗后加入胰酶进行消化,直至培养皿中细胞消化完成后加入终止液终止消化,将细胞悬液转移至离心管中离心并弃上层清液,再用适量培养液重悬细胞并计数,最后根据计数结果将细胞悬液种植于新培养皿进行培养;
s14、去除步骤s13中新培养皿中的培养液,然后通过生理盐水清洗后加入胰酶进行消化,直至培养皿中细胞消化完成后加入终止液终止消化,再用细胞筛过滤并将过滤后的细胞悬液转移至离心管中计数离心弃上层清液,再配置细胞制剂悬液并加入细胞制剂悬液重悬细胞,最后将细胞悬液转移至转移袋中并放入低温环境中待取,从而完成msc制剂的制备;
s15、对步骤s14中制备的msc制剂进行合格检测。
本实施例中,所述msc制剂采用人脐带间充质干细胞(humanumbilicalcordmesenchymalstemcells,huc-msc)制备而成,其制备过程均在消毒后的超净台中进行,且制备过程中所需器具和耗材等均需要75%酒精进行消毒,在制备过程中还需要对培养皿中的采集物或细胞以及操作具体过程进行详细标注;同时,在步骤s13和步骤s14之间还可以对干细胞进行冻存,若需要进行步骤s14干细胞制剂制备之前需要对冻存的干细胞进行复苏,其中干细胞冻存和复苏操作均属于现有技术,此处不再一一赘述。
本实施例中,对所述msc制剂进行合格检测还包括采集物质量检测、脐带间充质干细胞初级细胞库入库检测和脐带间充质干细胞主细胞库入库检测,合格检测的步骤与标准均与现有通行检测一致,此处不再一一赘述。
其中,所述步骤s3中的联合治疗是指:将步骤s1中所制备的msc制剂纳入msc治疗组中的联合治疗方案中,且msc制剂作为原有常规治疗方案中的唯一干扰因素对病毒性感染患者进行联合用药,同时在联合治疗方案中对联合用药情况进行跟踪记录。本实施例中,所述msc制剂中脐带间充质干细胞浓度为0.1×105-5×108细胞数/ml,在整个msc治疗组过程中msc制剂均采用外周静脉输注的方式并多次使用。其中使用次数可根据实际情况控制在1-10次之间。病毒性感染患者体内的单核细胞数量比健康人员体内更多,特别是cd14+单核细胞亚群(cd14+mono4和cd14+mono5,即cd14细胞第四亚群和cd14细胞第五亚群)在健康人员体内几乎没有发现,而cd14+mono5细胞亚群中的基因ifit1、基因ifit2、基因ifit3和基因isg15主要参与病毒防御进程,以及负责调控病毒基因组的复制和对干扰素α的细胞反应,同时cd14+mono4细胞亚群中的基因ppbp、基因pf4、基因treml1和基因pf4v1主要参与血小板脱粒进程,以及正向调控白细胞趋化性和对脂多糖反应,由此可知,在病毒性感染患者感染期间和并发症发生期间,细胞亚群cd14+mono5和cd14+mono5对于抗病毒、抗感染和凝血方面起着关键作用。
本实施例中,我们将所选择的普通型新冠阳性患者(即sars-cov-2病毒性感染患者)平均分成两组并作为msc治疗组样本和常规治疗组(即原有治疗方案)样本,待两组样本中的病毒性感染患者均治愈后再对愈后患者的外周血单个核细胞进行采样,然后利用单细胞测序技术分别对各组愈后患者所采集的外周血单个核细胞样本(即病毒性感染患者并发症的细胞样本)进行分组分析处理,得到msc治疗组和常规治疗的组愈后患者体内的抗病毒相关基因表达量和凝血功能相关基因表达量,具体情况如下:表1示出了单核细胞在msc治疗组和常规治疗组中抗病毒相关基因表达量,表2示出了msc治疗组与常规治疗组中对抵御病毒最有效的i型干扰素信号通路和抗病毒相关基因表达量,表3示出了msc治疗组和常规治疗组中凝血功能相关基因表达量。其中,需要说明的是,表中的p值小于0.01时表示msc治疗组与常规治疗组之间的数据具有显著差异,数据越小,其差异越大。
表1单核细胞在msc治疗组和常规治疗组中抗病毒相关基因表达量
表2示出了msc治疗组与常规治疗组中i型干扰素信号通路和抗病毒相关基因表达量
从表1、表2、图3、图4和图5中可以看出,cd14+mono5细胞亚群在健康人员体内几乎没有发现,因而可以说明单核细胞中的cd14+mono5细胞亚群只存在于病毒性感染患者体内,而且,在msc治疗组中cd14+mono5细胞亚群所占比例为1.4%,而常规治疗组中的cd14+mono5细胞亚群所占比例为6.0%,同时,与常规治疗组比较,msc治疗组中参与i型干扰素信号通路和抗病毒反应的一系列基因(如基因ifit1、基因ifit2、基因ifit3和基因isg15)的基因表达水平明显较低,msc治疗组的cd14+mono5细胞亚群的基因表达水平也较低。
表3msc治疗组和常规治疗组中凝血功能相关基因表达量
从表2、表3、图3、图4和图5中可以看出,cd14+mono4细胞亚群在健康人员体内几乎没有发现,因而说明了单核细胞中的cd14+mono4细胞亚群也只存在于病毒性感染患者体内,而且,在msc治疗组中cd14+mono4细胞亚群所占比例为3.3%,而常规治疗组中的cd14+mono5细胞亚群所占比例为5.3%,同时,与常规治疗组相比较,msc治疗组中参与i型干扰素信号通路的基因表达水平明显较低,msc治疗组的cd14+mono4细胞亚群的基因表达水平也较低。
综上所述,msc能够抑制病毒性感染患者体内单核细胞的过度激活,对于单核细胞从过度激活中恢复是极为有利的,通过msc能够有效抑制病毒性感染患者体内激活的单核细胞数(包括表达抗病毒相关基因的mono5和表达凝血相关基因的mono4),以及调控炎症基因的基因表达水平。因此,通过msc调控病毒性感染患者终末分化细胞基因表达能够改善病毒性感染患者的临床症状,大大降低了患者的死亡率,对于病毒性感染所诱发的并发症能够起到有效的治疗。
需要说明的是,在表1、表2、表3中,当avg-logfc值为正值时,表示该基因在msc治疗组中的表达量相对于常规治疗组上调,当avg-logfc值为负值时,表示该基因在msc治疗组中的表达量相对于常规治疗组下调,当p值小于0.05时,表示msc治疗组和常规治疗组中的基因表达量具有显著差异。
以上对本发明所提供的msc用于调控病毒性感染患者终末分化细胞基因表达的应用进行了详细介绍。本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!