盐酸去亚甲基小檗碱在制备预防或治疗克罗恩病药物中的应用的制作方法
本发明涉及生物医药领域,具体涉及盐酸去亚甲基小檗碱在制备预防或治疗克罗恩病药物中的应用。
背景技术:
克罗恩病(crohn'sdisease,cd)是胃肠道系统中的一种慢性复发性炎症疾病,病变可累及胃肠道各部位,以末端回肠及其邻近结肠为主,具有节段性、不对称性及透壁性等特点。cd病人临床表现出腹痛、便血、体重减轻、疲惫等症状,组织学标志为上皮样肉芽肿。从历史上看cd在西方国家中最为普遍,但目前在亚洲和拉丁美洲的国家中,cd的发病率也在上升。如果不加治疗,除了会引起一系列并发症外,cd患者的肠内和肠外患有恶性肿瘤的风险也将增加。cd确切的发病机制尚未研究清楚,可能是由遗传因素、环境因素和肠道菌群之间的相互作用导致异常粘膜免疫反应及上皮屏障功能受损而引发。传统观念认为,克罗恩病中异常免疫反应主要是由辅助性t细胞th1/th2细胞轴免疫偏倚导致,是一种以th1型免疫反应占主导的自身性免疫疾病,但是后来研究发现th17/treg细胞导致的免疫偏倚也起着重要的作用。th17主要分泌il-17而促进炎症的发生,导致免疫激活。th17/treg细胞之间平衡的打破及其导致的细胞因子微环境的改变是自身性免疫疾病发生的重要原因。treg细胞主要通过分泌白细胞介素(interleukin,il)10和转化生长因子β(transforminggrowthfactorβ,tgf-β)抑制自身性免疫t细胞的活化,从而诱导免疫耐受。除了上述免疫因子紊乱外,在cd患者中常存在较高水平的il-1β,其可诱导粒细胞的募集以及先天淋巴样细胞、树突状细胞、巨噬细胞的积累和活化,同时可与其他细胞因子协同作用刺激th17细胞的分化。il-1β的增多可能与tlr4/md2通路的激活相关,在cd患者中md2蛋白表达增多。在富含细菌的肠腔中,md2的表达增多会诱发产生严重的炎症反应,在cd发病期间起关键作用。
目前临床上常见的治疗cd方式有:1、药物治疗:1)皮质类固醇类药:布地奈德、泼尼松;2)免疫抑制剂:硫嘌呤类药物,硫唑嘌呤和巯基嘌呤;3)生物制剂:英夫利昔单抗、维多珠单抗;4)抗生素:抗生素的使用仅限于克罗恩病并发瘘管或脓肿。2、营养疗法:营养支持是控制克罗恩病患者体重减轻或营养不良的关键因素。3、手术:患有并发症(脓肿或恶性肿瘤)或不耐受药物治疗的克罗恩病患者适合进行手术。药物治疗的进步,使克罗恩病的疗效明显提高,但从目前的状况看,药物治疗仍不能代替外科治疗,半数以上的病人最终仍需手术。但是手术后患者如不进行后期维持治疗,其3年的复发率高达80~100%。目前治疗克罗恩病多采用逐级递增方案,该方案虽能避免不良反应大的药物,如糖皮质激素和免疫调节剂给机体带来的毒副作用,但仍无法根治。因此,研发安全有效的治疗克罗恩病的药物已成为当前药物研究的热点领域之一。
盐酸去亚甲基小檗碱,又名去亚甲基小檗碱盐酸盐或脱亚甲基小檗碱盐酸盐,如式(ⅰ)所示。
盐酸去亚甲基小檗碱(式ⅰ)的英文名为demethyleneberberinehydrochloride或demethyleneberberinechloride。本发明专利将它简称为dmb。式(ⅰ)中的骨架结构为去亚甲基小檗碱,它是盐酸去亚甲基小檗碱的活性成份。国际纯粹与应用化学联合会(iupac)将式(ⅰ)中的有机结构部分去亚甲基小檗碱命名9,10-dimethoxy-5,6-dihydroisoquinolino[2,1-b]isoquinolin-7-ium-2,3-diol,其中文名为9,10-二甲氧基-5,6-二氢异喹啉[2,1-b]异喹啉-7-鎓-2,3-二羟基。它的分子式:c19h18no4+,分子量为:324.35。化学文摘号(cas)为:25459-91-0。去亚甲基小檗碱可以与无机酸或有机酸形成多种盐,如氯化盐、硫酸盐、磷酸盐、溴化盐、碘化盐、枸橼酸盐、延胡索酸盐、马来酸盐、苹果酸盐和琥珀酸盐等分子形式存在。
去亚甲基小檗碱存在于天然药用植物芸香科植物黄柏(cortexphellodendrichinensis)中,安全性较高,但由于含量较低,相关活性研究很少。有报道认为它在体外对多种革兰氏阳性及阴性菌均具有抑制作用,可治疗多种疾病但尚未见有关盐酸去亚甲基小檗碱治疗克罗恩病的相关报道。
技术实现要素:
为了克服现有技术的不足,本发明的目的在于提供一种预防性治疗克罗恩病的化合物,特别是提供了如式(ⅰ)所示的盐酸去亚甲基小檗碱(dmb)作为预防性治疗克罗恩病的药物应用。
2,4,6-三硝基苯磺酸(tnbs)是一种有机弱酸,其作为一种化学性半抗原,常被用来制作克罗恩病模型。单独应用tnbs无法引发机体免疫反应,故常与乙醇合并灌肠造模。目前研究认为其造模机制可能为:乙醇溶解肠黏膜表面粘液破坏肠道屏障,促进tnbs进入结肠黏膜后,与赖氨酸第五个碳原子上的氨基共价结合,改变细胞表面蛋白,从而引起迟发型过敏反应和炎症反应。该模型与人类的克罗恩病症状表现近似,在造模前无需预先致敏动物或进行外科手术,是经典的人类克罗恩病模型。因此本项目成功地通过大鼠灌肠tnbs乙醇水溶液制备大鼠克罗恩病模型,考察盐酸去亚甲基小檗碱对克罗恩病的预防性治疗作用并探讨其抗炎免疫调节的作用机理。髓样分化抗原2(md2)与细胞表面受体tlr4作用,识别微生物相关分子lps引起炎症因子il-1β等表达。克罗恩病患者的血清中md2含量较高,此外患者肠道菌群常发生紊乱。由此可推测肠道菌群紊乱导致md2过度活化引发tlr4通路过度激活,造成cd患者严重的炎症反应。研究结果表明,盐酸去亚甲基小檗碱(dmb)可能通过作用于tlr4/md2通路降低炎症,对tnbs诱导的克罗恩病具有很好的治疗作用。
本发明以sd大鼠为实验动物,通过预防性给药治疗,考察盐酸去亚甲基小檗碱(dmb)对tnbs诱导的克罗恩病的预防性治疗作用。预防性治疗方案是:造模前及造模期间,灌胃不同剂量dmb,每天一次,共23天,给药组分别设置了200mg/kg(ig)和100mg/kg(ig)高低两个剂量组。第14天开始禁食40小时后将含有40mg/kg的tnbs、25%乙醇溶液灌肠。灌肠体积为:4ml/kg。造模前后每天记录大鼠饮食和体重变化,观察大鼠状态,造模结束后继续给药治疗7天,然后脱颈处死大鼠。实验结果分析表明,dmb低、高剂量治疗组均能显著提升tnbs造模的大鼠生存率,并且在造模后期改善大鼠摄食量和疾病活动指数。根据结肠组织实物图及结肠长度和结肠指数显示,dmb对tnbs诱导的克罗恩病具有明显的保护作用,能够改善结肠组织萎缩,水肿和肠组织粘连,促进肠道滞留粪便成型。此外,与模型组相比,从结肠组织h&e染色及结肠组织髓过氧化物酶(mpo)含量可以看出,dmb低、高剂量组均能有效的降低结肠中性粒细胞的浸润,起到抗炎作用,同时dmb能够降低结肠病变范围、维持结肠组织结构完整性。结肠组织丙二醛(mda)、谷胱甘肽(gsh)和一氧化氮(no)检测提示在tnbs造模中存在显著的结肠脂质过氧化及炎症反应,同时促炎因子il-1β、tnf-α的基因表达水平增高,但dmb给药组具有显著的抑制脂质过氧化及抗炎生物学活性。这些实验结果充分地说明了盐酸去亚甲基小檗碱(dmb)能够从抗炎抗氧化水平有效地预防性治疗tnbs诱导的克罗恩病。而对于dmb的作用位点研究,本发明通过分子对接软件预测了dmb与md2蛋白之间的作用位点,并构建md2蛋白的真核细胞表达载体pcdna3.1(+)-md2,且对作用位点进行定点突变进行药效评价从而确定dmb的可能作用位点。实验结果表明:dmb可能通过作用于md2蛋白的第23位色氨酸、76位苯丙氨酸、102位酪氨酸发挥抗炎作用。由此推断,dmb通过作用于md2蛋白,抑制下游炎症信号-传导进而治疗tnbs诱导的cd。
同时鉴于tnbs是一种化学性半抗原,可诱发机体发生免疫反应进而导致肠道结构损伤和免疫细胞类型改变,故本发明在检测dmb抑制固有免疫及抗炎水平之外,还检测了dmb对于获得性免疫细胞分型变化的调节,实验结果表明:th1型细胞特异性转录因子t-bet及特异性细胞因子ifn-γ在tnbs诱导后显著上调,提示可能存在th1型免疫反应,与此同时th2型细胞转录因子gata-3和特异性细胞因子il-12在tnbs模型中显著下调,这提示在tnbs模型中存在着th1/th2型免疫反应的紊乱。在th17/treg细胞分型检测中本发明以同样方法检测,发现th17细胞转录因子rorγt及其特异性细胞因子il-17在tnbs组中高表达,而treg细胞转录因子foxp3及其特异性细胞因子tgf-β1在tnbs组中低表达,dmb对于上述th1/th2、th17/treg细胞分型紊乱存在显著的调节作用。由此表明dmb可通过调节免疫细胞紊乱治疗tnbs诱导的cd。
本发明所用盐酸去亚甲基小檗碱(dmb)产品采用常规化学制备与分离纯化法制得。本实验室采用高效液相色谱(hplc)分析检测,其纯度达98%以上,并经化学法、红外色谱法、质谱(ms)法和核磁共振(1h-nmr)法分析鉴定,表明本研究所用盐酸去亚甲基小檗碱(dmb)产品化学结构正确。此项研究表明盐酸去亚甲基小檗碱(dmb)其纯度和化学结构符合开展体内、外生物学活性和药理作用研究要求。
本发明还涉及含有作为活性成份的盐酸去亚甲基小檗碱和常规药物赋形剂或辅剂的药物组合物。通常本发明药物组合物含有0.1~95%重量的盐酸去亚甲基小檗碱。在单元剂型中本发明化合物一般含量为0.1~100mg。
本发明化合物的药物组合物可根据本领域公知的方法制备。用于此目的时,如果需要,可将本发明化合物与一种或多种固体或液体药物赋形剂和/或辅剂结合,制成可作为人药或兽药使用的适当的施用形式或剂量形式。
本发明化合物或含有它的药物组合物可以单位剂量形式给药,给药途径可为肠道或非肠道,如口服、肌肉、皮下、鼻腔、口腔黏膜、皮肤、腹膜或直肠等。
本发明化合物或含有它的药物组合物的给药途径可为注射给药。注射包括静脉注射、肌肉注射、皮下注射、皮内注射和穴位注射等。
给药剂型可以是液体剂型、固体剂型。如液体剂型可以是真溶液类、胶体类、微粒剂型、乳剂剂型、混悬剂型。其他剂型例如片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、栓剂、冻干粉针剂等。
本发明化合物可以制成普通制剂、也可以是缓释制剂、控释制剂、靶向制剂及各种微粒给药系统。
例如为了将单位给药剂型制成片剂,可以广泛使用本领域公知的各种载体。关于载体的例子是,例如稀释剂与吸收剂,如淀粉、糊精、硫酸钙、乳糖、甘露醇、蔗糖、氯化钠、葡萄糖、尿素、碳酸钙、白陶土、微晶纤维素、硅酸铝等;湿润剂与粘合剂,如水、甘油、聚乙二醇、乙醇、丙醇、淀粉浆、糊精、糖浆、蜂蜜、葡萄糖溶液、阿拉伯胶浆、明胶浆、羧甲基纤维素钠、紫胶、甲基纤维素、磷酸钾、聚乙烯吡咯烷酮等;崩解剂,例如干燥淀粉、海藻酸盐、琼脂粉、褐藻淀粉、碳酸氢钠与枸橼酸、碳酸钙、聚氧乙烯山梨醇脂肪酸酯、十二烷基磺酸钠、甲基纤维素、乙基纤维素等;崩解抑制剂,例如蔗糖、三硬脂酸甘油酯、可可脂、氢化油等;吸收促进剂,例如季铵盐、十二烷基硫酸钠等;润滑剂,例如滑石粉、二氧化硅、玉米淀粉、硬脂酸盐、硼酸、液体石蜡、聚乙二醇等。还可以将片剂进一步制成包衣片,例如糖包衣片、薄膜包衣片、肠溶包衣片,或双层片和多层片。
例如为了将给药单元制成丸剂,可以广泛使用本领域公知的各种载体。关于载体的例子是,例如稀释剂与吸收剂,如葡萄糖、乳糖、淀粉、可可脂、氢化植物油、聚乙烯吡咯烷酮、单硬脂酸甘油脂、高岭土、滑石粉等;粘合剂,如阿拉伯胶、黄蓍胶、明胶、乙醇、蜂蜜、液糖、米糊或面糊等;崩解剂如琼脂粉、干燥粉、海藻酸盐、十二烷基磺酸钠、甲基纤维素、乙基纤维素等。
例如为了将给药单元制成胶囊,将有效成份本发明化合物盐酸去亚甲基小檗碱与上述的各种载体混合,并将由此得到的混合物置于硬的明胶胶囊或软胶囊中。也可将有效成分本发明化合物制成微囊剂,混悬于水性介质中形成混悬剂,亦可装入硬胶囊中或制成注射剂应用。
例如,将本发明化合物盐酸去亚甲基小檗碱制成注射用制剂,如溶液剂、混悬剂溶液剂、乳剂、冻干粉针剂,这种制剂可以是含水或非水的,可含一种和/或多种药效学上可接受的载体、稀释剂、粘合剂、润滑剂、防腐剂、表面活性剂、分散剂、渗透压调节剂、增溶剂和ph调节剂。如稀释可选用水、乙醇、聚乙二醇、1,3-丙二醇、乙氧基化的异硬脂醇、多氧化的异硬脂醇、聚氧乙烯山梨醇脂、脂肪酸酯等。渗透压调节剂可以是氯化钠、甘露醇、甘油、葡萄糖、磷酸盐、醋酸盐等;增溶剂或助溶剂可以是泊洛沙姆、卵磷脂、羟丙基β-环糊精等;ph调节剂可以是磷酸盐、醋酸盐、盐酸、氢氧化钠等。如制备冻干粉针剂,还可以加入甘露醇、葡萄糖等作为支撑剂。
此外,如需要,也可以向药物制剂中添加着色剂、防腐剂、香料、矫味剂、甜味剂或香料等。这些辅料是本领域常用的。
本发明所用的无菌介质都可以通过本领域技术人员众所周知的标准技术制得。可将它们灭菌,例如通过经由细菌过虑器过滤、通过向组合物中加入灭菌剂、通过将组合物放射处理、或通过将组合物加热灭菌。还可以在临用前将它们制成无菌可注射介质。
为了达到用药目的,增加治疗效果,本发明的药物或药物组合物可用任何公知的给药方法给药。当然用于实施本发明化合物的给药途径取决于疾病和需要治疗的部位。因为本发明化合物的药动学和药效学特征会有某种程度的不同,因此在组织中获得治疗浓度的最优选方法是逐渐增加剂量并监测临床效果。对于这样的逐渐增加治疗剂量,初始剂量将取决于给药途径。
对于任何特定患者,本发明化合物药物组合物的给药剂量取决于许多因素,例如所要预防或治疗疾病的性质和严重程度,患者或动物的性别、年龄、性格及个体反应,给药途径、给药次数、治疗目的,因此本发明的治疗剂量可以有较大范围的变化。根据所治疗患者的病症,可能必须对剂量作出某些改变,并且在任何情况下,都由医师决定个体患者的合适剂量。
给药剂量是指不包括载体重量(当使用载体时)在内的化合物的重量。一般来讲,本发明中药学成分的使用剂量是本领域技术人员公知的。可以根据本发明化合物组合物中最后的制剂中所含有的实际药物剂量,加以适当的调整,以达到其治疗有效量的要求,完成本发明的预防或治疗目的。可以是单一剂量形式给药或分成几个,例如二、三或四个剂量形式给药;这受限于给药医生的临床经验以及包括运用其它治疗手段的给药方案。本发明的化合物或组合物可单独服用,或与其他治疗药物或对症药物合并使用并调整剂量。
去亚甲基小檗碱既是药用植物中芸香科植物黄柏中存在的天然产物,又是小檗碱在体内肝脏中的代谢产物,天然环保,无毒高效。本发明提供了盐酸去亚甲基小檗碱在预防性治疗克罗恩病中的用途。
术语
dmb:盐酸去亚甲基小檗碱
tnbs:2,4,6-三硝基苯磺酸
dai:疾病活动指数
ig:灌胃
mpo:髓过氧化物酶
mda:丙二醛
no:一氧化氮
gsh:谷胱甘肽
cd:克罗恩病
il-17:白介素17
tgf-β1:转化生长因子β1
rorγt:视黄酸相关的孤儿受体γt
foxp3:叉头状转录因子3
ifn-γ:干扰素γ
il-12:白介素12
t-bet:t-box转录因子
gata-3:gata转录因子
md2:淋巴细胞抗原96
附图说明
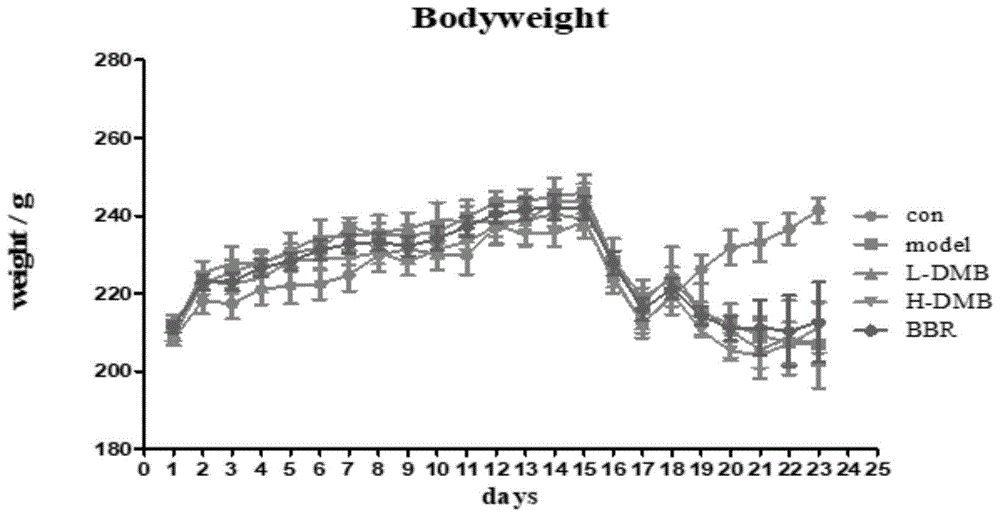
图1tnbs诱导的克罗恩病大鼠体重变化图
图2tnbs诱导的克罗恩病大鼠饮食变化图
图3dmb预防性治疗tnbs诱导的克罗恩病大鼠结肠组织形态图
图4dmb预防性治疗tnbs诱导的克罗恩病大鼠结肠长度散点图
图5dmb预防性治疗tnbs诱导的克罗恩病大鼠结肠组织微结构形态图
a:正常大鼠结肠组织he染色图(×200);
b:克罗恩病模型大鼠结肠组织he染色图(×200);
c:l-dmb100mg/kg组大鼠结肠组织he染色图(×200);
d:h-dmb200mg/kg组大鼠结肠组织he染色图(×200);
图6dmb预防性治疗tnbs诱导的克罗恩病大鼠结肠组织微结构形态图
a:正常大鼠结肠组织he染色图(×400);
b:克罗恩病模型大鼠结肠组织he染色图(×400);
c:l-dmb100mg/kg组大鼠结肠组织he染色图(×400);
d:h-dmb200mg/kg组大鼠结肠组织he染色图(×400);
图7dmb抑制tlr4信号通路中traf6、irf3蛋白的表达
图8dmb抑制lps刺激过表达md2的raw264.7细胞中促炎基因il-1β的表达,但对其作用位点突变后抑制作用下降
具体实施方式
下面的实施例可以帮助本领域的技术人员更全面地理解本发明,但不以任何方式限制本发明。
一、药理实验
实施例1.tnbs诱导的大鼠克罗恩病模型构建及大鼠死亡率检测
方法:对大鼠灌肠tnbs乙醇水溶液制备大鼠克罗恩病模型,用于评价dmb药效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有tnbs40mg/kg、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。造模后每天观察大鼠饮食和体重变化,同时记录大鼠状态,继续给药7天后处死大鼠,记录实验期间大鼠的死亡数目。
结果:死亡率如表1所示:模型组大鼠死亡2只,死亡率为25%,其死亡主要出现在造模后第4天,大鼠腹胀,未见排便,解剖显示存在严重的肠组织粘连和粪便潴留,低剂量组同样出现1例死亡,死亡率为12.5%,高剂量组大鼠未见死亡案例。
表1dmb预防性治疗对大鼠死亡率的影响
实施例2.dmb预防性治疗可减缓tnbs诱导的克罗恩病大鼠体重的下降并增加大鼠饮食量,改善大鼠疾病活动指数
方法:克罗恩病患者多出现明显的体重下降。本实验通过观察dmb对tnbs造模的大鼠体重下降有无减缓或抑制作用,从表观水平评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有tnbs40mg/kg、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。实验期间每天记录大鼠体重。在处理动物前一天检查大鼠大便性状和便隐血等,综合评估大鼠疾病活动指数。
结果:体重变化如图1,模型组大鼠体重从tnbs造模结束后持续下降,但给药治疗组tnbs造模后期体重上升。摄食量变化如图2,给药治疗组与模型组相比,摄食量得到恢复。在造模结束前一天,综合各组大鼠体重,大便性状及便血情况可知,tnbs造模后疾病活动指数显著上升,dmb两个治疗组均能明显降低大鼠疾病活动指数,结果如下表2所示。
表2dmb预防性治疗对tnbs诱导的克罗恩病大鼠dai指数的影响(n=8,mean±sd)
(*p<0.05,**p<0.01,***p<0.001vsmodel;#modelvscontrol)
实施例3.dmb预防性治疗可改善tnbs诱导的克罗恩病大鼠结肠指数
方法:克罗恩病患者结肠多出现明显的增生,导致结肠指数增加。本实验通过观察dmb对tnbs造模的大鼠结肠指数有无降低作用,评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有40mg/kgtnbs、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。实验结束后取各组大鼠结肠组织,清理肠内粪便残留物,称取结肠组织总重,计算结肠指数(结肠指数=结肠重量/体重*100%)。
结果:如下表3,经tnbs造模后大鼠结肠指数较对照组显著上升,dmb预防性治疗后可显著改善结肠指数。结肠组织形态、长度变化如图3、图4。
表3dmb预防性治疗对克罗恩病大鼠结肠指数的影响(n=8,mean±sd)
(*p<0.05,**p<0.01,***p<0.001vsmodel;#modelvscontrol)
实施例4.dmb预防性治疗可保护tnbs诱导的克罗恩病结肠病理组织损伤
方法:克罗恩病是一种慢性结肠炎性疾病,患者结肠组织损伤严重。本实验通过检测dmb对tnbs造模的大鼠结肠损伤有无抑制作用,评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有40mg/kgtnbs、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。实验结束后取各组大鼠同一部位结肠组织,以10%的中性福尔马林液固定,he染色进行病理学检查。
结果:如图5、图6所示,在显微视野下,正常组上皮细胞排列规则,杯状细胞较多,隐窝形态未见异常。与正常组相比模型组肠隐窝结构破坏,炎性细胞浸润增多,可见多处糜烂、溃疡形成,杯状细胞减少,粘膜层缺失,结肠粘膜固有层出现增厚现象,而给药治疗组以上形态得到改善。
实施例5.dmb预防性治疗可改善tnbs诱导的克罗恩病大鼠结肠组织炎症和过氧化水平。
方法:克罗恩病是一种慢性结肠炎性疾病,患者结肠组织炎症严重且抗氧化能力降低。本实验通过检测dmb对tnbs造模的大鼠结肠炎症有无抑制作用,评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有40mg/kgtnbs、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。取大鼠结肠组织,于冰上制备10%的结肠生理盐水匀浆,离心取上层匀浆液分别测定结肠组织髓过氧化物酶(mpo)、丙二醛(mda)、谷胱甘肽(gsh)及一氧化氮(no)含量,评价结肠组织炎症和过氧化水平。
结果:如下表4所示,tnbs造模能够显著诱导大鼠结肠组织mpo、no和mda含量上调,这提示tnbs造模能够诱导中性粒细胞向结肠组织浸润,同时加重结肠组织脂质过氧化和炎症反应,而抗氧化物质gsh在tnbs诱导的模型组中显著下调,提示机体自身的抗氧化系统出现了显著的抑制现象。dmb预防治疗组各项指标均有不同程度的改善,说明dmb可能从抗炎和抗氧化水平发挥治疗克罗恩病的作用。
表4dmb预防性治疗改善克罗恩病大鼠结肠组织炎症水平(n=8,mean±sd)
(*p<0.05,**p<0.01,***p<0.001vsmodel;#modelvscontrol)
实施例6.dmb预防性治疗对tnbs诱导的克罗恩病大鼠结肠炎症因子表达的影响
方法:克罗恩病患者通常结肠组织炎症因子表达紊乱。本实验通过检测dmb对tnbs造模的大鼠结肠炎症因子tnf-α和il-1β的表达有无抑制作用,评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有tnbs40mg/kg、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。准确称取大鼠结肠组织60mg,加入1mltrizol,提取结肠组织mrna,使用rt-pcr法检测结肠组织炎症因子tnf-α和il-1β的基因表达变化。
结果:实验结果如表5所示,模型组中tnf-α和il-1β基因表达上调,提示结肠组织存在显著的炎症反应,与此同时dmb治疗组能够显著的抑制tnf-α和il-1β基因过度表达,发挥抗炎活性。(表中,测量值的单位是以gapdh为内参基因的相对表达量。)
表5dmb预防性治疗对tnbs诱导的克罗恩病大鼠结肠炎症因子表达的影响(n=8,mean±sd)
(*p<0.05,**p<0.01,***p<0.001vsmodel;#modelvscontrol)
实施例7.dmb预防性给药可调节tnbs诱导的克罗恩病大鼠结肠th1/th2细胞平衡
方法:克罗恩病患者th1、th2细胞免疫平衡发生紊乱。本实验通过检测dmb对tnbs造模的大鼠结肠th1、th2细胞免疫平衡有无维持作用,评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有tnbs40mg/kg、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。使用trizol法提取大鼠结肠组织mrna,经逆转录后采用rt-pcr法检测th1和th2细胞特异性细胞因子及其转录因子基因表达水平,评估th1/th2细胞平衡。
结果:如表6所示,与对照组相比,模型组大鼠结肠组织th1相关细胞因子ifn-γ及其特异性转录因子t-bet基因表达水平显著升高。而th2细胞因子il-12及其转录因子gata-3在tnbs造模后显著下调,同时th1/th2细胞因子及转录因子比值极显著增高,这提示在tnbs模型中存在着th1/th2免疫细胞的紊乱,在dmb给药组,均能显著改善th1和th2细胞紊乱,且具有显著的剂量依赖性,高剂量给药组能够有效的维持机体免疫平衡水平。(表中,测量值的单位是以gapdh为内参基因的相对表达量。)
表6dmb预防性给药调节tnbs诱导的克罗恩病大鼠结肠th1/th2细胞平衡
(*p<0.05,**p<0.01,***p<0.001vsmodel;#modelvscontrol)
实施例8.dmb预防性给药可调节tnbs诱导的克罗恩病大鼠结肠th17/treg细胞平衡
方法:克罗恩病患者th17、treg细胞免疫平衡发生紊乱。本实验通过检测dmb对tnbs造模的大鼠结肠th17、treg细胞免疫平衡有无维持作用,评价药物是否有效。雌性spraguedawley(sd)大鼠,体重180-200克,随机分为四组,每组8只,分别为正常对照组(control)、tnbs模型组(model)、dmb低剂量给药组(l-dmb,100mg/kg,ig)和高剂量给药组(h-dmb,200mg/kg,ig)。给药组大鼠经灌胃给药dmb,每天一次,其余各组给予同体积的赋形剂。预防给药第14天开始禁食,40小时后使用水合氯醛麻醉大鼠(3.5ml/kg),大鼠头朝下45°,使用硅胶软管经肛门插入肠道7-8cm,缓慢灌肠注入含有tnbs40mg/kg、25%乙醇的水溶液。灌肠剂量为:4ml/kg体重,拔出软管后大鼠头朝下倒立1min,以防止药液流出。使用trizol法提取大鼠结肠组织mrna,经逆转录后采用rt-pcr法检测th17和treg细胞特异性细胞因子及其转录因子基因表达水平,评估th17/treg细胞变化。
结果:如表7所示,与对照组相比,模型组大鼠结肠组织th17相关细胞因子il-17及其特异性转录因子rorγt基因表达水平显著升高。而treg细胞因子tgf-β1及其转录因子foxp3在tnbs造模后显著下调,同时th17/treg细胞因子及转录因子比值显著增高,这提示在tnbs模型中同样存在着th17/treg细胞间的紊乱,但在dmb给药组,不同剂量dmb均能显著改善th17和treg细胞紊乱,且具有显著的剂量依赖性,高剂量给药组能够有效的维持机体免疫平衡水平。
表7dmb预防性给药调节tnbs诱导的克罗恩病大鼠结肠th17/treg细胞平衡
(*p<0.05,**p<0.01,***p<0.001vsmodel;#modelvscontrol)
二、生物活性试验
实施例9.盐酸去亚甲基小檗碱(dmb)作用于tlr4/md2通路发挥抗炎活性
方法:克罗恩病患者通常结肠组织炎症因子表达增多。tlr4/md2信号转导途径是常见的炎症通路之一,与cd的发病相关。tlr4信号通路下游有两条路径:1.myd88依赖性信号转导途径:脂多糖lps与md2作用后,引起tlr4蛋白的tir结构域与myd88的缔合从而引发irak1、irak4、traf6募集,并导致irak1和traf6的磷酸化,进而激活下游转录因子引发炎症。2.myd88非依赖性通路:脂多糖与md2作用后,引起tlr4蛋白与trif、tram作用,从而引发irf3的激活引起炎症。体外研究dmb作用于tlr4/md2通路的抗炎机制,将为开展dmb治疗cd提供理论基础。
本实施例中,以raw264.7为研究对象,细胞培养液中给与dmb20μm预处理12h,脂多糖lps刺激6h后收集细胞,ripa法提取细胞蛋白质,利用westernblot法检测dmb对tlr4/md2两条通路的抑制效应。
结果:westernblot法结果显示如图7,20μmdmb可抑制tlr4通路的两条路径。与脂多糖lps刺激组相比,不同剂量dmb给药组均降低了traf6、irf3的表达。推测dmb可作用于tlr4/md2通路发挥抗炎活性从而治疗tnbs诱导的cd。
实施例10.盐酸去亚甲基小檗碱(dmb)作用于md2蛋白发挥抗炎活性
方法:克罗恩病患者血清中有较高的md2蛋白水平以引发tlr4通路激活造成严重的炎症损伤。md2蛋白为tlr4通路的上游,md2与细胞表面受体tlr4作用,通过识别微生物相关分子lps引起炎症因子il-1β等表达。推测dmb可能通过作用于md2蛋白发挥抗炎活性。
本实施例中,通过分子对接软件预测dmb与md2蛋白的作用位点为md2蛋白的第23位色氨酸、76位苯丙氨酸、102位酪氨酸,以raw264.7为研究对象将正常md2及其位点突变体的表达载体pcdna3.1(+)转入raw264.7中。细胞培养液中给与dmb20μm预处理12h,脂多糖lps刺激6h后收集细胞,trizol法提取mrna,逆转录为cdna,利用rt-pcr法从细胞基因水平检测dmb抗炎变化。
结果:rt-pcr法结果显示如图8,20μmdmb可显著抑制脂多糖lps刺激表达正常md2的raw264.7细胞中产生的促炎因子,但在表达突变md2的raw264.7中,dmb的抗炎效果降低,推测dmb可能作用于以上位点治疗tnbs诱导的cd。(图中,*是都与模型组比,测量值的单位是以gapdh为内参基因的相对表达量。)。
- 还没有人留言评论。精彩留言会获得点赞!