小分子SR9009在抗衰老以及减轻衰老引起的慢性炎症中的用途
小分子sr9009在抗衰老以及减轻衰老引起的慢性炎症中的用途
技术领域
1.本发明属于生物技术领域,涉及小分子sr9009在抗衰老以及减轻衰老引起的慢性炎症中的用途。
背景技术:
2.在40年前,由hayflick和他的同事提出了细胞衰老这一概念,即细胞具有增殖极限,经历过有限传代次数后,所有的细胞失去了分裂的能力,但却能够维持细胞的生长代谢。最终,所有的细胞都丧失了分裂能力,然而这些细胞仍然能存活数周,人们将这种现象称为细胞衰老。
3.各种不同的细胞压力都能导致细胞衰老的发生,例如端粒缩短引起的复制衰老,活性氧(ros)诱导的衰老,dna损伤诱导的衰老以及致癌基因诱导的衰老。
4.细胞衰老的主要特征是失去了通过细胞周期的能力,衰老细胞通常细胞周期停滞在g1期,然而其仍然具有代谢活性。一旦生长停滞,即使合适的生长条件,细胞也不能进行复制。
5.细胞衰老在疾病中有着不利的作用,例如脂肪细胞衰老能够促进肥胖的发生;细胞衰老能够促进ⅱ型糖尿病以及动脉粥样硬化的发展,所以抑制衰老的发生对于治疗肥胖、糖尿病、动脉粥样硬化等慢性疾病具有重要的作用。
6.细胞衰老还会产生复杂的促炎症反应,称之为衰老相关的分泌表型(senescence-associated secretory phenotype,sasp)。sasp由nf-κb和cebpβ调控,这些因子包括分泌促炎症的细胞因子il-6,il-8,单核趋化因子(mcps),巨噬细胞炎症因子(mips),生长因子(tgf-β),粒细胞-巨噬细胞集落刺激因子(gm-csf)和蛋白酶。sasp具有强烈的自分泌和旁分泌的活性,这意味着衰老能创造一个促炎的微环境。
7.目前市场上可用的抑制衰老的小分子种类有限,靶点不明,效果参差不齐。因此,本领域迫切需要开发一种可以高效抑制细胞衰老,靶点明确的化合物,并研究其对于抗衰老,以及减轻衰老引起的慢性炎症,以及其他衰老相关的疾病的作用。
技术实现要素:
8.本发明的目的在于提供一种可以高效抑制细胞衰老,靶点明确的化合物,并研究其对于抗衰老,以及减轻衰老引起的慢性炎症,以及其他衰老相关的疾病的作用。
9.具体地,本发明提供了小分子化合物sr9009,在制备治疗、预防和/或缓解衰老,以及衰老引起的相关疾病,例如衰老引起的慢性炎症的药物中的用途。
10.在本发明的第一方面,提供了一种式i化合物或含所述化合物的制剂的用途,所述化合物用于制备预防、缓解和/或治疗a)衰老;和/或b)衰老引起的相关疾病的药物。
[0011][0012]
在另一优选例中,所述式i化合物选自:sr9009、sr9011、gsk4112、oltipraz、或其组合。
[0013]
在另一优选例中,所述衰老选自下组:化疗药物诱导的衰老、致癌基因诱导的衰老、辐照诱导的衰老、复制衰老、氧化压力诱导的衰老、dna损伤诱导的衰老、或其组合。
[0014]
在另一优选例中,所述衰老引起的相关疾病选自下组:慢性炎症、癌症、骨关节炎、动脉粥样硬化、肺纤维化及肝纤维化、糖尿病、或其组合。
[0015]
在另一优选例中,所述化合物或含所述化合物的制剂用于制备一药物组合物,所述药物组合物用于以下一种或多种用途:
[0016]
(1)降低sasp因子的表达;
[0017]
(2)降低dna损伤信号通路;
[0018]
(3)降低细胞内ros水平;
[0019]
(4)激活细胞内nrf2通路。
[0020]
在另一优选中,所述sasp因子选自下组:il-1α,il-1β,cxcl-1,cxcl-3,il-6,il-8、icam-1、或其组合。
[0021]
在另一优选中,所述dna损伤信号通路选自下组:nf-kb、p38、或其组合。
[0022]
在另一优选例中,所述细胞为哺乳动物细胞。
[0023]
在另一优选例中,所述哺乳动物选自:人、小鼠、兔、猪、或其组合。
[0024]
在另一优选例中,所述制剂为注射制剂或口服制剂。
[0025]
在另一优选例中,所述制剂选自下组:片剂、胶囊剂、颗粒剂、混悬剂、丸剂、溶液剂、糖浆剂、或注射剂。
[0026]
在本发明的第二方面,提供了一种药物组合物,所述药物组合物包含:
[0027]
(a1)式i化合物或其药学上可接受的盐;
[0028]
(a2)其他药学上可接受的载体或赋形剂。
[0029]
在另一优选例中,所述式i化合物选自::sr9009、sr9011、gsk4112、oltipraz、或其组合。
[0030]
在本发明的第三方面,提供了一种如第二方面所述的药物组合物的用途,用于制备预防、缓解和/或治疗a)衰老;和/或b)衰老引起的相关疾病的药物。
[0031]
在本发明的第四方面,提供了一种激活细胞内nrf2通路的方法,将所述细胞和医学有效量的式i化合物接触。
[0032]
在另一优选例中,所述式i化合物选自::sr9009、sr9011、gsk4112、oltipraz、或其组合。
[0033]
在另一优选例中,所述细胞为哺乳动物细胞。
[0034]
在另一优选例中,所述哺乳动物选自:人、小鼠、兔、猪、或其组合。
[0035]
在本发明的第五方面,提供了一种预防、缓解和/或治疗衰老和/或衰老引起的相关疾病的方法,为有需要的患者施用医学有效量的式i化合物。
[0036]
在另一优选例中,所述式i化合物选自::sr9009、sr9011、gsk4112、oltipraz、或其组合。
[0037]
在另一优选例中,所述衰老引起的相关疾病选自下组:慢性炎症、癌症、骨关节炎、动脉粥样硬化、肺纤维化及肝纤维化、糖尿病、或其组合。
[0038]
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
[0039]
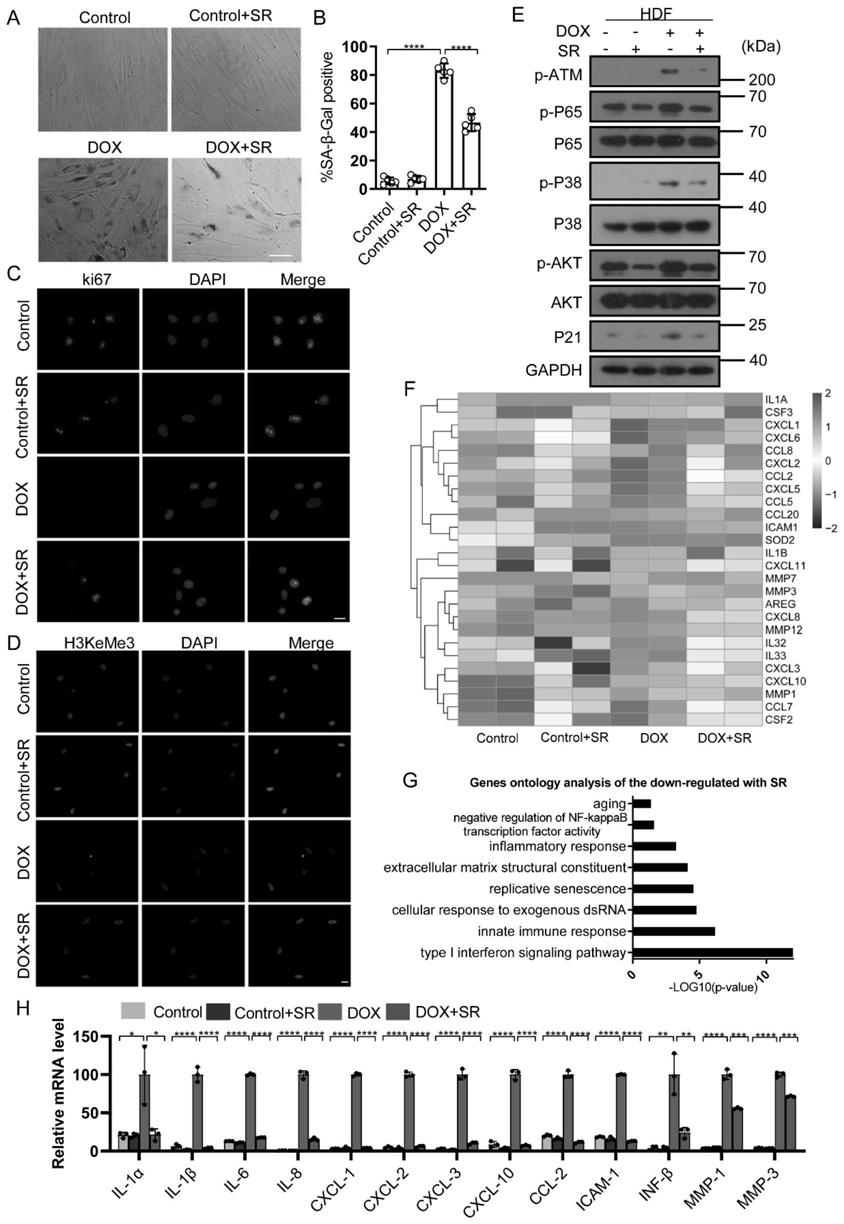
图1显示了小分子sr9009能抑制化疗药物诱导的细胞数衰老反应。其中,(a)化疗药物诱导的衰老模型,sa-β-gal染色检测sr处理后细胞衰老的变化。(b)定量统计分析sa-β-gal染色结果。(c)免疫荧光染色检测sr处理后ki67的表达变化。(d)免疫荧光染色sr处理后异染色质相关基因h3k9me3的表达变化。(e)western blot检测dna损伤相关基因以及调控sasp因子通路的表达变化。(f)热图显示rna-sequencing结果中sasp因子的表达变化。(g)rna-sequencing下调基因的功能富集分析。(h)qpcr检测sr处理后sasp因子的表达变化。
[0040]
图2显示了sr9009抑制sasp因子表达效率高于rapamycin。其中,(a)建立化疗药物诱导的衰老模型,加入rapamycin,sr9009,sa-β-gal染色检测细胞衰老的变化。(b)定量统计sa-β-gal染色结果。(c)western blot检测dna损伤相关基因p-atm,p-p53表达变化,细胞周期因子p21表达变化,调控sasp的转录因子p-p65的表达变化。(d)免疫荧光染色dna damage相关基因γ-h2ax。(e)免疫荧光染色增殖相关基因ki67。(f)qpcr检测sasp因子的表达变化。(g)比较sr9009与rapamycin抑制sasp因子的效率。
[0041]
图3显示了小分子sr9009不是通过结合nr1d1来抑制细胞衰老反应。其中,(a)western blot检测nr1d1的敲低效率。(b)western blot检测过表达nr1d1-δlbd的效率。(c)在敲低nr1d1的基础上,建立化疗药物诱导的衰老模型,加入sr,检测sasp因子的表达。(d)在过表达nr1d1-δlbd的基础上,建立化疗药物诱导的衰老模型,加入sr,检测sasp因子的表达。
[0042]
图4显示了小分子sr9009通过细胞内的ros来抑制细胞衰老反应。其中,(a)化疗药物诱导衰老模型中,sr9009处理后干性相关基因以及sirt1表达变化。(b)化疗药物诱导衰老模型中,sr9009处理后细胞内ros水平检测。(c)荧光强度定量表示ros水平。
[0043]
图5显示了小分子sr9009通过激活nrf2通路来抑制细胞衰老反应。其中,(a)sr处理后上调基因功能富集分析,主要富集在氧化还原反应,对活性氧的反应等。(b)热图显示nrf2的靶基因在sr处理后的表达变化。(c)sr处理后,qpcr检测nrf2以及其靶基因的表达变化。(d)sr处理后,western blot检测nrf2以及其靶基因的表达变化。(e)加入chx后,分别加与不加sr9009。分别在0min,20min,40min收蛋白,检测nrf2的降解速率。(f)相对定量分析nrf2的蛋白表达变化,从而计算其降解速率。(g)qpcr检测敲低nrf2的效率。(h)western blot检测nrf2的敲低效率。(i)敲低nrf2的基础上,建立化疗诱导的衰老模型,qpcr检测
sasp因子的表达。
[0044]
图6.1显示了sr9009能在体内抑制衰老反应。其中,(a)小鼠辐照前,给予sr9009处理,然后进行辐照,辐照后继续每隔一天进行腹腔注射100mg/kg sr9009,2个星期后进行sa-β-gal染色检测肝脏衰老细胞的比率。(b)对小鼠给予相同的处理,qpcr检测肝脏有代表性的sasp因子的表达变化。(c)qpcr检测肝脏免疫细胞marker,cd3;cd45的表达。(d)免疫组化检测肝脏免疫细胞的表达。(e)线虫寿命实验检测sr9009,rapamycin处理对线虫寿命的影响。
[0045]
图6.2显示了sr9009能在体内激活nrf2通路抑制辐照诱导的衰老。其中,(a)sr处理后,dcfda检测细胞内的活性氧的变化。(b)定量分析活性氧的变化。(c)sr处理后,western blot检测dna损伤因子p-atm,以及调控sasp因子的转录因子p-p65,p-p38,nrf2和nqo1,ho-1的表达变化。(d)sr处理后,免疫组化检测γ-h2ax,il-1α,p21,nrf2,nqo1,ho-1的表达。
具体实施方式
[0046]
本发明人经过广泛而深入地研究,首次意外发现一种能有效抗衰老的小分子化合物,在此基础上完成了本发明。
[0047]
具体地,本发明发现了小分子化合物sr9009能有效抗衰老,并且减少衰老引发的慢性炎症,可以被用于制备治疗、预防和/或缓解衰老以及衰老引起的慢性炎症或其他衰老引起的相关疾病的药物。
[0048]
术语
[0049]
本发明的化合物
[0050]
如本文所用,“本发明的化合物”,“本发明的式i化合物”,可互换使用,均值的是式i所示的化合物,优选地为sr9009。
[0051]
sr9009化学式为c
20h24
cln3o4s,结构式如式i所示:
[0052][0053]
衰老和抗衰老
[0054]
如本文所用,“衰老(aging)”指随时间增加,有机体在构成物质、组织结构、生理功能等方面发生的丧失和退化过程。在本发明中,衰老指生物学衰老。
[0055]
如本文所用,“抗衰老”是指延缓、阻滞、减少、停止和/或逆转衰老效果或进程。
[0056]
细胞衰老是这样的现象,其导致单独细胞无法持续分裂,使其在数次分裂之后停滞。为了检测细胞衰老,一般使用细胞染色测试,其检测衰老相关的标志物(如β-半乳糖苷酶活性)。衰老的细胞可以干扰整个有机体的重要功能和从而导致某些障碍。整个有机体的衰老伴随着某些障碍(比如疾病、并发症和症状)增加的风险。
[0057]
一些代表性的衰老细胞标记物或标志包括(但并不限于):sa-β-半乳糖苷酶(其表
达量上升提示衰老程度增加)、细胞增殖能力(其下降提示衰老程度增加)、sasp因子的增加。
[0058]
衰老相关的分泌表型(senescence-associated secretory phenotype,sasp)
[0059]
细胞衰老的典型特征是细胞周期的阻滞,同时衰老的细胞会分泌一系列炎症因子,趋化因子等,简称衰老相关的分泌因子(英文全称,sasp)。sasp由促炎细胞因子,生长因子,趋化因子和基质重塑酶等一系列细胞因子组成,主要受nf-κb、p38信号通路调控。其可以反作用于衰老细胞及其邻近细胞加速它们的衰老进程,并可作为新的细胞衰老效应机制。它们可以导致机体慢性低度炎症和疾病,加重疾病的进展。抑制sasp因子的表达可以减轻癌症、肝纤维化、骨关节炎等慢性疾病的发生发展。
[0060]
衰老引起的慢性炎症
[0061]
衰老引起的慢性低度的炎症,被称为“慢性发炎”。慢性炎性疾病被认为是最当今世界的重要死亡原因,其中超过50%所有死亡均归因于与炎症相关的疾病,例如如缺血性心脏病,中风,癌症,糖尿病,慢性肾脏疾病,非酒精性脂肪肝疾病(nafld)以及自身免疫和神经退行性疾病。
[0062]
线粒体功能异常,dna损伤反应以及细胞衰老后的活性氧以及sasp产生是产生慢性炎症的原因。因此抑制衰老以及sasp的产生对于减轻慢性炎症相关的衰老疾病至关重要。
[0063]
ros
[0064]
ros可以通过触发dna损伤反应(ddr)途径,在体外诱导衰老生长停滞,其中atm或atr激酶通过稳定p53和细胞周期蛋白依赖性激酶(cdk)抑制剂p21的转录激活来阻止细胞周期进程。反之,响应于持续的dna损伤,p38-mapk介导的线粒体功能障碍和ros产生而激活p16ink4a。也就是说ros能激活dna damage,dna damage又进一步激活ros,两者共同驱动细胞衰老的发生。nrf2是多种抗氧化防御机制的主要调控元素。nrf2调节200多种编码细胞保护性ii期脱毒和抗氧化酶的基因,包括ho-1,nqo1,从而降低ros水平。在正常条件下,nrf2被keap1同型二聚体隔离在胞质中。nrf2的半衰期很短,因为它被蛋白酶体泛素化并迅速降解。但是,当细胞受到压力时,由三个反应性半胱氨酸残基介导的keap1会发生构象变化,从而导致nrf2的释放。释放后,nrf2逃脱了cul3介导的降解途径,从而将其半衰期延长,进而调控其下游靶基因的表达降低细胞内的ros水平。
[0065]
生物线虫
[0066]
生物线虫是一种经典的模式生物,具有生命周期短、易于观察、遗传背景清晰等特点。除此之外,线虫基因与人类很多重要功能基因高度同源并且具有相似的信号传导通路,使其在病理学研究、新靶点发现以及药物筛选中受到越来越多的关注。
[0067]
生物线虫是抗衰老研究的重要模式生物之一,已被用于抗衰老物质的筛选和抗衰老的机理研究。
[0068]
药物组合物及施用方法
[0069]
本发明还提供了含有本发明化合物的组合物或制剂或产品,所述组合物或制剂或产品可用于抗衰老。代表性的组合物或制剂或产品包括抗衰老的药物、保健品、和化妆品。
[0070]
一种优选的组合物是药物组合物,它含有有效量的式i化合物,优选地为sr9009或其药学上可接受的盐和药学上可接受的载体。
[0071]
如本文所用,术语“有效量”或“有效剂量”是指可对人和/或动物产生功能或活性(即抗衰老功能)的且可被人和/或动物所接受的量。
[0072]
如本文所用,术语“药学上可接受的”的成分是适用于人和/或哺乳动物而无过度不良副反应(如毒性、刺激和变态反应)的,即具有合理的效益/风险比的物质。术语“药学上可接受的载体”指用于治疗剂给药的载体,包括各种赋形剂和稀释剂。
[0073]
本发明的药物组合物含有安全有效量的本发明的活性成分以及药学上可接受的载体。这类载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、及其组合。通常药物制剂应与给药方式相匹配,本发明的药物组合物的剂型为注射剂、口服制剂(片剂、胶囊、口服液)、透皮剂、缓释剂。例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。所述的药物组合物宜在无菌条件下制造。
[0074]
本发明所述的活性成分的有效量可随给药的模式和待治疗的疾病的严重程度等而变化。优选的有效量的选择可以由本领域普通技术人员根据各种因素来确定(例如通过临床试验)。所述的因素包括但不限于:所述的活性成分的药代动力学参数例如生物利用率、代谢、半衰期等;患者所要治疗的疾病的严重程度、患者的体重、患者的免疫状况、给药的途径等。通常,当本发明的活性成分每天以约0.00001mg-50mg/kg动物体重(较佳的0.0001mg-10mg/kg动物体重)的剂量给予,能得到令人满意的效果。例如,由治疗状况的迫切要求,可每天给予若干次分开的剂量,或将剂量按比例地减少。
[0075]
典型地,当以口服方式给予式i化合物,优选地sr9009时,一个60kg体重的对象(人),日平均剂量通常为10-500mg,较佳地20-300mg,更佳地50-250mg。所述日剂量可以分一次、二次或多次服用。
[0076]
本发明所述的药学上可接受的载体包括(但不限于):水、盐水、脂质体、脂质、肽类物质、纤维素、纳米凝胶、或其组合。载体的选择应与给药方式相匹配,这些都是本领域的普通技术人员所熟知的。
[0077]
抗衰老的方法
[0078]
本发明还提供一种抗衰老的方法,为有需要的患者施用医学有效量的式i化合物。
[0079]
在另一优选例中,所述式i化合物选自::sr9009、sr9011、gsk4112、oltipraz、或其组合。
[0080]
在另一优选例中,所述衰老引起的相关疾病为慢性炎症、癌症、骨关节炎、动脉粥样硬化、肺纤维化及肝纤维化、糖尿病、或其组合。
[0081]
本发明的主要优点在于:
[0082]
(a)首次发现式i化合物,优选地为sr9009,具有良好的抗衰老作用,并能够减轻或治疗衰老引起的慢性炎症,可以用于制备预防、缓解和/或治疗衰老;和/或衰老引起的相关疾病的药物。
[0083]
(b)首次发现sr9009通过激活nrf2通路,使得nrf2蛋白增加,从而抑制细胞内ros的水平,达到抗衰老的作用。
[0084]
(c)sr9009的抗衰老作用优于已知的能够抗衰老的小分子化合物rapamycin。
[0085]
本实施例中应用到的具体实验模型及方法如下所示:
[0086]
(一)人皮肤成纤维细胞(hdf)以及人胚肺成纤维细胞衰老模型建立以及sr9009处理
[0087]
化疗药物诱导的衰老:细胞培养至60-70%密度左右,加入10μm sr9009处理12-24h后,然后加入化疗药物doxorubicin至终浓度为300nm,24h后撤掉doxorubicin加入新鲜培养基继续培养,在此过程sr9009一直持续加入,每三天更换一次,7天左右细胞会进入衰老状态。
[0088]
致癌基因诱导的衰老:细胞铺至50-70%密度左右,加入10μm sr9009处理12-24h后,第一次加入hras
g12v
病毒液,24h后加入正常培养基继续培养,培养24后进行第二次病毒液继续感染24h,后加入正常培养基并加入终浓度为2μg/ml的嘌呤霉素进行筛选,在在此过程sr9009一直持续加入,每三天更换一次,3天后没死的细胞即为阳性的细胞,后续继续培养4-6天左右,细胞会进入衰老的状态。
[0089]
(二)辐照诱导的小鼠衰老模型以及sr9009处理
[0090]
8周龄大小的c57/b6小鼠,提前给予玉米油以及sr腹腔注射(50mg/kg),然后进行5gy剂量的辐照,辐照结束后,每隔一天进行玉米油以及sr腹腔注射(100mg/kg),3周后杀死小鼠,进行相关指标检测。
[0091]
(三)shrna敲低
[0092]
构建敲低用到的载体是plko.1载体,购买自addgene网站。分别设计靶向序列,分别是nr1d1shrna,ccagccctgaatccctctata;nrf2-shrna,ccggcatttcactaaacacaa。把靶向序列克隆进plko.1载体,后续进行慢病毒的包装及感染。
[0093]
(四)western blot
[0094]
细胞及组织总蛋白用含有蛋白酶抑制剂(roche)的冰冷ripa缓冲液提取。使用bca试剂盒(beyotime)确定浓度,并标准化至最低浓度。将不同组等量的蛋白在12%tris-glycine sds-page中进行电泳,电泳结束进行转膜。转膜结束后取膜用5%脱脂奶封闭,并在4℃下一抗孵育过夜。tbst进行洗涤,每次8min,3次,然后加入二抗进行孵育,按1:5000稀释,室温孵育1h。然后tbst进行洗涤,每次8min,3次。清洗完进行显影。
[0095]
(五)基因测序
[0096]
提取样品总rna并使用dnase消化dna后,用带有oligo(dt)的磁珠富集真核生物mrna(若为原核生物,则通过试剂盒去除rrna来富集mrna);加入打断试剂将mrna打断成短片段,以打断后的mrna为模板,用六碱基随机引物合成一链cdna,然后配制二链成反应体系合成二链cdna,并使用试剂盒纯化双链cdna;纯化的双链cdna再进行末端修复、加a尾并连接测序接头,然后进行片段大小选择,最后进行pcr扩增;构建好的文库用agilent 2100bioanalyzer质检合格后,使用illumina hiseqtm 2500或illumina hiseq x ten等测序仪进行测序,产生125bp或150bp的的双端数据。质检合格后,使用illumina测序仪进行测序。对测序的结果进行差异基因分析以及功能富集分析。
[0097]
(六)免疫荧光
[0098]
将细胞种植在盖玻片上,密度20-30%,pbs漂洗3次,每次5min,在含0.1%tritonx-100的透化试剂(0.1m pbs配)中室温透膜10min,于ph7.2,4%多聚甲醛(0.1m pbs配)溶液中固定10min,pbs漂洗3次,每次5min,5%bsa室温封闭1h,一抗孵育过夜,洗涤后,二抗常温孵育1h,洗涤后dapi孵育15-20min,洗涤后用dako(荧光固定剂)固定盖玻片,荧光显微镜或共聚焦显微镜拍照记录。
[0099]
(七)检测mrna的表达
[0100]
细胞及组织样品进行rna的抽提,然后反转录成cdna.定量pcr使用sybr green qpcr预混液(日本大阪,toyobo)根据说明书进行cdna以及引物的添加。qpcr反应在quantstudio 7实时pcr系统(thermo fisher scientific)上进行。所有数据均以rpl13a或gapdh作为内参进行标准化处理。
[0101]
实施例1小分子sr9009(简称sr,下同)抑制多种细胞压力诱导的细胞衰老反应
[0102]
1.1小分子sr9009抑制化疗药物诱导的细胞衰老
[0103]
为了探究sr9009能否抑制细胞衰老,我们提前加入sr9009,然后建立化疗药物doxorubicin诱导的hdf细胞衰老模型,sr9009给药,每3天换一次,持续7d。
[0104]
可以明显看到细胞变扁平,呈长梭性,sa-β-gal染色结果表明sr9009处理组相对于对照组其衰老细胞更少(图1a-b)。免疫荧光染色结果显示ki67阳性细胞数在doxorubicin处理后出现了明显的下调(图1c),sr9009处理后ki67阳性细胞数明显上调,异染色质marker h3k9me3在doxorubicin处理后出现了明显的下调,sr9009处理后其有一定程度的上调(图1d)。
[0105]
1.2小分子sr9009抑制化疗药物诱导的细胞衰老的通路
[0106]
为了更进一步探索sr9009处理后基因表达及通路的变化,我们接着做了rna-sequencing,衰老细胞会分泌大量的促炎细胞因子、趋化因子等,简称sasp。
[0107]
如热图所示sasp因子在sr9009处理后有明显的下调(图1f),我们也进一步检测了sasp因子的表达变化,与热图的结果一致,结果显示sr9009处理后il-1α,il-1β,cxcl-1,cxcl-3,il-6,il-8等表达明显降低(图1h),对rna-sequencing下调基因进行功能富集分析,发现下调的通路主要是衰老相关通路和nf-κb信号通路。
[0108]
接着我们检测dna损伤信号通路的变化,结果显示sr9009处理后p-atm,p-p53出现下调,细胞周期调控蛋白p21下调,调控sasp的主要转录因子nf-kb,p38也出现下调的情况(图1e),说明sr9009能降低dna损伤反应,下调nf-kb,p38通路从而减少sasp因子的表达。
[0109]
1.3小分子sr9009抑制其他压力诱导的细胞衰老
[0110]
除此之外,我们也利用了致癌基因诱导衰老模型以及辐照诱导的衰老模型,发现sr9009也具有抑制细胞衰老的作用。接着,我们也用了另外一种细胞系imr-90建立化疗药物诱导的衰老模型和致癌基因诱导的衰老模型,发现sr也能抑制其衰老反应。总的来说这些结果说明小分子sr能抑制各种压力诱导的细胞衰老反应。
[0111]
实施例2 sr9009抑制sasp因子表达效率高于rapamycin
[0112]
rapamycin作为一种多功能的小分子,其也能抑制衰老。为了比较一下rapamycin与sr9009抑制sasp因子的效果,我们提前加入rapamycin,然后加入化疗药物doxorubicin建立化疗药物诱导的衰老模型,7d后进行衰老相关的sa-β-gal染色。
[0113]
发现rapamycin能显著降低sa-β-gal阳性细胞数,且其降低比率与sr9009相当,(图2a-b),说明其能抑制细胞衰老的发生。免疫荧光染色结果显示rapamycin能增加ki67的表达,减轻dna损伤fociγ-h2ax降低(图2d-e)。作为对比,本发明人也进行了sasp因子的检测,发现其也能明显降低sasp因子的表达,包括il-1α,il-1β,il-6,cxcl-3,cxcl-10,icam-1等(图2f),dna损伤相关的基因p-atm,p-p53明显降低,细胞周期抑制因子p21也明显降低,调控sasp的转录因子p-p65也明显下降(图2c),说明rapamycin能抑制细胞衰老的发生。同时本发明人对比了一下sr9009抑制sasp的效率与rapamycin抑制sasp因子效率的对比,发
现整体上sr9009抑制sasp因子的比率更高(图2g)。
[0114]
由此可以推断,对比已知的具有抗衰老作用的小分子化合物rapamycin,本发明的sr9009的抗衰老的效果更好。
[0115]
实施例3小分子sr9009不是通过结合nr1d1来抑制细胞衰老反应
[0116]
为了探究小分子sr9009抑制细胞衰老的作用机制是否通过结合其配体nr1d1,我们利用shrna技术敲低nr1d1,利用western blot检测其敲低效率接近100%(图3a),我们利用敲低nr1d1的细胞系,提前加入sr9009,然后加入化疗药物doxorubicin建立化疗药物诱导的衰老模型,7d后进行衰老相关的sa-β-gal染色。
[0117]
发现sr处理后其阳性细胞数相对于未加sr处理组明显减少,我们也检测了sasp因子的表达,发现sr处理后,il-1α,il-1β,cxcl-1,cxcl-3,il-6,il-8,icam-1等出现了明显的下调(图3c),而且其下调的比率与未敲低nr1d1加sr处理相当,说明nr1d1的敲低,不会影响sr的抗衰老作用。因此推断,sr不是通过结合nr1d1来发挥抑制细胞衰老的作用的。
[0118]
nr1d1具有不同的结构域,其中lbd结构域是其结合配体的结构域。为了更加进一步确定sr是否是通过结合nr1d1来发挥作用,我们构建了nr1d1-δlbd载体并进行表达,western blot能明显检测到其表达,如图所示,其条带的位置比过表达nr1d1的位置稍低(图3b)。我们利用过表达nr1d1-δlbd细胞系,提前加入sr,然后加入化疗药物doxorubicin建立化疗药物诱导的衰老模型,7d后进行衰老相关的sa-β-gal染色。
[0119]
sr处理后其阳性细胞数相对于未加sr处理组明显减少,我们也检测了sasp因子的表达,发现sr处理后,il-1α,il-1β,cxcl-1,cxcl-3,il-6,il-8,icam-1等出现了明显的下调(图3d),而且其下调的比率与未过表达nr1d1-δlbd加sr处理相当。这说明,nr1d1-δlbd的过表达不影响sr发挥抗衰老作用,因此推定,sr不是通过结合nr1d1来发挥抑制细胞衰老的作用的。
[0120]
实施例4小分子sr9009通过降低细胞内的ros来抑制细胞衰老反应
[0121]
本发明人继续探索sr9009抑制衰老以及sasp的分子机制,有文献报导干性相关基因表达的增加能减轻衰老的发生,本发明人首先检测了一下sr处理后干性相关基因表达的变化,结果显示在化疗药物诱导的衰老以及致癌基因诱导的衰老中,sr9009处理后干性相关基因表达没有显著变化(图4a)。这说明sr不是通过影响干性相关基因的表达来抑制细胞衰老的发生。
[0122]
sirt家族与衰老有很大关系,于是接着本发明人检测了一下sirt1的表达,实验结果显示sr处理后其表达没有明显的变化(图4a)。
[0123]
有文献报导细胞内活性氧增加会增加dna损伤,促进异染色质的改变促进衰老的发生,本发明人发现sr9009处理后能减少化疗药物诱导的ros的增加(图4b,c)。
[0124]
实施例5小分子sr9009通过激活nrf2通路来抑制细胞衰老反应
[0125]
本发明人的测序结果显示sr9009处理后上调的基因富集的功能主要是氧化还原反应,对ros的反应等(图5a),这表明sr能降低细胞内ros水平相符合。
[0126]
由于nrf2能调控细胞内ros的反应,本发明人检测了sr9009处理后nrf2的相关情况。发现,nrf2的mrna水平没有明显的差异,但是其蛋白水平却有明显的增加(图5c),keap1作为能调控nrf2降解的分子其表达水平明显减少(图5d)。nrf2的靶基因nqo1,ho-1在本发明人测序结果中经sr处理后表达水平增高(图5b),本发明人也在mrna水平以及蛋白水平进
行了确证(图5c-d)。因此可以断定,sr能激活nrf2通路。至于nrf2蛋白水平增加,mrna水平不变,本发明人猜测可能是sr处理后其蛋白降解速率变慢了。
[0127]
本发明人加入chx抑制细胞转录,然后在不同的时间点去检测nrf2蛋白的表达,发现在chx处理0min,20min,40min后,sr处理后nrf2的蛋白水平相对于未加sr处理表达更多,说明sr处理后nrf2蛋白降解速率变慢,从而增加了nrf2的蛋白表达水平(图5e-f)。因此可以断定sr处理激活了nrf2通路,由于keap1调控nrf2降解速率降低的作用,使得nrf2蛋白表达增加,从而达到抗衰老的作用。
[0128]
为了进一步验证nrf2在衰老中的重要作用,本发明人利用shrna敲低nrf2,其敲除效率接近100%(图5g),然后加入化疗药物建立化疗诱导的衰老模型,进行sasp因子的检测,发现敲除nrf2后,sasp因子增加,包括il-1α,il-8,cxcl-1,cxcl-1,cxcl-3,icam-1等(图5h),说明敲低nrf2能增加sasp因子的表达,增加衰老。
[0129]
因此可以推定,小分子sr9009通过激活nrf2通路增加其靶基因的表达从而降低细胞内的ros水平来抑制细胞衰老反应。
[0130]
实施例6小分子sr9009在体内也能通过激活nrf2通路抑制衰老,降低慢性炎症的发生
[0131]
为了更加进一步确证sr9009在体内的作用,本发明人提前腹腔注射sr9009,然后利用辐照诱导衰老模型(其多种组织中皆具有衰老细胞),辐照结束后,每隔一天注射一次sr9009,3周后取肝组织进行检测。
[0132]
发现,sr处理后能明显降低肝脏组织的sa-β-gal染色的阳性率(图6.1a)。qpcr进行sasp因子检测,发现sr处理后il-1α,il-1β,cxcl-1,il-6明显降低(图6.1b)。sasp因子的增加会招募免疫细胞,导致慢性炎症的发生,本发明人检测了一下免疫细胞的招募,发现sr处理后免疫细胞的marker cd3,cd45表达降低(图6.1c),免疫组化的结果也显示免疫细胞的标志物cd3,mac2的表达降低(图6.1d),说明sr处理后能明显降低慢性炎症的发生。
[0133]
本发明人利用了模式生物线虫发现sr9009相对于rapamycin能显著延长线虫的寿命。另外本发明人利用western blot检测了dna损伤相关基因的表达,γ-h2ax,p-atm,p-p53表达降低(图6.2c),细胞周期相关抑制蛋白p21也明显降低,调控sasp因子的转录因子p-p65也明显降低(图6.2c),免疫组化的结果也显示sr处理后γ-h2ax表达降低,p21表达也降低,有代表性的sasp因子il-1α表达也降低(6.2d)。这些结果说明小分子sr9009能抑制衰老反应,减少sasp因子,降低慢性炎症的发生。
[0134]
本发明人之前的细胞实验结果表明小分子sr9009通过nrf2通路降低细胞内的ros水平从而抑制细胞衰老反应,为了确证小分子sr9009在体内抑制衰老反应的机制是否也是通过nrf2通路,本发明人取辐照组、辐照+sr9009组小鼠的肝脏进行消化,进行dcfh-da探针染色,流式分析,实验结果表明小分子能总体降低肝脏内的ros水平(图6.2a,b),免疫组化结果表明sr9009处理后nrf2表达增加,nrf2的靶基因nqo-1,ho-1表达也增加(图6.2d),这提示本发明人nrf2通路在小分子sr9009抑制衰老反应中起着重要的作用。
[0135]
综上所述,在体内试验中,sr也可以通过激活nrf2通路,降低ros水平,从而达到抗衰老的作用。
[0136]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可
以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1