冬凌草叶水提物粉末,其制备,抗肿瘤作用及应用的制作方法
1,3-己二烯羰氧)桂皮酰]奎尼酸, 3-o-[e-2-(7-羧基-1-庚烯羰氧)-3-(6-羟基-1-己烯羰氧)-4-(3-羧基-1-丙烯羰氧)-5-甲酰氧
ꢀ-
6-(6-羧基-1-己烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(4-羟基丁羰氧)-3,4-二(3-羧基丙羰氧)-5
-ꢀ
甲酰氧-6-(6-羧基-1-己烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(5-羧基-1-戊烯羰氧)-3-羧基乙酰氧-4,6-二(3-羧基丙烯酰氧)-5-甲酰氧桂皮酰]奎尼酸,3-o-[e-2,3-二(3-羧基-1-丙烯羰氧)-4-(3-羧基丙烯酰氧)-5-羧基乙酰氧-6-(4-羧基-1-丁烯羰氧)桂皮酰]奎尼酸, 3-o-[e-2,3,4-三(4-羟基丁羰氧)-5-甲酰氧-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸, 3-o-[e-2-(4-羟基-1,3-丁二烯羰氧)-3,4-二(3-羧基-1-丙烯羰氧)-5-甲酰氧-6-(6-羧基-1,3,5-己三烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(4-羟基-1,3-丁二烯羰氧)-3-羧乙酰氧-4-(3-羧基-1-丙烯羰氧)-5-甲酰氧-6-(4-羧基-1,3-丁二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2,3-二(3-羧基丙羰氧)-4-(3-羧基丙酰氧)-5-甲酰氧-6-(6-羧基-1-己烯羰氧)桂皮酰]奎尼酸,3-o-[e-2,3-二(3-羧基丙羰氧)-4-(3-羟基丙酰氧)-5-羟甲氧-6-(5-羧基戊羰氧)桂皮酰]奎尼酸,3-o-[e-2,6-二(5
-ꢀ
羧基-1-戊烯羰氧)-3-(3-羧基丙羰氧)-4-羧基乙酰氧-5-甲氧桂皮酰]奎尼酸,3-o-[e-2-(8-羧基-1-辛烯羰氧)-3-(3-羧基丙羰氧)-4-(7-羧基-1-庚烯羰氧)-5-羧基乙酰氧-6-(4-羧基-1-丁烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(9-羟基-1-壬烯羰氧)-3-(4-羟基丁羰氧)-4-(8-羟基-1-辛烯羰氧)-5-甲氧-6-(4-羧基-1-丁烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(7-羧基-1,3,5-庚三烯羰氧)-3,4-二(5-羧基-1,3-戊二烯羰氧)-5-羧基乙酰氧-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(4-羟基-1-丁烯羰氧)-3-(4-羧基-1-丁烯羰氧)-4-(3-羧基丙烯酰氧)-5-羧基乙酰氧-6-(4-羧基-1,3-丁二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(7-羧基-1,3,5-庚三烯羰氧)-3-(8-羟基-1,3,5,7-辛四烯羰氧)-4,5-二(4-羧基-1,3-丁二烯酰氧)-6-(6-羧基-1,3,5-己三烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(4-羟基丁羰氧)-3,4-二(3-羧基丙羰氧)-5-(3-羟基丙酰氧)-6-(4-羧基丁羰氧)桂皮酰]奎尼酸,3-o-[e-2,6-二(5-羧基-1-戊烯羰氧)-3-(3-羧基丙羰氧)-4-(3-羧基丙酰氧)-5-羟基桂皮酰]奎尼酸,3-o-[e-2,5-二(7-羧基-1,3-庚二烯羰氧)-3-(6-羟基-1,3-己二烯羰氧)-4-(4-羧基-1,3-丁二烯羰氧)-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸,3-o-[e-2-(5-羟基-1-戊烯羰氧)-3,4-二(4-羧基-1-丁烯羰氧)-5-羧基乙酰氧-6-(4-羧基-1,3-丁二烯羰氧)桂皮酰]奎尼酸和3-o-[e-2,5-二羧基乙酰氧-3-(10-羧基-1,3,5,7-癸四烯羰氧)-4-(8-羧基-1,3,5-辛三烯羰氧)-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸;所述11种槲皮素类化合物为3-o
-ꢀ
葡萄糖苷-2
’-
甲酰氧-3
’-
(3-羧基丙烯酰氧)-4
’-
羧基乙酰氧-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素,3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(10-羧基-1,3-癸二烯羰氧)-4
’-
(5-羧基
ꢀ-
2-戊烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素,3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(6-羧基-1-己烯羰氧)-4
’-
(6-羟基-2-己烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(5-羟基
ꢀ-
1-戊烯羰氧)槲皮素,3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(7-羟基-1,3,5-庚三烯羰氧)-4
’-
(4-羧基-2
-ꢀ
丁烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(7-羧基-1,3-庚二烯羰氧)槲皮素,3-o-葡萄糖苷-2
’-ꢀ
甲酰氧-3
’-
(8-羧基-1,3,5-辛三烯羰氧)-4
’-
(5-羧基-1-戊烯羰氧)-5
’-
(5-羧基-1,3-戊二烯羰氧)-6
’-
(6-羟基-1,3,5-己三烯羰氧)槲皮素,3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(4-羧基丁羰氧)-4
’-
(3-羧基丙羰氧)-5
’-
(4-羟基丁羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素,3-o-葡萄糖苷
ꢀ-2’-
甲酰氧-3’,6
’-
二(7-羟基-1-庚烯羰氧)-4
’-
(4-羧基-1-丁烯羰氧)-5
’-
(3-羧基-1-丙
羧基-1-丙烯羰氧)-5-甲酰氧-6-(6-羧基-1,3,5-己三烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0023]
图13冬凌草叶水提物粉末中的3-o-[e-2-(4-羟基-1,3-丁二烯羰氧)-3-羧乙酰氧-4-(3
-ꢀ
羧基-1-丙烯羰氧)-5-甲酰氧-6-(4-羧基-1,3-丁二烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0024]
图14冬凌草叶水提物粉末中的3-o-[e-2,3-二(3-羧基丙羰氧)-4-(3-羧基丙酰氧)-5-甲酰氧-6-(6-羧基-1-己烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0025]
图15冬凌草叶水提物粉末中的3-o-[e-2,3-二(3-羧基丙羰氧)-4-(3-羟基丙酰氧)-5-羟甲氧-6-(5-羧基戊羰氧)桂皮酰]奎尼酸及裂解产物。
[0026]
图16冬凌草叶水提物粉末中的3-o-[e-2,6-二(5-羧基-1-戊烯羰氧)-3-(3-羧基丙羰氧)-4-羧基乙酰氧-5-甲氧桂皮酰]奎尼酸及裂解产物。
[0027]
图17冬凌草叶水提物粉末中的3-o-[e-2-(8-羧基-1-辛烯羰氧)-3-(3-羧基丙羰氧)-4-(7
-ꢀ
羧基-1-庚烯羰氧)-5-羧基乙酰氧-6-(4-羧基-1-丁烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0028]
图18冬凌草叶水提物粉末中的3-o-[e-2-(9-羟基-1-壬烯羰氧)-3-(4-羟基丁羰氧)-4-(8
-ꢀ
羟基-1-辛烯羰氧)-5-甲氧-6-(4-羧基-1-丁烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0029]
图19冬凌草叶水提物粉末中的3-o-[e-2-(7-羧基-1,3,5-庚三烯羰氧)-3,4-二(5-羧基
ꢀ-
1,3-戊二烯羰氧)-5-羧基乙酰氧-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0030]
图20冬凌草叶水提物粉末中的3-o-[e-2-(4-羟基-1-丁烯羰氧)-3-(4-羧基-1-丁烯羰氧)-4-(3-羧基丙烯酰氧)-5-羧基乙酰氧-6-(4-羧基-1,3-丁二烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0031]
图21冬凌草叶水提物粉末中的3-o-[e-2-(7-羧基-1,3,5-庚三烯羰氧)-3-(8-羟基
ꢀ-
1,3,5,7-辛四烯羰氧)-4,5-二(4-羧基-1,3-丁二烯酰氧)-6-(6-羧基-1,3,5-己三烯羰氧)桂皮酰] 奎尼酸及裂解产物。
[0032]
图22冬凌草叶水提物粉末中的3-o-[e-2-(4-羟基丁羰氧)-3,4-二(3-羧基丙羰氧)-5-(3
-ꢀ
羟基丙酰氧)-6-(4-羧基丁羰氧)桂皮酰]奎尼酸及裂解产物。
[0033]
图23冬凌草叶水提物粉末中的3-o-[e-2,6-二(5-羧基-1-戊烯羰氧)-3-(3-羧基丙羰氧)-4-(3-羧基丙酰氧)-5-羟基桂皮酰]奎尼酸及裂解产物。
[0034]
图24冬凌草叶水提物粉末中的3-o-[e-2,5-二(7-羧基-1,3-庚二烯羰氧)-3-(6-羟基-1,3
-ꢀ
己二烯羰氧)-4-(4-羧基-1,3-丁二烯羰氧)-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0035]
图25冬凌草叶水提物粉末中的3-o-[e-2-(5-羟基-1-戊烯羰氧)-3,4-二(4-羧基-1-丁烯羰氧)-5-羧基乙酰氧-6-(4-羧基-1,3-丁二烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0036]
图26冬凌草叶水提物粉末中的3-o-[e-2,5-二羧基乙酰氧-3-(10-羧基-1,3,5,7-癸四烯羰氧)-4-(8-羧基-1,3,5-辛三烯羰氧)-6-(6-羧基-1,3-己二烯羰氧)桂皮酰]奎尼酸及裂解产物。
[0037]
图27冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(3-羧基丙烯酰氧)-4
’-
羧基乙酰氧-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素及裂解产物。
[0038]
图28冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(10-羧基-1,3-癸二烯羰氧)-4
’-
(5-羧基-2-戊烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素及裂解产物。
[0039]
图29冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(6-羧基-1-己烯羰氧)-4
’-
(6-羟基-2-己烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素及裂解产物。
[0040]
图30冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(7-羟基-1,3,5-庚三烯羰氧)-4
’-
(4-羧基-2-丁烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)-6
’-
(7-羧基-1,3-庚二烯羰氧)槲皮素及裂解产物。
[0041]
图31冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(8-羧基-1,3,5-辛三烯羰氧)-4
’-
(5-羧基-1-戊烯羰氧)-5
’-
(5-羧基-1,3-戊二烯羰氧)-6
’-
(6-羟基-1,3,5-己三烯羰氧)槲皮素及裂解产物。
[0042]
图32冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(4-羧基丁羰氧)-4
’-
(3-羧基丙羰氧)-5
’-
(4-羟基丁羰氧)-6
’-
(5-羟基-1-戊烯羰氧)槲皮素及裂解产物。
[0043]
图33冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3’,6
’-
二(7-羟基-1-庚烯羰氧)-4
’-
(4-羧基-1-丁烯羰氧)-5
’-
(3-羧基-1-丙烯羰氧)槲皮素及裂解产物。
[0044]
图34冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(7-羧基-1,3,5-庚三烯羰氧)-4’,5’,6
’-
三(5-羧基-1,3-丁二烯羰氧)槲皮素及裂解产物。
[0045]
图35冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(7-羧基-1,3,5-庚三烯羰氧)-4’,5
’-
二(5-羧基-1,3-戊二烯羰氧)-6
’-
(7-羧基-1,3-庚二烯羰氧)槲皮素及裂解产物。
[0046]
图36冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲酰氧-3
’-
(4-羧基丁羰氧)-4
’-
(3-羧基丙羰氧)-5
’-
(4-羟基丁羰氧)-6
’-
(5-羟基戊羰氧)槲皮素及裂解产物。
[0047]
图37冬凌草叶水提物粉末中的3-o-葡萄糖苷-2
’-
甲氧-3
’-
(7-羟基-1-庚烯羰氧)-4’,5
’-ꢀ
二(5-羟基-1-戊烯羰氧)-6
’-
(8-羟基-1,3-辛二烯羰氧)槲皮素及裂解产物。
具体实施方式
[0048]
为了进一步阐述本发明,下面给出一系列实施例。这些实施例完全是例证性的,它们仅用来对本发明进行具体描述,不应当理解为对本发明的限制。
[0049]
实施例1制备冬凌草叶水提物粉末
[0050]
干冬凌草叶用自来水洗洗净,取300g洗净的叶在700-1200ml蒸馏水中于 50℃-100℃加热0.5-4小时,同时搅拌(200-400rpm)。冷却至室温,过滤,滤液减压浓缩得到90g冬凌草叶水提物粉末。或者新鲜的冬凌草叶用自来水洗洗净,取1350g洗净的叶在1500-2500ml蒸馏水中于50℃-100℃加热0.5-4小时,同时搅拌(200-400rpm)。冷却至室温,过滤,滤液减压浓缩得到90g冬凌草叶水提物粉末。
[0051]
实施例2测定冬凌草叶水提物粉末的色谱和质谱离子流谱
[0052]
2-1.样品溶液的制备(10mg/ml)
[0053]
称取26.7mg冬凌草叶水提物粉末,用2.67ml超纯水中将粉末溶解。得到的溶液经超声震荡1分钟,之后再于13000r/min离心10分钟。取上清液,过0.22μm滤膜,置于样品瓶中
供色谱和质谱测定用。
[0054]
2-2色谱条件
[0055]
色谱柱:waters,acquityhss t3柱(2.1
×
100mm i.d.,1.7μm);进样体积:2μl; pda检测器:190-400nm;流动相:水(0.1%甲酸),乙腈;采用这种流动相并按表1的梯度洗色谱柱。
[0056]
表1流动相梯度表
[0057][0058]
2-3.测定色谱图
[0059]
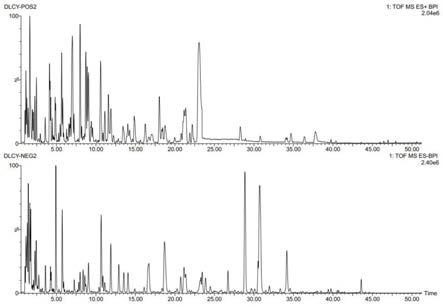
按照上面的色谱测定条件测定并记录冬凌草叶水提物粉末的uplc色谱图(见说明书附图1)。
[0060]
2-4.测定离子流谱和质谱的条件
[0061]
电喷雾离子化模式为正(pi)及负(ni)模式。离子模式参数:毛细管电压为1000v,去溶剂气流速为800l/h,温度450℃,源温度为120℃,锥孔气流速为50l/h,喷雾气压为6bar, 碎裂电压为20-45v,取样锥电压为6v,采集模式为mse continuum分辨率模式,带电粒子的质量数与电荷数之比(m/z)数据采集范围为100-1500,低能量通道trap碎裂电压为6v, 高能量通道trap碎裂电压选择梯度电压为20-60v,选取le(亮氨酸脑啡肽)为质量锁采集 m/z,范围为100-1500。
[0062]
2-5.记录离子流谱和质谱
[0063]
按照上面的条件测定并记录冬凌草叶水提物粉末的离子流谱(见说明书附图1)。
[0064]
实施例3指定冬凌草叶水提物粉末中36种组分的结构
[0065]
将实施例2的uplc色谱与质谱联接,测定冬凌草叶水提物粉末的uplc-质谱。质谱条件是电喷雾离子化的正离子和负离子两种模式。离子模式参数:毛细管电压为1000 v,去溶剂气流速为800l/h,温度450℃,源温度为120℃,锥孔气流速为50l/h,喷雾气压为6bar,碎裂电压为20-45v,取样锥电压为6v,采集模式为mse continuum分辨率模式,带电粒子的质量数与电荷数之比(m/z)数据采集范围为100-1500,低能量通道trap碎裂电压为6v,高能量通道trap碎裂电压选择梯度电压为20-60v,选取le(亮氨酸脑啡肽) 为质量锁采集m/z,范围为100-1500。在45分钟内分出36个独立峰。根据质谱裂解规律, 这些峰(按照总离子流图谱从左到右的峰顺序)的结构指定见表2。
[0066]
表2测得的总离子流图谱中峰对应组分保留时间,负离子质量数,结构及名称
[0067]
[0068]
[0069]
[0070]
[0071]
[0072][0073]
[0074]
实施例4评价冬凌草叶水提物粉末的抗肿瘤作用
[0075]
icr雄性小鼠,体重20
±
2g,从由北京维通利华实验动物技术有限公司购买。实验分为生理盐水(空白对照)组,阿霉素(阳性对照)组和冬凌草叶水提物粉末组。每组12只小鼠。小鼠腋皮下接种s180腹水瘤。无菌条件下抽取生长旺盛的s180腹水瘤瘤液,用生理盐水稀释成为1:2的液体之后充分混合。制得的肿瘤细胞悬液用新鲜配制的0.2%台盼蓝染色, 混匀后按白细胞计数方法计数,染蓝色者为死细胞,不染色者为活细胞。按公式计算细胞浓度和细胞存活率。即细胞浓度=4大方格内活细胞数/4
×
104×
稀释倍数=细胞数/ml。细胞存活率=活细胞数/(活细胞数+死细胞数)
×
100%。将存活率大于90%的瘤液用匀浆法制备成2.0
×
107个/ml的细胞悬液,按每只小鼠0.2ml细胞悬液接种于鼠腋皮下,造成s180腹水实体瘤小鼠模型。
[0076]
小鼠接种s180瘤细胞悬液之后,生理盐水组的小鼠每天按照0.2ml/只小鼠口服生理盐水,连续口服7天;阿霉素组的小鼠每天按照2μmol/kg腹腔注射阿霉素,连续注射7天;冬凌草茎水提物粉末组的小鼠每天按照35mg/kg口服;冬凌草茎水提物粉末,连续口服7 天。第8天称小鼠体重,乙醚麻醉之后脱颈椎处死。用镊子固定小鼠右腋肿瘤生长部位,剪开皮肤,暴露肿瘤,钝性剥离,称重。用瘤重表示冬凌草叶水提物粉末的抗肿瘤活性。结果见表3。结果表明在35mg/kg/天口服剂量下冬凌草叶水提物粉末有明确的抗肿瘤作用。
[0077]
表3冬凌草叶水提物粉末的抗肿瘤活性
[0078][0079]
a)与生理盐水比p<0.05;n=12。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1