一种治疗肝癌的联合用药物的制作方法
本发明涉及抗癌药物领域,具体涉及一种治疗肝细胞癌的联合用药物。
背景技术:
肝细胞癌是最常见的原发性肝癌病理亚型,是全球第五大原发性恶性肿瘤,也是癌症相关死亡的第二大原因。尽管目前临床上有多种肝癌治疗方法,由于肝细胞癌早期临床表现不典型,大多数肝细胞癌患者确诊时已经是晚期,错过最佳治疗时机,因而肝细胞癌预后极差。美国食品和药物管理局(fda)批准的肝癌一线治疗用药索拉非尼明显改善了肝细胞癌患者的中位生存期,但由于原发性耐药或继发性耐药的原因,索拉非尼在肝细胞癌治疗中的临床获益是有限的。
mtor通路激活见于多种肿瘤中,参与了肿瘤的发生发展,并且能够导致索拉非尼耐药。临床试验并没有足够的证据证明几种常用的mtor通路抑制剂的抗肿瘤疗效,因此目前并没有获批用于抗肿瘤常规临床应用的mtor抑制剂。
临床上肿瘤患者常伴有不同程度的心境障碍。五羟色胺抑制剂即选择性5-ht再摄取抑制剂(ssris),是临床上应用最广泛的抗抑郁药,常用于治疗肿瘤患者的抑郁心境。而舍曲林与氟西汀是这种抗抑郁药中最常见的类型。目前有临床研究表明,五羟色胺再摄取抑制剂的应用能够降低包括肝癌在内的多种肿瘤的发病率,众多临床前研究中也表明五羟色胺再摄取抑制剂能够抑制mtor通路。
然而,目前在肝细胞癌的治疗中,五羟色胺再摄取抑制剂对mtor通路的作用关系并不明确,因此,五羟色胺再摄取抑制剂与索拉菲尼联合用药治疗肝细胞癌的具体比例剂量及其确切的联合用药效果仍未见报道。
为了解决索拉菲尼耐药性的问题,探索临床常用的索拉菲尼和5-ht再摄取抑制剂的联合用药,对肝癌患者的治疗有非常重要的意义,具有很好的临床应用前景。
技术实现要素:
本发明的目的在于提供一种治疗肝癌的联合用药物。
本发明提供了一种治疗肝癌的联合用药物,其特征在于,它含有相同或不同规格单位制剂的用于同时或者分别给药的五羟色胺再摄取抑制剂和抗肿瘤药物,以及药学上可接受的载体;
所述五羟色胺再摄取抑制剂为舍曲林或氟西汀,和/或所述抗肿瘤药物为索拉菲尼。
进一步地,上述联合用药物是治疗肝细胞癌的联合用药物。
进一步地,上述舍曲林和抗肿瘤药物的浓度分别为2.5μm和5μm;或,上述舍曲林和抗肿瘤药物的质量比为1:1。
进一步地,上述氟西汀和抗肿瘤药物的浓度比为(3.75μm~5μm):5μm,摩尔比为(0.75~1):1。
更进一步地,上述氟西汀和抗肿瘤药物的浓度比为3.75μm:5μm或5μm:5μm,摩尔比为0.75:1或1:1。
本发明还提供了上述联合用药物在制备治疗肝癌的药物中的用途,优选地,所述治疗肝癌的药物是治疗肝细胞癌的药物。
本发明还提供了五羟色胺再摄取抑制剂和抗肿瘤药物在制备治疗肝癌的联合用药物中的用途,所述五羟色胺再摄取抑制剂为舍曲林或氟西汀,和/或所述抗肿瘤药物为索拉菲尼;优选地,所述治疗肝癌的联合用药物为治疗肝细胞癌的联合用药物。
进一步地,上述舍曲林和抗肿瘤药物的浓度分别为2.5μm和5μm;或,上述舍曲林和抗肿瘤药物的质量比为1:1。
进一步地,上述氟西汀和抗肿瘤药物的浓度比为(3.75μm~5μm):5μm,摩尔比为(0.75~1):1。
更进一步地,上述氟西汀和抗肿瘤药物的浓度比为3.75μm:5μm或5μm:5μm,摩尔比为0.75:1或1:1。
实验结果表明,本发明使用五羟色胺再摄取抑制剂舍曲林或氟西汀,与索拉非尼联合用药具有协同增效作用,可有效抑制肝细胞癌细胞系在体内或者体外的生长,其抗癌效果明显优于五羟色胺再摄取抑制剂舍曲林(sertraline)与氟西汀(fluoxetine)或索拉非尼单独使用。在此基础上可进一步通过药物辅料等药学上可接受的方式制成ssris和索拉菲尼的药用组合物或制剂。同时,本发明联合使用的舍曲林、氟西汀和索拉菲尼均为临床常用药,安全有效,具有很好的临床应用前景。
本发明所指的五羟色胺再摄取抑制剂又名5-ht再摄取抑制剂、选择性5-ht再摄取抑制剂、5-羟色胺再摄取抑制剂、ssris。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
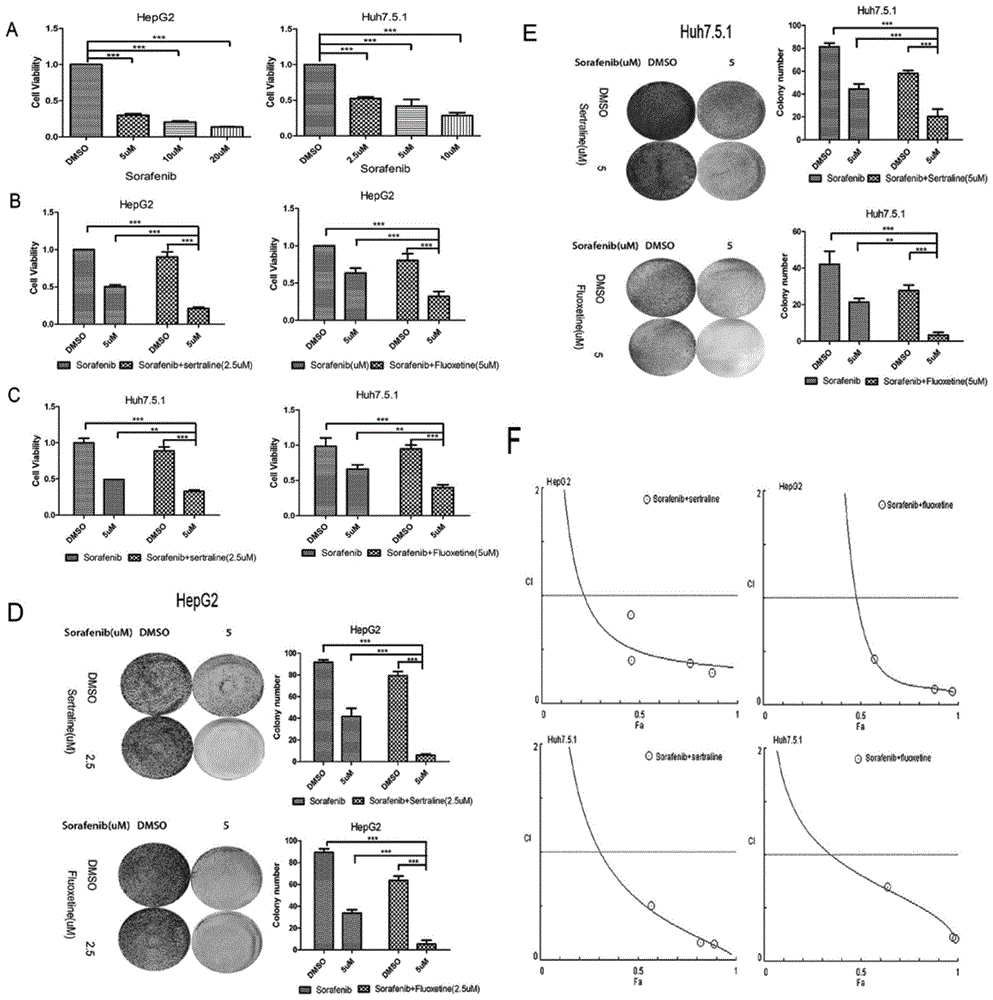
图1舍曲林或氟西汀增强了索拉非尼的细胞毒性作用:(a)索拉非尼作用后mtt检测细胞增殖;(b-c)舍曲林或氟西汀分别与索拉非尼联合后mtt检测细胞增殖;(d-e)舍曲林或氟西汀分别与索拉非尼联合后克隆形成实验;(f)联合指数;
图2(a-d)舍曲林与索拉非尼联合或氟西汀与索拉非尼联合作用hepg2、huh7.5.1细胞的蛋白免疫印迹。
图3原发性肝癌模型中舍曲林或氟西汀增强了索拉非尼的抗肝细胞癌作用:(a)原发性肝癌模型中舍曲林或氟西汀单独应用抑制了肿瘤体积,分别与索拉菲尼联合后能增强索拉非尼以及舍曲林或氟西汀单独应用抗肝癌的作用;(b)舍曲林或氟西汀单独应用或分别与索拉非尼联合应用体内抑制肿瘤体积统计图;(c)舍曲林或氟西汀单独应用或分别与索拉非尼联合应用体内抑制肿瘤数目统计图。
说明:附图中sertraline表示舍曲林,fluoxetine表示氟西汀,sorafenib代表索拉非尼,den代表二甲基亚硝胺,ccl4代表四氯化碳,dmso为二甲基亚砜,*表示显著差异(p<0.05);**表示极显著差异(p<0.01);***表示非常显著的差异(p<0.001)。
具体实施方式
实验原料:舍曲林,氟西汀与索拉非尼均购自上海陶素生化有限公司。dmem培养基(gibio,usa)、胎牛血清(gibio,usa)。mtt试剂盒(sigma)二甲基亚砜dmso(sigma)。二乙基亚硝胺den(梯希爱(上海)化成工业发展有限公司),四氯化碳ccl4(天津富宇精细化工有限公司),橄榄油(科隆测量仪器(上海)有限公司)。c57bl/6小鼠以及实验中所用裸鼠购自北京华阜康生物科技股份有限公司。细胞裂解液(sigma);酶标仪,bca试剂盒(sigma)。电泳电转系统(bio-rad)。抗体gapdh购自santa/santacruz,mtor,p-mtor购自proteintech,其余抗体购自abcam。pvdf膜(millipore,bedford,usa)孵育二抗(li-corbiosciences,usa)后膜曝光用odyssey双色红外荧光扫描成像系统。免疫组化实验所用试剂盒为从中杉金桥购买的免疫组化试剂盒(sp9001)。
实验例1舍曲林或氟西汀与索拉非尼联合使用的细胞毒性作用
1.实验材料
人源性肝癌细胞株:huh7.5.1,hepg2。
肝细胞癌靶向治疗药物:索拉非尼。
五羟色胺再摄取抑制剂:舍曲林,氟西汀。
2.实验方法
2.1实验处理:
mtt检测细胞增殖活性:使用二甲基亚砜dmso分别配制浓度为150mm的舍曲林与氟西汀溶液母液存放于-80℃。使用前用dmso稀释成浓度为20mm的工作液浓度,并且以此工作液按所需浓度加入培养基中,以0.1%dmso浓度的二甲基亚砜作为对照,单独使用索拉菲尼(2.5μm,5μm,10μm,20μm)、联合使用舍曲林(2.5μm)与索拉菲尼(5μm)、联合使用氟西汀(5μm)和索拉菲尼(5μm)分别处理huh7.5.1与hepg2肝癌细胞株48h。48h后用mtt法测细胞活性,mtt法:将细胞与含有mtt溶液(5mg/ml)的培养基孵育4h,然后去除培养基,将甲瓒晶体溶解于150ul的dmso中。用酶标仪测量490nm处的吸光度。
细胞克隆形成实验:以每孔8×103hepg2细胞,5×103huh7.5.1细胞的量接种于6孔板,使用二甲基亚砜dmso分别配制浓度为150mm的舍曲林与氟西汀溶液母液存放于-80℃。使用前用dmso稀释成浓度为20mm的工作液浓度。并且以此工作液按所需浓度加入培养基中,以0.1%dmso浓度的二甲基亚砜作为对照,联合使用舍曲林(2.5μm)与索拉菲尼(5μm)、联合使用氟西汀(5μm)与索拉菲尼(5μm)分别处理以上两种肝癌细胞株14天。在这期间每两天更换一次培养基与药物,用pbs轻轻洗涤细胞,4%多聚甲醛固定20分钟后用0.5%结晶紫溶液染色15分钟,然后用自来水冲洗板,拍照。
蛋白免疫印迹实验:以每孔20×104hepg2细胞,20×104huh7.5.1细胞的量接种于6孔板,接种后第二天加药。使用二甲基亚砜dmso分别配制浓度为150mm的舍曲林与氟西汀溶液母液存放于-80℃。使用前用dmso稀释成浓度为20mm的工作液浓度,并且以此工作液按所需浓度加入培养基中。以0.1%dmso浓度的二甲基亚砜作为对照,联合使用曲舍林(2.5μm)与索拉菲尼(2.5μm,5μm)、联合使用氟西汀(2.5μm,5μm)与索拉菲尼(2.5μm,5μm)分别处理huh7.5.1与hepg2肝癌细胞株48小时后用细胞裂解液裂解细胞,bca法测蛋白浓度后,进行免疫印迹实验。
2.2检测:
(1)mtt检测细胞增殖活性变化
实验处理48h后,采用mtt检测细胞增殖活性,并利用compusyn软件用周氏公式计算联合指数。
(2)观察细胞克隆形成
实验处理14天后,使用结晶紫染色,观察克隆数量。
(3)蛋白免疫印迹
实验处理48h后,提取细胞总蛋白,进行蛋白免疫印迹,检测β-catenin、c-myc(增殖相关蛋白)、p-erk(增殖相关蛋白)、bcl-xl(凋亡相关蛋白)、parp(凋亡相关蛋白)、p-mtor、mtor、p-akt、akt和gapdh(作为内参)。
3.实验结果
如图1a-f所示,联合使用舍曲林(2.5μm)与索拉非尼(5μm),hepg2细胞的相对增值比例低于25%,huh7.5.1细胞相对增值比例低于30%;hepg2细胞和huh7.5.1细胞克隆数量均低于10个单位数量;而单独使用索拉菲尼(5μm)对于hepg2和huh7.5.1细胞株的相对增值比例均达到了50%左右,hepg2细胞克隆数量达到40个单位数量,huh7.5.1细胞克隆数量超过30个单位数量,均显著高于联合用药组。说明舍曲林与索拉菲尼以0.5:1的摩尔比联合用药,相比于索拉菲尼单独用药具有更显著的抑制肝癌细胞增殖的能力。
联合使用氟西汀(5μm)与索拉非尼(5μm),hepg2细胞的相对增值比例低于30%,huh7.5.1细胞相对增值比例低于35%;hepg2细胞克隆数量约20个单位数量,huh7.5.1细胞克隆数量约5个单位数量;而单独使用索拉菲尼(5μm)对于hepg2和huh7.5.1细胞株的相对增值比例均达到了60%以上;hepg2细胞克隆数量超过40个单位数量,huh7.5.1细胞克隆数量超过20个单位数量,均显著高于联合用药组。说明氟西汀与索拉菲尼以1:1的摩尔比联合用药,相比于索拉菲尼单独用药具有更显著的抑制肝癌细胞增殖的能力。
而且,舍曲林与索拉菲尼联合用药、氟西汀与索拉菲尼联合用药的联合指数ci均小于1,说明本发明的联合用药物具有良好的协同作用。
如图2a-d所示,两种肝癌细胞株中,舍曲林与索拉非尼联合或氟西汀与索拉非尼联合降低了hepg2、huh7.5.1细胞中c-myc、p-erk、bcl-xl、parp、p-mtor、mtor、p-akt、akt蛋白的表达,与mtt实验和集落形成实验结果一致。
4.结论
舍曲林与索拉菲尼联合用药具有协同增效作用,氟西汀与索拉菲尼联合用药具有协同增效作用。本发明的联合用药物能够显著抑制体内肝癌细胞株的生长增殖,特别是2.5μm舍曲林与5μm索拉非尼联合使用的效果特别优良。
实验例2舍曲林或氟西汀与索拉非尼联合在体内抑制原发性肝癌生长
1.动物模型构建:动物模型构建:6-8周龄的雄性c57bl/6小鼠分为空白组、阳性对照组、舍曲林组、氟西汀组、索拉非尼组、舍曲林联合索拉非尼组、氟西汀联合索拉非尼组。除空白组小鼠外,其余组别小鼠从第一周开始腹腔注射用生理盐水配制的二乙基亚硝胺(den)(50mg/kg体重),7天以后再次注射相同剂量的den,再过7天以后再次注射相同剂量的den(den总共注射三次),从第四周开始,每周口服四氯化碳(ccl4),四氯化碳用橄榄油配制,按橄榄油:ccl4体积比为4:1配制,每次口服给药,按5ml/kg体重剂量给药,每周两次,直到从第一次注射ccl4后22周处死小鼠。
2.实验方法
2.1实验处理:原发性肝癌模型分为空白组、阳性对照组、舍曲林组、氟西汀组、索拉非尼作、舍曲林联合索拉非尼组、氟西汀联合索拉非尼组,从第一次应用ccl4后14周时开始给药:舍曲林组(20mg/kg体重,口服)每天一次;氟西汀组(10mg/kg体重,口服)每天一次;索拉非尼(20mg/kg体重,口服);舍曲林联合氟西汀组【舍曲林(20mg/kg体重,口服)每天一次+索拉非尼(20mg/kg体重,口服)】;氟西汀联合索拉非尼组【氟西汀(10mg/kg体重,口服)每天一次+索拉非尼(20mg/kg体重,口服)】,
直到实验结束。
2.2检测:
在第25周处死小鼠,测定并统计肿瘤体积,数目。
3.实验结果
如图3所示,肿瘤体积方面,与阳性对照组相比,舍曲林、氟西汀、索拉非尼单独用药抑制了肿瘤体积,减少了肿瘤数目,舍曲林或氟西汀分别与索拉非尼联合用药能够进一步减少肿瘤体积与数目。具体而言,舍曲林与索拉非尼按照1:1重量比联合用药能够比舍曲林单药或索拉非尼单药更明显减少肿瘤数目与肿瘤体积;氟西汀与索拉非尼按照1:1重量比联合用药能够比氟西汀单药或索拉非尼单药更明显减少肿瘤数目与肿瘤体积。
4.结论
舍曲林和索拉菲尼联合用药,或氟西汀与索拉菲尼联合用药,相比于舍曲林或氟西汀单独使用,以及索拉菲尼单独使用,能够更明显抑制体内肿瘤生长。
综上,五羟色胺再摄取抑制剂舍曲林或氟西汀能够显著抑制肝癌细胞增殖,并且在体内预防肝癌,五羟色胺再摄取抑制剂与索拉菲尼联合用药具有协同增效作用,其抗癌效果明显优于五羟色胺再摄取抑制剂舍曲林、氟西汀或索拉非尼单独使用。本发明的联合用药物不仅能够在体内外显著抑制肝癌细胞增殖,而且能够在体内发挥治疗原发性肝癌的作用,具有良好的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!