一种抗疲劳组合物及其应用的制作方法
1.本发明涉及药物技术领域,尤其涉及一种抗疲劳组合物及其应用。
背景技术:
2.疲劳已经成为现代中年主要的亚健康问题之一,在越演越烈的职场竞争和工作压力下,疲劳将会成为每个中年最大的困扰。所以,未来抗疲劳产品将越来越受到人们的青睐,并且具有广阔的市场。中医药作为我国独特的卫生资源、潜力巨大的经济资源、具有原创优势的科技资源、优秀的文化资源和重要的生态资源,将在抗疲劳产品的研发中扮演重要的角色。
3.因此,开发新的效果好的抗疲劳药物成为一大研究热点。
技术实现要素:
4.有鉴于此,本发明的目的在于提供一种抗疲劳组合物及其应用,本发明提供的抗疲劳组合物具有优异的抗疲劳效果。
5.为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了一种抗疲劳组合物,包括枸杞糖肽和鹿血多肽;所述枸杞糖肽和鹿血多肽的质量比为1:2~2:1;
7.所述枸杞糖肽的纯度≥80%;
8.所述鹿血多肽由鹿血经脂肪酶和木瓜蛋白酶特异性酶解制得。
9.优选地,所述枸杞糖肽和鹿血多肽的质量比为2:1。
10.优选地,所述枸杞糖肽由包括以下步骤的方法制备得到:
11.对枸杞粉进行亚临界丁烷萃取,收集萃取渣;
12.对所述萃取渣进行乙醇水溶液提取,收集枸杞渣;所述乙醇水溶液的体积浓度为75~85%;
13.对所述枸杞渣进行亚临界水提取,收集提取液,将所述提取液离心,收集上清液;
14.对所述上清液进行浓缩,得到浓缩液;
15.采用无机物-有机物-水体系对所述浓缩液进行萃取,收集无机物相为枸杞糖肽溶液;
16.将所述枸杞糖肽溶液稀释后,上吸附柱,收集吸附残液;
17.将所述吸附残液浓缩、冷冻干燥,得到所述枸杞糖肽。
18.优选地,所述亚临界丁烷萃取的料液比为1kg:(1.2~1.8)l;压力为0.3~0.8mpa,温度为25~40℃,时间为30~60min。
19.优选地,所述萃取渣与乙醇水溶液的用量比为1kg:(8~12)l,所述乙醇水溶液提取的温度为70~75℃,时间为2h,提取次数为1~2次。
20.优选地,所述亚临界水提取的料液比为1kg:(20~25)l,温度为115~125℃,时间为0.5h。
21.优选地,所述无机物-有机物-水体系中,无机物为磷酸二氢钾、磷酸氢二钾和硫酸铵中的一种或几种,无机物的质量百分含量为15~30%;有机物为聚乙二醇、乙二醇或无水乙醇,有机物的质量百分含量为15~30%。
22.优选地,所述鹿血多肽由包括以下步骤的方法制备得到:
23.将鹿血解冻后离心,收集血清溶液;
24.将所述血清溶液在ph值为5.28~5.32的条件下加热、离心,得到待酶解料液;
25.将所述待酶解料液、脂肪酶和木瓜蛋白酶混合,进行特异性酶解,得到酶解液;
26.将所述酶解液离心,收集上清液;
27.将所述上清液浓缩、冷冻干燥,得到所述鹿血多肽。
28.优选地,所述待酶解料液、脂肪酶和木瓜蛋白酶的用量比为100l:(18~22)g:(45~55)g。
29.本发明还提供了上述技术方案所述的抗疲劳组合物在功能食品和药物领域中的应用。
30.本发明提供了一种抗疲劳组合物,包括枸杞糖肽和鹿血多肽;所述枸杞糖肽和鹿血多肽的质量比为1:2~2:1;所述枸杞糖肽的纯度≥80%;所述鹿血多肽由鹿血经脂肪酶和木瓜蛋白酶特异性酶解制得。本发明将具有通过增加骨骼肌细胞有氧呼吸促进atp的产生从而发挥抗疲劳作用的枸杞糖肽,和富含支链氨基酸能够减少5-羟色胺的生成和积聚,同时通过减轻运动性肌肉损伤进而达到延缓和削弱运动性疲劳作用的鹿血多肽,按照固定剂量组合复配形成组合物,两者通过多种模式发挥抗疲劳作用。本发明的抗疲劳组合物相较于枸杞糖肽或鹿血多肽单独使用,缓解体力疲劳的作用更为显著,说明本发明提供的抗疲劳组合物具有更优的缓解体力疲劳功效,枸杞糖肽和鹿血多肽具有协同增效的作用。本发明的组合物能够作为功能食品、保健食品和药物的原料。
具体实施方式
31.本发明提供了一种抗疲劳组合物,包括枸杞糖肽和鹿血多肽。
32.在本发明中,所述枸杞糖肽和鹿血多肽的质量比为1:2~2:1,具体优选为1:2、1:1或2:1,最优选为2:1。在本发明中,所述枸杞糖肽的纯度≥80%。在本发明中,所述枸杞糖肽优选由包括以下步骤的方法制备得到:
33.对枸杞粉进行亚临界丁烷萃取,收集萃取渣;
34.对所述萃取渣进行乙醇水溶液提取,收集枸杞渣;所述乙醇水溶液的体积浓度为75~85%;
35.对所述枸杞渣进行亚临界水提取,收集提取液,将所述提取液离心,收集上清液;
36.对所述上清液进行浓缩,得到浓缩液;
37.采用无机物-有机物-水体系对所述浓缩液进行萃取,收集无机物相为枸杞糖肽溶液;
38.将所述枸杞糖肽溶液稀释后,上吸附柱,收集吸附残液;
39.将所述吸附残液浓缩、冷冻干燥,得到所述枸杞糖肽。
40.本发明对枸杞粉进行亚临界丁烷萃取,收集萃取渣。在本发明中,所述亚临界丁烷萃取的料液比优选为1kg:(1.2~1.8)l,进一步优选为1kg:1.5l;所述亚临界丁烷萃取的压
力优选为0.3~0.8mpa,进一步优选为0.4~0.7mpa,更优选为0.5~0.6mpa;所述亚临界丁烷萃取的温度优选为25~40℃,进一步优选为30~35℃;所述亚临界丁烷萃取的时间优选为30~60min。在本发明中,所述亚临界丁烷萃取能够将枸杞粉中的脂类和色素提取出来并除去。
41.得到萃取渣后,本发明对所述萃取渣进行乙醇水溶液提取,收集枸杞渣。在本发明中,所述乙醇水溶液的体积浓度优选为75~85%,进一步优选为80%。在本发明中,所述萃取渣与乙醇水溶液的用量比优选为1kg:(8~12)l,进一步优选为1kg:10l;所述乙醇水溶液提取的温度优选为70~75℃,时间优选为2h,提取次数优选为1~2次。在本发明中,所述乙醇水溶液提取优选在搅拌的条件下进行,所述搅拌的转速优选为120rpm。在本发明中,所述乙醇水溶液提取结束后,本发明优选还包括将所得乙醇水溶液提取体系进行滤液去除和离心;所述滤液去除优选在双联过滤器中进行;所述离心优选在三足式离心机上进行,所述三足式离心机的转速优选为3500rpm。在本发明中,当所述乙醇水溶液提取的次数优选为2次时,所述提取的具体过程优选为:将第一次提取所得的提取体系进行滤液去除,所得滤渣进行第二次提取;所述滤液去除优选在双联过滤器中进行。在本发明中,所述乙醇水溶液提取能够将萃取渣中的单糖、低聚糖、苷类及生物碱提取出来并除去,进一步纯化枸杞糖肽。
42.得到枸杞渣后,本发明对所述枸杞渣进行亚临界水提取,收集提取液,将所述提取液离心,收集上清液。在本发明中,所述亚临界水提取的料液比优选为1kg:(20~25)l,进一步优选为1kg:(22~24)l;所述亚临界水提取的温度优选为115~125℃,进一步优选为120℃;时间优选为0.5h。在本发明中,所述离心的转速优选为16000rpm;所述离心优选在管式离心机上进行。在发明中,所述亚临界水提取能够将枸杞渣中的枸杞糖肽提取出来,且能够使蛋白质变性,为后续的分离纯化带来方便。
43.得到上清液后,本发明对所述上清液进行浓缩,得到浓缩液。在本发明中,所述浓缩的方式优选为采用分子量为5kd的超滤膜膜系统进行浓缩;所述浓缩的压力为10bar,温度优选为40℃。
44.得到浓缩液后,本发明采用无机物-有机物-水体系对所述浓缩液进行萃取,收集无机物相为枸杞糖肽溶液。在本发明中,所述无机物-有机物-水体系中,无机物优选为磷酸二氢钾、磷酸氢二钾和硫酸铵中的一种或几种,进一步优选为硫酸铵;有机物优选为聚乙二醇、乙二醇或无水乙醇,进一步优选为无水乙醇;在本发明中,所述无机物-有机物-水体系中,无机物的质量百分含量优选为15~30%,进一步优选为20~25%;有机物的质量百分含量优选为15~30%,进一步优选20~28%。在本发明中,所述萃取优选在搅拌的条件下进行,所述搅拌的转速优选为120rpm,时间优选为1h。在本发明中,无机物-有机物-水体系的萃取能够进一步除去游离蛋白质,从而纯化枸杞糖肽。
45.得到枸杞糖肽溶液后,本发明将所述枸杞糖肽溶液稀释后,上吸附柱,收集吸附残液。在本发明中,所述稀释用溶剂优选为水,所述稀释用溶剂与枸杞糖肽溶液的体积比优选为10:1。在本发明中,所述吸附柱优选为lsa-900e的大孔吸附树脂串联柱;所述上吸附柱的流速优选为10~15bv/h,其中,bv代表柱体积。在本发明中,所述吸附柱能够将色素类物质吸附,进一步纯化枸杞糖肽。
46.得到吸附残液后,本发明将所述吸附残液浓缩、冷冻干燥,得到所述枸杞糖肽。在本发明中,所述浓缩的方式优选为采用分子量为5kd的超滤膜膜系统进行浓缩;所述浓缩的
压力优选为10bar,温度优选为40℃。在本发明中,所述冷冻干燥的参数优选包括:样品温度优选低于-25℃,冷阱温度优选低于-55℃,压力优选低于25pa。
47.本发明制备的枸杞糖肽纯度优选≥85%,不同于市面上的枸杞糖肽的水提取液,更容易通过增加骨骼肌细胞有氧呼吸促进atp的产生,从而发挥抗疲劳作用。
48.在本发明中,所述鹿血多肽由鹿血经脂肪酶和木瓜蛋白酶特异性酶解产生的。在本发明中,所述鹿血多肽优选由包括以下步骤的方法制备得到:
49.将鹿血解冻,离心,收集血清溶液;
50.将所述血清溶液在ph值为5.28~5.32的条件下加热、离心,得到待酶解料液;
51.将所述待酶解料液与脂肪酶和木瓜蛋白酶混合,进行特异性酶解,得到酶解液;
52.将所述酶解液离心,收集上清液;
53.将所述上清液浓缩、冷冻干燥,得到所述鹿血多肽。
54.本发明将鹿血解冻,离心,收集血清溶液。本发明对所述鹿血解冻的方式不做具体限定,采用本领域技术人员熟知的解冻手段即可。在本发明中,所述离心的转速优选为3000rpm,时间优选为20min。
55.得到血清溶液后,本发明将所述血清溶液在ph值为5.28~5.32的条件下加热、离心,得到待酶解料液。在本发明中,调节ph值的试剂优选为稀盐酸。在本发明中,所述加热的温度优选为60℃,时间优选为2h。在本发明中,所述清液在ph值为5.28~5.32的条件下进行加热的具体操作优选为:将所述清液加热至指定温度,然后调节ph值后,进行加热保温。在本发明中,所述离心的转速优选为3000rpm,时间优选为20min;所述离心优选在三足式离心机上进行。在本发明中,所述加热能够进一步促进酶解反应。
56.得到待酶解料液后,本发明将所述待酶解料液与脂肪酶和木瓜蛋白酶混合,进行特异性酶解,得到酶解液。在本发明中,所述待酶解料液与脂肪酶和木瓜蛋白酶的用量比优选为100l:(18~22)g:(45~55)g,进一步优选为100l:20g:50g。在本发明中,所述混合优选在搅拌的条件下进行,所述搅拌的时间优选为1.0h。在本发明中,所述特异性酶解的温度优选为90℃,时间优选为9h,在本发明中,所述特异性酶解的过程优选为:将混合料液升温至特异性酶解的温度,搅拌1h,然后停止搅拌,静置8h。在本发明中,所述特异性酶解能够将鹿血血清蛋白转化为多肽。
57.得到酶解液后,本发明将所述酶解液离心,收集上清液。在本发明中,所述离心的转速优选为16000rpm;所述离心优选在管式离心机上进行。
58.得到上清液后,本发明将所述上清液浓缩、冷冻干燥,得到所述鹿血多肽。在本发明中,所述浓缩的方式优选为采用分子量为360的纳滤膜膜系统进行浓缩,所述冷冻干燥的参数优选包括:样品温度低于-25℃,冷阱温度低于-55℃,压力低于25pa。
59.本发明使用的鹿血多肽支链氨基酸含量更高,具有良好的抗疲劳作用。
60.本发明还提供了上述技术方案所述的抗疲劳组合物在功能食品和药物领域中的应用。在本发明中,当所述抗疲劳组合物用于功能食品和药物领域时,对所述抗疲劳组合物的添加量不做具体限定,本领域技术人员根据实际情况进行选择即可。
61.下面结合实施例对本发明提供的抗疲劳组合物及其应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
62.实施例
63.枸杞糖肽由包括以下步骤的方法制备得到:
64.1)将粉碎的枸杞子25kg装入提取袋中,加入亚临界萃取装置中,按照料液比1kg:1.5l加入37.5l丁烷,设定萃取压力0.8mpa,萃取温度35℃,萃取时间60min。萃取结束后,回收丁烷,萃取液由排料口排出收集,打开亚临界萃取罐,将提取袋取出,获取萃取渣24kg。
65.2)将上述枸杞子渣装入500l提取罐,加入240l体积浓度为80%的乙醇水溶液,升温至70℃后开始搅拌提取,搅拌速度为120rpm,提取2h后,用双联过滤滤除提取液,再向提取罐中加入200l体积浓度为80%的乙醇水溶液,搅拌提取2h,双联过滤,三足式离心(转速3500rpm),得到枸杞渣16kg。
66.3)将枸杞渣加入亚临界水提取装置中,枸杞子粉末按料液比1kg:20l投料,温度120℃,时间30min,亚临界水提取结束后将提取液直接泵入管式离心机,离心速度16000rpm。
67.4)采用分子量为5kd的超滤膜膜系统对所述上清液进行浓缩,压力为10ba,温度40℃,收集浓缩液20l;
68.5)将上述20l浓缩液中加入20l双水相体系(硫酸铵:无水乙醇:水质量比为20:28:52),120rpm搅拌1h,静置4h,收集下层溶液28l。
69.6)将上述28l溶液中加入280l水,泵入lsa-900e的大孔吸附树脂串联柱,上样流速为15bv/h,收集吸附残液295l。
70.7)将上述吸附残液再次采用分子量为5kd的超滤膜膜系统浓缩,压力为10bar,温度40℃,收集浓缩液20l;
71.8)将上述20l浓缩液冷冻干燥,样品温度-25℃,冷阱温度-50℃,压力8pa,冷冻干燥48h,即得白色枸杞糖肽。
72.鹿血多肽由包括以下步骤的方法制备得到:
73.将鹿血解冻,加入管式离心机,3000rpm离心20min,收集血清溶液;
74.将50l血清加入酶解罐i中,加热至60℃,加入稀盐酸,调节ph值至5.3保温2h;采用三足式离心机进行离心,离心转速3000rpm,得到的待酶解液再次泵入酶解罐ii。
75.在酶解罐ii中加入脂肪酶和木瓜蛋白酶,搅拌1h,升温至90℃,搅拌0.5h,停止搅拌,静置8h;所述待酶解液和脂肪酶和木瓜蛋白酶的用量比为100l:20g:50g;
76.将酶解液在管式离心机中于16000rpm离心,收集上清液;
77.将所述上清液通过分子量为360的纳滤膜膜系统进行浓缩,浓缩液冷冻干燥,样品温度为-20℃,冷阱温度为-50℃,压力为20pa,冷冻干燥32h,得鹿血多肽。
78.活性试验(小鼠负重游泳试验)
79.1.动物分组及给药方案
80.购买体重处于19~21g之间的小白鼠,喂养1周之后,对参与实验的小鼠随机分为空白对照组(完全为生理盐水)、枸杞糖肽组(lbp:给药量300mg/kg)、鹿血多肽组(dbp:给药量300mg/kg)、枸杞糖肽和鹿血多肽2:1混合组(2lbp+dbp:给药量300mg/kg)、枸杞糖肽和鹿血多肽1:1混合组(lbp+dbp:给药量300mg/kg)、枸杞糖肽和鹿血多肽1:2混合组(lbp+2dbp:给药量300mg/kg),每组20只。枸杞糖肽和鹿血多肽用生理盐水配制。每天灌胃给药1次,灌胃体积均为10ml/kg,空白对照组动物每天灌胃给予等体积(10ml/kg)生理盐水,并保证每日灌胃的时间固定,持续30天。
81.2.小鼠负重游泳实验
82.在末次灌胃给药后1h,通过在小鼠尾部增添铅皮来完成负重处理,重量为小鼠体重的5%,然后将小鼠置于水温24
±
0.5℃、水深30cm的游泳箱中进行负重游泳。以小鼠头部沉入水中9s不再浮出水面为游泳终止时间,以此对游泳时长进行测定和记录,结果表1所示。
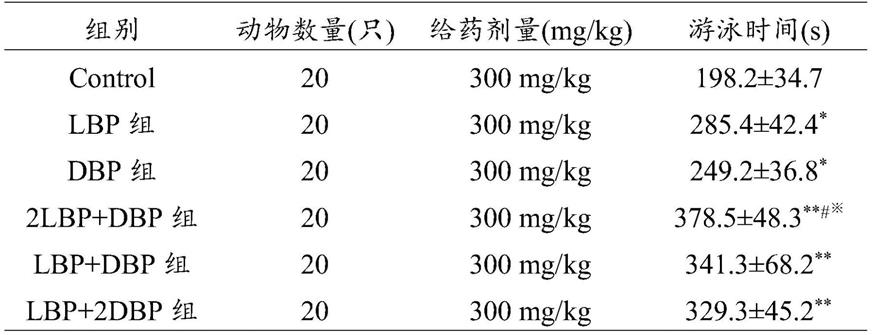
83.表1各组小鼠负重游泳时间比较
[0084][0085]
注:给药组与对照组比较:
*
p<0.05,
**
p<0.01,下同
[0086]
2lbp+dbp组与lbp组或者dbp组比较:
#
p<0.05,下同
[0087]
2lbp+dbp组与lbp+dbp组或者lbp+2dbp组比较:
※
p<0.05,下同
[0088]
从表1可以看出:与对照组相比,各给药组小鼠的负重游泳时间明显延长,其中lbp组和dbp组差异显著(p<0.05),lbp和dbp固定剂量组合组与对照组相比,差异及其显著(p<0.01)。说明:单独枸杞糖肽、单独鹿血多肽还是枸杞糖肽和鹿血多肽的组合,均具有良好的抗疲劳作用。2lbp+dbp组与lbp组或者dbp组相比,小鼠的游泳时间也明显延长,其差异显著(p<0.05),提示枸杞糖肽和鹿血多肽以固定剂量2:1组合给药组的抗疲劳作用明显优于枸杞糖肽或者鹿血多肽单个给药组,两者固定剂量组合具有协同增效的作用;并且,2lbp+dbp组与lbp+dbp组或lbp+2dbp组相比,小鼠的游泳时间也明显延长(p<0.05),说明枸杞糖肽和鹿血多肽以固定剂量2:1组合抗疲劳作用最优。
[0089]
3.生化指标测定
[0090]
小鼠出现力竭后迅速从游泳箱中捞出,休息1h后,眼球取血,静置0.5h,离心获取血清样本。眼球取血后将小鼠脱颈椎处死,取肝组织,加生理盐水匀浆。离心获取上清。按检测试剂盒说明书要求,检测疲劳小鼠丙二醛(mda)含量、乳酸(la)含量、及肝组织肝糖原(lg)含量和肌糖原(mg)含量。结果如表2和表3所示。
[0091]
表2各组小鼠血清mda和la含量比较
[0092][0093]
表3各组小鼠肝糖原lg和肌糖原mg含量比较
[0094][0095]
从表2和表3可以看出:2lbp+dbp组与lbp组或者dbp组单个给药组相比,或者与lbp+dbp组或lbp+2dbp组相比,小鼠运动后,丙二醛和乳酸含量明显下降,肝糖原和肌糖原含量明显上升,且均有显著性差异(p<0.05)。提示枸杞糖肽和鹿血多肽以固定剂量2:1组合给药组的抗疲劳作用,可能是通过下调丙二醛,加速乳酸的清除,提高小鼠糖原水平,为小鼠运动提供充足的能量,从而有效提高小鼠的运动耐力而实现的。
[0096]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1