一种润肠通便的益生菌中草药复方组合物及其应用的制作方法
本发明涉及保健食品技术领域技术领域,更具体的说是涉及一种润肠通便的益生菌中草药复方组合物及其应用。
背景技术:
肠道不仅是消化器官,更是人体最大的免疫排毒器官,人体70%的免疫功能配置在肠道,因此,肠道又被称为“身体健康的第一道防线”。现代生活方式和环境常常危害肠道健康,滥用抗生素、洗肠通便、清肠减肥、压力等,让人们的肠道长期处于亚健康状态,引发便秘、腹泻等症状,困扰人们的生活。
人的老化是从肠道开始的,随着年龄的增加,有益菌在人体内逐渐减少,益生菌的缺乏使肠道运动就越来越呆滞,越容易发生便秘等疾病。目前,市场上常用的润肠通便产品中大部分含有大黄、番泻叶、芦荟、决明子、何首乌等蒽醌类刺激性泻药,虽有短时的通便效果,但长期服用会引起肠道菌群的失调,进而加重便秘,造成营养不良;并且以上几种原料是目前公认的引起结肠黑变病的主要因素,部分蒽醌类泻药还有导致肝功能损伤的风险。
因此,需要提供一种能够有效润肠通便、维持肠道菌群稳定,促进肠道健康的产品。
技术实现要素:
有鉴于此,本发明提供了一种润肠通便的益生菌中草药复方组合物,可有效润肠通便、维持肠道菌群稳定,促进肠道健康。
为了实现上述目的,本发明采用如下技术方案:
一种润肠通便的益生菌中草药复方组合物,包括如下重量份数的原料:
益生菌55-129份,益生元14-134份,中药粉2-15份;
其中,益生菌为鼠李糖乳杆菌、植物乳杆菌、副干酪乳杆菌、乳双歧杆菌、嗜酸乳杆菌、长双歧杆菌、罗伊氏乳杆菌、瑞士乳杆菌、发酵乳杆菌、约氏乳杆菌、干酪乳杆菌、卷曲乳杆菌、短双歧杆菌、两歧双歧杆菌、婴儿双歧杆菌中的13-15种;
益生元为低聚异麦芽糖、菊粉、乳糖醇、水苏糖、低聚果糖、低聚木糖、低聚甘露糖、低聚半乳糖、燕麦β-葡聚糖、聚葡萄糖、可溶性大豆多糖、抗性糊精、壳寡糖10-13种;
中药粉为麦芽、山楂、乌梅、豆豉中的2-4种。
本发明通过添加特定益生菌,针对性地增强宿主肠道功能,平衡肠道菌群;通过添加益生元,可增加肠道中有益菌群的数量;特别添加药食同源中药粉,协同增效,共同促进肠道健康。
进一步地,益生菌中,按重量分数计:
鼠李糖乳杆菌为10-15份,
植物乳杆菌为3-21份,
副干酪乳杆菌为10-15份,
乳双歧杆菌为10-15份,
嗜酸乳杆菌为8-12份,
长双歧杆菌为3-6份,
罗伊氏乳杆菌为3-6份,
瑞士乳杆菌为3-6份,
发酵乳杆菌为3-6份,
约氏乳杆菌为3-6份,
干酪乳杆菌为3-6份,
卷曲乳杆菌为3-6份,
短双歧杆菌为1-3份,
两歧双歧杆菌为1-3份,
婴儿双歧杆菌为1-3份。
进一步地,益生菌中,
鼠李糖乳杆菌为1.3×1011-2.4×1011cfu/g,
植物乳杆菌为0.6×1011-2.7×1011cfu/g,
副干酪乳杆菌为1.3×1011-2.4×1011cfu/g,
乳双歧杆菌为0.8×1011-2×1011cfu/g,
嗜酸乳杆菌为1×1011-2×1011cfu/g,
长双歧杆菌为0.6×1011-4×1011cfu/g,
罗伊氏乳杆菌为0.6×1011-4×1011cfu/g,
瑞士乳杆菌为0.6×1011-4×1011cfu/g,
发酵乳杆菌为0.6×1011-4×1011cfu/g,
约氏乳杆菌为0.6×1011-2.7×1011cfu/g,
干酪乳杆菌为0.6×1011-2.7×1011cfu/g,
卷曲乳杆菌为0.6×1011-2.7×1011cfu/g,
短双歧杆菌为0.8×1011-4.8×1011cfu/g,
两歧双歧杆菌为0.8×1011-4.8×1011cfu/g,
婴儿双歧杆菌为1.3×1011-7.2×1011cfu/g。
进一步地,益生元中,按重量分数计:
低聚异麦芽糖为30-50份,
菊粉为8-11份,
乳糖醇为5-15份,
水苏糖为5-15份,
低聚果糖为1-5份,
低聚木糖为1-5份,
低聚甘露糖为1-5份,
低聚半乳糖为1-5份,
燕麦β-葡聚糖为1-5份,
聚葡萄糖为1-5份,
可溶性大豆多糖为1-5份,
抗性糊精为1-5份,
壳寡糖为1-3份。
进一步地,中药粉中,按重量分数计:
麦芽为0.5-2份,
山楂为0.3-0.7份,
乌梅为1-4份,
豆豉为1-4份。
上述润肠通便的益生菌中草药复方组合物可用于制备保健食品。
由上述技术方案可知,本发明将益生菌、益生元与中药粉复配使用,可有效增加排便数量,增加粪便含水量,发挥促排便作用,提高肠道菌群丰度,提高免疫力,提高防治效果;本发明组合物成分温和,所用中药粉均为药食同源中药,可克服现有润肠通便产品用药时间长有药物副作用的缺点;中药粉与益生菌、益生元共同使用,具有明显的协同增效作用。
附图说明
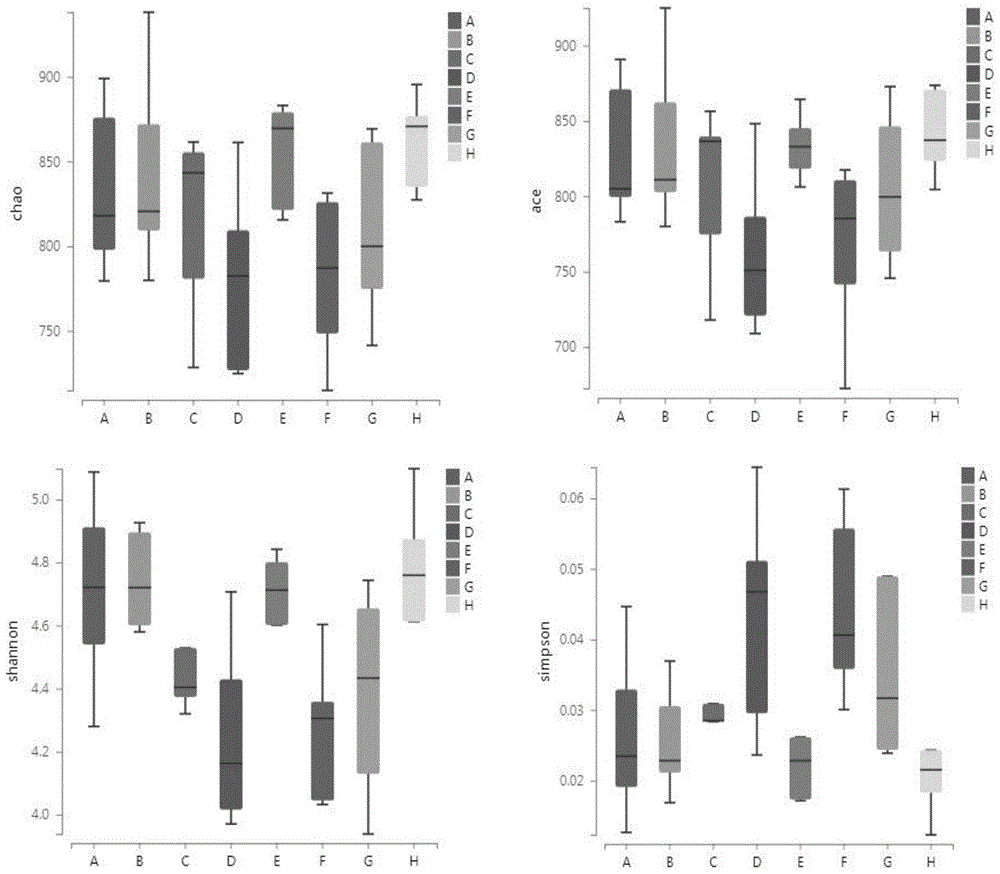
图1所示为物种α多样性分析结果。
图2所示为物种β多样性分析结果。
图3所示为物种在genus水平的丰富度分析结果。
图4所示为genus水平的关键物种的差异分析。
图5所示为各组大鼠结肠切片(标尺为100μm)。
具体实施方式
下面对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明实施例中所用益生菌均为市售益生菌,购自江苏新申奥生物科技有限公司。
实施例1
一种润肠通便组合物,包括:
益生菌:鼠李糖乳杆菌1.5g(3×1011cfu)、植物乳杆菌lp3a1.5g(3×1011cfu)、副干酪乳杆菌1.5g(3×1011cfu)、乳双歧杆菌1.5g(2×1011cfu)、嗜酸乳杆菌1.25g(1.5×1011cfu)、长双歧杆菌0.5g(1×1011cfu)、罗伊氏乳杆菌0.5g(1×1011cfu)、瑞士乳杆菌0.5g(1×1011cfu)、发酵乳杆菌0.5g(1×1011cfu)、约氏乳杆菌0.5g(6×1010cfu)、干酪乳杆菌0.5g(6×1010cfu)、卷曲乳杆菌0.5g(6×1010cfu)、短双歧杆菌0.25g(5×1010cfu);
益生元:低聚异麦芽糖4g、菊粉1g、乳糖醇1g、水苏糖1g、壳寡糖0.2g、低聚果糖0.3g、低聚木糖0.3g、低聚甘露糖0.2g、低聚半乳糖0.2g、燕麦β-葡聚糖0.2g、聚葡萄糖0.2g;
以上原料混合后即得润肠通便组合物2日量。
实施例2
一种润肠通便的益生菌中草药复方组合物,包括:
益生菌:鼠李糖乳杆菌1.5g(3×1011cfu)、植物乳杆菌lp3a1.5g(3×1011cfu)、副干酪乳杆菌1.5g(3×1011cfu)、乳双歧杆菌1.5g(2×1011cfu)、嗜酸乳杆菌1.25g(1.5×1011cfu)、长双歧杆菌0.5g(1×1011cfu)、罗伊氏乳杆菌0.5g(1×1011cfu)、瑞士乳杆菌0.5g(1×1011cfu)、发酵乳杆菌0.5g(1×1011cfu)、约氏乳杆菌0.5g(6×1010cfu)、干酪乳杆菌0.5g(6×1010cfu)、卷曲乳杆菌0.5g(6×1010cfu)、短双歧杆菌0.25g(5×1010cfu)、两歧双歧杆菌0.25g(5×1010cfu)、婴儿双歧杆菌0.25g(5×1010cfu);
益生元:低聚异麦芽糖4g、菊粉1g、乳糖醇1g、水苏糖1g、壳寡糖0.2g、低聚果糖0.3g、低聚木糖0.3g、低聚甘露糖0.2g、低聚半乳糖0.2g、燕麦β-葡聚糖0.2g、聚葡萄糖0.2g、抗性糊精0.2g;
中药粉:麦芽:0.5g、山楂:0.5g、豆豉0.5g;
以上原料混合后即得益生菌中草药复方组合物2日量。
实施例3
一种润肠通便的益生菌中草药复方组合物,包括:
益生菌:副干酪乳杆菌1.5g(3×1011cfu)、乳双歧杆菌1.5g(2×1011cfu)、嗜酸乳杆菌1.25g(1.5×1011cfu)、长双歧杆菌0.5g(1×1011cfu)、罗伊氏乳杆菌0.5g(1×1011cfu)、瑞士乳杆菌0.5g(1×1011cfu)、发酵乳杆菌0.5g(1×1011cfu)、约氏乳杆菌0.5g(6×1010cfu)、干酪乳杆菌0.5g(6×1010cfu)、植物乳杆菌ys40.5g(6×1010cfu)、卷曲乳杆菌0.5g(6×1010cfu)、短双歧杆菌0.25g(5×1010cfu)、两歧双歧杆菌0.25g(5×1010cfu)、婴儿双歧杆菌0.25g(5×1010cfu);
益生元:低聚异麦芽糖4g、菊粉1g、乳糖醇1g、水苏糖1g、壳寡糖0.2g、低聚果糖0.3g、低聚木糖0.3g、低聚甘露糖0.2g、低聚半乳糖0.2g、燕麦β-葡聚糖0.2g、聚葡萄糖0.2g;
中药粉:山楂:0.5g、乌梅0.5g;
以上原料混合后即得益生菌中草药复方组合物2日量。
实施例4
一种润肠通便的益生菌中草药复方组合物,包括:
益生菌:鼠李糖乳杆菌1.5g(3×1011cfu)、植物乳杆菌lp3a1.5g(3×1011cfu)、副干酪乳杆菌1.5g(3×1011cfu)、乳双歧杆菌1.5g(2×1011cfu)、嗜酸乳杆菌1.25g(1.5×1011cfu)、长双歧杆菌0.5g(1×1011cfu)、罗伊氏乳杆菌0.5g(1×1011cfu)、约氏乳杆菌0.5g(6×1010cfu)、干酪乳杆菌0.5g(6×1010cfu)、植物乳杆菌ys40.5g(6×1010cfu)、卷曲乳杆菌0.5g(6×1010cfu)、短双歧杆菌0.25g(5×1010cfu)、两歧双歧杆菌0.25g(5×1010cfu)、婴儿双歧杆菌0.25g(5×1010cfu);
益生元:低聚异麦芽糖4g、菊粉1g、乳糖醇1g、水苏糖1g、壳寡糖0.2g、低聚果糖0.3g、低聚木糖0.3g、低聚甘露糖0.2g、低聚半乳糖0.2g、燕麦β-葡聚糖0.2g、聚葡萄糖0.2g、可溶性大豆多糖0.2g;
中药粉:麦芽:0.5g、豆豉:0.5g、乌梅0.5g;
以上原料混合后即得益生菌中草药复方组合物2日量。
实施例5
一种润肠通便的益生菌中草药复方组合物,包括:
益生菌:鼠李糖乳杆菌1.5g(3×1011cfu)、植物乳杆菌lp3a1.5g(3×1011cfu)、副干酪乳杆菌1.5g(3×1011cfu)、乳双歧杆菌1.5g(2×1011cfu)、嗜酸乳杆菌1.25g(1.5×1011cfu)、长双歧杆菌0.5g(1×1011cfu)、罗伊氏乳杆菌0.5g(1×1011cfu)、瑞士乳杆菌0.5g(1×1011cfu)、发酵乳杆菌0.5g(1×1011cfu)、约氏乳杆菌0.5g(6×1010cfu)、干酪乳杆菌0.5g(6×1010cfu)、植物乳杆菌ys40.5g(6×1010cfu)、卷曲乳杆菌0.5g(6×1010cfu)、短双歧杆菌0.25g(5×1010cfu)、两歧双歧杆菌0.25g(5×1010cfu)、婴儿双歧杆菌0.25g(5×1010cfu);
益生元:低聚异麦芽糖4g、菊粉1g、乳糖醇1g、水苏糖1g、壳寡糖0.2g、低聚果糖0.3g、低聚木糖0.3g、低聚甘露糖0.2g、低聚半乳糖0.2g、燕麦β-葡聚糖0.2g、聚葡萄糖0.2g;
中药粉:麦芽:0.5g、山楂:0.5g;
以上原料混合后即得益生菌中草药复方组合物2日量。
实施例6
研究本发明益生菌中草药复方组合物对大鼠便秘模型的体重、排便粒数、排便含水率、小肠炭末推进率、菌群多样性、脏器指数、sod活力、总抗氧化能力、谷胱甘肽过氧化物酶活力、血清il-10水平、il-6水平、tgf-β水平、iga水平、igg水平、结肠组织切片、血清生化指标等的影响,以验证本发明的益生菌中草药复方组合物对便秘的功能作用。
将64只大鼠随机分成八组(每组8只),分为a、b、c、d、e、f、g和h组。实验第一周a组每天每只灌胃2ml生理盐水,b、c、d、d、f、g和h组每天每只灌胃2ml洛哌丁胺,灌胃时间为每天上午8:30-9:30;实验第二周a组继续灌胃生理盐水,b组改为灌生理盐水,c、d、e、f、g和h组改为灌对应编号的药物,灌胃体积均为2ml,具体分组如下:
a:正常组;
b:模型组;
c:取实施例1的样品作为供试样品,灌胃剂量581.4mg/(kg·d);
d:将番泻叶颗粒用研钵研磨成粉末状,灌胃剂量1938mg/(kg·d);
e:取实施例2的样品作为供试样品,灌胃剂量581.4mg/(kg·d);
f:取实施例3的样品作为供试样品,灌胃剂量581.4mg/(kg·d);
g:取实施例4的样品作为供试样品,灌胃剂量为581.4mg/(kg·d);
h:取实施例5的样品作为供试样品,灌胃剂量为581.4mg/(kg·d);
灌胃期间,每天收集粪便、记录鼠粮消耗、水的消耗。
造模结束当天收集一次便秘模型组的粪便(用于送华大基因测序),整个实验结束当天,灌胃1ml碳末溶液,同时取此时的新鲜粪便(用于送华大基因测序),30min后立即从老鼠眼球取血,血液放4℃冰箱过夜析出血清。老鼠处死后解剖老鼠并取整个肠道组织,按组铺好测量碳末迁移数据并拍照(炭末推进率(%)=炭末推进长度/小肠全长×100%);取结肠组织5mm置于固定液中用于切片制作和h&e染色(武汉赛维尔生物科技有限公司);收集并称取老鼠的脏器(肝、肾、脾);解剖实验结束后收集并记录老鼠最后24h内的粪便数。
1.大鼠体重变化
如表1所示,与正常组相比:造模后模型组及各给药组大鼠体重增长明显减慢(p<0.05);治疗后h治疗组大鼠体重增长明显较快(p<0.05),而f治疗组大鼠体重增长较慢(p<0.05);c,d组大鼠体重差异性小,无明显统计学意义;与模型组相比:造模前各治疗组大鼠及正常组体重无明显差异;治疗后各治疗组及正常组大鼠体重增长明显增快(p<0.05),且以h治疗组大鼠增长最明显。
表1大鼠体重(g)变化情况
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
2.灌胃结束最后24h粪便粒数
如表2所示,模型组排便量明显低于正常组(p<0.05),治疗后,各治疗组及正常组大鼠排便粒数显著升高(p<0.05),且以h治疗组大鼠升高最明显;与模型组相比:造模前各治疗组及正常组大鼠粪便粒数无明显差异;治疗后,治疗组及正常组大鼠粪便颗粒数明显增加(p<0.05),以h组大鼠升高最多。
表2大鼠排便粒数情况
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
3.粪便含水量变化
如表3所示,与正常组相比:造模后,模型组及各治疗组大鼠粪便含水率显著下降(p<0.05);治疗后,c、d、e、h浓度中药治疗组大鼠粪便含水率明显升高(p<0.05),其中以h组增长最为明显,此结果与排便粒数实验结果共同证明,本发明的益生菌中药复方组合物能增加便秘大鼠的粪便总量与含水量,改善便秘症状。
表3大鼠粪便含水率变化情况
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
4.碳末推进率变化
由表4结果可知,b组大鼠在第一周造模结束并恢复一周后,碳末推进率相比其它组低;而其它六组给药组是在造便秘模型结束后继续灌胃药物,其碳末推进率有所升高,治疗后h组大鼠大肠墨汁推进率明显增快(p<0.05),提示本发明的益生菌中药复方组合物能增强便秘大鼠肠道传输功能。
表4大鼠的碳末推进率(%)
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
5.肠道菌群多样性研究
使用无菌冻存管收集各组大鼠新鲜粪便样本,每只大鼠收集至少2粒粪便,立即放入液氮中,然后置-80℃冰箱中保存,送华大基因测序。
5.1物种α多样性分析
用于表示菌群α多样性的评价指标主要包括chao、ace、shannon和simpson指数,用于说明组内物种的丰富度,其中前面三个指数相比其它组越大表明丰富度越高,而最后面指数越小说明样品中的物种越丰富。
结果如图1所示,chao和ace指数展示的结果相似,符合文献报道的结果。h组的chao、ace、shannon指数在所有组别中最高,说明h组大鼠物种丰富度最高;便秘会明显降低肠道菌群的α多样性,说明便秘给肠道菌群的多样性带来负面效果,而在采用药物治疗后,大鼠的肠道菌群多样性会得到改善。
5.2物种β多样性
β多样性能反映各组间的整体差异性,通过比较各组间的β多样性,发现只有a组与b组的β多样性存在显著性差异(p<0.0001);其他各组和b组相比,有下降趋势;尤其是h组的β多样性与其它各组有显著性差异(p<0.05)。
5.3物种丰富度及关键菌属水平
根据物种柱状图genus水平菌群丰富度(图3)结果显示,灌胃给药不会给肠道菌群带来特别明显的结构组成改变,也没有造成原先肠道菌群紊乱。然而便秘组的螺杆菌属(helicobacter)丰度高于其它组;灌胃给药组相比对照组的clostridium丰度有所下降;a和b组的拟杆菌属(bacteroides)水平相对其它组较低;以上结果从关键菌属的水平(图4)中也可以得到验证。b组的螺杆菌属(helicobacter)丰度升高,在经过灌胃治疗之后,各组大鼠的螺杆菌属都有不同程度的降低。
6.脏器指数分析
脏器指数是反映大鼠健康状况的一个重要指标,如表5-7所示,实验结束后大鼠脏器指数在组间无明显差异,且指数均在正常健康大鼠的指数范围内。大鼠组间均无显著差异(p>0.05),说明组间大鼠健康状况类似。
表5大鼠肝脏指数
表6大鼠肾脏指数
表7大鼠脾脏指数
7.抗氧化能力影响
7.1大鼠sod活力
由表8可知,b、c、d、e、f、g、h组大鼠造便秘模型后,超氧化物歧化酶(sod)活性下降,可推测便秘对sod活力有一定影响;a组sod活性高于b组,且具有显著差异(p<0.05)。
表8大鼠sod活力
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
7.2大鼠总抗氧化能力
由表9可知,大鼠便秘后,总抗氧化能力均比正常组(a)低;g和h组总抗氧化能力相比其它给药组高;可推测便秘对总抗氧化能力有影响。a组和六组给药组均有显著差异(p<0.05)。
表9大鼠总抗氧化能力
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
7.3大鼠谷胱甘肽过氧化物酶活力
由表10可得知,大鼠便秘及给药后,谷胱甘肽过氧化物酶活力稍有差异,其中e、f和g稍低于其它组,h组最高,e、f组相比b组具有显著差异(p<0.05)。
表10大鼠谷胱甘肽过氧化物酶
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
8.免疫能力影响
8.1大鼠血清il-10水平
il-10是一种有重要免疫调节功能的多效细胞因子,能通过活化的巨噬细胞来抑制炎症因子如tnf-α、il-6、il-1等的表达。如表11所示,大鼠便秘后,il-10表达水平发生下降,继续灌胃给药后,c-h组il-10表达水平相比不给药的b组有所升高,但略低于a组。
表11大鼠血清中il-10水平
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
8.2大鼠血清中il-6水平
如表12所示,大鼠便秘后,il-6表达水平会升高,继续灌胃给药后,c、f、g、h组相比后阶段不给药的b组il-6表达水平低;说明便秘导致il-6升高,给药可以降低il-6水平;由于il-10的升高具有一定抑制il-6表达的功能,推测e组的il-6高于b与表11相相应。
表12大鼠血清il-6水平
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
8.3大鼠血清tgf-β水平
如表13所示,大鼠便秘后,tgf-β表达水平下降;继续灌胃给药后,h组具有升高tgf-β表达水平的趋势。b及各给药组相比a组有显著差异(p<0.05)。
表13大鼠的tgf-β水平
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
8.4大鼠血清中iga水平
由表14可知,大鼠便秘对iga的影响不明显;继续灌胃给药的d、e、f和h组的iga水平稍微高于其它组。各组间有差异,尤其是给药组高于b组,如h高于b组14.4%(p<0.05)。
表14大鼠的iga(ng/ml)水平
注:同列肩标的不同字母表示不同组之间存在显著差异(p<0.05)
8.5大鼠血清中igg水平
由表15可知,大鼠便秘及给药后igg水平比较接近对照组水平,便秘并没有严重影响到大鼠的igg水平。各组之间没有显著差异(p>0.05)。
表15大鼠的igg(ng/ml)水平
9.大鼠结肠组织切片分析
切片主要评价绒毛清晰情况,由图5可知,图片a至h依次为a、b、c、d、e、f、g、h组典型h&e染色切片,大部分h&e染色切片未有严重的隐窝结构受损、绒毛结构不完整以及炎症细胞浸润等情况;b组切片出现轻微绒毛受损,不完整;d组少部分区域出现绒毛不完整;e组有小部分区域绒毛较短,。
10.肝功能肾功能血清生化指标分析
选取能指示肝功能情况的谷丙转氨酶(alt)、谷草转氨酶(ast)指标,指示肾功能情况的尿素/尿素氮(bun)、尿酸(ua)进行elisa生化分析,结果如表16-18所示。
由表16可知,便秘能提高alt的水平,而灌胃药物有降低alt的趋势,且g和h组与b组相比,下降幅度大;
由表17可知,便秘能提高ast的水平,g和h组有降低ast的趋势,但各组大鼠之间无显著差异(p>0.05)。
由表18可知,便秘会稍微降低bun水平,而灌胃药物后,且g和h表现出阻止这种降低的趋势;
由表19可知,便秘会稍微升高ua的水平,然而,c、d、g、h表现出恢复这种症状的能力。
综上,便秘在一定程度上会影响肝肾功能,而灌胃的一些药物表现出恢复这种症状的潜力。
表16大鼠的血清生化指标alt
表17大鼠血清生化指标ast
表18大鼠血清生化指标bun
表19大鼠血清生化指标ua
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
- 还没有人留言评论。精彩留言会获得点赞!