一种用于乏氧肿瘤一氧化氮治疗的光催化剂及其制备方法与流程
1.本发明属于生物医药领域,具体涉及一种用于乏氧肿瘤一氧化氮治疗的光催化剂及其制备方法。
背景技术:
2.一氧化氮(no)通过破坏癌细胞的线粒体来抑制肿瘤生长,因此已广泛用于癌症治疗。小分子一氧化氮供体是将no递送至肿瘤最常用的选择,但是其释放的不可控性导致其治疗效率较低并且经常导致全身性不良副作用。受内源性no生物合成的启发,以精氨酸氧化产生no将是更具特异性的no生成手段。与自发释放no的小分子供体相比,精氨酸可以在人工设计的反应系统中受控地被氧化为no,从而避免了血液循环过程中不必要的副作用。但是,上述策略通常依赖于氧化剂,例如o2或h2o2。由于肿瘤微环境中的o2或h2o2并不充足,导致依靠精氨酸氧化产生no治疗通常无法在最佳条件下进行。因此,不依赖于肿瘤微环境的no可控产生是优化一氧化氮治疗的关键方向。
3.碳量子点掺杂的石墨相氮化碳作为一种半导体光敏剂材料,因其具有较高的比表面积和较好的光催化能力而受到广泛关注。但是,对于碳量子点掺杂的石墨相氮化碳的生物医学应用很少有报道。碳量子点掺杂的石墨相氮化碳的导带宽度较小,使其可以在>630 nm的红光照射下被激发,产生光生电子和光生空穴。并且,该光生空穴的电势较正,使其具有较强的氧化性。理论上,光生空穴可以与小分子发生氧化还原反应,使小分子被氧化,而光生空穴本身被消耗。由于精氨酸及其类似分子上的胍基结构经过氧化反应可以产生一氧化氮,因此,将碳量子点掺杂的石墨相氮化碳材料与精氨酸或多聚精氨酸分子共价偶联后,经红光激发产生的光生空穴很容易氧化胍基产生一氧化氮,对于实现不依赖于肿瘤微环境的一氧化氮光控产生具有重要的科学意义。
技术实现要素:
4.本发明的目的在于提供一种用于乏氧肿瘤一氧化氮治疗的光催化剂及其制备方法,其采用一种简单的方法设计出了一种不依赖于肿瘤微环境而可受控产生一氧化氮的光催化剂,可以实现高效的抗肿瘤治疗。
5.为实现上述目的,本发明采用如下技术方案:一种用于乏氧肿瘤一氧化氮治疗的光催化剂,其是以精氨酸或多聚精氨酸与碳量子点掺杂的石墨相氮化碳为原料,利用精氨酸或多聚精氨酸的氨基和碳量子点掺杂的石墨相氮化碳表面的羧基经酰胺缩合反应制得的,以精氨酸或多聚精氨酸进行表面修饰的碳量子点掺杂的石墨相氮化碳。
6.所述光催化剂的制备方法包括以下步骤:(1)碳量子点溶液的制备:将质量比4:1的柠檬酸和尿素溶解在二次蒸馏水中,置于聚四氟乙烯反应釜中,于160
‑
200℃高温反应16
‑
20h,然后冷却至室温,离心去除沉淀,再将上清液透析,然后经旋转蒸发,得到浓度浓度为2 mg l
‑1的碳量子点溶液;
(2)碳量子点掺杂的石墨相氮化碳的制备:将尿素溶解在步骤(1)制备的碳量子点溶液中,然后置入坩埚并加热至500
‑
600℃,反应2
‑
4h,待冷却后将产物研磨成粉并置于5mol/l的硝酸溶液中,130℃保温回流24h,冷却至室温后,将产物离心并用二次蒸馏水洗涤至ph=7,之后将产物在二次蒸馏水中超声分散4
‑
24 h,以5000 rpm的转速离心10 min取上清液,将上清液以8000 rpm的转速离心10 min得到沉淀,即为粒径约为100 nm
‑
200 nm的碳量子点掺杂的石墨相氮化碳;(3)光催化剂的制备:将精氨酸或多聚精氨酸与步骤(2)制备的碳量子点掺杂的石墨相氮化碳、酰胺化偶联试剂溶解在溶剂中并混合均匀,然后在20
‑
40 ℃反应4
‑
12 h,反应后将产物以8000 rpm的转速离心10 min,并用二次蒸馏水洗涤5
‑
7次,制备得到所述光催化剂。
7.步骤(2)中所用尿素的量按与碳量子点的质量比为105:1
‑
107:1进行换算。
8.步骤(3)中所用精氨酸或多聚精氨酸与碳量子点掺杂的石墨相氮化碳的质量比为0.5:1
‑
5:1;所用酰胺化偶联试剂与精氨酸或多聚精氨酸的摩尔比为(1
‑
10):1;所述溶剂为水或dmso。
9.所得光催化剂可用于作为一氧化氮抗肿瘤治疗药物。
10.本发明的有益效果在于:本发明提供了一种用于乏氧肿瘤一氧化氮治疗的光催化剂的制备方法,该方法简单、原料易得。所得光催化剂可以在>630 nm的红光照射下产生光生空穴,进而催化精氨酸或多聚精氨酸结构中的胍基氧化产生一氧化氮,从而达到诱导肿瘤细胞凋亡的目的,故可用于乏氧肿瘤的有效治疗。
附图说明
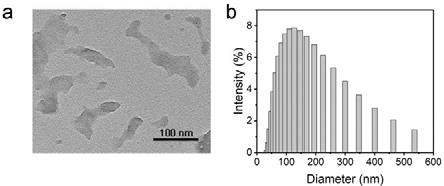
11.图1为实施例制备的多聚精氨酸修饰的碳量子点掺杂的石墨相氮化碳(argccn)的透射电镜图(a)和粒径分布图(b)。
12.图2为性能试验测试结果图,其中(a)为多聚精氨酸、碳量子点掺杂的石墨相氮化碳(ccn)、argccn在光照下产生一氧化氮的能力试验结果,(b)为多聚精氨酸、ccn、argccn在细胞内光照产生一氧化氮的能力情况图,(c)和(d)分别为在正常氧和乏氧条件下的多聚精氨酸、ccn、argccn诱导细胞死亡的情况图。
13.图3为多聚精氨酸、ccn和argccn诱导细胞凋亡反应的情况图。
具体实施方式
14.一种用于乏氧肿瘤一氧化氮治疗的光催化剂的制备方法包括以下步骤:(1)碳量子点溶液的制备:将质量比4:1的柠檬酸和尿素溶解在二次蒸馏水中,置于聚四氟乙烯反应釜中,于160
‑
200℃高温反应16
‑
20h,然后冷却至室温,将产物以≥10000 rpm的转速离心以去除沉淀,再将上清液置入透析袋中透析3
‑
7 d,然后经40
‑
60 ℃、真空度为25
‑
50 mbar条件下旋转蒸发,得到浓度浓度为2 mg l
‑1的碳量子点溶液;(2)碳量子点掺杂的石墨相氮化碳的制备:将尿素溶解在步骤(1)制备的碳量子点溶液中,然后置入坩埚并加热至500
‑
600℃,反应2
‑
4h,待冷却后将产物研磨成粉并置于5mol/l的硝酸溶液中,130℃保温回流24h,冷却至室温后,将产物离心并用二次蒸馏水洗涤
至ph=7,之后将产物在二次蒸馏水中超声分散4
‑
24 h,以5000 rpm的转速离心10 min取上清液,将上清液以8000 rpm的转速离心10 min得到沉淀,即为粒径约为100
‑
200 nm的碳量子点掺杂的石墨相氮化碳;(3)光催化剂的制备:将精氨酸或多聚精氨酸与步骤(2)制备的碳量子点掺杂的石墨相氮化碳、酰胺化偶联试剂溶解在溶剂中并混合均匀,然后在20
‑
40 ℃反应4
‑
12 h,反应后将产物以8000 rpm的转速离心10 min,并用二次蒸馏水洗涤5
‑
7次,制备得到所述光催化剂。
15.步骤(2)中所用尿素的量按与碳量子点的质量比为105:1
‑
107:1进行换算。
16.步骤(3)中所用精氨酸或多聚精氨酸与碳量子点掺杂的石墨相氮化碳的质量比为0.5:1
‑
5:1;所用酰胺化偶联试剂与精氨酸或多聚精氨酸的摩尔比为(1
‑
10):1,其中,所述酰胺化偶联试剂为常规已知的酰胺化偶联试剂中的任意一种,如4
‑
(4,6
‑
二甲氧基三嗪
‑2‑
基)
‑4‑
甲基吗啉盐酸盐、1,3
‑
二环己基碳二亚胺、1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐等;所述溶剂为水或dmso。
17.为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例
18.以多聚精氨酸修饰的碳量子点掺杂的石墨相氮化碳为例,其具体制备步骤如下:(1)将2 g的柠檬酸和0.5 g的尿素溶解在25 ml二次蒸馏水中,置于聚四氟乙烯反应釜中,升温至170 ℃,并保温反应18 h,然后冷却至室温,将产物以10000 rpm的转速离心10 min,将所得上清液置入截留分子量为10kda的透析袋中透析7天,之后将所得透析液在40 ℃、真空度为25 mbar的条件下旋转蒸发,制备得到碳量子点溶液,其浓度为2 mg l
‑1;(2)将10 g尿素溶解在5 ml上述制备的碳量子点溶液中,然后置入坩埚中并以5 ℃ min
‑1的升温速度加热至550 ℃,保持温度反应3 h。然后冷却至室温,将产物研磨成粉并置于5 m hno3溶液中,保持温度在130 ℃回流24h,冷却至室温后,将产物离心并用二次蒸馏水洗涤至ph=7,之后将产物在二次蒸馏水中超声分散24 h,以5000 rpm的转速离心10 min取上清液,将上清液以8000 rpm的转速离心10 min得到沉淀,即为碳量子点掺杂的石墨相氮化碳(ccn),其粒径约为100 nm
‑
120 nm;(3)将75 mg的多聚精氨酸(mw=3000
‑
5000)、30 mg的碳量子点掺杂的石墨相氮化碳、20 mg(0.104 mmol)的1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐溶解于80 ml的dmso中并混合均匀,然后在37 ℃反应12 h,然后以8000 rpm的转速离心10 min,并用二次蒸馏水洗涤7次,制备得到多聚精氨酸表面修饰的碳量子点掺杂的石墨相氮化碳(argccn)。
19.图1为制备得到的argccn的透射电镜图(a)和粒径分布图(b)。从图中可以观察到,多聚精氨酸表面修饰的碳量子点掺杂的石墨相氮化碳纳米颗粒尺寸均匀,其粒径集中分布在120 nm。
20.性能试验1.取多聚精氨酸、ccn和argccn样品各1 mg,分别分散于1 ml的pbs中,再用660nm的激光(200 mw cm
‑2)照射不同的时间(以argccn不加光照为对照),并每隔一定时间取反应液,8000 rpm离心3 min后,取上清50 μl,与一氧化氮检测试剂反应,用酶标仪测定540 nm
处的吸收值。
21.2. 以乳腺癌细胞系mcf
‑
7为验证模型。将mcf
‑
7细胞接种在6孔板中,在细胞培养箱或乏氧培养小室中孵育24 h,用浓度均为200 μg ml
‑1的多聚精氨酸、ccn或argccn的培养液孵育细胞2 h。然后用一氧化氮荧光探针孵育细胞20 min并用pbs清洗。之后用660 nm的激光(200 mw cm
‑2)照射细胞10 min(以argccn不加光照为对照),将细胞消化并用流式细胞仪测定荧光。
22.3. 以乳腺癌细胞系mcf
‑
7为验证模型。将mcf
‑
7细胞接种在96孔板中,孵育24 h,用pbs清洗三次。分别加入含有不同浓度(0、25、50、100、150、200μg/ml)的各样品(多聚精氨酸、ccn或argccn)的培养液100 μl,孵育2 h。然后用pbs清洗三次,用660 nm的激光(200 mw cm
‑2)照射细胞10 min(以argccn不加光照为对照)。之后取出培养液,加入含有cck
‑
8(cell counting kit
‑
8,碧云天)的培养基100 μl,孵育1h,用酶标仪测定450 nm的吸收值。
23.4. 以乳腺癌细胞系mcf
‑
7为验证模型。将mcf
‑
7细胞接种在96孔板中并将孔板放在乏氧培养小室中孵育24 h,用pbs清洗三次。分别加入含有不同浓度(0、25、50、100、150、200μg/ml)的各样品(多聚精氨酸、ccn或argccn)的培养液100 μl,继续在乏氧培养小室中孵育2 h。然后用pbs清洗三次,用660 nm的激光(200 mw cm
‑2)照射细胞10 min(以argccn不加光照为对照)。之后取出培养液,加入含有cck
‑
8(cell counting kit
‑
8,碧云天)的培养基100 μl,在乏氧培养小室中孵育1h,用酶标仪测定450 nm的吸收值。
24.5. 以乳腺癌细胞系mcf
‑
7为验证模型。将mcf
‑
7细胞接种在6孔板中,在细胞培养箱或乏氧培养小室中孵育24 h,用浓度均为200 μg ml
‑1的多聚精氨酸、ccn或argccn的培养液孵育细胞2 h,然后用660 nm的激光(200 mw cm
‑2)照射细胞10 min(以argccn不加光照为对照)。再在细胞培养箱或乏氧培养小室中孵育6 h后,将细胞用细胞凋亡检测试剂孵育30 min进行荧光染色,之后将细胞消化并用流式细胞仪测定荧光。
25.图2为性能试验测试结果图,其中(a)为多聚精氨酸、ccn、argccn在光照下产生一氧化氮的能力情况图,由图中可见,argccn在红光照射下可以大量产生一氧化氮,这说明ccn可以在红光激发下催化多聚精氨酸中的胍基产生一氧化氮。
26.(b)为多聚精氨酸、ccn、argccn在细胞内经光照产生一氧化氮的能力情况图。由图中可以看出,在正常氧或乏氧的环境下,argccn都可以产生一氧化氮,且产生量并无明显区别,表现出其不依赖于微环境的性质。
27.(c)和(d)分别为在正常氧和乏氧条件下多聚精氨酸、ccn、argccn诱导细胞死亡的情况图。图中可以观察到,在正常氧或乏氧的环境下,argccn在光照下都具有杀伤细胞的能力,且细胞毒性并无明显区别,表现出其对乏氧细胞的治疗潜力。
28.图3为多聚精氨酸、ccn、argccn诱导细胞凋亡反应的情况图。图中可以观察到,argccn在正常氧和乏氧条件下都可以经光照实现细胞凋亡的诱导。
29.由上述试验可见,本发明所提供的argccn可以在红光照射下产生大量一氧化氮,诱导细胞的凋亡,而不依赖于微环境。
30.总之,本发明提供了一种用于乏氧肿瘤一氧化氮治疗的光催化剂的制备方法,其将精氨酸或多聚精氨酸共价偶联到碳量子点掺杂的石墨相氮化碳光催化剂上,其方法简单,所制备的材料具有很高的光稳定性。同时,所制备的材料在红光照射下具有产生一氧化氮的能力,能够诱导细胞凋亡,并且其一氧化氮生成能力不会受到肿瘤微环境的限制,展现
出对乏氧肿瘤的治疗潜力。
31.以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1