一种无干细胞和生长因子负载的可注射聚(4-羟基丁酸酯)(P4HB)多孔微球制剂
一种无干细胞和生长因子负载的可注射聚(4
‑
羟基丁酸酯)(p4hb)多孔微球制剂
技术领域
1.本发明涉及医药技术领域,具体涉及一种无干细胞和生长因子负载的可注射聚(4
‑
羟基丁酸酯)(p4hb)多孔微球制剂。
背景技术:
2.由创伤、感染或骨肿瘤等因素导致的骨缺损使病患难以通过自身实现骨修复愈合。治疗此类骨缺损是临床上面临的巨大挑战。临床上多采用自体骨、同种异体骨或人工骨材料修复骨缺损。自体骨是临床治疗骨缺损的黄金标准,但却存在增加额外创伤、来源少、增加失血量或手术感染风险增加等缺点。虽然同种异体骨来源丰富,但会带来较为严重的免疫反应、疾病交叉感染和愈合缓慢等问题。人工骨材料是一种具有特殊功能的骨组织代替材料,为患者快速恢复,同时避免自体骨和同种异体骨移植带来的问题提供了一种解决方法。
3.在人类胎儿时期,大多数骨骼是以软骨内骨化方式实现骨增长。然而,目前主要的骨修复生物材料则通过膜内骨化法达到治疗骨缺损的目的。在临床上,仅有少数的骨裂是以膜内骨化方式修复,多数情况下成功的骨再生是通过软骨内骨化的方式。软骨内骨化方式为解决大面积骨缺损提供了另一种可能的途径。通过负载分化或未分化的祖细胞、生长因子等可促进软骨内骨化。然而,目前鲜有依靠单一生物材料自身实现诱导软骨内骨化以促进骨缺损再生的报道。
4.聚(4
‑
羟基丁酸酯)(p4hb)即聚γ丁内酯,是美国食品药物管理局(u.s.food and drug administration,u.s.fda)批准的一种生物可降解医用高分子聚酯,已在手术缝合线和疝气补片等领域获得应用,其降解机理主要为表面降解,因此可与骨再生速率相匹配,是一种优异的骨再生生物医用材料。综上所述,本发明研发一类与细胞外基质机械性能相近的新型多孔聚(4
‑
羟基丁酸酯)微球以增强祖细胞聚集从而支持骨的内在修复能力,实现以单一材料完成软骨内骨化修复骨缺损的目的,本发明在基础理论研究和临床应用等方面均具有重要的意义。
技术实现要素:
5.本发明的目的是提供一种无干细胞和生长因子负载的可注射聚 (4
‑
羟基丁酸酯)(p4hb)多孔微球制剂并提供该多孔微球的制备方法和在骨组织修复中的应用。本发明提供的多孔聚(4
‑
羟基丁酸酯) 微球具有与细胞外基质相似的机械性能、优异的生物相容性、组织相容性、可降解性和诱导骨再生等特点,可实现单一材料诱导软骨内骨化。
6.本发明的技术方案是提供一种无干细胞和生长因子负载的可注射聚(4
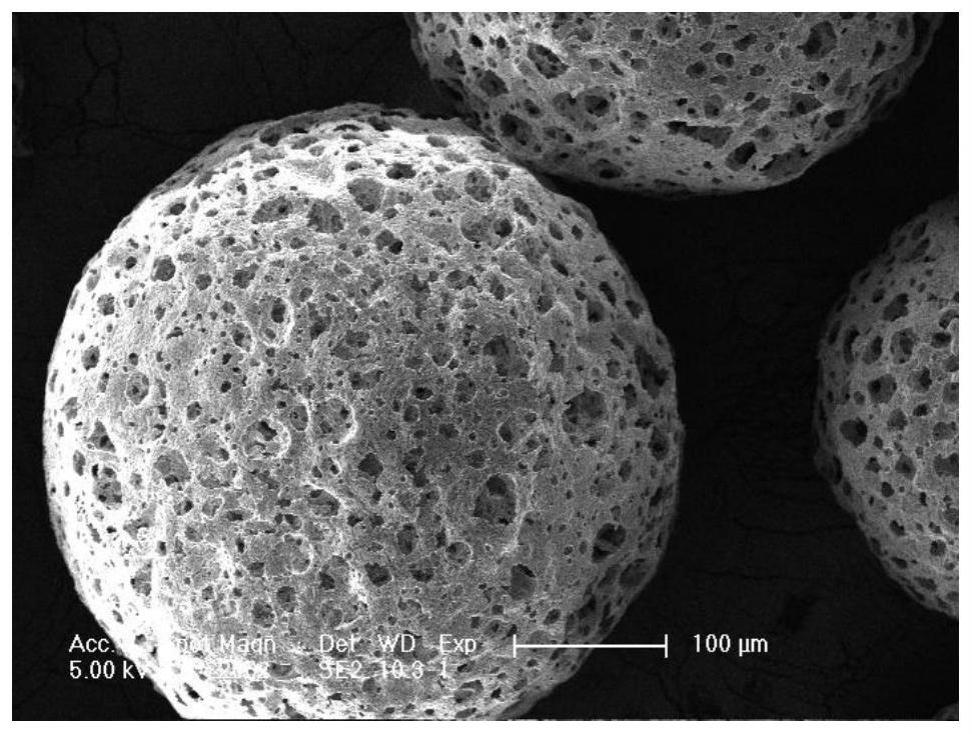
‑
羟基丁酸酯)(p4hb)多孔微球制剂,所述的多孔微球的平均粒径10~1000μm;平均孔径为2~900μm;
7.优选的,所述的多孔微球的平均粒径为100~300μm;平均孔径为10~50μm;
8.所述的多孔微球材料为聚(4
‑
羟基丁酸酯)及其共聚物。
9.优选的,用于制备多孔微球的材料为聚(4
‑
羟基丁酸酯),重均分子量为50000~500000g/mol。
10.所述的致孔剂为无机盐或亲水性物质,包括碳酸盐、碳酸氢盐、聚乙二醇、羟丙基纤维素、聚乙烯吡咯烷酮等中的一种或多种,致孔剂用量与微球材料的质量比为5:100~100:100(w/w)。
11.优选的,致孔剂为碳酸氢铵,其与微球材料的质量比10:100 ~20:100(w/w)。
12.本发明还提供一种无干细胞和生长因子负载的可注射聚(4
‑
羟基丁酸酯)多孔微球制剂的制备方法,包括以下步骤:
13.(1)将聚(4
‑
羟基丁酸酯)溶于有机溶剂再加入致孔剂混合并匀浆,制得初乳液。
14.(2)将初乳液加入含表面活性剂的水溶液中,匀浆并挥发溶剂,制备多孔聚(4
‑
羟基丁酸酯)微球,然后离心收集,清洗并冷冻干燥。
15.步骤1中所述的有机溶剂为氯仿、丙酮、二氯甲烷、三氯甲烷、乙酸乙酯和四氢呋喃等中的一种或多种。
16.步骤2中的表面活性剂包括离子型和非离子型中的一种或多种。
17.优选的,所述的表面活性剂为非离子型表面活性剂,非离子型表面活性剂的优选方案为聚乙烯醇、聚氧化乙烯、聚氧乙烯醚、环氧乙烷
‑
环氧丙烷嵌段共聚物、乙氧基化硅氧烷、n
‑
烷基吡咯烷酮和烷基多苷等中的一种或多种。
18.本发明还提供一种无干细胞和生长因子负载的可注射聚(4
‑
羟基丁酸酯)多孔微球制剂在骨组织修复中的应用。
19.所述的应用方式,具体是指通过注射的方式将多孔微球直接注射到骨缺损部位。
20.本发明具有以下优点:(1)聚(4
‑
羟基丁酸酯)降解方式为部分表面降解型,其降解速率可控,降解速率可与骨再生速率匹配;(2) 多孔微球具有和细胞外基质相似的机械性能和结构,细胞粘附和增值提供较好的载体;(3)多孔微球的通道状多孔结构可有效引导骨修复过程中的软骨内骨化。
21.本发明提供的一种无干细胞和生长因子负载的可注射聚(4
‑
羟基丁酸酯)(p4hb)多孔微球制剂,所使用的物质都具有优异的生物相容性。大鼠颅骨实验表明可注射聚(4
‑
羟基丁酸酯)多孔微球可直接注射至骨缺损部位并能有效促进骨组织再生。
附图说明
22.图1为本发明的聚(4
‑
羟基丁酸酯)(p4hb)即聚γ丁内酯(pγbl) 的分子结构式。
23.图2为本发明的聚(4
‑
羟基丁酸酯)多孔微球结构的扫面电镜图。
24.图3为本发明的聚(4
‑
羟基丁酸酯)多孔微球的脂肪干细胞相容性图。
25.其中a:live/dead染色荧光图;b:明场与live/dead染色荧光叠加图
26.图4为本发明的聚(4
‑
羟基丁酸酯)多孔微球皮下相容性马松染色图(masson staining)。
27.图5为本发明的聚(4
‑
羟基丁酸酯)多孔微球颅骨修复图;
28.其中a:空白组;b:多孔微球组。
具体实施方式
29.以下通过具体实施方式对本发明作进一步的详细说明,但不应将此理解为本发明的范围仅限于以下的实例。在不脱离本发明上述方法思想的情况下,根据本领域普通技术知识和惯用手段做出的各种替换或变更,均应包含在本发明的范围内。
30.实施例1制备小孔径聚(4
‑
羟基丁酸酯)微球
31.称取100mg聚(4
‑
羟基丁酸酯),重均分子量80000g/mol,加入2ml氯仿使其溶解得溶液a。
32.称取10mg聚乙二醇,分子量1000g/mol,加入1ml超纯水中使其溶解得溶液b。
33.将溶液a和b混合并匀浆处理5min获得初乳液。
34.将初乳液倒入聚乙烯醇(1%)水溶液中搅拌挥发溶剂、离心后冷冻干燥、灭菌封装最终制得小孔聚(4
‑
羟基丁酸酯)微球制剂,其粒径为100~200μm,平均孔径为2~10μm。
35.实施例2制备大孔聚(4
‑
羟基丁酸酯)微球
36.称取200mg聚(4
‑
羟基丁酸酯),重均分子量100000g/mol,加入4ml氯仿使其溶解得溶液a。
37.称取20mg碳酸氢铵,加入2ml超纯水中使其溶解得溶液b。
38.将溶液a和b混合并匀浆处理5min获得初乳液。
39.将初乳液倒入聚乙烯醇(1%)水溶液中搅拌挥发溶剂、离心后冷冻干燥。
40.采用氢氧化钠(0.1m)溶液对多孔聚(4
‑
羟基丁酸酯)微球进行水解处理,再经超纯水清洗、离心和冷冻干燥、灭菌封装最终制得大孔聚(4
‑
羟基丁酸酯)微球制剂,其粒径为300~500μm,平均孔径为20~50μm。
41.实施例3制备多孔聚乙二醇
‑
聚(4
‑
羟基丁酸酯)两嵌段共聚物微球
42.称取200mg聚乙二醇
‑
聚(4
‑
羟基丁酸酯)两嵌段共聚物,数均分子量9300g/mol,加入2ml氯仿使其溶解得溶液a。
43.称取10mg碳酸氢铵,加入1ml超纯水中使其溶解得溶液b。
44.将溶液a和b混合并匀浆处理10min获得初乳液。
45.将初乳液倒入聚乙烯醇(2%)水溶液中搅拌挥发溶剂、离心后冷冻干燥、灭菌封装,获得聚乙二醇
‑
聚(4
‑
羟基丁酸酯)两嵌段共聚物多孔微球制剂,其粒径为50~100μm,平均孔径为2~10μm。
46.实施例4制备大孔聚乳酸
‑
聚(4
‑
羟基丁酸酯)两嵌段共聚物微球
47.称取300mg聚(4
‑
羟基丁酸酯),重均分子量80000g/mol,加入6ml氯仿使其溶解得溶液a。
48.称取30mg碳酸钠,加入3ml超纯水中使其溶解得溶液b。
49.将溶液a和b混合并匀浆处理12min获得初乳液。
50.将初乳液倒入聚乙烯醇(2%)水溶液中搅拌挥发溶剂、离心后冷冻干燥。
51.采用氢氧化钠(0.2m)溶液对多孔聚乳酸
‑
聚(4
‑
羟基丁酸酯) 两嵌段共聚物微球进行水解处理,再经超纯水清洗、离心和冷冻干燥、灭菌封装最终制得大孔聚(4
‑
羟基丁酸酯)微球制剂,其粒径为600 ~1000μm,平均孔径为80~120μm。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1