一种均匀给药的载药微球-微针阵列、制备方法及应用与流程
1.本发明属于生物材料技术领域,具体涉及一种均匀给药的载药微球-微针阵列、制备方法及应用,该载药微球-微针阵列可以便携、高效地应用于皮肤无痛给药等技术领域中。
背景技术:
2.水凝胶微球是一种高效的药物微载体。由于水凝胶柔软,生物相容性好,可降解,药物包封率高的优点,广泛应用在给药领域。将微球释放到创伤部位的传统方式包括喷射,皮下注射等。由于聚合物微球黏着性强,将其释放在病灶部位时,微球容易相互黏着发生聚集,导致药物释放不均匀,效率低,创伤部位恢复时间长。另外,传统喷射方式释放在创伤部位的载药微球容易从皮肤上脱落,给药效率低,限制了它的应用。
3.所以,我们提出用微针辅助微球进入皮肤,释放药物。微针通常是由一个基底和排列整齐的针尖构成,针尖可以穿透皮肤角质层形成通道。将载药微球填充在微针里,微针可以辅助微球均匀分布到皮下,微球在创伤部位可以均匀的释放药物。载药微球-微针的制备方法简单,药物包封率高,生物相容性好,是一种无痛、高效、方便的给药手段。
4.因此,在本发明中,我们以微针辅助,设计发明了一种可均匀给药的聚合物微球-微针阵列,用于经皮给药领域。
技术实现要素:
5.本发明的目的是针对现有技术的不足,提供一种均匀给药的载药微球-微针阵列、制备方法及应用,以解决微球在创伤部位分布不均匀易脱落的问题。
6.本发明采用以下技术方案:一种均匀给药的载药微球-微针阵列的制备方法,包括以下步骤:s1、载药微球的制备将药物与水凝胶混合,配制成水凝胶和药物混合溶液作为内相,外相为与内相互不相溶的油相,将外相和内相注入微流控装置,利用两相溶液间的剪切力形成单分散的单乳液液滴,固化并收集,用酒精、去离子水漂洗数次,得到粒径均匀的聚合物载药微球;s2、载药微球-微针阵列的制备配制水凝胶溶液,将水凝胶溶液滴加到微针模板内,并通过抽真空使水凝胶溶液填满微针模板的空隙;将s1中得到的载药微球填充在微针模板的针尖部位,固化后从微针模板剥离,得到载药微球-微针阵列。
7.进一步的,s1中,所述水凝胶选自甲基丙烯酸化水凝胶(gelma)、透明质酸(ha)、聚乳酸(pla)、壳聚糖的一种或多种。
8.进一步的,s1中,可通过调节微流控内相和外相的流速改变液滴大小。
9.进一步的,s1中,所制备的载药微球的直径在100~300 μm之间。
10.进一步的,s1中,所述外相为葵花籽油。
11.进一步的,s2中,所述微针底部边长为200~600 μm,针长为300~1000 μm。
12.进一步的,s2中,水凝胶材料选自聚乙二醇双丙烯酸酯(pegda)、聚乳酸-羟基乙酸共聚物(plga)、海藻糖、聚乙二醇(peg)、二甲基丙烯酸乙二醇酯(egdma)中的一种或多种材料混合。
13.进一步的,所述的载药微球-微针阵列中,载药微球粒径小于针尖底部边长,可填充入微针针尖且载药微球的球形度不被影响。
14.本发明还提供一种均匀给药的载药微球-微针阵列,根据以上所述的制备方法制备而成。
15.本发明还提供以上所述的载药微球-微针阵列在经皮给药领域中的应用。
16.本发明的有益效果:(1)本发明以微流控方式制备水凝胶载药微球,方法简单,成本低,易对载药微球的尺寸进行控制;(2)本发明将载药微球填充入微针阵列,所得到的微球-微针阵列可牢固地贴附于皮肤上,实现了均匀给药和药物释放的效果,克服了微球在创伤部位分布不均匀且易脱落的缺点;(3)本发明水凝胶载药微球和微针材料选择广泛,并且由于微流控对微球尺寸的可控,可得到不同尺寸的微球匹配于不同直径的微针,微球-微针除了用于载药领域还可用于细胞培养等领域,有很强的实用价值。
附图说明
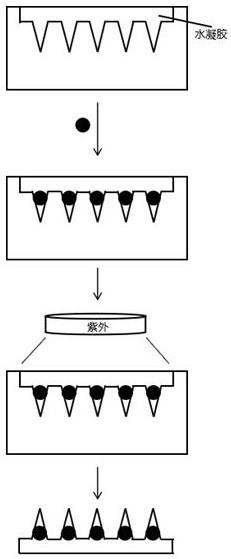
17.图1为本发明载药微球示意图;图2 为本发明载药微球-微针制备流程图;图3为本发明载药微球-微针光镜图片;图4为本发明载药微球-微针均匀给药的荧光图片。
18.具体实施方式:为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中未注明的实施条件通常为常规实验中的条件。
19.本发明提供一种均匀给药的载药微球-微针阵列的制备方法,包括以下步骤:s1、载药微球的制备将药物与水凝胶混合,配制成水凝胶和药物混合溶液作为内相,外相为与内相互不相溶的油相(葵花籽油),将外相和内相注入微流控装置,利用两相溶液间的剪切力形成单分散的单乳液液滴,并可通过调节微流控内相和外相的流速改变液滴大小;液滴经紫外固化并收集,用酒精、去离子水漂洗数次,得到粒径均匀的聚合物载药微球(直径在100~300 μm之间);所述水凝胶选自甲基丙烯酸化水凝胶(gelma)、透明质酸(ha)、聚乳酸(pla)、壳聚糖的一种或多种。
20.s2、载药微球-微针阵列的制备
配制水凝胶溶液,将水凝胶溶液滴加到微针模板内,并通过抽真空使水凝胶溶液填满微针模板的空隙;将s1中得到的载药微球填充在微针模板的针尖部位,进行紫外交联固化,随后从微针模板剥离,得到载药微球-微针阵列;所述微针底部边长为200~600 μm,针长为300~1000 μm。水凝胶材料选自聚乙二醇双丙烯酸酯(pegda)、聚乳酸-羟基乙酸共聚物(plga)、海藻糖、聚乙二醇(peg)、二甲基丙烯酸乙二醇酯(egdma)中的一种或多种材料混合。所述的载药微球-微针阵列中,载药微球粒径小于针尖底部边长,可填充入微针针尖且载药微球的球形度不被影响。
21.实施例1——均匀给药的载药微球-微针阵列的制备s1、载药微球的制备通过外径1 mm内径500 μm的毛细管制备微流控装置,内相管用机器拉制并磨制成需要的口径,外相管经十八烷基三甲氧基硅烷疏水处理,内外相管同轴组装;内相管通20% gelma溶液、vegf溶液和1% 光引发剂混合溶液,外相管通葵花籽油,用蠕动泵控制内外相流速以控制液滴大小;用紫外灯垂直照射产生的单乳液液滴30s,再用无水乙醇和超纯水各洗涤3次,每次1分钟,得到粒径为150 μm的载药微球。
22.s2、载药微球-微针阵列的制备配制20% peg、50% pegda和1% 光引发剂的混合溶液,将配制的溶液滴加到微针模板(针长610μm,针底部边长290*290μm,针尖距离800μm,数量阵列20*20),抽真空5分钟,使混合溶液充分填充在微针模板的针尖中;将第s1中得到的载药微球逐个填充于微针模板的针尖部位,之后用紫外垂直照射15s固化,最后从模板中小心地剥离,得到载药微球-微针阵列。
23.实施例2——均匀给药的载药微球-微针阵列的制备s1、载药微球的制备通过外径1 mm内径800 μm的毛细管制备微流控装置,内相管用机器拉制并磨制成需要的口径,外相管经十八烷基三甲氧基硅烷疏水处理,内外相管同轴组装;内相管通15% gelma溶液、vegf溶液和1% 光引发剂混合溶液,外相管通葵花籽油,用蠕动泵控制内外相流速以控制液滴大小;用紫外灯垂直照射产生的单乳液液滴30s,再用无水乙醇和超纯水各洗涤3次,每次1分钟,得到粒径为250 μm的载药微球。
24.s2、载药微球-微针阵列的制备配制20% peg、50% pegda和1% 光引发剂的混合溶液,将配制的溶液滴加到微针模板(针长800μm,针底部边长410*410μm,针尖距离800μm,数量阵列10*10),抽真空5分钟,使混合溶液充分填充在微针模板的针尖中;将第s1中得到的载药微球逐个填充于微针模板的针尖部位,之后用紫外垂直照射15s固化,最后从模板中小心地剥离,得到载药微球-微针阵列。
25.以上仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的技术方案均属于本发明的保护范围,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理前提下的若干改进和润饰,应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1