长链脂酰辅酶A合成酶4的抑制剂在治疗帕金森疾病中的应用的制作方法
本发明涉及帕金森疾病治疗技术领域,具体而言,涉及长链脂酰辅酶a合成酶4的抑制剂在治疗帕金森疾病中的应用。
背景技术:
帕金森病(pd)是好发于老年人的神经变性病,主要由可以生成多巴胺的脑细胞缺失造成。临床主要特征为运动障碍包括进行性运动迟缓、肌强直、静止性震颤和姿势步态异常等,此外还可伴有大量非运动症状(nms),如嗅觉减退、便秘、抑郁、睡眠障碍等。随着病程的进展,运动症状和非运动症状逐渐加重,疾病后期常出现运动并发症,包括药物疗效减退、“开·关”现象、异动症等。疾病后期患者常因平衡障碍、跌倒、冻结步态、吞咽困难和语言障碍等导致生活无法自理,甚至长期卧床,生活质量严重下降。
据统计,中国有将近300万的帕金森病患者,占全球帕金森病患者的一半,是世界上该病患者最多的国家。而每年新增患者约10万,65岁以上发病率为1.7%,而就诊率仅占四成,由于漏诊、误诊等原因,这300万帕金森病患者中,能够真正被诊断和治疗的,不到50万人。统计显示,从1990年至2015年,全球的帕金森病患者人数翻了一番,超过620万人。专家预测,到2040年,这一数字将达到1200万。帕金森疾病给社会造成了极大地经济负担,其直接或间接性的支出方向主要包括:疾病治疗支出、社会保险支出、无工作能力而失去收入等,仅美国地区的这些患者每年的支出将高达2500万美元。
技术实现要素:
本发明的目的在于提供长链脂酰辅酶a合成酶4的抑制剂在治疗帕金森疾病中的应用。本发明的研究发现,以长链脂酰辅酶a合成酶4(acsl4)为靶点,使用acsl4的抑制剂可以改善帕金森疾病的相关症状,对帕金森疾病具有治疗作用;本发明为帕金森疾病的治疗提供了新的靶点和策略。
本发明是这样实现的:
一方面,本发明提供长链脂酰辅酶a合成酶4的抑制剂在制备用于预防或治疗帕金森疾病的药物中的应用。
本发明实施通过对帕金森病患者血清和脑组织中分离的黑质致密部(snpc)神经元进行全基因组转录组分析发现:帕金森病患者脑组织snpc神经元和血清的acsl4转录水平显著上调。通过进一步的实验发现,抑制acsl4的表达和活性能够明显改善帕金森病模型小鼠的运动症状,挽救帕金森病模型小鼠sn神经元的死亡。说明acsl4是治疗帕金森病的潜在靶点。通过抑制acsl4例如抑制患者acsl4或其编码基因的表达,或者抑制患者体内acsl4生物活性对治疗帕金森病具有改善作用,至少可以缓解患者的运动障碍,减少酪氨酸羟化酶的降低,减少多巴胺神经元的死亡。
基于此,本发明提出长链脂酰辅酶a合成酶4的抑制剂作为作为预防或治疗帕金森疾病的药物,具有治疗帕金森疾病的作用。
本发明揭示了acsl4在帕金森病运动障碍和发生发展中的关键作用,为帕金森疾病的研究和治疗提供了全新的理论和策略,并为帕金森病相关治疗药物的开发奠定了基础。
可选的,在本发明的一些实施方案中,所述抑制剂选自triacsinc和吡格列酮的任意一种。
基于本发明公开的内容,本领域技术人员可以选择合适的长链脂酰辅酶a合成酶4抑制剂用于治疗帕金森病,这些抑制剂包括但不限于上述的triacsinc和吡格列酮。只要是采用以长链脂酰辅酶a合成酶4为靶点抑制其活性的物质作为治疗帕金森病的药物即属于本发明的保护范围。
可选的,在本发明的一些实施方案中,所述抑制剂为抑制长链脂酰辅酶a合成酶4表达的病毒载体。
基于本发明公开的内容,本领域技术人员也可以采用基因治疗技术例如使用合适病毒载体导入患者体内实现帕金森病的治疗,只要该病毒载体能够抑制长链脂酰辅酶a合成酶4的表达例如抑制其基因表达以减低长链脂酰辅酶a合成酶4的水平,即可实现帕金森病的治疗效果。
可选的,在本发明的一些实施方案中,所述病毒载体为腺病毒相关病毒载体。
可选的,在本发明的一些实施方案中,所述腺病毒相关病毒载体为aav8病毒载体。
在其他的实施例中,腺病毒相关病毒载体也可以选用aav1、aav2、aav5、aav6、aav7或aav9等,本领域技术人员可以根据需要选择合适类型的病毒载体。
需要说明的是,长链脂酰辅酶a合成酶4和其基因序列已知的前提下,本领域技术人员通过本领域常规技术能够容易地制备出抑制acsl4基因表达的相关病毒载体。
此外,本领域技术人员也可以采用rna干扰技术在转录水平上抑制患者acsl4基因的表达,因此,将以抑制acsl4基因为目的并适用于rna干扰技术的相关产品作为治疗帕金森病的药物也是属于本发明的保护范围。
可选的,在本发明的一些实施方案中,所述药物的剂型为注射剂。
本领域技术人员可以根据需要,对上述抑制剂使用合适的剂型治疗帕金森病,包括但不限于注射剂,无论使用何种剂型都是不需要本领域技术人员付出创造性的劳动,因此,使用任意剂型的上述抑制剂治疗帕金森病都属于本发明的保护范围。
另一方面,本发明提供一种用于预防或治疗帕金森疾病的药物,所述药物以长链脂酰辅酶a合成酶4或其编码基因为靶点,抑制长链脂酰辅酶a合成酶4的活性或其表达水平。
基于本发明实施例的研究结果,本领域技术人员容易想到以长链脂酰辅酶a合成酶4作为靶点或靶标对帕金森疾病进行治疗,而相应的药物是本领域技术人员基于本发明的研究结果容易获得或筛选得到。这些药物可以是抑制长链脂酰辅酶a合成酶4的活性,使其失去正常的生物学功能;也可以是抑制长链脂酰辅酶a合成酶4基因的表达例如抑制转录或抑制翻译等,这类药物都是以长链脂酰辅酶a合成酶4作为靶点治疗帕金森疾病,其都属于本发明的保护范围。
另一方面,本发明提供一种用于预防或治疗帕金森疾病的药物的制备方法,其包括:以长链脂酰辅酶a合成酶4的抑制剂为主要活性成分将其与药学上可接受的辅料混合。
基于本发明公开的内容,本发明提供一种新的制备帕金森疾病治疗药物的方法,该方法以长链脂酰辅酶a合成酶4的抑制剂为主要活性成分。所制得的药物能够对帕金森疾病有治疗作用。
可选的,在本发明的一些实施方案中,所述抑制剂选自triacsinc和吡格列酮的任意一种。
可选的,在本发明的一些实施方案中,所述抑制剂为抑制长链脂酰辅酶a合成酶4表达的病毒载体。
可选的,在本发明的一些实施方案中,所述病毒载体为腺病毒相关病毒载体。
可选的,在本发明的一些实施方案中,所述腺病毒相关病毒载体为aav8病毒载体。
需要说明的是,药学上可接受的辅料是本领域技术人员根据需要合理选择,无论选用何种辅料均属于本发明的保护范围。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
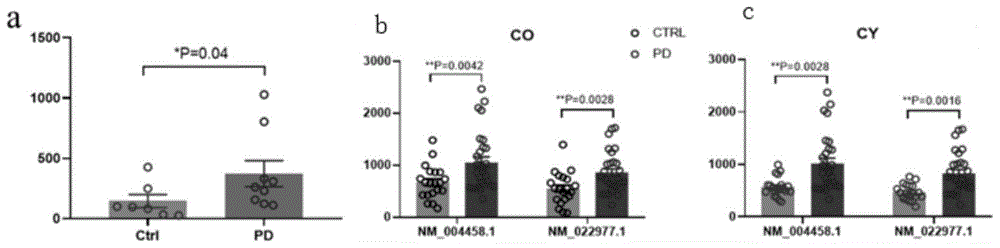
图1为帕金森病患者及年龄匹配正常人群有显著差异的长链脂酰辅酶a合成酶4表达量;
图中:
a:对人源黑质转录组学数据库gse20141数据进行分析,发现帕金森病人黑质长链脂酰辅酶a合成酶4基因(ensg00000068366)表达增加;
b:对人源血清acsl4转录组学(基因编号:nm_004458.1)数据进行分析,发现帕金森疾病患者血清acsl4表达较年轻正常对照增加;
c:对人源血清acsl4转录组学(基因编号:nm_022977.1)数据进行分析,发现帕金森疾病患者血清acsl4表达较老年正常对照增加。
图2为帕金森病模型小鼠有明显的运动障碍和长链脂酰辅酶a合成酶4表达异常;
图中:
a:westernblot检测帕金森疾病模型小鼠及其对照组小鼠大脑黑质区酪氨酸羟化酶(th)的表达水平;
b:爬杆测试检测帕金森疾病模型小鼠及其对照组小鼠运动能力,比较二者的转头时间(timetoturn);
c:旷场测试检测帕金森疾病模型小鼠及其对照组小鼠运动能力,比较二者的运动速度(ambulatoryepisodesaveragespeed)。
图3为aav8介导的acsl4敲除(knockout(ko))能够缓解帕金森病模型小鼠的运动障碍;
图中:
a:爬杆测试检测注射acsl4敲除病毒的帕金森疾病模型小鼠及其对照组小鼠运动能力,比较三组的转头时间(timetoturn);
b:转棒测试检测注射acsl4敲除病毒的帕金森疾病模型小鼠及其对照组小鼠运动能力,比较三组小鼠在棒上停留的时间(latencytofall);
c/d:步态测试注射acsl4敲除病毒的帕金森疾病模型小鼠及其对照组小鼠运动能力,分别统计三组小鼠的步宽和运动失调系数;fore代表前脚,hind代表后脚,leftfore代表左前脚,rightfore代表右前脚,lefthind代表左后脚,righthind代表右后脚;
e:westernblot检测注射acsl4敲除病毒的小鼠及其对照组小鼠脑内黑质区acsl4的表达水平。
图4为aav8介导的acsl4ko能够逆转帕金森疾病模型小鼠多巴胺神经元的死亡;
图中:
a/b:westernblot检测注射acsl4敲除病毒的帕金森疾病模型小鼠及其对照组小鼠脑内黑质区酪氨酸羟化酶(th)的表达水平,并做统计;
c/d:免疫组织化学染色检测射acsl4敲除病毒的帕金森疾病模型小鼠及其对照组小鼠脑内黑质区酪氨酸羟化酶阳性神经元的数量,通过体视学显微镜计数统计。
图5为acsl4抑制剂triacsinc治疗能够明显缓解帕金森疾病模型小鼠的运动障碍;
图中:
a:爬杆测试检测鼻腔给药triacsinc的帕金森疾病模型小鼠及其对照组小鼠运动能力,比较三组小鼠的转头时间(timetoturn);
b:旷场测试检测鼻腔给药triacsinc的帕金森疾病模型小鼠及其对照组小鼠运动能力,比较三组小鼠的运动速度(ambulatoryepisodesaveragespeed);
c:westernblot检测鼻腔给药triacsinc治疗的帕金森疾病模型小鼠及其对照组小鼠脑内黑质区酪氨酸羟化酶(th)的表达水平,并做统计。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
基于已发表的人源数据库gse20141数据,对其中长链脂酰辅酶a合成酶4的转录组数据进行统计分析,发现其中帕金森病患者snpc的长链脂酰辅酶a合成酶4基因(ensg00000068366)表达增加(图1中a),血清中基因表达也增加(图1中b,c)。
实施例2
1-甲基-4-苯基-1,2,3,6-四氢吡啶(mptp)能在黑质细胞内脱氢生成mpp+离子,这种离子抑制线粒体复合酶,使该细胞死亡。mptp是制作动物帕金森病模型的常用药物之一。
c57小鼠腹腔注射mptp(20mg/kg),八小时注射四次,每两小时注射一次。注射后第19天至第21天开展行为学测试。爬杆测试显示注射mptp的小鼠转头时间明显更长,旷场测试显示mptp注射小鼠的运动速度明显变慢,表明小鼠的运动能力受到损伤(图2中b,c);第21天安乐死小鼠,pbs灌流后,取左侧大脑黑质部位检测酪氨酸羟化酶(tyrosinehydroxylase)和acsl4的表达,右侧大脑浸泡在4%多聚甲醛中,通过病理切片检测多巴胺神经的数量。结果显示:帕金森病模型小鼠黑质部位酪氨酸羟化酶的表达显著降低,acsl4的表达显著升高(图2中a),行为学检测反映出帕金森病模型小鼠的运动能力严重受损(图2中b,c)。
实施例3
aav病毒载体在神经系统的体内应用具有安全、高效和毒性低等优势,非常适用于神经系统的研究。通过在小鼠黑质部位注射能敲除小鼠acsl4基因的aav8-acsl4病毒载体,实现了黑质acsl4表达的敲低(图3中e),病毒注射30天后,构建帕金森病mptp模型,通过行为学检测以及病理切片检测评价黑质acsl4敲除对帕金森病模型的保护作用。结果显示:aav8介导的acsl4基因敲除能够缓解帕金森病模型小鼠的运动障碍(图3中a-d)和挽救mptp造模后酪氨酸羟化酶的表达的降低(图4中a,b)以及减少多巴胺神经元的死亡(图4中c,d)。
实施例4
triacsinc来自金黄色链霉菌(streptomycesaureofaciens),是一种天然细胞内长链酰基辅酶a合成酶(acsl)抑制剂,能够有效抑制acsl1和acsl4的活性。通过腹腔注射mptp模型(剂量同实施例1),造模第二天开始鼻腔注射25ul,5mg/ml的triacsinc,连续注射8天,mptp造模后第19天至21天行为学检测triacsinc治疗效果,第21天处死小鼠,灌流,收集小鼠脑组织的左侧黑质,右侧脑组织浸泡在4%多聚甲醛中用于后续的病理切片。结果:triacsinc治疗8天后,能够明显缓解pd模型小鼠的运动障碍(图5中a,b),改善pd模型小鼠黑质的多巴胺神经元标记物酪氨酸羟化酶的表达量(图5中c)。
以上结果充分说明说明,acsl4可以作为帕金森疾病的治疗靶点,通过对帕金森疾病患者施用acsl4的抑制剂例如,能够改善帕金森疾病的相关症状例如缓解运动障碍、减少酪氨酸羟化酶的表达降低、减少多巴胺神经元的死亡等。
上述实施例中所涉及相关检测方法如下:
(1)蛋白免疫印迹(westernblot)
1)蛋白收集及浓度测定:将解剖出来的组织在4℃裂解液中匀浆,匀浆后静置15-20分钟;或收集的细胞在4℃裂解液中静置30分钟。4℃13000g离心20分钟,取上清。取96孔板,每个样重复3个孔。每孔内加18μlpbs,2μl提取的上清,及200μlbca液,混匀,在37℃下孵育30分钟。在562nm下测吸光度。根据蛋白浓度与吸光度之间关系的标准曲线计算蛋白浓度(μg/μl)。
2)配上样体系:根据目的蛋白在总提取蛋白中可能的含量比例,以及提取的总蛋白浓度,取20-50μg总蛋白进行电泳分离。以配含20μg蛋白的20μl体系为例,体系中加入算得的蛋白液体积、10xreducingagent2μl、4xsampleloadingbuffer5μl,加入蒸馏水补齐20μl。将体系在100℃变性5分钟。
3)上样与电泳:样品体系冷却到室温后直接上样到预制胶加样孔内。留一个孔加蛋白分子量参考marker“see
4)转膜:剪切合适尺寸的pvdf膜和滤纸。将切好的pvdf膜在甲醇中激活2-10s,变色即可使用。随后将滤纸、海绵垫、激活的膜放在有转移液的盘里。将电泳胶从夹板中剥离,放入含有转移液的盘里。转移液盘里的胶、膜、滤纸和海绵依负极到正极分别是海绵-三层滤纸-胶-膜-三层滤纸-海绵的顺序摆放。整个过程均在放置有转膜缓冲液的盘中进行。完成以上转膜结构后,将其放入转膜夹中,再放入转膜槽中,加满转膜缓冲液,然后放置在4℃层析柜中,一般用100v转移1h,具体应根据蛋白质大小确定。
5)免疫反应:将含有蛋白条带的pvdf膜取出后pbs稍加漂洗,用镊子移至含有5%脱脂奶粉封闭液的平皿中,室温下水平摇床上摇动封闭1h。封闭完成后去掉封闭液,使用适量tbst(淹没过膜即可),室温在水平摇床上洗2次,每次5分钟。将一抗用tbst稀释至适当浓度(查看抗体说明书,确定稀释倍数),去掉平皿中洗膜液,加入抗体,置于水平摇床上,4℃过夜。回收或倒掉一抗,用tbst在室温下水平摇床上洗3次,每次5分钟。将二抗用tbst稀释至适当浓度,室温下孵育1h。去掉二抗,用tbst在室温水平摇床上洗3次,每次10分钟,随后进行化学发光反应。
6)化学发光显影:显影液依说明书配制比例现配现用。将膜放于显影仪中,滴加发光液,设置曝光参数,根据曝光结果可微调曝光时间。曝光结果将用于后续统计分析。
(2)免疫酶组化:
1)洗片:使用pbs清洗切片3次,每次5分钟。
2)封闭:室温静置封闭1小时,封闭液:0.3%tritonx-100+5%ngsin1xpbs。
3)一抗:依据抗体说明书推荐浓度,使用封闭液稀释抗体,4℃孵育过夜。随后将抗体溶液去除,用0.2%tween-20in1xpbs清洗切片3次,每次5分钟。
4)二抗:带hrp(辣根过氧化物酶)标签的二抗,依据抗体说明书推荐浓度,使用封闭液稀释抗体,室温孵育2小时。随后将抗体溶液去除,用0.2%tween-20in1xpbs清洗切片3次,每次5分钟。
5)显色:使用dab进行进一步标记。dab按试剂说明书配置,镜下观察,至目的组织出现棕黄色阳性颗粒而周围组织无非特异性显色时,蒸馏水终止,洗去dab溶液。
6)封片:使用中性树胶封片。
(3)爬杆测试:
将小鼠垂直放置在直径1厘米高50厘米的垂直木杆上。在测试前一天(第1天)进行适应,具体操作是将小鼠头朝上放在木杆顶端,依其本能往下滑或者调头爬向地面,连续进行五次试验。然后在测试当天(第2天)通过视频录制软件记录小鼠整个爬杆过程,实验结束后根据录制的视频分析小鼠从头部朝上到调头身体完全朝下的时间间隔(转身时间,tturn)和从木杆顶部完全下至地面的时间间隔(完成时间,tcomplete)。每只小鼠进行了五次试验,并且将平均值用于分析。
(4)转棒测试(3b):
将小鼠放在4r/min匀速运行的转棒仪上,随后开始加速程序(5分钟内从4r/min加速到40r/min)。记录小鼠从开始到掉落的时间。每只小鼠重复3次,每次间隔30分钟,取平均值做统计分析。
(5)旷场测试(2c,5b):
使用medassociate公司的env-510行为监测系统,红外记录小鼠自由活动。具体是小鼠放置在27.31cm×27.31cm×20.32cm(长×宽×高)的透明箱内,关上柜门,适应10分钟,随后记录50分钟内小鼠的运动距离、运动时间、平均速度等参数。
(6)步态测试(3c,3d):
使用digigaittm影像系统对小鼠的行走步态进行量化分析。具体是将小鼠放在透明机械跑步带上行走,跑步带的运行速度是15cm/s(此速度根据预实验确定,依据是小鼠在此速度下可以稳定爬行,不是低速下的探索性或觅食样行走,或者高速下的无法行走),高速相机录取小鼠爬行大概1分钟的视频,选取其中稳定运行约4s左右的视频进行分析。digigait8软件可以识别高速相机录制的视频中小鼠前后肢接触跑步带的面积与时间,进而统计出多项步态动力学的姿势和运动学指标。
(7)aav8-acsl4病毒载体的制备方法:
将小鼠acsl4cdna导入agei和saci切割质粒pssaav-cp-egfp中,生成pssaav-macsl4。设计用于敲除acsl4的sgrna,将sgrna与pssaav-macsl4载体连接,对连接后的载体编辑效率进行筛选。用于敲除acsl4pssaav-macsl4-sp.g3和egfp表达质粒pssaav-cb-egfp制备血清8型raav载体(raav8)。所有raav8载体均采用三质粒共转染法在人胚胎肾293细胞中生成。转染后72小时收集raav8载体,进行两轮cscl梯度超离心纯化,随后进行银染和基因组拷贝滴定。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!