一种复合组织粘合剂及其制备方法和应用与流程
1.本发明涉及创面粘合技术领域,更具体地涉及一种复合组织粘合剂及其制备方法和应用。
背景技术:
2.在外科手术中,较大的创口通常需要医用缝线或者打钉对其进行吻合封闭,后续为防止伤口渗血或感染,会采用组织封堵胶(如白云医用胶)或敷料等对缝隙进行填充和封闭,对于一些组织间小的缝隙,直接采用组织封堵胶闭合。但临床上创面往往伴随着血液或组织液的持续渗出,存在渗漏的情况,创面比较湿润。虽然部分手术部位较易清理渗液,但是对于创面较深等特殊部位则难以清理,因此急需一款可以很好的处理湿润创面的组织胶产品。目前市售的组织胶在湿润的创面使用时存在与组织粘附强度低或不粘附的问题,也有的存在在湿润条件下成胶发生放热和不可降解等问题,不能很好地满足临床上对于湿润创面进行闭合修复的需求。
3.cn106075553a公开了一种生物医用粘合剂及其制备方法,其公开的是一种能与伤口皮肤组织发生交联反应的生物医用粘合剂,所述粘合剂按照如下方法制备得到:首先,用高碘酸钠氧化海藻酸钠制得双醛海藻酸钠,透析、干燥后将产物溶于mes缓冲溶液中,然后加入羧甲基壳聚糖,搅拌反应6~12h后,依次加入一定量的n
‑
羟基琥珀酰亚胺、1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺盐酸盐和多巴胺,在氮气保护下继续搅拌反应8~24h,透析、冻干、阴凉干燥处保存。使用前,用双氧水预处理伤口,然后将冻干的粘合剂用pbs缓冲液溶解后立即涂覆到创面伤口处,2~10min内即可粘合伤口。该粘合剂在体内湿润环境下有较强的粘合强度,生物相容性好,可生物降解,能有效地促进伤口愈合。但是该生物医用粘合剂存在自身力学强度差,无法对创面形成较强的封堵,使用前需要溶解而操作不方便等不足。
4.因此,研发一种在湿润的创面使用时可以与组织很好的粘附,并且自身具有良好的力学强度,具有使用便利性的新型复合组织粘合剂对于湿润创面的修复具有重要的意义。
技术实现要素:
5.本发明的目的是针对现有技术中湿润创面修复粘合的组织粘合剂的组织粘附强度低、使用过程中粘合剂自身缺乏一定力学强度的缺陷和不足,提供一种复合组织粘合剂。
6.本发明的另一目的在于提供一种复合组织粘合剂的制备方法。
7.本发明的再一目的在于提供一种复合组织粘合剂在制备湿润创面粘合产品中的应用。
8.本发明上述目的通过以下技术方案实现:
9.一种复合组织粘合剂,所述复合组织粘合剂包括三维多孔基质以及吸附在基质表面的增强粘附因子,所述三维多孔基质由甲基丙烯酸酐化明胶和接枝n
‑
羟基琥珀酰亚胺的聚丙烯酸的复合水凝胶冻干得到,所述增强粘附因子为聚多巴胺。
10.本发明的复合组织粘合剂的作用机理如下:本发明的复合组织粘合剂为干态,无需低温保存,无需使用前溶解,在湿润创面上使用时,复合组织粘合剂所具有三维多孔结构可以吸收湿润创面的液体,使所接触的湿润创面快速形成干燥创面,同时,复合组织粘合剂的三维多孔结构所吸附的聚多巴胺以及复合组织粘合剂上接枝的n
‑
羟基琥珀酰亚胺(nhs)都可以与创面组织的氨基键合,具有强组织粘附强度,有利于粘合封堵创面。
11.进一步地,复合组织粘合剂还包括聚赖氨酸和/或聚乙烯亚胺,所述聚赖氨酸和/或聚乙烯亚的羧基与聚丙烯酸的琥珀酰亚胺端基通过肽键连接,聚赖氨酸和/或聚乙烯亚胺与聚丙烯酸形成聚合物网络结构,进一步加强了复合组织粘合剂的湿态力学强度。
12.进一步地,复合组织粘合剂的聚多巴胺负载量为10%(w/w)~30%(w/w),接枝n
‑
羟基琥珀酰亚胺(nhs)的聚丙烯酸的接枝率为1%~10%。复合组织粘合剂同时具有聚多巴胺及琥珀酰亚胺基团这两种粘附因子,可以很好地在湿润创面环境中进行粘合封堵。
13.进一步地,复合组织粘合剂的吸液量≥500%,优选为600%~1500%;湿态力学强度≥50n,组织粘附强度≥180kpa。
14.本发明同时还保护一种复合组织粘合剂的制备方法,包括如下步骤:
15.s1:将甲基丙烯酸酐化明胶和聚丙烯酸或丙烯酸单体进行均匀混合,并对聚丙烯酸或丙烯酸单体进行n
‑
羟基琥珀酰亚胺接枝;
16.s2:将s1中接枝后的混合物进行光交联,形成复合水凝胶;
17.s3:将s2中复合水凝胶低温冷冻后进行第一次冻干,得到海绵状的三维多孔基质;
18.s4:将s3中三维多孔基质浸泡在ph为8~10含有多巴胺的溶液中,并在通氧气条件下浸泡不少于20h;优选地,所述溶液的ph为8.5,并在通氧气条件下浸泡20~25h,得到复合组织粘合剂前体;
19.s5:将s4中浸泡后的复合组织粘合剂前体取出,进行第二次低温冷冻后进行第二次冻干,辐照灭菌制得复合组织粘合剂。
20.其中,需要说明的是:
21.s1中甲基丙烯酸酐化明胶由甲基丙烯酸酐与明胶制备获得,是一种光敏性的生物水凝胶材料,该材料具有优异的生物相容性,且可由紫外光或可见光激发固化反应,形成适于细胞生长与分化且有较高强度的三维结构。对聚丙烯酸或丙烯酸单体进行n
‑
羟基琥珀酰亚胺(nhs)接枝,修饰上的琥珀酰亚胺基团可以与组织上的氨基反应,增强复合组织粘合剂和湿润创面的组织粘附强度,并且接枝nhs可以进一步和其他聚合物键合来增加复合组织粘合剂的自身力学强度。本发明在甲基丙烯酸酐化明胶形成水凝胶前,先将甲基丙烯酸酐化明胶与聚丙烯酸或丙烯酸均匀混合,可以使得接枝nhs后的聚丙烯酸均匀分布在凝胶产品中。
22.优选地,s1中所述甲基丙烯酸酐化明胶中甲基丙烯酸的取代率≥40%,甲基丙烯酸的取代率越高,复合组织粘合剂的力学性能越强。
23.优选地,s1中所述聚丙烯酸的nhs接枝的接枝率为1%~10%,进一步优选所述聚丙烯酸的nhs接枝的接枝率为3%~10%。
24.优选地,s1中所述甲基丙烯酸酐化明胶和聚丙烯酸或丙烯酸的质量为1:(1~100),其中优选1:(50~100)。
25.s2中,甲基丙烯酸酐化明胶和丙烯酸或聚丙烯酸在光照条件下均可单独进行交
联,形成水凝胶。本发明中甲基丙烯酸酐化明胶增强接枝n
‑
羟基琥珀酰亚胺的聚丙烯酸水凝胶的力学强度;聚丙烯酸接枝一定量的n
‑
羟基琥珀酰亚胺后可以和人体组织上的氨基反应,具有一定的粘附强度。
26.优选地,s2中光交联的交联剂为i2959紫外光引发剂、lap蓝光引发剂或α
‑
酮戊二酸;光交联的交联剂的添加量为接枝后的混合物质量的0.05%~5%。
27.s3中,第一次冻干后的海绵状三维多孔基的湿态力学强度≥20n,组织粘附强度≥70kpa,先低温冷冻后冻干,所得到三维多孔的结构孔隙率更高,吸液性能更好,以便后续过程吸附更多的聚多巴胺,跟现有的化学接枝法相比,使用三维多孔基吸附聚多巴胺可以不受可接枝基团的限制,使得复合组织粘合剂表面得到更多的聚多巴胺,增强复合组织粘合剂的组织粘附效果。
28.s4中,多巴胺在碱性并通氧气的条件下可在三维多孔基表面形成聚多巴胺,聚多巴胺可以在湿润的组织创面也具有较好的粘附性。
29.优选地,s4中溶液的多巴胺的浓度为0.5g/ml~6g/ml。
30.优选地,s4中所述溶液的ph为8.5,并在通氧气条件下浸泡20~25h。
31.进一步优选地,利用聚乙烯亚胺和聚赖氨酸作为缓冲对调配提供ph8.5的溶液环境,聚乙烯亚胺和聚赖氨酸具有伯氨基,可以和聚丙烯酸所接枝的n
‑
羟基琥珀酰亚胺中的一部分反应,进一步巩固聚丙烯酸形成的交联网络,增强复合组织粘合剂的湿态力学强度。
32.优选地,s4的多巴胺溶液中的溶剂为pbs缓冲溶液或pbs
‑
聚乙烯亚胺溶液或pbs
‑
聚赖氨酸溶液或聚赖氨酸和聚乙烯亚胺组成的混合溶液。
33.另外,本发明还具体保护上述复合组织粘合剂在制备湿润创面粘合产品中的应用。
34.与现有技术相比,本发明的有益效果是:
35.本发明的复合组织粘合剂具有多孔结构,可以吸收湿润创面的液体,使湿润创面快速形成干燥创面,且聚丙烯酸带有负电荷的羧酸基团,其一定程度上可以加快组织粘合剂的水化膨胀效果,加快组织表面干燥速度,因而复合组织粘合剂具有500%以上的吸液量,优选600%~1500%。
36.另一方面,本发明的复合组织粘合剂具有两种基团可与创面组织上的氨基进行键合,很大程度上提高了粘合剂与创面的粘合强度,可以达到180kpa以上的组织粘附强度,同时,复合组织粘合剂自身具有50n以上的力学强度。
37.本发明的复合组织粘合剂是一种干态的组织粘合剂,无需低温储存,便于储存和运输,其具有较高的液体吸收性和超强粘附性能,在湿润创面可以直接使用,且具有可降解,在成胶时不放热,可以达到很好的湿润创面粘合效果,满足临床需求。
38.本发明的复合组织粘合剂的制备方法通过得到甲基丙烯酸酐化明胶与聚丙烯酸
‑
nhs的复合三维多孔基质,表面吸附聚多巴胺,可以避免一般化学接枝法的接枝率低,修饰上的聚多巴胺含量低的不足,使得复合组织粘合剂表面具有更多的多巴胺进而具有更高的组织粘附强度。
39.另一方面,本发明的制备方法得到的复合组织粘合剂上同时具有聚多巴胺和琥珀酰亚胺端基,可与创面组织上的氨基形成键合,使粘合剂与创面粘合在一起,可以很好地增加粘合剂的组织粘附强度,制备过程还可以加入聚赖氨酸和/或聚乙烯亚胺进一步增强复
合组织粘合剂的湿态力学强度。
具体实施方式
40.下面结合具体实施方式对本发明作进一步的说明,但实施例并不对本发明做任何形式的限定。除非另有说明,本发明实施例采用的原料试剂为常规购买的原料试剂。
41.实施例1
42.一种复合组织粘合剂,复合组织粘合剂包括三维多孔基质以及吸附在基质表面的增强粘附因子,三维多孔基质由甲基丙烯酸酐化明胶和接枝n
‑
羟基琥珀酰亚胺的聚丙烯酸的复合水凝胶冻干得到,增强粘附因子为聚多巴胺,
43.复合组织粘合剂还包括聚赖氨酸和聚乙烯亚胺,聚赖氨酸和聚乙烯亚的羧基与所述聚丙烯酸接枝的琥珀酰亚胺端基通过肽键连接。
44.复合组织粘合剂的制备方法,包括如下步骤:
45.s1:将甲基丙烯酸酐化明胶(甲基丙烯酸的取代率为75%)和聚丙烯酸进行混合,并对聚丙烯酸进行nhs接枝:称量20ml水于烧杯中,先后加入聚丙烯酸2g,edc0.5g,nhs 0.1g,甲基丙烯酸酐化明胶0.02g,搅拌溶解均匀,甲基丙烯酸酐化明胶和聚丙烯酸的质量比为1:100;
46.s2:加入0.05gα
‑
酮戊二酸,搅拌均匀后转移适量溶液至无氧的成型模具中(厚度不超过1.5mm),将s1中接枝后的混合物进行光交联,使用284nm,10w紫外灯照射30~120min,直至完全固化成水凝胶状,光交联的交联剂的添加量为1.9%(w/w);
47.s3:将s2中水凝胶放置在
‑
80℃冰箱中冷冻过夜,然后转移至冷冻干燥机,进行第一次低温冷冻干燥,制成三维多孔基质;
48.s4:将s3中三维多孔基质样品2.0g浸泡在含有.0.6g/ml多巴胺的用聚赖氨酸和聚乙烯亚胺调节至ph为8.5的溶液中,并往溶液中持续通氧气,浸泡24h后取出,得到复合粘合剂前体;
49.s5:将s4中浸泡后的复合粘合剂前体进行第二次低温冷冻后进行第二次冻干,将组织粘合剂进行密封包装后,辐照灭菌制得复合组织粘合剂。
50.实施例2
51.一种复合组织粘合剂,复合组织粘合剂包括三维多孔基质以及吸附在基质表面的增强粘附因子,三维多孔基质由甲基丙烯酸酐化明胶和接枝n
‑
羟基琥珀酰亚胺的聚丙烯酸的复合水凝胶冻干得到,增强粘附因子为聚多巴胺,
52.复合组织粘合剂还包括聚赖氨酸,聚赖氨酸的羧基与所述聚丙烯酸接枝的琥珀酰亚胺端基通过肽键连接。
53.复合组织粘合剂的制备方法,包括如下步骤:
54.s1:将甲基丙烯酸酐化明胶(甲基丙烯酸的取代率为95%)和聚丙烯酸进行混合,并对聚丙烯酸进行nhs接枝:称量20ml水于烧杯中,先后加入聚丙烯酸5g,edc2g,nhs 0.5g,甲基丙烯酸酐化明胶0.1g,搅拌溶解均匀,甲基丙烯酸酐化明胶和聚丙烯酸的质量比为1:50;
55.s2:加入0.2g i2959紫外光引发剂,搅拌均匀后转移适量溶液至无氧的成型模具中(厚度不超过1.5mm),s1中接枝后的混合物进行光交联,使用284nm,10w紫外灯照射30~
120min,直至完全固化成水凝胶状,光交联的交联剂的添加量为2.6%(w/w);
56.s3:将s2中水凝胶放置在
‑
80℃冰箱中冷冻过夜,然后转移至冷冻干燥机,进行第一次低温冷冻干燥,制成三维多孔基质;
57.s4:将s3中三维多孔基质样品3.0g浸泡在含有0.2g多巴胺的ph为8.5的聚赖氨酸
‑
pbs30ml溶液中,并往溶液中持续通氧气,浸泡24h后取出,得到复合粘合剂前体;
58.s5:将s4中浸泡后的复合粘合剂前体进行第二次低温冷冻后进行第二次冻干,将组织粘合剂进行密封包装后,辐照灭菌制得复合组织粘合剂。
59.实施例3
60.一种复合组织粘合剂,复合组织粘合剂包括三维多孔基质以及吸附在基质表面的增强粘附因子,三维多孔基质由甲基丙烯酸酐化明胶和接枝n
‑
羟基琥珀酰亚胺的聚丙烯酸的复合水凝胶冻干得到,增强粘附因子为聚多巴胺,
61.复合组织粘合剂还包括聚乙烯亚胺,聚乙烯亚的羧基与所述聚丙烯酸接枝的琥珀酰亚胺端基通过肽键连接。
62.复合组织粘合剂的制备方法,包括如下步骤:
63.s1:将甲基丙烯酸酐化明胶(甲基丙烯酸的取代率为85%)和聚丙烯酸进行混合,并对聚丙烯酸进行nhs接枝:称量20ml水于烧杯中,先后加入聚丙烯酸3g,edc1g,nhs 0.2g和甲基丙烯酸酐化明胶0.06g,搅拌溶解均匀,甲基丙烯酸酐化明胶和聚丙烯酸的质量比为1:50;
64.s2:加入0.13g lap蓝光引发剂,搅拌均匀后转移适量溶液至无氧的成型模具中(厚度不超过1.5mm),s1中接枝后的混合物进行光交联,使用405nm,10w紫外灯照射30~120min,直至完全固化成水凝胶状,光交联的交联剂的添加量为3.1%(w/w);
65.s3:将s2中水凝胶放置在
‑
80℃冰箱中冷冻过夜,然后转移至冷冻干燥机,进行第一次低温冷冻干燥,制成三维多孔基质;
66.s4:将s3中三维多孔基质样品3.0g浸泡在含有0.4g多巴胺的ph为8.5的聚乙烯亚胺
‑
pbs的35ml溶液中,并往溶液中持续通氧气,浸泡24h后取出,得到复合粘合剂前体;
67.s5:将s4中浸泡后的复合粘合剂前体进行第二次低温冷冻后进行第二次冻干,将组织粘合剂进行密封包装后,辐照灭菌制得复合组织粘合剂。
68.实施例4
69.一种复合组织粘合剂,复合组织粘合剂包括三维多孔基质以及吸附在基质表面的增强粘附因子,三维多孔基质由甲基丙烯酸酐化明胶和接枝n
‑
羟基琥珀酰亚胺的聚丙烯酸的复合水凝胶冻干得到,增强粘附因子为聚多巴胺。
70.复合组织粘合剂的制备方法,包括如下步骤:
71.s1:将甲基丙烯酸酐化明胶(甲基丙烯酸的取代率为95%)和聚丙烯酸进行混合,并对聚丙烯酸进行nhs接枝:称量20ml水于烧杯中,先后加入聚丙烯酸2g,edc0.5g,nhs 0.1g,甲基丙烯酸酐化明胶0.02g,搅拌溶解均匀,甲基丙烯酸酐化明胶和聚丙烯酸的质量比为1:100;
72.s2:加入0.05gα
‑
酮戊二酸,搅拌均匀后转移适量溶液至无氧的成型模具中(厚度不超过1.5mm),将s1中接枝后的混合物进行光交联,使用284nm,10w紫外灯照射30~120min,直至完全固化成水凝胶状,光交联的交联剂的添加量为1.9%(w/w);
73.s3:将s2中水凝胶放置在
‑
80℃冰箱中冷冻过夜,然后转移至冷冻干燥机,进行第一次低温冷冻干燥,制成三维多孔基质;
74.s4:将s3中三维多孔基质样品2.0g浸泡在含有0.3g多巴胺的ph8.5的10ml pbs溶液中,并往溶液中持续通氧气,浸泡24h后取出,得到复合粘合剂前体;
75.s5:将s4中浸泡后的复合粘合剂前体进行第二次低温冷冻后进行第二次冻干,将组织粘合剂进行密封包装后,辐照灭菌制得复合组织粘合剂。
76.对比例1
77.一种复合组织粘合剂,制备方法包括如下步骤:
78.s1:将甲基丙烯酸酐化明胶(甲基丙烯酸的取代率为75%)和聚丙烯酸体进行混合:称量20ml水于烧杯中,先后加入聚丙烯酸2g,甲基丙烯酸明胶0.02g,搅拌溶解均匀,甲基丙烯酸酐化明胶和聚丙烯酸的质量比为1:100;
79.s2:加入0.05gα
‑
酮戊二酸,搅拌均匀后转移适量溶液至无氧的成型模具中(厚度不超过1.5mm),将s1中接枝后的混合物进行光交联,使用284nm,10w紫外灯照射30~120min,直至完全固化成水凝胶状;
80.s3:将s2中水凝胶放置在
‑
80℃冰箱中冷冻过夜,然后转移至冷冻干燥机,进行第一次低温冷冻干燥,制成三维多孔基质;
81.s4:将s3中三维多孔基质样品2g浸泡在含有0.6g多巴胺的ph8.5为聚赖氨酸和聚乙烯亚胺溶液中,并往溶液中持续通氧气,浸泡24h后取出,得到复合粘合剂前体;
82.s5:将s4中浸泡后的复合粘合剂前体进行第二次低温冷冻后进行第二次冻干,将组织粘合剂进行密封包装后,辐照灭菌制得复合组织粘合剂。
83.对比例2
84.一种复合组织粘合剂,制备方法包括如下步骤:
85.s1:将甲基丙烯酸酐化明胶(甲基丙烯酸的取代率为85%)和聚丙烯酸进行混合,并对聚丙烯酸进行nhs接枝:称量20ml水于烧杯中,先后加入聚丙烯酸2g,edc0.5g,nhs 0.1g,甲基丙烯酸明胶0.02g,搅拌溶解均匀,甲基丙烯酸酐化明胶和聚丙烯酸的质量比为1:100;
86.s2:加入0.05gα
‑
酮戊二酸,搅拌均匀后转移适量溶液至无氧的成型模具中(厚度不超过1.5mm),将s1中接枝后的混合物进行光交联,使用284nm,10w紫外灯照射30
‑
120min,直至完全固化成水凝胶状,得到复合组织粘合剂。
87.结果检测
88.(1)聚多巴胺含量检测
89.步骤1:取1g复合组织粘合剂,放入50ml离心管中,加入纯化水使其完全浸没复合组织粘合剂,盖上盖子密封。
90.步骤2:将离心管放在震荡仪上高速震荡20分钟。
91.步骤3:将溶液至一个洁净烧杯a中,复合组织粘合剂依然留着离心管里,
92.步骤4:向离心管中继续加入纯化水,使其完全浸没复合组织粘合剂。重复步骤2
‑
步骤3。将溶液倒继续导入烧杯a中。
93.步骤5:重复步骤2
‑
步骤4,直至溶液中不可见黑色颗粒。
94.步骤6:将烧杯a中溶液放入低温冰箱,使其固化。使用冷冻干燥机,冻干样品。得到
干燥样品。
95.步骤7:称重得到的干燥样品。
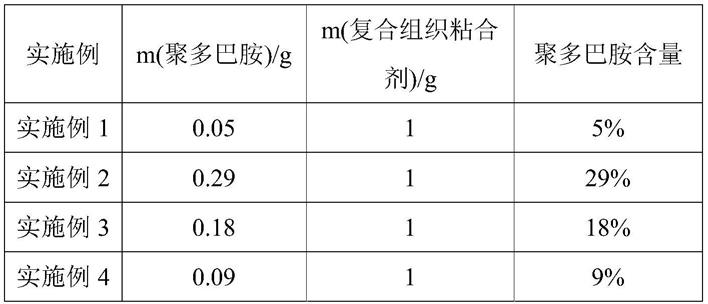
96.检测结果如表1所示。
97.表1
[0098][0099]
(2)nhs接枝率检测
[0100]
检测方法为紫外
‑
可见分光光度法测定nhs浓度。
[0101]
标准曲线:
[0102]
称取n
‑
羟基琥珀酰亚胺(简称:nhs)12.5mg至100ml容量瓶中,用ph7.4的pbs缓冲溶液溶解并稀释至刻度,作为对照品储备溶液。分别移取0.4ml,0.8ml,1.2ml,1.6ml,2.0ml于5个10ml容量瓶中,分别加入pbs缓冲溶液稀释定容。获得浓度为0.5mg/ml,1.0mg/ml,1.5mg/ml,2.0mg/ml,2.5mg/ml的溶液。按照《中国药典》2020年版四部通则0401紫外
‑
可见分光光度法,用紫外分光光度计在最大吸收波长260nm处检测其吸光度值。同时以pbs缓冲溶液作为空白试验,平行检测两次,取平均值。以nhs浓度为横坐标,以吸光度为纵坐标绘制标准曲线。
[0103]
检验液制备:
[0104]
称取复合组织粘合剂约1g,放置在洁净的研钵中,研磨至无明显块状,然后转移至离心管中,向离心管中加入25mlph值为7.4pbs缓冲溶液,封口。将离心管放置在震荡仪上震荡2分钟,然后将离心管置于37℃
±
1℃进行浸提5h。对离心管中的溶液进行过滤。取滤液,并使用pbs缓冲溶液对滤液进行稀释100倍作为检验液。
[0105]
检测结果计算:
[0106]
取上述检验液,按照《中国药典》2020年版四部通则0401紫外
‑
可见分光光度法,用紫外分光光度计在最大吸收波长260nm处检测其吸光度值。计算nhs含量。
[0107]
m(nhs)=100*c*v,
[0108]
其中:
[0109]
m(nhs)为nhs的含量,mg;
[0110]
c为标准曲线查得nhs质量浓度,mg/ml;
[0111]
v为使用pbs缓冲溶液稀释100后滤液的体积,ml。
[0112]
则nhs的接枝率=m(nhs)/m(聚丙烯酸或丙烯酸单体)*10
‑
3*100%
[0113]
检测结果见表2。
[0114]
表2
[0115]
实施例m(nhs)/mgm(聚丙烯酸或丙烯酸单体)/g接枝率实施例18524.25%实施例238557.7%实施例315535.17%实施例48024.0%
[0116]
(3)液体吸收性评价
[0117]
分别取上述实施例和对比例中的复合组织粘合剂,称重记为m0,完全浸没于pbs溶液中并开始计时,浸泡5min后取出拭去水凝胶表面多余的水,并称重,重量记为m1。
[0118]
按以下公式计算液体吸收率:
[0119]
液体吸收率=(m1
‑
m0)/m0*100%
[0120]
检测结果见表3。
[0121]
表3
[0122]
实施例液体吸收率实施例1670%实施例21205%实施例3838%实施例41156%对比例1650%对比例2132%
[0123]
(4)力学测试和粘附强度评价
[0124]
分别取上述实施例和对比例中第一次冻干得到的三维多孔基质和第二次冻干得到的复合组织粘合剂,进行力学测试和粘附强度评价。检测方法如下:
[0125]
力学测试:用生理盐水润湿样品,使其呈水凝胶状,将水凝胶裁成1cm*4cm的样条。将样条分别夹在万能拉力机上,启动拉力机,记录凝胶被拉断的最大力。
[0126]
粘附强度测试:分别取上述实施例和对比例中第一次冻干得到的三维多孔基质和第二次冻干得到的,在湿润的猪皮和猪肝上进行粘附测试。试验前,先将猪皮分别浸泡于水中30min,取出后,分别将复合组织粘合剂贴附在湿润的猪皮上,并按压5min。观察粘附效果,并使用拉力机进行抗撕裂测试,测试拉开复合组织粘合剂所需的最大力。
[0127]
检测结果见表4
[0128]
表4
[0129]
[0130][0131]
结合上述数据可知,含有多孔结构吸附了聚多巴胺的复合组织粘附剂的组织粘附强度均大于甲基丙烯酸酐化明胶和接枝nh s聚丙烯酸
‑
的复合冻干形成的三维多孔基质,并且能稳固地封堵湿润的创面;而实施例1~3还复合了聚赖氨酸和/或聚乙烯亚胺,得到的复合组织粘合剂的力学性能得到进一步加强。
[0132]
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1