瞬时受体电位MELASTATIN8(TRPM8)拮抗剂和相关方法
瞬时受体电位melastatin 8(trpm8)拮抗剂和相关方法
1.相关申请
2.本技术要求2019年2月1日提交的美国临时申请系列号 62/800,114、2019年2月1日提交的美国临时申请系列号62/800,143 和2019年12月13日提交的美国临时申请系列号62/947,742的优先权,每个所述临时申请的全部公开内容通过参考并入本文。
技术领域
3.本文公开的主题内容总的来说涉及瞬时受体电位melastatin 8 (trpm8)拮抗剂和相关方法。具体来说,本文公开的主题内容的某些实施方式涉及trpm8拮抗剂和使用这些拮抗剂治疗疼痛的方法。
背景技术:
4.通常被称为“冷感受器”的trpm8是一种躯体感觉神经系统的多觉型伤害感受器,并且是人类中冷伤害感受的主要传感蛋白。trpm8 表达在背根神经节(drg)和三叉神经节(tg)的初级感觉神经元(aδ和c
‑
纤维)以及某些其他非神经元组织中,尽管与其他温度敏感性trp 通道trpa1和trpv1相比有所不同。在初级感觉神经元中,trpm8 存在于外周和中枢神经末梢两者上,支持在躯体感觉和中枢神经系统中发挥作用。这种冷感应伤害感受器在被微凉温度(15
‑
25℃)、化学试剂例如(
‑
)
‑
薄荷醇((1r,2s,5r)
‑5‑
甲基
‑2‑
(1
‑
甲基乙基)
‑
环己醇)和“超级激动剂”icilin(3
‑
(2
‑
羟基苯基)
‑6‑
(3
‑
硝基苯基)
‑
3,4
‑
二氢嘧啶
‑
2(1h)
‑ꢀ
酮,也被称为ag 3
‑
5)和内源性脂质pip2激活后启动感觉神经冲动。 trpm8被薄荷醇的最大刺激通过四个薄荷醇分子的配体化学计量发生,每个薄荷醇分子占据一个功能性trpm8四聚体的单体。
5.trpm8似乎是多种治疗性干预的潜在靶点。已探索了将trpm8 激动剂用于良性前列腺增生和前列腺癌,而拮抗剂激起了更多兴趣,用于神经病理性疼痛中的冷超敏和偏头痛等。
6.已认识到许多专用trpm8拮抗剂,它们主要是通过内部化学文库的高通量筛选发现的。但是,关于这些拮抗剂如何与人类trpm8结合并随后影响其门控机制以及它们的潜在药效团的精确分子细节仍有待阐明,尤其是在最近通过冷冻电子显微术(cryo
‑
em)成功揭示了trpm8 和trp通道的结构生物学之后。
7.在trpm8介导的ca
2+
通量测定法中,公知的trpm8拮抗剂似乎表现出适度或可变的效力。例如,基于喹啉的pf
‑
05105679(pfizer,1 期,nct01393652)抑制电压和ws
‑
12介导的人类trpm8的激活效应,ic
50
值为103
±
29.4nm和181
±
7.21nm,而5,6,7,8
‑
四氢
‑
1,7
‑
萘啶类似物amg2850(amgen)对大鼠和人类trpm8的薄荷醇、icilin和冷的激活表现出7
‑
156nm范围内的ic
50
值。2
‑
苯甲氧基
‑
苯甲酸酰胺衍生物amtb(bayer)对人类trpm8的icilin介导的响应提供较弱抑制,pic
50
为6.23
±
0.02。然而,迄今为止,还没有trpm8拮抗剂被推进到临床应用;例如,pf
‑
05105679在实现未结合的血浆浓度高于其ic
50
值所需的高剂量(600mg和900mg)下不具有可测量的治疗指数。同样地,烟酸类似物amg 333的1期研究(amgen,
nct02132429)因未公开的原因而终止。对引入强效、合理特异的并因此在成功的临床前开发后维持成功通过临床试验的可能性的更多trpm8拮抗剂,仍存在着需求。
8.此外,具有广泛化学多样性的各种激动剂和拮抗剂支架已被用于解读trpm8在各种不同疾病状态例如口面部和神经病理性疼痛、膀胱过度活动症(oab)和膀胱疼痛综合征、涉及体温调节的疾病、口腔鳞状细胞癌、尼古丁成瘾行为和慢性阻塞性肺病中的作用。在某些情况下,使用这些配体作为工具分子来探测trpm8的药理学产生了冲突的数据,特别是在确定其在慢性神经病理性疼痛中的作用方面。需要基于同源配体(
‑
)
‑
薄荷醇的具有拮抗剂属性的高效化学探针从早期药物发现的角度重新审视trpm8领域,目前该领域缺乏这种化学型的小分子。
9.最近获得的脱辅基和激动剂结合的禽类trpm8两者的cryo
‑
em 结构(trpm8
fa
,pdb代码6bpq6nr2和6nr3和6nr3),与在小鼠、大鼠、松鼠和人类直向同源物中的支持性体外和体内诱变研究相结合,指出了原型配体薄荷醇和icilin的明确结合位点,其可能与冷感应解偶联。诱变研究表明位于电压感应蛋白样结构域 (vsld)的跨膜s1螺旋中部的保守的tyr745,对于薄荷醇结合(通过使用[3h]
‑
薄荷醇的放射性配体置换研究所确定的)以及效能两者来说是关键的。这些研究与复合有薄荷醇类似物ws
‑
12的禽类trpm8 的结构(pdb 6nr2)相一致。分离的s1
‑
s4感应结构域的构建也表明该区域对薄荷醇识别来说是关键的,正如通过微型热泳和nmr所确定的。其他薄荷醇敏感的残基包括tyr1005和leu1009,这两者是保守的,并位于trp螺旋跨膜结构域中,靠近胞质结构域界面。在结合有ws
‑
12 的结构中可以看到这两个残基的位置等同物(trpm8
fa
中的tyr1004 和leu1008)。这个口袋还用相似的残基结合icilin,包括tyr745和 leu1009以及s3螺旋中的gly805、asn799和asp802。结合有icilin 的禽类trpm8的cryo
‑
em结构加强了下述观点,即在所有trpm亚型中保守的残基tyr745是用于识别薄荷醇和icilin两者的共同trpm8 残基,尽管它们的化学型不同,而asn799和asp802以及gln782和 glu785对于ca
2+
依赖性icilin结合来说是必需的。其他的icilin结合残基排列在vsld和trp螺旋内的正性结合位点中,包括phe838、arg841、 his844和tyr1004(在htrpm8中分别为phe839、arg842、his845和 tyr1005)。该配体结合位点还与关键的电压敏感和冷敏感的残基重叠: s4螺旋中的保守arg841(htrpm8中的arg842),表明trpm8充当配体和电压刺激的多重感应蛋白的能力部分源自于这个由vsld内的 s1
‑
s4螺旋组成的共同位点。冬眠地松鼠和大鼠的转基因模型暗示负责冷和icilin激活的残基,分别散布在连接tm螺旋的环中的整个vsld 中,在第726(s1结构域前)、762(s1
‑
s2环)、819位(s3
‑
s4环) 处,以及连接孔螺旋(ph)和s6螺旋的环中的第927、946、947位处。从大鼠、松鼠和人类trpm8直向同源物的序列比对中,大鼠中的6个冷赋予残基中的4个残基在人类直向同源物中是保守的(tyr726、 ser762、ser819和asn947),这提高了在人类中配体和冷激活发生在拓扑学不同的区域处的可能性。另一方面,剩余的两个错配残基在人类和耐寒冬眠地松鼠中是保守的(ala927、his946),表明这些残基不支持冷表型,或者通过别构调节而有助于冷反应。
[0010]
因此,鉴于上述研究,在治疗疼痛中有用的另外的trpm8拮抗剂既是非常需要的,也是有益的。
技术实现要素:
[0011]
本公开的主题内容满足部分或所有上述需求,正如对于本领域普通技术人员来说在研究了本文件中提供的信息后会变得显而易见的。
[0012]
发明内容部分描述了本公开的主题内容的几个实施方式,并且在许多情况下列出了这些实施方式的变化和排列。发明内容部分仅仅是大量不同实施方式的示例。提及给定实施方式的一个或多个代表性特点同样是示例性的。此类实施方式通常可以在具有或不具有所提及的特点的情况下存在;同样地,这些特点可以适用于本公开的主体内容的其他实施方式,不论是否在发明内容部分中列出。为避免过多重复,发明内容部分未列出或提出此类特点的所有可能组合。
[0013]
在本公开的主题内容的某些实施方式中,提供了一种包含式(i)的 trpm8拮抗剂:
[0014][0015]
其中r1选自环烷基、双环烷基或三环烷基,所述环烷基、双环烷基或三环烷基各自具有5至12个碳原子、各自任选地被具有1至5个碳原子的烷基或具有4至12个碳原子的环烷基取代、并且各自任选为饱和或部分不饱和的。在某些实施方式中,r1是双环烷基,并且所述双环烷基是稠合、桥接或螺连的双环烷基。在某些实施方式中,r1是环烷基,例如在某些实施方式中是支链或取代的环烷基。
[0016]
在所述式(i)的化合物的某些实施方式中,r1选自选自选自及其类似物。
[0017]
在某些实施方式中,r1选自
及其类似物。
[0018]
在其他实施方式中,r1是选自下述的双环烷基或三环烷基:是选自下述的双环烷基或三环烷基:及其类似物。
[0019]
在某些实施方式中,r1是选自下述的环烷基:及其类似物。
[0020]
在某些实施方式中,r1是选自下述的螺连的双环烷基:是选自下述的螺连的双环烷基:及其类似物。
[0021]
在某些实施方式中,r1是选自下述的环烷基:是选自下述的环烷基:及其类似物。
[0022]
在某些实施方式中,r1是选自下述的双环烷基或三环烷基:及其类似物。
[0023]
在本公开的主题内容的某些实施方式中还提供了药物组合物。在某些实施方式中,提供了一种药物组合物,其包含本公开的主题内容的trpm8拮抗剂(例如式(i)的trpm8拮抗剂)和可药用介质、载体或赋形剂。
[0024]
在本公开的主题内容的某些实施方式中,还提供了治疗疼痛的方法。在某些实施方式中,提供了一种治疗疼痛的方法,所述方法包括向需要的对象给药有效量的包含上文中描述的式(i)的trpm8拮抗剂。在所述治疗方法的某些实施方式中,所述疼痛是神经病理性疼痛,例如在某些实施方式中是异常性疼痛、慢性神经病理性疼痛或化疗诱导的神经病理性疼痛。在某些实施方式中,给药所述trpm8拮抗剂可以包括静脉内、腹膜内、肌肉内或皮下注射所述trpm8拮抗剂。在某些实施方式中,所述对象是人类。
[0025]
在研究了本文件中的描述、附图和非限制性实施例后,本发明的其他特点和优点对于本领域普通技术人员来说会变得显而易见。
附图说明
[0026]
图1的图示出了已报道的trpm8拮抗剂,包括在ca
2+
通量测定法中确定的所述拮抗剂针对薄荷醇和/或icilin(icilin:3
‑
(2
‑
羟基苯基)
‑6‑
(3
‑
硝基苯基)
‑
3,4
‑
二氢嘧啶
‑
2(1h)
‑
酮)的效应的ic
50
值;
[0027]
图2a
‑
2d包括的示意图和图示出了在md模拟期间(
‑
)
‑
薄荷基化合物1和htrpm8的收敛参数,其包括:(图2a)示出了化合物1 在htrpm8中的对接位姿(md前)的示意图,其中(
‑
)
‑
薄荷基化合物 1被显示为洋红色棍,其中重要残基被显示为棍,其中示出了各个螺旋 (1(蓝色),s2(褪绿色),s4(黄绿色),trp螺旋(红色)),并且其中在cpk显示中示出了ca
2+
离子(绿色);(图2b)示出了在 100ns md后化合物1在htrpm8中的结合模式(md后)的示意图,其中(
‑
)
‑
薄荷基化合物1被显示为灰色棍;(图2c)示出了在md模拟期间化合物1和htrpm8的均方根差(rmsd)的图;以及(图2d) 示出了htrpm8中对化合物1的结合有贡献的关键残基的能量分解的图;并且其中htrpm8同源性模型使用trpm8
fa
的cryo
‑
em结构(pdb 6bpq)作为模板来构建;
[0028]
图3a
‑
3d包括的示意图和图示出了在md模拟期间amg2850和 htrpm8的收敛参数,其包括:(图3a)示出了amg2850在htrpm8 中的对接位姿(md前)的示意图,其中amg2850被显示为洋红色棍,其中重要残基被显示为棍,其中示出了各个螺旋(s2(褪绿色),s3 (绿色),s4(黄绿色),trp螺旋(红色)),并且其中在cpk显示中示出了ca
2+
离子(绿色);(图3b)示出了在100ns md后amg2850 在htrpm8中的结合模式(md后)的示意图,其中amg2850被显示为灰色棍;(图3c)示出了在md模拟期间amg2850和htrpm8的 rmsd的图;(图3d)示出了htrpm8中对amg2850的结合有贡献的关键残基的能量分解的图;并且其中htrpm8同源性模型使用 trpm8
fa
的cryo
‑
em结构(pdb 6bpq)作为模板来构建;
[0029]
图4是示出了amg2850和(
‑
)
‑
薄荷基化合物1的来自于它们的 md位姿(绿色和洋红色:trpm8和(
‑
)
‑
薄荷基化合物1的md位姿,蓝色和灰色:trpm8和amg2850的md位姿)的叠加
的示意图;
[0030]
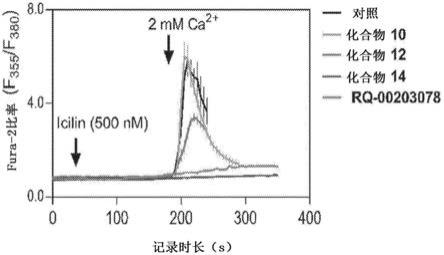
图5的图示出了使用稳定表达人类trpm8的hek
‑
293细胞的基于fura
‑
2的ca
2+
成像进行的测试化合物对icilin诱发的ca
2+
进入信号的任何影响的评估,其中将浸泡在无ca
2+
细胞外溶液中的装载有fura
‑
2 的细胞在含有或不含各种不同浓度(对于本图来说均为3nm,而相应的柱状图提供在图15中)的合成化合物或已知trpm8拮抗剂 rq
‑
00203078的情况下暴露于icilin(500nm),其中在添加化合物大约4min后,将无ca
2+
浸泡溶液用含有2mm ca
2+
的浸泡溶液代替,其中ca
2+
流入量作为fura
‑
2荧光比率(f
355
/f
380
)来监测,并且其中每个数据点代表平均值
±
sem(n≥35个细胞,来自于在不同的3天进行的3次独立实验);
[0031]
图6a
‑
6b包括的图像示出了化合物5(图6a)和化合物7(图6b) 在htrpm8中的结合模式,其中化合物5和7分别被显示为黄色和橙色棍,其中重要的残基被显示为棍,其中示出了各个螺旋(s1(蓝色), s2(褪绿色),s4(黄绿色)和trp螺旋(红色)),其中在cpk显示中示出了ca
2+
离子(绿色),并且其中htrpm8同源性模型使用 trpm8
fa
的冷冻电子显微术(cryo
‑
em)结构(pdb 6bpq)作为模板来构建;
[0032]
图7a
‑
7b包括的图示出了薄荷醇诱发的trpm8电流被化合物14 的抑制,其中电流通过用人类trpm8瞬时转染的hek
‑
293细胞的全细胞膜片钳电生理来测量,所述图包括:(图7a)示出了在暴露到500 μm饱和浓度的薄荷醇和不同浓度的化合物14后通过+80mv电压脉冲测量的平均电流迹线(n=4)的图;和(图7b)示出了在500μm薄荷醇存在下,在+80mv下,在1nm至1μm浓度下测量的化合物14 的剂量响应的图,其中电流响应被归一化到每个细胞在没有拮抗剂的情况下测量到的最大电流量,其中数据用单一结合位点希尔方程拟合,并且ic
50
经计算为64
±
2nm(n=6个细胞),并且其中误差条表示平均值的标准误差;
[0033]
图8a
‑
8d包括的示意图和图示出了在md模拟期间化合物14和 htrpm8的收敛参数,包括:(图8a)示出了化合物14在htrpm8 中的结合模式(md前)的图,其中化合物14被显示为洋红色棍,其中重要的残基被显示为棍,其中示出了各个螺旋(s1(蓝色),s2(褪绿色),s3(绿色),s4(黄绿色),trp螺旋(红色))并且其中在cpk显示中示出了ca
2+
离子(绿色);(图8b)示出了化合物14 在htrpm8中的结合模式(md后)的示意图;(图8c)示出了化合物14和htrpm8的rmsd的图;和(图8d)示出了htrpm8中对化合物14的结合有贡献的关键残基的能量分解的图,其中htrpm8同源性模型使用trpm8
fa
的cryo
‑
em结构(pdb 6bpq)作为模板来构建;
[0034]
图9包括的相关示意图示出了化合物14在trpm8、trpa1和 trpv1中的结合口袋和它们的结合模式,包括:(图(a))示出了化合物14在trpm8、trpa1和trpv1中的结合口袋的位置的示意图; (图(b))示出了化合物14在htrpa1(pdb 3j9p)中的结合模式的示意图;(图(c))示出了化合物14在htrpm8中的结合模式的示意图,其中htrpm8同源性模型使用trpm8
fa
的冷冻电子显微术 (cryo
‑
em)结构(pdb 6bpq)作为模板来构建;和(图(d))示出了化合物14在htrpv1(pdb 3j5r)中的结合模式的示意图;
[0035]
图10的图示出了在icr(cd1)小鼠中化合物14对icilin诱导的湿狗样抖动(wds)的影响,其中化合物或介质在icilin注射之前30 分钟给药,其中加巴喷丁(25mg/kg)在icilin注射之前1h给药,其中在icilin(10mg/kg)的i.p.注射后,在30min内计数wds的次数,并且其中数据作为平均值
±
sem(n=6)给出(双向anova和bonferroni 事后检验,**p<0.01);
[0036]
图11的图示出了在雄性c57
‑
小鼠中化合物14对奥沙利铂(oxp) 诱导的冷异常性
疼痛的影响,其中小鼠被隔日提供oxp(6mg/kg)或介质(盐水和5%甘露糖醇溶液,黑线(对照))的三次i.p.注射,其中在给药后第7天,通过丙酮试验评估冷异常性疼痛,其中示出了在没有化合物注射(绿线)或注射0.1μg(蓝线)或1.0μg(红线)化合物14的情况下冷异常性疼痛的时间过程,并且其中数据作为平均值
±
sem(n=6)给出(单向anova和dunnett’s事后检验,*p<0.05; ***p<0.001;****p<0.0001);
[0037]
图12是示出了白领姬鹟(禽类)、人类和大鼠trpm8的s1
‑
s4 螺旋(vsld)、s5
‑
s6螺旋(孔结构域)、孔螺旋(ph)和trp螺旋的序列比对的示意图,其中来自于trpm8
fa
(u3jd03,1103个残基)、 htrpm8(q7z2w7,1104个残基)和rtrpm8(q8r455,1104个残基)的全序列的vsld结构域(s1
‑
s4)、孔结构域(s5
‑
s6和孔螺旋 ph)和trp螺旋从uniprotkb/swiss
‑
prot检索,并使用clustal omega 程序将所述三个结构域比对,其中相似的氨基酸被突出显示,其中显示出trpm8
fa
在上述区域中与人类和大鼠trpm8高度同源(分别具有86%和87%序列同一性),并且其中星号表示对薄荷醇(绿色)、icilin (黄色)、电压(金色)和ca
2+
(洋红色)敏感的残基;
[0038]
图13的图示出了在稳定表达htrpm8的hek293细胞中icilin的浓度响应曲线,其中响应通过在所指示的icilin浓度下指示细胞内游离 ca
2+
浓度的最大变化的峰值荧光(fura
‑
2)比率来报告,并且其中每个数据点将峰值荧光比率表示为平均值
±
sem(n≥30个细胞,来自于在不同的3天进行的3次独立实验);
[0039]
图14的图示出了在hek
‑
293
‑
htrpm8细胞中(
‑
)薄荷醇诱发的 ca
2+
进入的浓度响应曲线,其中每个数据点表示在同源浓度下的平均响应,被表示成在基于fura
‑
2的ca
2+
成像测定法中最大ca
2+
进入的百分比,其中误差条表示sem(n≥35个细胞,来自于在不同的3天进行的3次独立实验)并且其中线表示使用prism 7(graphpad inc.)完成的四参数逻辑曲线拟合;
[0040]
图15包括的图示出了在稳定表达人类trpm8的hek
‑
293细胞中化合物对icilin诱发的ca
2+
进入的影响的评估,其中每个条表示峰值 fura
‑
2比率,其被归一化到icilin(500nm)响应的峰值比率,并被表示为平均值
±
sem(n≥35个细胞,来自于在不同的3天进行的3次独立实验),并且其中使用单向anova然后使用dunnett's检验来比较测试化合物相对于对照(icilin)的功效(*p<0.001);
[0041]
图16的图示出了rq
‑
00203078的浓度响应曲线,其中所述响应通过归一化到由单独的500nm icilin引发的峰值响应的峰值荧光(fura
‑
2) 比率来报告,并且其中每个数据点表示平均值
±
sem(n≥30个细胞,来自于在不同的3天进行的3次独立实验);
[0042]
图17的图示出了化合物14的浓度响应曲线,其中所述响应通过归一化到由单独的500nm icilin引发的峰值响应的峰值荧光(fura
‑
2) 比率来报告,并且其中每个数据点表示平均值
±
sem(n≥30个细胞,来自于在不同的3天进行的3次独立实验);
[0043]
图18a的图示出了呈现了使用hek
‑
293
‑
htrm8细胞的基于 fura
‑
2的ca
2+
成像获得的化合物14(3nm)对(
‑
)
‑
薄荷醇(100μm) 诱发的ca
2+
进入信号的影响的典型迹线,其中每个数据点表示平均值
±
sem(n≥35个细胞,来自于在不同的3天进行的3次独立实验);
[0044]
图18b的图示出了在hek
‑
293
‑
htrpm8中3nm化合物14对(
‑
) 薄荷醇诱发的ca
2+
进入的影响的评估,其中每个条表示峰值fura
‑
2比率,其被归一化到薄荷醇(100μm)响应的峰值比率并被表示为平均值
±
sem(n≥35个细胞,来自于在不同的3天进行的3次独立实验),并
且其中两个组之间的平均响应使用双尾未配对学生t
‑
检验来比较;
[0045]
图19的图示出了所选的联苯基酰胺类似物的固有htrpm8活性,其中使用含有ca
2+
(2mm)的细胞外溶液进行基于fura
‑
2的比率测量 ca
2+
成像,并且其中每个数据点表示平均值
±
sem(n≥20个细胞,来自于在不同的3天进行的3次独立实验);
[0046]
图20的图示出了htrpa1m的aitc活化的激动剂剂量响应,其中ec
50
=7.62
±
0.89μm,并且其中每个数据点表示平均值
±
sem,n= 5或10个独立实验;
[0047]
图21的图示出了aitc活化的(10μm)htrpa1响应的钌红阻断,其中ic
50
=162
±
33nm,并且其中每个数据点表示平均值
±
sem, n=5个独立实验;
[0048]
图22的图示出了htrpv1的辣椒素活化的激动剂剂量响应,其中ec
50
=19
±
2.5nm,并且其中每个数据点表示平均值
±
sem,n=5或 10个独立实验;以及
[0049]
图23的图示出了辣椒素活化的(100nm)htrpv1响应的辣椒平阻断,其中ic
50
=451
±
48nm,并且其中每个数据点表示平均值
±
sem, n=5个独立实验。
具体实施方式
[0050]
本文中阐述了本公开的主题内容的一个或多个实施方式的详细情况。对于本领域普通技术人员来说,在研究了本文中提供的信息后,本文中描述的实施方式的修改和其他实施方式会是显而易见的。本文中提供的信息、特别是所描述的示例性实施方式的具体细节,主要是为了清晰地理解而提供,并且不应从中理解到不必要的限制。在有冲突的情况下,以本文的说明书包括定义为准。
[0051]
尽管相信本文中使用的术语被本领域普通技术人员充分理解,但仍阐述了某些定义以便于解释本公开的主题内容。
[0052]
除非另有定义,否则本文中使用的所有技术和科学术语均具有与本发明所属领域的专业技术人员通常理解的相同的含义。
[0053]
在整个本公开中提到的所有专利、专利申请、出版的申请和出版物、genbank序列、uniprot或swiss
‑
prot数据库、网站和其他出版的材料,除非另有指明,否则均整体通过参考并入本文。
[0054]
在提及url或其他此类标识符或地址的情况下,应该理解此类标识符可以改变,并且互联网上的特定信息可以变化,但通过搜索互联网可以发现等效的信息。对这些信息的引用证明了此类信息的可用性和公开传播。
[0055]
当在本文中使用时,任何保护基团、氨基酸和其他化合物的缩写,除非另有指明,否则均符合它们的常见用法、公认的缩略语或 iupac
‑
iub生物化学命名委员会(参见biochem.(1972) 11(9):1726
‑
1732)。
[0056]
尽管与本文中描述的相似或等同的任何方法、装置和材料均可用于本公开主题内容的实践或测试,但在本文中描述了代表性方法、装置和材料。
[0057]
本技术可以“包含(开放性)”本公开主题内容的组分以及本文中描述的其他成分或要素,“由它们组成(封闭性)”或“基本上由它们组成”。当在本文中使用时,“包含”是开放性的,并意味着所叙述的要素或它们的结构或功能等同物再加上未叙述的任何其他一个或多个要素。术语“具有”和“包括”也应被解释为开放性的,除非上下文另有说明。
[0058]
遵循长期存在的专利法惯例,当在本技术包括权利要求书中使用时,没有具体数
目的指称是指“一个或多个”。因此,例如,对“细胞”的指称包括多个此类细胞等。
[0059]
除非另有指明,否则在本说明书和权利要求书中使用的表示成分的量、性质例如反应条件等的所有数字,均应被理解为在所有情况下被术语“约”修饰。因此,除非另有说明,否则本说明书和权利要求书中阐述的数值参数均为近似值,其可以根据试图通过本公开的主题内容获得的所需性质而变。
[0060]
当在本文中使用时,术语“约”在指称值或质量、重量、时间、体积、浓度或百分率的量时,意味着涵盖了与指定的量相比在某些实施方式中
±
20%、在某些实施方式中
±
10%、在某些实施方式中
±
5%、在某些实施方式中
±
1%、在某些实施方式中
±
0.5%、在某些实施方式中
±
0.1%的变化,因为这种变化适合于执行所公开的方法。
[0061]
当在本文中使用时,范围可以被表述为从“约”一个特定值和/或到“约”另一个特定值。还应该理解,存在多个本文中公开的值,并且每个值在本文中除了所述值本身之外也被公开为“约”该特定值。例如,如果公开了值“10”,则“约10”也被公开。还应该理解,两个特定单元之间的每个单元也被公开。例如,如果公开了10和15,则 11、12、13和14也被公开。
[0062]
当在本文中使用时,“任选的”或“任选地”意味着随后描述的事件或情景将会发生或不会发生,并且所述描述包括了所述事件或情景发生的情况和不发生的情况。例如,任选的变体部分意味着所述部分是变体或非变体。
[0063]
本公开的主题内容至少部分是基于小分子trpm8拮抗剂的开发,所述拮抗剂具有结构相似性和构象刚性,并被用于通过它们的来自于在基于禽类trpm8
fa
的cryo
‑
em结构(pdb 6bpq,)的人类 trpm8同源性模型中的分子动力学(md)模拟的位姿,来揭示用于配体识别的相似分子决定簇。这些见解允许设计用于trpm8介导的感觉神经病变的新型trpm8化学探针和治疗化合物,它们在某些实施方式中被鉴定为与目前已知的trpm8拮抗剂例如2
‑
苯甲氧基
‑
苯甲酸酰胺衍生物amtb以及具有双功能trpm8拮抗剂活性的trpv1拮抗剂例如吡啶基哌嗪甲酰胺bctc和脲sb
‑
452533相比具有更高的效能(图 1)。
[0064]
在临床前模型中,已认识到在c57/bl6小鼠中基于色氨酸的 trpm8拮抗剂逆转奥沙利铂诱导的冷异常性疼痛。就此而言,已发现目前公开的、化学上新颖的、具有纳摩尔浓度高效价和适度的trpm8 选择性的基于联苯基酰胺的trpm8拮抗剂,在具有化疗(奥沙利铂) 诱导的慢性神经病理性疼痛(其也被称为化疗诱导的外周神经病变或 cipn)的c57/bl6小鼠中逆转冷异常性疼痛。此外,本文公开的trpm8 拮抗剂可用于其他疼痛状态,例如与慢性神经病理性疼痛相关的冷异常性疼痛和机械异常性疼痛。现有的trpm8拮抗剂dfl23448和 dfl23693在神经病理性疼痛的慢性压迫性损伤(cci)诱导的冷异常性疼痛和机械异常性疼痛模型中显著减弱伤害感受性反应。同样地,现有的trpm8拮抗剂pbmc在临床前模型中降低cci诱导的冷异常性疼痛。与这些观察相一致,trpm8
─
/
─
小鼠在坐骨神经的cci后,不显示出冷诱导的敏感性(冷异常性疼痛)的提高;类似地,使用trpm8 反义寡核苷酸(鞘内给药)下调与cci诱导的神经损伤同侧的l5背根神经节(drg)中的trpm8,导致冷痛觉过敏减弱。不希望受到任何特定理论或机制限制,因此相信本文中描述的trpm8拮抗剂也可缓解慢性神经病理性疼痛状态中的温度异常性疼痛和机械异常性疼痛,具有为慢性疼痛的治疗提供新的非阿片类疗法的潜力,从而为阿片类成瘾提供新的治疗。在本发明的某些实施方式中,trpm8代表了本文中描述的trpm8拮抗剂的靶点,所述trpm8拮抗剂用于在外周和/或 cns水平上控制对疼痛刺激的感觉反应的新型疼痛药物疗法。在某些实施方式中,本
文描述的trpm8拮抗剂还可以在其他疾病中发现效用,例如炎性疼痛中的冷过敏、口面部疼痛、膀胱过度活动症和膀胱疼痛综合征、涉及体温调节的疾病包括在其中诱导低温或降低体温是有益的疾病(例如在心脏骤停、新生儿脑病、中风等期间)、偏头痛、前列腺癌、口腔鳞细胞癌、尼古状丁成瘾行为等。
[0065]
因此,本公开的主题内容包括trpm8拮抗剂和相关方法。具体来说,本公开的主题内容的某些实施方式涉及trpm8拮抗剂和使用这些拮抗剂治疗疼痛的方法。
[0066]
在本公开的主题内容的某些实施方式中,提供了一种具有下式(i) 的trpm8拮抗剂:
[0067][0068]
其中r1选自环烷基、双环烷基或三环烷基,所述环烷基、双环烷基或三环烷基各自具有4至12个碳原子、各自任选地被具有1至6个碳原子的烷基或具有4至12个碳原子的环烷基取代、并且各自任选为饱和或部分不饱和的。正如下文所示,在本文中用于指示各种不同的r1基团的附连点。
[0069]
术语“环烷基”在本文中通常用于指称约3至约12个碳原子,例如3、4、5、6、7、8、9、10、11或12个碳原子的非芳香族单环环系统,尽管在某些实施方式中此类环烷基还包括芳香环。代表性的单环环烷基环包括但不限于环丙基、环丁基、环戊基、环己基、环庚基等。
[0070]
在某些实施方式中,此类环烷基还可以合并以产生多环环系统,例如在某些实施方式中包括两个环系统的“双环烷基”基团或在其他实施方式中包括三个环系统的“三环烷基”基团。在某些实施方式中,此类双环烷基可以是稠合的双环烷基,其中所述两个环彼此直接相连并共用两个相邻原子。在其他实施方式中,所述双环烷基是桥接的双环烷基,其中所述两个环共用三个或更多个原子,其中两个桥头原子被所述两个环共用并被含有至少一个原子的桥隔开。在其他实施方式中,所述双环烷基是螺连的双环烷基,其中所述两个环通过单个原子相连。
[0071]
在某些实施方式中,本文中描述的环烷基也可以任选为饱和或部分不饱和的。所述环烷基也可以任选地被本文中所定义的烷基或另一个环烷基取代。在某些实施方式中,所述环烷基是支链环烷基,其中所述环烷基附连到另一个化学组成部分例如烷基。
[0072]
对于本文中描述的并且可用于任选地取代本公开主题内容的环烷基、双环烷基或三环烷基的烷基而言,术语“烷基”在本文中用于指称c1
‑
20(含)、线性(即“直链”)、支链、饱和或至少部分不饱和并且在某些情况下完全不饱和的(即烯基和炔基)烃链,包括例如甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基、戊基、己基、辛基、乙烯基、丙烯基、丁烯基、戊烯基、己烯基、辛烯基、丁二烯基、丙炔基、甲基丙炔基、丁炔基、戊炔基、己炔基、庚炔基和丙二烯基。当在本文中用于指称烷基时,“支链”是指其中通常将短链烷基例如甲基、乙基或丙基附连到直链烷基链的烷基。“短链烷基”是指具有1 至约8个碳原子(即c1
‑
8烷基),例如1、2、3、4、5、6、7或8个碳原子的烷基。另一方面,“长链烷基”是指具有约10至约20个碳原子,例
如10、11、12、13、14、15、16、17、18、19或20个碳原子的烷基。在某些实施方式中,“烷基”具体来说是指c1
‑
8直链烷基。在其他实施方式中,“烷基”具体来说是指c1
‑
8支链烷基。
[0073]
在本公开的主题内容的某些实施方式中,提供了上述式(i)的化合物,其中r1选自:
[0074][0075][0075]
及其类似物。
[0076]
在某些实施方式中,r1是选自下述的双环烷基或三环烷基:
[0077][0077]
及其类似物。
[0078]
在其他实施方式中,r1是选自下述的环烷基:
[0079]
及其类似物。
[0080]
在其他实施方式中,r1是选自下述的螺连的双环烷基:
[0081]
及其类似物。
[0082]
在某些实施方式中,r1是选自下述的环烷基:
[0083]
及其类似物。
[0084]
在某些实施方式中,r1是选自下述的双环烷基或三环烷基:
[0085]
及其类似物。
[0086]
在本公开的主题内容的式(i)的其他实施方式中,r1选自:
[0087][0088]
例如,在某些实施方式中,提供了具有下式(ii)的trpm8拮抗剂,其在本文中也被称为化合物1:
[0089][0090]
作为另一个实例,在某些实施方式中,提供了具有下式(iii)的 trpm8拮抗剂,其在本文中也被称为化合物2:
[0091][0092]
作为另一个实例,在某些实施方式中,提供了具有下式(iv)的 trpm8拮抗剂,其在本文中也被称为化合物3:
[0093][0094]
作为另一个实例,在某些实施方式中,提供了具有下式(v)的trpm8拮抗剂,其在本文中也被称为化合物4:
[0095][0096]
作为另一个实例,在某些实施方式中,提供了具有下式(vi)的 trpm8拮抗剂,其在本文中也被称为化合物5:
[0097][0098]
作为另一个实例,在某些实施方式中,提供了具有下式(vii)的trpm8拮抗剂,其在本文中也被称为化合物6:
[0099][0100]
作为另一个实例,在某些实施方式中,提供了具有下式(viii)的 trpm8拮抗剂,其在本文中也被称为化合物7:
[0101][0102]
作为另一个实例,在某些实施方式中,提供了具有下式(ix)的 trpm8拮抗剂,其在本文中也被称为化合物8:
[0103][0104]
作为另一个实例,在某些实施方式中,提供了具有下式(x)的 trpm8拮抗剂,其在本文中也被称为化合物9:
[0105][0106]
作为另一个实例,在某些实施方式中,提供了具有下式(xi)的 trpm8拮抗剂,其在本文中也被称为化合物10或12:
[0107][0108]
在某些实施方式中,上述具有下式(xi)的trpm8拮抗剂可以以多种异构体形式提供,包括但不限于:
[0109][0110]
作为另一个实例,在某些实施方式中,提供了具有下式(xii)的 trpm8拮抗剂,其在本文中也被称为化合物11:
[0111][0112]
作为另一个实例,在某些实施方式中,提供了具有下式(xiii)的 trpm8拮抗剂,其在本文中也被称为化合物15:
[0113][0114]
作为另一个实例,在某些实施方式中,提供了具有下式(xiv)的 trpm8拮抗剂,其
在本文中也被称为化合物13:
[0115][0116]
作为另一个实例,在某些实施方式中,提供了具有下式(xv)的trpm8拮抗剂,其在本文中也被称为化合物14:
[0117][0118]
在本公开的主题内容的某些实施方式中,还提供了包含本文中描述的trpm8拮抗剂和可药用介质、载体或赋形剂的药物组合物。事实上,当提及本文中的某些实施方式时,术语“trpm8拮抗剂”和/或“化合物”可以用于也可以不用于指称包含所述trpm8拮抗剂的药物组合物。
[0119]
当在本文中使用时,术语“可药用载体”是指无菌水性或非水性溶液、分散系、悬液或乳液以及用于在即将使用前重构成无菌可注射溶液或分散系的无菌粉剂。适合的流动性可以例如通过使用包衣材料例如卵磷脂、在分散系的情况下通过维持所需的粒度以及通过使用表面活性剂来维持。这些组合物也可以含有佐剂,例如防腐剂、润湿剂、乳化剂和分散剂。通过包含各种不同的抗细菌剂和抗真菌剂例如对羟基苯甲酸酯、氯丁醇、苯酚、山梨酸等,可以确保阻止微生物的作用。可能还需要包含等渗剂例如糖类、氯化钠等。
[0120]
可注射药物形式的延长吸收可以通过包含延迟吸收的试剂例如单硬脂酸铝和明胶来实现。可注射储库形式通过在可生物降解聚合物例如聚丙交酯
‑
聚乙交酯、聚原酸酯和聚酸酐中形成药物的微囊基质来制造。取决于化合物与可生物降解聚合物的比例以及所采用的特定可生物降解聚合物的性质,可以控制化合物的释放速率。储库型可注射制剂也可以通过将化合物包裹在与身体组织相容的脂质体或微乳液中来制备。所述可注射制剂可被灭菌,例如通过细菌截留滤器过滤或通过并入采取无菌固体组合物形式的灭菌剂,所述灭菌剂可在即将使用前溶解或分散在无菌水或其他无菌可注射介质中。适合的惰性载体可包括糖类例如乳糖。
[0121]
适合的制剂还可包括水性和非水性无菌注射溶液,其可以含有抗氧化剂、缓冲剂、抑菌剂、杀菌抗生素和使制剂与目标受体的体液等渗的溶质,以及水性和非水性无菌悬液,
其可以包含悬浮剂和增稠剂。
[0122]
所述组合物还可以采取例如在油性或水性介质中的悬液、溶液或乳液的形式,并且可以含有配制剂例如悬浮剂、稳定剂和/或分散剂。可选地,所述化合物可以采取粉末形式,用于在使用前用适合的介质例如无菌无热原水配制。
[0123]
所述制剂可以存在于单位剂量或多剂量容器例如密封的安瓿和小瓶中,并且可以在冷冻或冷冻干燥(冻干)条件下储存,只需在即将使用前添加无菌液体载体。
[0124]
对于口服给药来说,所述组合物可以采取例如通过常规技术使用可药用赋形剂制备的片剂或胶囊的形式,所述赋形剂例如粘合剂(如预明胶化玉米淀粉、聚乙烯吡咯烷酮或羟丙基甲基纤维素)、填充剂 (如乳糖、微晶纤维素或磷酸氢钙)、润滑剂(如硬脂酸镁、滑石或二氧化硅)、崩解剂(如马铃薯淀粉或羟基乙酸淀粉钠)或润湿剂(如十二烷基硫酸钠)。所述片剂可以通过本领域已知的方法进行包衣。
[0125]
用于口服给药的液体制剂可以采取例如溶液、糖浆或悬液的形式,或者它们可以作为干燥产品存在,在使用前用水或其他适合的介质重构。此类液体制剂可以通过常规技术使用可药用添加剂来制备,所述添加剂例如悬浮剂(如山梨糖醇糖浆、纤维素衍生物或氢化食用脂肪)、乳化剂(如卵磷脂或阿拉伯胶)、非水性介质(如杏仁油、油性酯、乙醇或分馏植物油)和防腐剂(如对羟基苯甲酸甲酯或丙酯或山梨酸)。所述制剂也可视情况而定含有缓冲盐、调味剂、着色剂和甜味剂。可以适合地配制用于口服给药的制剂以提供活性化合物的受控释放。对于颊给药来说,所述组合物可以采取用以常规方式配制的片剂或含片的形式。
[0126]
所述组合物也可以配制成用于植入或注射的制剂。因此,例如,所述化合物可以用适合的聚合物或疏水材料(例如作为在可接受的油中的乳液)或离子交换树脂配制,或作为微溶衍生物(例如作为微溶盐)配制。所述化合物还可以配制成直肠组合物、霜剂或洗剂或透皮贴片。
[0127]
在本公开的主题内容的某些实施方式中,还提供了利用本文中描述的trpm8拮抗剂治疗疼痛的方法。当在本文中使用时,术语“治疗”涉及感兴趣的病症(例如疼痛)的任何治疗,包括但不限于预防性治疗和治疗性治疗。因此,术语“治疗”包括但不限于:减少感兴趣的病症的发生或感兴趣的病症的发展;抑制感兴趣的病症的进展;停止或减少感兴趣的病症的进一步发展;降低感兴趣的病症的严重程度;改善或缓解与感兴趣的病症相关的症状;以及引起感兴趣的病症或与感兴趣的病症相关的一种或多种症状的消退。
[0128]
术语“疼痛”在本文中用于一般性描述由疾病或损伤引起的身体痛苦或不适,并且通常由感觉神经元传送到对象的大脑以发出身体的实际或潜在损伤的信号。此类疼痛可能由包括损伤和疾病在内的多种情况引起,但也可能由心理病症例如抑郁症引起,或者不存在可识别的触发因素。疼痛包括急性疼痛和慢性疼痛。急性疼痛通常由组织损伤例如皮肤烧伤、骨折、头痛和肌肉痉挛引起,并且通常随着损伤愈合或疼痛原因(刺激物)的消除而消失。另一方面,慢性疼痛持续或进展很长一段时间内,并且通常对药物治疗具有抵抗力。此类慢性疼痛可能由许多不同的医学病症引起,包括但不限于糖尿病、关节炎、偏头痛、纤维肌痛、癌症、带状疱疹、坐骨神经痛和以前的外伤或损伤,并且可能因环境和/或心理因素而恶化。其他类型的慢性疼痛包括异常性疼痛、痛觉过敏和幻肢痛,以及由于神经系统的至少一些损伤造成或加重的其他类型的长期持续性疼痛(即神经病理性疼痛)。在本文描述的方
gilman's the pharmacological basis of therapeutics),第9版, mcgraw
‑
hill health professions division,new york;ebadi,(1998) 《crc临床药理学桌面参考》(crc desk reference of clinical pharmacology),crc press,boca raton,florida;katzung,(2001)《基础和临床药理学》(basic&clinical pharmacology),第8版,lange medical books/mcgraw
‑
hill medical pub.division,new york; remington等,(1975)《remington制药学》(remington's pharmaceutical sciences),第15版,mack pub.co.,easton,pennsylvania;和speight 等,(1997)《avery的药物治疗:疾病管理中药物的性质、选择、治疗用途和经济价值指南》(avery's drug treatment:a guide to the properties,choice,therapeutic use and economic value of drugs in disease management),第4版,adis international,auckland/philadelphia; duch等,(1998)toxicol.lett.100
‑
101:255
‑
263。
[0134]
当在本文中使用时,术语“对象”包括人类和动物对象两者。因此,根据本文公开的主题内容提供了兽医治疗性用途。因此,本公开的主题内容提供了对哺乳动物的治疗,所述哺乳动物例如人类,以及因濒危而重要的哺乳动物例如东北虎,具有经济重要性的哺乳动物例如在农场饲养以供人类食用的动物;和/或对人类具有社会重要性的动物例如作为宠物或在动物园中饲养的动物。此类动物的实例包括但不限于:食肉动物,例如猫和狗;猪科动物,包括猪、阉猪和野猪;反刍动物和/或有蹄类动物,例如牛、公牛、绵羊、长颈鹿、鹿、山羊、野牛和骆驼;以及马。还提供了对鸟类的治疗,包括对那些濒临灭绝和/或饲养在动物园中的鸟类以及禽类,更特别是驯养禽类即家禽,例如火鸡、鸡、鸭、鹅、珍珠鸡等,因为它们对人类也具有经济重要性。因此,还提供了对牲畜的治疗,包括但不限于驯养的猪、反刍动物、有蹄类动物、马(包括赛马)、家禽等。
[0135]
本公开的主题内容通过下述特定但非限制性实施例进一步说明。
[0136]
实施例
[0137]
材料和方法
[0138]
分子建模
[0139]
htrpm8的同源性建模。在白领姬鹟(ficedula albicollis)的 cryo
‑
em结构(trpm8
fa
,pdb:6bpq,分辨率:)的基础上建立人类trpm8模型,其中htrpm8与trpm8
fa
享有83%的序列同一性。所述cryo
‑
em结构从蛋白质数据库(protein data bank)下载。使用sybyl
‑
x 1.3修复所有残基并最小化能量。htrpm8的全序列(q7z2w7,1104个残基)从uniprotkb/swiss
‑
prot检索。序列比对和同源性建模使用以前报道的方案。
[0140]
使用modeller 9.18构建htrpm8模型。在产生所述3d模型后,使用sybyl
‑
x 1.3进行能量最小化。简单来说,在sybyl中定义的参数如下:梯度被设定到0.5kcal/mol,最大迭代次数被设定到5000,力场被设定到mmff94s,并且电荷被设定到mmff94。所有这些设置均与以前描述的相同。然后使用prosa
‑
web z
‑
评分和procheck拉马钱德兰图来检查所述3d模型的总体质量。
[0141]
将配体分子对接到htrpm8中。使用在sybyl
‑
x 1.3中执行的对接程序surflex
‑
dock geomx(sfxc)建立trpm8
‑
配体复合物,其中总评分用
‑
log
10
(k
d
)表示。然后使用sybyl
‑
x 1.3中的molcad模块探索htrpm8的潜在结合口袋,其包括残基phe738(s1)、tyr745(s1)、 glu782(s2)、glu785(s2)、trp798(s3)、asn799(s3)、asp802 (s3)、ala805(s3)、arg842
(s4)、his845(s4)、ile846(s4)、 val849(s4)、glu1004(trp螺旋)、tyr1005(trp螺旋)、arg1008 (trp螺旋)和leu1009(trp螺旋)。分子对接的所有参数和方案可以在以前的报道中找到。
[0142]
分子动力学(md)模拟。为了加速md模拟,选择htrpm8的跨膜结构域(从gln671至asn1010的残基)来进行trpm8与不同配体的模拟。trpm8受体的每个单体与一个配体复合,使得每个模拟存在4个(相同的)配体。然后将所述系统在0.15mol/l nacl溶液中溶剂化,包括514个1
‑
棕榈酰基
‑2‑
油酰基
‑
sn
‑
甘油
‑3‑
磷酸胆碱(popc) 脂质、51470个水分子以及156个cl
‑
离子和140个na
+
离子。从分子对接研究获取trpm8和配体的初始构象。初始模拟盒的尺寸被设定到将amber ff14sb力场施加到trpm8并将 amber lipid14力场施加到脂质。水分子用tip3p水模型处理。
[0143]
然后使用amber16软件包中的pmemd.mpi和pmemd.cuda模块进行所有md模拟。为了避免可能的空间冲突,对每个系统执行了几个最小化步骤。然后,将每个系统在加热阶段中从0k逐渐加热到 300k,然后是时间步长为2fs的平衡和生产阶段(300k)。使用周期性边界条件维持恒定的温度和压力(npt)系综。将压力设定到1atm,并通过各向异性(x
‑
,y
‑
,z
‑
)压力缩放方案控制,压力弛豫时间为1ps。温度受朗之万动力学约束,碰撞频率为2ps
‑1。长程静电学通过粒子网格ewald(pme)方法处理,实空间相互作用的截止值被设定到所有涉及氢原子的共价键都受shake算法约束。每个系统进行100nsmd模拟,并且每100ps保存每个模拟系统的轨迹。
[0144]
分子力学/广义波恩表面积(mm/gbsa)计算。对于每个md模拟的保存的轨迹来说,使用mm/gbsa方法计算trpm8在不同配体处理下的结合能。为了计算平均结合能,使用下述公式从90至100ns中每 200ps的每个轨迹提取50个快照:
[0145]
△
e
结合
=
△
e
mm
+
△
e
sol
=
△
e
mm
+
△
e
gb
+
△
e
sa
[0146]
其中
△
e
结合
是结合能,
△
e
mm
表示真空中分子机械能的总和,并且可以进一步分为静电、范德华和内部能的贡献。该项可以通过分子力学方法计算。
△
e
sol
是溶剂化能,其包括使用广义玻恩(gb)近似模型计算的极性溶剂化能(
△
e
gb
)和通过用成对重叠的线性组合 (lcpo)模型拟合溶剂可及表面积(sasa)而得到的非极性部分(
△ꢀ
e
sa
)。此外,将每个残基的能量分解到骨架和侧链原子中。通过能量分解,可以分析关键残基对生物学活性的贡献。
[0147]
化学方法.薄层层析在analtech硅胶gf 250微米tlc板上进行。所述板用254nm uv光可视化并用碘染色。快速层析在f60硅胶 230
‑
400目,400目,上进行。自动快速层析在具有多可变波长(200
‑
400nm)检测器(iso
‑
psv型)的biotage isoleraprime主动快速纯化系统上进行,使用装有biotage hp
‑
sphere
tm
25微米球形硅胶的biotage snap ultra柱套(10g或25g),并使用溶剂a (二氯甲烷)/溶剂b(二乙醚)的二元梯度(对于化合物2来说: 99/1
→
94/6,对于化合物4来说:100/0
→
96:4,对于化合物5、6、9、 10、12、14、15来说:100/0
→
98/2,对于化合物7来说:96/4
→
94/6;对于化合物13来说:100/0
→
94/6),流速为12或25ml/min。在254 和280nm处监测洗脱峰。nmr在bruker ascent 400mhz nmr上使用 cdcl3来记录。质谱在agilent 1290infinity和6490triple quad lc/ms 上使用电喷雾电离(esi)模式获得。化合物2及其异构体(2a、2b、 2c)以及化合物10和12的lc
‑
uv
‑
ms使用accela uhplc系统(thermoscientific,san jose,ca,usa)进行,所述系
统由accela 1250泵、开放式自动进样器和pda检测器组成,然后连接到thermo q exactiveorbitrap质谱仪。色谱分离在agilent eclipse xdb c18柱(1.8μm粒子,尺寸为2.1mm
×
100mm,带有2.1mm
×
5mm保护柱)上进行,使用由a:lc
‑
ms级水中的0.1%甲酸(v/v)和b:乙腈中的0.1%甲酸(v/v) 组成的流动相和两种不同的洗脱方法。梯度洗脱方法用于化合物2及其异构体(2a、2b、2c),其包括在8分钟内从0%b到95%b,然后是柱清洁和平衡时间,总共20分钟。等度洗脱方法用于化合物10 和12,其是58%b保持恒定20分钟。对于两种色谱方法来说,流速为300μl/min,并且进样5μl样品。uv检测使用跨越200至600nm 范围的pda检测器来实现,并监测特定通道波长(280nm、254nm和 214nm)。质谱仪参数包括采取正离子模式的电喷雾电离,在3.7kv 电喷雾电压下以全ms模式扫描,分辨率设置为70,000,agc靶为1e6,最大it为100ms,扫描范围为m/z 150
‑
1000。数据处理使用thermoxcalibur 4.1.31.9版中的qual browser进行。元素分析由atlanticmicrolabs,norcross,ga进行。所有最终化合物的纯度高于99.6%。
[0148]
通用酰胺化程序。向[1,1
′‑
联苯基]
‑4‑
甲酸(1.00
‑
1.5当量)在thf (0.1m)中的搅拌的溶液添加edci(1.04
‑
1.56当量)、hobt(1.04
‑
1.56 当量)和et3n(1.2
‑
3.3当量),并将所述反应在室温搅拌1h。向该混合物添加取代的胺(1.0
‑
1.2当量)在thf中的溶液,并将所述反应在40℃搅拌2
‑
3hr或在室温搅拌1
‑
3天。将所述反应用etoac和h2o 稀释。将合并的有机层用饱和nacl(水溶液)洗涤,在na2so4上干燥,过滤并浓缩。
[0149]
n
‑
(2
‑
异丙基
‑5‑
甲基环己基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物2,通过lcms发现以30:21:49的比例存在的三种异构体的混合物)。按照通用程序,使用5
‑
甲基
‑2‑
(丙
‑2‑
基)环己
‑1‑
胺(62mg,0.40mmol)制备。将粗品残留物使用己烷/二乙醚/nh4oh(100/0/0
→
95/5/0.5)通过快速层析进行纯化,然后进行自动快速层析,以62%的得率得到83mg 标题材料。1h nmr(混合物)(400mhz,cdcl3)δ7.87
–
7.78(m,6h), 7.69
–
7.63(m,7h),7.63
–
7.58(m,6h),7.51
–
7.35(m,8h),6.22(d,j= 9.0hz,2h),6.16(d,j=8.4hz,1h),5.82(d,j=9.5hz,1h),4.63
–
4.55 (m,2h),4.39(tt,j=7.8,3.9hz,1h),4.03(qd,j=10.9,3.9hz,1h),2.15
ꢀ–
2.07(m,1h),2.06
–
1.91(m,4h),1.90
–
1.60(m,4h),1.56
–
1.23(m, 3h),1.22
‑
1.11(m,6h),1.09
–
0.82(m,27h)。ms(esi)(混合物)m/z336.30(m+h)
+
。lcms(混合物),r
t
(峰1)=8.76min,m/z(m+h)
+
= 336.2;lcms r
t
(峰2)=8.84min,m/z(m+h)
+
=336.2;lcms r
t
(峰 3)=9.05min,m/z(m+h)
+
=336.2。分析计算值:对于c
23
h
29
no(混合物)来说:c,82.34;h,8.71;n,4.18;实测值:c,82.07;h, 8.58;n,4.29。
[0150]
化合物2(50mg)的异构体分离通过制备型薄层层析(tlc)(2000 微米,20
×
20cm,analtech),使用己烷:etoac:nh4oh(79.6:20.0: 0.4)来进行。将板两次暴露于上述溶剂系统,得到异构体2a(15mg) 和异构体2b与2c的混合物(33mg)。异构体2b和2c混合物的另外的制备型tlc使用己烷:etoac:nh4oh的梯度(89.6:9.9: 0.5
→
84.6/14.9/0.5)来进行,得到异构体2b(2.3mg)和异构体2b和 2c(16.6mg)。
[0151]
分离的异构体2a:1h nmr(400mhz,cdcl3)δ7.86
‑
7.84(m,2h), 7.70
‑
7.67(m,2h),7.65
‑
7.62(m,2h),7.51
‑
7.48(m,2h),7.44
‑
7.39(m, 1h),6.24(d,j=8hz,1h),4.64
‑
4.59(m,1h),2.08
‑
2.03(m,1h), 1.99
‑
1.95(m,1h),1.85
‑
1.81(m,1h),1.54(br s,1h),1.48
‑
1.41(m,1h), 1.28(s,1h),1.22
‑
1.04(m,3h),1.00
‑
0.92(m,9h)。lcms r
t
=9.26min, m/z(m+h)
+
=336.2。tlc(sio2)r
f
0.37(8:2的己烷:二乙醚+2滴 nh4oh)。
[0152]
分离的异构体2b:1h nmr(400mhz,cdcl3)δ7.85
‑
7.82(m,2h), 7.67
‑
7.60(m,4h),7.49
‑
7.36(m,3h),5.79(d,j=8hz,1h),4.03(qd,j= 10.9,3.8hz,1h),2.16
‑
2.12(m,1h),2.05
‑
1.85(m,1h),1.79
‑
1.70(m,1h), 1.25
‑
1.15(m,5h),1.04
‑
1.00(m,1h),0.95
‑
0.85(m,9h)。lcms r
t
= 8.85min,m/z(m+h)
+
=336.2。tlc(sio2)r
f 0.31(8:2的己烷:二乙醚+2滴nh4oh)。
[0153]
异构体2c(作为70:30比例的2b:2c获得):1h nmr(400mhz, cdcl3)δ7.87
‑
7.83(m,2h),7.69
‑
7.67(m,2h),7.64
‑
7.62(m,2h), 7.51
‑
7.47(m,2h),7.43
‑
7.39(m,1h),6.18(2c,d,j=8hz,0.5h),5.84 (2b,j=12hz,1h),4.39(2c,tt,j=7.8,3.9hz,1h),4.05(2b,qd,j=10.9,3.8hz,1h),2.16
‑
2.12(m,1h),2.05
‑
1.99(m,1h),1.89(br s,1h), 1.81
‑
1.61(m,4h),1.57
‑
1.54(m,1h),1.48
‑
1.15(m,4h),1.06
‑
0.98(2c,m, 4h),0.96
‑
0.88(2b,m,9h)。lcms r
t
(异构体b)=8.93min,m/z(m+h)
+
=336.2。lcms r
t
(异构体c)=9.00min,m/z(m+h)
+
=336.2。tlc(异构体c)(sio2)r
f 0.28(8:2的己烷:二乙醚+2滴nh4oh)。
[0154]
n
‑
环己基
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物3)。按照通用程序,使用环己胺.hcl(342mg,2.52mmol)来制备。将粗品残留物用30ml 己烷/乙醚(90/10)研磨,然后用15ml meoh研磨进行纯化,以76%的得率得到536mg标题材料。1h nmr(400mhz,cdcl3)δ7.86
–
7.79 (m,2h),7.68
–
7.57(m,4h),7.51
–
7.42(m,2h),7.42
–
7.34(m,1h), 6.00(d,j=8.1hz,1h),4.01(dddd,j=14.7,10.7,8.0,4.0hz,1h),2.07
ꢀ–
2.04(m,2h),1.77(dt,j=13.7,3.7hz,2h),1.67(dt,j=12.7,3.7hz, 1h),1.52
–
1.37(m,2h),1.33
–
1.14(m,3h)。ms(esi)m/z 280.3(m+h)
+
。分析计算值:对于c
19
h
21
no.0.3h2o来说:c,80.13;h,7.65;n, 4.92;实测值:c,80.15;h,7.37;n,4.99。
[0155]
n
‑
(双环[2.2.1]庚
‑2‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物4,单一异构体)。按照通用程序,使用双环[2.2.1]庚
‑2‑
胺.hcl(106mg,0.72mmol) 来制备。将粗品残留物通过自动快速层析进行纯化,以38%的得率得到80mg标题材料。1h nmr(400mhz,cdcl3)δ7.88
–
7.77(m,2h), 7.69
–
7.58(m,4h),7.51
–
7.42(m,2h),7.47
–
7.34(m,1h),6.17(d,j= 7.2hz,1h),4.35(dddd,j=11.3,6.8,4.4,1.6hz,1h),2.59(br s,1h), 2.39
–
2.14(m,2h),1.71
–
1.44(m,2h),1.39(ddt,j=9.9,3.2,1.7hz, 1h),1.34
–
1.23(m,1h),0.86(ddd,j=12.9,4.7,3.0hz,1h)。ms(esi) m/z 292.4(m+h)
+
。分析计算值:对于c
20
h
21
no来说:c,82.44;h, 7.26;n,4.81;实测值:c,82.05;h,7.10;n,4.84。
[0156]
n
‑
环庚基
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物5)。按照通用程序,使用环庚胺(100mg,0.88mmol)来制备。将粗品残留物通过自动快速层析进行纯化,以77%的得率得到200mg标题材料。1h nmr(400 mhz,cdcl3)δ7.86
–
7.78(m,2h),7.69
–
7.57(m,4h),7.50
–
7.43(m, 2h),7.42
–
7.35(m,1h),6.07(d,j=8.1hz,1h),4.18(ddt,j=12.8,8.4, 3.6hz,1h),2.17
–
1.98(m,3h),1.73
–
1.60(m,4h),1.58
–
1.49(m,5h)。 ms(esi)m/z 294.3(m+h)
+
。分析计算值:对于c
20
h
23
no来说:c,81.87; h,7.90;n,4.77;实测值:c,81.84;h,7.76;n,4.67。
[0157]
n
‑
(双环[3.2.1]辛
‑3‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物6)。按照通用程序,使用双环[3.2.1]辛
‑3‑
胺.hcl(90mg,0.55mmol)来制备。将粗品残留物通过自动快速层析进行纯化,以32%的得率得到54mg 标题材料。1h nmr(400mhz,cdcl3)δ7.84
–
7.77(m,2h),7.70
–
7.56 (m,4h),7.51
–
7.42(m,2h),7.42
–
7.34(m,1h),5.86(d,j=8.4hz,1h), 4.33(tdt,j=11.5,8.4,5.8hz,1h),2.31(br s,2h),2.06
–
1.97(m,2h), 1.69(br s,4h),1.54
–
1.44(m,1h),1.40(d,j=11.2hz,1h),1.33
–ꢀ
1.23(m,2h)。ms(esi)m/z 306.3(m+h)
+
。分析计算值:对于c
21
h
23
no 来说:c,82.58;h,7.59;n,4.59;实测值:c,82.35;h,7.68; n,4.58。
[0158]
n
‑
环辛基
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物7)。按照通用程序,使用环辛胺(500mg,3.93mmol)来制备。将粗品残留物使用己烷/etoac (95/5
→
30/70)通过快速层析,然后通过自动快速层析进行纯化,以 50%的得率得到605mg标题材料。1h nmr(400mhz,cdcl3)δ7.86
–ꢀ
7.78(m,2h),7.68
–
7.56(m,4h),7.51
–
7.42(m,2h),7.42
–
7.34(m, 1h),6.08(d,j=8.1hz,1h),4.23(ddq,j=12.0,8.0,3.7hz,1h),2.01
–ꢀ
1.89(m,2h),1.78
–
1.60(m,12h)。ms(esi)m/z 308.3(m+h)
+
。分析计算值:对于c
21
h
25
no来说:c,82.04;h,8.20;n,4.56;实测值: c,81.93;h,8.10;n,4.58。
[0159]
n
‑
(十氢萘
‑1‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物8,三种异构体的混合物)。按照通用程序,使用十氢萘
‑1‑
胺hcl(91mg,0.483mmol) 来制备。将粗品残留物使用15ml meoh通过研磨进行纯化,以84%的得率得到136mg标题材料。1h nmr(400mhz,cdcl3)δ7.87
–
7.79 (m,6h),7.72
–
7.57(m,12h),7.51
–
7.42(m,6h),7.42
–
7.35(m,3h), 6.05(d,j=8.5hz,1h),5.82(d,j=9.3hz,2h),4.15(ddt,j=11.8,7.9, 4.0hz,1h),3.89
–
3.75(m,2h),2.16
–
2.06(m,3h),1.97
–
0.81(m, 45h)。ms(esi)m/z 334.30(m+h)
+
。分析计算值:对于c
23
h
27
no.0.3h2o 来说:c,81.52;h,8.21;n,4.13;实测值:c,81.44;h,7.94; n,4.16。
[0160]
n
‑
(1,2,3,4
‑
四氢萘
‑1‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物9)。按照通用程序,使用1,2,3,4
‑
四氢
‑1‑
萘胺(250mg,1.70mmol)来制备。将粗品残留物通过自动快速层析进行纯化,以69%的得率得到384mg 标题材料。1h nmr(400mhz,cdcl3)δ7.90
–
7.82(m,2h),7.69
–
7.57 (m,4h),7.51
–
7.43(m,2h),7.42
–
7.34(m,2h),7.24
–
7.12(m,3h), 6.37(d,j=8.4hz,1h),5.48
–
5.38(m,1h),2.94
–
2.75(m,2h),2.24
–ꢀ
2.12(m,1h),2.03
–
1.86(m,3h)。ms(esi)m/z 328.20(m+h)
+
。分析计算值:对于c
23
h
21
no来说:c,84.37;h,6.46;n,4.28;实测值: c,84.14;h,6.37;n,4.17。
[0161]
n
‑
(十氢萘
‑2‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物10,通过lcms 分析以86:13的比例存在的两种异构体的混合物)和n
‑
((2sr,9rs,10sr)
‑ꢀ
十氢萘
‑2‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物12,单一异构体)。按照通用程序,使用十氢萘
‑2‑
胺(63mg,0.41mmol)来制备。将粗品残留物通过自动快速层析进行纯化,得到化合物10(111mg,80%)和化合物12(28mg,20%)。1h nmr(混合物)(400mhz,cdcl3,10) δ7.87
–
7.78(m,3h),7.69
–
7.57(m,6h),7.50
–
7.42(m,3h),7.42
–ꢀ
7.35(m,1h),6.00(d,j=8.1hz,1h),5.94(d,j=8.4hz,0.31h),4.20(s, 0.26h),4.00(tdt,j=11.9,8.2,4.2hz,1h),2.18
–
1.59(m,9h),1.57
–ꢀ
0.84(m,8h)。ms(esi)(混合物)m/z 334.3(m+h)
+
。lcms(混合物) r
t
(峰1(主要异构体)对应于化合物12)=7.91min,m/z(m+h)
+
=334.2; lcms r
t
(峰2(次要异构体))=8.70min,m/z(m+h)
+
=334.2。分析计算值:对于c
23
h
27
no(混合物)来说:c,82.84;h,8.16;n,4.20;实测值:c,82.57;h,7.97;n,4.20。tlc(主要异构体,对应于化合物12)(sio2)r
f
0.54(8:2的己烷:etoac)。tlc(次要异构体)(sio2) r
f 0.59(8:2的己烷:etoac)。
[0162]1h nmr(400mhz,cdcl3,化合物12,单一异构体)δ7.87
–
7.79(m, 2h),7.70
–
7.57(m,4h),7.51
–
7.43(m,2h),7.42
–
7.35(m,1h),6.00(d, j=8.1hz,1h),4.01(tdt,j=12.0,8.4,4.3hz,1h),1.96
–
1.58(m,8h), 1.56
–
1.20(m,8h)。ms(esi)(单一异构体)m/z 334.3(m+h)
+
。lcms (单一异构体)r
t
=8.04min,m/z(m+h)
+
=334.2。分析计算值:对于 c
23
h
27
no(单
一异构体)来说:c,82.84;h,8.16;n,4.20;实测值: c,82.73;h,8.13;n,4.14。tlc(sio2)r
f
0.54(8:2的己烷:etoac)。
[0163]
化合物12的1h、
13
c、gcosy、noesy、ghsqcad、ghmbcad、 gh2bc。所有实验在装备有onenmr探针的agilent ddr2 500mhz 波谱仪上进行,对于1h和
13
c来说分别以499.90mhz和125.71mhz 的共振频率运行。实验在环境温度下使用cdcl3作为溶剂运行。1h波谱以残留的质子化溶剂(7.26ppm)为参比,
13
c参比于77ppm。波谱使用mestrenova(12.0.3)nmr处理程序进行处理。
[0164]1h nmr:10秒弛豫延迟,8013hz波谱窗口,2.04秒采集时间, 8次扫描。使用whittaker平滑器(自动检测)进行基线校正。
[0165]
13
c nmr:宽带1h
‑
解耦,1秒弛豫延迟,512次扫描,31250hz 波谱窗口,1.05秒采集时间。使用whittaker平滑器(自动检测)进行基线校正,并使用0.5hz指数乘法。
[0166]
gcosy:1秒弛豫延迟,每个增量4次扫描,200个增量,4882hz 波谱窗口,0.15秒采集时间。在傅立叶变换之前,将f1和f2乘以正弦平方ii函数(50%),正如通过mestrenova所实施的。在f1中进行了针对1024个点的线性预测(zhu
‑
bax)。使用whittaker平滑器(自动检测)对两个维度进行基线校正。
[0167]
gh2bc:1秒弛豫延迟,每个增量8次扫描,200个增量,8013、 25141hz波谱窗口(分别为1h和
13
c),0.15秒采集时间。在傅立叶变换之前,将f1乘以高斯函数并将f2乘以正弦平方ii函数(50%),正如通过mestrenova所实施的。使用whittaker平滑器(自动检测) 对两个维度进行基线校正。在f1中进行了针对2048个点的线性预测 (zhu
‑
bax)。
[0168]
ghmbcad:1秒弛豫延迟,每个增量8次扫描,320个增量,8013、 30166hz波谱窗口(分别为1h和
13
c),0.15秒采集时间。在傅立叶变换之前,将f2乘以高斯函数并将f1乘以正弦平方ii函数(50%),正如通过mestrenova所实施的。使用whittaker平滑器(自动检测) 对两个维度进行基线校正。在f1中进行了针对2048个点的线性预测 (zhu
‑
bax)。
[0169]
ghsqcad:1秒弛豫延迟,每个增量4次扫描,200个增量,8013、25141hz波谱窗口(分别为1h和
13
c),0.15秒采集时间。在傅立叶变换之前,将f1和f2乘以高斯函数。使用whittaker平滑器(自动检测)对两个维度进行基线校正。在f1中进行了针对2048个点的线性预测(zhu
‑
bax)。
[0170]
n
‑
(1,2,3,4
‑
四氢萘
‑2‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物11)。按照通用程序,使用1,2,3,4
‑
四氢萘
‑2‑
胺.hcl(197mg,1.34mmol)来制备。将粗品残留物使用15ml meoh通过研磨进行纯化,以75%的得率得到328mg标题材料。1h nmr(400mhz,cdcl3)δ7.95
‑
7.93(m,2h), 7.77
‑
7.71(m,4h),7.57
‑
7.50(m,3h),7.37(s,1h),7.23
‑
7.26(m,3h), 6.29(d,j=4hz,1h),4.65(br s,1h),3.39(d,j=20hz,1h),3.07(br s, 1h),2.88
‑
2.94(m,1h),2.33
‑
2.30(m,1h),2.09
‑
2.00(m,1h),1.70(s,1h)。 ms(esi)m/z 328.2(m+h)
+
。分析计算值:对于c
23
h
21
no来说:c,84.37; h,6.46;n,4.28;实测值:c,84.10;h,6.42;n,4.25。
[0171]
n
‑
(螺[5.5]十一烷
‑3‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物13)。按照通用程序,使用螺[5.5]十一烷
‑3‑
胺.hcl(90mg,0.44mmol)来制备。将粗品残留物通过自动快速层析进行纯化,以84%的得率得到130mg 标题材料。1h nmr(400mhz,cdcl3)δ7.86
–
7.79(m,2h),7.69
–
7.57 (m,4h),7.51
–
7.43(m,2h),7.42
–
7.35(m,1h),6.02(d,j=8.1hz,1h), 3.97(dddd,j=14.9,10.7,8.3,4.2hz,1h),1.88(ddd,j=13.1,6.2,3.8 hz,3h),1.67(d,j=
13.6hz,3h),1.42(br s,8h),1.25(td,j=12.7,4.4 hz,4h)。ms(esi)m/z 348.4(m+h)
+
。分析计算值:对于c
24
h
29
no来说:c,82.95;h,8.41;n,4.03;实测值:c,82.99;h,8.42;n, 3.99。
[0172]
n
‑
(螺[4.5]癸
‑8‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物14)。按照通用程序,使用螺[4.5]癸
‑8‑
胺.hcl(91mg,0.48mmol)来制备。将粗品残留物通过自动快速层析进行纯化,以68%的得率得到110mg标题材料。1h nmr(400mhz,cdcl3)δ7.87
–
7.79(m,2h),7.69
–
7.57(m,4h), 7.51
–
7.43(m,2h),7.42
–
7.35(m,1h),6.01(d,j=8.1hz,1h),4.05
–ꢀ
3.93(m,1h),2.00
–
1.91(m,2h),1.67
–
1.60(m,3h),1.58
–
1.31(m, 11h)。ms(esi)m/z 334.3(m+h)
+
。分析计算值:对于c
23
h
27
no来说: c,82.84;h,8.16;n,4.20;实测值:c,82.57;h,8.16;n,4.22。
[0173]
n
‑
(金刚烷
‑1‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物15)。按照通用程序,使用1
‑
金刚烷胺.hcl(100mg,0.54mmol)来制备。将粗品残留物通过自动快速层析进行纯化,以62%的得率得到110mg标题材料。1h nmr(400mhz,cdcl3)δ7.83
–
7.75(m,2h),7.67
–
7.57(m,4h), 7.51
–
7.42(m,2h),7.42
–
7.34(m,1h),5.84(s,1h),2.15(br s,9h),1.73 (br s,6h)。ms(esi)m/z 332.3(m+h)
+
。分析计算值:对于 c
23
h
25
no.0.1h2o来说:c,82.89;h,7.62;n,4.20;实测值:c, 82.87;h,7.47;n,4.18。
[0174]
体外药理学
[0175]
使用ca
2+
成像评估trpm8激动剂和拮抗剂活性。使用基于fura
‑
2 的ca
2+
成像评估合成的化合物对icilin诱发的ca
2+
信号的影响。首先将稳定表达人类trpm8的hek
‑
293细胞(来自于thomas voets教授的善意馈赠,laboratory of ion channels research,ku leuven,belgium) 用fura
‑
2 am装载45min,然后另外静置40min以允许染料去酯化。然后将所述细胞浸泡在无ca
2+
hbss缓冲液中,并与测试化合物温育5 min,然后向浸泡溶液添加公知的trpm8激动剂icilin(500nm,来自于tocris)。在icilin添加后1min,向所述浸泡溶液添加2mm ca
2+
。
[0176]
使用安装在nikon eclipse ti
‑
s显微镜上的qiclick
tm
数字ccd相机(qimaging,bc,canada)捕获比率荧光图像。连续激发由在355nm (f
355
)和380nm(f
380
)波长led两者之间交替的dual optoled电源(cairn)提供。在510nm(470nm
–
550nm)处收集发射荧光。使用(molecular devices,usa)每5秒采集12位图像。在每个时间点提取355nm和380nm波长的荧光,对自发荧光进行校正,然后计算355nm/380nm比率(f
355
/f
380
)以代表ca
2+
流入。所有ca
2+
成像实验在室温(22℃)进行。为了比较,将每种化合物的峰值ca
2+
响应归一化到icilin(500nm)的响应。rq
‑
00203078购自tocris。
[0177]
为了获得icilin的浓度响应曲线,将装载有fura
‑
2的稳定表达人类trpm8的hek
‑
293细胞在不同的皮氏培养皿中浸泡在无ca
2+
hbss 中,并首先与梯度浓度(10
‑9至10
‑6m)的icilin温育。在icilin添加后 1min,向浸泡溶液添加2mm ca
2+
并记录得到的ca
2+
流入(作为fura
‑
2 荧光比率)。从相应的浓度响应曲线获得ec
50
。
[0178]
为了确定所设计的化合物(例如来自于下面的表1)的拮抗剂活性,将浸泡在无ca
2+
hank's平衡盐溶液(无ca
2+
hbss)中的细胞首先与不同浓度(1nm、3nm、10nm、30nm、100nm、300nm、1μm、 3μm、10μm、30μm和100μm)的化合物2
‑
15温育3min。然后添加500nm icilin并继续温育1min,将无ca
2+
hbss用含有2mm游离 ca
2+
的hbss代替,并测量得到的ca
2+
信号。由于在文献中报告的 trpm8拮抗剂rq
‑
00203078相比于其他拮抗剂对htrpm8的高纳摩尔效能(<10nm),rq
‑
00203078被用作阳性对照并且用于比较目的。将ic
50
值≤100nm的化合物在10μm
的单一浓度下单独测试,以获得它们诱导ca
2+
流入的固有(激动剂)活性,并与500nm icilin的效果进行比较。
[0179]
trpa1和trpv1选择性测定法。ca
2+
通量测定法利用fluo
‑
8 ca
2+
染料,并使用flipr
tetra
读板器(molecular devices)在470
‑
495nm 的激发波长和515
‑
575nm的发射波长下测量荧光。测试了总共8种化合物的激动剂(固有)和拮抗剂活性,它们的使用浓度大约对应于针对trpm8的ic
90
和10
×
ic
90
,以证实10倍选择性。将稳定表达人类 trpa1(eurofins目录号cyl3066)和人类trpv1(eurofins目录号 cyl3063)的重组hek293细胞系用于所述研究。细胞在增补有10% fbs、1%非必需氨基酸和400μg/ml遗传霉素的dmem
‑
f12培养基中培养和维持。将异硫氰酸烯丙酯(aitc,millipore sigma)和辣椒素 (tocris)用作参比激动剂,而钌红(tocris)和辣椒平(millipore sigma) 分别作为针对trpa1和trpv1的参比拮抗剂。对于所述实验来说,将细胞铺于胶原蛋白包被的平底384孔板中,并在37℃ 5%co2下温育。温育24h后,吸出培养基并向每个孔中的细胞添加40μl含有5 μg/ml fluo
‑
8 ca
2+
染料的染料载样缓冲液(改良的hanks平衡盐溶液 (hbss),其中对hbss进行增补以含有20mm hepes和2.5mm丙磺舒,ph 7.4),并在加湿培养箱中在30℃(5%co2)温育80分钟,然后开始flipr tetra流程。首先将测试化合物溶解在dmso中,以制备300
×
最终测定浓度,然后在测定缓冲液(改良的hanks平衡盐溶液(hbss),其中对hbss进行增补以含有20mm hepes,ph 7.4) 中稀释到最终稀释度。对于激动剂测定来说,在建立荧光基线后向测试板添加测试化合物、介质对照和参比激动剂(e
max
=300μm(aitc) 和3μm(辣椒素)),温育180秒。对于拮抗剂测定来说,将细胞与测试化合物或阳性对照(已知的拮抗剂)在室温下预温育五(5)分钟,然后在建立荧光基线后用ec
80
浓度的参比激动剂(aitc ec
80
=10 μm,辣椒素ec
80
=0.1μm)激惹180秒。激动剂:在归一化到e
max
时25%激活。拮抗剂:在归一化到ec
80
时25%抑制。
[0180]
全细胞膜片钳电生理学
[0181]
hek
‑
293细胞培养。将人类胚胎肾(hek)293细胞(atcccrl
‑
1573)在包含90%dulbecco’s改良的eagle’s培养基、10%胎牛血清、100u
·
ml
‑
1青霉素
‑
链霉素和2mm l
‑
谷氨酰胺(gibco)的生长培养基中培养。细胞在35mm聚苯乙烯培养皿(falcon)中,在37℃和 5%co2存在下培养。将细胞用含有egfp作为报告物的pires2质粒中的人类trpm8瞬时转染。该质粒表达双顺反子mrna,所述mrna 具有位于trpm8基因与荧光蛋白报告物基因之间的内部核糖体进入位点(ires),使得所述报告物不被共价融合到trpm8。瞬时转染在 35mm培养皿(falcon)中,使用fugene 6转染试剂(promega)和0.5 μg质粒以每μg质粒3μl转染试剂的比例,按照制造商的流程进行。hek
‑
293细胞通过多态性遗传标志物测试(dna diagnostics centermedical)进行认证。
[0182]
全细胞膜片钳电生理学。在转染后48小时,通过简短暴露于0.25%胰蛋白酶/edta(gibco)使细胞从培养皿脱离,重悬浮在增补过的 duldmem中,在盖玻片上铺板,并允许其在37℃和5%co2中恢复1
–
2 h。选择表现出指示成功转染的绿色荧光的细胞用于电生理学测量。将细胞置于含有细胞外溶液的区室中,所述细胞外溶液含有(以mm为单位)nacl 132、kcl 4.8、mgcl
2 1.2、cacl
2 2、hepes 10和葡萄糖5,使用naoh将ph调整到7.4并使用蔗糖将渗透压重量摩尔浓度调整到 310mosm。在移液管中装入溶液,所述溶液含有(以mm为单位)葡萄糖酸钾135、kcl 5、mgcl
2 1、egta 5和hepes 10,用koh将ph 调整到7.2,并用蔗糖将渗透压重量摩尔浓度调整到300mosm。化学品从sigma
‑
aldrich获得。渗透压重量摩尔浓度使
用vapro 5600蒸汽压渗透压计(wescor)测量。全细胞电压钳电流测量使用axopatch 200b 放大器(axon instruments)和pclamp 10.3软件(axon instruments) 来进行。数据以2khz获取并以1khz过滤。使用p
‑
2000激光拉拔器 (sutter instruments)从硼硅酸盐玻璃毛细管(world precisioninstruments)拉出膜片移液管,并使用mf
‑
830显微拉制仪(narishige) 进行热抛光。当在细胞外溶液中测量时,移液管具有2
–
5mω的电阻。将参比电极置于2%琼脂桥中,其由与细胞外溶液相似的组合物制成,但不添加葡萄糖。实验在23
±
1℃下进行。在dmso中分别制备1m 和3.6mm的薄荷醇和化合物14储用溶液。通过在细胞外溶液中将薄荷醇稀释到500μm薄荷醇并将化合物14稀释到不同浓度(从1至1000 nm),制备了一系列灌注溶液。将灌注毛细管靠近细胞放置,并在整个记录过程中灌注溶液。在每种浓度的化合物14下测量来自于每个细胞的电流响应。每个盖玻片仅测量一个细胞,以防止以前暴露于薄荷醇和化合物14的混杂影响。
[0183]
数据分析。对于每个细胞来说,通过除以在500μm薄荷醇和不含拮抗剂的情况下测量到的最大电流,将每种浓度的化合物14下的电流量归一化。在每种拮抗剂浓度下,将来自于6个细胞的归一化的电流平均,并计算每个点的平均值的标准误差。将数据在sigmaplot中作图,拟合到单位点竞争模型。其中i是电流强度,[拮抗剂]是在特定i值下化合物14的浓度。
[0184]
肝脏代谢稳定性
[0185]
在肝微粒体中的稳定性。雄性cd
‑
1小鼠肝微粒体(lot#1710069) 购自xenotech。如下所述制备减去nadph的反应混合物。将化合物14以1μm的终浓度添加到所述反应混合物中。在单独的反应中,将对照化合物睾酮与化合物14同时进行反应。将反应混合物(不含辅因子) 的等分试样在振摇水浴中在37℃平衡3分钟。通过添加辅因子启动反应,并将所述混合物在振摇水浴中在37℃温育。在0、10、20、30和 60分钟取出等分试样(100μl)。将化合物14和睾酮样品立即与400μl 冰冷的50/50乙腈(acn)/含有0.1%甲酸和内标的h2o合并,以终止反应。然后将样品混合并离心以沉淀蛋白质。所有样品均通过 lc
‑
ms/ms使用电喷雾电离进行测定。将分析条件与0时的parr进行比较,以确定在每个时间点的剩余百分比。使用graphpad软件计算半衰期和内在清除率,拟合到单相指数衰减方程。
[0186]
反应组合物
[0187][0188]
睾酮对照
[0189]
[0190][0191]
分析方法
[0192]
液相色谱柱:thermo bds hypersil c18 30x 2.1mm,3μm,带有保护柱
[0193]
m.p.缓冲液:25mm甲酸铵缓冲液,ph 3.5
[0194]
水性储液(a):90%水,10%缓冲液
[0195]
有机储液(b):90%乙腈,10%缓冲液
[0196]
流速:350μl/min
[0197]
梯度程序:
[0198][0199]
总运行时间:2.5分钟
[0200]
自动进样器:10μl进样体积
[0201]
自动进样器清洗:水/甲醇/2
‑
丙醇:1/1/1;含有0.2%甲酸
[0202][0203][0204]
tem:500;cad:7;cur:20;gs1:20;gs2:30
[0205]
体内测定法。将c57小鼠(≈30g)(harlam,holland)用于所述研究。所有实验得到实验进行之地universidad miguel hernandez的学术动物和伦理委员会批准,并且符合欧洲经济共同体和国际疼痛研究联合会的研究和伦理问题委员会的指导方针。所述研究的涉及动物护理的所有部分均在兽医的控制下进行。
[0206]
湿狗样抖动测定法。将icilin这种trpm8激动剂溶解在含有20% dmso和1%吐温
80的蒸馏水中,并以10mg/kg的量腹膜内(i.p.)注射。每只动物在icilin给药之前连续2天适应30min。化合物14储用液在dmso中制备,并在注射用盐水中稀释。将加巴喷丁溶解在盐水中,并在icilin注射前60min以25mg/kg的剂量s.c.给药。对照动物接受介质注射。
[0207]
冷异常性疼痛。将奥沙利铂(tocris)溶解在轻度加温的水中,并在第1、3和5天以6mg/kg的剂量皮下(s.c.)注射。在给药后第7天进行实验。与奥沙利铂注射一起,将盐水和5%甘露糖醇溶液腹膜内注射,以防止肾损伤和脱水。化合物14储用液在dmso(sigma
‑
aldrich) 中制备,并在注射用盐水中稀释。将不同剂量(0.1至1μg)的化合物注射到小鼠右后爪的跖面中(25μl)。使用丙酮滴加法评估冷化学热敏感性。将小鼠置于金属网笼中并允许其熟悉环境大约30分钟,以使它们适应环境。将新鲜分配的丙酮液滴(10μl)轻柔施加到后爪的跖面中部上。对舔爪的冷化学敏感性反应被记录为阳性反应(伤害感受性疼痛反应)。所述反应使用数字秒表测量20秒。对于每次测量来说,对爪取样两次并计算平均值。每次施加丙酮之间的时间间隔为大约5 分钟。
[0208]
药理学评估
[0209]
使用ca
2+
成像评估trpm8激动剂和拮抗剂活性。在稳定表达htrpm8的hek
‑
293细胞中,使用基于fura
‑
2的ca
2+
成像评估化合物 2
‑
15调节trpm8功能的能力。所述细胞是来自于thomas voets (laboratory of ion channels research,ku leuven,belgium)的善意馈赠。细胞内游离ca
2+
的浓度([ca
2+
]
i
)作为fura
‑
2荧光比率(f
355
/f
380
)被监测。
[0210]
评估了所述化合物针对由icilin(ag
‑3‑
5)诱发的ca
2+
流入([ca
2+
]
i
)。 icilin以500nm的浓度使用,因为在我们的剂量响应研究中发现在该浓度下发生最大ca
2+
进入。在测定中选择icilin来刺激trpm8,这是因为它在初始的浓度响应研究中明显比(
‑
)
‑
薄荷醇更加有效(ec
50
:~70 nm相比于6μm)(图13
‑
14),并且这与以前的报告大体一致。
[0211]
trpv1和trpa1激动剂和拮抗剂ca
2+
通量测定法(选择性情况分析)。在eurofins pharma discovery services(st.charles,mo),使用高通量的基于flipr的ca
2+
通量测定法,评估了htrpm8 ic
50
值≤100 nm的化合物在两个相关的温度敏感性亚型htrpa1和htrpv1处的脱靶效应。化合物在对应于在trpm8处大约90%的靶覆盖率的单一浓度下进行评估,然后在10倍高的浓度下通过单点测定法进行评估,以证明>10倍的选择性。在稳定表达人类trpa1或trpv1的重组hek293 细胞系中评估激动剂(固有)活性,并分别归一化到激动剂异硫氰酸烯丙酯或辣椒素的最大效应(emax)。在这些细胞系中,通过测量类似物通过抑制ca
2+
流入来抑制aitc或辣椒素诱导的细胞溶质[ca2
+
]提高的能力,对拮抗剂活性进行评估,并与用作参比拮抗剂的钌红 (trpa1)和辣椒平(trpv1)的效果进行比较。
[0212]
化合物14的全细胞膜片钳电生理学。在钙通量测定法中化合物 14的功能活性使用全细胞膜片钳电生理学得以确认。如先前所述,人类trpm8全细胞膜片钳电生理学在23
±
1℃下,在通过多态性遗传标志物测试(dna diagnostics center medical)验证的人类胚胎肾(hek) 293细胞(atcc crl
‑
1573)上进行。使用了500μm薄荷醇和可变浓度(从0至1μm)化合物14的一系列溶液。在化合物14的每种浓度下测量细胞电流响应。为了确定ic
50
,在拮抗剂的每种浓度下将来自于 6个细胞的归一化的电流平均,并计算每个点处平均值的标准误差。将数据拟合到单一位点竞争模型,以获得ic
50
。ic
50
全细胞膜片钳实验特意针对饱和(500μm)薄荷醇浓度进行,这是因为薄荷醇电流不是ca
2+
依赖性的,并且提供可重复和鲁棒的电流。同样地,研究化合物14对饱和薄荷醇的抑制性效应,允许与在全细胞膜片钳测量中
使用这些条件的其他已发表的trpm8拮抗研究进行直接比较。
[0213]
体外代谢稳定性。使用absorption systems(exton,pa),通过确定在nadph存在下与小鼠肝微粒体一起温育时在0、10、20、30 和60分钟时剩余的百分比,对化合物14在小鼠肝微粒体中的代谢稳定性进行了评估。计算了化合物14以及对照(睾酮)的半衰期(t
1/2
) 和体外内在清除率(cl
int
)。
[0214]
结果和讨论
[0215]
关于包括(
‑
)
‑
薄荷基化合物1和amg2850在内的已知trpm8拮抗剂的可用功能数据来自于大鼠和人类trpm8,对于它们来说尚不存在解析的结构,而禽类直向同源物的结构最近已使用cryo
‑
em阐明。为了首先评估这些物种之间的序列保守程度,进行了禽类、人类和大鼠trpm8的跨膜s1
‑
s4螺旋(vsld)、s5
‑
s6螺旋(孔结构域)、孔螺旋(ph)和trp螺旋的序列比对(图12)。正如上文详述的,据报道vsld和trp螺旋内的残基对激动剂(薄荷醇)结合、激动剂(薄荷醇、icilin)响应或功效和电压敏感性来说是重要的。有趣的是,全长禽类与人类trpm8之间的高度同源性(83%)在这个含有配体结合位点的跨膜区域内得以保持(86%);此外,在禽类与大鼠直向同源物之间,在这个相同区域中存在可比的高序列同一性(87%)(图12)。因此,禽类trpm8结构被认为是用于建立htrpm8的同源性模型的可靠模板,其目的是首先预测已知trpm8拮抗剂(
‑
)
‑
薄荷基化合物1和 amg2850的合理结合模式,并建立相关的结构
‑
功能关联性。后者反过来可以为设计新型trpm8拮抗剂探针提供基于结构的策略。
[0216]
实施例1
‑
md模拟
[0217]
没有可用的htrpm8结构。因此,首先在白领姬鹟(ficedulaalbicollis)的cryo
‑
em结构(trpm8
fa
,pdb:6bpq)的基础上建立 htrpm8的同源性模型,其中htrpm8与全长trpm8
fa
享有83%的序列同一性,并且在含有配体结合位点的区域中享有86%的序列同一性。尝试主要集中于trpm8的跨膜区,其由vsld(s1
‑
s4螺旋,也被称为感应结构域sd)和孔结构域以及trp螺旋构成,并使用从gln671 至asn1010的序列(340个残基)建立htrpm8的同源性模型。正如上文讨论的,vsld和trp螺旋结合小分子激动剂,而分离的vsld (包括s1结构域前)据报道重现了与全长htrpm8(1104个残基)的功能性激活相一致的结合表型。
[0218]
将ca
2+
离子置于vlsd中,与glu782、gln785、asn799和asp802 配位,以使所述人类模型更加类似于相关的人类melastatin亚型m2 (pdb 6mj2)和m4(pdb 6bqv)的cryo
‑
em结构,并为我们使用trpm8 激动剂icilin作为激活剂的ca
2+
通量研究提供了结构背景(表1)。这些结构捕获了结合的ca
2+
离子,所述钙离子配位到在vlsd中取向相近的4个侧链,其中三个在trpm8、trpm2和trpm4之间保守:glu782 (trpm8,s2螺旋)/glu843(trpm2,s2)/glu828(trpm4,s2); gln785(trpm8,s2)/gln846(trpm2,s2)/gln831(trpm4,s2);和asn799(trpm8,s3)/asn869(trpm2,s3)/asn865(trpm4, s3)。将剩余的非保守ca
2+
结合残基考虑在内,选择asp802(s3)作为最终的螯合氨基酸以满足四面体复合物,对应于m4亚型(s3螺旋) 中的asp868。值得注意的是,asn799和asp802是公知的icilin敏感的残基。最近报道的结合有icilin的trpm8结构(pdb 6nr3,) 揭示出ca
2+
离子结合到现在明确确定的ca
2+
结合位点内的这四个残基,与本同源性模型相一致。
[0219]
随后,将(
‑
)
‑
薄荷基化合物1、amg2850和化合物14对接到 htrpm8的配体结合位点中,对htrpm8中的每种化合物进行100ns 分子动力学(md)模拟,并且如下文所详述的分析结果。在ca
2+
通量测定法中被描述为针对大鼠trpm8的有效且选择性的trpm8拮抗剂 (ic
50
相比于20μm薄荷醇,20
±
2nm;ic
50
相比于0.25μm icilin,50
ꢀ±
10nm)的(
‑
)
‑
薄荷基化合物1,目前在文献中被用作trpm8工具分子(也被描述为omdm233),amg2850也是如此。
[0220]
实施例2
‑
(
‑
)
‑
薄荷基化合物1和htrpm8
[0221]
如图2c中所示,结果显示在所述模拟期间,htrpm8(约) 和(
‑
)
‑
薄荷基化合物1两者的均方根偏差(rmsd)在50ns 后保持稳定,表明100ns的时间尺度是合理的。
[0222]
化合物1的联苯基在md模拟期间保持稳定,突入到采取扩展构象的结合腔的底部,朝向trp螺旋,与asn741(s1,未示出) 和保守的val849(s4,)形成强疏水相互作用,正如在图2b中所示,与ws
‑
12的相应的甲氧基苯基占据相似的空间。这个位姿与对该支架的sar研究相一致,在所述研究中联苯基取代提供了研究的所有类似物中最高的trpm8效力。
[0223]
与联苯基组成部分相反,当比较在md前(图2a)和md后(图 2b)的结合模式时,发现化合物1的柔性部分即(
‑
)
‑
薄荷基组成部分在 md模拟期间承受构象变化。然而,在md期间可以观察到化合物1 与某些残基之间的相互作用。例如,化合物1的(
‑
)
‑
薄荷基与保守的 arg1008(trp螺旋,未示出)相互作用(图2b),所述残基采取与在结合有ws
‑
12的结构中看到的相似的折叠构象,并且可能代表了trpm8对小分子配体的共同结合残基。为了探索这些残基对化合物1的结合的贡献,使用mm/gbsa方法分解了自由能,如图2d中所示。从所述能量分解,发现arg1008对化合物1的结合有极大贡献。尽管化合物1与arg842(s4)之间的距离约为但在md模拟期间(
‑
)
‑
薄荷基组成部分接近保守的leu778(s2,未示出)(图 2b),与ws
‑
12和icilin分别的(
‑
)
‑
薄荷基和硝基苯基结合区重叠,使得arg842与leu778相比对结合自由能的贡献较少。所述结果与使用 mm/gbsa方法的自由能分解的结果(图2d)一致。有趣的是,(
‑
)
‑ꢀ
薄荷基不接触tyr745(s1),正如通过放射性配体置换研究对(
‑
)
‑
薄荷醇所表明的,结合有ws
‑
12的结构也是如此,这可能是由于联苯基的锚定性质,其与正构位点的底部形成广泛的疏水相互作用。这里的研究首次尝试了使用迄今为止描述的trpm8结构生物学来研究基于薄荷醇的拮抗剂介导的分子事件。
[0224]
实施例3
‑
amg2850和htrpm8
[0225]
也对amg2850和htrpm8进行了100ns md模拟。发现在60ns 后,htrpm8的rmsd平衡(约),正如在图3c中所示。amg2850 的rmsd保持稳定在(图3c)。由于amg2850的稳定性,100 ns的时间尺度对于探索它的潜在结合模式来说是合理的。比较md前 (图3a)和md后(图3b)amg2850的结合模式,发现amg2850 与htrpm8之间的几个重要相互作用保持稳定。例如,保守的arg842 (s4)与amg2850的脲羰基形成强的氢键类似于ws
‑
12 的酰胺羰基和icilin的二氢嘧啶酮羰基,表明了通过这个共同残基发生的trpm8配体识别的共同氢键受体特点。与这种预测的相互作用相一致,含有四氢噻吩并吡啶核心的amg2850前体系列的sar研究突出了脲组成部分的重要性,其中该基团的缺失消除了trpm8活性 (tamayo等人报道的衍生物24
‑
26)。md结果也显示,保守的trp798 (s3)与相距的amg2850的三氟苯基cf3基团形成氢键,与前体四氢噻吩并吡啶系列的sar研究相一致,在所述研究中4
‑
cf3提供最佳的功能和药代动力学性质。有趣的是,amg2850的相关四氢异喹
啉类似物的无活性的s
‑
对映异构体将该三氟苯基定位在相反方向上,远离trp798,而相应的r
‑
对映异构体具有报道的trpm8 ic
50
:56
±
24 nm(tamayo等人报道的衍生物87
‑
88)。此外,leu841(s4)(距离:未示出)和arg842的骨架(距离:未示出)通过疏水相互作用与amg2850的三氟苯基cf3基团相互作用。tyr1005(保守残基,trp螺旋)与相距的5,6,7,8
‑
四氢
‑
1,7
‑
萘啶形成强疏水相互作用。该残基(trpm8
fa
中的tyr1004)与icilin的硝基和ws
‑
12 的酰胺氮形成氢键,表明了另一个共同的trpm8结合残基,与薄荷醇的功能研究相一致。同样,这种相互作用与该系列的sar数据相一致,表明了所述离子通道与氮杂四氢喹啉之间的疏水相互作用的重要性。包括除去芳香环、将哌啶扩展一个碳(成为氮杂)和通过8
‑
位处的甲基取代进行构象限制在内的修饰,可能扰乱这种疏水相互作用,导致trpm8活性的显著丧失或无活性(horne等人和tamayo等人报道的衍生物32、72和86)。可选地,这些类似物可能破坏arg842与 amg2850的脲羰基之间的氢键,导致trpm8活性的显著丧失。
[0226]
在分子的另一侧上,观察到asp781(s2)通过氢键与相距的三氟丙基cf3相互作用。与之前讨论的相互作用类似,这种相互作用与氮杂四氢喹啉酮和四氢异喹啉支架上该区域的sar研究相一致,其中三氟丙基提供了高trpm8效力。连同与arg842和trp798的氢键相互作用一起,它们使amg2850以t形构象定向,其中分子的任一端跨越vsld口袋的上部,与此相比使用(
‑
)
‑
薄荷基化合物1时看到扩展构象。另一方面,amg2850的氮杂四氢喹啉环深深刺入到腔内,朝向 trp螺旋,与化合物1的联苯基相似。此外,观察到leu778与相距的三氟丙基cf3形成强疏水相互作用(未显示),类似于化合物 1的(
‑
)
‑
薄荷基。这些结果与使用mm/gbsa方法的自由能分解的结果 (图3d)相一致。
[0227]
值得注意的是,从所述md研究中没有发现所研究的两种拮抗剂与ca
2+
结合残基之间的直接相互作用,这可能指向它们充当拮抗剂的能力的可能的基于结构的解释。在amg2850与arg842之间观察到相互作用,这在理论上可以通过asp802加强人类trpm8中的四面体ca
2+
复合物,类似于在人类trpm4结构中看到的(相应的trpm4残基为 arg905和asp868)。与arg842的这种相互作用可能使结合的ca
2+
失稳,从而导致通道抑制。另一方面,trpm8
fa
(禽类)结构没有将相应的残基arg841描绘为与ca
2+
结合残基相互作用,而是与icilin羰基直接相互作用。
[0228]
实施例4
‑
基于结构的设计
[0229]
通过将来自于md模拟的amg2850和(
‑
)
‑
薄荷基化合物1的预测结合模式叠加,观察到s2和trp螺旋中的几个重要残基形成vsld 内的疏水性口袋(图4)。leu778(s2)与化合物1和amg2850的(
‑
)
‑ꢀ
薄荷基和三氟丙基两者相互作用。就在附近,arg1008(trp螺旋)与 (
‑
)
‑
薄荷基形成关键的疏水相互作用。这些相互作用允许将上述基团叠加在vsld中,并表明化合物1支架可以被其他亲脂基团例如核心环己基环的扩环类似物、双环和三环、含芳香基团和螺取代的双环取代。
[0230]
通过比率测定ca
2+
成像在人类trpm8上在所述化合物1支架上探索了这些取代(代表性实验示出在图5中,相应的柱状图示出在图 15中),同时保留联苯基,因为从以前的sar研究发现这是trpm8 拮抗剂高活性的最佳取代。为此,如下面的反应路线1中所示,通过标准的edci/hobt介导的可商购的取代胺和[1,1
′‑
联苯基]
‑4‑
甲酸i
‑
1 的酰胺化,制备了化
合物1的(
‑
)
‑
薄荷基组成部分的各种不同的亲脂性取代。
[0231][0232]
反应路线1.化合物22
‑
15的合成。试剂和条件:(a)r1‑
nh2,edci, hobt,et3n。
[0233]
实施例5
‑
(
‑
)
‑
薄荷基化合物1的结构
‑
活性关系(sar)分析
[0234]
在这种测定中原型icilin的剂量响应研究以74
±
3nm的ec
50
引起 ca
2+
流入(图13),并且似乎比以前报道的位于120
‑
200nm范围内的值更加有效,但这非常可能是由细胞类型差异(cho相比于hek细胞) 或icilin敏感性的物种依赖性变化(人类相比于小鼠)造成的。在本研究中,icilin诱发的ca
2+
信号在500nm时开始达到平台。由于 rq
‑
00203078的有效trpm8拮抗剂活性,将其用作阳性对照以及用于 sar研究的参比标准品。在所述测定中,rq
‑
00203078以2.96
±
0.99nm 的ic
50
抑制icilin诱发的ca
2+
信号(图16),这低于以前针对表达 htrpm8的hek细胞中30μm薄荷醇诱发的ca
2+
流入所报道的值(~8 nm)。
[0235]
对于本发明合成的化合物来说,ic
50
值被示出在表1中,并被表示成产生icilin刺激的ca
2+
流入的半最高抑制所需的浓度。也使用以前报道的方法重新合成了(
‑
)
‑
薄荷基化合物1以充当对htrpm8的生物化学测定的另外的标准品,这是由于它在钙通量测定中对rtrpm8的有效拮抗剂活性(ic
50
相对于20μm薄荷醇,20
±
2nm;ic
50
相对于0.25 μm薄荷醇,50
±
10nm)和对htrpv1和rtrpa1的弱固有(激动剂) 活性。有趣的是,在用人类trpm8转染的hek
‑
293细胞中,化合物1 在所述测定中显示出急剧降低的效力(ic
50
为16
±
1μm)(表1)。在钙通量测定法中对人类相比于大鼠trpm8观察到的ic
50
值的差异表明了这种化合物在trpm8直向同源物之间的物种差异。已知在不同 trpm8直向同源物之间存在物种差异,尽管序列高度保守。对rtrpm8 的其他研究可以在这一系列的所有类似物上进行,以确定是否观察到类似的效力漂移。尽管人类trpm8与大鼠直向同源物高度同源,在 vsld结构域、孔结构域和trp螺旋中具有96%的序列同一性(第 734
‑
1009位残基,通过clustal omega计算,数据未示出),但存在少量不同氨基酸残基,这可能是在钙通量测定中在这些直向同源物之间观察到差异的原因。在trp螺旋中第1007位处的一个这样的残基位于结合口袋中(htrpm8中的丝氨酸,rtrpm8中的天冬酰胺)。正在进行研究以进一步表征化合物1,并且将在适当时候报道。
[0236]
去除化合物1的手性以给出异构体混合物化合物2,使得在目前描述的测定法中htrpm8的活性(htrpm8 ic
50
:468
±
1nm)相对于化合物1提高30倍(表1),表明所述混合物含有与化合物1相比在 c1、c2和c5位置处具有更优立体化学排布的异构体。相对于薄荷醇异构体混合物化合物2,去除c5甲基和c2异丙基(如在化合物3中) 和核心环己基环的构象限制(如在化合物4中)导致trpm8效力降低,在μm范围内,突出了整个(
‑
)
‑
薄荷基支架以及环己基环的构象灵活性,以及可能取代与leu778和arg1008的疏水相互作用,正如我们的md 研究所表明的。
[0237]
表1.在稳定表达htrpm8的hek
‑
293细胞中通过细胞ca
2+
通量测定法确定的以nm为单位的化合物的ic
50
值,并表示为来自于3个独立实验的平均值
±
sem。ic
50
由抑制50%的icilin诱发的ca
2+
进入的化合物浓度定义。
[0238]
[0239][0240]
另一方面,扩环类似物(环庚基化合物5和环辛基化合物7)将 htrpm8效力相对于化合物2提高8
‑
9倍,ic
50
值分别为52
±
1nm和 62
±
1nm,表明了在口袋中捕获另外的相互作用的能力。为了使这些结果合理化,将化合物5和7对接到htrpm8同源性模型中(图6)。对于两种化合物来说,联苯基环位于s1和s4螺旋与trp螺旋之间,类似于化合物1。除了phe738(保守的,s1,)、leu1001(保守的,trp螺旋,)与薄荷醇敏感和icilin敏感的tyr1005(保守的,trp螺旋,)之外,两种类似物的联苯基环还与val849 (保守的,s4,)形成强疏水相互作用,对于化合物1的联苯基也观察到同样的相互作用。1
‑
苯基与phe738和tyr1005两者形成边对面的π
‑
π堆积。这些另外的相互作用可能有助于在ca
2+
通量测定中相比于化合物1这些类似物提高的效力。有趣的是,amg2850的5,6,7,8
‑ꢀ
四氢
‑
1,7
‑
萘啶与tyr1005形成疏水接触(图3),与化合物1的1
‑
苯基位置非常相近(图4)。这强化了tyr1005作为共同小分子结合残基的见解。化合物5和7的酰胺nh和羰基o两者与arg1008(保守的, trp螺旋)以强氢键相互作用发生相互作用,可能驱动了它的强大功能活性;与此相比在化合物1中看到该残基仅与(
‑
)
‑
薄荷基组成部分形成疏水接触。这些结果表明arg1008是识别化合物1及其类似物两者的关键残基。此外,两种配体的环庚基和环辛基组成部分以相似的疏水相互作用接近三个残基,包括电压敏感和icilin敏感的arg842(保
守的,s4,)、icilin敏感的his845(保守的,s4,) 和ile846(保守的,s4,),它们位于vsld的与leu778和 arg1008的相反一侧上。合在一起,这些结果表明正构位点能够容纳比在化合物1中看到的更大的疏水性取代,其中多种其他亲脂性残基在上文提及,而联苯基提供了与腔底部的锚定相互作用。
[0241]
与化合物3和4相似,化合物5(到双环[3.2.1]辛
‑3‑
基,化合物6) 的构象限制导致效力急剧下降,这可能是由于与arg1008的多个氢键接触的丧失。使用双环和三环取代进行了探索,以进一步探测我们的系列化合物周围的亲脂空间。
[0242]
十氢萘
‑1‑
基(化合物8)导致htrpm8效力相对于化合物5和7 显著下降,在μm范围内,表明口袋具有鉴别性体积;同样,四氢萘
‑1‑ꢀ
基(化合物9)相比于化合物8遭受效力的3倍损失,同样表明在支架的这个区域处需要柔性。形成鲜明对比的是,两种异构体的混合物十氢萘
‑2‑
基(化合物10)相对于化合物8将trpm8效力提高3,500倍(ic
50
: 6
±
1nm),并且与环庚基(化合物5)和环辛基(化合物7)类似物两者相比具有高10倍的效力,表明十氢萘
‑2‑
基环占据亲脂性口袋,以最大化可用的疏水相互作用。与使用化合物8和9看到的sar趋势相一致,使用四氢萘
‑2‑
基的取代(化合物11)将htrpm8效力降低9倍,尽管对htrpm8仍保持nm的效力,并且ic
50
为52
±
1nm。通过色谱分离出化合物10的异构体之一以得到化合物12,令人欣慰地提供了在个位数nm范围内的效力,ic
50
为1.4
±
1.0nm,比非对映异构体混合物高4倍。化合物10有可能与vsld内的残基形成多重接触以给出高 htrpm8效力,类似于单一异构体化合物12。化合物10和12的lc
‑
ms 分析表明作为两种非对映异构体的混合物的化合物10包含>85%的化合物12异构体,从而解释了它的强力ic
50
值。
[0243]
通过1h、
13
c、gcosy、noesy、ghsqcad、ghmbcad和gh2bc 建立了化合物12的相对立体化学构型(表2)。包括十氢萘环质子和碳化学位移与文献值的比较在内的nmr数据的分析,表明所述化合物是顺式十氢萘,在2
‑
位中具有联苯基酰胺组成部分。noesy数据的分析表明所述酰胺基团与十氢萘桥质子呈反式(见下文结构,不能建立绝对立体化学)。
[0244]
表2.n
‑
((2sr,9rs,10sr)
‑
十氢萘
‑2‑
基)
‑
[1,1'
‑
联苯基]
‑4‑
甲酰胺(化合物 12)的1h
‑
和
13
c
‑
nmr化学位移的指派
[0245]
[0246][0247][0248]
所述结构被确定为顺式
‑
十氢萘是因为碳和质子化学位移更加符合该构型(参见dodziuk等)。顺式
‑
十氢萘桥碳(c9,10)在36.1ppm 处共振,而反式
‑
十氢萘中的所述碳在42.5ppm处共振。此外,在反式
ꢀ‑
十氢萘中桥头质子在比对于该结构观察到的更低的ppm处共振(比较 1.91、1.68ppm相比于反式
‑
十氢萘的0.87ppm)。也参见browne等。
[0249]
酰胺组成部分的相对立体化学更难确定。noesy数据与提议的结构相一致;然而,严重的化学位移重叠,尤其是h10和h1,使明确的指派变得不可能。noesy数据确定了h9(1.91ppm)和h2(4.01ppm) 在同一面上。这个结果与化学位移数据相结合,与在反式
‑2‑
位中被联苯基甲酰胺取代的顺式
‑
十氢萘相符。
[0250]
然后探测了化合物1的(
‑
)
‑
薄荷基的螺取代的双环替换。螺[5.5]
‑ꢀ
十一烷
‑3‑
基(化合物13)保留了与化合物5和7相近的效力,ic
50
为 40
±
1nm,尽管不像十氢萘
‑1‑
基(化合物10和12)那样在高nm范围内,表明受体腔的互补区域具有固定体积,并且不能容忍两个环
己基环的螺排布。
[0251]
将化合物13缩环一个碳(成为螺[4.5]癸
‑8‑
基,化合物14)重现了十氢萘
‑1‑
基异构体(化合物12)的强力活性(ic
50
:2.4
±
1.0nm),在这种测定法中具有与高效trpm8拮抗剂rq
‑
00203078可比的活性。螺[4.5]癸
‑8‑
基(化合物14)具有与化合物12相近的效力,进一步表明了口袋的受限或鉴别性质。该系列化合物的结合位点可以使用结构生物学技术例如cryo
‑
em或x
‑
射线晶体学以产生人类trpm8的结合有配体的结构,并与突变研究相结合来明确确定。目前,人类trpm8的结构未知。值得注意的是,化合物14与科学和专利文献中报道的其他有效trpm8拮抗剂享有几个共同结构特点。螺基团(螺
‑
异噁唑啉) 和联苯基芳香族排布两者在基于苯并咪唑的高效trpm8拮抗剂 jnj41876666/tc
‑
i 2014(ctrpm8 ic
50
(icilin):0.8nm)中也被看到。由glenmark pharmaceuticals报道的另一种trpm8拮抗剂(r)
‑
(
‑
)
‑
10e (htrpm8 ic
50
(
45
ca
2+
摄入):8.9nm)含有3,4
‑
二氢螺[色烯
‑
2,4
′‑
哌啶]。同样地,raqualia pharma报道了一系列氮杂螺trpm8拮抗剂,其含有通过酮连接到被芳香环和杂环对位取代的苯基环的环系统,例如1
‑
氧杂
‑3‑
氮杂螺[4.5]癸
‑2‑
酮、1,3
‑
二氮杂螺[4.5]癸烷
‑
2,4
‑
二酮和1
‑
氧杂
‑3‑ꢀ
氮杂螺[4.5]癸烷
‑
2,4
‑
二酮。
[0252]
然后从图15中示出的数据构建了化合物14的剂量响应曲线。选择化合物14用于进一步表征,这是鉴于它与化合物12不同,缺少手性中心。如图17中所示,化合物14剂量依赖性地抑制icilin诱导的 ca
2+
流入,ic
50
=2.4
±
1.0nm,并且在更高浓度下几乎废止ca
2+
流入(图 15和17)。
[0253]
为了在ca
2+
通量测定法中确定化合物14抑制薄荷醇的能力,首先在稳定表达htrpm8的hek
‑
293细胞中评估了薄荷醇响应,并发现 ec
50
~6μm(图14)。所述观察到的薄荷醇效力与以前在hek293细胞的相似的钙成像中对于htrpm8报道的值相当。化合物14仍能引起 icilin诱发的trpm8介导的ca
2+
进入的显著降低的最低浓度是3nm(图17)。化合物14在同样的最低(即3nm)浓度下针对最大(100μm) 薄荷醇诱发的trpm8介导的ca
2+
进入进行了测试(图s6a)。正如可以在图18b中看到的,3nm的化合物14也能显著(p<0.01)降低由薄荷醇引发的trpm8介导的ca
2+
进入。除了我们使用icilin进行的sar 研究之外,这些研究也为在使用薄荷醇作为激动剂的这种测定法中探索化合物14的效应提供了另外的支持。
[0254]
金刚烷基(化合物15)提供比化合物14略低的效力,ic
50
为16
±ꢀ
1nm,表明可以容忍三环以及双环,(化合物10
‑
14)。总而言之,在人类trpm8转染的细胞中ic
50
值在≤10nm的范围内的化合物10、12、 14和15在ca
2+
通量测定法中的拮抗剂活性,超过已报道的具有体内活性的trpm8拮抗剂的ca
2+
通量活性或与其相当,所述已报道的拮抗剂包括pf
‑
05105679(pfizer,1期,htrpm8 ic
50
=181nm)、amg 333 (amgen,1期,htrpm8 ic
50
=13
±
4nm)、amg2850(amgen)、 rq
‑
00203078(raqualia pharma)、amtb(bayer)、芳基甘氨酸衍生物12和乙烯基环烷基取代的苯并咪唑25(janssen)、dfl23448和 dfl23693、m8
‑
b、m8
‑
an、色氨酸衍生物14等。在ca
2+
通量测定法中htrpm8 ic
50
值≤100nm的化合物(化合物5、7、10
‑
15)均不能单独地在10μm的单一高浓度下刺激所述通道(图19),与在我们的拮抗剂测定法中获得的结果相一致。
[0255]
实施例6
‑
对trpa1和trpv1的体外选择性情况分析
[0256]
接下来确定新型化合物5、7和10
‑
15对两种温度相关的trp亚型 htrpa1和htrpv1的选择性情况。许多trp配体具有相反的行为,例如,trpm8激动剂薄荷醇阻断trpv1和
trpa1,而在较低浓度下激活trpa1。同样,trpv1激动剂辣椒素能够抑制trpm8介导的响应。另一方面,trpv1拮抗剂辣椒平、bctc和sb
‑
452533等表现出 trpm8的剂量依赖性阻断。这些研究表明配体识别在trpm8、trpa1 和trpv1之间重叠。与trpm8类似,trpa1在体外和体内均被低温激活,尽管在略微更低的温度下。在ca
2+
通量测定法中,icilin也在μm 浓度下激活trpa1。
[0257]
在呈现的trpa1 ca
2+
通量测定法中,trpa1激动剂aitc的剂量响应研究提供了7.62
±
0.89μm的ec
50
(图20),与以前的研究相一致。在所述测定法中用作标准品和阳性对照的trpa1拮抗剂钌红剂量依赖性地阻断aitc(10μm)激活的[ca
2+
]
i
释放,ic
50
为162
±
33nm (剂量响应曲线示出在图21中),在与klionsky及其同事报道的相同的范围内,他们报道了针对80μm aitc的作用ic
50
为29
±
6nm。对于trpv1来说,trpv1激动剂辣椒素(ec
50 19
±
2.5nm,图22)和拮抗剂辣椒平(ic
50 451
±
48nm,图23)的ec
50
和ic
50
值与el kouhen 等人报道的值相近。包含在图20
‑
23中的曲线以
±
95%置信区间列出。
[0258]
表s1.trpa1激动剂数据(归一化到e
max
对照的活化百分率)。所有数据被归一化到参比激动剂aitc的e
max
。
[0259][0260]
*
n=10
[0261]
表s2.trpa1拮抗剂数据(归一化到ec
80
对照的抑制百分率)。所有数据被归一化到参比激动剂aitc的ec
80
。
[0262]
[0263][0264]
表s3.trpv1激动剂数据(归一化到e
max
对照的活化百分率)。所有数据被归一化到参比激动剂辣椒素的e
max
。
[0265][0266]
*
n=10
[0267]
表s4.trpv1拮抗剂数据(归一化到ec
80
对照的抑制百分率)。所有数据被归一化到参比激动剂辣椒素的ec
80
。
[0268]
trpv1拮抗剂测定:辣椒平参比对照
[0269][0270]
在具有显著的trpm8拮抗剂活性的化合物中,除了化合物5、7 和11之外的所有类似物在对htrpv1和htrpa1两者的ca
2+
通量测定法中,在对应于它们的htrpm8 ic
50
值的大约2倍的浓度下和比前者值高10倍的浓度下均具有可忽略的固有(激动剂)和拮抗剂活性。具体来说,在所测试的两种浓度下,当归一化到参比激动剂aitc(300μm) 和辣椒素(3μm)的e
max
浓度时,所有化合物对htrpa1和htrpv1 均未显示出超过25%的活化。同样地,当用ec
80
浓度的aitc和辣椒素(分别为10μm和0.1μm)激惹时,这些类似物均不能抑制任一亚型超过25%。例如,即使在比其6
±
1nm的htrpm8 ic
50
值高17倍的浓度下,化合物10也不激活或抑制htrpa1或htrpv1。同样,化合物12、13、14和15在比它们的1.4
±
1nm、40
±
1nm、2.4
±
1.0nm 和16
±
1nm的htrpm8 ic
50
值分别高21、25、13和19倍的浓度下,不影响htrpa1和htrpv1介导的响应。因此,相比于相关温度敏感性trp,trpa1和trpv1,本系列中的许多化合物对trpm8具有至少10倍的选择性。
[0271]
表3.在ca
2+
通量测定法中确定的所选联苯基酰胺对trpa1和trpv1 受体的固有和拮抗剂功能活性
[0272]
[0273][0274]
a
数据被归一化到由500nm icilin引发的最大响应。
b
数据被归一化到分别对应于trpa1和trpv1激动剂aitc(300μm)和辣椒素(3μm) 的e
max
值的浓度。
c
数据被归一化到的aitc(10μm)和辣椒素(0.1 μm)的ec
80
。
[0275]
实施例7
‑
化合物14的全细胞膜片钳电生理学
[0276]
使用同族配体薄荷醇刺激通道,并用全细胞膜片钳电生理学进一步研究和验证了化合物14对htrpm8的拮抗剂活性(图7)。在膜片钳实验中,在转染的hek
‑
293细胞或表达trpm8的爪蟾卵母细胞中, trpm8被icilin的激活依赖于细胞外ca
2+
的存在,此外,icilin以高度可变的潜伏期和显著的脱敏激活通道,这种效应在使用薄荷醇时没有看到。考虑到这些因素,我们进一步探索了化合物14在htrpm8处抑制薄荷醇介导的响应的能力,正如在以前的出版物中详述的。与全细胞记录中ca
2+
和ph依赖性的icilin诱发的响应相反,薄荷醇在电压钳测定法中诱导trpm8的鲁棒激活,允许进行更好的比较研究。考虑到这些因素,评估了化合物14影响由激动剂薄荷醇诱导的电流的能力。
[0277]
与使用icilin的ca
2+
通量研究相一致,这种化合物以浓度依赖性方式抑制薄荷醇诱导的trpm8响应,ic
50
为64
±
4nm,证实化合物14 是一种真正且功能鲁棒的trpm8拮抗剂,具有在nm浓度下抑制由不同化学刺激引发的trpm8响应的能力。在同一种测定法中,化合物 14的拮抗剂活性比基于色胺的拮抗剂高6倍,与含有三个不稳定酯基团的β
‑
内酰胺拮抗剂具有相近的效力。尽管化合物14的ic
50
值不与公知的trpm8拮抗剂pbmc在这种测定法中的值(ic
50
:0.4
‑
0.6nm) 接近,但这种含有不稳定的酯和氨基甲酸酯基团的amtb的苯甲氧基
‑ꢀ
苯基甲基氨基甲酸酯类似物似乎作为化学探针的效应有限。pbmc在神经病理性疼痛的不同行为模型中给出可变的响应,并且在cipn模型中不能阻断冷敏化。总而言之,化合物14可以克服与不同化学激活剂相关的测定法特异的细微差别,当用icilin和薄荷醇两者激惹时,在 ca
2+
通量和全细胞膜片钳测定两者中表现出鲁棒且高效的拮抗剂活性。化合物14在药理学上已被充分表征,并且与其他小分子trpm8配体相比在许多测定法中具有trpm8活性,证实了它作为探测trpm8介导的药理学的化学工具的可行性。正如下文讨论的,化合物14与arg842 和tyr1005相互作用,所述残基也已显示与icilin和薄荷醇类似物 ws
‑
12结合。与这些残基的结合可能说明了化合物14为什么能够分别在ca
2+
通量和电生理学测定法中抑制icilin和薄荷醇介导的响应两者;然而,位点特异性诱变研究可以提供进一步的见解。
[0278]
实施例8
‑
化合物14和htrpm8
[0279]
接下来进行实验,通过进行100ns md模拟,使化合物14在人类 trpm8同源性模型的背景中的强效拮抗剂活性合理化。简单来说,对 htrpm8中的高效拮抗剂螺[4.5]癸
‑8‑
基
化合物14进行100ns md模拟。如图8c中所示,发现htrpm8(约)和化合物14的 rmsd在30ns后均保持稳定,表明100ns的时间尺度是合理的。
[0280]
如图8a中所示,化合物14的环戊基与下方s4螺旋内保守的 arg842(s4,侧链,)和ile846(s4,)残基形成强疏水相互作用,类似于化合5和7的环庚基和环辛基(图6)。在md模拟之前,联苯基接触trp螺旋中保守的leu1001(未示出)和tyr1005 (薄荷醇敏感的,)残基。图8b示出了在md模拟后化合物14 在trpm8中的结合位姿。如图8b中所示,观察到化合物14的联苯基与ile846/leu1001(3.3a,未示出)/tyr1005之间的相互作用在md期间保持稳定。ile846转而与联苯基发生疏水性接触,类似于leu1001和tyr1005。与leu1001和tyr1005的相互作用同样与化合物5和7的对接位姿相一致,正如以前讨论的。
[0281]
ile846、leu1001和tyr1005将联苯基锚定在vsld的底部中,在那里它比化合物1的联苯基埋藏得更深,再次表明这是这些化学型的激动剂相比于拮抗剂介导的行为的看似合理的基本原理。重要的是,在tyr1005与联苯基之间观察到的疏水相互作用在amg2850的md后位姿中也被看到。正如前面讨论的,这个残基也通过极性相互作用接触ws
‑
12和icilin,强化了tyr1005作为配体识别的共同trpm8残基的观点。与化合物1和ws
‑
12不同,含芳香族基团在vsld中不重叠。
[0282]
令人吃惊的是,已发现螺[4.5]癸
‑8‑
基维持与arg842的疏水接触,尽管具有环己基环。与ile846、leu1001和tyr1005一起,关键残基的能量分解进一步支持了这四个残基可能比其他残基对化合物14在 trpm8中的识别贡献更大的观点,如图8d中所示。arg842代表了通过以前对amg2850的cryo
‑
em研究和md研究所表明的用于小分子结合的另一个共同残基,相对于薄荷醇结合位点在vsld的相反一侧上,接近结合的ca
2+
离子并与s2
‑
s3螺旋中的残基配位。这迫使所述分子进入伸展构型。vsld正构位点的这个区域(下方s2螺旋和s3
‑
s4 螺旋)含有多个疏水和极性残基,并且可能偏好性地容纳我们的联苯基酰胺系列化合物上的较大疏水性取代,例如在我们的强效纳摩尔拮抗剂/化合物5、7和10
‑
15与s1和上方s2螺旋中的薄荷醇结合区域的比较中看到的,为我们通过实验观察到的sar趋势提供了结构背景。据报道,这附近的残基(glu782、arg842(trpm8
fa
中的arg841)和 his845(trpm8
fa
中的his844)等)采纳多种构象,允许trpm8结合 ws
‑
12和icilin两者。
[0283]
大体积残基例如距螺环己基3.6和的trp798(s3)和his845 (s4)的存在,可能在空间上排斥化合物8和9的十氢萘
‑1‑
基和四氢萘
ꢀ‑1‑
基环,与我们的系列化合物中在该区域具有更大程度的构象灵活性(如在化合物5和7中)或更适合的双环排布(化合物10
‑
14)的其他类似物相比,将它们的trpm8效力有效地降低到μm范围。
[0284]
有趣的是,化合物14不与arg1008相互作用(在化合物1、5和 7的情况下)或形成氢键,而是在结合腔内形成广泛的疏水性接触,类似于在最近报道的与拮抗剂amtb和jnj41876666/tc
‑
i 2014结合的鹦鹉(parus major)trpm8(pmtrpm8)的结构(分别为pdb 6o6r和 6o72)中看到的。化合物14的md后位姿与jnj41876666/tc
‑
i 2014 复合结构的比较揭示出两种拮抗剂的联苯基在vsld内重叠,支持了我们的md结果,而含螺环的组成部分在口袋中取向相反。观察到的化合物14的螺[4.5]癸
‑8‑
基相比于jnj41876666/tc
‑
i 2014的
螺
‑
异噁唑啉的相反取向分别归因于任一基团从酰胺(三角平面几何形状,120
°
) 相比于构象刚性的苯并咪唑的突出。
[0285]
实施例9
‑
对trpa1和trpv1的计算机模拟选择性情况分析
[0286]
为了解释化合物14的选择性情况,将该化合物对接到rtrpv1 (pdb 3j5r)和htrpa1(pdb 3j9p)的cryo
‑
em结构中,并将这些位姿与htrpm8同源性模型中的md前(对接的)位姿进行比较。有趣的是,trpm8、trpv1和trpa1的结合口袋占据vlsd(s1
‑
s4)、由s5
‑
s6形成的孔结构域和孔螺旋的不同区域(图9)。香草酸配体树脂胶毒素(rtx)这种辣椒素样高香草基酯拮抗剂和竞争性拮抗剂辣椒平以和结合到s3和s4螺旋以及s4
‑
s5连接物中的trpv1 残基。与结合口袋被定义在s1
‑
s4螺旋和trp螺旋内的禽类trpm8 的结合有配体的cryo
‑
em结构合在一起,这些结构表明对于两种trp 亚型来说,对结构完全不同的天然产物配体(分别为薄荷醇和辣椒素) 不存在中心结合位点。相反,这些分子结合到每种通道的vsld内的不同区域。尽管trpa1的结构不带有配体但关键的phe909 残基的cryo
‑
em以及诱变研究表明天然产物激动剂异硫氰酸烯丙酯 (aitc)和拮抗剂a
‑
967079结合在由s5、s6和孔螺旋中的残基所定义的位点中,再次表明来自于自然界的原型trp通道激动剂结合到它们相应亚型上的不同口袋。
[0287]
为了解释所述化合物的选择性,将化合物14对接到trpa1和 trpv1,并将这些结果与化合物14在trpm8上的对接位姿(md前) (在trpm8上的对接能为
‑
9.9kcal/mol)进行比较。如图9c中所示,所述对接位姿显示化合物14与trpm8形成广泛相互作用。几个重要残基对化合物14的结合有贡献,包括trp798、arg842、his845、ile846、 leu1001和tyr1005。图9b示出了化合物14与trpa1之间的相互作用。trpa1的结合口袋揭示出由s5、s6和第一孔螺旋,包括phe909 (孔螺旋1)、leu881(s5)、ile878(s5)、phe877(s5)和thr874 (s5)形成的口袋内的独特密度,这与报道的结合位点相一致。通过分析所述相互作用,发现thr874与化合物14形成氢键,而phe909、leu881、 ile878和leu871对疏水相互作用有贡献。图9d示出了化合物14在 trpv1中的结合位姿。trpv1中的口袋由来自于两个相邻单体的5个跨膜结构域形成,包括s3、s4、s4
‑
s5连接物、s5和s6。所述结合口袋内的几个重要残基示出在图9d中,包括tyr511(s3)、leu515(s3)、 leu574(s4)、thr550(s4)、arg557(s4
‑
s5连接物)、glu570(第一单体的s5)和leu672(第二单体的s6)。已发现thr550与化合物 14形成强氢键,而leu515和leu574与化合物14形成疏水性接触。化合物14在trpm8、trpa1和trpv1上的对接能是
‑
9.9kcal/mol、
‑
7.1 kcal/mol和
‑
8.3kcal/mol,表明化合物14应该偏好性地与trpm8结合。从表3中的高通量flipr分析看到,化合物14对trpm8相比于trpa1 和trpv1具有适度选择性(13倍)。
[0288]
在小鼠肝微粒体中进行了化合物14的代谢稳定性测试,以确定它在体内作为trpm8化学探针的适合性。化合物14在小鼠肝微粒体中具有30min的半衰期(t
1/2
),并且内在清除率(cl
int
)为0.0455 ml/min/mg;表明了足以进行行为测定法的代谢稳定性(表s5)。化合物14可能经历螺环或芳香环的cyp450羟基化,导致t
1/2
=30min。
[0289]
表s5.化合物14在小鼠肝微粒体中的稳定性
[0290][0291]
a
内在清除率(cl
int
)在cl
int
=k/p的基础上计算,其中k是消除速率常数,p是温育中的蛋白质浓度。
[0292]
实施例10
‑
体内分析
[0293]
湿狗样抖动(wds)测定法。为了确定观察到的化合物14在体外有效抑制trpm8活性的能力是否也转化为体内trpm8依赖性抗伤害感受性活性,进行了“湿狗样抖动”(wds)测定法。在这种测定法中,将icilin(10mg/kg,腹膜内,i.p.)注射到用化合物14或介质治疗的小鼠中。在小鼠中,已知trpm8与已用于体外测定法的大鼠 trpm8具有高度同源性。icilin在小鼠中的注射产生鲜明且可量化的 trpm8介导的抖动行为。化合物14(1、30和50mg/kg)或其介质在 icilin注射之前30分钟皮下(s.c.)给药。
[0294]
冷异常性疼痛。越来越多的证据表明trpm8在由奥沙利铂(oxp) 诱发的化疗诱导的神经病理性疼痛的小鼠模型中发挥作用,这是一种模拟由化疗诱导的外周神经病变(cipn)引起的冷超敏性的病症。急性和慢性oxp诱导的冷超敏性两者已在大鼠中重现,并与trpm8表达和功能相关联。mizoguchi等人报道,在啮齿动物模型中,oxp注射后的急性冷异常性疼痛被trpm8阻断剂n
‑
(2
‑
氨基乙基)
‑
n
‑
[4
‑
(苯甲氧基)
‑3‑
甲氧基苯甲基]
‑
n
’‑
(1s)
‑1‑
(苯基)乙基]脲和tc
‑
i 2014减轻。根据这些发现,使用丙酮作为冷刺激,研究了化合物14在oxp诱导的冷异常性疼痛模型中的效果。考虑到在oxp处理的患者中冷疼痛阈值从≈12℃提高到≈26℃,丙酮刺激被认为在oxp处理的小鼠中诱发疼痛。
[0295]
如图10中所示,化合物14产生显著的、剂量依赖性的抗伤害感受行为。在50mg/kg的最高剂量下,化合物14在小鼠中抑制wds样冷超敏性,具有与使用标准止痛剂量的加巴喷丁(25mg/kg,s.c.)时观察到的可比的功效。
[0296]
这些结果将化合物14在ca
2+
通量和膜片钳测定法中的拮抗剂活性与在完整动物模型中的trpm8在机制上联系在一起,因为在trpm8 失活小鼠中icilin诱导的wds行为不可重现。该数据证实了化学或药理学探针分子的关键属性。
[0297]
包括trpm8、trpa1、trpv1、trpv2和trpv4在内的温度敏感性trp在文献中被描述为是用于治疗化疗诱导的外周神经病变 (cipn)的潜在新靶点。对寒冷的感官知觉的缺陷表现为冷异常性疼痛,其被定义为从通常非疼痛性冷刺激经历疼痛,以及冷痛觉过敏这种从疼痛性冷刺激引起的疼痛反应加剧等。在临床上,此类冷缺陷可见于化疗诱导的异常性疼痛、神经病理性疼痛、复杂的局部疼痛综合征和膀胱疼痛综合征。对冷暴露的异常急性和感官反应发生在用化疗药剂奥沙利铂的第一轮治疗之后,所述奥沙利铂是用于结肠直肠癌等
的最常用抗肿瘤治疗;此外,奥沙利铂沉淀物提高对薄荷醇的敏感度,可能是由于trpm8的过表达或活性。值得注意的是,结肠直肠癌是癌症死亡的第二大原因,也是第四大最常见的恶性疾病。作为奥沙利铂治疗的结果出现冷敏感
‑
感觉异常和导致吞咽困难的咽部痉挛,它们代表了与奥沙利铂相关的感觉神经毒性(snt)。此外,已知用于治疗肺癌、睾丸癌和卵巢癌的所有铂类药物包括顺铂、卡铂和奥沙利铂,都诱导感觉神经病变。
[0298]
温度痛觉过敏是奥沙利铂神经毒性在早期发作时的临床标志物,可以预测严重的神经病变。冷超敏性是奥沙利铂诱导的神经病变的标志。正如通过敲除研究证实的,在临床前,奥沙利铂诱导的对无害和有害冷刺激的超敏性通过trpm8依赖性机制产生。使用双功能 trpm8/trpv1拮抗剂辣椒平的trpm8阻断在体内剂量依赖性地抑制奥沙利铂诱导的冷异常性疼痛,这种作用在使用trpv1拮抗剂5
′‑
碘代树脂胶毒素时未看到。类似地,在单次注射奥沙利铂引起的冷异常性疼痛后,drg中trpm8 mrna的表达显著提高,这种效应在功能上与体内对trpm8刺激的响应增加有关。这些研究与之前的文献一致,之前的文献报道了在通过奥沙利铂治疗和奥沙利铂代谢物草酸盐治疗诱导冷痛觉过敏后,l4
‑
l6 drg中trpm8 mrna的表达类似地提高。在体外,在奥沙利铂治疗的drg神经元中,trpm8 mrna水平也显著提高。在奥沙利铂诱导的外周神经病理性疼痛模型中评估了化合物 14阻断对冷的感觉应答的能力,因为冷超敏性是奥沙利铂诱导的神经病变的标志。尽管使用新的和更有针对性的化学疗法在癌症治疗中取得了进展,但目前还没有可用于cipn的药物疗法。用于糖尿病性神经病变的度洛西汀对奥沙利铂诱导的cipn患者只有轻度镇痛作用。
[0299]
在c57/bl6小鼠中,在三次腹膜内注射oxp(6mg/kg)后7天,在发生冷异常性疼痛时评估了化合物14的活性。在化合物14的单次皮下给药(0.1和1μg)后,减弱的冷异常性疼痛在15min时变得明显,并在给药后30min达到最大抑制(图11),并采取剂量依赖性方式。这一数据表明化合物14可能是用于治疗cipn的可行的治疗性支架。
[0300]
在同一测定法中,化合物14的抗伤害感受活性超过另一种已报道的高效trpm8拮抗剂(r)
‑
(
‑
)
‑
10e。(r)
‑
(
‑
)
‑
10e抑制奥沙利铂诱导的疼痛反应性舔爪,尽管在p.o.给药时剂量高出>10,000倍。同样,在c57/bl6 小鼠中基于色氨酸的trpm8拮抗剂在与化合物14相同的剂量下逆转奥沙利铂诱导的冷异常性疼痛,然而它的作用持续时间短,可能是由于不稳定的酯基团。在等于两个t
1/2
值的60分钟时,化合物14显著抑制oxp效应,表明存在其他的现象。例如,化合物14可能在体内通过由其亲脂性赋予的药物贮积效应发挥作用。同样重要的是,化合物14和本文中报告的其他薄荷醇样拮抗剂,可能是在体内探索trpm8 在其他疼痛状态例如慢性神经病理性疼痛中的作用的有用化学工具,该离子通道对这种疼痛的作用是有争议的。此类小分子支架然后可以为感觉神经病变提供药物治疗。
[0301]
简而言之,正如通过本文中所描述并在上述人类trpm8同源性模型中进行的trpm8拮抗剂支架的计算研究所指示的,探测用亲脂性组成部分代替化合物1的(
‑
)
‑
薄荷基环,允许发现在ca
2+
通量测定法中具有高效htrpm8拮抗剂活性并且相比于trpv1和trpa1具有>10倍选择性的一系列新型小分子配体。这些薄荷醇优化的类似物可用作化学探针,与dendreon(d
‑
3263等)和proctor&gamble所报道的对人类trpm8具有纳摩尔激动剂活性的基于薄荷醇的激动剂一起用于调查trpm8药理学、结构
‑
功能研究和结构生物学研究。这一系列化合物还可能为奥沙利铂诱导的cipn和其他与trpm8相关的感觉神经病变的药物治疗提供可能性,因为化合物14能够在体内减弱奥沙利铂诱导的冷异常性疼痛。此外,这些化合物
可能还有助于trpm8药效团的鉴定,以合理设计小分子配体和治疗性支架。鉴定到的最有效的类似物之一(化合物14)在ca
2+
通量和膜片钳测定法两者中均具有优异的拮抗剂活性,并且可以在各种体外和体内测定法中剂量依赖性地抑制多种trpm8激活剂(icilin、薄荷醇和冷)的作用。化合物14很容易从酰胺化反应合成,并且不具有手性中心,因此提高了它的吸引力。化合物14是迄今为止描述的最有效的trpm8拮抗剂之一。上述sar 研究表明,与同源配体(
‑
)
‑
薄荷醇相比,它的螺[4.5]癸
‑8‑
基组成部分是 trpm8识别的优选支架,代表了最佳的薄荷醇替代物。本领域正在等待与薄荷醇衍生的拮抗剂复合的trpm8结构,以解决围绕通道激活与失活的微妙问题,特别是在基于天然产物的支架的情形中。化合物14 这种拮抗剂代表了这些研究的可行选择,以与薄荷醇类似物ws
‑
12一起,用于解析trpm8上的拮抗剂与激动剂介导的分子事件。
[0302]
本说明书中提及的所有出版物、专利和专利申请均通过参考并入本文,包括在下表中列出的参考文献:
[0303]
参考文献
[0304]
1.winchester,w.j.;gore,k.;glatt,s.;petit,w.;gardiner,j.c.; conlon,k.;postlethwaite,m.;saintot,p.p.;roberts,s.;gosset,j.r.; matsuura,t.;andrews,m.d.;glossop,p.a.;palmer,m.j.;clear,n.; collins,s.;beaumont,k.;reynolds,d.s.(2014)在人类冷加压试验中 trpm8通道的抑制降低疼痛(inhibition of trpm8 channels reduces pain in the cold pressor test in humans),j.pharmacol.exp.ther.351, 259
‑
269.
[0305]
2.kobayashi,k.;fukuoka,t.;obata,k.;yamanaka,h.;dai,y.; tokunaga,a.;noguchi,k.(2005)trpm8、trpa1和trpv1 mrna在具有adelta/c纤维的大鼠初级传入神经元中的不同表达和与trk受体的共定位(distinct expression of trpm8,trpa1,and trpv1 mrnas in rat primary afferent neurons with adelta/c
‑
fibers and colocalization with trk receptors),j.comp.neurol.493,596
‑
606.
[0306]
3.proudfoot,c.j.;garry,e.m.;cottrell,d.f.;rosie,r.; anderson,h.;robertson,d.c.;fleetwood
‑
walker,s.m.;mitchell,r. (2006)在慢性神经病理性疼痛中由trpm8冷受体介导的镇痛作用 (analgesia mediated by the trpm8 cold receptor in chronic neuropathic pain),curr.biol.16,1591
‑
1605.
[0307]
4.mckemy,d.d.;neuhausser,w.m.;julius,d.(2002)冷受体的鉴定揭示出trp通道在温度感觉中的普遍作用(identification of a cold receptor reveals a general role for trp channels in thermosensation), nature 416,52
‑
58.
[0308]
5.janssens,a.;voets,t.(2011)冷和薄荷醇激活的通道trpm8 的配体化学计量学(ligand stoichiometry of the cold
‑
and menthol
‑
activated channel trpm8),j.physiol.589,4827
‑
4835.
[0309]
6.perez de vega,m.j.;gomez
‑
monterrey,i.;ferrer
‑
montiel,a.; gonzalez
‑
muniz,r.(2016)瞬时受体电位melastatin 8通道(trpm8) 调节:治疗疼痛和癌症的冷入口(transient receptor potential melastatin 8channel(trpm8)modulation:cool entryway for treating pain and cancer),j.med.chem.59,10006
‑
10029.
[0310]
7.yin,y.;wu,m.;zubcevic,l.;borschel,w.f.;lander,g.c.; lee,s.y.(2017)
blockade of trpm8 ion channels alters cold and cold pain responses in mice),plos one 6,e25894.
[0336]
33.andersson,d.a.;chase,h.w.;bevan,s.(2004)trpm8被薄荷醇、icilin和冷的激活受细胞内ph的差异调节(trpm8 activation by menthol,icilin,and cold is differentially modulated by intracellular ph), j.neurosci.24,5364
‑
5369.
[0337]
34.andersson,d.a.;nash,m.;bevan,s.(2007)溶血磷脂和多不饱和脂肪酸对冷激活通道trpm8的调节(modulation of the cold
‑
activated channel trpm8 by lysophospholipids and polyunsaturated fatty acids),j.neurosci.27,3347
‑
3355.
[0338]
35.hilton,j.k.;salehpour,t.;sisco,n.j.;rath,p.;van horn,w. d.(2018)trp的磷酸肌醇相互作用调节剂(pirt)对人类和小鼠 trpm8离子通道具有相反的作用(phosphoinositide
‑
interacting regulator of trp(pirt)has opposing effects on human and mouse trpm8 ion channels),j.biol.chem.293,9423
‑
9434.
[0339]
36.bertamino,a.;ostacolo,c.;ambrosino,p.;musella,s.;di sarno,v.;ciaglia,t.;soldovieri,m.v.;iraci,n.;fernandez carvajal,a.; de la torre
‑
martinez,r.;ferrer
‑
montiel,a.;gonzalez muniz,r.; novellino,e.;taglialatela,m.;campiglia,p.;gomez
‑
monterrey,i.(2016) 基于色胺的衍生物作为瞬时受体电位melastatin 8型(trpm8)通道的调节剂(tryptamine
‑
based derivatives as transient receptor potential melastatin type 8(trpm8)channel modulators),j.med.chem.59, 2179
‑
2191.
[0340]
37.de la torre
‑
martinez,r.;bonache,m.a.;llabres
‑
campaner,p. j.;balsera,b.;fernandez
‑
carvajal,a.;fernandez
‑
ballester,g.; ferrer
‑
montiel,a.;perez de vega,m.j.;gonzalez
‑
muniz,r.(2017)作为trpm8拮抗剂的β
‑
内酰胺衍生物的合成、高通量筛选和药理学表征 (synthesis,high
‑
throughput screening and pharmacological characterization of beta
‑
lactam derivatives as trpm8 antagonists),sci. rep.7,10766.
[0341]
38.bertamino,a.;iraci,n.;ostacolo,c.;ambrosino,p.;musella, s.;di sarno,v.;ciaglia,t.;pepe,g.;sala,m.;soldovieri,m.v.;mosca, i.;gonzalez
‑
rodriguez,s.;fernandez
‑
carvajal,a.;ferrer
‑
montiel,a.; novellino,e.;taglialatela,m.;campiglia,p.;gomez
‑
monterrey,i.(2018) 具有体内镇痛活性的基于色氨酸的强效trpm8拮抗剂的鉴定(identification of a potent tryptophan
‑
based trpm8 antagonist with in vivo analgesic activity),j.med.chem.61,6140
‑
6152.
[0342]
39.wang,l.;fu,t.m.;zhou,y.;xia,s.;greka,a.;wu,h.(2018) 人类trpm2的结构和门控机制(structures and gating mechanism of human trpm2),science 362,eaav4809.
[0343]
40.de petrocellis,l.;ligresti,a.;schiano moriello,a.;iappelli, m.;verde,r.;stott,c.g.;cristino,l.;orlando,p.;di marzo,v.(2013) 非thc大麻素类物质在体外和体内抑制前列腺癌生长:促凋亡作用和潜在机制(non
‑
thc cannabinoids inhibit prostate carcinoma growth in vitro and in vivo:pro
‑
apoptotic effects and underlying mechanisms),br. j.pharmacol.168,79
‑
102.
[0344]
41.ha,m.a.;smith,g.j.;cichocki,j.a.;fan,l.;liu,y.s.; caceres,a.i.;jordt,s.e.;morris,j.b.(2015)在暴露于香烟烟雾的小鼠中薄荷醇减弱呼吸道刺激并提高血液可的宁水平(menthol attenuates respiratory irritation and elevates blood cotinine in cigarette smoke exposed mice),plos one 10,e0117128.
[0345]
42.tamayo,n.a.;bo,y.;gore,v.;ma,v.;nishimura,n.;tang, p.;deng,h.;klionsky,l.;lehto,s.g.;wang,w.;youngblood,b.;chen, j.;correll,t.l.;bartberger,m.d.;gavva,n.r.;norman,m.h.(2012) 稠合哌啶作为一类新的强效且可口服利用的瞬时受体电位melastatin 8 型(trpm8)拮抗剂(fused piperidines as a novel class of potent and orally available transient receptor potential melastatin type 8(trpm8) antagonists),j.med.chem.55,1593
‑
1611.
[0346]
43.ohmi,m.;shishido,y.;inoue,t.;ando,k.;fujiuchi,a.; yamada,a.;watanabe,s.;kawamura,k.(2014)作为选择性和具有口服活性的trpm8拮抗剂的新的2
‑
吡啶基
‑
苯磺酰胺衍生物 rq
‑
00203078的鉴定(identification of a novel 2
‑
pyridyl
‑
benzensulfonamide derivative,rq
‑
00203078,as a selective and orally active trpm8 antagonist),bioorg.med.chem.lett.24, 5364
‑
5368.
[0347]
44.caceres,a.i.;liu,b.;jabba,s.v.;achanta,s.;morris,j.b.; jordt,s.e.(2017)瞬时受体电位阳离子通道亚家族m成员8介导桉油精的抗炎作用(transient receptor potential cation channel subfamily m member 8channels mediate the anti
‑
inflammatory effects of eucalyptol), br.j.pharmacol.174,867
‑
879.
[0348]
45.dodziuk,h.;jaszunski,m.;schilf,w.(2005)反式和顺式十氢萘中的1h和13c nmr化学位移和自旋
‑
自旋耦合常数(1h and 13c nmr chemical shifts and spin
‑
spin coupling constants in trans
‑
and cis
‑
decalins),magn.reson.chem.43,639
‑
646.
[0349]
46.browne,l.m.;klinck,r.e.;stothers,j.b.(1979)carbon
‑
13 nmr studies:82.carbon
‑
13spectra of several几种10
‑
甲基
‑
顺
‑ꢀ
十氢萘的碳
‑
13波谱:一些顺
‑
十氢萘衍生物的构象偏好(carbon
‑
13 spectra of several 10
‑
methyl
‑
cis
‑
decalins.conformational preferences of some cis
‑
decalin derivatives),org.magn.reson.12,561
‑
568.
[0350]
47.player,m.r.;parks,d.j.;parsons,w.;meegalla,s.k.;illig,c. r.;ballentine,s.k.作为trpm8调节剂的杂环苯并咪唑类化合物 (heterocyclic benzimidazoles as trpm8 modulators),us 20100093788 a1.
[0351]
48.chaudhari,s.s.;kadam,a.b.;khairatkar
‑
joshi,n.; mukhopadhyay,i.;karnik,p.v.;raghuram,a.;rao,s.s.;vaiyapuri,t. s.;wale,d.p.;bhosale,v.m.;gudi,g.s.;sangana,r.r.;thomas,a. (2013)作为trpm8拮抗剂的新的n
‑
芳基
‑
3,4
‑
二氢
‑
1'h
‑
螺[色烯
‑
2,4'
‑ꢀ
哌啶]
‑
1'
‑
甲酰胺的合成和药理学评估(synthesis and pharmacological evaluation of novel n
‑
aryl
‑
3,4
‑
dihydro
‑
1'h
‑
spiro[chromene
‑
2,4'
‑
piperidine]
‑
1'
‑
carboxamides as trpm8 antagonists),bioorg.med.chem.21,6542
‑
6553.
[0352]
49.shishido,y.;ohmi,m.;ando,k.作为trpm8拮抗剂的氮杂螺衍生物的制备(preparation of azaspiro derivatives as trpm8antagonists),wo 2015136947 a1.
[0353]
50.klein,a.h.;iodi carstens,m.;mccluskey,t.s.;blancher,g.;simons,
activated by cold temperatures),cell 112,819
‑
829.
[0362]
59.karashima,y.;talavera,k.;everaerts,w.;janssens,a.;kwan, k.y.;vennekens,r.;nilius,b.;voets,t.(2009)trpa1在体外和体内充当冷感受蛋白(trpa1 acts as a cold sensor in vitro and in vivo),proc. natl.acad.sci.u s a 106,1273
‑
1278.
[0363]
60.mcnamara,c.r.;mandel
‑
brehm,j.;bautista,d.m.;siemens, j.;deranian,k.l.;zhao,m.;hayward,n.j.;chong,j.a.;julius,d.; moran,m.m.;fanger,c.m.(2007)trpa1介导福尔马林诱导的疼痛 (trpa1 mediates formalin
‑
induced pain),proc.natl.acad.sci.u s a 104,13525
‑
13530.
[0364]
61.klionsky,l.;tamir,r.;gao,b.;wang,w.;immke,d.c.; nishimura,n.;gavva,n.r.(2007)三氟(硫烷基)乙基苯甲酰胺作为瞬时受体电位锚蛋白1(trpa1)拮抗剂的物种特异性药理学 (species
‑
specific pharmacology of trichloro(sulfanyl)ethyl benzamides as transient receptor potential ankyrin 1(trpa1)antagonists),mol.pain 3, 39.
[0365]
62.el kouhen,r.;surowy,c.s.;bianchi,b.r.;neelands,t.r.; mcdonald,h.a.;niforatos,w.;gomtsyan,a.;lee,c.h.;honore,p.; sullivan,j.p.;jarvis,m.f.;faltynek,c.r.(2005)新型选择性瞬时受体电位v1型受体拮抗剂a
‑
425619[1
‑
异喹啉
‑5‑
基
‑3‑
(4
‑
三氟甲基
‑
苯甲基)
‑
脲]阻断通道被香草酸类化合物、热和酸的激活(a
‑
425619 [1
‑
isoquinolin
‑5‑
yl
‑3‑
(4
‑
trifluoromethyl
‑
benzyl)
‑
urea],a novel and selective transient receptor potential type v1 receptor antagonist,blocks channel activation by vanilloids,heat,and acid),j.pharmacol.exp.ther. 314,400
‑
409.
[0366]
63.diver,m.m.;cheng,y.;julius,d.(2019)对trpm8抑制和脱敏的结构洞察(structural insights into trpm8 inhibition and desensitization),science 365,1434
‑
1440.
[0367]
64.gao,y.;cao,e.;julius,d.;cheng,y.(2016)纳米盘中的 trpv1结构揭示出配体和脂质作用的机制(trpv1 structures in nanodiscs reveal mechanisms of ligand and lipid action),nature 534, 347
‑
351.
[0368]
65.paulsen,c.e.;armache,j.p.;gao,y.;cheng,y.;julius,d. (2015)trpa1离子通道的结构表明了调控机制(structure of the trpa1 ion channel suggests regulatory mechanisms),nature 525,552.
[0369]
66.wei,e.t.(1983)在大鼠中通过胆碱能和肾上腺素能药剂的中枢给药抑制抖动(inhibition of shaking movements in rats by central administration of cholinergic and adrenergic agents),psychopharmacology (berl)81,111
‑
114.
[0370]
67.wei,e.t.;seid,d.a.(1983)ag
‑3‑
5:一种产生冷感觉的化学物质(ag
‑3‑
5:a chemical producing sensations of cold),j.pharm. pharmacol.35,110
‑
112.
[0371]
68.colburn,r.w.;lubin,m.l.;stone,d.j.,jr.;wang,y.; lawrence,d.;d'andrea,m.r.;brandt,m.r.;liu,y.;flores,c.m.;qin, n.(2007)在trpm8失活小鼠中冷敏感性减弱(attenuated cold sensitivity in trpm8 null mice),neuron 54,379
‑
386.
[0372]
69.kono,t.;satomi,m.;suno,m.;kimura,n.;yamazaki,h.; furukawa,h.;
matsubara,k.(2012)奥沙利铂诱导的神经毒性涉及在对冷感觉的急性超敏感性的机制中的trpm8(oxaliplatin
‑
induced neurotoxicity involves trpm8 in the mechanism of acute hypersensitivity to cold sensation),brain behav.2,68
‑
73.
[0373]
70.ling,b.;authier,n.;balayssac,d.;eschalier,a.;coudore,f. (2007)大鼠中奥沙利铂诱导的疼痛性神经病变的行为和药理描述 (behavioral and pharmacological description of oxaliplatin
‑
induced painful neuropathy in rat),pain 128,225
‑
234.
[0374]
71.mizoguchi,s.;andoh,t.;yakura,t.;kuraishi,y.(2016)在小鼠中c
‑
myc介导的瞬时受体电位melastati 8表达参与奥沙利铂诱导的冷异常性疼痛(involvement of c
‑
myc
‑
mediated transient receptor potential melastati 8expression in oxaliplatin
‑
induced cold allodynia in mice),pharmacol.rep.68,645
‑
648.
[0375]
72.deuis,j.r.;dvorakova,l.s.;vetter,i.(2017)用于在啮齿动物中评估疼痛行为的方法(methods used to evaluate pain behaviors inrodents),front.mol.neurosci.10,284。
[0376]
73.naziroglu,m.;braidy,n.(2017)温度敏感性trp通道:用于治疗化疗诱导的外周疼痛的新靶点(thermo
‑
sensitive trp channels: novel targets for treating chemotherapy
‑
induced peripheral pain),front. physiol.8,1040.
[0377]
74.jensen,t.s.;finnerup,n.b.(2014)神经病理性疼痛中的异常性疼痛和痛觉过敏:临床表现和机制(allodynia and hyperalgesia in neuropathic pain:clinical manifestations and mechanisms),lancet neurol. 13,924
‑
935.
[0378]
75.binder,a.;stengel,m.;maag,r.;wasner,g.;schoch,r.; moosig,f.;schommer,b.;baron,r.(2007)奥沙利铂诱导的神经病变中的疼痛——外周和中枢伤害感受系统中的敏化(pain in oxaliplatin
‑
induced neuropathy
‑‑
sensitisation in the peripheral and central nociceptive system),eur.j.cancer.43,2658
‑
2663.
[0379]
76.attal,n.;bouhassira,d.;gautron,m.;vaillant,j.n.;mitry,e.; lepere,c.;rougier,p.;guirimand,f.(2009)温度痛觉过敏作为奥沙利铂神经毒性的标志物:前瞻性量化感官评估研究(thermal hyperalgesia as a marker of oxaliplatin neurotoxicity:a prospective quantified sensory assessment study),pain 144,245
‑
252.
[0380]
77.grothey,a.(2003)奥沙利铂安全性情况分析:神经毒性(oxaliplatin
‑
safety profile:neurotoxicity),semin.oncol.30,5
‑
13.
[0381]
78.kelland,l.(2007)基于铂的癌症化疗的复兴(the resurgence of platinum
‑
based cancer chemotherapy),nat.rev.cancer 7,573
‑
584.
[0382]
79.descoeur,j.;pereira,v.;pizzoccaro,a.;francois,a.;ling,b.; maffre,v.;couette,b.;busserolles,j.;courteix,c.;noel,j.;lazdunski, m.;eschalier,a.;authier,n.;bourinet,e.(2011)奥沙利铂诱导的冷超敏是由伤害感受器中离体通道表达的重塑造成的(oxaliplatin
‑
induced cold hypersensitivity is due to remodelling of ion channel expression in nociceptors),embo mol.med.3,266
‑
278.
[0383]
80.gauchan,p.;andoh,t.;kato,a.;kuraishi,y.(2009)在小鼠中瞬时受体电位
melastatin 8的提高的表达参与奥沙利铂诱导的冷异常性疼痛(involvement of increased expression of transient receptor potential melastatin 8in oxaliplatin
‑
induced cold allodynia in mice),neurosci.lett.458,93
‑
95.
[0384]
81.kawashiri,t.;egashira,n.;kurobe,k.;tsutsumi,k.; yamashita,y.;ushio,s.;yano,t.;oishi,r.(2012)在大鼠中l型 ca(2)+通道阻断剂阻止奥沙利铂诱导的冷痛觉过敏和trpm8过表达(l type ca(2)+channel blockers prevent oxaliplatin
‑
induced cold hyperalgesia and trpm8 overexpression in rats),mol.pain 8,7.
[0385]
82.ta,l.e.;bieber,a.j.;carlton,s.m.;loprinzi,c.l.;low,p. a.;windebank,a.j.(2010)在小鼠中瞬时受体电位香草酸1对于顺铂诱导的热痛觉过敏来说是必需的(transient receptor potential vanilloid 1is essential for cisplatin
‑
induced heat hyperalgesia in mice),mol.pain 6, 15.
[0386]
83.staff,n.p.;grisold,a.;grisold,w.;windebank,a.j.(2017) 化疗诱导的外周神经病变:当前综述(chemotherapy
‑
induced peripheral neuropathy:a current review),ann.neurol.81,772
‑
781.
[0387]
84.shapiro,c.l.(2016)癌症患者及其幸存者生命质量管理的最新发现的亮点(highlights of recent findings on quality
‑
of
‑
life management for patients with cancer and their survivors),jama oncol. 2,1401
‑
1402.
[0388]
85.moran,m.m.;szallasi,a.(2018)靶向伤害感受性瞬时受体电位通道以治疗慢性疼痛:领域的现有状态(targeting nociceptive transient receptor potential channels to treat chronic pain:current state of the field),br.j.pharmacol.175,2185
‑
2203.
[0389]
86.yelm,k.e.;wos,j.a.;bunke,g.m.;frederick,h.;haught,j. c.;hoke,s.h.;sreekrishna,k.t.;lin,y.可以在消费品中用作增感剂的芳基环己烷甲酰胺衍生物的合成(synthesis of aryl cyclohexane carboxamide derivatives useful as sensates in consumer products), 20170057911a1.
[0390]
87.wos,j.a.;yelm,k.e.;bunke,g.m.;frederick,h.a.;reilly, m.;haught,j.c.;sreekrishna,k.t.;lin,y.可以在消费品中用作清凉增感剂的环己烷酯衍生物的合成(synthesis of cyclohexane ester derivatives useful as cooling sensates in consumer products),2017106279 a1.
[0391]
88.moreno,o.;natarajan,s.;duncan,d.f.trp
‑
p8活性的小分子调节剂(small
‑
molecule modulators of trp
‑
p8 activity),20080255185 a1.
[0392]
89.sybyl
‑
x;1.3tripos international,1699south hanley rd.st. louis,missouri,63144,usa.,2010.
[0393]
90.xie,x.q.;chen,j.z.;billings,e.m.(2003)g
‑
蛋白偶联的大麻素类cb2受体的3d结构模型(3d structural model of the g
‑
protein
‑
coupled cannabinoid cb2 receptor),proteins 53,307
‑
319.
[0394]
91.marti
‑
renom,m.a.;stuart,a.c.;fiser,a.;sanchez,r.;melo, f.;sali,a.(2000)基因和基因组的比较性蛋白质结构建模 (comparative protein structure modeling of genes and genomes),annu. rev.biophys.biomol.struct.29,291
‑
325.
[0395]
92.chen,j.z.;wang,j.;xie,x.q.(2007)用于cb2拮抗剂搜索的基于gpcr结构的虚拟筛选方法(gpcr structure
‑
based virtual screening approach for cb2 antagonist search),j.chem.inf.model.47, 1626
‑
1637.
[0396]
93.feng,z.;alqarni,m.h.;yang,p.;tong,q.;chowdhury,a.; wang,l.;xie,x.q.(2014)基于gpcr的已知晶体结构的大麻素受体2 结构的建模、分子动力学模拟和突变验证(modeling,molecular dynamics simulation,and mutation validation for structure of cannabinoid receptor 2based on known crystal structures of gpcrs),j.chem inf. model.54,2483
‑
2499.
[0397]
94.teramachi,j.;silbermann,r.;yang,p.;zhao,w.;mohammad, k.s.;guo,j.;anderson,j.l.;zhou,d.;feng,r.;myint,k.z.;maertz, n.;beumer,j.h.;eiseman,j.l.;windle,j.j.;xie,x.q.;roodman,g. d.;kurihara,n.(2016)阻断sequestosome 1/p62的zz结构域在体外抑制骨髓瘤生长和破骨细胞形成,并在体内诱导带有骨髓瘤的骨骼中剧烈的骨形成(blocking the zz domain of sequestosome1/p62 suppresses myeloma growth and osteoclast formation in vitro and induces dramatic bone formation in myeloma
‑
bearing bones in vivo),leukemia 30, 390
‑
398.
[0398]
95.feng,z.;pearce,l.v.;xu,x.;yang,x.;yang,p.;blumberg,p. m.;xie,x.q.(2015)来自于同源性建模、分子对接、分子动力学模拟、虚拟筛选和生物测定验证的对四聚体htrpv1的结构洞察(structural insight into tetrameric htrpv1 from homology modeling,molecular docking,molecular dynamics simulation,virtual screening,and bioassay validations),j.chem.inf.model.55,572
‑
588.
[0399]
96.wiederstein,m.;sippl,m.j.(2007)prosa
‑
web:用于识别蛋白质三维结构中的错误的交互式网络服务(prosa
‑
web:interactive web service for the recognition of errors in three
‑
dimensional structures of proteins),nucleic acids res.35,w407
‑
410.
[0400]
97.laskowski,r.a.;macarthur,m.w.;moss,d.s.;thornton,j. m.(1993)procheck:检查蛋白质结构的立体化学质量的程序 (procheck:a program to check the stereochemical quality of protein structures),journal of applied crystallography 26,283
‑
291.
[0401]
98.jain,a.n.(1996)对非共价蛋白质
‑
配体相互作用进行评分:为计算结合亲和性而调整的连续可微分函数(scoring noncovalent protein
‑
ligand interactions:a continuous differentiable function tuned to compute binding affinities),j.comput.aided mol.des.10,427
‑
440.
[0402]
99.maier,j.a.;martinez,c.;kasavajhala,k.;wickstrom,l.; hauser,k.e.;simmerling,c.(2015)ff14sb:从ff99sb提高蛋白质侧链和骨架参数的准确性(ff14sb:improving the accuracy of protein side chain and backbone parameters from ff99sb),j.chem.theory comput. 11,3696
‑
3713.
[0403]
100.dickson,c.j.;madej,b.d.;skjevik,a.a.;betz,r.m.; teigen,k.;gould,i.r.;walker,r.c.(2014)脂质14:安布尔脂质力场 (lipid14:the amber lipid force field),j.chem.theory comput.10, 865
‑
879.
atomic charges from a dielectric medium)the journal of physical chemistry 100,19824
–
19839.
[0415]
112.kollman,p.a.;massova,i.;reyes,c.;kuhn,b.;huo,s.; chong,l.;lee,m.;lee,t.;duan,y.;wang,w.;donini,o.;cieplak,p.; srinivasan,j.;case,d.a.;cheatham,t.e.,3rd(2000)计算复杂分子的结构和自由能:结合分子力学和连续介质模型(calculating structures and free energies of complex molecules:combining molecular mechanics and continuum models),acc.chem.res.33,889
‑
897.
[0416]
113.tsui,v.;case,d.a.(2000)广义波恩溶剂化模型在大分子模拟中的理论与应用(theory and applications of the generalized born solvation model in macromolecular simulations),biopolymers 56, 275
‑
291.
[0417]
114.bashford,d.;case,d.a.(2000)大分子溶剂化效应的广义波恩模型(generalized born models of macromolecular solvation effects), annu.rev.phys.chem.51,129
‑
152.
[0418]
115.sitkoff,d.;sharp,k.a.;honig,b.(1994)使用宏观溶剂模型准确计算水合自由能(accurate calculation of hydration free energies using macroscopic solvent models),the journal of physical chemistry 98 1978
–
1988.
[0419]
116.still,w.c.;tempczyk,a.;hawley,r.c.;hendrickson,t. (1990)用于分子力学和动力学的溶剂化的半分析处理(semianalytical treatment of solvation for molecular mechanics and dynamics),journal of the american chemical society 112,6127
–
6129.
[0420]
117.weiser,j.;shenkin,p.s.;still,w.c.(1999)来自于成对重叠的线性组合(lcpo)的近似原子表面(approximate atomic surfaces fromlinear combinations of pairwise overlaps(lcpo)),journal of computational chemistry 20,217
‑
230.
[0421]
118.hu,j.;feng,z.;ma,s.;zhang,y.;tong,q.;alqarni,m.h.; gou,x.;xie,x.q.(2016)大麻素受体亚型cb2的无活性和活性状态的差异和影响:从构象到药物发现(difference and influence of inactive and active states of cannabinoid receptor subtype cb2:from conformation to drug discovery),j.chem.inf.model.56,1152
‑
1163.
[0422]
应当理解,本文公开的主题内容的各种不同细节可以被改变,而不背离本文公开的主题内容的范围。此外,前述描述仅用于说明的目的,而不是用于限制的目的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1