用于治疗细菌性尿路感染的吉泊达星的制作方法
用于治疗细菌性尿路感染的吉泊达星
1.相关申请的交叉引用
2.本技术要求us 62/828801、us 62/834112、us 62/841363、us 62/895594、us 62/841375、us 62/895590、us 62/841384和us 62/895601的权益,其公开的内容通过引用整体并入本文。
3.关于联邦资助研究的声明
4.本发明是在美利坚合众国卫生和公共服务部负责准备和响应的助理部长生物医学高级研究和发展管理局(barda)的政府支持下完成的,在美国卫生与公众服务部负责准备和响应的助理部长办公室内签署协议编号:hhs0100201300011c。政府享有本发明的某些权利。
技术领域
5.本发明涉及用于治疗由革兰氏阳性和革兰氏阴性细菌引起的细菌感染的方法和/或用途,其包括施用如本文所述的吉泊达星(gepotidacin)或其药学上可接受的盐,和/或相应的药物组合物。
背景技术:
6.在过去的几十年里,抗微生物药物耐药性的频率及其与严重传染病的关联以惊人的速度增加。
7.例如,在美国,疾病控制和预防中心估计,每年大约有170万例医院相关感染,来自包括细菌在内的所有类型的微生物,合并、导致或促成99,000人死亡。
8.由多药耐药革兰氏阳性菌和革兰氏阴性菌引起的感染是主要的公共卫生负担,不仅在发病率和死亡率方面,而且在患者管理和感染控制措施实施的支出增加方面。例如,在已经进行医院调查的欧洲,革兰氏阴性感染类别估计占每年25,000例死亡人数的三分之二。医院感染可导致严重的肺炎以及泌尿道、血液和身体其他部位的感染。很多类型难以用抗生素攻击,并且抗生素耐药性正在蔓延到可以感染医院外人员的革兰氏阴性菌(参见,pollack,andrew."rising threat of infections unfazed by antibiotics"new york times,feb.27,2010)。这种高耐药率增加了与医院感染相关的发病率、死亡率和成本。
9.尿路感染(uti)非常常见,大约11%的18岁以上女性每年至少发生1次急性膀胱炎。其中,一半会在其一生中经历1次以上的反复发作。发病高峰发生在18至29岁的年轻、性活跃的女性中。尿路感染可能由多种尿路病原体引起;在社区获得性uti中分离出的主要尿路病原体是大肠杆菌(escherichia coli)(75%至90%)和腐生葡萄球菌(staphylococcus saprophyticus)(5%至15%),但也有其他细菌的报道。
10.由于多药耐药病原体和产生超广谱β-内酰胺酶的肠杆菌科病原体的增加,治疗方法变得有限,因此需要针对uti的新的有效口服抗生素治疗方案,这些病原体正在影响目前可用的口服抗菌治疗方案的功效。在决定治疗方案时,还必须考虑患者对某些抗生素的过敏或耐受性。
morganii)、雷氏普罗威登斯菌(providencia rettgeri)、耐药肺炎克雷伯氏菌(klebsiella pneumoniae)、耐药大肠杆菌(escherichia coli)、温和食酸菌(acidovorax temperans)、非丙二酸柠檬酸杆菌(citrobacter amalonaticus)、斯氏普罗威登斯菌(providencia stuartii)、恶臭假单胞菌(pseudomonas putida);
20.路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)、前庭链球菌(streptococcus vestibularis);
21.沃氏嗜胆菌(bilophila wadsworthia)、华德萨特氏菌(sutterella wadsworthensis)、双酶梭状芽孢杆菌(clostridium bifermentans)、艰难梭状芽孢杆菌(clostridium difficile)、迟缓埃格特菌(eggethella lenta)、厌氧消化链球菌(peptostreptococcus anaerobius)、厌氧消化链球菌(peptostreptococcus anaerobius)、粪便拟杆菌(bacteroides caccae)、脆弱拟杆菌(bacteroides fragilis)、卵形拟杆菌(bacteroides ovatus)、粪便拟杆菌(bacteroides stercoris)、多形拟杆菌(bacteroides thetaiotaomicron)、单形拟杆菌(bacteroides uniformis)、普通拟杆菌(bacteroides vulgatus)、坏死梭形杆菌(fusobacterium necrophorum)、具核梭形杆菌(fusobacterium nucleatum)、不解糖卟啉单胞菌(porphyromonas asaccharolytica)、牙髓卟啉单胞菌(porphyromonas endodontalis)、牙龈卟啉单胞菌(porphyromonas gingivalis)、利氏卟啉单胞菌(porphyromonas levii)、索氏卟啉单胞菌(porphyromonas somerae)、二路普雷沃尔菌(prevotella bivia)、颊普雷沃菌(prevotella buccae)、栖牙普雷沃菌(prevotella denticola)、解糖胨普雷沃菌(prevotella disiens)、产黑色普雷沃菌(prevotella melaninogenica)、殊异产碱韦荣氏球菌(veillonella alcalescens dispar)、小韦荣球菌(veillonella parvula)、青春双岐杆菌(bifidobacterium adolescentis)、短双歧杆菌(bifidobacterium breve)、齿双歧杆菌(bifidobacterium dentium)、长双歧杆菌(bifidobacterium longum)、假小链双歧杆菌(bifidobacterium pseudocatenulatum)、产气柯林斯菌(真杆菌)(collinsella(eubacterium)aerofaciens)、粘液真杆菌(eubacterium limosum)、缠结优杆菌(eubacterium nodatum)、嗜酸乳酸杆菌(lactobacillus acidophilus)、卷曲乳酸杆菌(lactobacillus crispatus)、发酵乳酸杆
anaerobius)、粪便拟杆菌(bacteroides caccae)、脆弱拟杆菌(bacteroides fragilis)、卵形拟杆菌(bacteroides ovatus)、粪便拟杆菌(bacteroides stercoris)、多形拟杆菌(bacteroides thetaiotaomicron)、单形拟杆菌(bacteroides uniformis)、普通拟杆菌(bacteroides vulgatus)、坏死梭形杆菌(fusobacterium necrophorum)、具核梭形杆菌(fusobacterium nucleatum)、不解糖卟啉单胞菌(porphyromonas asaccharolytica)、牙髓卟啉单胞菌(porphyromonas endodontalis)、牙龈卟啉单胞菌(porphyromonas gingivalis)、利氏卟啉单胞菌(porphyromonas levii)、索氏卟啉单胞菌(porphyromonas somerae)、二路普雷沃尔菌(prevotella bivia)、颊普雷沃菌(prevotella buccae)、栖牙普雷沃菌(prevotella denticola)、解糖胨普雷沃菌(prevotella disiens)、产黑色普雷沃菌(prevotella melaninogenica)、殊异产碱韦荣氏球菌(veillonella alcalescens dispar)、小韦荣球菌(veillonella parvula)、青春双岐杆菌(bifidobacterium adolescentis)、短双歧杆菌(bifidobacterium breve)、齿双歧杆菌(bifidobacterium dentium)、长双歧杆菌(bifidobacterium longum)、假小链双歧杆菌(bifidobacterium pseudocatenulatum)、产气柯林斯菌(真杆菌)(collinsella(eubacterium)aerofaciens)、粘液真杆菌(eubacterium limosum)、缠结优杆菌(eubacterium nodatum)、嗜酸乳酸杆菌(lactobacillus acidophilus)、卷曲乳酸杆菌(lactobacillus crispatus)、发酵乳酸杆菌(lactobacillus fermentum)、加氏乳酸杆菌(lactobacillus gasseri)、惰性乳酸杆菌(lactobacillus iners)、詹氏乳酸杆菌(lactobacillus jensenii)、植物乳酸杆菌(lactobacillus plantarum)和鼠李糖乳酸杆菌(lactobacillus rhamnosus)。
27.在另一个方面中,本发明提供了吉泊达星或其药学上可接受的盐在制备用于治疗uti的药物中的用途,其中所述uti是由选自以下的一种或多种细菌引起的:
28.腐生葡萄球菌(staphylococcus saprophyticus);鲍曼不动杆菌(acinetobacter baumannii)、无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)、皮蒂不动杆菌(acinetobacter pittii)、弗氏柠檬酸杆菌复合菌(citrobacter freundii complex)、克氏柠檬酸杆菌(citrobacter koseri)、副流感嗜血杆菌(haemophilus parainfluenzae)、副嗜沫嗜血杆菌(haemophilus paraphrophilus)、产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、非脱羧勒克菌(leclercia adecarboxylata)、豪氏变形杆菌(proteus hauseri)、潘纳氏变形杆菌(proteus peneri)、粘质沙雷氏菌(serratia marcescens)、鲍氏志贺菌(shigella boydii)、弗氏志贺菌(shigella flexneri)、宋内氏志贺菌(shigella sonnei)、摩氏摩根菌(morganella morganii)、雷氏普罗威登斯菌(providencia rettgeri)、耐药肺炎克雷伯氏菌(klebsiella pneumoniae)、耐药大肠杆菌(escherichia coli)、温和食酸菌(acidovorax temperans)、非丙二酸柠檬酸杆菌(citrobacter amalonaticus)、斯氏普罗威登斯菌(providencia stuartii)、恶臭假单胞菌(pseudomonas putida);
29.路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、
中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)、前庭链球菌(streptococcus vestibularis);
30.沃氏嗜胆菌(bilophila wadsworthia)、华德萨特氏菌(sutterella wadsworthensis)、双酶梭状芽孢杆菌(clostridium bifermentans)、艰难梭状芽孢杆菌(clostridium difficile)、迟缓埃格特菌(eggethella lenta)、厌氧消化链球菌(peptostreptococcus anaerobius)、厌氧消化链球菌(peptostreptococcus anaerobius)、粪便拟杆菌(bacteroides caccae)、脆弱拟杆菌(bacteroides fragilis)、卵形拟杆菌(bacteroides ovatus)、粪便拟杆菌(bacteroides stercoris)、多形拟杆菌(bacteroides thetaiotaomicron)、单形拟杆菌(bacteroides uniformis)、普通拟杆菌(bacteroides vulgatus)、坏死梭形杆菌(fusobacterium necrophorum)、具核梭形杆菌(fusobacterium nucleatum)、不解糖卟啉单胞菌(porphyromonas asaccharolytica)、牙髓卟啉单胞菌(porphyromonas endodontalis)、牙龈卟啉单胞菌(porphyromonas gingivalis)、利氏卟啉单胞菌(porphyromonas levii)、索氏卟啉单胞菌(porphyromonas somerae)、二路普雷沃尔菌(prevotella bivia)、颊普雷沃菌(prevotella buccae)、栖牙普雷沃菌(prevotella denticola)、解糖胨普雷沃菌(prevotella disiens)、产黑色普雷沃菌(prevotella melaninogenica)、殊异产碱韦荣氏球菌(veillonella alcalescens dispar)、小韦荣球菌(veillonella parvula)、青春双岐杆菌(bifidobacterium adolescentis)、短双歧杆菌(bifidobacterium breve)、齿双歧杆菌(bifidobacterium dentium)、长双歧杆菌(bifidobacterium longum)、假小链双歧杆菌(bifidobacterium pseudocatenulatum)、产气柯林斯菌(真杆菌)(collinsella(eubacterium)aerofaciens)、粘液真杆菌(eubacterium limosum)、缠结优杆菌(eubacterium nodatum)、嗜酸乳酸杆菌(lactobacillus acidophilus)、卷曲乳酸杆菌(lactobacillus crispatus)、发酵乳酸杆菌(lactobacillus fermentum)、加氏乳酸杆菌(lactobacillus gasseri)、惰性乳酸杆菌(lactobacillus iners)、詹氏乳酸杆菌(lactobacillus jensenii)、植物乳酸杆菌(lactobacillus plantarum)和鼠李糖乳酸杆菌(lactobacillus rhamnosus)。
附图说明
31.图1显示了在实施例3中所述的iia期临床试验的参与者分布和研究提纲。bid=每天两次;pk=药代动力学;toc=治愈检测;wbc=白细胞。
32.图2显示了微生物意向治疗人群选择的基线算法,如实施例3中所述。cfu=集落形成单位;微-itt=微生物意向治疗。
33.图3显示了随着时间的推移基线定性尿路病原体的定量细菌计数(cfu/ml)(微-itt人群),如实施例3中所述。
34.图4显示了单个临床症状评分以及总评分随着时间推移的箱线图(itt人群),如实施例3中所述。
35.图5显示了bid口服施用吉泊达星(1500mg)后以天计的吉泊达星的中位c
t
血浆浓度,如实施例3中所述。
36.图6显示了单次和bid口服施用(1500mg)后吉泊达星的中位血浆浓度时间曲线,如实施例3中所述。
37.图7显示了单次和bid口服施用吉泊达星(1500mg)后的中位尿液浓度时间曲线,如实施例3中所述。
38.图8显示了在大鼠肾盂肾炎和大腿感染模型中的血浆、肾脏和大腿浓度对时间的曲线,如实施例4中所述。
39.图9显示了因变量与预测的关系,以及条件加权残差与时间和预测的关系,如实施例4中所述。dv=因变量,cwres=条件加权残差,pred=预测。
40.图10显示了在中性粒细胞减少的大腿模型中有效性与pk/pd指数(fauc和fcmax)之间的相关性,如实施例4中所述。
具体实施方式
41.如本文所用,术语“抗生素”与“抗菌”和“抗微生物”同义。
42.吉泊达星是一个同类首创的三氮杂苊抗生素,其具有通过任何目前批准的人类治疗剂均未使用的方式选择性抑制细菌dna复制的独特能力,因此为解决未满足的医疗需求提供了机会。吉泊达星及其外消旋形式公开于wo2008/1289422中。吉泊达星是(2r)-2-({4-[(3,4-二氢-2h-吡喃并[2,3-c]吡啶-6-基甲基)氨基]-1-哌啶基}甲基)-1,2-二氢-3h,8h-2a,5,8a-三氮杂苊-3,8-二酮:
[0043][0044]
如本文所用,术语“吉泊达星”可以指吉泊达星的游离碱或吉泊达星的盐。当组合物包含吉泊达星的盐时,组合物中吉泊达星的所示量指相应吉泊达星游离碱的量。
[0045]
现在已经发现吉泊达星对某些细菌具有惊人的活性,以前没有证明对这些细菌具有活性。其独特的作用方式意味着其可以为某些细菌感染提供传统抗生素的替代疗法。此外,现已发现吉泊达星特别适用于治疗uti,因为其对某些引起uti的细菌具有特异性功效、其体内安全性质以及其活性受尿液影响最小的事实。而且,已显示吉泊达星在体内维持高且持续的尿液浓度(参见本文实施例)。吉泊达星的这些出乎意料的性质使其非常适合用于治uti。
[0046]
在第一个方面中,本发明提供了一种治疗uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述uti是由如本文所述的一种或多种细菌引起的。
[0047]
如本文所用,短语“由细菌引起”可以指(1)技术人员怀疑引起uti发作的细菌的身份,例如由于患者病史或当地流行病学;或者(2)技术人员使用从受感染患者获得的培养(或其他诊断测试)信息来证明或确定致病细菌的身份。因此,在一个实施方式中,本发明提供了一种治疗uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述uti已证明是由本文所述的一种或多种细菌引起的。在另一个实施方式中,本发明提供了一种治疗uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述uti疑似或强烈疑似是由本文所定义的一种或多种细菌引起的。
[0048]
在一个实施方式中,本发明提供了一种治疗uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述uti是由如本文所述的细菌菌株引起的,其对吉泊达星或其药学上可接受的盐敏感。
[0049]
本领域技术人员将理解,“易感”是指当推荐剂量用于感染部位时,微生物的分离株被通常可达到的浓度的抗微生物剂抑制。对吉泊达星的易感性可由技术人员从感染受试者的样品中回收的分离株中确定,使用标准方法,如由例如美国联邦药品管理局(抗菌药敏试验解释标准)、临床和实验室标准研究所(例如,抗菌药物敏感性测试性能标准,29th ed.clsi supplement m100.wayne,pa:clinical and laboratory standards institute;2019)或者欧盟抗微生物药敏试验委员会。
[0050]
在一个实施方式中,如本文所用,“对吉泊达星易感”或“吉泊达星易感的”指细菌分离株的吉泊达星mic(可在体外或体内测量)为32mg/l或更低,如根据临床和实验室标准协会指南通过肉汤微量稀释所测量的。在一个实施方式中,其指16mg/l或更低。在一个实施方式中,其指8mg/l或更低。在一个实施方式中,其指4mg/l或更低。在另一个实施方式中,其指2mg/l或更低。在另一个实施方式中,其指1mg/l或更低。
[0051]
在一个实施方式中,在施用吉泊达星或其药学上可接受的盐之前,确定uti是由如上所定义的一种或多种细菌引起的。可以通过任何常规方法进行确定。例如,样品如尿液或血浆样品可以从怀疑患有uti的人获得,然后使用任何常规手段测试其是否存在如本发明中定义的一种或多种细菌。如果该培养信息表明存在一种或多种本发明定义的细菌,并且根据已知的诊断标准确定为uti的原因,则以治疗有效量施用吉泊达星或其药学上可接受的盐。技术人员可以使用已建立的诊断标准,如尿液中游样本中超过103cfu/ml、104cfu/ml或105cfu/ml的尿路病原体的细菌计数(参见例如,kunin c.urinary tract infections,in detection,prevention and management.1997,lea&febiger;european association of urology,guidelines on urological infections 2015),以确定uti发作的致病细菌。
[0052]
在一个实施方式中,本发明提供了一种治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的膀胱炎的方法,所述方法包括向有需要的患者施用吉泊达星或其药学上可接受的盐。在一个实施方式中,所述膀胱炎是急性膀胱炎。
[0053]
在第二个方面中,本发明提供了一种治疗尿路感染(uti)的方法,包括以下步骤(a)确定来自疑似患有uti的人的样品是否含有本发明中定义的一种或多种细菌,和(b)如
果在步骤(a)中在样品中鉴定出一种或多种细菌并且确定其是uti的原因,则向受试者施用治疗有效量的吉泊达星或其药学上可接受的盐。如上所述,可以使用任何常规手段来确定样品中存在本发明的细菌。
[0054]
在一个实施方式中,在步骤(a)中使用的样品是尿液样品。在另一个实施方式中,样品是血液、血浆或组织样品。
[0055]
在第三个方面中,本发明提供了用于治疗uti的吉泊达星或其药学上可接受的盐,其中所述uti是由如上文所定义的一种或多种细菌引起的。
[0056]
在另一个方面中,本发明提供了吉泊达星或其药学上可接受的盐用于治疗由革兰氏阳性需氧菌或革兰氏阴性需氧菌引起的尿路感染的用途;
[0057]
其中:
[0058]
所述革兰氏阳性需氧菌是腐生葡萄球菌(staphylococcus saprophyticus);
[0059]
所述革兰氏阴性需氧菌选自无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)、皮蒂不动杆菌(acinetobacter pittii);副流感嗜血杆菌(haemophilus parainfluenzae)、副嗜沫嗜血杆菌(haemophilus paraphrophilus)、产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、变形杆菌(proteus hauseri)或潘纳氏变形杆菌(proteus peneri)。
[0060]
在一个实施方式中,在本发明的任何方面中,所述细菌选自:腐生葡萄球菌(staphylococcus saprophyticus);鲍曼不动杆菌(acinetobacter baumannii)、无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)、皮蒂不动杆菌(acinetobacter pittii)、弗氏柠檬酸杆菌复合菌(citrobacter freundii complex)、克氏柠檬酸杆菌(citrobacter koseri)、副流感嗜血杆菌(haemophilus parainfluenzae)、副嗜沫嗜血杆菌(haemophilus paraphrophilus)、产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、非脱羧勒克菌(leclercia adecarboxylata)、豪氏变形杆菌(proteus hauseri)、潘纳氏变形杆菌(proteus peneri)、粘质沙雷氏菌(serratia marcescens)、鲍氏志贺菌(shigella boydii)、弗氏志贺菌(shigella flexneri)、宋内氏志贺菌(shigella sonnei)、摩氏摩根菌(morganella morganii)、雷氏普罗威登斯菌(providencia rettgeri)、耐药肺炎克雷伯氏菌(klebsiella pneumoniae)、耐药大肠杆菌(escherichia coli)、温和食酸菌(acidovorax temperans)、非丙二酸柠檬酸杆菌(citrobacter amalonaticus)、斯氏普罗威登斯菌(providencia stuartii)、恶臭假单胞菌(pseudomonas putida)。
[0061]
在一个实施方式中,在本发明的任何方面中,所述细菌选自:腐生葡萄球菌(staphylococcus saprophyticus)、无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)、皮蒂不动杆菌(acinetobacter pittii)、弗氏柠檬酸杆菌复合体(citrobacter freundii complex)、克氏柠檬酸杆菌(citrobacter koseri)、副流感嗜血杆菌(haemophilus parainfluenzae)、副嗜沫嗜血杆菌(haemophilus paraphrophilus)、产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、非脱羧勒克菌(leclercia adecarboxylata)、豪氏变形杆菌(proteus hauseri)、潘纳氏变形杆菌(proteus peneri)、摩氏摩根菌(morganella morganii)、雷氏普罗威登斯菌(providencia rettgeri)和鲍氏志贺菌(shigella boydii)。
saprophyticus)或者耐药大肠杆菌(escherichia coli)(e.coli)和耐药肺炎克雷伯菌(k.pneumoniae)。
[0072]
如本文所用,术语“耐药”细菌与“不易感”细菌同义,指一种细菌形式,其可以抵抗抗生素的作用,或者对抗生素的易感性降低或没有易感性。“耐药细菌”包括,例如,产生超广谱β-内酰胺酶(esbl)的细菌;产生碳青霉烯酶的细菌(如kpc、ges、oxa-48-样、ndm、vim和imp);由于oprd丢失或外流而对碳青霉烯类耐药的细菌;产生ampc的细菌;以及在gyra和parc基因的喹诺酮耐药性决定区(qrdr)中具有突变的细菌。
[0073]
在本发明中,在一个实施方式中,可能怀疑细菌的耐药性(例如,通过了解患者的病史,例如,复发性uti)。在另一个实施方式中,可以通过已建立的技术证明耐药性,包括表型或基因型测定。
[0074]
在一个实施方式中,在本发明中,“耐药性”是指m100 clsi定义的耐药性或非易感性。
[0075]
在一个实施方式中,引起uti的细菌对选自以下的抗生素有耐药性或怀疑有耐药性:氟喹诺酮类抗生素,包括环丙沙星和左氧氟沙星;氨苄西林;阿莫西林/克拉维酸盐;甲氧苄啶-磺胺甲噁唑;头孢唑啉;阿奇霉素;甲氧西林;四环素;硝羟喹啉;美西林;头孢曲松,头孢克肟;呋喃妥因;和磷霉素。在一个实施方式中,引起uti的细菌是多药耐药的。在一个实施方式中,本发明中的“多药耐药”是指对两种临床相关的抗生素类别具有耐药性。在一个实施方式中,“多药耐药”指对三个或更多个临床相关的抗生素类别具有耐药性。
[0076]
在另一个方面中,本发明提供或涉及革兰氏阴性和/或革兰氏阳性需氧菌或厌氧菌对选自但不限于环丙沙星、阿奇霉素和四环素的抗生素耐药的情况。
[0077]
在一个实施方式中,在本发明的任何方面中,所述细菌选自:耐药肺炎克雷伯氏菌(klebsiella pneumoniae)和耐药大肠杆菌(escherichia coli)。在一个实施方式中,耐药腐生葡萄球菌(staphylococcus saprophyticus)、耐药肺炎克雷伯氏菌(klebsiella pneumoniae)或耐药大肠杆菌(escherichia coli)分别对选自以下的一种或多种抗生素耐药:氟喹诺酮类抗生素,包括环丙沙星和左氧氟沙星;氨苄西林;阿莫西林/克拉维酸盐;甲氧苄啶-磺胺甲噁唑;头孢唑啉;阿奇霉素;甲氧西林;四环素;硝羟喹啉;美西林;头孢曲松,头孢克肟;呋喃妥因;和磷霉素。在一个实施方式中,耐药腐生葡萄球菌(staphylococcus saprophyticus)、耐药克氏柠檬酸杆菌(citrobacter koseri)和耐药肺炎克雷伯氏菌(klebsiella pneumoniae)分别对氨苄西林耐药。
[0078]
在另一个方面中,本发明涉及用于治疗由革兰氏阴性和/或革兰氏阳性需氧生物引起的如本发明定义的细菌感染或其他疾病的方法、化合物和/或用途,其中革兰氏阴性需氧菌、大肠杆菌(escherichia coli)或肺炎克雷伯氏菌(k.pneumoniae)对选自但不限于氨苄青霉素、甲氧苄啶-磺胺甲噁唑和环丙沙星/左氧氟沙星和头孢唑林的抗生素具有耐药性。
[0079]
在一个实施方式中,革兰氏阴性和/或革兰氏阳性需氧菌对选自但不限于选自环丙沙星、阿奇霉素或四环素的抗生素耐药。
[0080]
在一个实施方式中,耐药细菌是e.coli,其对两种或更多种类别的抗生素耐药。
[0081]
在一个实施方式中,耐药细菌是e.coli,其对三种或更多种类别的抗生素耐药。
[0082]
在一个实施方式中,所述耐药菌是:
[0083]
a)腐生葡萄球菌(staphylococcus saprophyticus)或克氏柠檬酸杆菌(citrobacter koseri);
[0084]
b)对氨苄西林耐药的腐生葡萄球菌(staphylococcus saprophyticus);
[0085]
c)对甲氧西林耐药的腐生葡萄球菌(staphylococcus saprophyticus);
[0086]
d)对氨苄西林耐药的克氏柠檬酸杆菌(citrobacter koseri);
[0087]
e)对氨苄西林耐药的肺炎克雷伯氏菌(klebsiella pneumoniae);或者
[0088]
f)对氨苄西林耐药的大肠杆菌(escherichia coli);
[0089]
g)对甲氧苄啶-磺胺甲噁唑耐药的大肠杆菌(escherichia coli);
[0090]
h)环丙沙星耐药的大肠杆菌(escherichia coli);
[0091]
i)头孢唑啉耐药的大肠杆菌(escherichia coli);
[0092]
j)对氨苄西林、环丙沙星和甲氧苄啶-磺胺甲噁唑耐药的大肠杆菌(escherichia coli);
[0093]
k)对氨苄西林、头孢唑啉和甲氧苄啶-磺胺甲噁唑耐药的大肠杆菌(escherichia coli);
[0094]
l)对甲氧西林耐药的表皮葡萄球菌(staphylococcus epidermidis)。
[0095]
在一个方面中,本发明提供了一种治疗非复杂性uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述非复杂性uti是由选自以下的一种或多种细菌引起的:腐生葡萄球菌(staphylococcus saprophyticus)、耐药腐生葡萄球菌(staphylococcus saprophyticus)、豪氏变形杆菌(proteus hauseri)、潘纳氏变形杆菌(proteus peneri)、摩氏摩根菌(morganella morganii)、雷氏普罗威登斯菌(providencia rettgeri)、温和食酸菌(acidovorax temperans)、非丙二酸柠檬酸杆菌(citrobacter amalonaticus)、斯氏普罗威登斯菌(providencia stuartii)、恶臭假单胞菌(pseudomonas putida)、耐药肺炎克雷伯氏菌(klebsiella pneumoniae)和耐药大肠杆菌(escherichia coli)。
[0096]
在一个方面中,本发明提供了一种治疗非复杂性uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述非复杂性uti是由选自以下的一种或多种细菌引起的:腐生葡萄球菌(staphylococcus saprophyticus)、耐药腐生葡萄球菌(staphylococcus saprophyticus)。
[0097]
在一个方面中,本发明提供了一种治疗非复杂性uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述非复杂性uti是由耐药e.coli引起的。
[0098]
在一个方面中,本发明提供了一种治疗非复杂性uti的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述非复杂性uti是由多药耐药e.coli引起的。
[0099]
在一个实施方式中,在本发明的任何方面中,所述细菌选自:路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌
(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)和前庭链球菌(streptococcus vestibularis)。
[0100]
在一个实施方式中,本发明提供了一种治疗由选自以下的革兰氏阳性需氧菌引起的尿路感染的方法:路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)和前庭链球菌(streptococcus vestibularis),其包括向有需要的受试者施用吉泊达星或其药学上可接受的盐。
[0101]
在一个实施方式中,本发明提供了一种治疗选自以下的细菌感染的方法:血液感染、上呼吸道感染、下呼吸道感染、皮肤感染、软组织感染、腹腔内感染、胃肠道感染、生殖道感染和泌尿道感染;由选自以下的革兰氏阳性需氧菌引起:路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌
(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)和前庭链球菌(streptococcus vestibularis),其包括向有需要的受试者施用吉泊达星或其药学上可接受的盐。
[0102]
在一个实施方式中,所述革兰氏阳性需氧菌选自凝固酶阴性葡萄球菌,其选自:s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans and s.warneri;or a viridans streptococci is selected from s.anginosus、s.australis、s.constellatus、s.cristatus、s.gordonii、s.infantarius、s.infantis、s.intermedius、s.massiliensis、s.mutans、s.oralis、s.parasanguinis、s.salivarius、s.sanguinis和s.vestibularis。
[0103]
在一个实施方式中,在本发明的任何方面中,所述细菌选自:路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)和前庭链球菌(streptococcus vestibularis)。
[0104]
在一个实施方式中,所述细菌是无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌
(streptococcus sanguinis)和前庭链球菌(streptococcus vestibularis)。
[0105]
在一个实施方式中,所述细菌是无乳链球菌(streptococcus agalactiae)。
[0106]
在另一个实施方式中,所述细菌是路敦葡萄球菌(staphylococcus lugdenensis)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)或沃氏葡萄球菌(staphylococcus warneri)。
[0107]
在另一个方面中,本发明涉及一种治疗由选自以下的革兰氏阳性需氧菌引起的尿路感染的方法:凝固酶阴性葡萄球菌,其选自:s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri;其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0108]
在另一个方面中,本发明涉及一种治疗由选自以下的革兰氏阳性需氧菌引起的尿路感染的方法:凝固酶阴性葡萄球菌,其选自:s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri;其包括向有需要的患者施用药物组合物,所述药物组合物包含[a]吉泊达星或其药学上可接受的盐;和[b]至少一种或多种药学上可接受的赋形剂。
[0109]
在另一个方面中,本发明涉及一种治疗由本文所述的革兰氏阳性需氧菌引起的尿路感染的方法,其中所述尿路感染选自非复杂性尿路感染(uuti)、膀胱炎和急性膀胱炎。
[0110]
在另一个方面中,本发明涉及一种治疗由选自以下的革兰氏阳性需氧菌引起的膀胱炎或急性膀胱炎的方法:凝固酶阴性葡萄球菌,其选自:s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri;其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0111]
在另一个方面中,本发明涉及一种治疗由选自以下的革兰氏阳性需氧菌引起的膀胱炎或急性膀胱炎的方法:凝固酶阴性葡萄球菌,其选自:s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri;其包括向有需要的患者施用药物组合物,所述药物组合物包含[a]吉泊达星或其药学上可接受的盐;和[b]至少一种或多种药学上可接受的赋形剂。
[0112]
在另一个方面中,本发明涉及一种治疗由选自以下的革兰氏阳性需氧菌引起的非复杂性尿路感染(uuti)的方法:凝固酶阴性葡萄球菌,其选自:s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri;其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0113]
在另一个方面中,本发明涉及一种治疗由其是凝固酶阴性葡萄球菌的革兰氏阳性需氧菌引起的非复杂性尿路感染(uuti)的方法,所述凝固酶阴性葡萄球菌选自s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri;其包括向有需要的患者施用药物组合物,所述药物组合物包含:
[0114]
[a]吉泊达星或其药学上可接受的盐;和
[0115]
[b]至少一种或多种药学上可接受的赋形剂。
[0116]
在另一个方面中,本发明涉及治疗由本技术通篇所述的革兰氏阳性需氧菌引起的
尿路感染的方法,其中所述革兰氏阳性需氧菌是非耐药性或耐药性的。
[0117]
在另一个方面中,本发明提供了一种治疗选自以下的细菌感染的方法:血液感染、上呼吸道感染、下呼吸道感染、皮肤感染、软组织感染、腹腔内感染、胃肠道感染、生殖道感染和泌尿道感染;由选自以下的革兰氏阴性需氧菌和/或革兰氏阳性需氧菌引起:沃氏嗜胆菌(bilophila wadsworthia)、华德萨特氏菌(sutterella wadsworthensis)、双酶梭状芽孢杆菌(clostridium bifermentans)、艰难梭状芽孢杆菌(clostridium difficile)、迟缓埃格特菌(eggethella lenta)、厌氧消化链球菌(peptostreptococcus anaerobius)、厌氧消化链球菌(peptostreptococcus anaerobius)、粪便拟杆菌(bacteroides caccae)、脆弱拟杆菌(bacteroides fragilis)、卵形拟杆菌(bacteroides ovatus)、粪便拟杆菌(bacteroides stercoris)、多形拟杆菌(bacteroides thetaiotaomicron)、单形拟杆菌(bacteroides uniformis)、普通拟杆菌(bacteroides vulgatus)、坏死梭杆菌(fusobacterium necrophorum)、具核梭杆菌(fusobacterium nucleatum)、不解糖卟啉单胞菌(porphyromonas asaccharolytica)、牙髓卟啉单胞菌(porphyromonas endodontalis)、牙龈卟啉单胞菌(porphyromonas gingivalis)、利氏卟啉单胞菌(porphyromonas levii)、索氏卟啉单胞菌(porphyromonas somerae)、二路普雷沃尔菌(prevotella bivia)、颊普雷沃菌(prevotella buccae)、栖牙普雷沃菌(prevotella denticola)、解糖胨普雷沃菌(prevotella disiens)、产黑色普雷沃菌(prevotella melaninogenica)、殊异产碱韦荣氏球菌(veillonella alcalescens dispar)、小韦荣球菌(veillonella parvula)、青春双岐杆菌(bifidobacterium adolescentis)、短双歧杆菌(bifidobacterium breve)、齿双歧杆菌(bifidobacterium dentium)、长双歧杆菌(bifidobacterium longum)、假小链双歧杆菌(bifidobacterium pseudocatenulatum)、产气柯林斯菌(真杆菌)(collinsella(eubacterium)aerofaciens)、粘液真杆菌(eubacterium limosum)、缠结优杆菌(eubacterium nodatum)、嗜酸乳酸杆菌(lactobacillus acidophilus)、卷曲乳酸杆菌(lactobacillus crispatus)、发酵乳酸杆菌(lactobacillus fermentum)、加氏乳酸杆菌(lactobacillus gasseri)、惰性乳酸杆菌(lactobacillus iners)、詹氏乳酸杆菌(lactobacillus jensenii)、植物乳酸杆菌(lactobacillus plantarum)和鼠李糖乳酸杆菌(lactobacillus rhamnosus),其包括向有需要的对象施用吉泊达星或其药学上可接受的盐。
[0118]
在另一个方面中,本发明涉及一种治疗由如本文所述的革兰氏阴性需氧菌和/或革兰氏阳性需氧菌引起的细菌感染的方法,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0119]
在另一个方面中,本发明涉及一种治疗由如本文所述的革兰氏阴性需氧菌和/或革兰氏阳性需氧菌引起的细菌感染的方法,其包括向有需要的患者施用吉泊达星。
[0120]
在另一个方面中,本发明涉及一种治疗由如本文所述的革兰氏阴性需氧菌和/或革兰氏阳性需氧菌引起的细菌感染的方法,其包括向有需要的患者施用药物组合物,所述药物组合物包含:
[0121]
[a]吉泊达星或其药学上可接受的盐;和
[0122]
[b]至少一种或多种药学上可接受的赋形剂。
[0123]
在另一个方面中,本发明涉及一种治疗由以下引起的细菌感染的方法、化合物和/
或用途:
[0124]
沃氏嗜胆菌(bilophila wadsworthia)、华德萨特氏菌(sutterella wadsworthensis)、双酶梭状芽孢杆菌(clostridium bifermentans)、艰难梭状芽孢杆菌(clostridium difficile)、迟缓埃格特菌(eggethella lenta)、厌氧消化链球菌(peptostreptococcus anaerobius)、厌氧消化链球菌(peptostreptococcus anaerobius)、粪便拟杆菌(bacteroides caccae)、脆弱拟杆菌(bacteroides fragilis)、卵形拟杆菌(bacteroides ovatus)、粪便拟杆菌(bacteroides stercoris)、多形拟杆菌(bacteroides thetaiotaomicron)、单形拟杆菌(bacteroides uniformis)、普通拟杆菌(bacteroides vulgatus)、坏死梭形杆菌(fusobacterium necrophorum)、具核梭形杆菌(fusobacterium nucleatum)、不解糖卟啉单胞菌(porphyromonas asaccharolytica)、牙髓卟啉单胞菌(porphyromonas endodontalis)、牙龈卟啉单胞菌(porphyromonas gingivalis)、利氏卟啉单胞菌(porphyromonas levii)、索氏卟啉单胞菌(porphyromonas somerae)、二路普雷沃尔菌(prevotella bivia)、颊普雷沃菌(prevotella buccae)、栖牙普雷沃菌(prevotella denticola)、解糖胨普雷沃菌(prevotella disiens)、产黑色普雷沃菌(prevotella melaninogenica)、殊异产碱韦荣氏球菌(veillonella alcalescens dispar)、小韦荣球菌(veillonella parvula)、青春双岐杆菌(bifidobacterium adolescentis)、短双歧杆菌(bifidobacterium breve)、齿双歧杆菌(bifidobacterium dentium)、长双歧杆菌(bifidobacterium longum)、假小链双歧杆菌(bifidobacterium pseudocatenulatum)、产气柯林斯菌(真杆菌)(collinsella(eubacterium)aerofaciens)、粘液真杆菌(eubacterium limosum)、缠结优杆菌(eubacterium nodatum)、嗜酸乳酸杆菌(lactobacillus acidophilus)、卷曲乳酸杆菌(lactobacillus crispatus)、发酵乳酸杆菌(lactobacillus fermentum)、加氏乳酸杆菌(lactobacillus gasseri)、惰性乳酸杆菌(lactobacillus iners)、詹氏乳酸杆菌(lactobacillus jensenii)、植物乳酸杆菌(lactobacillus plantarum)和鼠李糖乳酸杆菌(lactobacillus rhamnosus);
[0125]
其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0126]
在一个实施方式中,所述细菌感染由对头孢曲松、克林霉素、亚胺培南、莫西沙星或哌拉西林-他唑巴坦耐药的拟杆菌属物种引起,其中所述拟杆菌属物种选自:粪便拟杆菌(bacteroides caccae)、脆弱拟杆菌(bacteroides fragilis)、卵状拟杆菌(bacteroides ovatus)、粪便拟杆菌(bacteroides stercoris)、多形拟杆菌(bacteroides thetaiotaomicron)、单形拟杆菌(bacteroides uniformis)和普通拟杆菌(bacteroides vulgatus)。
[0127]
在一个实施方式中,所述细菌感染是由选自以下的一种或多种细菌引起的:对甲硝唑耐药的利氏卟啉单胞菌(porphyromonas levii)、对甲硝唑耐药的华德萨特氏菌(sutterella wadsworthensis)、对克林霉素耐药的假链双歧杆菌(bifidobacterium pseudocatenulatum)、对头孢曲松、克林霉素、亚胺培南或莫西沙星耐药的艰难梭状芽孢杆菌(clostridioides difficile)、对头孢曲松、克林霉素或莫西沙星耐药的迟缓埃格特菌(eggerthella lenta)、对甲硝唑耐药的缠结优杆菌(eubacterium nodatum),对克林霉素或莫西沙星耐药的厌氧消化链球菌(peptostreptococcus anaerobius)。
[0128]
在另一个方面中,本发明涉及一种治疗由如本文所述的革兰氏阴性厌氧菌和/或
革兰氏阳性厌氧菌引起的细菌感染的方法,其中所述革兰氏阴性和/或革兰氏阳性厌氧菌是非耐药的或耐药的。
[0129]
本发明还提供了用于治疗如本文所述的革兰氏阳性和革兰氏阴性需氧菌或厌氧菌引起的细菌感染的方法、化合物和/或用途,其包括向有需要的患者施用包含吉泊达星或其药学上可接受的盐的药物组合物。
[0130]
在另一个方面中,本发明涉及用于治疗由革兰氏阴性或革兰氏阴性需氧菌或厌氧菌引起的细菌感染的方法、化合物和/或用途,其中所述革兰氏阴性需氧菌是:
[0131]-不动杆菌属,选自鲍曼不动杆菌(acinetobacter baumannii)、无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)和皮蒂不动杆菌(acinetobacter pittii);
[0132]-嗜血杆菌属,选自副流感嗜血杆菌(haemophilus parainfluenzae)和副嗜沫嗜血杆菌(haemophilus paraphrophilus);
[0133]-克雷伯氏菌属,选自产酸克雷伯氏菌(klebsiella oxytoca)和变栖克雷伯氏菌(klebsiella variicola);或者
[0134]-变形杆菌属,选自变形杆菌(proteus hauseri)和潘纳氏变形杆菌(proteus peneri)。
[0135]
通过方法/用途治疗的适应症
[0136]
在本发明的另一个方面中,如本文所定义的尿路感染还可以包括急性尿路感染,其中由于突然、突然发作和严重、进展且需要紧急护理而发生的此类细菌感染。
[0137]
在另一个方面中,本发明涉及用于治疗由革兰氏阴性或革兰氏阳性需氧或需氧或厌氧菌引起的细菌感染的方法、化合物和/或用途,其中细菌感染通常选自尿路感染,其可以分别是但不限于非复杂性尿路感染和/或急性尿路感染,其可以包括但不限于膀胱炎或急性膀胱炎。
[0138]
膀胱炎是膀胱的感染。根据本发明,急性膀胱炎是由细菌感染引起的膀胱突然炎症,通常称为尿路感染(uti)。参见例如“泌尿系统感染指南”(欧洲泌尿学会),https://uroweb.org/guideline/urological-infections,其中将“非复杂性uti”解释为“急性、散发性或复发性低位(非复杂性膀胱炎)和/或上部(非复杂性肾盂肾炎)uti,仅限于在泌尿道内没有已知相关解剖和功能异常或合并症的非孕妇”。急性膀胱炎的症状可能会突然出现,常见的症状包括:即使排空膀胱后也有频繁和强烈的小便冲动;排尿困难,排尿时疼痛或灼热感;恶臭或强烈气味的尿液;尿液混浊;下腹部或背部中部有压迫感、膀胱胀满感或痉挛感;低烧;发冷;和/或尿液中存在血液。
[0139]
如本文所用,“膀胱炎”通常指膀胱的炎症,并且最常见的类型是“uti”。如本文所用,“急性非复杂性膀胱炎”与“非复杂性uti”或“uuti”同义。
[0140]
uuti可见于其他健康受试者,主要是女性,没有相关的泌尿道结构和功能异常、肾脏疾病或合并症,这些异常可能导致更严重的结局并需要额外关注。
[0141]
如本文所用,“复发性uuti”是指无并发症的uti复发,频率至少为每年3次或在过去六个月中至少2次。复发性uuti的治疗需要特殊考虑,例如通过尿培养诊断感染,例如鉴定中段尿样中的泌尿病原体。例如,在一个实施方式中,细菌计数至少103cfu/ml表示复发uuti。
[0142]
uti也可以是“复杂性uti”,这是一种与疾病相关的感染,例如泌尿生殖道的结构
或功能异常,或潜在疾病的存在,在没有确定风险因素或治疗失败的个体中,这会增加比uti预期更严重结局的风险。在本发明中,“uti的治疗”包括治疗非复杂性uti和治疗复杂性uti。
[0143]
在一个实施方式中,在本发明的任何方面中,尿路感染选自非复杂性尿路感染(uuti)、膀胱炎和急性膀胱炎。
[0144]
在一个实施方式中,在本发明的任何方面中,uti是非复杂性uti。在一个实施方式中,在本发明的任何方面中,uti是复杂性uti。在一个实施方式中,在本发明的任何方面中,人是女性。
[0145]
在一个实施方式中,在本发明的任何方面中,吉泊达星是吉泊达星的游离碱。
[0146]
在一个实施方式中,在本发明的任何方面中,吉泊达星是甲磺酸吉泊达星。
[0147]
在一个实施方式中,在本发明的任何方面中,uti复发性非复杂性uti。
[0148]
在一个实施方式中,在本发明的任何方面中,人是孕妇、青少年或儿童。如本文所用,“青少年”指年龄12、13、14、15、16或17岁(即,12-17岁(含))。如本文所用,“儿童”指年龄11岁或更小。
[0149]
在一个实施方式中,在本发明的任何方面中,所述人之前至少一种治疗失败。在一个实施方式中,此前的治疗可能是抗生素,如头孢菌素、碳青霉烯类、呋喃妥因、甲氧苄啶单独使用,或与磺胺、阿莫西林-克拉维酸、磷霉素或氟喹诺酮类药物,如环丙沙星、左氧氟沙星、吉米沙星、莫西沙星、诺氟沙星或氧氟沙星联合使用。可以根据已有指南定义治疗失败;例如,可以将在使用抗生素治疗3、4、5、6或7天后缺乏症状改善认为是失败。
[0150]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的细菌感染的方法、化合物和/或用途,其中吉泊达星的药学上可接受的盐是酸加成盐。
[0151]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的细菌感染的方法、化合物和/或用途,其中吉泊达星的酸加成盐是由以下形成的:[a]无机酸,选自盐酸、氢溴酸、硫酸、硝酸和磷酸;或者,[b]有机酸,选自醋酸、富马酸、琥珀酸、马来酸、柠檬酸、苯甲酸、对甲苯磺酸、甲磺酸、萘磺酸和酒石酸。
[0152]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的细菌感染的方法、化合物和/或用途,其中所述吉泊达星的酸加成盐是甲磺酸盐。
[0153]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的细菌感染的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0154]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)感染引起的细菌感染的方法、化合物和/或用途,其包括向有需要的患者施用药物组合物,所述药物组合物包含:
[0155]
[a]吉泊达星或其药学上可接受的盐;和
[0156]
[b]药学上可接受的赋形剂。
[0157]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的尿路感染的方法、化合物和/或用途,其包括向有需要的患者施用吉
泊达星或其药学上可接受的盐。
[0158]
在另一个方面中,本发明涉及一种治疗由腐生葡萄球菌(staphylococcus saprophyticus)和/或革兰氏阴性需氧菌引起的尿路感染的方法,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐;其中所述革兰氏阴性需氧菌选自:无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)、皮蒂不动杆菌(acinetobacter pittii)、副流感嗜血杆菌(haemophilus parainfluenzae)、副嗜沫嗜血杆菌(haemophilus paraphrophilus);产酸克雷伯氏菌(klebsiella oxytoca)或变栖克雷伯氏菌(klebsiella variicola);变形杆菌(proteus hauseri)或潘纳氏变形杆菌(proteus peneri)。
[0159]
在另一个方面中,本发明涉及一种治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli、耐药肺炎克雷伯氏菌(k.pneumoniae)引起的尿路感染的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0160]
在另一个方面中,本发明涉及一种治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli、耐药肺炎克雷伯氏菌(k.pneumoniae)引起的膀胱炎的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0161]
在另一个方面中,本发明涉及一种治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli、耐药肺炎克雷伯氏菌(k.pneumoniae)引起的急性膀胱炎的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0162]
在另一个方面中,如本文所述的本发明涉及用于治疗由本技术中定义的生物体引起的细菌感染和/或用于治疗更具体的感染的方法、化合物,其可以包括但不限于尿路感染,所述尿路感染包括但不限于非复杂性尿路感染(uuti)和/或膀胱炎,所述膀胱炎包括但不限于如本文所定义的急性膀胱炎。
[0163]
在另一个方面中,本发明还涉及:
[0164]-一种用于治疗由革兰氏阳性需氧菌和/或革兰氏阴性需氧菌引起的细菌感染的方法、化合物和/或用途;
[0165]-一种用于治疗由革兰氏阳性需氧菌引起的细菌感染的方法、化合物和/或用途,例如但不限于腐生葡萄球菌(staphylococcus saprophyticus);
[0166]-一种治疗尿路感染的方法、化合物和/或用途,其包括,但不限于:
[0167]
·
非复杂性尿路感染(uuti);
[0168]
·
膀胱炎;
[0169]
·
急性膀胱炎;
[0170]
·
复杂性uti;
[0171]-一种治疗细菌感染,如非复杂性尿路感染(uuti)和/或膀胱炎的方法、化合物和/或用途,其可以包括但不限于由耐药e.coli或耐药肺炎克雷伯氏菌(k.pneumoniae)引起的急性膀胱炎;
[0172]-一种用于治疗细菌感染的非复杂性尿路感染(uuti)和/或膀胱炎的方法、化合物和/或用途,其可以包括但不限于由腐生葡萄球菌(s.saprophyticus)引起的急性膀胱炎;
[0173]-一种用于治疗细菌感染的非复杂性尿路感染(uuti)和/或膀胱炎的方法、化合物和/或用途,其可以包括但不限于由革兰氏阴性细菌引起的急性膀胱炎;
[0174]
其中:
[0175]
每种前述或上文定义的方法或用途分别包括给药吉泊达星或其药学上可接受的盐和/或其相应的药物组合物,如贯穿本说明书全文所定义的。
[0176]
在另一个方面中,本发明涉及治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的膀胱炎的方法、化合物和/或用途,其中所述膀胱炎是急性膀胱炎。
[0177]
在另一个方面中,本发明涉及如本文和整个本说明书所定义的化合物的用途,其中由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli或耐药肺炎克雷伯氏菌(k.pneumoniae)引起的膀胱炎是急性膀胱炎。
[0178]
在一个实施方式中,本发明提供了一种治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的膀胱炎的方法,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0179]
在一个实施方式中,本发明提供了一种治疗非复杂性尿路感染、膀胱炎或急性膀胱炎的方法,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0180]
在一个实施方式中,本发明提供了一种治疗非复杂性尿路感染、膀胱炎或急性膀胱炎的方法,其包括向有需要的患者施用吉泊达星。
[0181]
在一个实施方式中,本发明提供了本发明提供了一种治疗非复杂性尿路感染、膀胱炎或急性膀胱炎的方法,其包括向有需要的患者施用药物组合物,所述药物组合物包含:
[0182]
[a]吉泊达星或其药学上可接受的盐;和
[0183]
[b]药学上可接受的赋形剂。
[0184]
在一个实施方式中,本发明提供了一种治疗由革兰氏阴性需氧菌引起的尿路感染的方法,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0185]
在一个实施方式中,本发明提供了一种用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli或耐药k.pneumoniae引起的非复杂性尿路感染、膀胱炎或急性膀胱炎的吉泊达星或其药学上可接受的盐。
[0186]
在一个实施方式中,本发明提供了吉泊达星或其药学上可接受的盐用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli、耐药k.pneumoniae或革兰氏阴性需氧菌引起的非复杂性尿路感染、膀胱炎或急性膀胱炎的用途。
[0187]
在另一个方面中,本发明涉及吉泊达星或其药学上可接受的盐治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的尿路感染的用途。
[0188]
在另一个方面中,本发明涉及吉泊达星或其药学上可接受的盐治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的膀胱炎的用途。
[0189]
在另一个方面中,本发明涉及吉泊达星或其药学上可接受的盐或其药学上可接受的盐治疗由腐生葡萄球菌(staphylococcus saprophyticus)引起的急性膀胱炎的用途。
[0190]
在另一个方面中,本发明涉及吉泊达星或其药学上可接受的盐治疗由革兰氏阴性需氧菌引起的尿路感染的用途。
[0191]
在另一个方面中,本发明涉及治疗由以下引起的感染的方法、化合物和/或用途:
[0192]-革兰氏阳性菌,选自腐生葡萄球菌(staphylococcus saprophyticus);或
[0193]-革兰氏阴性需氧菌,选自鲍曼不动杆菌(acinetobacter baumannii)、无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)、皮蒂不动杆菌(acinetobacter pittii)、弗氏柠檬酸杆菌复合体(citrobacter freundii complex)、克氏柠檬酸杆菌
(citrobacter koseri)、副流感嗜血杆菌(haemophilus parainfluenzae)、副嗜沫嗜血杆菌(haemophilus paraphrophilus)、产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、非脱羧勒克菌(leclercia adecarboxylata)、豪氏变形杆菌(proteus hauseri)、潘纳氏变形杆菌(proteus peneri)和粘质沙雷氏菌(serratia marcescens);
[0194]
其包括向有需要的受试者施用:
[0195]
[a]药物组合物,其包含吉泊达星或其药学上可接受的盐;和
[0196]
[b]药学上可接受的赋形剂。
[0197]
在另一个方面中,本发明涉及用于治疗由耐药e.coli或耐药k.pneumoniae引起的非复杂性尿路感染(uuti)、膀胱炎或急性膀胱炎的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0198]
在另一个方面中,本发明涉及用于治疗由耐药e.coli或耐药k.pneumoniae引起非复杂性尿路感染(uuti)、膀胱炎或急性膀胱炎的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星。
[0199]
在另一个方面中,本发明涉及用于治疗由耐药e.coli或耐药k.pneumoniae引起非复杂性尿路感染(uuti)、膀胱炎或急性膀胱炎的方法、化合物和/或用途,其包括向有需要的患者施用包含以下的药物组合物:
[0200]
[a]吉泊达星或其药学上可接受的盐;和
[0201]
[b]药学上可接受的赋形剂。
[0202]
在另一个方面中,本发明涉及用于治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli或耐药k.pneumoniae引起膀胱炎的方法、化合物和/或用途,其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0203]
在另一个方面中,本发明涉及用于治疗由革兰氏阴性和/或革兰氏阳性需氧菌引起的如本技术中所定义的细菌感染或其他疾病的方法、化合物和/或用途,其中革兰氏阴性和/或革兰氏阳性需氧菌是非耐药的或耐药的。
[0204]
在另一个方面中,本发明涉及用于治疗由革兰氏阴性和/或革兰氏阳性需氧菌引起的如本技术中所定义的细菌感染或其他疾病的方法、化合物和/或用途,其中所述革兰氏阴性和/或革兰氏阳性需氧菌是对抗生素耐药的,并且选自但不限于选自下组:氟喹诺酮类(包括环丙沙星)、阿奇霉素、四环素、呋喃妥因、甲氧苄啶/磺胺甲噁唑和磷霉素。
[0205]
在另一个方面中,本发明涉及用于治疗由革兰氏阴性和/或革兰氏阳性需氧菌引起的如本技术中所定义的细菌感染或其他疾病的方法、化合物和/或用途,其中革兰氏阴性需氧菌、耐药大肠杆菌(escherichia coli)或耐药k.pneumoniae对选自以下的抗生素具有抗性,但不限于:氨苄青霉素、甲氧苄啶-磺胺甲噁唑和环丙沙星/左氧氟沙星或头孢唑林。
[0206]
在另一个方面中,本发明涉及吉泊达星或其药学上可接受的盐用于在有需要的患者中治疗由耐药e.coli或耐药k.pneumoniae引起的非复杂尿路感染(uuti)、膀胱炎或急性膀胱炎的用途。
[0207]
在另一个方面中,本发明涉及药物组合物在有需要的患者中治疗由耐药e.coli或耐药k.pneumoniae引起的尿路感染(uuti)、膀胱炎或急性膀胱炎的用途,所述药物组合物包含:
[0208]
[a]吉泊达星或其药学上可接受的盐;和
[0209]
[b]药学上可接受的赋形剂。
[0210]
在另一个方面中,本发明涉及用于在有需要的患者中治疗由腐生葡萄球菌(staphylococcus saprophyticus)、耐药e.coli或耐药k.pneumoniae引起膀胱炎的吉泊达星或其药学上可接受的盐。
[0211]
在另一个方面中,本发明涉及用于治疗由以下引起的尿路感染的方法、化合物和/或用途:
[0212]-革兰氏阳性菌,选自腐生葡萄球菌(staphylococcus saprophyticus);或
[0213]-革兰氏阴性需氧菌,选自不动杆菌属、柠檬酸杆菌属、嗜血杆菌属、克雷伯氏菌属、脱羧蜡杆菌属、变形杆菌属和粘质沙雷氏菌(serratia marcescens);其中
[0214]-不动杆菌属,选自鲍曼不动杆菌(acinetobacter baumannii)、无硝鲍曼不动杆菌(acinetobacter baumannii anitratus)和皮蒂不动杆菌(acinetobacter pittii);
[0215]-柠檬酸杆菌属,选自弗氏柠檬酸杆菌复合体(citrobacter freundii complex)和克氏柠檬酸杆菌(citrobacter koseri),
[0216]-嗜血杆菌属,选自副流感嗜血杆菌(h.parainfluenzae)和副嗜沫嗜血杆菌(h.paraphrophilus);
[0217]-克雷伯氏菌属,选自产酸克雷伯氏菌(klebsiella oxytoca)和变栖克雷伯氏菌(klebsiella variicola);或
[0218]-变形杆菌属,选自变形杆菌(proteus hauseri)和潘纳氏变形杆菌(proteus peneri);
[0219]
其包括向有需要的患者施用吉泊达星或其药学上可接受的盐。
[0220]
在另一个方面中,本发明涉及一种用于治疗由以下引起的尿路感染的方法、化合物和/或用途:
[0221]-革兰氏阳性菌,选自腐生葡萄球菌(staphylococcus saprophyticus);或
[0222]-革兰氏阴性需氧菌,选自不动杆菌属、柠檬酸杆菌属、嗜血杆菌属、克雷伯氏菌属、脱羧蜡杆菌属、变形杆菌属或粘质沙雷氏菌(serratia marcescens);
[0223]-其中不动杆菌属选自鲍曼不动杆菌(acinetobacter baumannii)、无硝鲍曼不动杆菌(acinetobacter anitratus)和皮蒂不动杆菌(acinetobacter pittii);
[0224]-柠檬酸杆菌属选自弗氏柠檬酸杆菌复合体(citrobacter freundii complex)和克氏柠檬酸杆菌(citrobacter koseri),
[0225]-嗜血杆菌属选自副流感嗜血杆菌(h.parainfluenzae)和副嗜沫嗜血杆菌(h.paraphrophilus);
[0226]-克雷伯氏菌属选自产酸克雷伯氏菌(klebsiella oxytoca)和变栖克雷伯氏菌(klebsiella variicola);和
[0227]-变形杆菌属选自变形杆菌(proteus hauseri)和潘纳氏变形杆菌(proteus peneri);
[0228]
其包含向有需要的患者施用药物组合物,其包含
[0229]
[a]吉泊达星或其药学上可接受的盐;和
[0230]
[b]药学上可接受的赋形剂。
[0231]
在一个方面中,本发明提供了单独或分别用于治疗细菌感染(如uit)的如本文所定义的方法、化合物和/或用途,其由革兰氏阳性需氧菌引起,其中:
[0232]
所述革兰氏阳性需氧菌选自路敦葡萄球菌(staphylococcus lugdenensis)、无乳链球菌(streptococcus agalactiae)、f组链球菌(streptococcus group f)、g组链球菌(streptococcus group g)、头状葡萄球菌(staphylococcus capitis)、山羊葡萄球菌(staphylococcus caprae)、科氏葡萄球菌(staphylococcus cohnii)、表皮葡萄球菌(staphylococcus epidermidis)、溶血葡萄球菌(staphylococcus haemolyticus)、人葡萄球菌(staphylococcus hominis)、中间葡萄球菌(staphylococcus intermedius)、模仿葡萄球菌(staphylococcus simulans)、沃氏葡萄球菌(staphylococcus warneri)、咽峡炎链球菌(streptococcus anginosus)、澳大利亚链球菌(streptococcus australis)、星座链球菌(streptococcus constellatus)、嵴链球菌(streptococcus cristatus)、格氏链球菌(streptococcus gordonii)、婴儿链球菌(streptococcus infantarius)、婴幼儿链球菌(streptococcus infantis)、中间链球菌(streptococcus intermedius)、马西里链球菌(streptococcus massiliensis)、缓症链球菌(streptococcus mitis)、口腔链球菌(streptococcus oralis)、变形链球菌(streptococcus mutans)、副血链球菌(streptococcus parasanguinis)、唾液链球菌(streptococcus salivarius)、血链球菌(streptococcus sanguinis)和前庭链球菌(streptococcus vestibularis)。
[0233]
在本发明中使用的化合物
[0234]
wo2008/128942公开了吉泊达星的游离碱和盐酸盐的制备。
[0235]
此外,将理解的是,短语“吉泊达星或其药学上可接受的盐”旨在涵盖吉泊达星、吉泊达星a的药学上可接受的盐、吉泊达星的溶剂化物或者这些的任何药学上可接受的组合。因此,通过此处用于说明目的的非限制性实例,
“”
吉泊达星或其药学上可接受的盐”可以包括进一步作为溶剂化物存在的吉泊达星的药学上可接受的盐。
[0236]
如本文所用,术语“本发明的化合物”指任何形式的吉泊达星,即任何盐或非盐形式(例如,作为游离碱,或作为药学上可接受的盐)及其任何物理形式,例如,包括非固体形式(例如,液体或半固体形式)和固体形式(例如,无定形或结晶修饰、特定的多晶型形式、溶剂化合物,包括水合物),以及各种形式的混合物。
[0237]
适宜的药学上可接受的盐包括由berge,bighley和monkhouse j.pharm.sci(1977)66,pp 1-19描述的那些。
[0238]
当本发明的化合物是碱(包含碱性部分)时,可以通过本领域已知的任何适合的方法制备所需的盐形式,该方法包括将游离碱用无机酸处理,例如盐酸、氢溴酸、硫酸、硝酸、磷酸等,或将游离碱用有机酸处理,例如乙酸、三氟乙酸、马来酸、琥珀酸、扁桃酸、富马酸、丙二酸、丙酮酸、草酸、乙醇酸、水杨酸、吡喃糖苷酸(例如葡萄糖醛酸或半乳糖醛酸)、α-羟基酸(例如柠檬酸或酒石酸)、氨基酸(例如天冬氨酸或谷氨酸)、芳香族酸(例如苯甲酸或肉桂酸)、磺酸(例如对甲苯磺酸、甲磺酸、乙磺酸等)。药学上可接受的盐的实例包括硫酸盐、焦硫酸盐、硫酸氢盐、亚硫酸盐、亚硫酸氢盐、磷酸盐、氯化物、溴化物、碘化物、乙酸盐、丙酸盐、癸酸盐、辛酸盐、丙烯酸盐、甲酸盐、异丁酸盐、己酸盐、庚酸盐、丙酸盐、草酸盐、丙二酸盐、琥珀酸盐、辛二酸盐、癸二酸盐、富马酸盐、马来酸盐、丁炔-1,4-二酸盐、己炔-1,6-二酸盐、苯甲酸盐、氯苯甲酸盐、甲基苯甲酸盐、二硝基苯甲酸盐、羟基苯甲酸盐、甲氧基苯甲酸
盐、邻苯二甲酸盐、苯乙酸盐、苯丙酸盐、苯丁酸盐、柠檬酸盐、乳酸盐、g-羟基丁酸盐、乙醇酸盐、酒石酸盐、扁桃酸盐和磺酸盐,例如二甲苯磺酸盐、甲磺酸盐、丙磺酸盐、萘-1-磺酸盐和萘-2-磺酸盐。
[0239]
吉泊达星的药学上可接受的盐包括酸加成盐,例如其与无机酸的盐,例如,盐酸、氢溴酸、硫酸硝酸或磷酸,或有机酸,例如,乙酸、富马酸、琥珀酸、马来酸、柠檬酸、苯甲酸、对甲苯磺酸、甲磺酸、萘磺酸或酒石酸。
[0240]
本发明在其范围内包括所有可能的化学计量和非化学计量的盐形式。
[0241]
本发明还包括本发明化合物或其药学上可接受的盐的各种氘代形式。每个与碳原子相连的可用氢原子可以独立地被氘原子取代。例如,氘代材料,如烷基可以通过常规技术制备(参见例如:甲基-d3-胺可获自aldrich chemical co.,milwaukee,wi,目录号489,689-2)。
[0242]
药物组合物和制剂
[0243]
可接受和适用于本发明的方法和/或用途的药物组合物和制剂是使用本领域已知的药物组合物、制剂或化学材料、处方赋形剂、制备手段、工艺和/或方法以及常规技术等制备的。
[0244]
特别地,本发明中使用的吉泊达星或其药学上可接受的盐可以通过与其他抗菌剂/抗结核化合物类似的方式配制成用于以任何方便的方式用于人类或兽药的施用。
[0245]
本发明中使用的药物组合物可以配制成通过任何途径施用,包括适合口服、局部或肠胃外使用的形式的药物组合物,并且可以用于哺乳动物,包括人。
[0246]
组合物可以是片剂、胶囊剂、粉剂、颗粒剂、锭剂、栓剂、乳膏剂或液体制剂,如口服或无菌肠胃外溶液剂或混悬剂。
[0247]
在一个实施方式中,本发明的吉泊达星或其药学上可接受的盐为片剂或胶囊剂形式。在一个实施方式中,其是片剂形式。在一个实施方式中,所述片剂是750mg片剂。
[0248]
制剂还可以含有相容的常规载体,如乳膏或软膏基质以及用于洗剂的乙醇或油醇。
[0249]
本发明中用于口服给药的片剂和胶囊剂可以是单位剂量形式,并且可以含有常规赋形剂,如粘合剂、填充剂、压片润滑剂、崩解剂或润湿剂。可以根据常规制药实践中众所周知的方法对片剂进行包衣。口服液体制剂可以是例如水性或油性悬浮液、溶液、乳剂、糖浆或酏剂的形式,或者可以作为干燥产品存在,以便在使用前用水或其他合适的赋形剂重新配制。此类液体制剂可包含常规添加剂,如悬浮剂,例如山梨糖醇、甲基纤维素、葡萄糖浆、明胶、羟乙基纤维素、羧甲基纤维素、硬脂酸铝凝胶或氢化食用脂肪、乳化剂,例如卵磷脂、脱水山梨糖醇单油酸酯或阿拉伯树胶;非水性载体(其可以包括食用油),例如杏仁油、油性酯如甘油、丙二醇或乙醇;防腐剂,例如对羟基苯甲酸甲酯或丙酯或山梨酸,以及,如果需要,常规调味剂或着色剂。
[0250]
栓剂将包含常规栓剂基质,例如,可可脂或其他甘油酯。
[0251]
对于肠胃外给药,使用化合物和无菌载剂制备流体单位剂型,优选水。根据所使用的载体和浓度,化合物可以悬浮或溶解在载剂中。在制备溶液时,可将化合物溶解在注射用水中并过滤灭菌,然后装入合适的小瓶或安瓿并密封。
[0252]
有利地,诸如局部麻醉剂、防腐剂和缓冲剂之类的试剂可以溶解在载剂中。为了提
高稳定性,组合物可以在装入小瓶后冷冻,并在真空下除去水。然后将干燥的冻干粉末密封在小瓶中并且可以提供伴随的注射用水小瓶以在使用前重构液体。肠胃外悬浮液以基本相同的方式制备,不同之处在于化合物悬浮在载剂中而不是溶解,并且不能通过过滤实现灭菌。该化合物可以通过在悬浮在无菌载剂中之前暴露于环氧乙烷进行灭菌。有利地,组合物中包含表面活性剂或润湿剂以促进化合物的均匀分布。
[0253]
此外,用于本发明的化合物或药物组合物的给药量将根据患者和给药方式而变化,并且可以是任何有效量。
[0254]
根据本发明的任何给药方法,术语“治疗有效量”,如本文所用,在其含义内通常包括无毒但足够量的特定药物,其所指的是提供所需的治疗效果。所需的确切数量因受试者而异,具体取决于患者的总体健康状况、患者的年龄等因素。
[0255]
本领域普通技术人员也可以容易地确定用于施用本发明中使用的化合物和/或药物组合物的治疗方案。本发明中使用的化合物和/或药物组合物的给药量可以在很宽的范围内变化,以在单位剂量中提供基于患者每天体重的有效量以实现所需的效果。
[0256]
取决于施用方法,组合物可以含有0.1重量%,优选10-60重量%的活性物质。当组合物包含剂量单位时,每个单位将优选包含50-100mg的活性成分。
[0257]
除非另有说明,活性成分(即吉泊达星)的量是指吉泊达星游离碱的量。
[0258]
根据给药途径和频率,本发明中用于成人治疗的剂量优选为每天100至3000mg,例如每天1500mg。这样的剂量对应于每天约1.5至约50mg/kg(每公斤患者体重mg的吉泊达星)。适宜的剂量为每天5至30mg/kg。在一个实施方式中,剂量是1500mg,每天两次(即,3000mg每天)。在一个实施方式中,一天中的两个剂量间隔6-12小时。
[0259]
因此,在一个实施方式中,本发明提供了一种治疗尿路感染(uti)的方法,其包括向有需要的人施用治疗有效量的吉泊达星或其药学上可接受的盐,其中所述uti是由本发明的第一个方面中定义的一种或多种细菌引起的,并且吉泊达星或其药学上可接受的盐以1500mg每天两次施用,间隔6-12小时。
[0260]
特别地,本发明的组合物以单位剂量存在并且优选每天服用1至5次,如每天服用一次或两次以达到期望的效果。在一个实施方式中,吉泊达星或其药学上可接受的盐连续施用3、4、5、6或7天中的任何天。在一个实施方式中,在本发明的任何方面中,吉泊达星或其药学上可接受的盐施用连续5天。
[0261]
常规施用方法可适用于本发明。根据所进行的治疗,本发明的化合物和/或组合物可以口服、血管内、腹膜内、皮下、肌肉内或局部施用。优选地,该组合物适于口服施用。
[0262]
在本发明中使用的epotidacin或其药学上可接受的盐可以是本发明组合物中的唯一治疗剂或与其他抗菌剂的组合。如果另一种抗菌剂是β-内酰胺,则也可以使用β-内酰胺酶抑制剂。
[0263]
下面列出的实施例是对本发明的说明,并不打算以任何方式限制本发明的范围。
[0264]
实施例
[0265]
除非另有说明,临床和实验室标准协会(clsi)推荐的程序如clsi批准标准m07版本中所述。测试时采用对需氧生长的细菌进行稀释抗菌药敏试验的方法。
[0266]
实施例1
[0267]
生物活性测定(体外测定)
variicola)、非脱羧勒克菌(leclercia adecarboxylata)和粘质沙雷氏菌(serratia marcescens)(对上面列出的每种生物的至少一种菌株的mic≤8μg/ml)的体外活性。
[0285]
针对方法2的其他信息
[0286]
材料/方法:
[0287]
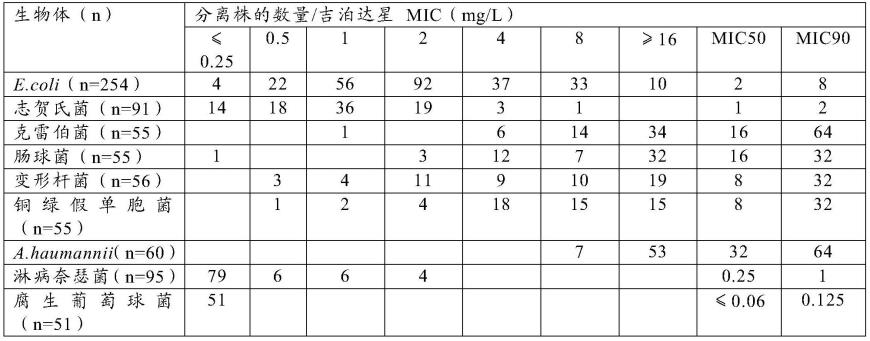
该嵌板包含511种肠杆菌(以前称为肠杆菌科),包括e.coli、产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、肺炎克雷伯氏菌(klebsiella pneumoniae)、产气肠杆菌(enterobacter aerogenes)、阴沟肠杆菌复合菌(enterobacter cloacae complex)、奇异变形杆菌(proteus mirabilis)、彭氏变形杆菌(proteus penneri)、变形杆菌(proteus hauseri)和鲍氏志贺氏菌(shigella boydii)、弗氏志贺菌(shigella flexneri)和宋内氏志贺菌(shigella sonnei),富集以包括具有esbl、ampc或碳青霉烯酶的分离株;55种铜绿假单胞菌(pseudomonas aeruginosa),选择以包括因oprd丢失和/或外流而具有碳青霉烯酶、esbl或碳青霉烯耐药性的分离株;95个淋病奈瑟菌(neisseria gonorrhoeae),包括对β-内酰胺类、环丙沙星、阿奇霉素、四环素或壮观霉素具有耐药性或敏感性降低的淋病奈瑟菌;和51个腐生葡萄球菌(staphylococcus saprophyticus)分离株。
[0288]
根据clsi琼脂稀释指南确定mic。
[0289]
结果:
[0290]
吉泊达星对e.coli的mic范围≤0.06-64mg/l,浓度≤8mg/l时对测试分离株的抑制率为96.1%。吉泊达星对e.coli的活性不受左氧氟沙星非易感性或gyra和parc的qrdr中与喹诺酮耐药性相关的氨基酸取代的影响(可用于254株e.coli分离株中的188株)。吉泊达星mic分布也与β-内酰胺酶耐药机制无关;100%的ndm、94.6%的kpc和92.1%的oxa-48样生产e.coli在≤8mg/l的吉泊达星时被抑制。
[0291]
吉泊达星对志贺氏菌的mic范围为0.125-8mg/l,95.6%的测试分离株在≤2mg/l时被抑制,100%在≤8mg/l时被抑制。具体而言,吉泊达星对鲍氏志贺氏菌(shigella boydii)(n=3)的mic为2mg/l;吉泊达星对弗氏志贺菌(shigella flexneri)(n=24)的mic90为2mg/l,而对宋内氏志贺菌(shigella sonnei)(n=64)的mic90为2mg/l。吉泊达星的活性不受左氧氟沙星非易感性或gyra和parc qrdr中氨基酸取代的影响(数据可用),吉泊达星mic分布也与β-内酰胺酶耐药机制无关。
[0292]
吉泊达星针对克雷伯氏菌(产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯氏菌(klebsiella variicola)、肺炎克雷伯氏菌(klebsiella pneumoniae))、肠杆菌(产气肠杆菌(enterobacter aerogenes)、阴沟肠杆菌复合菌(enterobacter cloacae complex))和变形杆菌(奇异变形杆菌(proteus mirabilis)、彭氏变形杆菌(proteus penneri)、变形杆菌(proteus hauseri))的mic范围更高,其mic90分别为64、32和32mg/l。具体地,吉泊达星对产酸克雷伯氏菌(klebsiella oxytoca)、变栖克雷伯菌(klebsiella variicola)、变形杆菌(proteus hauseri)、彭氏变形杆菌(proteus penneri)的mic至少为4mg/l;在每种情况下,至少针对一种分离株。
[0293]
测试的所有肠杆菌科细菌的mic与左氧氟沙星耐药性或gyra和parc的qrdr中的氨基酸取代无关。
[0294]
p.aeruginosa和a.baumannii的mic90分别为32和64mg/l,与左氧氟沙星耐药无
关。
[0295]
所有s.saprophyticus的mic均≤0.125mg/l(与方法2中显示的数据相同)。
[0296]
表1
[0297][0298]
结论:
[0299]
吉泊达星针对腐生葡萄球菌(s.saprophyticus)具有体外活性(100%≤0.125mg/l)。
[0300]
在8mg/l时,吉泊达星对耐药性e.coli(96.1%)和志贺氏菌(100%)具有活性,但对其他测试的革兰氏阴性菌的活性较低。
[0301]
方法3
[0302]
抗菌活性通过使用clsi推荐程序的肉汤微量稀释来确定。
[0303]
化合物在连续两倍稀释中进行测试,将最小抑制浓度(mic)确定为抑制可见生长的化合物的最低浓度。
[0304]
特别是,针对来自俄亥俄州韦斯特莱克的laboratory specialists,inc.的分离株集合中的6株腐生葡萄球菌(staphylococcus saprophyticus),对吉泊达星进行了测试。
[0305]
研究中将左氧氟沙星作为阳性对照,以确定尿液对吉泊达星对腐生葡萄球菌(staphylococcus saprophyticus)的体外活性的影响。根据clsi方法通过肉汤微量稀释确定mic。
[0306]
吉泊达星的最低抑菌浓度(mic)范围是0.03-0.5μg/ml针对3株对甲氧西林易感的腐生葡萄球菌(s.saprophyticus)分离株和0.06-0.5μg/ml针对3株甲氧西林耐药腐生葡萄球菌(s.saprophyticus)分离株。针对甲氧西林易感的腐生葡萄球菌(s.saprophyticus),吉泊达星的mic值比左氧氟沙星低8-32倍,针对每种甲氧西林耐药的腐生葡萄球菌(s.saprophyticus),其mic值比左氧氟沙星低4倍。
[0307]
测试了至少一种示例性的吉泊达星盐(如甲磺酸盐)。
[0308]
吉泊达星对至少一种对甲氧西林易感或对甲氧西林耐药的腐生葡萄球菌(s.saprophyticus)菌株的mic≤0.5μg/ml。
[0309]
下表中显示的数据是用上述相同的腐生葡萄球菌(s.saprophyticus)分离株进行的体外研究的结果,以确定尿液对吉泊达星和左氧氟沙星对腐生葡萄球菌(s.saprophyticus)的体外活性的影响。根据参考clsi肉汤微量稀释方法,使用阳离子调整的mueller hinton肉汤(camhb)并添加25%、50%和100%尿液(未调整ph,ph 6.42)和100%尿液(调整ph,7.31和8.07),测试研究菌株的mic(最低抑制浓度)。在100%混合尿液
中,吉泊达星和左氧氟沙星的mic结果(平均稀释度差异)略高(平均稀释度差异为0.67-1.54),但似乎不是ph值的函数。
[0310]
表2:clsi mic肉汤微量稀释参考方法(camhb)对尿液条件的比较
[0311][0312][0313][0314]
总之,这些研究表明,吉泊达星对于对甲氧西林易感的和对甲氧西林耐药的s.saprophyticus分离株具有体外活性,测得mic≤0.5μg/ml,并且略高于在100%尿液中的mic(平均稀释度差异1.18-1.54)。令人惊讶的是,吉泊达星的活性不受尿液的显着影响,并使其成为uti的合适治疗选择。
[0315]
实施例2:在健康和感染参与者的组织和体液中吉泊达星的分布和暴露
[0316]
抗生素靶点暴露起着关键作用,因为次优水平可能导致治疗失败和耐药性。在多项临床研究中,评估了血浆和其他基质(如尿液、唾液、上皮内衬液(elf)和肺泡巨噬细胞(am)中吉泊达星的暴露量。
[0317]
收集支气管肺泡灌洗样品以确定健康受试者单次1000mg iv输注2小时后在elf和am中的吉泊达星暴露量。在150mg口服单次给药后在健康志愿者中评估唾液暴露量。在患有急性uuti的女性中,在口服1500mg bid 5天后,评估了尿液中的吉泊达星暴露量。
[0318]
elf和am auc(0-12)与未结合血浆的比率分别为1.84和178,表明良好的elf暴露和出色的细胞渗透。唾液浓度与血浆浓度呈线性关系(r2=0.76)。唾液auc与未结合血浆auc的比率接近于1。uuti患者尿液中的吉泊达星暴露量(auc[0-tau])很高(第1天为3742μg
·
h/ml;第4天为5973μg
·
h/ml)。从第3天起,尿液ctau暴露范围为322至352μg/ml。在12小时的给药间隔内,最低吉泊达星尿液浓度保持高于4μg/ml的mic。uuti参与者的吉泊达星肾脏排泄高于健康受试者(剂量的20%与7.5%)。从患有急性uuti的女性身上采集的拭子测量了吉泊达星的游离药物浓度。
[0319]
总之,吉泊达星表现出有利的分布特征,如增强的细胞内渗透,elf水平优于血浆和唾液暴露类似于血浆。此外,高尿暴露量涵盖了治疗uti的目标mic值。
[0320]
实施例3:评价吉泊达星治疗非复杂性尿路感染的ii期研究
[0321]
方法:
[0322]
这项iia期单中心研究在患有急性膀胱炎的女性受试者中评估了口服吉泊达星1500mg bid 5天的安全性、耐受性、药代动力学和有效性。通过标准方法获得清洁捕获的中段尿标本用于定量培养。在治疗前(基线)和所有基线后访视时从所有参与者采集尿液样品。所有尿液样本均送至中心实验室(ppd global clinical laboratories,highland heights,ky,usa)进行革兰氏染色、定量培养、病原体鉴定和药敏试验。参与者分布和研究大纲见图1。
[0323]
a.微生物研究
[0324]
进行了clsi肉汤微量稀释和梯度扩散(仅磷霉素)的易感性测试(clsi,2015,需氧细菌的稀释抗菌易感性测试方法;批准的标准第十版;和clsi,2018,抗菌药物易感性测试的性能标准;第二十七次信息补充m100-s28)。纳入微生物意向治疗人群(微-itt),需要符合条件的基线尿路病原体的生长(≥105cfu/ml)。基线算法参见图2。将微生物学成功定义为培养确认根除合格基线尿路病原体(无生长,《103cfu/ml),并在治愈测试(toc;第10-13天)和随访访视(第28天)时确定。
[0325]
出于本研究的目的,将多药耐药(mdr)定义为对≥3种相关抗生素类别具有抗性的泌尿病原体;并且,将超广谱β-内酰胺酶(esbl)产生定义为e.coli和k.pneumoniae泌尿病原体使用头孢他啶、氨曲南、头孢噻肟或头孢曲松的mic≥2μg/ml。
[0326]
结果:
[0327]
在22名参与者中,8名(36%)具有符合基线条件的泌尿病原体(5名e.coli、1名s.saprophyticus、1名k.pneumoniae和1名c.koseri)并且包括在微-itt中。14名参与者(64%)不具有符合基线条件的泌尿病原体(表3)。
[0328]
表3:基线疾病特征总结-回收的符合条件的泌尿病原体(意向治疗人群)
[0329][0330][0331]
*每个参与者仅回收1个泌尿病原体。
[0332]
吉泊达星针对8种符合条件的泌尿病原体的mic范围为0.06-4μg/ml。两个e.coli分离株是多药耐药的(定义为对≥3个抗生素类别耐药),由于其对氨苄西林、甲氧苄啶-磺胺甲噁唑和环丙沙星/左氧氟沙星或头孢唑林耐药。一个另外的e.coli分离株是氨苄西林耐药的。参见表4。
[0333]
表4:选定的抗e.coli抗生素的mic(μg/ml)(微-itt群,基线访视)
[0334][0335]
a.mdr和氟喹诺酮抗性;b.mdr
[0336]
b.如由m100-s29 clsi断点定义的抗性
[0337]
所有其他结果显示了如由m100-s29 clsi断点定义的易感性
[0338]
针对符合条件的泌尿病原体的微生物学应答
[0339]
治愈试验(toc)和随访时的微生物应答见表5。toc(e.coli)的一个微生物失败是由于无法报告(不稳定)的尿液样本,而不是泌尿病原体的持续生长造成的。在微-itt人群中,治疗后仅2个分离株观察到了生长,包括在第3天时的1个e.coli分离株和在随访期时的1个c.koseri分离株。图3显示了随着时间的推移(微-itt人群)基线定性泌尿病原体的定量细菌计数(cfu/ml)。在微-itt的8名参与者中,在toc和随访期访视时分别获得了7次(88%)和6次(75%)微生物学成功。
[0340]
表5:在toc和随访期访视时的微生物学应答总结(微-itt人群)
[0341][0342]
a.将在toc访视时认为微生物学失败的参与者认为在随访期访视时的微生物学失败。将不能确定微生物学结局认为是微生物学失败。
[0343]
符合条件的泌尿病原体的抗菌药物敏感性
[0344]
2个符合条件的其他革兰氏阴性尿路病原体(c.koseri和k.pneumoniae)均对氨苄西林具有抗性,并且对所有其他测试的抗微生物剂均敏感。1个符合条件的s.saprophyticus泌尿病原体对所有测试的抗菌剂菌敏感。回收的基线泌尿病原体无一对呋喃妥因、磷霉素、哌拉西林/他唑巴坦或美罗培南耐药。没有回收到表型产esbl的泌尿病原体。没有证据表明基线时获得的泌尿病原体和随后访视时相同的泌尿病原体之间对吉泊达星的敏感性降低(定义为mic增加≥4倍)。
[0345]
对于具有可用稳态pk、符合肠杆菌科泌尿病原体条件且在toc微生物学上取得成功的4名参与者,血浆fauc24h/mic范围为7至90.5,尿液auc24h/mic范围为1292至121,698。血浆fauc/mic(7)和尿液auc24h/mic(1292)最低的参与者具有k.pneumoniae,吉泊达星mic为4μg/ml。
[0346]
除了上述符合条件的泌尿病原体以外,还确定了两种基线泌尿病原体的mic值,这些病原体由于在较低的细菌计数(《105cfu/ml)下被回收而没有资格纳入微生物治疗人群:皮蒂不动杆菌(acinetobacter pittii)(mic 1mg/l)和弗氏柠檬酸杆菌复合体(citrobacter freundii complex)(mic 1mg/l)。
[0347]
pk/pd:
[0348]
对于具有可用稳态pk、符合肠杆菌科泌尿病原体条件且在toc微生物学上取得成功的4名参与者,血浆fauc24h/mic范围为6.99-90.5,尿液auc24h/mic范围为1292至121,698(表6)。血浆fauc/mic(6.99)和尿液auc24h/mic(1292)最低的参与者具有k.pneumoniae,吉泊达星mic为4μg/ml,且具有微生物学成功(表6)。
[0349]
表6:根据基线时分离的符合要求的泌尿病原体在toc和随访期访视时血浆和尿液pk/pd和微生物学应答的总结(微-itt人群)
[0350][0351]
a.mdr和氟喹诺酮抗性
[0352]
b.由于尿液样本稳定性不合格而失败
[0353]
c.将在toc访视时的微生物学失败认为是在随访期访视时的微生物学失败
[0354]
d.mdr
[0355]
na=不可用(稳态pk不可用);gep=吉泊达星
[0356]
结论
[0357]
在微-itt人群中,在toc和随访期时,分别有8名参与者中的7名(88%)和8名参与者中的6名(75%)达到微生物学成功。针对回收的所有基线泌尿病原体,吉泊达星mic值的范围从0.06至4μg/ml。没有参与者出现治疗后泌尿病原体对吉泊达星的敏感性降低(即,吉泊达星mic增加≥4倍)。
[0358]
b.iia期研究的临床有效性和安全性分析
[0359]
方法:
[0360]
对第1天的第1剂研究治疗和第4天的时间匹配给药进行了系列血液和尿液pk采样。参与者将所有剂量的吉泊达星与食物一起服用并留在诊所完成总10剂。指示参与者返回进行toc(第10至13天)和随访期(第28
±
3天)访视。
[0361]
结果:
[0362]
探索性终点总结(itt人群)。
[0363]
临床有效性:在治疗的24至48小时内,所有受试者的临床症状(排尿困难、尿频、尿急、下腹痛)均有显着改善。大多数受试者(20/22;90.9%)在治愈测试(toc)和随访(f/u)中实现了症状消退。微生物根除的实现与基线cfu无关。
[0364]
安全性终点:大多数常见ae出现在消化道(腹泻18/22[82%]&恶心17/22[77%])。根据研究者的观察,重复给药观察到对恶心的耐受性。没有因ae的退出。在安全性实验室评估、ecg或生命体征方面没有临床相关的趋势。
[0365]
其他信息
[0366]
结果
[0367]
有关个体临床症状评分和总评分随时间变化的箱线图(意向治疗人群),请参见图4。注:该方框代表25%到75%的百分位数。在方框内,水平线是中位数,方点是平均值。上下须代表1.5倍四分位距。空心圆圈代表个体参与者异常值分数。
[0368]
对于由排尿困难、尿频、尿急和下腹部或耻骨上疼痛组成的4类急性膀胱炎症状,基线时itt人群的平均总临床症状评分为7.9(范围:4至12)(每个类别的评分范围为0至3)。在入组该iia期研究的22名参与者中,在toc和随访期访视时分别有19名(86%)和18名(82%)参与者达到临床成功的临床应答。在toc时,在19名参与者(1名参与者退出研究;1名参与者未报告分数,和1名参与者未完成给药[6剂]的评分为2分)中实现了症状恢复(即,临床体征和症状评分为0)。在随访期,在20名参与者(2名参与者退出研究)中实现了症状恢复。基线时的下腹部或耻骨上疼痛是变化最大的症状类别,一半的参与者报告低分0(27%)或1(23%),另一半参与者报告高分2(41%)或3(9%)。对于其他症状类别,大多数参与者的评分为2分。
[0369]
表7:按照系统器官分类和首选术语的不良事件》5%的总结
[0370][0371][0372]
参与者在给药期间住院,最常见的不良事件涉及胃肠道;所有gi ae的强度均为轻度或中度,在第1天发作时,重复给药后有所改善。4名参与者的呕吐发作被认为与药物有关,其为轻度或中度,且不受治疗限制。止吐药的使用不常见且持续时间较短。吉泊达星的安全性与之前研究中观察到的相似,胃肠道事件主要是轻度或中度严重程度,报告为最常见的ae。
[0373]
结论
[0374]
安全性:总体而言,以1500mg bid的剂量口服吉泊达星5天是可以耐受的,没有剂量限制性ae。报告最多的ae涉及胃肠道(例如,主要是腹泻和恶心)。根据研究者的观察,重复给药观察到对恶心的耐受性。没有因ae而退出或停止研究治疗。安全性实验室参数、生命体征或ecg间隔没有临床显着变化。
[0375]
c.血浆和尿液药代动力学
[0376]
方法:
[0377]
对于药代动力学评估,在第1天和第4天早晨给药后至给药后12小时(
t
)收集系列血液和尿液样本,以评估吉泊达星pk浓度。在第1-5天收集c
t
(谷值)浓度。使用经验证的lc-ms/ms生物分析测定法测量血浆和尿液中吉泊达星的pk浓度。
[0378]
结果:
[0379]
吉泊达星快速吸收,其中位t
max
值为1.50至1.92小时。在bid给药后第3天达到稳态,在血浆中中度蓄积(1.4倍),这与6.6小时的有效消除半衰期一致。稳态尿液谷浓度较高,并在12小时内保持在4μg/ml的最低抑菌浓度(mic)以上。在第1天的12小时给药间隔内,大约20%的剂量从尿液中排泄,在第4天增加到31%。尿液auc(0-24)(11,945μg
·
hr/ml)高于游离血浆auc(0-24)(39.4μg
·
hr/ml)。与i期健康受试者相比,在uuti患者中观察到的吉泊达星血浆和尿液暴露量略高。
[0380]
血浆
[0381]
每天重复口服施用1500mg两次后,吉泊达星的血浆浓度迅速达到峰值,中位t
max
值为1.50和1.92小时(分别为第1天和第4天),并以多相方式下降。根据c
t
(谷值)血浆浓度,第3天达到稳态。根据auc观察到吉泊达星中等1.4倍蓄积,这与6.6小时的有效消除半衰期一致。参见图5,针对在bid口服给药吉泊达星(1500mg)后按天计算的吉泊达星中值c
t
血浆浓度,以及参见图6,针对单次和bid口服给药(1500mg)后的吉泊达星中位血浆浓度-时间曲线。
[0382]
表8:针对关键吉泊达星血浆pk参数的几何平均值(%cvb)估计值
[0383]
参数(单位)第1天第4天auc(0-t)(μg
·
hr/ml)20.2(28.6)[n=20]29.3(31.8)[n=21]cmax(μg/ml)5.89(47.3)[n=20]8.44(38.0)[n=21]ct(μg/ml) 0.851(41.1)[n=21]
[0384]
尿液
[0385]
每天重复口服两次1500mg吉泊达星后,稳态尿谷浓度很高,并且在12小时给药间隔内保持高于4μg/ml的mic。在第1天的12小时给药间隔内,大约20%的吉泊达星剂量从尿液中排泄,在第4天增加到31%。在第4天,吉泊达星的稳态尿液auc(0-24)(11,945μg
·
hr/ml)高于游离血浆auc(0-24)(39.3mg
·
h/ml)。
[0386]
表9:针对关键吉泊达星尿液pk参数的几何平均值(%cvb)估计值
[0387]
参数(单位)第1天第4天auc(0-t)(μg
·
hr/ml)3742(93.9)[n=16]5973(87.2)[n=18]ct(μg/ml) 327(248.7)[n=21]
[0388]
单次和bid口服施用吉泊达星(1500mg)后的中位尿液浓度时间曲线见图7。
[0389]
pk/pd
[0390]
每天重复两次口服1500mg后,在基线访视时具有符合条件的e.coli泌尿病原体的4名参与者中,平均吉泊达星尿液auc(0-24)/mic比值(15,914)高于吉泊达星游离血浆auc(0-24)/mic比值(37.0)。
[0391]
结论
[0392]
在第3天时达到稳态吉泊达星血浆暴露。bid给药后,吉泊达星在血浆中有中度
(1.4倍)蓄积。稳态尿液吉泊达星暴露量(auc[0-24])超过游离血浆暴露量约300倍。针对常见uuti病原体,如e.coli,尿液浓度也高于吉泊达星mic
90
值(mic
90
=4μg/ml)。考虑到膀胱是急性膀胱炎的主要感染部位,这支持使用吉泊达星治疗本发明所述的uti。在这项iia期研究中证明的吉泊达星的有效性提供了进一步的支持。
[0393]
实施例4:吉泊达星在小鼠肾盂肾炎和大腿感染模型中的药代动力学-药效学(pk-pd)
[0394]
本研究的目的是表征在中性粒细胞减少症小鼠大腿和肾盂肾炎模型中,吉泊达星针对5种e.coli分离株的药代动力学-药效学(pk/pd)关系,涵盖mic范围(1至4μg/ml),以支持潜在的尿路感染适应症的剂量选择。
[0395]
方法:
[0396]
在小鼠(雄性cd-1小鼠)大腿和肾感染中进行使用吉泊达星的pk和pd研究。所施用的剂量范围为从感染后1h开始每6小时sc 1至200mg/kg。在感染后24h,针对细菌负荷对感染组织进行评价(基线对照在感染后1h时)。
[0397]
在15、30、60、120、240和360分钟收集血浆和组织样品(肾或大腿匀浆)。在nonmem中使用血浆暴露量构建群体pk(poppk)模型。
[0398]
在大腿感染中性粒细胞减少(i-)小鼠中针对e.coli all、997577、atcc25922、ir5和nctc13441(mic 1至4μg/ml)和在肾脏感染免疫功能正常(i+)和i-小鼠中针对e.coli all确定了有效性。将poppk模型用于确定与有效性相关的gep暴露量。使用phoenix winnonlin 6.3(pharsight)进行pk-pd分析。log
10
集落形成单位(cfu)相对于基线的变化与游离药物(f)auc:mic相关,使用来自phoenix库的抑制模型,将每个分离株的模型参数值用于计算与在cfu中停滞、1或2-log
10
降低相关的血浆fauc:mic。
[0399]
结果:
[0400]
通过使用1阶消除的1室iv模型将血浆pk数据最佳拟合,并且其在i+vs.i-以及大腿vs.肾感染小鼠中像似。
[0401]
吉泊达星在肾脏中的auc
0-6
比血浆中的auc
0-6
高约4至5倍,而大腿中的auc
0-6
约为血浆的一半。
[0402]
在大腿模型中,在cfu中停滞、1或2-log
10
降低的中位血浆fauc:mic比值分别为11、16和25(范围3-17、4-25和7-40)。在大腿或肾脏中感染的i-小鼠中有效性vs.e.coli all相似。在i+小鼠中,pk-pd目标降低一半。
[0403]
结论:
[0404]
中位fauc:mic目标范围从11至25。在肾盂肾炎对比大腿感染模型中,肾脏与血浆或大腿中较高的药物水平并没有转化为更高的有效性。
[0405]
实施例4中的其他信息
[0406]
方法
[0407]
药代动力学研究
[0408]
在整个pk和pd研究中使用重量~27g的无特定病原体雄性cd-2小鼠。对于大多数研究,小鼠在第-4天(150mg/kg)和第-1天(100mg/kg)用两个ip剂量的环磷酰胺使中性粒细胞减少。单次皮下(sc)给药6.25-200mg/kg后,在给药后15、30、60、120、240和360分钟从功能正常或中性粒细胞减少的感染小鼠(n=3只/组)收集血浆和组织样品(肾脏和/或大腿)。
通过lc/ms/ms测定样品;定量下限为0.05ug/ml。
[0409]
药效学研究
[0410]
在中性粒细胞减少或功能正常的小鼠中使用大腿和/或肾脏感染模型进行pd研究(n=5只/组)。使用对数期的细菌悬液感染小鼠:左大腿肌肉内100μl或两个肾脏内各50μl(共计100ml)。所有分离株的最终接种量为6.0至7.0log
10 cfu/小鼠。使用5个分离株进行剂量-范围研究(见表1)。感染后1h开始,每6小时(q6)以离散剂量1-200mg/kg sc(0.2ml/小鼠)给予gep,持续24小时时间段(共计4剂)。初始治疗后24hr将小鼠安乐死(末次给药后6hr),并对受感染的大腿或肾脏进行处理以确定活菌计数(cfu)。在感染后1hr,从未治疗小鼠获得基线cfu,以及在24hr从生理盐水治疗小鼠获得生长对照cfu。
[0411]
数据分析:
[0412]
非房室分析(nca):使用phoenix winnonlin 6.3(pharsight)和线性想上对数向下方法进行血浆nca。
[0413]
群体药代动力学(poppk):
[0414]
·
根据小鼠中24%的蛋白质结合率,将血浆中的总药物浓度转换为游离药物值。
[0415]
·
使用nonmem(7.3)和软件r(版本3.4.0)建立了一个poppk模型来描述血浆中药物随时间的暴露情况,用于诊断图。
[0416]
·
将最终模型用于模拟在有效性研究中评价的多剂量水平的暴露量。
[0417]
使用模拟数据进行nca分析。接下来,计算24hr内药物暴露的pk/pd参数:获得mic曲线下的游离药物面积(fauc/mic)、药物浓度保持高于mic值(ft》mic)的时间以及高于mic的游离药物cmax值(fcmax/mic)。
[0418]
使用phoenix winnonlin 6.3(pharsight)进行pk-pd分析:
[0419]
·
来自每组的log
10
集落形成单位(cfu)使用来自phoenix库的几种抑制模型与pk-pd参数相关联。
[0420]
·
将针对每个分离株的模型参数值用于计算与同基线1h对照相比的停滞、1-log或2-log降低相关联的pk-pd参数值。
[0421]
结果
[0422]
与血浆或大腿匀浆相比,在肾脏中吉泊达星浓度更高(见图8-血浆、肾脏和大腿浓度对时间曲线)。auc和cmax大致与剂量成正比。中性粒细胞减少与免疫活性动物的pk没有显着差异。最好地描述了吉泊达星在血浆中的分布的poppk模型是使用组合误差模型的具有一级消除的单隔室静脉吸收模型。最终参数估计值为清除率0.104l/h、分布容积0.151l和输注持续时间0.262h(参数值与nca一致)、比例误差41%和累加误差14.6mg/ml。诊断图(图9:因变量与预测、条件加权残差与时间和预测)表明开发模型的适用性。
[0423]
抑制作用sigmoid imax模型在pk-pd分析中呈现最佳结果:
[0424][0425]
其中e是与基线对照(δcfu)相比在研究结束时log 10
cfu的变化;e0是未治疗对照的δcfu;i
max
是在未治疗对照与所检测的最高剂量之间的cfu最大变化;ic
50
是产生50%i
max
所需的pkpd指数值;以及gamma是形状参数。
[0426]
与此前在体外和体内pk/pd研究中获得的结果一致,当所有分离株的数据汇总在一起时,fauc/mic与吉泊达星的有效性相关性良好(图10)。表10和表11显示了在整个研究中与同基线相比的停滞、1-log或2-log降低相关的血浆中的每日fauc/mic:
[0427]
表10:在中性粒细胞减少大腿模型中针对有效性的每日fauc/mic比值
[0428][0429]
表11:使用菌株“all”在整个研究中的每日fauc/mic比值
[0430]
模型mic停滞1-log下降2-log下降中性粒细胞减少大腿43.06.513.8中性粒细胞减少uti44.38.715.6功能正常uti40.73.38.1
[0431]
结论
[0432]
针对停滞、1-log和2-log下降的中位fauc/mic靶点分别为11、16和25。在大腿和肾脏感染之间的fauc/mic靶点非常接近。在非中性粒细胞减少小鼠中fauc/mic靶点降低约一半。与血浆或大腿相比,肾匀浆中更高的药物水平并未转化为肾盂肾炎与大腿感染模型相比的有效性提高。
[0433]
实施例5:针对需氧菌的体外测定
[0434]
方法1
[0435]
以连续两倍稀释的方式,针对101个凝固酶阴性葡萄球菌和105个草绿色链球菌对吉泊达星进行了检测,并将最小抑制浓度(mic)确定为抑制可见生长的化合物的最低浓度。
[0436]
所有临床分离株均于2009-2012年从北美、欧洲、拉丁美洲和亚太医疗中心的患者感染中收集,主要来自有记录的医院和社区获得性呼吸道感染、血流感染以及皮肤和皮肤结构感染的患者。
[0437]
当检测草绿色链球菌分离株时,将头孢曲松、美罗培南、青霉素、左氧氟沙星、莫西沙星和利奈唑胺作为阳性对照。当检测凝固酶阴性葡萄球菌分离株时,将苯唑西林、左氧氟沙星、莫西沙星和利奈唑胺纳入作为阳性对照。根据clsi方法通过肉汤微量稀释测定mic。
[0438]
针对所检测的所有凝固酶阴性葡萄球菌(包括s.capitis、s.caprae、s.cohnii、s.epidermidis、s.haemolyticus、s.hominis、s.intermedius、s.simulans和s.warneri)和草绿色链球菌(包括s.anginosus、s.australis、s.constellatus、s.cristatus、s.gordonii、s.infantarius、s.infantis、s.intermedius、s.massiliensis、s.mitis、s.oralis、s.mutans、s.parasanguinis、s.salivarius、s.sanguinis和s.vestibularis)分离株,吉泊达星的mic90为0.5μg/ml。除了美罗培南和莫西沙星针对草绿色链球菌(两者的mic90均为0.25μg/ml)以外,该mic90至少比所测试的阳性对照低2至64倍。
[0439]
此外,在每种情况下,针对至少一种测试的分离株,吉泊达星mic值针对摩氏摩根菌(morganella morganii)为4mg/l和针对雷氏普罗威登斯菌(providencia rettgeri)为
8mg/l。
[0440]
第二项研究通过clsi肉汤微量稀释测试了吉泊达星针对从2013年至2014年间急性细菌性皮肤和软组织感染患者收集的细菌分离物。
[0441]
纳入阿莫西林/克拉维酸、利奈唑胺、夫西地酸、头孢曲松、头孢洛林、万古霉素、青霉素、奎奴普汀/达福普汀、红霉素、克林霉素、美罗培南、四环素、氯霉素、氟氯西林、特拉万星、达托霉素、甲氧苄啶/磺胺甲恶唑、庆大霉素、左氧氟沙星、替加环素和头孢呋辛作为对照。根据clsi方法通过肉汤微量稀释测定mic。
[0442]
此外,mic是根据clsi方法通过肉汤微量稀释确定的,并且针对选自以下的革兰氏阳性需氧菌评估了上述列表中的所有阳性对照:s.lugdenensis、s.agalactiae、g组链球菌和f组链球菌。
[0443]
针对上文列出的每种菌的至少一个菌株吉泊达星的mic≤2μg/ml。
[0444]
方法2
[0445]
化合物在连续两倍稀释中进行测试,将最小抑制浓度(mic)确定为抑制可见生长的化合物的最低浓度。
[0446]
具体而言,针对来自俄亥俄州西湖的laboratory specialists,inc.的分离株集合中的4株表皮葡萄球菌(staphylococcus epidermidis),对吉泊达星进行了测试。
[0447]
研究中将左氧氟沙星作为对照,以确定尿液对吉泊达星对表皮葡萄球菌(staphylococcus epidermidis)的体外活性的影响。根据clsi方法通过肉汤微量稀释测定mic。
[0448]
吉泊达星的最小抑制浓度(mic)针对2个对甲氧西林易感的s.epidermidis分离株为0.5μg/ml,以及针对2个对甲氧西林耐药的s.epidermidis分离株的mic范围为0.25-0.5μg/ml。对于甲氧西林易感的s.epidermidis,吉泊达星的mic值比左氧氟沙星的mic大2倍,并且对每个对甲氧西林耐药的s.epidermidis,比左氧氟沙星的mic大4倍。
[0449]
检测了至少一种示例性的吉泊达星的盐(即,如甲磺酸盐)。
[0450]
针对对甲氧西林易感的和对甲氧西林耐药的s.epidermidis,吉泊达星的mic≤0.5μg/ml。
[0451]
下表中显示的数据是用上述相同s.epidermidis分离株进行的体外研究的结果,目的是确定尿液对吉泊达星和左氧氟沙星对s.epidermidis的体外活性的影响。根据参考clsi肉汤微量稀释方法,使用阳离子调整的mueller hinton肉汤(camhb)并添加25%、50%和100%尿液(未调整ph值,ph 6.42)和100%尿液(ph值调整为7.31和8.07),对研究菌株的mic进行测试。加入尿液对吉泊达星的mic结果(平均稀释度差异)没有显着影响(平均稀释度差异为0到-1.01)。左氧氟沙星的mic结果更受ph 8.07的100%混合尿液影响,平均稀释度差异约为1.8。
[0452]
表12:clsi mic肉汤微量稀释参考方法(camhb)对尿液条件的比较
[0453][0454][0455][0456]
总之,这些研究证明了使用mic≤0.5μg/ml检测的吉泊达星针对甲氧西林敏感和甲氧西林耐药s.epidermidis分离株的体外活性,并且在100%尿液中,mic没有显著变化(平均稀释度差异为0至-0.26)。吉泊达星活性不受尿液显着影响的事实使其成为uti的合适治疗选择。
[0457]
实施例6:针对厌氧菌的体外测定
[0458]
如在以下方法中所鉴定的,进行研究以评估吉泊达星和特定比较化合物的体外活性。
[0459]
方法1
[0460]
抗菌活性是使用临床和实验室标准协会(clsi)推荐的程序通过琼脂稀释来确定的。
[0461]
化合物在连续两倍稀释中进行测试,将最小抑制浓度(mic)确定为抑制可见生长的化合物的最低浓度。吉泊达星对2000年至2017年从北美和欧洲的临床样本中收集的333株革兰氏阴性厌氧菌和203株革兰氏阳性厌氧菌进行了检测;其大多数是从2013年到2016年收集的。
[0462]
纳入头孢曲松、克林霉素、亚胺培南、甲硝唑、莫西沙星和哌拉西林/他唑巴坦作为对照。
[0463]
吉泊达星对革兰氏阴性和革兰氏阳性厌氧菌的mic90(抑制90%测试分离株的mic)≤4μg/ml,如下表所示。
[0464]
表13:吉泊达星对革兰氏阴性厌氧病原体的评价
[0465][0466]
关键:
[0467]
a=bacteroides spp.(n):b.caccae(2),b.fragilis(114),b.ovatus(11),b.stercons(3),b.thetaiotaomicron(48),b.uniformis(4),b.vulgatus(9).
[0468]
b=fusobacterium spp.(n):f.necrophorum(3),f.nucleatum(17),fusobacterium,non-speciated(5).
[0469]
c=porphyromonasspp.(n):p.asaccharolytica(9),p.endodontaliis(2),p.gingivalis(2),p.levii(1),p.somerae(5),porphyromonas,non-speciated(7).
[0470]
d=prevotellaspp.(n):p.bivia(11),p.buccae(10),p.denticola(5),p.disiens(1),p.melaninogenica(3).
[0471]
e=veillonella spp.(n):v.alcalescens dispar(1),v.parvula(9),veillonella,non-speciated(15).
[0472]
表14:吉泊达星对革兰氏阳性厌氧病原体的评价
[0473][0474]
a=bifidobacterium spp.(n):b.adolescentis(5),b.breve(3),b.dentium(4),b.longum(7),b.pseudocatenulatum(3),bifidobacterium,non-speciated(4).
[0475]
b=eubacterium spp.(n):collinsella(eubacterium)aerofaciens(5),e.limosum(2),e.nodatum(1),eubacterium,non-speciated(23).
[0476]
c=lactobacillusspp.(n):l.acidophilus(1),l.crispatus(3),l.fermentum(5),l.gasseri(21),l.iners(2),l.jensenii(6),l.plantarum(1),l.rhamnosus(19),lactobacillus,non-speciated(33).
[0477]
对于所有组合的革兰氏阴性厌氧生物,吉泊达星mic90为4μg/ml。该mic90值低于头孢曲松、克林霉素、莫西沙星和哌拉西林/他唑巴坦(总体mic90值分别为512、>8、8、16μg/ml),高于亚胺培南和甲硝唑(总体mic90值分别为0.5和2μg/ml)。
[0478]
对于组合的革兰氏阳性厌氧菌,吉泊达星mic90为2μg/ml。基于mic90,与头孢曲松(256μg/ml)、克林霉素(>8μg/ml)、亚胺培南(8μg/ml)、莫西沙星(>8μg/ml)和哌拉西林-他唑巴坦相比,吉泊达星对革兰氏阳性厌氧菌的活性增加(16μg/ml),与甲硝唑(0.5μg/ml)相比活性降低。
[0479]
第二项研究通过clsi琼脂稀释测试了吉泊达星针对来自glaxosmithkline upper providence培养物保藏中心的革兰氏阳性和革兰氏阴性厌氧细菌分离株。
[0480]
针对10个bacteroides spp.、3个fusobacterium spp.、1个prevotella spp.、1个双发酵梭菌(clostridium bifermentans)和4个peptostreptococcus spp.检测的吉泊达星的mic分别为0.0.12-16、0.12-1、4、0.06和0.12-2μg/ml。
[0481]
将阿莫西林、阿奇霉素、左氧氟沙星和头孢呋辛纳入作为对照。
[0482]
方法1的结论
[0483]
这些研究显示了吉泊达星针对革兰氏阴性厌氧菌(mic90=4μg/ml)和革兰氏阳性厌氧菌(mic90=2μg/ml)的体外活性(针对列出的每种菌的至少一个菌株mic≤2μg/ml)。
[0484]
来自方法1的附加数据
[0485]
对上述方法1中描述的研究结果进行了其他分析,以确定吉泊达星对革兰氏阴性和革兰氏阳性厌氧生物的体外活性,这些菌对头孢曲松、克林霉素、亚胺培南、甲硝唑、莫西沙星和哌拉西林/他唑巴坦具有抗性。
[0486]
表15显示了当通过琼脂稀释检测时针对耐药拟杆菌属(bacteroides spp.)的mic范围。针对大多数耐药子集,由于分离株数量较少(n《10)无法计算mic
50
/mic
90
。
[0487]
表15:通过琼脂稀释检测的针对耐药拟杆菌属(bacteroides spp.)的吉泊达星mic(μg/ml)
[0488]
[0489][0490]
表16显示了当通过肉汤微量稀释检测时针对耐药bacteroides spp.的mic范围。针对大多数耐药子集,由于分离株数量较少(n《10)无法计算mic
50
/mic
90
。
[0491]
表16:通过肉汤微量稀释检测的针对耐药bacteroides spp.的吉泊达星mic(μg/ml)
[0492][0493][0494]
表17显示了当通过琼脂稀释检测时针对革兰氏阴性厌氧菌(bacteroides spp.除外)的mic范围。针对大多数耐药子集,由于分离株数量较少(n《10)无法计算mic
50
/mic
90
。
[0495]
表17:通过琼脂稀释检测的针对革兰氏阴性厌氧菌(bacteroides spp.除外)的吉泊达星mic(μg/ml)
[0496][0497]
表18显示了当通过琼脂稀释检测时针对耐药革兰氏阳性厌氧菌的mic范围。针对大多数耐药子集,由于分离株数量较少(n《10)无法计算mic
50
/mic
90
。
[0498]
表18:通过琼脂稀释检测的针对革兰氏阳性厌氧菌的吉泊达星mic(μg/ml)
[0499][0500]
来自方法1的附加数据的结论
[0501]
本研究证明了当通过琼脂稀释测试时,吉泊达星对上表中列出的每种耐药表型中的至少一种菌株对耐药革兰氏阴性和革兰氏阳性厌氧菌的体外活性mic≤4μg/ml,但是1个粪便拟杆菌(bacteroides caccae)分离株除外,其mic=8mg/l。
[0502]
实施例7:针对革兰氏阴性需氧菌的体外测定
[0503]
针对从uti患者中获得的以下微生物对吉泊达星进行了检测,连续两倍稀释。根据clsi方法,通过肉汤微量稀释确定最低抑制浓度(mic)。
[0504]
对于温和食酸菌(acidovorax temperans)(n=1),吉泊达星mic为1mg/ml。
[0505]
对于无丙二酸柠檬酸杆菌(citrobacter amalonaticus)(n=1),吉泊达星mic为2mg/ml。
[0506]
对于斯氏普罗威登斯菌(providencia stuartii)(n=1),吉泊达星mic为32mg/ml。
[0507]
对于恶臭假单胞菌(pseudomonas putida)(n=4),吉泊达星mic为8或16mg/ml。
[0508]
应当理解,本发明不限于上文所示的方面或实施方式,并且保留对所示方面或实施方式以及落入以下权利要求范围内的所有修改的权利。
[0509]
在此引用的对期刊、专利和其他出版物的各种参考包括现有技术并且通过引用将其并入本文,就好像完全阐述一样。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1