新方法与流程
新方法
1.相关申请的交叉引用
2.本技术要求于2019年7月7日提交的美国临时申请第62/871,170号的优先权和权益,该申请的内容通过引用整体并入本文。
技术领域
3.本公开内容涉及任选为氘化形式的游离或可药用盐形式的卢美哌隆(lumateperone)用于治疗ii型双相性精神障碍的用途。
4.背景
5.被取代的杂环稠合的γ-咔啉如卢美哌隆已知是5-ht
2a
或5-ht
2a
/d2受体配体,它们可用于治疗中枢神经系统疾病。这些化合物拮抗血清素-2a(5-ht
2a
)受体和/或在关键细胞内磷蛋白水平上调控多巴胺受体信号传导。已知这类化合物主要可用于治疗精神分裂症的阳性和阴性症状。在多巴胺d2受体处,这些化合物具有双重特性,可作为突触后拮抗剂和突触前部分激动剂发挥作用。它们还以中脑边缘特异性方式刺激谷氨酸能nmda nr2b或glun2b受体的磷酸化。据信,在被认为介导抗精神病药物功效的脑区域中的这种区域选择性,连同血清素能、谷氨酸能和多巴胺能相互作用,可导致对与精神分裂症相关的阳性、阴性、情感和认知症状的抗精神病功效。所述化合物还表现出血清素再摄取抑制作用,提供了抗抑郁活性用于治疗分裂情感性障碍、共病抑郁(comorbid depression)和/或作为重症抑郁的独立治疗。所述的5-ht
2a
或5-ht
2a
/d2受体配体还可用于治疗双相性精神障碍和其它精神性疾病和神经变性疾病,特别是与痴呆、孤独症和其它cns疾病相关的行为障碍。这些特征可能能够提高精神分裂症患者的生活质量,增强社交功能以允许他们更充分地融入他们的家庭和他们的工作场所。这些化合物显示出不同的剂量依赖性作用,在低剂量下选择性地靶向5-ht
2a
受体,而在较高剂量下逐渐与d2受体相互作用。因此,在较低剂量下,它们可用于治疗睡眠、攻击性和躁动。在高剂量时,它们可治疗急性加重的和残留的精神分裂症、双相性精神障碍和心境障碍。
6.卢美哌隆,其为4-((6br,10as)-3-甲基-2,3,6b,9,10,10a-六氢-1h-吡啶并[3',4':4,5]吡咯并[1,2,3-de]喹喔啉-8(7h)-基)-1-(4-氟苯基)-1-丁酮,具有下式:
[0007][0008]
它是一种目前正在进行临床试验的治疗剂。卢美哌隆提供了血清素、多巴胺和谷氨酸神经传递的选择性和同步调节。它表现出强效(ki=0.5nm)的5-ht
2a
受体拮抗作用、作为符合体内突触前d2受体部分激动和突触后d2受体拮抗的中脑边缘/中脑皮质选择性多巴胺受体蛋白磷酸化调节剂的活性(ki=32nm)、高d1受体亲和力(ki=52nm)和血清素转运蛋白(sert)抑制作用(ki=26-62nm,使用不同的sert活性测定)。卢美哌隆在2019年被美国食
品药品监督管理局批准用于治疗精神分裂症,目前处于或已经处于iii期临床开发阶段用于治疗痴呆、包括阿尔茨海默病中的双相抑郁和躁动。
[0009]
卢美哌隆和相关化合物已经在美国专利6,548,493、7,238,690、6,552,017、6,713,471、u.s.re39,680和u.s.re39,679中作为可用于治疗与5-ht
2a
受体调节相关的疾病的新化合物公开,所述疾病例如有焦虑、抑郁、精神病、精神分裂症、睡眠障碍、性功能障碍、偏头痛、伴有头痛的病症和社交恐惧症。pct/us08/03340和美国专利7,081,455还公开了制备被取代的杂环稠合的γ-咔啉的方法以及这些γ-咔啉作为血清素激动剂和拮抗剂可用于控制和预防中枢神经系统疾病如成瘾行为和睡眠障碍的用途。wo2009/145900和us8,598,119以及wo2013/155506和us2015/0080404(各自以引用方式并入本文)公开了特定取代的杂环稠合的γ-咔啉用于治疗精神病和抑郁症的组合以及用于精神病或帕金森病患者的睡眠、抑郁和/或心境障碍的用途,以及用于治疗或预防与痴呆相关的障碍、特别是行为或心境障碍、例如激动、刺激、攻击性/好动武行为、愤怒、身体或情绪爆发和与痴呆相关的精神病和睡眠障碍的用途。wo2009/114181和us8,648,077和us2020/0157100(各自通过引用并入本文)公开了制备特定取代杂环稠合的γ-咔啉的甲苯磺酸加成盐晶体的方法,例如卢美哌隆的甲苯磺酸加成盐(单甲苯磺酸盐和双甲苯磺酸盐)。
[0010]
wo2011/133224和us8,993,572(各自以引用方式并入本文)公开了取代的杂环稠合的γ-咔啉的前药/代谢物用于改进的制剂如延长/控制释放制剂。该申请公开,被4-氟苯基(4-羟基)丁基部分n-取代的杂环稠合的γ-咔啉相对于含有4-氟苯基丁酮的杂环稠合的γ-咔啉显示出对血清素转运蛋白(sert)的高选择性。
[0011]
wo2009/145900(和us8,598,119)教导了所选择的取代的杂环稠合的γ-咔啉化合物对血清素再摄取转运蛋白(sert)具有纳摩尔亲和力,因此是选择性血清素再摄取抑制剂。
[0012]
如wo2015/154025、us2017/0183350、wo2017/165843和us2019/231780(各自通过引用并入本文)中公开的那样,卢美哌隆和相关化合物的氘化形式已经被证明具有改善的代谢稳定性。
[0013]
根据美国国家精神卫生研究所(national institute of mental health),双相性精神障碍,也称为躁狂抑郁症,是一种导致心境、精力、活动水平和执行日常任务的能力发生异常变化的脑疾病。双相性精神障碍有四种基本类型;所有这些都涉及心境、精力和活动水平的明显变化。这些心境的范围从极度“高亢”、振奋和精力充沛的行为的时期(称为躁狂发作)到非常悲伤、“沮丧”或绝望的时期(称为抑郁发作)。不太严重的躁狂期被称为轻躁狂发作。
[0014]
a.i型双相性精神障碍——定义为持续至少7天的躁狂发作,或严重到患者需要立即住院护理的躁狂症状。经常也会发生抑郁发作,通常持续至少2周。具有混合特征(同时具有抑郁和躁狂症状)的抑郁发作也是可能的。
[0015]
b.ii型双相性精神障碍——定义为抑郁发作和轻躁狂发作的模式,而不是上述的全面躁狂发作。
[0016]
c.循环性情感障碍(也称为循环性气质)——定义为持续至少2年(儿童和青少年为1年)的多个轻躁狂症状期和多个抑郁症状期。但是,这些症状不符合轻躁狂发作和抑郁发作的诊断要求。
[0017]
d.其它说明和未说明的双相性精神障碍和相关障碍——定义为与上文列出的三个类别不匹配的双相性精神障碍症状。
[0018]
双相性精神障碍的病因学尚不清楚,该疾病对治疗有抗性。药物治疗包括情绪稳定药物、例如锂或抗惊厥药(如卡马西平、拉莫三嗪和丙戊酸盐)。传统的抗抑郁药如选择性血清素再摄取抑制剂(ssris)不仅对治疗双相抑郁的效果不如重症抑郁,而且它们可通过引发躁狂发作和快速循环而造成伤害。
[0019]
抗精神病药物通常对i型双相性精神障碍中的双相躁狂发作的短期治疗有效,但是它们通常对治疗ii型双相性精神障碍和在抑郁发作期间维持治疗无效。而且,很多抗精神病药物呈现出显著的副作用,例如锥体外系症状,包括急性运动障碍和张力障碍反应、迟发性运动障碍、帕金森综合征、运动不能、静坐不能和精神抑制药恶性综合征。
[0020]
例如,广泛评估了非典型抗精神病药阿立哌唑用于治疗双相性精神障碍,但临床数据的回顾得出如下结论:“虽然阿立哌唑已经证明了对急性躁狂症和预防躁狂症有效,但迄今可获得的证据并不支持阿立哌唑用于治疗急性双相抑郁和预防抑郁复发的功效。”yatham ln,“a clinical review of aripiprazole in bipolar depression and maintenance therapy of bipolar disorder”j.affect.disord.2011年1月;128增刊1:s21-8。阿立哌唑目前在美国被批准用于“与i型双相相关的躁狂和混合发作的急性治疗”。目前尚未批准用于治疗ii型双相性精神障碍。
[0021]
虽然有很多抗精神病药被批准用于治疗与i型双相性精神障碍相关的躁狂症,但是目前在美国只有四种抗精神病药被批准用于治疗与i型双相性精神障碍相关的抑郁症,并且目前在美国只有一种抗精神病药被批准用于治疗ii型双相性精神障碍,喹硫平然而,已经报道了喹硫平具有高度镇静作用,引起多种代谢副作用,例如高血糖、血脂异常和体重增加。它还与一些患者出现自杀念头有关。
[0022]
估计数有不同,但据信约30-60%的双相性精神障碍患者患有ii型双相性精神障碍。尽管很普遍,但是ii型双相性精神障碍经常被误诊为重症抑郁性障碍或i型双相性精神障碍,并因此被不正确地治疗。需要更安全和更有效的ii型双相性精神障碍治疗以及有效治疗i型双相性精神障碍和ii型双相性精神障碍的疗法。
[0023]
简述
[0024]
我们出人意料地发现,卢美哌隆可用于治疗ii型双相性精神障碍。临床结果表明,卢美哌隆在这种适应症中至少与治疗双相性精神障碍的现有抗精神病药一样有效,在ii型双相性精神障碍中具有特别出人意料的功效,而ii型双相性精神障碍通常对抗精神病药治疗具有抗性。而且,卢美哌隆呈现出良好的安全性。临床试验证明,与很多其它抗精神病药不同,卢美哌隆不会增加静坐不能、多动或其它运动障碍,不会增加自杀意念,并且没有明显的代谢副作用。
[0025]
因此,在第一方面,本公开提供了在需要其的患者中治疗ii型双相性精神障碍的方法,该方法包括给需要其的患者施用治疗有效量的任选为氘化形式的游离碱或可药用盐形式的卢美哌隆。
[0026]
其它实施方案将从以下详述和实施例中显而易见。
[0027]
详述
[0028]
在评价卢美哌隆作为单药疗法治疗与i型或ii型双相性精神障碍相关的重症抑郁
发作的3期临床试验中,每天42mg卢美哌隆(作为60mg甲苯磺酸盐口服施用)达到了改善抑郁的主要终点(如抑郁评定量表(madrs)总评分上由基线变化相对于安慰剂所测量的(p《0.001;效应量=0.56))以及其关键次要终点,双相性精神障碍严重程度临床总体印象量表(clinical global impression scale for bipolar for severity of illness,cgi-bp-s)总评分(p《0.001;效应量=0.46)。
[0029]
而且,患者没有出现如通过杨氏躁狂量表(young mania rating scale,ymrs)所测定的躁狂出现和躁狂严重度具体临床总体印象,这意味着该药物有效预防了躁狂或轻躁狂的出现,并且没有触发躁狂发作或引起快速循环,而快速循环经常与治疗双相性精神障碍的ssris相关。
[0030]
预料不到的是,鉴于抗精神病药在ii型双相性精神障碍中普遍有限的功效,对ii型双相性精神障碍患者的亚组分析显示,每天42mg卢美哌隆的madrs总评分在统计学上显著优于安慰剂。
[0031]
卢美哌隆在该试验中表现出良好的安全性,与安慰剂相当。与喹硫平不同,卢美哌隆没有显示出具有任何明显的代谢作用,例如高血糖、血脂异常或体重增加。没有关于自杀意念的不良事件报告,没有自杀,并且没有因自杀念头而停药。同样重要的是,也没有锥体外系症状如静坐不能、多动或其它运动副作用的不良事件报告。
[0032]
静坐不能已经与大多数抗精神病药和抗抑郁药的使用相关联,特别是在双相性精神障碍中。静坐不能已经与自杀相关。这突显了卢美哌隆的临床重要性,因为它可以治疗ii型双相性精神障碍而不引起静坐不能,因此不太可能引起自杀行为。
[0033]
在第一方面,本公开提供了治疗ii型双相性精神障碍的方法(方法1),该方法包括向需要其的患者施用治疗有效量的任选为氘化形式的游离碱或可药用盐形式的卢美哌隆。在第一方面的进一步的实施方案中,本公开提供了:
[0034]
1.1.方法1,其中卢美哌隆是甲苯磺酸盐的形式(例如,甲苯磺酸的酸加成盐,例如单甲苯磺酸盐或双甲苯磺酸盐),任选地其中所述盐是固体结晶盐,例如us2011/112105和/或us2020/0157100中公开的那些,所述文献各自的内容通过引用整体并入本文。
[0035]
1.2.方法1,其中卢美哌隆为游离碱形式。
[0036]
1.3.任意前述方法,其中卢美哌隆为氘化形式,例如,其中指定的键合碳的氢原子的氘:氕比例显著高于天然同位素比,例如至少2倍,例如至少10倍。
[0037]
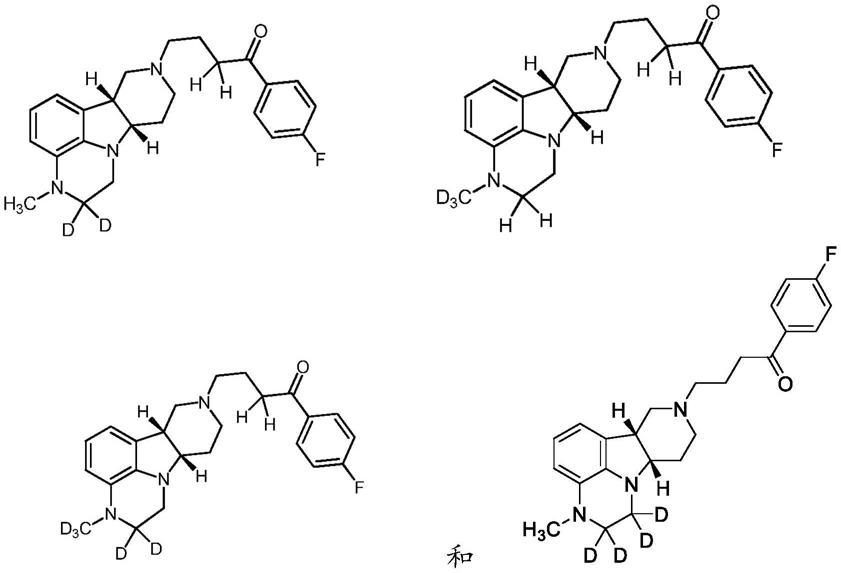
1.4.方法1.3,其中卢美哌隆是选自以下的氘代形式:
[0038][0039]
其中d代表具有显著高于天然氘掺入量的氢位置(即显著高于0.0156%),例如,高于60%、或高于70%、或高于80%、或高于90%或高于95%、或高于96%、或高于97%、或高于98%、或高于99%,
[0040]
为游离或可药用盐形式,例如甲苯磺酸盐形式。
[0041]
1.5.任意前述方法,其中任选为氘化形式的游离或可药用盐形式的卢美哌隆以相当于6-60mg游离碱、例如相当于20-50mg游离碱的总日剂量施用。
[0042]
1.6.任意前述方法,其中任选为氘化形式的游离或可药用盐形式的卢美哌隆以相当于25-30mg游离碱的总日剂量施用。
[0043]
1.7.任意前述方法,其中任选为氘化形式的游离或可药用盐形式的卢美哌隆以相当于40-45mg游离碱的总日剂量施用。
[0044]
1.8.任意前述方法,其中所述方法包括每日一次施用用于口服施用的单位剂量,例如片剂或胶囊剂,其包含与可药用稀释剂或载体组合或联合的、任选为氘化形式的游离或可药用盐形式的约42mg卢美哌隆游离碱等同物。
[0045]
1.9.任意前述方法,其中所述方法包括每日一次施用片剂或胶囊剂,所述片剂或胶囊剂包含与可药用稀释剂或载体组合或联合的、任选氘化形式的约60mg卢美哌隆甲苯磺酸盐。
[0046]
1.10.任意前述方法,其中所述方法包括每日一次施用用于口服施用的单位剂量,例如片剂或胶囊剂,其包含与可药用稀释剂或载体组合或联合的、任选为氘化形式的游离或可药用盐形式的约28mg卢美哌隆游离碱等同物。
[0047]
1.11.任意前述方法,其中所述方法包括每日一次施用片剂或胶囊剂,所述片剂或胶囊剂包含与可药用稀释剂或载体组合或联合的、任选氘化形式的约40mg卢美哌隆甲苯磺酸盐。
[0048]
1.12.任意前述方法,其中所述方法包括每日一次施用用于皮下或经粘膜施用的
单位剂量,例如舌下或颊口腔崩解片剂或膜剂,其包含相当于10-60mg游离碱的量的任选为氘化形式的游离或可药用盐形式的卢美哌隆和可药用稀释剂或载体。
[0049]
1.13.任意前述方法,其中所述方法包括以长效可注射形式施用任选为氘化形式的游离或可药用盐形式的卢美哌隆。
[0050]
1.14.任意前述方法,其中患者已经被诊断患有ii型双相性精神障碍。
[0051]
1.15.任意前述方法,其中待治疗的病症是ii型双相性精神障碍中的抑郁,或与ii型双相性精神障碍相关的抑郁发作(例如重症抑郁发作)。
[0052]
1.16.任意前述方法,其中待治疗的病症包括ii型双相性精神障碍中的混合情感发作。
[0053]
1.17.任意前述方法,其中待治疗的病症包括轻躁狂发作。
[0054]
1.18.任意前述方法,其中所述治疗抑制躁狂或轻躁狂。
[0055]
1.19.任意前述方法,其中所述治疗不引发躁狂或轻躁狂发作或快速循环。
[0056]
1.20.任意前述方法,其中在治疗过程中,患者没有出现如通过杨氏躁狂量表(ymrs)所测定的躁狂或轻躁狂。
[0057]
1.21.任意前述方法,其中在治疗过程中,患者显示出抑郁症状的改善,例如采用抑郁评定量表(madrs)、汉密尔顿抑郁评定量表(ham-d)、贝克抑郁量表(bdi)、zung抑郁自评量表、wechsler抑郁评定量表、raskin抑郁评定量表、抑郁症状量表(inventory of depressive symptomatology,ids)或抑郁症状快速量表(quick inventory of depressive symptomatology,qids)中的一种或多种所测定的。
[0058]
1.22.任意前述方法,其中在治疗过程中,患者显示出抑郁评定量表(madrs)总评分的改善(例如,在开始治疗后8天或更短时间内的改善)。
[0059]
1.23.任意前述方法,其中在治疗后,患者显示出双相性精神障碍严重程度临床总体印象量表(cgi-bp-s)中的改善(例如,在治疗开始后8天或更短时间内的改善)。
[0060]
1.24.任意前述方法,其中在治疗过程中,患者显示出双相性抑郁严重程度临床总体印象量表(clinical global impression scale for bipolar depression for severity of illness,cgi-bp-抑郁-s)中的改善(例如,在开始治疗后8天或更短时间内的改善)。
[0061]
1.25.任意前述方法,其中在治疗过程中,患者没有显示出双相性躁狂严重程度临床总体印象量表(clinical global impression scale for bipolar mania for severity of illness,cgi-bp-躁狂-s)中的增加。
[0062]
1.26.任意前述方法,其中在治疗过程中,患者显示出整体精神健康的改善,例如采用临床总体印象-严重度(cgi-s)或临床总体印象-改善(cgi-i)所测定的(例如,在开始治疗后8天或更短时间内的改善)。
[0063]
1.27.任意前述方法,其中所述治疗不导致代谢副作用,例如不导致高血糖、血脂异常或体重增加中的一种或多种。
[0064]
1.28.任意前述方法,其中所述治疗不诱发自杀意念或自杀想法。
[0065]
1.29.任意前述方法,其中所述治疗不诱发锥体外系症状,例如静坐不能、运动不能、多动、急性运动障碍、张力障碍反应、迟发性运动障碍、帕金森样症状或精神抑制药恶性
综合征中的一种或多种。
[0066]
1.30.任意前述方法,其中所述治疗不诱发静坐不能。
[0067]
1.31.任意前述方法,其中任选氘化形式的游离碱或可药用盐形式的卢美哌隆作为单一疗法施用以治疗ii型双相性精神障碍。
[0068]
1.32.任意前述方法,其中患者并行地接受情绪稳定剂,例如选自锂、卡马西平、奥卡西平、拉莫三嗪和丙戊酸盐(包括双丙戊酸钠(又名丙戊酸半钠)、丙戊酸钠和丙戊酸的其它游离形式、盐形式或复合形式)。
[0069]
1.33.任意前述方法,其中患者并行地接受锂或丙戊酸盐。
[0070]
1.34.任意前述方法,其中患者是18岁以下。
[0071]
1.35.任意前述方法,其中患者是成人,例如18岁以上,例如18至75岁之间,包括端点。
[0072]
1.36.任意前述方法,其中患者是老年人,例如65岁或以上,例如75岁或以上。
[0073]
1.37.任意前述方法,其中游离或盐形式的卢美哌隆被指示用于治疗i型双相性精神障碍和ii型双相性精神障碍中的抑郁。
[0074]
1.38.任意前述方法,其中治疗持续时间为六周或更短时间。
[0075]
1.39.任意前述方法,其中所述治疗是维持治疗。
[0076]
1.40.任意前述方法,其中治疗持续时间为六周或更长时间。
[0077]
1.41.任意前述方法,其中患者先前用ssri进行了治疗(例如,这种治疗无效和/或中断,例如由于副作用中断)。
[0078]
1.42.方法1.41,其中所述ssri选自西酞普兰、依他普仑、氟西汀、氟伏沙明、帕罗西汀和舍曲林。
[0079]
1.43.任意前述方法,其中患者先前用抗精神病药、例如非典型抗精神病药进行了治疗(例如,这种治疗无效和/或中断,例如由于副作用中断)。
[0080]
1.44.方法1.43,其中所述抗精神病药选自氟哌啶醇、阿立哌唑、喹硫平、奥氮平、利培酮、鲁拉西酮(lurasidone)、帕潘立酮、伊潘立酮、齐拉西酮、依匹哌唑(brexipiprazole)、阿塞那平(asenapine)、氯氮平和佐替平。
[0081]
在另一方面,本公开提供了任选为氘化形式的游离或可药用盐形式的卢美哌隆,用于治疗ii型双相性精神障碍,例如用于方法1及以下等等中的任一种。
[0082]
在另一方面,本公开提供了任选为氘化形式的游离或可药用盐形式的卢美哌隆在制备药剂中的用途,所述药剂用于治疗ii型双相性精神障碍,例如用于方法1及以下等等中的任一种。
[0083]
用词“治疗”应相应地理解为包括疾病症状的预防和治疗或改善和/或疾病病因的治疗。在特定的实施方案中,用词“治疗”指疾病症状的预防或改善。
[0084]
本文所用的“患者”指人类患者,另有说明除外。
[0085]
卢美哌隆的可药用盐包括可药用的酸加成盐,例如甲苯磺酸加成盐(甲苯磺酸盐)。卢美哌隆的甲苯磺酸盐包括单甲苯磺酸盐和双甲苯磺酸盐。除非另有说明,否则术语“卢美哌隆甲苯磺酸盐”指单甲苯磺酸盐。卢美哌隆甲苯磺酸盐作为caplyta
tm
出售。当以重量给出盐的剂量或量时,例如毫克/天或毫克/单位剂量,盐的剂量以相应游离碱的重量给出,另有说明除外。
[0086]
术语“并行”当涉及治疗使用时指两种或更多种活性成分作为用于治疗疾病或病症的方案的一部分施用给患者,无论所述两种或更多种活性剂同时或不同时间给予或者通过相同或不同的施用途径给予。两种或更多种活性成分的并行施用可以在同一天的不同时间、或不同日期或以不同频率进行。
[0087]
用于实施本公开的剂量当然将根据例如待治疗的特定疾病或病症、所用的具体活性化合物、施用方式和预期疗法而变化。游离形式或可药用盐形式的、任选氘化形式的卢美哌隆可以通过任意适宜的途径施用,包括口服、胃肠外、经皮或经粘膜,例如以片剂、胶囊剂、皮下注射、长效可注射(贮库)或用于舌下或颊施用的口服快速崩解片或膜的形式。
[0088]
在一些实施方案中,卢美哌隆作为用于口服施用的片剂或胶囊提供,其包含与可药用稀释剂或载体组合的卢美哌隆甲苯磺酸盐。
[0089]
在一些实施方案中,卢美哌隆作为用于舌下或颊施用的快速崩解片剂或膜提供,其包含与可药用稀释剂或载体组合的卢美哌隆甲苯磺酸盐。
[0090]
在一些实施方案中,任选为氘化形式的游离或可药用盐形式的卢美哌隆作为贮库制剂进行施用,例如通过将化合物分散、溶解、混悬或包封在聚合物基质(如本文所述)中,以便化合物因为聚合物随时间降解而不断地释放。卢美哌隆从聚合物基质中的释放提供了受控和/或延迟和/或持续释放,例如从药物贮库组合物释放到施用了药物贮库的个体、例如温血动物、例如人。因此,药物贮库历经持续的时间段、例如1周至3个月以有效治疗特定疾病或医学病症的浓度向个体递送卢美哌隆。
[0091]
可用于本发明的组合物(例如,本发明的贮库组合物)中的聚合物基质的聚合物可以包括羟基脂肪酸的聚酯及其衍生物或其它物质,例如聚乳酸、聚乙醇酸、聚柠檬酸、聚苹果酸、聚-β-羟基丁酸、ε-己内酯开环聚合物、乳酸-乙醇酸共聚物、2-羟基丁酸-乙醇酸共聚物、聚乳酸-聚乙二醇共聚物或聚乙醇酸-聚乙二醇共聚物),α-氰基丙烯酸烷基酯(例如聚(2-氰基丙烯酸丁酯))、聚草酸亚烷基酯(例如聚草酸三亚甲基酯或聚草酸四亚甲基酯)、聚原酸酯、聚碳酸酯(例如聚乙烯碳酸酯或聚乙烯丙烯碳酸酯)、聚原碳酸酯(polyortho-carbonate)、聚氨基酸(例如聚-γ-l-丙氨酸、聚-γ-苄基-l-谷氨酸或聚-γ-甲基-l-谷氨酸)、透明质酸酯等,可以使用这些聚合物中的一种或多种。
[0092]
如果聚合物是共聚物,它们可以是无规、嵌段和/或接枝共聚物中的任一种。当上述α-羟基羧酸、羟基二羧酸和羟基三羧酸在其分子中具有旋光活性时,可以使用d-异构体、l-异构体和/或dl-异构体中的任一种。其中,可以使用α-羟基羧酸聚合物(优选乳酸-乙醇酸聚合物)、其酯、聚-α-氰基丙烯酸酯等,乳酸-乙醇酸共聚物(也称为聚(丙交酯-α-乙交酯)或聚(乳酸-共-乙醇酸),下文称为plga)是优选的。因此,在一方面,可用于聚合物基质的聚合物是plga。如本文所用的术语plga包括乳酸聚合物(也称为聚丙交酯、聚(乳酸)或pla)。最优选地,聚合物是可生物降解的聚(d,l-丙交酯-共-乙交酯)聚合物,例如plga 50:50、plga 85:15和plga 90:10。
[0093]
在一个这类实施方案中,本发明的聚合物基质是生物相容的和生物可降解的聚合物材料。术语“生物相容”定义为聚合物材料是无毒的、非致癌的,并且不显著引起身体组织的炎症。基质材料应当是生物可降解的,其中聚合物材料应当通过身体过程降解成容易被身体丢弃的产物并且不应当在体内聚集。生物降解的产物还应当与身体是生物相容的,因为聚合物基质与身体是生物相容的。聚合物基质材料的特别有用的实例包括聚(乙醇酸)、
聚-d,l-乳酸、聚-l-乳酸、前述物质的共聚物、聚(脂肪族羧酸)、共聚草酸酯、聚己内酯、聚二噁烷酮、聚(原碳酸酯)、聚(缩醛)、聚(乳酸-己内酯)、聚原酸酯、聚(乙醇酸-己内酯)、聚酐和天然聚合物,包括白蛋白、酪蛋白和蜡,例如单和二硬脂酸甘油酯,等等。一种适用于实施本发明的聚合物是dl(聚丙交酯-共-乙交酯)。在一个实施方案中,该共聚物中丙交酯与乙交酯的摩尔比在约75:25至50:50的范围。
[0094]
有用的plga聚合物可具有约5,000至500,000道尔顿、优选约150,000道尔顿的重均分子量。根据要达到的降解速率,可以使用不同分子量的聚合物。对于药物释放的扩散机制,聚合物应当保持完整,直到所有药物从聚合物基质中释放出来,然后降解。药物还可以随着聚合物赋形剂的生物侵蚀从聚合物基质中释放出来。
[0095]
plga可以通过任意常规方法制备,或者可以购买获得。例如,plga可以由环状丙交酯、乙交酯等通过采用适宜催化剂进行开环聚合来生产(参见ep-0058481b2;聚合变量对plga性质的影响:分子量、组成和链结构)。
[0096]
据信,plga可通过整个固体聚合物组合物的降解而是生物可降解的,这是由于可水解和可酶促裂解的酯键在生物条件下(例如在温血动物如人的组织中发现的生物酶和水的存在下)裂解形成乳酸和乙醇酸。乳酸和乙醇酸都是水溶性的、无毒的正常代谢产物,它们可以进一步生物降解形成二氧化碳和水。换言之,据信plga通过在水的存在下(例如在温血动物如人的身体中)酯基水解而降解,产生乳酸和乙醇酸并产生酸性小气候。乳酸和乙醇酸是温血动物如人在正常生理条件下体内各种代谢途径的副产物,因此被良好地耐受性和产生最小的全身毒性。
[0097]
为免生疑惑,数字范围的任何公开、例如“直至x”的量旨在包括上限x。因此,“直到60mg”的公开旨在包括60mg。
[0098]
本文引用的所有文献均通过引用整体并入本文。如果本公开中的定义与所引用文献中的定义相冲突,则以本公开为准。
[0099]
在以下实施例中进一步说明了本公开,这些实施例旨在示例而非限制。
[0100]
实施例1:i型双相性精神障碍和ii型双相性精神障碍患者的临床试验
[0101]
基本按照以下方案进行了多中心、多国、随机、双盲、固定剂量、安慰剂对照的临床试验。
[0102]
根据以下标准招募患者:
[0103]-主要纳入标准:任何种族的男性或女性个体,年龄18-75岁、包括端值,临床诊断为i型或ii型双相性精神障碍,正在经历当前的重症抑郁发作,能够提供书面知情同意书。
[0104]-主要排除标准:任何怀孕或哺乳的女性个体,被判断为医学上不适合参与研究的任何个体。
[0105]
将根据上述标准招募的总共381名患者以1:1随机分配到两个研究组:(i)卢美哌隆42mg(作为60mg卢美哌隆甲苯磺酸盐口服施用)和(ii)安慰剂。在卢美哌隆组中,每天晚上施用一次卢美哌隆(卢美哌隆甲苯磺酸盐60mg),持续6周。在安慰剂组中,每天晚上施用一次安慰剂,持续6周。患者没有接受其它用于治疗双相性精神障碍的药物。该研究是四重掩蔽的(即对参与者、护理提供者、研究者和结果评估者)。
[0106]
整个研究持续时间为约10周,包括长达2周的筛选期(禁用药物洗脱期)、6周的双盲治疗期和2周的安全性随访期。
[0107]
主要结果度量是抑郁评定量表(madrs)[时间框:第43天]。次要结果度量是临床总体印象量表-双相障碍版(cgi-bp)[时间框:第43天]和生活质量享受和满意度问卷-简表(quality oflife enjoyment and satisfaction questionanaire-short form,q-les-q-sf)[时间框:第43天]。
[0108]
本研究的另一个目标是确定卢美哌隆与安慰剂相比的安全性和耐受性,如通过以下项所测定:
[0109]
a.不良事件(aes)发生率
[0110]
b.杨氏躁狂量表(ymrs)
[0111]
c.哥伦比亚自杀严重程度评定量表(c-ssrs)
[0112]
d.异常不自主运动量表(aims)
[0113]
e.巴恩斯(barnes)静坐不能评定量表(bars)
[0114]
f.辛普森-安格斯(simpson angus)量表(sas)
[0115]
g.临床实验室评估
[0116]
h.心电图(ecg)
[0117]
i.生命体征测量
[0118]
j.体格检查和神经病学发现
[0119]
患者处置如下:
[0120]
表1
[0121][0122]
madrs总评分中从基线到第43天看到的变化如下:
[0123]
表2
[0124]
[0125]
cgi-bp-s总评分中从基线到第43天看到的变化如下:
[0126]
表3
[0127][0128]
因此,卢美哌隆42mg优于安慰剂,如madrs总评分和cgi-bp-s的统计学显著的改善所证明的那样,madrs总评分和cgi-bp-s是本研究中的主要和关键次要度量。本研究中用卢美哌隆42mg观察到的改善被认为具有临床意义。
[0129]
卢美哌隆的安全性与安慰剂相似。治疗中出现的不良事件(teaes)概况如下:
[0130]
表4
[0131][0132][0133]
卢美哌隆42mg通常是安全和良好耐受性的。观察到的发生率高于5%且高于安慰剂的最常报道的不良事件是头痛、嗜睡和恶心。重要的是,静坐不能和锥体外系症状的发生率低于1%,与安慰剂相似。
[0134]
在本试验中,每天一次卢美哌隆42mg达到了主要终点,在第6周(试验终点)相比于安慰剂有统计学上显著的更高的改善,如通过madrs总评分从基线的变化来测量的。在意向性治疗(itt)研究群体中,卢美哌隆42mg从基线的最小二乘法(ls)平均降低为16.7分,安慰剂为12.1分(ls平均差异=4.6分;效应量=0.56,p《0.001)。而且,早在第1周,卢美哌隆42mg就显示出与安慰剂的统计学上显著的分离,在整个试验的每个时间点都保持了这种分离。
[0135]
卢美哌隆42mg还达到了cgi-bp-s总评分(p《0.001;效应量=0.46)和专门评估抑郁的cgi分量(cgi-s抑郁评分;p《0.001;效应量=0.5)统计学上显著改善的关键次要终点。
[0136]
这些结果得到了响应率和缓解率的统计学显著益处的支持,证明了主要结果的临床意义。此外,在ii型双相性精神障碍患者的亚组分析中,卢美哌隆42mg就madrs总评分而言统计学上显著地优于安慰剂。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1