曲坦微穿孔递送系统的制作方法
曲坦微穿孔递送系统
1.背景
2.领域
3.本技术涉及用于透皮药物递送的组合物、装置和方法,并且具体涉及曲坦组合物和通过透皮微穿孔设备向个体施用曲坦的方法。
4.描述
5.偏头痛是影响全世界约10%的成年人群的病症,影响约6亿人,仅在美国就有约2800万人。女性患偏头痛性头痛的频率比男性高三倍。偏头痛性头痛与发炎和扩张的血管有关,导致严重的单侧疼痛,并在身体活动时恶化。约五分之一的偏头痛患者经历先兆或视觉症状,例如光斑、锯齿线或视线变灰。偏头痛通常持续长达24小时,但可以是4至72小时,并且患者经常经历每月一两次的偏头痛发作。
6.偏头痛可以由许多不同的因素触发,包括生活压力,某些食物或饮食习惯,昼夜节律、日程安排或睡眠模式的变化以及诸如气压或海拔的气候变化以及月经周期期间激素水平的周期性变化。药理学干预构成了治疗偏头痛的主流,并且可用于急性治疗(中止性)和预防(预防性)。
7.曲坦是可以用于治疗中度至重度的急性偏头痛的血清素受体激动剂。当这些药剂在发作过程的早期使用时,曲坦在两个小时内中止超过80%的偏头痛。然而,有几种不同的曲坦产品可用,该类中不同药物的功效和耐受性方面存在差异。曲坦也可用于各种制剂。非口服制剂通常用于患有恶心或呕吐的胃肠道症状的患者以及需要更快速的起效时。曲坦被认为通过激活三叉神经血管神经末梢上的血清素(5-ht)受体起作用,抑制引起疼痛性颅血管舒张的神经递质的释放。此外,曲坦产生主动血管收缩,并且可以通过刺激颅血管上的5-ht受体来减轻偏头痛的症状。含有曲坦的口服片剂通常具有不足的功效并且缺乏足够快的起效。皮下注射显示出较高的功效和快速起效,但有时会引起严重的副作用。口服途径和经鼻途径经常引起不希望的味道问题,并且难以对恶心和呕吐的偏头痛患者施用。
8.被动透皮药物递送是施用各种治疗剂的方便且有效的方式。这种给药途径是非侵入性的并且在延长的时间段内产生稳定的药物递送。尽管常规的透皮系统(例如药物贴片)已经证明了经由皮肤递送药物的益处,但它们仅适用于极其有限数量的药物。这是因为数百万的死皮细胞在皮肤表面上形成保护屏障(角质层),阻止大多数治疗分子进入皮肤。
9.角质层主要负责皮肤的屏障特性。因此,正是该层对药物或其它分子进入体内和分析物排出体外的透皮通量提供了最大的屏障。角质层(皮肤的外角化层)是由脂质结构域分开的致密角质化细胞残余物的复杂结构。与口腔或胃粘膜相比,角质层对身体外部或内部的分子的渗透性均小得多。角质层由角质形成细胞形成,所述角质形成细胞包括大部分失去其细胞核并变成角化细胞的表皮细胞。这些死细胞构成角质层,其厚度仅为约10至30微米,并且保护身体免受外源性物质的侵入以及内源性流体和溶解分子的向外迁移。角质层通过在脱皮期间角质层细胞的脱落和角质化过程形成新的角质层细胞而不断更新。
10.在历史上,大多数药物已经通过口服或注射递送。然而,口服或注射途径均不太适于在延长的时间段内连续递送药物。此外,注射施用方法既不方便也不舒适;另外,针在其
使用后继续造成危险。因此,透皮药物递送至身体已经是将有限数量的渗透物递送至生物体的流行且有效的方法。
11.被动透皮贴片通常限于分子量小于500道尔顿的脂溶性药物。为了增强透皮药物递送,存在用于增加皮肤对药物的渗透性的已知方法。例如,第8,116,860号美国专利描述了透皮渗透物递送系统和方法,其在几毫秒内在角质层中无痛地产生水性微孔。这些水性通道使水溶性药物能够从透皮贴片中流出,进入活性表皮,然后进入体循环。贴片可以被配制成提供推注或持续透皮递送。
12.正在以passport商品名开发透皮渗透物递送系统。passport系统包括可重复使用的手持式施用器和具有药物贴片的一次性穿孔器。按压施用器的激活按钮,向穿孔器释放能量脉冲。该能量快速传导至皮肤表面,无痛地烧蚀每个细丝下的角质层,以产生微通道。然后将简单的透皮贴片应用于经烧蚀的皮肤并开始药物递送。
13.2013年美国食品和药物管理局(fda)批准了用于透皮递送曲坦的离子导入系统。该系统以商品名zecuity销售,使用电池供电的离子导入贴片来递送舒马曲坦。然而,在2016年,在制造商收到了在用zecuity治疗的患者中被描述为“烧伤”和/或“疤痕”的应用部位反应的上市后报告之后,将它从市场召回。这些反应的描述包括佩戴贴片处的严重的发红、皮肤裂伤、起泡或焊伤,以及烧伤或疤痕。患者描述了严重的疼痛、瘙痒或烧伤。尽管许多病例在数小时至数周内消退,但存在皮肤反应(通常是皮肤变色)在几个月后仍未消退的病例的报道。
14.因此,仍然长期需要用于透皮递送曲坦的改善的组合物、装置和方法。
技术实现要素:
15.在一些方面,本文描述了用于向有需要的个体递送曲坦药物的贴片。贴片可以包括:包含粘合剂的顶层;包含曲坦的中间层;以及底层,其中底层包括离型内衬。
16.在一些实施方案中,中间层还包含皮肤刺激减弱剂。
17.在一些实施方案中,中间层还包含约0.01g/cm2至约0.5g/cm2的量的稳定剂。
18.在一些实施方案中,曲坦和皮肤刺激减弱剂的量的摩尔比为约1:0.5至约1:2。
19.在一些实施方案中,曲坦选自舒马曲坦、利扎曲坦或佐米曲坦。
20.在一些实施方案中,皮肤刺激减弱剂是有机酸或其盐。
21.在一些实施方案中,有机酸选自抗坏血酸、柠檬酸、琥珀酸、酒石酸、马来酸、乳酸、苯甲酸和山梨酸或其组合。
22.在一些实施方案中,稳定剂是糖。
23.在一些实施方案中,糖选自甘露糖醇、麦芽糖、海藻糖、木糖醇、木糖、右旋糖、乳糖、山梨糖醇、蔗糖、果糖、麦芽糖醇、赤藓糖醇、乳糖醇、异麦芽酮糖醇和环糊精或其组合。
24.在一些实施方案中,中间层还包括配置成容纳曲坦的贮存器。
25.在一些实施方案中,贮存器包含基质。
26.在一些实施方案中,基质具有约0.1mg/cm2至约10mg/cm2的保水能力。
27.在一些实施方案中,基质包括非织造织物。
28.在一些实施方案中,基质具有约10μm至约100μm的厚度。
29.在一些实施方案中,基质面积重量为约10g/m2至约100g/m2。
30.在一些实施方案中,基质的尺寸为约0.25cm2至约5cm2。
31.在一些实施方案中,贴片还包含抗微生物剂。
32.在一些实施方案中,抗微生物剂选自苯甲酸、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、苯扎氯铵、氯己定、甲酚、水杨酸、山梨酸和苄索氯铵中的至少一种或其组合。
33.在一些实施方案中,皮肤刺激减弱剂是非有机酸或其盐。
34.在一些实施方案中,非有机酸选自盐酸、磷酸、硼酸和乙酸。
35.在一些实施方案中,基质包含约0.1至约5.0mg/cm2的佐米曲坦。
36.在一些实施方案中,佐米曲坦和皮肤刺激减弱剂的量为约1:0.75至约1:1.15。
37.在一些实施方案中,基质的尺寸为约0.25cm2至约4cm2。
38.在一些实施方案中,稳定剂是蔗糖。
39.在一些实施方案中,每单位面积的基质具有的佐米曲坦和稳定剂的总量为0.05至0.5mg/cm2。
40.在一些方面,本文描述了治疗有需要的个体的方法。所述方法可以包括鉴定患有偏头痛的个体,在个体的皮肤中打开多个微孔,将贴片应用于个体的皮肤,在微孔上持续一定的时间段,其中贴片包括:包含粘合剂的顶层;包含曲坦的中间层;以及底层,其中底层包括离型内衬,其中选择所述时间段以通过多个微孔递送治疗有效量的曲坦。
41.在一些实施方案中,中间层还包含皮肤刺激减弱剂和稳定剂。
42.在一些实施方案中,在个体的皮肤中打开多个微孔包括对个体的皮肤应用透皮微穿孔设备。
43.在一些实施方案中,透皮微穿孔是热组织烧蚀。
44.在一些实施方案中,透皮微穿孔产生穿过角质层至表皮的微孔。
45.在一些实施方案中,透皮微穿孔设备具有约2至约5mj/细丝的穿孔能量。
46.在一些实施方案中,透皮微穿孔设备具有约200至约500细丝/cm2的穿孔能量密度。
47.在一些实施方案中,透皮微穿孔设备具有约400细丝/cm2的穿孔能量密度。
48.在一些实施方案中,透皮微穿孔穿孔能量为约4mj/细丝,并且穿孔能量密度为约400细丝/cm2。
49.在一些实施方案中,透皮微穿孔细丝阵列尺寸为约0.5至约5cm2。
50.在一些实施方案中,曲坦和皮肤刺激减弱剂为约1:0.5至约1:2。
51.在一些方面,本文描述了用于递送药物的透皮药物递送贴片系统。透皮药物递送贴片系统包括用于加热皮肤表面的透皮微穿孔设备;以及曲坦药物递送贴片。
52.在一些实施方案中,曲坦药物递送贴片系统包括:包含粘合剂的顶层;具有配置成容纳曲坦的至少一个贮存器的中间层;以及底层,其中底层包括离型内衬。
53.在一些实施方案中,中间层还包含皮肤刺激减弱剂和稳定剂。
54.在一些实施方案中,微穿孔设备包括传导构件,所述传导构件被配置成在操作期间基于流过传导构件的电流产生热能,并且将热能供应至与传导构件接触的皮肤表面。
55.在一些实施方案中,透皮药物递送贴片系统还包括电源,所述电源被配置成将电流以多个脉冲以电源电流值提供至传导构件
56.下面将更详细地描述这些和其它实施方案。
57.附图简述
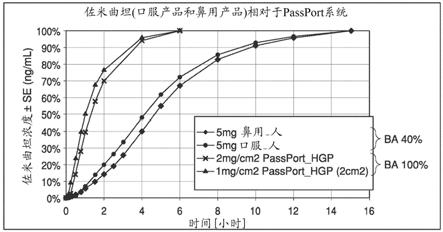
58.附图并入本说明书中并构成本说明书的一部分,附图例示出以下描述的几个方面,并与描述一起用于解释本发明的原理。在所有附图中,相同的数字表示相同的元件。
59.图1例示了对无毛大鼠的施用途径比较研究的结果。
60.图2例示了对豚鼠的施用途径比较研究的结果。
61.图3例示了人和无毛豚鼠的数据的比较。
62.图4例示了不同细丝密度的药代动力学(pk)曲线。
63.图5例示了不同细丝密度的pk曲线。
64.图6例示了细丝密度与pk结果之间的关系。
65.图7例示了不同细丝密度的皮肤刺激结果。
66.图8例示了不同细丝密度的皮肤刺激结果。
67.图9例示了细丝密度与副作用之间的关系。
68.图10例示了不同穿孔能量的pk曲线。
69.图11例示了穿孔能量与pk结果之间的关系。
70.图12例示了不同穿孔能量的皮肤刺激结果。
71.图13例示了穿孔能量与副作用之间的关系。
72.图14例示了不同细丝阵列尺寸的pk曲线。
73.图15例示了不同细丝阵列尺寸的剂量响应。
74.图16例示了不同细丝阵列尺寸的皮肤刺激结果。
75.图17例示了剂量与副作用之间的关系。
76.图18例示了皮下注射途径与透皮微穿孔系统的比较结果。
具体实施方式
77.通过参考下面的详细描述、实施例、附图和权利要求以及它们的先前和随后的描述,可以更容易地理解本发明。然而,在公开和描述本技术装置、系统和/或方法之前,应理解,除非另有说明,本发明不限于所公开的特定装置、系统和/或方法。还应理解,本文使用的术语仅用于描述特定方面的目的,而不必旨在限制。
78.提供该描述作为本发明的有效教导。为此,相关领域的技术人员将认识和理解,可以对本文描述的本发明的各个方面进行许多改变,同时仍然获得有益的结果。还将显而易见的是,通过选择本文所述的一些特征而不利用其它特征,可以获得一些期望的益处。因此,本领域技术人员将认识到,对本说明书的许多修改和调整是可能的,并且甚至在某些情况下是期望的,并且是本发明的一部分。因此,提供该描述是为了说明本发明的某些原理,而不是限制本发明。
79.定义
80.如全文使用,单数形式“一(a)”、“一(an)”和“所述(the)”包括复数指代物,除非上下文另有明确规定。因此,例如,提及的“细丝”可以包括两个或更多个这样的细丝,除非上下文另有说明。
81.本文可将范围表示为从“约”一个特定值,和/或至“约”另一个特定值。当表示这样的范围时,另一方面包括从一个特定值和/或至另一个特定值。类似地,当通过使用先行词“约”将值表示为近似值时,应理解,特定值构成了另一方面。还应理解,每个范围的端点既与另一端点相关,又独立于另一端点而有意义。
82.如本文使用,“任选的”或“任选地”意指随后描述的事件或情况可能发生或可能不发生,并且该描述包括所述事件或情况发生的例子和所述事件或情况不发生的例子。
83.如本文使用,“角质层”是指皮肤的最外层,其由处于不同干燥阶段的约15至约20层细胞组成。角质层提供了防止水从身体内部流失到外部环境以及防止外部环境对身体内部造成损伤的屏障。
84.如本文使用,“组织”是指特定种类的细胞与构成结构材料的其细胞间物质的聚集体。组织的至少一个表面必须是装置可接近的。优选的组织是皮肤。适用于本发明的其它组织包括粘膜组织和软器官。
85.如本文使用,术语“间质液”是占据体内细胞之间的空间的透明流体。如本文使用,术语“生物流体”定义为源自生物有机体的流体,包括血清或全血以及间质液。
86.如本文使用,“组织膜”可以是个体的任何一个或多个表皮层。例如,在一个方面,组织膜是皮肤层,其包括皮肤的最外层,即角质层。在一个替代方面,皮肤层可以包括表皮的一个或多个背衬层,通常被认定为颗粒层、有棘层和生发层。本领域普通技术人员应理解,对穿过表皮的背衬层运输或吸收渗透物基本上没有阻力或没有阻力。因此,在一个方面,至少一个在个体的皮肤层中形成的路径是个体的角质层中的路径。此外,如本文使用,“角质层”是指皮肤的最外层,通常由处于不同干燥阶段的约15至约20层细胞组成。角质层提供了防止水从身体内部流失到外部环境以及防止外部环境对身体内部造成损伤的屏障。此外,如本文使用,“组织膜”可以是指特定种类的细胞与其细胞间物质一起形成结构材料的聚集体。在各种实施方案中,组织膜的至少一个表面是本文所述的一个或多个穿孔装置和/或渗透物组合物可接近的。如上所述,优选的组织膜是皮肤。适合与这种装置和组合物一起使用的其它组织包括粘膜组织和软器官。
87.如本文使用,术语“皮下流体”可以包括但不限于水分、血浆、血液、一种或多种蛋白质、间质液及其任意组合。在一个方面,根据本说明书的皮下流体是包含水的水分源。
88.如本文使用,“穿孔”、“微穿孔”或任何这样的类似术语意指在组织或生物膜(例如皮肤或粘膜)或生物体的外层中,或者穿过组织或生物膜(例如皮肤或粘膜)或生物体的外层形成小孔或缝隙(随后也称为“微孔”),以出于选择的目的降低该生物膜的屏障性质来使至少一种渗透物从生物膜的一侧通过到另一侧。优选地,这样形成的洞或“微孔”的直径为约1至1000微米,并延伸到生物膜中,足以破坏角质层的屏障性质,而不会对下面的组织产生不利影响。应理解,为了简单起见,术语“微孔”以单数形式使用,但本文所述的微穿孔装置可以形成多个人造开口。出于选择的目的或出于某些医疗或手术目的,穿孔可以降低生物膜至体内的屏障性质。出于本技术的目的,“穿孔”和“微穿孔”可互换使用,并且意指相同的事情。
[0089]“微穿孔器”或“穿孔器”是用于能够进行微穿孔的微穿孔装置的组件。微穿孔器或穿孔器的实例包括,但不限于,能够经由直接接触生物膜而传导地递送热能以使烧蚀膜的一部分的深度足以形成微孔的细丝、光学加热的局部染料/吸收层、机电致动器、微型刺血针、微型针或刺血针的阵列、声能烧蚀器、激光烧蚀系统、高压流体射流穿刺器等。如本文使用,“微穿孔器”和“穿孔器”可互换使用。
[0090]
如本文使用,“穿透”意指由烟火元件爆炸时释放的热能和动能引起的细胞的受控去除,这导致生物膜的细胞和可能的一些相邻细胞“吹离”该部位。如本文使用,“可熔的”和“熔断器”是指当足够量的能量或热量被施加到电路上时可以将其自身从电路中去除的元件。即,当电阻性的、电激活的穿孔元件被设计为可熔元件时,这意味着在生物膜中形成微孔的期间或之后,在启动时,该元件断开,从而阻止电流流过该元件。
[0091]
如本文使用,“穿透增强”或“渗透增强”意指生物膜对药物、生物活性组合物或其它化学分子、化合物、颗粒或物质(也称为“渗透物”)的渗透性增加,从而增加药物、生物活性组合物或其它化学分子、化合物或颗粒渗透生物膜的速率。
[0092]
如本文使用,“增强剂”、“化学增强剂”、“穿透增强剂”、“渗透增强剂”等包括增加渗透物、分析物或其它分子跨生物膜的通量的所有增强剂,并且仅受功能限制。换而言之,旨在包括所有细胞包膜无序化合物和溶剂以及任何其它化学增强剂。另外,包括所有主动力增强剂技术,例如应用声能、机械抽吸、压力或组织的局部变形、离子导入或电穿孔。一种或多种增强剂技术可以依次或同时组合。例如,可以首先应用化学增强剂以使毛细血管壁可渗透,然后可以应用离子导入或声能场以主动地驱动渗透物进入围绕并包括毛细血管床的那些组织。
[0093]
如本文使用,“透皮”或“经皮”是指使渗透物进入和通过生物膜以实现渗透物的有效治疗血液水平或局部组织水平,或使存在于体内的分子或流体(“分析物”)通过生物膜流出,使得可以在身体外部收集分析物分子。
[0094]
如本文使用,术语“渗透物”、“药物”、“渗透物组合物”或“药理学活性剂”或任何其它类似术语可互换使用,是指通过本领域先前已知的方法和/或通过本说明书中教导的方法适于透皮施用的任何化学或生物材料或化合物,其诱导所需的生物学或药理学作用,其可以包括但不限于(1)对生物体具有预防性作用并防止不期望的生物学作用,例如感染,(2)缓解由疾病引起的病况,例如缓解疼痛或炎症,和/或(3)缓解、减轻或完全消除生物体的疾病。所述作用可以是局部的,例如提供局部麻醉作用,或者可以是全身的。此类物质包括通常(包括通过身体表面和膜,包括皮肤)递送到体内的多种化合物。通常,例如但不意味着限制,此类物质可以包括诱导所需生物学或药理学作用的任何生物活性剂,例如药物、化学或生物材料。为此,在一个方面,渗透物可以是小分子药剂。在另一方面,渗透物可以是大分子药剂。在各种实施方案中,渗透物是曲坦。曲坦的实例包括舒马曲坦、佐米曲坦、利扎曲坦、那拉曲坦、依来曲坦、多尼曲坦、阿莫曲坦、夫罗曲坦、阿维曲坦、ly-334370、l0703,664和gr 46611。
[0095]
在各种实施方案中,可以与本文所述的组合物和方法一起使用和/或适于与本文所述的组合物和方法一起使用的透皮渗透物递送系统和方法描述于第6022316号、第6142939号、第6173202号、第6183434号、第6508785号、第6527716号、第6692456号、第6730028号、第7141034号、第7392080、第7758561号、第8016811号、第8116860号和/或第9498609号美国专利中的一个或多个中,所述美国专利全部通过引用整体据此并入,并且尤其出于描述此类系统和方法的目的。在各种实施方案中,以passport商品名商购自nitto denko corporation的透皮渗透物递送系统可以用于或适用于递送本文所述的渗透物组合物。
[0096]
如本文使用,药理学活性剂的“有效”量意指足以在参与任何医学治疗时以合理的
益处/风险比提供所需的局部或全身作用和性能的化合物的量。如本文使用的渗透增强剂或化学增强剂的“有效”量意指所选择的量以提供生物膜渗透性、所需的穿透深度、施用速率和所递送药物的量的所需增加。
[0097]
如本文使用,“动物”或“生物体”是指可以适用本发明的人和其它活的生物体,包括植物。
[0098]
如本文使用,“分析物”意指适于通过本发明教导的技术或通过本领域先前已知的技术穿过生物膜的任何化学或生物材料或化合物,其中个体可能希望知道体内的浓度或活性。葡萄糖是分析物的具体实例,因为它是适于穿过皮肤的糖,并且个体,例如患有糖尿病的个体,可能希望知道其血糖水平。分析物的其它实例包括但不限于诸如钠、钾、胆红素、尿素、氨、钙、铅、铁、锂、水杨酸盐等的化合物。
[0099]
如本文使用,“透皮通量率”是指任何分析物通过个体、人或动物的皮肤离开的穿过速率,或者任何渗透物、药物、药理活性剂、染料或颜料进入并通过生物体的皮肤的穿过速率。
[0100]
如本文使用,“非侵入性”意指不需要针、导管或其它侵入性医疗器械进入身体的一部分。
[0101]
如本文使用,“微创”是指使用侵入角质层以产生小洞或微孔而不会对下面的组织造成实质性损伤的机械、液压或电气机构。
[0102]
如本文使用,“药物可接受的载体”是指其中可以提供用于递送的物质(例如药物可接受的药物)的载体。药物可接受的载体描述在本领域中,例如,在“remington:the science and practice of pharmacy”,mack publishing company,pennsylvania,1995中,其公开内容通过引用并入本文。载体可以包括,例如,水和其它水溶液,糖,多糖,缓冲剂,赋形剂,以及可生物降解的聚合物,例如聚酯、聚酐、聚氨基酸、脂质体及其混合物。
[0103]
如本文使用,“贮存器”是指装置内的指定区域或腔室,其被设计成容纳用于通过生物膜中的人造开口递送到生物体内的渗透物,或者可以被设计成接收通过生物膜中的人造开口从生物体中提取的生物流体样品。贮存器还可以含有增强单独容纳的生物活性渗透物的作用的赋形剂化合物。另外,贮存器可以包含设计成允许测量或检测提取的生物流体中的选定分析物的反应性酶或试剂或用其处理。贮存器可以由开放的体积空间、凝胶、已经用选定的化合物涂覆或处理用于随后释放或反应的平面空间、或可渗透的固体结构(例如丸剂、片剂或多孔聚合物)组成。
[0104]
本公开内容的装置和方法可以用于跨皮肤透皮递送曲坦。在一些方面,贴片可以包括:包含粘合剂的顶层、包含曲坦的中间层、以及底层。在一些实施方案中,底层包括离型内衬。在一些实施方案中,中间层还包含皮肤刺激减弱剂。在一些实施方案中,中间层还包含稳定剂。在一些实施方案中,贴片包括组织界面层。
[0105]
在第7,392,080号美国专利中描述了合适的组织界面层的实例,所述美国专利通过引用整体据此并入,特别是出于描述透皮药物递送贴片系统的目的。在一些方面,组织界面层可以包括以下中的一些或全部:用于实现组织穿孔的元件,用于将装置附接至组织的粘合剂,容纳用于递送的渗透物的贮存器,用于容纳提取的生物流体的贮存器,以及用于测定分析物的试剂。组织界面层还可以包括亲水和疏水表面处理物以用作流体流动改变剂,用于控制所收集的液体渗透物或生物流体的运动。组织界面层还可以掺入抗微生物剂以防
止脓毒病,或者掺入抗血凝剂或抗凝剂以控制渗透物或所提取的生物流体的聚集。组织界面层也可以用渗透增强剂或用于ph稳定的缓冲液处理。组织界面层可以包含充满有益渗透物的刺激响应性聚合物凝胶区段,其可以通过热、化学或电刺激触发来释放有益渗透物。当被例如组织界面层上的穿孔元件或其它类似元件加热时,组织界面层可以根据需要释放有益渗透物。组织界面层可以包含压电元件,用于将声能传送到组织或被递送的渗透物或被提取的生物流体中。
[0106]
在一些方面,组织界面层可以包括一个或多个贮存器。在多个贮存器的情况下,这些贮存器可以用于保持不同的和可能不相容的渗透物分开。从贮存器递送渗透物可以同时或依次进行。在一些实施方案中,可以对贮存器壁进行穿孔以在贮存器膜上打开缺口并允许将渗透物递送到组织中。用与用于对组织进行穿孔的类型相同的穿孔元件来完成对贮存器的这种穿孔。在该贮存器上打开缺口之前,贮存器可以保持渗透物的稳定、密封且无菌的环境,从而允许有效且经济地制造和包装集成装置的整个一次性部分。在贮存器上打开缺口可以根据需要在组织的穿孔之前、同时或之后发生。另外,如果所有其它因素例如微孔密度或离子导入电流相同,则从特定贮存器进入组织的渗透物的通量率与将贮存器联接至生物膜的微孔的面积成比例。贮存器最初可以是空的或含有吸收材料,以便用作提取的生物流体的存储位置。用于测定生物流体中的分析物的试剂通常位于所提取的生物流体存储贮存器的入口处。
[0107]
此外,如本文使用,“曲坦”意指在治疗偏头痛和丛集性头痛中用作中止药物的一类或一族基于色胺的药物。曲坦的实例包括但不限于舒马曲坦、利扎曲坦、那拉曲坦、依来曲坦、多尼曲坦、阿莫曲坦、夫罗曲坦、阿维曲坦和佐米曲坦。在一些实施方案中,曲坦包括佐米曲坦、舒马曲坦或利扎曲坦。在一些实施方案中,曲坦包括佐米曲坦。
[0108]
在一些方面,皮肤刺激减弱剂是有机酸。在一些实施方案中,皮肤刺激减弱剂是有机酸的盐形式。在一些实施方案中,有机酸选自抗坏血酸、柠檬酸、琥珀酸、酒石酸、马来酸、乳酸、苯甲酸和山梨酸或其组合。在一些实施方案中,皮肤刺激减弱剂选自非有机酸。在一些实施方案中,皮肤刺激减弱剂是非有机酸的盐形式。在一些实施方案中,非有机酸是盐酸、磷酸、硼酸、乙酸或其组合。在一些实施方案中,非有机酸在制造过程期间蒸发。
[0109]
在一些方面,稳定剂是糖。在一些实施方案中,糖选自甘露糖醇、麦芽糖、海藻糖、木糖醇、木糖、右旋糖、乳糖、山梨糖醇、蔗糖、果糖、麦芽糖醇、赤藓糖醇、乳糖醇、异麦芽酮糖醇和环糊精或其组合。在一些实施方案中,稳定剂是蔗糖。
[0110]
在一些实施方案中,贴片中的曲坦和皮肤刺激减弱剂的量的摩尔比为约1:0.5至约1:2。在一些实施方案中,曲坦和皮肤刺激减弱剂的摩尔比为约1:0.75至约1:1.5。
[0111]
在一些方面,贴片的中间层包括贮存器。在一些实施方案中,贮存器包含约0.1重量%至约90重量%的曲坦。在一些实施方案中,曲坦占中间层的约20重量%至约80重量%,包括中间层的例如25重量%、30重量%、35重量%、40重量%、45重量%、50重量%、55重量%、60重量%、65重量%、70重量%和75重量%,并且包括由这些值得到的任何重量百分比范围。
[0112]
在一些实施方案中,中间层包含约0.1重量%至约90重量%的稳定剂。在一些实施方案中,稳定剂占中间层的约20重量%至约80重量%,包括中间层的例如25重量%、30重量%、35重量%、40重量%、45重量%、50重量%、55重量%、60重量%、65重量%、70重量%
和75重量%,并且包括由这些值得到的任何重量百分比范围。
[0113]
在一些实施方案中,中间层包含约0.1重量%至约90重量%的皮肤刺激减弱剂。在一些实施方案中,皮肤刺激减弱剂占中间层的约20重量%至约80重量%,包括中间层的例如25重量%、30重量%、35重量%、40重量%、45重量%、50重量%、55重量%、60重量%、65重量%、70重量%和75重量%,并且包括由这些值得到的任何重量百分比范围。
[0114]
在一些方面,中间层包含基质。在一些实施方案中,基质是非织造织物。
[0115]
在一些实施方案中,基质具有约0.1mg/cm2至约10mg/cm2的基质保水能力(whc)。基质的保水能力意指基质每1cm2可以保持的水分的量。具体地,制备1cm2基质,将其浸入溶液(含有0.1%表面活性剂(吐温80)的磷酸盐缓冲盐水)中持续足够长的时间。然后,将基质从溶液中缓慢拉出约5秒钟,从保持有液体的样品的重量中减去预先测量的样品在浸入之前的重量,然后可以确定每单位面积(1cm2)的基质的保水能力。在一些实施方案中,基质保水能力为约0.5mg/cm2至约8mg/cm2。在一些实施方案中,基质保水能力为约1mg/cm2至约6mg/cm2。在一些实施方案中,基质保水能力为约2mg/cm2至约5mg/cm2。
[0116]
基质的保水能力可以通过调节基质的厚度和重量来控制。优选基质具有100μm或更小的厚度。在一些实施方案中,基质具有约10μm至约100μm的厚度。在一些实施方案中,基质厚度为约20μm至约90μm。在一些实施方案中,基质厚度为约30μm至约80μm。在一些实施方案中,基质厚度为约40μm至约60μm。
[0117]
在一些实施方案中,基质面积重量为约10g/m2至约100g/m2。在一些实施方案中,基质面积重量为约20g/m2至约80g/m2。在一些实施方案中,基质面积重量为约30g/m2至约70g/m2。在一些实施方案中,基质面积重量为约40g/m2至约60g/m2。
[0118]
在一些实施方案中,基质面积重量为约0.1mg/cm2至约30mg/cm2。在一些实施方案中,基质面积重量为约5mg/cm2至约30mg/cm2。在一些实施方案中,基质面积重量为约10mg/cm2至约30mg/cm2。在一些实施方案中,基质面积重量为约20mg/cm2至约30mg/cm2。在一些实施方案中,基质面积重量为约0.5mg/cm2至约5mg/cm2。在一些实施方案中,基质面积重量为约0.5mg/cm2至约10mg/cm2。
[0119]
在一些实施方案中,基质的尺寸为约0.25cm2至约4cm2。在一些实施方案中,基质的尺寸为约0.5cm2至约3cm2。在一些实施方案中,基质的尺寸为约1cm2至约2cm2。在一些实施方案中,基质的尺寸为约1cm2。在一些实施方案中,基质的尺寸为约2cm2。在一些实施方案中,基质的尺寸为约3cm2。
[0120]
在一些实施方案中,每单位面积的基质的曲坦和稳定剂的总量为0.05mg/cm2至0.5mg/cm2。在一些实施方案中,每单位面积的基质的曲坦和稳定剂的总量为0.1mg/cm2至0.5mg/cm2。在一些实施方案中,每单位面积的基质的曲坦和稳定剂的总量为0.2mg/cm2至0.5mg/cm2。在一些实施方案中,每单位面积的基质的曲坦和稳定剂的总量为0.3mg/cm2至0.5mg/cm2。在一些实施方案中,每单位面积的基质的曲坦和稳定剂的总量为0.05mg/cm2至0.5mg/cm2。
[0121]
在一些实施方案中,基质成分的ph为约3至约6。在一些实施方案中,基质的ph为约4至约6。在一些实施方案中,基质的ph为约5至约6。在一些实施方案中,基质的ph为约3。在一些实施方案中,基质的ph为约4。在一些实施方案中,基质的ph为约5。在一些实施方案中,基质的ph为约6。
[0122]
在一些方面,基质包含约0.1mg/cm2至约5.0mg/cm2的曲坦。在一些实施方案中,基质包含约0.1mg/cm2至约3.0mg/cm2的曲坦。在一些实施方案中,基质包含约0.5mg/cm2至约5.0mg/cm2的曲坦。在一些实施方案中,基质包含约0.5mg/cm2至约3.0mg/cm2的曲坦。在一些实施方案中,基质包含约0.5mg/cm2至约2.0mg/cm2的曲坦。在一些实施方案中,基质包含约0.5mg/cm2的曲坦。在一些实施方案中,基质包含约1mg/cm2的曲坦。在一些实施方案中,基质包含约2mg/cm2的曲坦。在优选实施方案中,曲坦是佐米曲坦。
[0123]
在一些方面,基质包含约0.1mg/cm2至约5.0mg/cm2的稳定剂。在一些实施方案中,基质包含约0.1mg/cm2至约3.0mg/cm2的稳定剂。在一些实施方案中,基质包含约0.5mg/cm2至约5.0mg/cm2的稳定剂。在一些实施方案中,基质包含约0.5mg/cm2至约3.0mg/cm2的稳定剂。在一些实施方案中,基质包含约0.5mg/cm2至约2.0mg/cm2的稳定剂。在一些实施方案中,基质包含约0.5mg/cm2的稳定剂。在一些实施方案中,基质包含约1mg/cm2的稳定剂。在一些实施方案中,基质包含约2mg/cm2的稳定剂。在优选实施方案中,稳定剂是蔗糖。
[0124]
在一些方面,贴片还包含抗微生物剂。在一些实施方案中,抗微生物剂选自苯甲酸、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、苯扎氯铵、氯己定、甲酚、水杨酸、山梨酸和苄索氯铵及其组合。
[0125]
在一些方面,本技术还包括使用如本文所述的贴片向有需要的个体施用曲坦的方法。在一些实施方案中,治疗个体的方法包括:鉴定患有偏头痛的个体;在个体的皮肤中打开多个微孔;以及将贴片应用于个体的皮肤,在微孔上持续一定的时间段。在一些实施方案中,贴片包括:包含粘合剂的顶层、包含曲坦的中间层、以及底层。在一些实施方案中,底层包括离型内衬。在一些实施方案中,选择时间段以通过多个微孔递送治疗量的曲坦。
[0126]
在一些实施方案中,在个体的皮肤中打开多个微孔包括对个体的皮肤应用透皮微穿孔设备。在一些实施方案中,透皮微穿孔设备包括传导构件,所述传导构件包括导电细丝的阵列。在一些实施方案中,透皮微穿孔设备包括传导构件,所述传导构件包括导电细丝的阵列。在一些实施方案中,透皮微穿孔通过热组织烧蚀打开微孔。在一些实施方案中,透皮微穿孔产生穿过角质层至表皮的微孔。
[0127]
在一些实施方案中,透皮微穿孔设备具有约2mj/细丝至约8mj/细丝的穿孔能量。在一些实施方案中,透皮微穿孔设备具有约200细丝/cm2至约500细丝/cm2的细丝密度。在一些实施方案中,透皮微穿孔设备具有约400细丝/cm2的细丝密度。在一些实施方案中,透皮微穿孔穿孔能量为约4mj/细丝至约5mj/细丝,并且细丝密度为约400细丝/cm2。在一些实施方案中,透皮微穿孔细丝阵列尺寸为约0.5cm2至约3cm2。
[0128]
在一些实施方案中,贴片基本上不刺激个体的皮肤。如本文使用,术语“基本上不刺激个体的皮肤”包括在去除贴片时产生的皮肤红斑分数为约3.0或更低、优选约2.0或更低、更优选约1.0或更低。在另一个实施方案中,状况“基本上不刺激个体的皮肤”可以是指皮肤刺激缓解天数为约4.0或更少、优选约3.0或更少、更优选约2.5或更少。在另一个实施方案中,状况“基本上不刺激个体的皮肤”是指在去除贴片时产生的皮肤红斑分数为约3.0或更低、优选约2.0或更低、更优选约1.0或更低,并且皮肤刺激缓解天数为约4.0或更少、优选约3.0或更少、更优选约2.5或更少。
[0129]
在一些方面,本技术还包括使用贴片向有需要的个体施用曲坦的系统。在一些实施方案中,透皮药物递送贴片系统包括:用于加热皮肤表面的透皮微穿孔设备和曲坦药物
递送贴片,包括但不限于如本文所述的曲坦药物递送贴片。在一些实施方案中,药物递送贴片系统包括:包含粘合剂的顶层;具有用于包含曲坦的至少一个贮存器的中间层;以及底层,其中所述底层包括离型内衬。在一些实施方案中,微穿孔设备包括传导构件,所述传导构件被配置成在操作期间基于流过所述传导构件的电流产生热能并且将热能供应至与传导构件接触的皮肤表面。在一些实施方案中,透皮药物递送贴片系统还包括电源,所述电源被配置成将电流以多个脉冲以电源电流值提供至传导构件,所述传导构件有效地在皮肤表面上打开微孔。
[0130]
实施例
[0131]
在以下实施例中进一步详细地公开了各种实施方案和替代方案,这些实施方案和替代方案不旨在以任何方式限制权利要求的范围。在下文中,zol=佐米曲坦;ca=柠檬酸一水合物;suc=蔗糖;aa=抗坏血酸;sb=苯甲酸钠;ta=酒石酸。使用passport微穿孔系统。使用具有100至400根热穿孔细丝的阵列的设备(例如来自nitto denko corporation的passport
tm
热穿孔系统)通过热穿孔在动物个体的皮肤上提供施用部位。
[0132]
佐米曲坦和苯甲酸利扎曲坦购自inke s.a.(西班牙)。琥珀酸舒马曲坦购自lgm pharma(美国)。实施例1至实施例10中使用的药物贴片的基质是eh-1212(japan vilene company,ltd,日本,whc=4mg/cm2),为非织造织物材料。这种材料通过热粘结两种材料(白色聚酯纤维聚集体和透明聚酯膜)(12微米)来制造,以制造固结的片材。
[0133]
实施例1
[0134]
药物贴片制剂
[0135]
根据以下方法制备以下实施例1至实施例3的药物贴片。
[0136]
根据以下方法制备贴片。首先,使用冲模形成预定尺寸的背衬层材料。例如,25
×
25mm2。然后,使用冲模将基质材料(例如非织造织物)形成预定尺寸,例如10
×
10mm2。将形成的基质材料固定到背衬层材料的中心部分(在下文中称为空白贴片)。然后,称量添加剂(例如,ca、aa、suc)和药物。然后将溶液添加至添加剂和药物中。使用的溶液是去离子水或醇。然后,搅拌溶液直至添加剂和药物完全溶解,从而制备药物溶液。使用机械移液管将所需的药物溶液滴到空白贴片的基质材料区域上。将基质材料在例如60℃的烘箱中干燥20至50分钟以形成贴片结构。在贴片结构上涂覆离型涂层,例如离型内衬。通过用热封机密封,将完成的贴片与干燥剂一起制成小袋或不与干燥剂一起制成小袋。
[0137]
动物实验:通过微穿孔的透皮递送
[0138]
将77至84天大的无毛豚鼠用作实验动物。将药物贴片固定在已经在期望的穿孔条件下进行穿孔处理的实验动物的皮肤的侧面。细丝密度主要影响用于在皮肤与贴片之间转移体液和成分的区域。细丝密度是200或400细丝/cm2,并且穿孔能量是约4mj/细丝和约5mj/细丝。通过将贴片应用于1cm2微穿孔的施用部位,在每个测试个体上测试各个药物贴片。在固定贴片的时期期间,并且在贴片粘附之后,在所需时间收集血液,根据常规方法提取每种药物组分。然后,通过高效液相色谱(lc-ms/ms)定量血液浓度。表1至表3给出的生物利用度是针对皮下注射的相对生物利用度。
[0139]
皮肤刺激分数标准
[0140]
在去除贴片后进行皮肤刺激检查。皮肤刺激检查量表是对基质正下方的皮肤的评估。皮肤刺激检查量表示于表1。
[0141]
表1
[0142][0143][0144]
该实施例描述了皮肤刺激减弱剂和微穿孔条件对曲坦诱导的皮肤刺激的影响。表2概述了结果。
[0145]
表2
[0146][0147]
实施例2
[0148]
该实施例描述了皮肤刺激减弱剂和微穿孔条件对曲坦诱导的皮肤刺激的作用。表3概述了结果。
[0149]
表3
[0150][0151][0152]
实施例3
[0153]
该实施例描述了皮肤刺激减弱剂和微穿孔条件对曲坦诱导的皮肤刺激的作用。表4概述了结果。
[0154]
表4
[0155][0156]
实施例4
[0157]
本实施例描述了无毛大鼠的施用途径研究。在该研究中,在以下条件下测试四组无毛大鼠:(1)第1组(2mg佐米曲坦,口服施用);(2)第2组(2mg佐米曲坦,鼻内施用;(3)第3组(2mg佐米曲坦,静脉注射);以及(4)第4组(2mg佐米曲坦,透皮微穿孔)。图1和表5概述了结果。
[0158]
动物实验:口服施用,第1组
[0159]
将无毛大鼠用作实验动物。在口服施用含有2.0mg佐米曲坦的药物溶液(2.0ml)后,在所需时间收集血液,根据常规方法提取每种药物组分,然后通过高效液相色谱(lc-ms/ms)定量血液浓度。
[0160]
动物实验:鼻内施用,第2组
[0161]
将无毛大鼠用作实验动物。在静脉施用含有2.0mg佐米曲坦的药物溶液(10μl)后,在所需时间收集血液,根据常规方法提取每种药物组分,然后通过高效液相色谱(lc-ms/
ms)定量血液浓度。
[0162]
动物实验:静脉施用,第3组
[0163]
将无毛大鼠用作实验动物。在静脉施用含有2mg佐米曲坦的药物溶液(200μl)后,在所需时间收集血液,根据常规方法提取每种药物组分,然后通过高效液相色谱(lc-ms/ms)定量血液浓度。
[0164]
动物实验:通过微穿孔的透皮递送,第4组
[0165]
将无毛大鼠用作实验动物。将药物贴片固定在已经在所需条件下进行微穿孔处理的实验动物的皮肤的侧面。在本研究中,透皮微穿孔的微穿孔条件为400孔/cm2、5.2mj/细丝。施用部位为1cm2。在固定贴片的时期期间,并且在贴片粘附之后,在所需时间收集血液,根据常规方法提取每种药物组分,然后通过高效液相色谱(lc-ms/ms)定量血液浓度。本研究的贴片制剂为2mg佐米曲坦、蔗糖0.5mg、aa 4mg、1cm2非织造基质(eh-1212,whc=4mg/cm2)。
[0166]
表5给出的生物利用度是针对iv注射的绝对生物利用度。
[0167]
表5
[0168][0169]
实施例5
[0170]
本实施例描述了使用与实施例4中所述相同的方法在豚鼠中进行的施用途径研究。在本研究中,碱是指佐米曲坦。透皮微穿孔的穿孔条件和药物贴片的基质与实施例4的第4组相同。
[0171]
在本研究中,在以下条件下测试五组豚鼠:(1)第1组(10mg碱/4ml,口服途径);(2)第2组(5mg碱/2ml,口服途径);(3)第3组(2mg碱/4ml,口服途径);(4)第4组(2.0mg碱/cm2,透皮微穿孔);以及(5)第5组(2mg/200μl,subq)。图2和表6概述了结果。表6给出的生物利用度是针对皮下注射的相对生物利用度。
[0172]
在进一步的研究中,进行了比较人与无毛豚鼠(hgp)的pk研究。图3概述了结果(headache 2006,46,138-149)。
[0173]
表6
[0174]
组auc(ng/ml*hr)ba(%)cmax(ng/ml)tmax(小时)1138716.29100.4423538.32590.563774.5250.334143984.28640.50
51709100.038780.09
[0175]
实施例6
[0176]
本实施例描述了各种稳定剂和皮肤刺激减弱剂与微穿孔。基质与以上相同。简言之,透皮微穿孔的微穿孔条件如下;孔密度为400孔/cm2,穿孔能量为4mj/细丝,细丝密度为400细丝/cm2。施用部位为1cm2。表7至表11概述了结果。表7描述了使用豚鼠进行微穿孔的柠檬酸量研究。表7至表10给出的生物利用度是针对皮下注射的相对生物利用度。
[0177]
表7
[0178][0179][0180]
表8概述了使用有机酸作为皮肤刺激减弱剂对豚鼠进行微穿孔的研究的结果。
[0181]
表8
[0182][0183]
表9描述了对豚鼠使用稳定剂、蔗糖和微穿孔进行研究的概述结果。
[0184]
表9
[0185][0186][0187]
表10概述了使用佐米曲坦对豚鼠进行微穿孔的研究结果。
[0188]
表10
[0189][0190]
表11概述了使用无毛大鼠的剂量比较研究的结果
[0191]
表11
[0192]
[0193][0194]
表11给定的生物利用度是针对iv注射的绝对生物利用度。
[0195]
实施例7
[0196]
本实施例描述了细丝密度的各种作用。为了研究细丝密度对pk曲线的作用和副作用(由穿孔引起的疼痛和皮肤刺激),进行了这些研究。细丝密度主要影响用于在皮肤与贴片之间转移体液和成分的面积。细丝密度的范围是100细丝/cm2至400细丝/cm2,并且穿孔能量为3mj/细丝至4mj/细丝。详细条件概述在表12中。
[0197]
表12
[0198][0199]
至于pk曲线的结果,100细丝/cm2的密度显示出较低的cmax和较慢的tmax,这意味着该曲线是一种持续释放的形状(参见图4和图5)。这表明100细丝/cm2的密度较慢地将药物递送到体循环中。另一方面,较高的密度导致较高的cmax和较快的tmax。特别地,在测试组中,具有4mj能量的400细丝/cm2的密度显示最高的cmax和最快的tmax。另外,条件的相对ba为约100%。在测试条件下,似乎400细丝/cm2的密度是优异的候选选项,以产生足够的面积来获得用于溶解成分的体液,然后递送曲坦药物。pk数据概述在图6和表13中。
[0200]
表13
[0201][0202][0203]
从副作用的角度来看,100细丝/cm2的密度是对由穿孔引起的疼痛和皮肤刺激而言最温和的条件,这是合理的(图7、图8、图9)。比较200细丝/cm2的密度和400细丝/cm2的密度,没有观察到显著的差异,并且两个条件都不会引起严重的副作用。
[0204]
表13给出的生物利用度是针对sc注射的相对生物利用度。
[0205]
实施例8
[0206]
本实施例描述了加热能量的各种作用。穿孔能量与孔形状有关,例如深度和宽度。在这些动物研究中,如表14中所示,对于400细丝/cm2的密度,使用2至5mj/细丝的穿孔能量。
[0207]
表14
[0208][0209]
作为pk研究的结果,所有评估数据(auc、ba、cmax和tmax)在2至4mj/细丝的范围内显示出几乎成比例的趋势,并且4mj/细丝在任何评估项目中均是最期望的条件(参见图10和图11)。然而,比较4mj/细丝和5mj/细丝,5mj/细丝的pk结果与4mj/细丝的结果几乎相同或甚至稍差于4mj/细丝的结果。这意味着5mj/细丝产生比所需的更大的孔并诱导比2mg剂量制剂所需的更多的体液。换而言之,在2mg剂量制剂的情况下,由5mj/细丝能量诱导的体液中的药物浓度可以低于由4mj/细丝能量诱导的体液中的药物浓度。因此,在5mj/细丝情况下的药物的渗透压和扩散也低于在4mj/细丝情况下的药物的渗透压和扩散。这就是为什么400细丝/cm2的细丝密度与4mj/细丝的穿孔能量是2mg剂型的优异条件。
[0210]
在副作用方面,测试的穿孔能量之间没有显著差异,如图12和图13中所示。虽然较高的能量可能导致稍微更严重的不利影响,但似乎它们的分数在可接受的范围内。
[0211]
简言之,已根据剂量确定合适的穿孔条件。然而,目前细丝密度应高达400细丝/cm2,并且如果不必要的话,设定较低的细丝加热能量更好。对于2mg剂量制剂,在测试条件中,400细丝/cm2的细丝密度和4mj/细丝是最有效的。数据概述在表15中。
[0212]
表15
[0213][0214][0215]
表15给出的生物利用度是针对sc注射的相对生物利用度。
[0216]
实施例9
[0217]
本实施例描述了期望的细丝阵列尺寸的选择。假设在400细丝/cm2的细丝密度和4或5mj/细丝的能量的条件下,剂量高于2mg剂量,则可能需要使细丝阵列尺寸更大。剂量范围为0.5至4mg,细丝阵列尺寸范围为1.0至2.0cm2。表16概述了结果。
[0218]
表16
[0219][0220]
如图14和图15中所述,pk数据表明,当使用4mj/细丝的能量时,对高达4mg剂量,2cm2的细丝阵列尺寸表现了良好的剂量响应。对于4mg剂量,1.5cm2不太有效。这意味着对于400细丝/cm2的密度和4mj/细丝的能量,每1cm2穿孔面积2mg剂量是本研究中最佳的条件。在5mj/细丝的能量的情况下,1.5cm2的细丝阵列尺寸对于4mg剂量可能是足够的。然而,对于4mg剂量,前者条件(400细丝/cm2的密度,4mj/细丝,2cm2)优于后者条件(400细丝/cm2的密度,5mj/细丝,1.5cm2)。
[0221]
关于副作用,更宽的穿孔面积和更高的能量似乎引起稍微更严重的副作用,如图16和图17中所示。特别地,由1.5cm2和2.0cm2穿孔引起的疼痛更大。
[0222]
简言之,当使用400细丝/cm2的密度和4mj/细丝的能量时,每1cm2穿孔面积2mg剂量是本研究中最佳的条件。如果需要比1cm2更宽的穿孔面积和比2mg更高的剂量,则应该考虑由穿孔引起的疼痛。数据概述在表17中。
[0223]
表17
[0224][0225][0226]
*:无法计算平均值。个体结果为2.0、5.0、》7.0、》7.0(n=4)。
[0227]
表17给出的生物利用度是针对sc注射的相对生物利用度。
[0228]
实施例10
[0229]
本实施例描述了用琥珀酸苏马曲坦对无毛大鼠的施用途径研究。在本研究中,在
以下条件下测试四组无毛大鼠:(1)第1组(3mg游离碱api,suc:0.5mg,aa:1mg);(2)第2组(6mg游离碱api,suc:0.5mg,aa:1mg);(3)第3组(9mg游离碱api,suc:0.5mg,aa:1mg);以及(4)第4组(6mg游离碱api/100μl生理盐水)。在这些研究的上下文中,术语“游离碱”是指存在的舒马曲坦游离碱的重量(例如,参考实施例1,使用4.2mg琥珀酸舒马曲坦,其含有3.0mg舒马曲坦游离碱)。另外,例如参考图18,“4.2ss”是指存在4.2mg琥珀酸舒马曲坦。透皮微穿孔的穿孔条件和药物贴片的基质与实施例4的第4组相同。图18和表18概述了结果。
[0230]
表18
[0231][0232]
表18给出的生物利用度是针对sc注射的相对生物利用度。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1