用于提高免疫疗法和疫苗功效的组合物和方法
1.本发明一般地涉及用于提高免疫疗法和疫苗功效的组合物和方法。尤其,本发明涉及通过给药药剂(例如,包含纤维的益生元剂(例如,表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖))(例如,褪黑激素)与免疫疗法或疫苗来提升受试者肠道微生物组的丰富度和多样性。这样的组合物和方法可用于治疗癌症、感染性病原体、自身免疫性疾病、神经疾患和/或肥胖症。
背景技术:
2.癌症免疫疗法正在彻底改变肿瘤学领域。然而,免疫检查点疗法仅适用于一部分患者(通常为10-30%)。非常需要改善免疫检查点阻断的功效。另外,人们对改善疫苗有着广泛的研究兴趣。
3.本发明解决了这些需求。
技术实现要素:
4.在开发本发明的实施方式的期间进行的实验从fda批准的药物或膳食补充剂(例如益生元剂)中鉴定出新的化合物,这些化合物可以被摄入以改善免疫检查点疗法的功效。结果表明,药剂(例如,包含纤维的益生元剂(例如,表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖))(例如,褪黑激素)的口服制剂可以改变肠道微生物组,从而增加有益菌的频率并与通过全身注射给予的免疫检查点阻断剂协同作用。事实上,结果表明,并行给药益生元剂(例如,菊糖)与免疫疗法(例如,α-pd-1疗法)导致更强的抗肿瘤功效、更强的免疫应答(例如,pbmc中的ah1特异性cd8+ t细胞频率)、抑制肿瘤生长、增强t细胞的肿瘤内浸润、脾cd8+ t细胞中更高的ifn-γ表达,以及受试者肠道微生物组内阿克曼菌属(akkermansia)、乳杆菌属(lactobacillus)、瘤胃球菌属(ruminococcus)、罗氏菌属(roseburia)和丁酸球菌属(butyricicoccus)的丰度增加。
5.因此,本发明一般地涉及用于提高免疫疗法和疫苗功效的组合物和方法。尤其,本发明涉及通过给药药剂(例如,包含纤维的益生元剂(例如,表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖))(例如,褪黑激素)与免疫疗法或疫苗来提升受试者肠道微生物组的丰富度和多样性。这样的组合物和方法可用于治疗癌症、感染性病原体、自身免疫性疾病、神经疾患和/或肥胖症。
6.在某些实施方式中,本发明提供了一种用于提高癌症免疫疗法或疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)的功效的方法,所述通过向受试者给药1)癌症免疫疗法或疫苗,以及2)给药能够提升所述受试者肠道微生物组的丰富度和多样性的药剂。
7.在某些实施方式中,本发明提供了一种用于抑制癌症细胞诱导免疫功能障碍的能力的方法,所述方法包括向受试者给药1)癌症免疫疗法或癌症疫苗,以及2)给药能够提升所述受试者肠道微生物组的丰富度和多样性的药剂。
8.在某些实施方式中,本发明提供了一种用于治疗或预防受试者中的癌症的方法,
所述方法包括向所述受试者给药1)对于受试者的癌症免疫疗法或癌症疫苗,以及2)能够提升所述受试者肠道微生物组的丰富度和多样性的药剂。
9.这样的方法不限于以下项的特定给药方式:1)向受试者给药癌症免疫疗法或疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗),以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。在一些实施方式中,给药所述能够提升所述受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗(例如癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法之前、并行和/或之后发生。在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂与给药所述疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法并行发生。在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法之前发生。在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法之前和并行发生。
10.这样的方法不限于特定类型的受试者。在一些实施方式中,所述受试者是人受试者。
11.这样的方法不限于能够提升受试者肠道微生物组的丰富度和多样性的药剂的特定类型或种类。在一些实施方式中,所述药剂是包含纤维的益生元剂。在一些实施方式中,所述包含纤维的益生元剂选自表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖。
12.在一些实施方式中,所述药剂是菊糖。菊糖是属于果聚糖组的多糖。它由β-2-1连接的果糖分子链组成,该链在其末端在还原端具有α-d-葡萄糖单元。菊糖以经济可回收的量存在于各种植物诸如例如菊苣根和大丽花块茎中。另外,菊糖已在例如菊芋和朝鲜蓟中发现。各种菊糖的平均链长及其物理化学特性因植物物种而异。在一些实施方式中,所述药剂是基于凝胶的菊糖制剂。在一些实施方式中,所述药剂是基于凝胶的菊糖制剂,所述基于凝胶的菊糖制剂具有的平均聚合度为20或高于20至47或小于47。在一些实施方式中,所述药剂是基于凝胶的菊糖制剂,所述基于凝胶的菊糖制剂具有的平均聚合度为大约28(例如,23、24、25、26、27、28、29、30、31、32、33)(参见实施例xiii,示出具有平均聚合度为大约28的基于凝胶的菊糖制剂的出人意料的抗肿瘤功效)。
13.在一些实施方式中,所述基于凝胶的菊糖制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。在一些实施方式中,所述药剂是褪黑激素。
14.这样的方法不限于特定类型或种类的癌症免疫疗法。在一些实施方式中,所述癌症免疫疗法包括一种或多种免疫检查点抑制剂(ici)抑制剂。在一些实施方式中,所述一种或多种ici抑制剂能够结合、阻断和/或抑制以下项的一种或多种的活性:ctla-4、pdl1、pdl2、pd1、btla、hvem、tim3、gal9、lag3、vista、kir、2b4、cd160和cgen-15049。在一些实施方式中,所述一种或多种ici抑制剂选自曲美木单抗(tremelimumab,ctla-4封闭抗体)、抗ox40、pd-l1单克隆抗体(抗b7-h1;medi4736)、mk-3475(pd-1阻断剂)、纳武利尤单抗
(nivolumab,抗pd1抗体)、ct-011(抗pd1抗体)、by55单克隆抗体、amp224(抗pdl1抗体)、bms-936559(抗pdl1抗体)、mpldl3280a(抗pdl1抗体)、msb0010718c(抗pdl1抗体)和伊匹单抗(yervoy)/伊匹木单抗(ipilimumab,抗ctla-4检查点抑制剂)。
15.这样的方法不限于特定类型或种类的癌症。在一些实施方式中,所述癌症是对癌症免疫疗法或癌症疫苗治疗有反应的任何类型的癌症。在一些实施方式中,所述癌症是以下中的一种或多种:乳腺癌、卵巢癌、前列腺癌、肺癌、肾癌、胃癌、结肠癌、睾丸癌、头颈癌、胰腺癌、脑癌、黑素瘤以及其他组织器官肿瘤和血液肿瘤,例如淋巴瘤和白血病,包括急性髓细胞性白血病、慢性髓细胞性白血病、慢性淋巴细胞性白血病、t细胞淋巴细胞性白血病和b细胞淋巴瘤。
16.在一些实施方式中,这样的方法进一步包括向所述受试者给药一种或多种化疗剂,所述化疗剂选自由以下组成的组:烷化剂、抗代谢物、蒽环素、抗肿瘤抗生素、单克隆抗体、铂剂、植物生物碱、拓扑异构酶抑制剂、长春花生物碱、紫杉烷和表鬼臼毒素。
17.这样的方法不限于给药能够提升受试者肠道微生物组的丰富度和多样性的药剂的特定方式。在一些实施方式中,所述药剂是口服给药。在一些实施方式中,所述药剂通过口服灌胃给药。
18.在对于这样的方法的一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂导致所述受试者肠道微生物组内阿克曼菌属、乳杆菌属、瘤胃球菌属、罗氏菌属和丁酸球菌属的相对丰度增加。
19.在对于这样的的方法的一些实施方式中,向受试者给药1)癌症免疫疗法或疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗),以及2)给药能够提升所述受试者肠道微生物组的丰富度和多样性的药剂,导致以下项的一种或多种:癌症免疫疗法或疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)的增加的抗肿瘤功效,更强的免疫应答(例如,pbmc中增加的抗肿瘤t细胞频率)以及增强的肿瘤生长抑制。
20.在某些实施方式中,本发明提供了包括基于凝胶的菊糖制剂的组合物。在一些实施方式中,所述基于凝胶的菊糖制剂具有的平均聚合度为20或高于20至47或小于47。在一些实施方式中,所述基于凝胶的菊糖制剂具有的平均聚合度为大约28(例如,23、24、25、26、27、28、29、30、31、32、33)。
21.在一些实施方式中,所述基于凝胶的菊糖制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
22.在某些实施方式中,本发明提供了一种用于治疗或预防以肠道微生物组活性失调为特征的病症的方法,所述方法包括向所述受试者给药能够提升所述受试者肠道微生物组的丰富度和多样性的药剂。
23.在一些实施方式中,所述受试者是人受试者。
24.在一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂是包含纤维的益生元剂。在一些实施方式中,所述包含纤维的益生元剂选自表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖。在一些实施方式中,所述包
含纤维的益生元剂是基于凝胶的菊糖制剂。在一些实施方式中,所述基于凝胶的菊糖制剂具有的平均聚合度为20或高于20至47或小于47。在一些实施方式中,所述基于凝胶的菊糖制剂具有的平均聚合度为大约28(例如,23、24、25、26、27、28、29、30、31、32、33)。在一些实施方式中,所述基于凝胶的菊糖制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。在一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂是褪黑激素。
25.在一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂是口服给药。
26.在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂导致所述受试者肠道微生物组内阿克曼菌属、乳杆菌属、瘤胃球菌属、罗氏菌属和丁酸球菌属的相对丰度增加。
27.在一些实施方式中,所述以肠道微生物组活性失调为特征的病症是自身免疫性疾病、神经疾患、糖尿病和/或肥胖症。
28.在一些实施方式中,所述以肠道微生物组活性失调为特征的病症选自类风湿性关节炎、多发性硬化糖尿病(例如,1型糖尿病)、甲状腺自身免疫性疾病(例如,桥本甲状腺炎、格雷夫斯病)、甲状腺相关性眼病和皮肤病、甲状旁腺功能减退症、艾迪生病、卵巢早衰、自身免疫性垂体炎、垂体自身免疫性疾病、免疫性胃炎(immunogastritis)、恶性贫血(pernicious angemis)、乳糜泻、白癜风、重症肌无力、寻常型天疱疮和变体、大疱性类天疱疮、疱疹样皮炎、获得性大疱性表皮松解症、系统性硬化病、混合性结缔组织病、干燥综合征、系统性红斑狼疮、肺出血肾炎综合征、风湿性心脏病、自身免疫性多内分泌腺综合征1型、aicardi-gouti
è
res综合征、急性胰腺炎、年龄相关性黄斑变性、酒精性肝病、肝纤维化、转移、心肌梗死、非酒精性脂肪肝炎(nash)、帕金森病、多关节炎/胎儿和新生儿贫血、脓毒症和炎性肠病。
29.在一些实施方式中,所述方法进一步包括向所述受试者给药以下额外的治疗剂的一种或多种:改善疾病的抗风湿药物(例如,来氟米特(leflunomide)、甲氨蝶呤(methotrexate)、柳氮磺胺吡啶(sulfasalazine)、羟氯喹(hydroxychloroquine))、生物剂(例如,利妥昔单抗(rituximab)、英利昔单抗(infliximab)、依那西普(etanercept)、阿达木单抗(adalimumab)、戈利木单抗(golimumab))、非甾体抗炎药物(例如,布洛芬(ibuprofen)、塞来昔布(celecoxib)、酮洛芬(ketoprofen)、萘普生(naproxen)、吡罗昔康(piroxicam)、双氯芬酸(diclofenac))、镇痛剂(例如,对乙酰氨基酚、曲马多(tramadol))、免疫调节剂(例如,阿那白滞素(anakinra)、阿巴西普(abatacept))、糖皮质激素(例如,泼尼松(prednisone)、甲泼尼松(methylprednisone))、tnf-α抑制剂(例如,阿达木单抗、培化舍单抗(certolizumab pegol)、依那西普、戈利木单抗、英利昔单抗)、il-1抑制剂和金属蛋白酶抑制剂。在一些实施方式中,治疗剂包括但不限于英利昔单抗、阿达木单抗、依那西普、肠胃外金或口服金。
30.在某些实施方式中,本发明提供了一种用于提高疫苗功效的方法,所述方法通过向受试者给药1)疫苗,以及2)给药能够提升所述受试者肠道微生物组的丰富度和多样性的
药剂。
31.在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗之前、并行和/或之后发生。
32.在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂与给药所述疫苗并行发生;或者给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗之前发生。在一些实施方式中,其中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗之前和并行发生。
33.在一些实施方式中,所述疫苗是用于治疗癌症的疫苗,和/或用于治疗和/或保护免受感染性病原体的疫苗。
34.在一些实施方式中,所述受试者是人受试者。
35.在一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂是包含纤维的益生元剂。在一些实施方式中,所述包含纤维的益生元剂选自表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖。在一些实施方式中,所述包含纤维的益生元剂是基于凝胶的菊糖制剂。在一些实施方式中,所述基于凝胶的菊糖制剂具有的平均聚合度为20或高于20至47或小于47。在一些实施方式中,所述基于凝胶的菊糖制剂具有的平均聚合度为大约28(例如,23、24、25、26、27、28、29、30、31、32、33)。在一些实施方式中,所述基于凝胶的菊糖制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。在一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂是褪黑激素。
36.在一些实施方式中,所述能够提升受试者肠道微生物组的丰富度和多样性的药剂是口服给药。
37.在一些实施方式中,给药所述能够提升受试者肠道微生物组的丰富度和多样性的药剂导致所述受试者肠道微生物组内阿克曼菌属、乳杆菌属、瘤胃球菌属、罗氏菌属和丁酸球菌属的相对丰度增加。
38.本发明还提供了试剂盒,所述试剂盒包括能够提升受试者肠道微生物组的丰富度和多样性的药剂(例如,基于纤维的益生元),以及疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)和癌症免疫疗法(例如,ici抑制剂)的一种或多种。试剂盒可以任选地包含其他治疗剂。
39.在某些实施方式中,本发明提供了包括与细菌结合的(例如,复合的、缀合的、包封的、吸收的、吸附的、混合的)益生元制剂的组合物。
40.在一些实施方式中,所述益生元制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、菊糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
41.在一些实施方式中,所述益生元化合物是基于凝胶的。在一些实施方式中,所述益生元化合物是基于凝胶的菊糖。
42.在一些实施方式中,所述细菌是大肠杆菌(e.coli)。在一些实施方式中,所述细菌
在向受试者给药后能够改变受试者的肠道微生物组。
43.在一些实施方式中,所述组合物被配置用于向受试者口服给药。
44.在某些实施方式中,本发明提供了用于将细菌结肠递送至受试者的方法,包括向受试者给药这样的包括与细菌结合的(例如,复合的、缀合的、包封的、吸收的、吸附的、混合的)益生元制剂(例如,基于凝胶的菊糖)。
45.在某些实施方式中,本发明提供了包括与一种或多种益生菌细胞结合的(例如,复合的、缀合的、包封的、吸收的、吸附的、混合的)益生元制剂的组合物。在某些实施方式中,本发明提供了用于提高受试者消化系统中益生菌生物生长的方法,包括向受试者(例如哺乳动物受试者;人受试者)给药这样的组合物。
46.在一些实施方式中,所述益生元制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、菊糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
47.在一些实施方式中,所述益生元化合物是基于凝胶的。在一些实施方式中,所述益生元化合物是基于凝胶的菊糖。
48.在一些实施方式中,所述一种或多种益生菌细胞在向受试者给药后能够改变所述受试者的肠道微生物组。
49.在一些实施方式中,所述组合物被配置用于向受试者口服给药。
50.在一些实施方式中,所述一种或多种益生菌细胞包括有益菌。在一些实施方式中,所述有益菌包括以下项的一种或多种:酿酒酵母(saccharomyces cereviseae)、凝结芽孢杆菌(bacillus coagulans)、地衣芽孢杆菌(bacillus licheniformis)、枯草芽孢杆菌(bacillus subtilis)、角双歧杆菌(bifidobacterium angulatum)、动物双歧杆菌(bifidobacterium animalis)、两歧双歧杆菌(bifidobacterium bifidum)、短双歧杆菌(bifidobacterium breve)、婴儿双歧杆菌(bifidobacterium infantis)、乳酸双歧杆菌(bifidobacterium lactis)、长双歧杆菌(bifidobacterium longum)、屎肠球菌(enterococcus faecium)、粪肠球菌(enterococcus faecalis)、嗜酸乳杆菌(lactobacillus acidophilus)、食淀粉乳杆菌(lactobacillus amylovorus)、消化乳杆菌(lactobacillus alimentarius)、保加利亚乳杆菌(lactobacillus bulgaricus)、干酪乳杆菌干酪亚种(lactobacillus casei subsp.casei)、干酪乳杆菌代田株(lactobacillus casei shirota)、弯曲乳杆菌(lactobacillus curvatus)、德氏乳杆菌乳酸亚种(lactobacillus delbrueckii subsp.lactis)、发酵乳杆菌(lactobacillus fermentum)、香肠乳杆菌(lactobacillus farciminus)、格氏乳杆菌(lactobacillus gasseri)、瑞士乳杆菌(lactobacillus helveticus)、约氏乳杆菌(lactobacillus johnsonii)、乳酸乳杆菌(lactobacillus lacti)、副干酪乳杆菌(lactobacillus paracasei)、戊糖乳杆菌(lactobacillus pentosaceus)、植物乳杆菌(lactobacillus plantarum)、罗伊氏乳杆菌(lactobacillus reuteri)、鼠李糖乳杆菌(lactobacillus rhamnosus)(乳杆菌gg)、清酒乳杆菌(lactobacillus sake)、唾液乳杆菌(lactobacillus salivarius)、乳酸乳球菌(lactococcus lactis)、耐热乳杆菌(lactobacillus thermotolerans)、黏膜乳杆菌(lactobacillus mucosae)、变异微球菌(micrococcus varians)、乳酸片球菌
(pediococcus acidilactici)、戊糖片球菌(pediococcus pentosaceus)、乳酸片球菌、嗜盐片球菌(pediococcus halophilus)、粪链球菌(streptococcus faecalis)、嗜热链球菌(streptococcus thermophilus)、肉糖葡萄球菌(staphylococcus carnosus)和木糖葡萄球菌(staphylococcus xylosus)。
51.在一些实施方式中,所述组合物是糖包衣片剂、凝胶胶囊、凝胶、乳剂、片剂、扁胶囊、水凝胶、纳米纤维凝胶、电纺纤维、食品棒、糖果点心、发酵乳、发酵乳酪、口香糖、粉末或牙膏。
52.在某些实施方式中,本发明提供了包括基于凝胶的益生元制剂的组合物。在一些实施方式中,所述组合物被配置用于口服摄取。在一些实施方式中,所述组合物是糖包衣片剂、凝胶胶囊、凝胶、乳剂、片剂、扁胶囊、水凝胶、纳米纤维凝胶、电纺纤维、食品棒、糖果点心、发酵乳、发酵乳酪、口香糖、粉末或牙膏。
53.在一些实施方式中,所述益生元制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、菊糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
54.在一些实施方式中,所述基于凝胶的益生元制剂与一种或多种益生菌生物结合。在一些实施方式中,所述一种或多种益生菌生物选自乳杆菌属物种和双歧杆菌属物种。在一些实施方式中,所述基于凝胶的益生元制剂与一种或多种噬菌体结合,所述一种或多种噬菌体特异性于:鲍特菌(bordetella)、疏螺旋体(borrelia)、布鲁氏菌(brucella)、弯曲杆菌(campylobacter)、衣原体(chlamydia)和嗜衣体属(chlamydophila)、梭菌(clostridium)、棒状杆菌(corynebacterium)、肠球菌(enterococcus)、埃希菌(escherichia)、弗朗西丝菌(francisella)、嗜血杆菌(haemophilus)、螺杆菌(helicobacter)、军团菌(legionella)、钩端螺旋体(leptospira)、李斯特菌(listeria)、分枝杆菌(mycobacterium)、支原体(mycoplasma)、奈瑟菌(neisseria)、假单胞菌(pseudomonas)、立克次体(rickettsia)、沙门菌(salmonella)、志贺菌(shigella)、葡萄球菌(staphylococcus)、链球菌(streptococcus)、密螺旋体(treponema)、弧菌(vibrio)和耶尔森菌(yersinia)。在一些实施方式中,所述一种或多种益生菌生物选自嗜酸乳杆菌、食淀粉乳杆菌、短乳杆菌、干酪乳杆菌(l.casei)、干酪乳杆菌鼠李糖亚种(l.casei subsp.rhamnosus)(乳杆菌gg)、高加索乳杆菌(l.caucasicus)、卷曲乳杆菌(l.crispatus)、德氏乳杆菌保加利亚亚种(l.delbrueckii subsp.bulgaricus)(保加利亚乳杆菌(l.bulgaricus))、发酵乳杆菌(酶乳杆菌(l.fermenti))、格氏乳杆菌、瑞士乳杆菌、约氏乳杆菌、乳酸乳杆菌、莱希曼氏乳杆菌、副干酪乳杆菌、植物乳杆菌、罗伊氏乳杆菌或鼠李糖乳杆菌。
附图说明
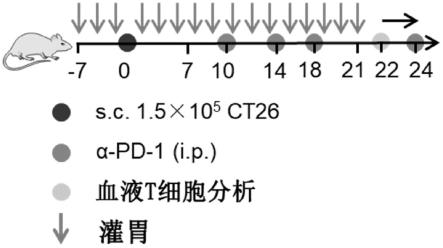
55.图1a-f:候选材料的体内筛选以预防性地改善α-pd-1的抗肿瘤功效。(a)在第-7天对小鼠预防性灌胃各种样品3次。然后在第0天将1.5
×
105个ct26细胞皮下(s.c.)接种到balb/c小鼠中。在肿瘤接种后的第一周再次灌胃小鼠3次,并且从第7天起每周灌胃5次。在第10、14、18和24天以100μg/剂量i.p.注射α-pd-1。用各种化合物灌胃的小鼠的(b)个体肿
瘤生长曲线和(c)平均肿瘤生长曲线。(d)各组的存活率曲线。(e)第22天外周血中ah1特异性cd8
+ t细胞的平均频率。(f)经由流式细胞术测量代表性散点图。数据代表平均值
±
sem。
*
p《0.05,
**
p《0.01,通过双因素anova(b)或t检验(e)、对数秩(mantel-cox)检验(d)进行分析。
56.图2a-g:候选材料的体内筛选以改善α-pd-1的抗肿瘤功效。(a)在第0天将1.5
×
105个ct26细胞皮下(sc)接种到balb/c小鼠中。从第7天灌胃小鼠(每周5次)。在第11、15、19和23天,以每剂100μg腹腔内(ip)注射α-pd-1。(b)用各种化合物灌胃的小鼠的平均肿瘤生长曲线。数据代表平均值
±
sem。各组的(c)个体肿瘤生长曲线和(d)存活率曲线。在第18天和第24天,采集外周血。在(e)第18天、(f)第24天的ah1特异性cd8
+ t细胞的平均频率以及(g)经由流式细胞术测量代表性散点图。数据代表平均值
±
sd。所有数据均来自2-3次独立实验;n=10(b、c、d),n=7-10(e、f)
*
p《0.05,
**
p《0.01,通过双因素anova(b)、单因素anova(e、f)或对数秩(mantel-cox)检验进行分析。
57.图3a-h:褪黑激素和菊糖与α-pd-1联合的剂量效应的体内评估。在第0天将1.5
×
105个ct26细胞s.c.接种到balb/c小鼠中。从第7天灌胃小鼠(每周5次)。在第11、15、19和23天,以每剂100μg i.p.注射α-pd-1。用不同剂量的(a)褪黑激素和(b)菊糖灌胃的小鼠的平均肿瘤生长曲线。用不同剂量的(c)褪黑激素和(d)菊糖治疗后第18天ah1特异性cd8
+ t细胞的平均频率。第24天,用不同剂量的(e)褪黑激素和(f)菊糖治疗后整个肿瘤组织中cd45
+
cd8
+ t细胞的百分比。第24天,用不同剂量的(g)褪黑激素和(h)菊糖治疗后所有细胞中cd45
+
cd4
+ t细胞的百分比。数据代表平均值
±
sem(n=5)。
*
p《0.05,
**
p《0.01,
***
p《0.001,通过双因素anova(a,b)或双尾非配对t检验(d)、单因素anova(e、f、g、h)进行分析。
58.图4a-h:肠道微生物区系的多样性、丰富度和结构的响应。将1.5
×
105个ct26细胞皮下接种到balb/c小鼠中,并从第7天灌胃(每周5次)。在第11、15、19和23天ip注射α-pd-1(每剂100μg)。在第21天收集粪便团粒用于16s rna分析。各组中肠道微生物区系的(a)otu数、(b)逆辛普森多样性和(c)非度量多维标度(nmds)评分图(基于bray-curtis)。(d)科水平和(i)属水平的肠道微生物区系的相对丰度。(f)各组中乳杆菌属、阿克曼菌属、罗氏菌属和瘤胃球菌属_1的相对丰度。(g)肿瘤大小与乳杆菌属、阿克曼菌属、罗氏菌属和瘤胃球菌属_1相对丰度的关系。(h)粪便团粒中各组的scfa(乳酸、丙酸和丁酸)水平的热图。数据代表平均值
±
sem。
*
p《0.05,
**
p《0.01,
****
p《0.0001,通过单因素anova(a、b、f)进行分析。
59.图5a-c:肠道微生物区系分析。将1.5
×
105个ct26细胞皮下接种到balb/c小鼠中,并从第7天灌胃(每周5次)。在第11、15、19和23天ip注射α-pd-1(每剂100μg)。在第21天收集粪便团粒用于16s rna分析。各组中肠道微生物区系的(a)otu数、(b)nmds评分图。(c)属水平的肠道微生物区系的相对丰度。数据代表平均值
±
sem。
60.图6a-i:菊糖凝胶进一步增强α-pd-1的治疗功效。(a)菊糖凝胶图像和sem图像。(b)用菊糖或菊糖凝胶(60mg/剂量)灌胃的小鼠的平均肿瘤生长曲线和个体肿瘤生长曲线。将1.5
×
105个ct26细胞皮下接种到balb/c小鼠中。从第7天开始灌胃(每周5次),并且在第11、15、19、23和27天ip注射100μg的α-pd-1。(c)各组的存活率曲线。(d)向在菊糖凝胶联合α-pd-1组中的肿瘤根除小鼠注射1.5
×
105个ct26细胞并监测肿瘤大小。使用pbs作为对照。(e)第23天ah1特异性cd8
+ t细胞的平均频率和代表性散点图。(f)肿瘤微环境分析:以下项的百分比:整个肿瘤中的cd45
+
cd8
+ t细胞;dapi-cd45
+
cd8
+ t细胞中的ah1-四聚物阳性;整
个肿瘤中的成熟dc细胞(dapi-cd45
+
细胞中的cd11c
+
cd86
+ t细胞)和cd45
+
cd4
+ t细胞。(g、h)在第23天,获得脾用于ifn-γelispot测试。(i)在第8、11和16天,将ct26荷瘤balb/c小鼠注射200μg的靶向cd8
+
t细胞(αcd8)、cd4
+ t细胞(αcd4)和nk细胞(αasialo gm1)的抗体。α-pd-1注射以及样品灌胃采用上述相同的方案。示出了荷瘤小鼠的平均和个体肿瘤生长曲线。使用igg抗体作为对照组。数据代表平均值
±
sem。所有数据均来自2-3次独立实验;n=10(b,c),n=5(d,i),n=10-15(e),n=4-7(g,f),
*
p《0.05,
**
p《0.01,
***
p《0.001,通过单因素anova(e、f)、双因素anova(b、i)或对数秩(mantel-cox)检验(c)进行分析。
61.图7a-b:(a)将菊糖凝胶通过注射器(1ml)注入di水中。菊糖凝胶的图像示出在水中的稳定性。(b)当将菊糖凝胶在强酸性环境(ph 2)下分别孵育2和24h时,菊糖凝胶的稳定性。在探针处使用dns试剂并测量吸光度以验证还原糖的含量。将未经酸处理的菊糖凝胶用作标准,并且将菊糖用作对照。
62.图8a-i:菊糖凝胶表现出延长的结肠保留。(a)不同时间点菊糖凝胶的肠道保留的ivis成像(白框表示结肠区域)和(b)结肠区域相应的平均荧光强度。菊糖用fitc标记。(c)灌胃后不同时间点粪便团粒中菊糖-fitc的荧光强度。(d)通过商业菊糖试剂盒测定的结肠消化物中的菊糖含量。箭头表示菊糖的曲线下面积(auc)值。在第21天收集粪便团粒并进行16s rna分析。(e)各组中肠道微生物区系的otu数、逆辛普森多样性和(f)nmds评分图(基于bray-curtis)。(g)肠道微生物区系属水平和(h)的相对丰度。(i)将幼稚小鼠饲喂广谱抗生素(氨苄青霉素+黏菌素+链霉素)一周。然后将1.5
×
105个ct26细胞皮下接种到balb/c小鼠中,饲喂小鼠正常饮水5天,随后持续给予广谱抗生素治疗。α-pd-1注射以及样品灌胃采用上述相同的方案。示出了平均肿瘤生长曲线。数据代表平均值
±
sem。数据来自2-3个独立实验(a-d);
*
p《0.05,
**
p《0.01,
***
p《0.001,
****
p《0.0001,通过单因素anova(c、e、h)或双因素anova(i)进行分析
63.图9a-e:(a)在c57bl/6小鼠上建立mc38肿瘤模型并接受α-pd-1注射和样品灌胃。(b)在第20天,获得pbmc用于ifn-γelispot测定。各组的(d)存活率曲线和(e)平均和个体肿瘤生长曲线。数据代表平均值
±
sem。
*
p《0.05,
**
p《0.01,
***
p《0.001,
****
p《0.0001,通过单因素anova(a、b、g)进行分析。
64.图10a-c:菊糖凝胶与α-pd-1联合的生物安全性研究。(a)包括以下项的全血细胞计数图:嗜酸性粒细胞、淋巴细胞、单核细胞、血小板计数、红细胞计数、rdw、血红蛋白、mch和平均血小板体积。(b)包括以下项的生化图:alp、alt、ast、bun、cpk、总蛋白、胆固醇和葡萄糖。(c)第29天,菊糖凝胶与α-pd-1联合治疗后心脏、肝脏、脾、肺、肾脏的h&e染色。
65.图11:大肠杆菌生长曲线和gfp表达。将大肠杆菌培养在250ml锥形瓶中。以不同的时间间隔对培养物进行采样。测量od
600
和相对荧光强度。
66.图12:分别在pbs中孵育和菊糖凝胶包封24小时后通过荧光强度测定的细胞生存力。
67.图13a-e:验证菊糖凝胶加α-pd-1联合疗法在其他模型中的抗肿瘤功效。(a)来自塔科尼农场(taconic farm)或查理士河(charles river)的ct26荷瘤balb/c小鼠的治疗方案。示出了来自(b)塔科尼农场或(c)查理士河的balb/c小鼠中的肿瘤生长。d-e)将具有(d)mc-38结肠癌和(e)b16f10黑素瘤的c57bl/6小鼠按所示进行治疗(菊糖:60mg/剂),并监测肿瘤生长。
68.图14:各种菊糖样品的1h nmr谱。
69.图15:菊糖样品的maldi-tof质谱。
70.图16:菊糖浓度和平均dp对菊糖凝胶形成的影响。使用不同dp的菊糖形成各种菊糖凝胶制剂。将平均dp为7、10、23、26和28的菊糖以不同浓度溶解在水中。在经由加热和冷却诱导凝胶化后,在高菊糖浓度和高dp下观察菊糖凝胶形成。
71.图17:通过频率扫描测量用不同的平均dp形成的菊糖凝胶制剂的凝胶流变性。g'代表弹性模量,g”代表粘性模量。菊糖凝胶样品#1具有平均dp≈7。菊糖凝胶样品#3具有平均dp≈23。菊糖凝胶样品#5具有平均dp≈28。
72.图18:用具有不同平均dp的菊糖凝胶口服灌胃幼稚小鼠,并随时间测定粪便样品中的菊糖含量。数据示出平均值
±
sem。
73.图19:使用用各种dp形成的菊糖凝胶的口服灌胃(60mg/剂)加α-pd-1的腹腔给药(100ug/剂)对具有s.c.侧腹ct26肿瘤的balb/c小鼠进行治疗。监测动物的肿瘤生长。数据示出平均值
±
sem。
74.图20:使用用各种dp形成的菊糖凝胶的口服灌胃(60mg/剂)加α-pd-1的腹腔给药(100ug/剂)对具有s.c.侧腹ct26肿瘤的balb/c小鼠进行治疗。监测动物的体重变化。数据示出平均值
±
sem。
75.图21:菊糖凝胶形成的浓度和温度依赖性。将具有dp 23的菊糖与水混合,得到15、20、25和30%w/v的期望浓度。将混合物分别加热至40、50、60、70℃,保持5分钟,随后冷却。检查凝胶形成。
76.图22:将食品级马铃薯淀粉在水中以0.1、0.5、2.5和5%w/v的浓度预水合,随后在70℃温和搅拌。冷却后,检查凝胶形成。
77.图23:新型纤维凝胶的凝胶化过程。#1菊糖凝胶,#2包含抗性马铃薯淀粉的菊糖凝胶,#3包含瓜尔胶的菊糖凝胶,#4包含果胶的菊糖凝胶,和#5包含豆胶的菊糖凝胶。首先将这些成分在水中混合(上图),在70℃加热5分钟(中图),随后在室温下冷却过夜,从而形成纤维凝胶(下图)。
78.图24:加入不同量的天然纤维或赋形剂后形成菊糖凝胶。示出的值是可以添加到23%w/w菊糖凝胶而不破坏凝胶形成的每种成分的最大量。
79.图25:不同纤维凝胶制剂的凝胶流变性。通过频率扫描测量的粘弹性(左)和粘度的流动曲线(右)。
80.定义
81.为了促进对本公开的原理的理解,现在将参考优选实施方式并且将使用特定语言对其进行描述。然而,应当理解,并不旨在限制本公开的范围,如本文所示的本公开的这种改变和进一步修改,是如本公开所涉及的本领域技术人员通常会想到的。
82.如本文所用,冠词“一个(a)”和“一种(an)”是指冠词的一个或多于一个(即至少一个)语法对象。例如,“元素”意指至少一个元素并且可以包括多于一个元素。
[0083]“约”用于通过提供给定值可能“略高于”或“略低于”端点而不影响期望结果来为数值范围端点提供灵活性。
[0084]
本文所用的术语“包括(including)”、“包括(comprising)”或“具有”及其变体意指涵括其后列出的元素及其等同物以及额外的元素。列举为“包括(including)”、“包括
(comprising)/*”或“具有”某些元素的实施方式也被考虑为“基本上由那些某些元素组成”和“由那些某些元素组成”。
[0085]
除非在本文中另有说明,否则本文中数值范围的列举仅旨在用作单独引用落入该范围内的每个单独值的简略表达方式的方法,并且每个单独的值被并入说明书中,就如它在本文中单独列举一样。例如,如果将浓度范围规定为1%至50%,则旨在本说明书中明确列举了诸如2%至40%、10%至30%或1%至3%等值。这些仅仅是具体意图的实例,并且在所列举的最低值和最高值之间并且包括所列举的最低值和最高值的数值的所有可能的组合将被视为在本公开中明确表达。
[0086]
与“包括(including)”、“包含”或“特征在于
……”
同义的过渡性术语“包括(comprising)”是包括性的或开放式的,并且不排除额外的、未列举的元素或方法步骤。相比之下,过渡性短语“由
……
组成”排除了权利要求中未指定的任何元素、步骤或成分。过渡性短语“基本上由
……
组成”将权利要求的范围限制为特定的材料或步骤“以及不会实质影响要求保护的发明的基本和一个或多个新颖特征的那些”。
[0087]
如本文所用,术语“免疫检查点抑制剂”(ici)、“检查点抑制剂”等是指抑制免疫系统控制机制活性的化合物。免疫系统检查点或免疫检查点是免疫系统中的抑制途径,通常用于维持自身耐受性或调节生理免疫应答的持续时间和幅度,以最小化附带组织损伤。ici可以通过抑制通路中蛋白的活性来抑制免疫系统检查点。ici蛋白包括但不限于cd80、cd28、cd86、细胞毒性t淋巴细胞相关蛋白4(ctla-4)、pd-l1、pd-l2、pd-1、可诱导t细胞共刺激物的配体(l-icos)、可诱导t细胞共刺激物(icos)、cd276和包含v-set结构域的t细胞活化抑制剂1(vtcn1)。因此,ici抑制剂包括例如ici诸如ctla4、pd1或pd-l1的拮抗剂。例如,与ctla4、pd-1或pd-l1结合并拮抗其功能的抗体是ici抑制剂。此外,抑制ici的抑制功能的任何分子(例如肽、核酸、小分子等)都是ici抑制剂。
[0088]“受试者”可以是脊椎动物、哺乳动物或人。哺乳动物包括但不限于农场动物、运动动物、宠物、灵长类动物、小鼠和大鼠。在一个方面,受试者是人。
[0089]
除非另有定义,否则本文所用的所有技术术语与本公开所属领域的普通技术人员通常理解的含义相同。
具体实施方式
[0090]
新兴研究表明,肠道微生物组在调节免疫应答中起着至关重要的作用。事实上,已经有人努力使用粪便微生物区系转移或益生菌来促进免疫检查点阻断的功效。
[0091]
免疫检查点疗法靶向t细胞中的调节途径以增强抗肿瘤免疫应答,已导致重要的临床进展,并提供了对抗癌症的新武器。这种疗法引起了持久的临床应答,并且在一小部分患者中引起了长期缓解,其中患者多年来没有表现出癌症的临床症状。
[0092]
已知许多的这些免疫检查点,诸如ctla-4(细胞毒性t淋巴细胞抗原4)和pd-1(程序性死亡1)阻止t细胞攻击肿瘤细胞。已知包括靶向ctla-4(例如伊匹木单抗)和pd-1(例如纳武利尤单抗和派姆单抗)的抗体的疗法可以促进针对癌细胞的免疫应答,并已显示出治疗某些癌症中的功效。然而,成本和所需的给药途径(iv)以及有害的副作用是患者依从性的障碍。
[0093]
在开发本发明的实施方式的期间进行的实验从fda批准的药物或膳食补充剂(例
如益生元剂)中鉴定出新的化合物,这些化合物可以被摄入以改善免疫检查点疗法的功效。结果表明,药剂(例如,包含纤维的益生元剂(例如,表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖))(例如,褪黑激素)的口服制剂可以改变肠道微生物组,从而增加有益菌的频率并与通过全身注射给予的免疫检查点阻断剂协同作用。事实上,结果表明,并行给药益生元剂(例如,菊糖)与免疫疗法(例如,α-pd-1疗法)导致更强的抗肿瘤功效、更强的免疫应答(例如,pbmc中的ah1特异性cd8
+ t细胞频率)、抑制肿瘤生长、增强t细胞的肿瘤内浸润、脾cd8
+ t细胞中更高的ifn-γ表达,以及受试者肠道微生物组内阿克曼菌属、乳杆菌属、瘤胃球菌属、罗氏菌属和丁酸球菌属的丰度增加。
[0094]
因此,本发明一般地涉及用于提高免疫疗法和疫苗功效的组合物和方法。尤其,本发明涉及通过给药药剂(例如,包含纤维的益生元剂(例如,表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖))(例如,褪黑激素)与给药免疫疗法或疫苗来提升受试者肠道微生物组的丰富度和多样性。这样的组合物和方法可用于治疗癌症、感染性病原体、自身免疫性疾病、神经疾患和/或肥胖症。
[0095]
在某些实施方式中,本发明提供了一种用于提高癌症免疫疗法功效的方法,其通过向受试者给药1)癌症免疫疗法,以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0096]
在某些实施方式中,本发明提供了抑制癌细胞诱导免疫功能障碍的能力的方法,其包括向受试者给药1)癌症免疫疗法,以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0097]
在某些实施方式中,本发明提供了一种用于提高疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)的功效的方法,其通过向受试者给药1)疫苗,以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0098]
在某些实施方式中,本发明提供了抑制癌细胞诱导免疫功能障碍的能力的方法,其包括向受试者给药1)癌症疫苗,以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0099]
在某些实施方式中,本发明提供了用于治疗癌症的方法,其包括向受试者给药1)癌症免疫疗法,以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0100]
在某些实施方式中,本发明提供了用于治疗癌症的方法,其包括向受试者给药1)癌症疫苗,以及2)给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0101]
在某些实施方式中,本发明提供了用于治疗以肠道微生物组活性失调为特征的病症的方法,其包括给药能够提升受试者肠道微生物组的丰富度和多样性的药剂。
[0102]
在一些实施方式中,这种给药能够提升所述受试者肠道微生物组的丰富度和多样性的药剂在给药疫苗(例如癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法之前、并行或之后发生。在一些实施方式中,这种给药能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药所述疫苗(例如,癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法之前发生。在一些实施方式中,这种给药能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药疫苗(例如癌症疫苗)(例如,针对感染性病原体的疫苗)或癌症免疫疗法之前、并行和之后发生。
[0103]
这种方法不限于特定的受试者。在一些实施方式中,受试者是哺乳动物。在一些实
施方式中,受试者是人受试者。在一些实施方式中,受试者是被诊断患有癌症的人受试者。在一些实施方式中,受试者是处于发展癌症风险的人受试者。在一些实施方式中,受试者是患有以肠道微生物组活性失调为特征的病症的人受试者。
[0104]
这种方法不限于能够提升受试者肠道微生物组的丰富度和多样性的特定的药剂。在一些实施方式中,药剂是包含纤维的益生元剂(例如,表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖)。在一些实施方式中,药剂是褪黑激素。在一些实施方式中,药剂是能够诱导受试者肠道微生物组内阿克曼菌属、乳杆菌属、瘤胃球菌属、罗氏菌属和丁酸球菌属的丰度增加。在一些实施方式中,包含纤维的益生元剂是基于凝胶的包含纤维的益生元剂(例如,基于凝胶的菊糖)。
[0105]
事实上,在适合作为任何食物的部分或作为补充剂用于治疗的益生元中,包括以下组分:1,4-二羟基-2-萘甲酸(dhna)、菊糖、反式低聚半乳糖(gos)、乳果糖、甘露寡糖(mos)、低聚果糖(fos)、新琼寡糖(naos)、焦糊精、低聚木糖(xos)、低聚异麦芽糖(imos)、抗直链淀粉、大豆寡糖(sbos)、乳糖醇、低聚乳果糖(ls)、异麦芽酮糖(包括帕拉金糖(palatinose))、阿拉伯木寡糖(axos)、棉子寡糖(rfo)、阿拉伯木聚糖(ax)、多酚或能够以期望作用改变微生物区系组成的任何其他化合物。
[0106]
这种方法不限于特定的癌症免疫疗法。
[0107]
在一些实施方式中,癌症免疫疗法是一种或多种免疫检查点抑制剂(ici)抑制剂。
[0108]
ici包括以统计学显著方式阻断或抑制免疫系统抑制途径的任何药剂。可以靶向阻断或抑制的示例性ici包括但不限于ctla-4、pdl1、pdl2、pd1、b7-h3、b7-h4、btla、hvem、gal9、lag3、tim3、vista、kir、2b4(属于cd2分子家族,并且在所有nk、γδ和记忆cd8+(αβt细胞上表达)、cd160(也称为by55)、cgen-15049、chk 1和chk 2激酶、a2ar和各种b-7家族配体。b7家族配体包括但不限于b7-1、b7-2、b7-dc、b7-h1、b7-h2、b7-h3、b7-h4、b7-h5、b7-h6和b7-h7。ici包括抗体或其抗原结合片段、其他结合蛋白、生物治疗剂或小分子,它们结合并阻断或抑制以下项中一种或多种的活性:ctla-4、pdl1、pdl2、pd1、btla、hvem、tim3、gal9、lag3、vista、kir、2b4、cd160和cgen-15049。示例性ici包括曲美木单抗(ctla-4封闭抗体)、抗ox40、pd-l1单克隆抗体(抗b7-h1;medi4736)、mk-3475(pd-1阻断剂)、纳武利尤单抗(抗pd1抗体)、ct-011(抗pd1抗体)、by55单克隆抗体、amp224(抗pdl1抗体)、bms-936559(抗pdl1抗体)、mpldl3280a(抗pdl1抗体)、msb0010718c(抗pdl1抗体)和伊匹单抗/伊匹木单抗(抗ctla-4检查点抑制剂)。检查点蛋白配体包括但不限于pd-l1、pd-l2、b7-h3、b7-h4、cd28、cd86和tim-3。
[0109]
在一些实施方式中,本发明涵盖使用特定类别的ici,其为阻断免疫检查点受体程序性细胞死亡蛋白1(pd-1)与其配体pd-l1之间相互作用的药物(参见mullard,nature reviews:drug discovery(2013)),12:489-492。pd-1在t细胞上表达并调节其活性。具体来说,当pd-1未与pdl-1结合时,t细胞可以接合并杀死靶细胞。然而,当pd-1与pdl-1结合时,它会引起t细胞停止接合和杀死靶细胞。此外,与其他检查点不同,pd-1的作用接近于使pdl直接在癌症细胞上过度表达,从而导致与表达pd-1的t细胞的结合增加。
[0110]
在一些实施方式中,提供了作为抗体的ici,其可以充当pd-1的激动剂,从而调节受pd-1调节的免疫应答。在一个实施方式中,抗pd-1抗体可以是抗原结合片段。本文公开的抗pd-1抗体能够结合人pd-1并激动pd-1的活性,从而抑制表达pd-1的免疫细胞的功能。
[0111]
在一些实施方式中,本发明涵盖使用特定类别的ici,其为抑制ctla-4的药物。用于本发明方法的合适的抗ctla4拮抗剂包括但不限于抗ctla4抗体、人抗ctla4抗体、小鼠抗ctla4抗体、哺乳动物抗ctla4抗体、人源化抗ctla4抗体、单克隆抗ctla4抗体、多克隆抗ctla4抗体、嵌合抗ctla4抗体、mdx-010(伊匹木单抗)、曲美木单抗、抗cd28抗体、抗ctla4 adnectin、抗ctla4结构域抗体、单链抗ctla4片段、重链抗ctla4片段、轻链抗ctla4片段、激动共刺激途径的ctla4抑制剂、pct公开号wo 2001/014424中公开的抗体、pct公开号wo 2004/035607中公开的抗体、美国公开号2005/0201994中公开的抗体以及授权的欧洲专利号ep 1212422b1中公开的抗体。在美国专利号5,811,097、5,855,887、6,051,227和6,984,720中;在pct公开号wo 01/14424和wo 00/37504中;以及在美国公开号2002/0039581和2002/086014中描述了额外的ctla-4抗体。可以用于本发明方法的其他抗ctla-4抗体包括例如以下项中公开的那些:wo 98/42752;美国专利号6,682,736和6,207,156;hurwitz et al.,proc.natl.acad.sci.usa,95(17):10067-10071(1998);camacho et al.,j.clin.oncology,22(145):abstract no.2505(2004)(antibody cp-675206);mokyr et al.,cancer res.,58:5301-5304(1998),以及美国专利号5,977,318、6,682,736、7,109,003和7,132,281。
[0112]
额外的抗ctla4拮抗剂包括但不限于以下:为以下项的任何抑制剂:该抑制剂能够破坏cd28抗原与其同源配体结合的能力、抑制ctla4与其同源配体结合的能力、经由共刺激途径增强t细胞应答、破坏b7与cd28和/或ctla4结合的能力、破坏b7激活共刺激途径的能力、破坏cd80与cd28和/或ctla4结合的能力、破坏cd80激活共刺激途径的能力、破坏cd86与cd28和/或ctla4结合的能力、破坏cd86激活共刺激途径的能力、以及破坏通常被激活的共刺激途径。这必然包括cd28、cd80、cd86、ctla4以及共刺激途径的其他成员的小分子抑制剂;针对cd28、cd80、cd86、ctla4以及共刺激途径的其他成员的抗体;针对cd28、cd80、cd86、ctla4以及共刺激途径的其他成员的反义分子;直接针对cd28、cd80、cd86、ctla4以及共刺激途径的其他成员的adnectin,cd28、cd80、cd86、ctla4以及共刺激途径的其他成员的rnai抑制剂(单链和双链两者),以及其他抗ctla4拮抗剂。
[0113]
在一些实施方式中,本发明涵盖使用特定类别的ici,其为抑制tim-3的药物。通过配体阻断tim-3的活化,导致th1细胞活化增加。此外,tim-3已被确定为耗竭的cd8+ t细胞表达的重要抑制性受体。tim-3也被报道为核酸介导的抗肿瘤免疫的关键调节剂。在一个实例中,已显示tim-3在肿瘤相关树突状细胞(tadc)上被上调。
[0114]
这种方法不限于使用特定的癌症疫苗。事实上,癌症免疫疗法所采用的一种方法是术语“肿瘤疫苗”或“癌症疫苗”所涵盖的领域,其中包括用肿瘤特异性或过表达的抗原进行免疫。在这种方法中,特异性于肿瘤细胞或在肿瘤细胞中过表达的一种或多种抗原单独地或与佐剂一起,作为递送抗原的微生物(例如单核细胞增生李斯特菌)的部分,或在与免疫细胞(包括但不限于树突状细胞)离体孵育后注射,以引发细胞和/或体液免疫应答。
[0115]
在一些实施方式中,癌症是癌。癌是上皮起源的癌症。在一些实施方式中,癌选自由以下项组成的组:腺泡癌、腺泡状癌、肺泡腺癌、腺瘤(carcinoma adenomatosum)、腺癌(adenocarcinoma)、肾上腺皮质癌、肺泡癌、肺泡细胞癌、基底细胞癌(basal cell carcinoma)、基细胞癌(carcinoma basocellular)、类基底细胞癌、基底鳞状细胞癌、乳腺癌、细支气管肺泡癌、气管癌、脑样癌、胆管细胞癌、绒毛膜癌、胶体癌、粉刺性癌、子宫体癌、
筛状癌、胸甲癌、癌疮、柱状癌(cylindrical carcinoma)、柱状细胞癌、导管癌、硬癌、胚胎癌、髓样癌、眼球上癌(epibulbar carcinoma)、表皮样癌、上皮腺样癌(carcinoma epitheliate adenoids)、溃疡性癌(carcinoma exulcere)、纤维癌、胶样癌(gelatinform carcinoma)、胶状癌(gelatinous carcinoma)、巨细胞癌(giant cell carcinoma)、巨细胞癌(gigantocellulare)、腺癌(glandular carcinoma)、颗粒细胞癌、毛基质癌、多血癌、肝细胞癌、hurthle细胞癌、胶样癌(hyaline carcinoma)、肾上腺样癌、卵黄囊性癌、原位癌、表皮内癌、上皮内癌、侵蚀性溃疡(krompecher's carcinoma)、库尔契茨基细胞癌(kulchitzky-cell carcinoma)、豆状癌(lentivular carcinoma)、豆状癌(carcinoma lenticulare)、脂瘤样癌(lipomatous carcinoma)、淋巴上皮癌、乳炎性癌(carcinoma mastotoids)、髓样癌(carcinoma medullare)、髓样癌(medullary carcinoma)、黑色素癌(carcinoma melanodes)、黑素癌(melanotonic carcinoma)、粘液癌(mucinous carcinoma)、黏液癌(carcinoma muciparum)、carcinoma mucocullare、粘液表皮样癌、粘液癌(mucous carcinoma)、粘液瘤样癌、鼻咽癌、黑色素癌(carcinoma nigrum)、燕麦细胞癌、骨化性癌、骨样癌(osteroid carcinoma)、卵巢癌、乳头状癌、门静脉周围癌、浸润前癌、前列腺癌、肾脏的肾细胞癌、贮备细胞癌、肉瘤样癌(carcinoma sarcomatodes)、施奈德癌(scheinderian carcinoma)、慢性癌、阴囊癌、印戒细胞癌、单纯癌、小细胞癌、马铃薯状癌(solandoid carcinoma)、球形细胞癌、梭形细胞癌、软癌、鳞状癌、鳞状细胞癌、绳捆癌(string carcinoma)、毛细管扩张癌(carcinoma telangiectaticum)、毛细管扩张癌(carcinoma telangiectodes)、移行细胞癌、块状癌(carcinoma tuberrosum)、结节性癌(tuberous carcinoma)、疣状癌(verrucous carcinoma)、绒毛状癌(carcinoma vilosum)。
[0116]
在一些实施方式中,癌症是肉瘤。肉瘤是出现在骨骼和软组织中的间充质赘生物。在一些实施方式中,肉瘤选自脂肪肉瘤(包括粘液样脂肪肉瘤和多形性脂肪肉瘤)、平滑肌肉瘤、横纹肌肉瘤、神经纤维肉瘤、恶性外周神经鞘肿瘤、尤因氏瘤(包括骨、骨骼外或非骨的malignant peripheral nerve sheath tumor)和原始神经外胚瘤(pnet)、滑膜肉瘤、血管内皮瘤、纤维肉瘤、硬纤维瘤、隆突性皮纤维肉瘤(dfsp)、恶性纤维组织细胞瘤(mfh)、血管外皮细胞瘤、恶性间叶瘤、肺泡状软组织肉瘤(alveolar soft-part sarcoma)、上皮样肉瘤、透明细胞肉瘤、促促结缔织增生性小细胞肿瘤(desmoplastic small cell tumor)、胃肠道间质瘤(gist)和骨肉瘤(也称为骨骼和骨骼外骨原性肉瘤,以及软骨肉瘤。
[0117]
在一些实施方式中,癌症是难治性或响应性癌症。如本文所用,难治性癌症是对规定的普通护理标准有抗性的癌症。这些癌症虽然最初对治疗有响应但会复发和/或可能对治疗完全无响应。
[0118]
在一些实施方式中,癌症是免疫原性癌症。免疫原性癌症的实例包括恶性黑素瘤和肾细胞癌、套细胞淋巴瘤、滤泡性淋巴瘤、弥漫性大b细胞淋巴瘤、t细胞急性淋巴细胞白血病、伯基特淋巴瘤、骨髓瘤、免疫细胞瘤、急性早幼粒细胞白血病、慢性髓系/急性淋巴细胞白血病、急性白血病、b细胞急性淋巴细胞白血病、间变性大细胞白血病(anaplastic large cell leukemia)、骨髓增生异常综合征/急性髓系白血病、非霍奇金淋巴瘤、慢性淋巴细胞白血病、急性髓细胞性白血病(aml)、普通(pre-b)急性淋巴细胞白血病、恶性黑素瘤、t细胞淋巴瘤、白血病、b细胞淋巴瘤、上皮恶性肿瘤、淋巴恶性肿瘤、妇科癌、胆管腺癌和胰腺导管腺癌。
[0119]
在一些实施方式中,这种方法进一步包括给药其他疗法,诸如例如放射疗法、手术、常规化学疗法或与一种或多种额外的疗法的联合。这样的其他活性成分包括但不限于谷胱甘肽拮抗剂、血管生成抑制剂、化疗剂和抗体(例如,癌症抗体)。本发明中描述的药剂可以同时或依次给药。给药之间的时间间隔可以是数分钟、数小时、数天或它可以更长。
[0120]
例如,能够提升受试者肠道微生物组的丰富度和多样性的药剂和癌症免疫疗法或癌症疫苗可以在额外的化疗剂和/或细胞毒性剂之前、之后或同时给药,额外的化疗剂和/或细胞毒性剂为诸如烷化剂(例如,苯丁酸氮芥、环磷酰胺、罗氮芥(ccnu)、美法仑、丙卡巴肼、噻替哌、卡氮芥(bcnu)和白消安),抗代谢物(例如,6-巯基嘌呤和5-氟尿嘧啶),蒽环素(例如,柔红霉素(daunorubicin)、多柔比星(doxorubicin)、伊达比星(idarubicin)、表柔比星(epirubicin)和米托蒽醌(epirubicin)),抗肿瘤抗生素(例如,博来霉素(bleomycin)),单克隆抗体(例如,阿仑珠单抗(alemtuzumab)、贝伐珠单抗(bevacizumab)、西妥昔单抗(cetuximab)、吉妥珠单抗(gemtuzumab)、替伊莫单抗(ibritumomab)、帕木单抗(panitumumab)、利妥昔单抗(rituximab)、托西莫单抗(tositumomab)和曲司珠单抗(trastuzumab)),铂(例如,顺铂、奥沙利铂(oxaliplatin)和卡铂),植物生物碱(例如,长春新碱(vincristine)),拓扑异构酶i或ii抑制剂(例如,伊立替康(irinotecan)、拓泊替康(topotecan)、安吖啶(topotecan)、依托泊苷(etoposide)、磷酸依托泊苷和替尼泊苷(teniposide))、长春花生物碱(例如,长春新碱、长春碱(vinblastine)、长春瑞滨(vinorelbine)和长春地辛(vindesine)、紫杉烷(例如,紫杉醇和多西他赛(docetaxel)、表鬼臼毒素(例如,依托泊苷和替尼泊苷),核苷类似物和血管生成抑制剂(例如,贝伐单抗(avastin)(贝伐珠单抗),一种特异性于vegf-a的人源化单克隆抗体)。
[0121]
谷胱甘肽拮抗剂的实例包括但不限于丁硫氨酸亚砜亚胺、环磷酰胺、异环磷酰胺、放线菌素-d和n-(4-羟苯基)视黄酰胺(4-hpr)。血管生成抑制剂的实例包括但不限于2-甲氧基雌二醇(2-me)、ag3340、血管抑制素、抗凝血酶-iii、抗vegf抗体、巴马司他(batimastat)、贝伐珠单抗(贝伐单抗)、bms-275291、ca1、人血管能抑素、康普瑞汀(combretastatin)、康普瑞汀-a4磷酸盐、cc-5013、卡托普利(captopril)、塞来昔布(celecoxib)、达肝素(dalteparin)、emd121974、内皮抑素、厄洛替尼(erlotinib)、吉非替尼(gefitinib)、染料木黄酮、卤夫酮、id 1、id3、im862、甲磺酸伊马替尼、可诱导的蛋白10、干扰素-α、白介素-12、薰草菌素-a(lavendustin-a)、ly317615或ae-941、马立马司他(marimastat)、mapsin、醋酸甲羟孕酮、meth-1、meth-2、新伐司他(neovastat)、骨桥蛋白切割产物、pex、色素上皮生长因子(pegf)、血小板生长因子4、催乳素片段、增殖蛋白相关蛋白(prp)、ptk787/zk222584、重组人血小板因子-4(rpf4)、休眠蛋白、角鲨胺、su5416、su6668、舒拉明钠(suramin)、泰素、tecogalan、沙利度胺、四硫钼酸盐(tm)、血小板应答蛋白、tnp-470、肌钙蛋白i、血管抑制因子(vasostatin)、vegf1、vegf-tpvap和zd6474。在一些实施方式中,血管生成抑制剂是vrgf拮抗剂。vegf拮抗剂可以是vegf结合分子。vegf结合分子包括vegf抗体或其一种或多种抗原结合片段。vegf拮抗剂的一个实例是nexstar。
[0122]
可用于本文公开的任何方法或药剂的化疗剂类别的实例包括但不限于dna损伤剂并且这些包括拓扑异构酶抑制剂(例如,依托泊苷、喜树碱、拓泊替康、伊立替康、替尼泊苷、米托蒽醌)、抗微管剂(例如,长春新碱、长春碱)、抗代谢药物剂(例如,阿糖胞苷、甲氨蝶呤、羟基脲、5-氟尿嘧啶、氟尿苷(flouridine)、6-硫鸟嘌呤、6-巯基嘌呤、氟达拉滨、喷司他丁、
氯脱氧腺苷)、dna烷化剂(例如,顺铂、甲氯乙胺(mecholorethamine)、环磷酰胺、异环磷酰胺、美法仑、苯丁酸氮芥、白消安、塞替派(thiotepa)、卡莫司汀(carmustine)、洛莫司汀(lomustine)、卡铂(carboplatin)、达卡巴嗪(dacarbazine)、丙卡巴肼(procarbazine))和dna链断裂诱导剂(例如,博来霉素、多柔比星、柔红霉素、伊达比星、丝裂霉素c(mitomycin c))。
[0123]
化疗剂包括合成的、半合成的和天然来源的药剂。重要的化疗剂包括但不限于勒碱(avicine)、阿柔比星(aclarubicin)、阿考达唑(acodazole)、阿克罗宁(acronine)、阿多来新(adozelesin)、阿霉素(adriamycin)、阿地白介素(aldesleukin)、阿利维a酸(alitretinoin)、别嘌呤醇钠(auopurinol sodium)、六甲蜜胺(altretamine)、安波霉素(ambomycin)、醋酸阿美蒽醌(ametantrone acetate)、氨鲁米特(aminoglutethimide)、安吖啶(amsacrine)、阿那曲唑(anastrazole)、番荔枝内酯(annonaceous acetogenins)、氨茴霉素(anthramycin)、asimicin、天冬酰胺酶(asparaginase)、曲林菌素(asperlin)、阿扎胞苷(azacitidine)、阿扎替派(azetepa)、阿佐霉素(azotomycin)、巴马司他(batimastat)、苯佐替派(benzodepa)、贝沙罗汀(bexarotene)、比卡鲁胺(bicalutamide)、比生群(bisantrene)、双萘法德(bisnafide)、比折来新(bizelesin)、博来霉素(bleomycin)、布喹那(brequinar)、溴匹立明(bropirimine)、布拉它辛(bullatacin)、白消安(busulfan)、卡麦角林(cabergoline)、放线菌素(cactinomycin)、卡鲁睾酮(calusterone)、卡醋胺(caracemide)、卡贝替姆(carbetimer)、卡铂(carboplatin)、卡莫司汀、卡柔比星(carubicin)、卡折来新(carzelesin)、西地芬戈(cedefingol)、苯丁酸氮芥(chlorambucil)、塞来昔布(celecoxib)、西罗霉素(cirolemycin)、顺铂、克拉立滨(cladribine)、克立那托(crisnatol)、环磷酰胺、阿糖胞苷(cytarabine)、达卡巴嗪(dacarbazine)、daca、放线菌素、柔红霉素、道诺霉素(daunomycin)、地西他滨(decitabine)、地尼白介素(denileukin)、右奥马铂(dexormaplatin)、地扎胍宁(dezaguanine)、地吖醌(diaziquone)、多西他赛(docetaxel)、多柔比星(doxorubicin)、屈洛昔芬(droloxifene)、屈他雄酮(dromostalone)、达佐霉素(duazomycin)、依达曲沙(edatrexate)、依氟鸟氨酸(eflornithine)、依沙芦星(elsamitrucin)、雌莫司汀(estramustine)、依他硝唑(etanidazole)、依托泊苷(etoposide)、氯苯乙嘧胺(etoprine)、法罗唑(fadrozole)、法扎拉滨(fazarabine)、芬维a胺(fenretinide)、氟尿苷(floxuridine)、氟达拉滨(fludarabine)、氟尿嘧啶(fluorouracil)、氟西他宾(flurocitabine)、5-fdump、磷喹酮(fosquidone)、福司曲星(fosteuecine)、fk-317、fk-973、fr-66979、fr-900482、吉西他滨(gemcitabine)、吉妥珠单抗(gemtuzumab)、奥加米星(ozogamicin)、金aul 98、戈舍瑞林(goserelin)、guanacone、羟基脲(hydroxyurea)、伊达比星(idarubicin)、伊莫福新(ilmofosine)、干扰素α及类似物、异丙铂(iproplatin)、伊立替康(irinotecan)、兰瑞肽(lanreotide)、来曲唑(letrozole)、亮丙瑞林(leuprolide)、利阿罗唑(liarozole)、洛美曲索(lometrexol)、洛莫司汀(lomustine)、洛索蒽醌(losoxantrone)、马索罗酚(masoprocol)、美登素(maytansine)、氮芥(mechlorethamine)、甲地孕酮(megestrol)、美仑孕酮(melengestrol)、美法仑(melphalan)、美诺立尔(menogaril)、氯苯氨啶(metoprine)、美妥替哌(maturedepa)、米丁度胺(mitindomide)、米托卡星(mitocarcin)、米托洁林(mitogillin)、佩利霉素(mitomalacin)、丝裂霉素、丝裂霉
素c、米托司培(mitosper)、米托坦(mitotane)、米托蒽醌(mitoxantrone)、霉酚酸(mycophenolic acid)、诺考达唑(nocodazole)、诺加霉素(nogalamycin)、奥普瑞白介素(oprelvekin)、奥马铂(ormaplatin)、奥昔舒仑(oxisuran)、紫杉醇(paclitaxel)、帕米膦酸(pamidronate)、培门冬酶(pegaspargase)、培利霉素(peliomycin)、戊氮芥(pentamustine)、培洛霉素(peplomycin)、培磷酰胺(perfosfamide)、哌泊溴烷(pipobroman)、哌泊舒凡(piposulfan)、吡罗蒽醌(piroxantrone)、普卡霉素(plicamycin)、普洛美坦(plomestane)、卟吩姆(porfimer)、泊非霉素(porfiromycin)、泼尼莫司汀(prednimustine)、丙卡巴肼(procarbazine)、嘌呤霉素(puromycin)、吡唑呋喃菌素(pyrazofurin)、利波腺苷(riboprine)、利妥昔单抗(rituximab)、罗谷亚胺(rogletimide)、罗林尼阿司他汀(rolliniastatin)、沙芬戈(safingol)、钐(samarium)、司莫司汀(semustine)、辛曲秦(simtrazene)、sparfosate、稀疏霉素(sparsomycin)、锗螺胺(spirogermanium)、螺莫司汀(spiromustine)、螺铂(spiroplatin)、多鳞番荔枝辛(squamocin)、squamotacin、链黑菌素(streptonigrin)、链脲霉素(streptozocin)、src12、磺氯苯脲(sulphofenur)、他利霉素(talisomycin)、紫杉烷类(taxane)、类毒素(toxoid)、tecoglan、替加氟(tegafur)、替洛蒽醌(teloxantrone)、替莫泊芬(temoporfin)、替尼泊苷(teniposide)、替罗昔隆(teroxirone)、睾内酯(testolactone)、硫咪嘌呤(thiamiprine)、塞替派(thiotepa)、诺拉曲特(thymitaq)、噻唑呋林(tiazofurin)、替拉扎明(tirapazamine)、雷替曲塞(tomudex)、top-53、拓扑替康(topotecan)、托瑞米芬(toremixifme)、曲妥珠单抗(trastuzumab)、曲托龙(trestolone)、曲西瑞宾(triciribine)、曲西立滨(triciribine)、三甲曲沙(trimetrexate)、三甲曲沙葡萄糖醛酸(trimetrexate glucuronate)、曲普瑞林(triptorelin)、妥布氯唑(tubulozole)、尿嘧啶氮芥(uracil mustard)、乌瑞替派(uredepa)、戊柔比星(valrubicin)、伐普肽(vapreotide)、长春碱(vinblastine)、长春新碱(vincristine)、长春地辛(vindesine)、长春匹定(vinepidine)、长春甘酯(vinglycinate)、长春罗新(vinleurosine)、长春瑞滨(vinorelbine)、长春罗定(vinrosidine)、长春利定(vinzolidine)、伏氯唑(vorozole)、折尼铂(zeniplatin)、净司他丁(zinostatin)、佐柔比星(zorubicin)、2-氯脱氧腺苷(2-cholrodeoxyrubicine)、2'-脱氧型霉素(2'-deoxyformycin)、9-氨基喜树碱(9-aminocamptothecin)、雷替曲塞(raltitrexed)、n-炔丙基-5,8-二脱氮杂叶酸(n-propargyl-5,8-didezafolic acid)、2-氯-2'-阿糖氟-2'脱氧腺苷(2-cholo-2'arabinofluoro-2'deoxyadenosine)、2-氯-2'-脱氧腺苷(2-cholo-2'-deoxyadenosine)、茴香霉素(anisomycin)、曲古霉素(trichostatin)、hprl-g129r、cep-751、三羧氨基喹啉(linomide)、硫芥子气(sulfur mustard)、氮芥(nitrogen mustard)、n-甲基-n-亚硝基脲(n-methyl-n-nitrosourea)、福莫司汀(fotemustine)、链脲佐菌素(streptozotocin)、达卡巴嗪(dacarbazine)、米托唑胺(mitozolomide)、替莫唑胺(temozolomide)、(azq)、奥马铂(ormaplatin)、ci-973、dwa21 14r、jm216、jm335、二铂(bisplatinum)、雷替曲塞(tomudex)、阿扎胞苷(azacitidine)、cytrabincine、吉西他滨(gemcitabine)、6-巯基嘌呤(6-mercaptopurine)、次黄嘌呤(hypoxanthine)、替尼泊苷(teniposide)、cpt-11、多柔比星(doxorubicin)、柔红霉素(daunorubicin)、表柔比星(epirubicin)、依道红菌素(darubicin)、洛索蒽醌(losoxantrone)、安吖啶(amsacrine)、吡唑啉吖啶
(pyrazoloacridine)、全反式视黄醇、14-羟基反式视黄醇(14-hydroxy-retro-retinol)、全反式视黄酸、n-(4-羟基苯基)维甲酸胺、13-顺式视黄酸、3-甲基ttneb、9-顺式维甲酸、氟达拉滨(fludarabine)和2-cda。
[0124]
其他化疗剂包括:20-epi-1,25-二羟基维生素d3、5-乙炔基尿嘧啶、阿比特龙(abiraterone)、阿柔比星、酰基富烯(acylfulvene)、阿迪西潘诺(adecylpenol)、阿多来新(adozelesin)、阿地白介素、all-tk拮抗剂、六甲蜜胺、氨莫司汀(ambumastine)、amidox、氨磷汀(amifostine)、氨基戊酮酸、阿那格雷(anagrelide)、阿那罗唑(anastrozole)、穿心莲内酯、血管生成抑制剂、一种或多种拮抗剂d、antarelix、抗背部化形态发生蛋白-1(anti-dorsalizing morphogenetic protein-1)、抗雄激素、抗雌激素、抗瘤酮、反义寡核苷酸、阿非迪霉素(aphidicolin)、细胞凋亡基因调节剂、细胞凋亡调节剂、脱嘌呤酸(apurinic acid)、ara-cdp-dl-ptba、精氨酸氨基酶、asulacrine、阿他美坦(atamestine)、阿莫司汀(atrimustine)、axinamastine 1和axinamastine2、axinamastine3、阿扎司琼(azasetron)、阿扎毒素(azatoxin)、重氮酪氨酸(azatyrosine)、浆果赤霉素ⅲ衍生物、balanol、bcr/abl拮抗剂、苯并二氢卟酚(benzochlorin)、苯甲酰基星形孢菌素(benzoylsaurosporine)、β-内酰胺衍生物、beta-alethine、紫苏子醇(perillyl alcohol)、苯连氮霉素(phenozenomyein)、乙酸苯酯、磷酸酶抑制剂、溶链菌制剂、pilocarbine及其盐或其类似物、吡柔比星(pirarubucin)、吡曲克辛(piritrexim)、placetin a、placetin b、纤溶酶原激活物抑制剂、铂络合物、苯基乙基异硫氰酸酯及其类似物、铂化合物、铂三胺络合物、鬼臼毒素(podophylotoxin)、卟吩姆钠(porfimer sodium)、紫菜霉素(porphyromycin)、丙基双吖啶酮(propyl bis acridones)、前列腺素j2、蛋白激酶抑制剂、基于蛋白a的免疫调节剂、pkc抑制剂、微藻(microalgal)、蛋白酪氨酸磷酸酶抑制剂、嘌呤核苷磷酸化酶抑制剂、红紫素(purpurin)、吡唑啉吖啶、吡哆酰基化血红素聚氧乙烯缀合物、raf拮抗剂、雷替曲塞(raltitrexed)、雷莫司琼(ramosetron)、ras法尼基蛋白转移酶抑制剂、ras抑制剂(rasinhibitor)、as-gap抑制剂、脱甲基ratellitptine、依替膦酸铼re186(rhenium re 186etidronate)、根霉素(rhizoxine)、核酶、rii retinide、罗谷亚胺、罗格列酮(rosagliatazone)及其类似物和衍生物、罗希吐碱罗莫肽、罗喹美克(roquinimex)、rubiginone b1、ruboxyl、沙芬戈(safingol)、saintopin、sarcnu、sarcophytol a、沙格司亭(sargrmostim)、sdi 1模拟物、司莫司汀(semustine)、衰老衍生抑制剂1、正义寡核苷酸、信号转导抑制剂、信号转导调节剂、单链抗原结合蛋白、西佐喃(sizofiran)、索布佐生(sobuzoxane)、硼卡钠(sodium borocaptate)、苯乙酸钠、solverol、生长调节素结合蛋白、索纳明(sonermin)、膦门冬酸(sparfosic acid)、穗霉素d(spicamycin d)、螺旋氮芥(spiromustin)、splenopentine、海绵抑制素1(spongistatin 1)、角鲨胺、干细胞抑制剂、干细胞分裂抑制剂、stipiamide、基质溶素(stromelysin)、sulfinosine、超活性血管活性肠肽拮抗剂、suradista、siramin、苦马豆素、合成糖胺聚糖、他莫司汀(tallimustine)、他莫昔芬甲碘化物(tamoxifen methiodide)、牛磺莫司汀(tauromustine)、他扎罗汀(tazarotene)、替可加兰钠(tacogalan sodium)、替加氟(tegafur)、tellurapyrilium、端粒酶抑制剂、替莫泊芬(temoporfin)、替莫唑胺(tmeozolomide)、替尼泊苷(teniposide)、四氯十氧化物(tetrachlorodecaoxide)、四唑胺(tetrazomine)、沙利布拉司汀(thaliblastine)、沙利度胺(thalidomide)、噻可拉林
(thiocoraline)、血小板生成素(thrombopoetin)及其模拟物、胸腺法新(thymalfasin)、胸腺生成素(thymopoetin)受体激动剂、胸腺曲南(thymotrinan)、促甲状腺激素、锡乙基etiopurpin、替拉扎明(tirapazamine)、茂钛(titanocene)及其盐、拓扑替康(topotecan)、topsentin、托瑞米芬(toremifene)、全能干细胞因子、翻译抑制剂、维甲酸、三乙酰尿苷(triacetyluridine)、tricribine、三甲曲沙(trimetrexate)、曲普瑞林(triptorelin)、托烷司琼(tropisetron)、妥罗雄脲(turosteride)、酪氨酸激酶抑制剂、酪氨酸磷酸化抑制剂(tyrphostin)、ubc抑制剂、乌苯美司(ubenimex)、泌尿生殖窦源性生长抑制因子、尿激酶受体拮抗剂、伐普肽(vapreotide)、variolin b、载体系统、红细胞基因疗法、维拉雷琐(velaresol)、黎芦胺、verdins、维替泊芬(verteporfin)、长春瑞滨、vinxaltine、vitaxin、伏氯唑(vorozole)、扎诺特隆(zanoterone)、折尼铂(zeniplatin)、亚苄维(zilascorb)和净司他丁(zinostatin)。
[0125]
其他化疗剂包括:抗增殖剂(例如,吡曲克辛异硫氰酸酯(piritrexim))、抗前列腺肥大剂(西托糖苷((sitogluside))、良性前列腺增生治疗剂(例如,tomsulosine、rbx2258)、前列腺生长抑制剂(喷托孟(pentomone))和放射性剂:纤维蛋白原i125、氟代脱氧葡萄糖(fludeoxyglucose)f18、氟多巴(flurodopa)f18、胰岛素1125、碘苄胍(iobenguane)1123、胆影酸钠1131、碘代安替比林1131、碘胆甾醇1131、碘吡啦啥(iodopyracet)1125、碘非他胺(iofetamine)hcl 1123、iomethin 1131、iomethin 1131、碘酞钠1125、碘酞酸盐1131、碘酪氨酸1131、碘塞罗宁(liothyronine)1125、merosproprol hgl97、甲基碘苯并鸟嘌呤(mibg-i131或mibgi123)硒代蛋氨酸se75、锝tc99m呋膦、锝tc99m葡庚糖酸盐、tc99m biscisate、tc99m地索苯宁(disofenin)、99mtc葡庚糖酸盐、tc99m利多苯宁(lidofenin)、tc99m甲溴苯宁(mebrofenin)、tc99m亚甲基二膦酸及其钠盐、tc99m巯替肽(mertiatide)、tc99m奥昔膦酸(oxidronate)、tc99m喷替酸及其盐、tc99m司他比(sestambi)、tc99m西硼肟锝(siboroxime)、tc99m二巯丁二酸(succimer)、tc99m硫胶体(sulfur colloid)、tc99m替肟(teboroxime)、tc99m替曲膦(tetrofosmin)、tc99m tiatide、甲状腺素1125、甲状腺素1131、托泊酮(tolpovidone)1131、三油精(triolein)1125和treoline 1125、和treoline131、mibg-i123和mibg i131是与本发明的包含硝基呋喃的药物组合物共同给药的特别优选的化疗剂。
[0126]
其他类化疗剂是抗癌补充增效剂,例如抗抑郁药物(丙咪嗪(imipramine)、地昔帕明(desipramine)、阿米替林(amitriptyline)、氯米帕明(clomipramine)、曲米帕明(trimipramine)、多塞平(doxepin)、去甲替林(nortriptyline)、普罗替林(protriptyline)、阿莫沙平(amoxapine)和马普替林(maprotiline))或非三环抗抑郁药物(舍曲林(sertraline)、曲唑酮(trazodone)和西酞普兰(citalopram))、ca++拮抗剂(维拉帕米(verapamil)、硝苯地平(nifedipine)、尼群地平(nitrendipine)和卡洛维林(caroverine))、钙调蛋白抑制剂(普尼拉明(prenylamine)、三氟拉嗪(trifluoperazine)和氯米帕明(clomipramine))、两性霉素b、曲帕拉醇类似物(例如,他莫昔芬(tamoxifen))、抗心律失常药物(例如,奎尼丁(quinidine))、抗高血压药物(例如,利血平(reserpine))、硫醇消耗剂(例如,丁硫氨酸和亚砜亚胺(sulfoximine))和多种抗药性还原剂,诸如克列莫佛el(cremophor el)。
[0127]
在一些实施方式中,以肠道微生物组活性失调为特征的病症是自身免疫性疾病、
神经疾患、糖尿病和/或肥胖症。这样的病症的实例包括但不限于类风湿性关节炎、多发性硬化糖尿病(例如,1型糖尿病)、甲状腺自身免疫性疾病(例如,桥本甲状腺炎、格雷夫斯病)、甲状腺相关性眼病和皮肤病、甲状旁腺功能减退症、艾迪生病、卵巢早衰、自身免疫性垂体炎、垂体自身免疫性疾病、免疫性胃炎、恶性贫血、乳糜泻、白癜风、重症肌无力、寻常型天疱疮和变体、大疱性类天疱疮、疱疹样皮炎、获得性大疱性表皮松解症、系统性硬化病、混合性结缔组织病、干燥综合征、系统性红斑狼疮、肺出血肾炎综合征、风湿性心脏病、自身免疫性多内分泌腺综合征1型、aicardi-gouti
è
res综合征、急性胰腺炎、年龄相关性黄斑变性、酒精性肝病、肝纤维化、转移、心肌梗死、非酒精性脂肪肝炎(nash)、帕金森病、多关节炎/胎儿和新生儿贫血、脓毒症和炎性肠病。
[0128]
在一些实施方式中,这种用于治疗或预防以肠道微生物组活性疾患失调为特征的病症的方法进一步包括给药(例如,同时或在不同时间)额外的治疗剂。这样的治疗剂的实例包括但不限于改善疾病的抗风湿药物(例如,来氟米特、甲氨蝶呤、柳氮磺胺吡啶、羟氯喹)、生物剂(例如,利妥昔单抗、英利昔单抗、依那西普、阿达木单抗、戈利木单抗)、非甾体抗炎药物(例如,布洛芬、塞来昔布、酮洛芬、萘普生、吡罗昔康、双氯芬酸)、镇痛剂(例如,对乙酰氨基酚、曲马多)、免疫调节剂(例如,阿那白滞素、阿巴西普)、糖皮质激素(例如,泼尼松、甲泼尼松)、tnf-α抑制剂(例如,阿达木单抗、培化舍单抗、依那西普、戈利木单抗、英利昔单抗)、il-1抑制剂和金属蛋白酶抑制剂。在一些实施方式中,治疗剂包括但不限于英利昔单抗、阿达木单抗、依那西普、肠胃外金或口服金。
[0129]
在某些实施方式中,本发明提供了包括基于凝胶的菊糖制剂的组合物。在一些实施方式中,基于凝胶的菊糖制剂具有的平均聚合度为20或高于20至47或小于47。在一些实施方式中,基于凝胶的菊糖制剂具有的平均聚合度为大约28(例如,23、24、25、26、27、28、29、30、31、32、33)。在一些实施方式中,基于凝胶的菊糖制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
[0130]
在某些实施方式中,本发明提供了一种用于提高疫苗功效的方法,其通过向受试者给药1)疫苗,以及2)给药能够提升所述受试者肠道微生物组的丰富度和多样性的药剂。
[0131]
在一些实施方式中,给药能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药疫苗之前、并行和/或之后发生。
[0132]
在一些实施方式中,给药能够提升受试者肠道微生物组的丰富度和多样性的药剂与给药疫苗并行发生;或者给药能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药疫苗之前发生。在一些实施方式中,其中,给药能够提升受试者肠道微生物组的丰富度和多样性的药剂在给药疫苗之前和并行发生。
[0133]
在一些实施方式中,疫苗是用于治疗癌症的疫苗,和/或用于治疗和/或保护免受感染性病原体的疫苗。
[0134]
在一些实施方式中,受试者是人受试者。
[0135]
在一些实施方式中,能够提升受试者肠道微生物组的丰富度和多样性的药剂是包含纤维的益生元剂。在一些实施方式中,包含纤维的益生元剂选自表没食子儿茶素没食子酸酯(egcg)、岩藻多糖、马铃薯淀粉、低聚果糖和菊糖。在一些实施方式中,包含纤维的益生
元剂是基于凝胶的菊糖制剂。在一些实施方式中,基于凝胶的菊糖制剂具有的平均聚合度为20或高于20至47或小于47。在一些实施方式中,基于凝胶的菊糖制剂具有的平均聚合度为大约28(例如,23、24、25、26、27、28、29、30、31、32、33)。在一些实施方式中,基于凝胶的菊糖制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。在一些实施方式中,能够提升受试者肠道微生物组的丰富度和多样性的药剂是褪黑激素。
[0136]
在一些实施方式中,能够提升受试者肠道微生物组的丰富度和多样性的药剂是口服给药。
[0137]
在一些实施方式中,给药能够提升受试者肠道微生物组的丰富度和多样性的药剂导致受试者肠道微生物组内阿克曼菌属、乳杆菌属、瘤胃球菌属、罗氏菌属和丁酸球菌属的相对丰度增加。
[0138]
在某些实施方式中,本发明提供了包括与细菌结合的(例如,复合的、缀合的、包封的、吸收的、吸附的、混合的)益生元制剂的组合物。
[0139]
在一些实施方式中,益生元制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、菊糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
[0140]
在一些实施方式中,益生元化合物是基于凝胶的。在一些实施方式中,益生元化合物是基于凝胶的菊糖。
[0141]
在一些实施方式中,细菌是大肠杆菌。在一些实施方式中,细菌在向受试者给药后能够改变受试者的肠道微生物组。
[0142]
在一些实施方式中,组合物被配置用于向受试者口服给药。
[0143]
在某些实施方式中,本发明提供了用于将细菌结肠递送至受试者的方法,包括向受试者给药这样的包括与细菌结合的(例如,复合的、缀合的、包封的、吸收的、吸附的、混合的)益生元制剂(例如,基于凝胶的菊糖)。
[0144]
在某些实施方式中,本发明提供了包括与一种或多种益生菌细胞结合的(例如,复合的、缀合的、包封的、吸收的、吸附的、混合的)益生元制剂的组合物。在某些实施方式中,本发明提供了用于提高受试者消化系统中益生菌生物生长的方法,包括向受试者(例如哺乳动物受试者;人受试者)给药这样的组合物。
[0145]
在一些实施方式中,益生元制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、菊糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
[0146]
在一些实施方式中,益生元化合物是基于凝胶的。在一些实施方式中,益生元化合物是基于凝胶的菊糖。
[0147]
在一些实施方式中,一种或多种益生菌细胞在向受试者给药后能够改变受试者的肠道微生物组。
[0148]
在一些实施方式中,组合物被配置用于向受试者口服给药。
[0149]
在一些实施方式中,一种或多种益生菌细胞包括有益菌。在一些实施方式中,有益菌包括以下项的一种或多种:酿酒酵母、凝结芽孢杆菌、地衣芽孢杆菌、枯草芽孢杆菌、角双歧杆菌、动物双歧杆菌、两歧双歧杆菌、短双歧杆菌、婴儿双歧杆菌、乳酸双歧杆菌、长双歧杆菌、屎肠球菌、粪肠球菌、嗜酸乳杆菌、食淀粉乳杆菌、消化乳杆菌、保加利亚乳杆菌、干酪乳杆菌干酪亚种、干酪乳杆菌代田株、弯曲乳杆菌、德氏乳杆菌乳酸亚种、发酵乳杆菌、香肠乳杆菌、格氏乳杆菌、瑞士乳杆菌、约氏乳杆菌、乳酸乳杆菌、副干酪乳杆菌、戊糖乳杆菌、植物乳杆菌、罗伊氏乳杆菌、鼠李糖乳杆菌(乳杆菌gg)、清酒乳杆菌、唾液乳杆菌、乳酸乳球菌、耐热乳杆菌、黏膜乳杆菌、变异微球菌、乳酸片球菌、戊糖片球菌、乳酸片球菌、嗜盐片球菌、粪链球菌、嗜热链球菌、肉糖葡萄球菌和木糖葡萄球菌。
[0150]
在一些实施方式中,组合物是糖包衣片剂、凝胶胶囊、凝胶、乳剂、片剂、扁胶囊、水凝胶、纳米纤维凝胶、电纺纤维、食品棒、糖果点心、发酵乳、发酵乳酪、口香糖、粉末或牙膏。
[0151]
在某些实施方式中,本发明提供了包括基于凝胶的益生元制剂的组合物。在一些实施方式中,组合物被配置用于口服摄取。在一些实施方式中,组合物是糖包衣片剂、凝胶胶囊、凝胶、乳剂、片剂、扁胶囊、水凝胶、纳米纤维凝胶、电纺纤维、食品棒、糖果点心、发酵乳、发酵乳酪、口香糖、粉末或牙膏。
[0152]
在一些实施方式中,益生元制剂包括选自以下项的一种或多种益生元化合物:低聚果糖、短链低聚果糖、菊糖、低聚异麦芽糖、反式低聚半乳糖、果胶、低聚木糖、低聚壳聚糖、β-葡聚糖、阿拉伯胶改性淀粉、抗性马铃薯淀粉、瓜尔胶、豆胶、明胶、甘油、聚葡萄糖、d-塔格糖、金合欢纤维、角豆、燕麦和柑橘纤维。
[0153]
在一些实施方式中,基于凝胶的益生元制剂与一种或多种益生菌生物结合。在一些实施方式中,一种或多种益生菌生物选自乳杆菌属物种和双歧杆菌属物种。在一些实施方式中,基于凝胶的益生元制剂与一种或多种噬菌体结合,该一种或多种噬菌体特异性于:鲍特菌、疏螺旋体、布鲁氏菌、弯曲杆菌、衣原体和嗜衣体属、梭菌、棒状杆菌、肠球菌、埃希菌、弗朗西丝菌、嗜血杆菌、螺杆菌、军团菌、钩端螺旋体、李斯特菌、分枝杆菌、支原体、奈瑟菌、假单胞菌、立克次体、沙门菌、志贺菌、葡萄球菌、链球菌、密螺旋体、弧菌和耶尔森菌。在一些实施方式中,一种或多种益生菌生物选自嗜酸乳杆菌、食淀粉乳杆菌、短乳杆菌、干酪乳杆菌、干酪乳杆菌鼠李糖亚种(乳杆菌gg)、高加索乳杆菌、卷曲乳杆菌、德氏乳杆菌保加利亚亚种(保加利亚乳杆菌)、发酵乳杆菌(酶乳杆菌)、格氏乳杆菌、瑞士乳杆菌、约氏乳杆菌、乳酸乳杆菌、莱希曼氏乳杆菌、副干酪乳杆菌、植物乳杆菌、罗伊氏乳杆菌或鼠李糖乳杆菌。
[0154]
这样的方法不限于给药能够提升受试者肠道微生物组的丰富度和多样性的药剂的特定方式。在一些实施方式中,药剂优选口服给药(例如,通过口服灌胃)。然而,给药可以通过任何合适的给药途径,包括颊、牙、宫颈内、肌内、吸入、颅内、淋巴管内、肌内、眼内、腹腔内、胸膜内、鞘内、气管内、子宫内、血管内、静脉内、膀胱内、鼻内、眼、耳、胆道灌注、心脏灌注、牙周、直肠、脊髓皮下、舌下、局部、阴道内、经皮、输尿管或尿道。剂型可以是气溶胶(包括计量气溶胶)、咀嚼棒、胶囊、包含包衣小丸的胶囊、包含延迟释放小丸的胶囊、包含延长释放小丸的胶囊、浓缩物、乳膏、增强乳膏、栓剂乳膏、圆片、敷料、酏剂、乳剂、灌肠剂、延长释放纤维、延长释放膜、气体、凝胶、计量凝胶、颗粒、延迟释放颗粒、泡腾颗粒、口香糖、植
入物、吸入剂、注射剂、注射脂质复合物、注射脂质体、插入物、延长释放插入物、子宫内装置、果冻、液体、延长释放液体、洗剂、增强洗剂、洗发水洗剂、油、软膏、增强软膏、糊剂、锭剂、团粒、粉末、延长释放粉末、计量粉末、环、洗发水、肥皂溶液、泥浆化溶液(solution for slush)、溶液/滴剂、浓缩溶液、凝胶形成溶液/滴剂、海绵、喷雾剂、计量喷雾剂、栓剂、混悬剂、混悬剂/滴剂、延长释放混悬剂、拭子、糖浆、片剂、咀嚼片剂、包含包衣颗粒的片剂、延迟释放片剂、分散片剂、泡腾片剂、延长释放片剂、口服崩解片剂、填塞物、胶带或糖锭/锭片剂。
[0155]
眼内给药可以包括通过注射(包括玻璃体内注射),通过滴眼剂和通过经巩膜递送给药。
[0156]
给药也可以通过包括在哺乳动物的饮食中,诸如在用于人或伴生动物的功能性食品中。
[0157]
如前所述,优选地这样的能够提升受试者肠道微生物组的丰富度和多样性的药剂是被口服给药的。这样的制剂优选被包封并与合适的载体配制在固体剂型中。合适的载体、赋形剂和稀释剂的一些实例包括乳糖、右旋糖、蔗糖、山梨糖醇、甘露糖醇、淀粉、阿拉伯胶、磷酸钙、藻酸盐、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、明胶、糖浆、甲基纤维素、甲基苯甲酸丙酯和羟基苯甲酸丙酯、滑石、镁、硬脂酸盐、水、矿物油等。制剂可以额外地包括润滑剂、润湿剂、乳化剂和助悬剂、防腐剂、甜味剂或芳香剂。通过采用本领域公知的程序,可以配制组合物以便在向患者给药之后提供活性成分的快速、持续或延迟释放。制剂还可以包含减少蛋白水解降解并促进吸收的物质,诸如例如表面活性剂。
[0158]
特定剂量可以根据患者的大概体重或体表面积或所待占据的身体空间的体积来计算。剂量还将取决于所选择的特定给药途径。确定治疗的适当剂量所需的计算的进一步细化由本领域普通技术人员常规进行。这样的计算可以由本领域技术人员根据测定配制剂(诸如已在别处描述的某些化合物(参见例如,howitz et al.,nature 425:191-196,2003和论文随附的补充信息))中的活性进行,而无需过度实验。可以结合标准剂量响应研究确定确切的剂量。应当理解,实际给药的组合物的量将由从业者根据相关情况确定,该相关情况包括待治疗的一种或多种病症、待给药的组合物的选择、个体患者的年龄、体重和响应、患者症状的严重程度以及所选择的给药途径。
[0159]
本发明还提供了试剂盒,其包括能够提升受试者肠道微生物组的丰富度和多样性的药剂(例如,基于纤维的益生元),以及一种或多种疫苗(例如,癌症疫苗)(例如,用于治疗和/或预防感染性病原体的疫苗)和癌症免疫疗法(例如,ici抑制剂)。试剂盒可以任选地包含其他治疗剂。
[0160]
实验
[0161]
提供以下实施例以证明并进一步说明本发明的某些优选实施方式,并且不应被解释为限制其范围。
[0162]
实施例i.
[0163]
本实施例展示了免疫检查点阻断剂与益生元在预防性环境中的功效改善。
[0164]
在fda的列表中,选择了五种候选材料进行初步筛选。存在于松果腺和胃肠道中的褪黑激素调节睡眠周期和昼夜节律。表没食子儿茶素没食子酸酯(egcg)是植物中的天然抗氧化剂。岩藻多糖、低聚果糖和菊糖是广泛用于食品和膳食补充剂的植物多糖。首先测试了
这些候选材料以预防方式改善α-pd-1疗法的抗肿瘤功效的能力。将wt balb/c小鼠在肿瘤接种前一周经由口服灌胃用这些材料治疗(图1a)。与单独用α-pd-1相比,所有这些药剂与α-pd-1疗法联合均表现出更强的抗肿瘤功效,并且菊糖表现出最佳的功效(图1b和c)。菊糖与α-pd-1的联合延长了动物的存活,60%的小鼠在第50天仍存活(图1d)。
[0165]
接下来测试这些材料对全身免疫应答的作用。采用肿瘤特异性抗原的替代标志物,ct-26gp70(ah1)的mhc-i最小表位(h-2l
d-限制性spsyvyhqf(seq id no.:1))来量化外周血单核细胞(pbmc)中ah1特异性cd8
+ t细胞的频率。与单独用α-pd-1治疗相比,用与α-pd-1igg联合的菊糖和褪黑激素口服灌胃的小鼠诱导ah1特异性cd8
+ t细胞的频率是单独用α-pd-1治疗的1.7倍和1.8倍高(图1e和f)。
[0166]
实施例ii.
[0167]
本实施例描述了免疫检查点阻断剂与益生元在治疗环境中功效的改善。
[0168]
将菊糖确定为有希望的候选者后,接下来在治疗环境中对这些药剂进行了测试。在用ct-26细胞接种balb/c小鼠后,从第7天开始用口服灌胃治疗荷瘤小鼠(图2a)。与预防性治疗一致,菊糖联合α-pd-1igg疗法表现出最强的抗肿瘤功效(图2b和c),并延长了动物存活(图2d)。在第18天和第24天,菊糖还引起了pbmc中显著更高的ah1特异cd8
+ t细胞(图2e-g)。
[0169]
实施例iii.
[0170]
本实施例描述了菊糖和褪黑激素(melanotinin)的剂量效应。
[0171]
接下来检查菊糖和褪黑激素的剂量效应,它们是上面确定的前2种候选物。将菊糖和褪黑激素的剂量减半(即,菊糖60mg和褪黑激素50mg/kg)并没有损害它们与α-pd-1联合对抗肿瘤生长的功效(图3a、b),表明了菊糖和褪黑激素的相对宽的治疗窗口。在pbmc中ah1特异性cd8+ t细胞的频率中也发现了类似的结果(图3c、d)。由于肿瘤浸润淋巴细胞在免疫疗法的结果中起关键作用,因此检查了肿瘤微环境中的t淋巴细胞。与单独的α-pd-1igg相比,与α-pd-1igg联合的菊糖或褪黑激素治疗显著增强了t细胞的肿瘤内浸润(图3e-h)。
[0172]
实施例iv.
[0173]
本实施例描述了肠道微生物组的变化。
[0174]
经由16s rdna测序分析检查治疗期间肠道微生物组的组成。与pbs组相比,这些材料的口服灌胃增加了操作分类单位(out,图4a)以及逆辛普森多样性值(图4b),表明这些治疗提升了肠道微生物组的丰富度和多样性。非度量多维尺度分析(nmds)清楚地示出,与pbs或游离α-pd-1相比,这些材料的口服灌胃导致微生物群落结构的明显聚集,特别是对于菊糖(图4c)。科/属水平中的进一步分析示出,与单独α-pd-1或pbs组相比,口服给药菊糖,随后进行α-pd-1治疗增加了阿克曼菌属、乳杆菌属、瘤胃球菌属和丁酸球菌属的相对丰度(图4d-f、图5)。最近的研究已经示出,乳杆菌属和阿克曼菌属可以改善荷瘤小鼠中免疫检查点阻断的抗肿瘤功效,而丁酸球菌属和瘤胃球菌属已知会生成包括丁酸在内的短链脂肪酸(scfa)作为代谢物。已知微生物组代谢物scfa,尤其是丁酸,改善免疫应答以及抑制炎症。令人惊讶的是,与pbs组相比,还发现游离α-pd-1治疗将罗氏菌属(另一种重要的产丁酸菌)的丰度显著降低至几乎0%(图4f)。候选药剂,尤其是菊糖的口服灌胃增加了肠道中罗氏菌属的丰度。粪便团粒中scfa的分析进一步证实,菊糖的口服灌胃增加了乳酸、丙酸和丁酸的浓度(图4g)。相比之下,与pbs组相比,游离α-pd-1组具有较低的丙酸和丁酸。此外,拟合曲
线和斯皮尔曼相关系数分析示出,肿瘤大小与阿克曼菌属、乳杆菌属、罗氏菌属、瘤胃球菌属和丁酸球菌属的相对丰度呈负相关(图4h),表明这些共生细菌对癌症治疗的有益作用。nmds和微生物组组成结果进一步清楚地表明,在与α-pd-1联合治疗期间,游离菊糖和褪黑激素(而不是α-pd-1)在操纵微生物群落结构中起主导作用(图5)。
[0175]
实施例v.
[0176]
该实施例证明菊糖凝胶进一步改善了免疫检查点阻断的功效。
[0177]
鉴于菊糖在这些候选材料中与α-pd-1示出出最好的功效,并且降低的剂量(60mg/剂量)没有明显损害该功效,因此在以下研究中选择60mg/剂量的菊糖。经由加热-冷却方法制备菊糖凝胶,这确保了易于大规模生产(图6a)。该凝胶是可注射的以用于口服灌胃(图7a)。扫描电子显微镜(sem)显示菊糖凝胶表现出类似织物的表面形态(图6a)。还原糖测定验证了菊糖凝胶在胃样酸性环境中2小时的稳定性(图7b)。将联合α-pd-1的抗肿瘤作用与游离菊糖或菊糖凝胶进行比较。引人注目的是,菊糖凝胶表现出比游离菊糖显著更高的肿瘤抑制功效(图7b)。菊糖凝胶组的存活率显著延长,并且60%的小鼠完全根除已形成的肿瘤(图6c)。这些幸存者在用1.5
×
105ct26肿瘤细胞进行肿瘤再次攻击时受到保护(图6d),证明了对肿瘤复发的长期免疫。四聚物染色测定显示,与游离菊糖相比,菊糖凝胶灌胃后pbmc中ah1特异性cd8
+ t细胞的频率显著提升(图6e)。同时,肿瘤浸润cd45
+
cd8
+ t细胞、cd45
+
cd4
+ t细胞以及成熟dc细胞(cd86
+
cd11c
+
)的量显著增加(图6f)。应注意,与菊糖组相比,菊糖凝胶组中的这些肿瘤浸润cd8
+ t细胞在改善细胞表面的ah1-四聚物
+
和减少pd-1
+
生物标志物方面表现出更好的抗肿瘤功能。脾中的ifn-γelispot测定进一步揭示,菊糖凝胶联合α-pd-1引起cd8
+ t细胞中强烈的ifn-γ表达(图6g和h),其分别是菊糖+α-pd-1组和α-pd-1组的3.5倍和4.6倍高。此外,α-cd8耗竭抗体的给药完全消除了菊糖凝胶+α-pd-1的抗肿瘤功效。与此形成鲜明对比的是,α-asialo gm1或α-cd4抗体的给药不影响菊糖凝胶+α-pd-1疗法的治疗功效(图6i),揭示了cd8
+ t细胞是抑制并根除肿瘤的关键淋巴细胞,而不是cd4
+ t细胞或nk细胞。
[0178]
实施例vi.
[0179]
该实施例表明,在结肠中具有改善的保留的菊糖凝胶改变了肠道微生物组。
[0180]
采用fitc-菊糖合成fitc标记的菊糖凝胶。体内胃肠道保留成像示出,与游离菊糖组相比,菊糖凝胶组在灌胃后4.5小时表现出改善的盲肠和结肠中的积聚和保留(图8a、b)。在fitc-菊糖或fitc-菊糖凝胶灌胃后的预设时间点收集粪便团粒,并证实与菊糖相比,fitc-菊糖凝胶的保留增加(图8c)。使用菊糖检测试剂盒证实了这些结果,并且曲线下面积值清楚地表明与菊糖相比,菊糖凝胶在结肠中更好地保留(图8d)。
[0181]
菊糖凝胶的这种延长保留导致增加的otu和逆辛普森多样性值(图8e)。nmds结果和科水平的微生物组分析示出,菊糖和菊糖凝胶组之间的微生物群落结构在一定程度上发生了变化(图8f)。属水平的微生物组组成揭示,与菊糖组相比,菊糖凝胶灌胃后阿克曼菌属、瘤胃球菌属和罗氏菌属的相对丰度显著增加(图8g、h),而乳杆菌属和丁酸球菌属的丰度在这两组之间是相当的。
[0182]
为了证实肠道微生物组在抗肿瘤功效中的作用,在肿瘤接种前给予在无特定病原体(spf)饲养条件下的小鼠广谱抗生素(氨苄青霉素+黏菌素+链霉素)7天,并且从肿瘤接种后第5天开始持续抗生素治疗。广谱抗生素治疗显著损害了菊糖凝胶联合α-pd-1的抗肿瘤
作用(图8i),证明了肠道微生物组在菊糖凝胶联合α-pd-1疗法中的关键作用。
[0183]
实施例vii.
[0184]
该实施例展示了菊糖凝胶在第二个肿瘤模型中的治疗功效。
[0185]
使用c57bl/6小鼠作为另一种小鼠品系,在mc38肿瘤模型中评价菊糖凝胶系统(图9a)。先前的研究示出,在h-2db分子的情况下,mc38细胞在adpgk蛋白内具有突变的新表位(asmtnrelm(seq id no.:2)
→
asmtnmelm(seq id no.:3)突变)。与α-pd-1、菊糖凝胶或游离菊糖+α-pd-1相比,经由ifn-γelispot测定,菊糖凝胶联合α-pd-1诱导了脾cd8
+ t细胞中更高的ifn-γ表达(图9b、c)。结果,菊糖凝胶显著减慢了肿瘤生长并延长了荷瘤小鼠的存活(图9d、e)。
[0186]
实施例viii.
[0187]
该实施例证明了菊糖凝胶加α-pd-1疗法的安全性。
[0188]
评价了菊糖凝胶系统的安全性。与pbs治疗的小鼠相比,用菊糖凝胶加α-pd-1疗法治疗的小鼠在全血细胞计数和血液化学组中没有表现出任何变化。另外,在菊糖凝胶加α-pd-1后,主要器官的h&e染色未示出明显炎症或组织损伤的任何体征,表明联合疗法的安全性。
[0189]
实施例ix.
[0190]
该实施例提供了实施例i-viii中使用的材料和方法。
[0191]
菊糖水凝胶的制备和表征
[0192]
将300mg菊糖(sigma-aldrich)溶解在1.2ml di水中。然后将菊糖溶液在70℃加热5min并在室温下保持12h以获得菊糖凝胶。对于sem观察,将菊糖凝胶在液氮中快速冷冻并冻干。然后将样品用金溅射包衣30s。使用mira3 tescan(电压15kv)对样品进行可视化。为了模拟菊糖凝胶在胃酸环境中的潜在降解,将菊糖凝胶在强酸性水(ph 2)中温和搅拌孵育2或24h。将样品离心并收集上清液。将二硝基水杨酸(dns)方法(miller,1959)用于定量分析上清液中的还原糖。使用酶标仪在540nm处测量显色强度。
[0193]
体内癌症免疫疗法
[0194]
在联邦、州和地方的指南下护理小鼠。所有实验动物程序均经密歇根大学安娜堡分校(university of michigan,ann arbor)的动物使用和护理大学委员会(university committee on use and care of animal,ucuca)批准。从杰克逊实验室获得6-8周龄的雌性c57bl/6或balb/c小鼠。在第0天通过皮下注射在右侧腹,balb/c小鼠每只小鼠接种1.5
×
105个ct26细胞,而c57bl/6小鼠每只小鼠接种1.2
×
106个mc38细胞。在第5天,将荷瘤小鼠随机分配到不同的组。对于预防性抗肿瘤研究,小鼠接受褪黑激素(100mg/kg体重/剂量)、egcg(100mg/kg体重/剂量)、岩藻多糖(200mg/kg体重/剂量)、低聚果糖(120mg/剂量)或菊糖(120mg/剂量)的口服灌胃3次,持续一周,之后进行肿瘤接种。肿瘤接种后,小鼠在第一周接受口服灌胃3次,随后每周5次。在肿瘤接种后第10、14、18和22天,向小鼠i.p.注射α-pd-1抗体(100μg/剂量)。对于治疗性疗法,小鼠如上所示在第0天接种肿瘤细胞,并在肿瘤接种后第7天开始通过口服灌胃所示样品来治疗。小鼠每周接受指定样品的口服灌胃(与预防性抗肿瘤研究相同的剂量)5次,同时在肿瘤接种后第11、15、19和23天注射α-pd-1抗体(100μg/剂量)。在预设时间测量肿瘤大小,并且将肿瘤体积计算为长度
×
宽度2。对于菊糖凝胶的抗肿瘤研究,菊糖凝胶或菊糖的剂量为60mg/剂量。对于存活研究,当肿瘤大小达到1.5cm直
径或当动物因体重严重减轻(》20%)或具有的肿瘤溃疡超过肿瘤体积的50%而濒临垂死时,将荷瘤小鼠安乐死。在抗体耗竭研究中,ct26荷瘤小鼠接受了用菊糖凝胶(60mg/剂量)和α-pd-1治疗的口服灌胃,如上所述。cd8 t细胞、cd4 t细胞和nk细胞分别通过在第8、11和16天i.p.给药200μg/剂量的抗cd8(bioxcell,克隆2.43,#bp0061)、抗cd4(bioxcell,克隆gk1.5,#bp0003-1)或抗asialo gm1(wako chemicals usa,inc,#986-10001)耗竭。
[0195]
pbmc中的四聚物分析
[0196]
在预设时间收集外周血单个核细胞(pbmc)以分析体循环中的肿瘤抗原特异性cd8
+ t细胞。将红细胞裂解,并且将剩余细胞用抗cd16/32抗体封闭10min,并用肽-mhc四聚物(包括h-2l
d-限制的spsyvyhqf(seq id no.:1)或h-2d
b-限制的asmtnmelm(seq id no.:3))染色。两种四聚物均由nih tetramer core facility提供。还将细胞用抗cd8-apc(bd biosciences,#553035)和dapi染色以进行流式细胞术分析。
[0197]
肿瘤微环境分析
[0198]
在用各种样品处理后,在预设时间点切除肿瘤组织以分析肿瘤浸润t细胞。切除肿瘤组织,切成小块,并与iv型胶原酶(1mg/ml)和dna酶i(0.1mg/ml)一起温育,伴随轻轻摇动。30min后,细胞悬浮液通过70-μm过滤器过滤。将细胞用facs缓冲液洗涤并用抗cd16/32抗体封闭。然后用各种抗体(cd4单克隆抗体(gk1.5)-pe(ebioscience)、apc-抗cd45大鼠单克隆抗体(克隆:30-f11)、fitc-抗cd45大鼠单克隆抗体(克隆:30-f11)、fitc-大鼠抗小鼠cd8a克隆53-6.7(bd biosciences)、pe标记的h-2l
d-限制的spsyvyhqf(seq id no.:1)、fitc-抗cd86大鼠单克隆抗体(克隆:gl-1,biolegend)、pe-cd11c亚美尼亚仓鼠抗小鼠(克隆:n418,ebioscience)、pe-cy7-抗小鼠pd-1(克隆:29f.1a12,biolegend)、fitc-cd44大鼠抗人/小鼠(克隆:im7,ebioscience)、pe-cy7-cd62l单克隆抗体(mel-14)(ebioscience)、pe-tcf1/tcf7(c63d9)兔mab(cell signaling technology,#14456)、pe-cy7-抗小鼠cd86(克隆:gl1,bd bioscience)、fitc抗小鼠/人cd11b(m1/70,biolegend)、pe-抗小鼠f4/80(bm8,biolegend)或apc抗小鼠cd206(mmr,biolegend))染色细胞。将细胞洗涤并用dapi、7-aad或efluor 450染色以进行流式细胞术分析。
[0199]
肠道微生物组分析
[0200]
荷瘤小鼠接受上述治疗。在第20天,收集粪便团粒并在-80℃下储存,之后进行肠道微生物分析。微生物组dna分离和16s rrna测序两者均由密歇根大学微生物系统分子生物学实验室(university of michigan microbial systems molecular biology laboratory)完成。使用qiagen magattract power microbiome试剂盒从小鼠粪便样品中分离微生物dna。使用由kozich et al.(1)开发的条形码双索引引物从提取的dna中扩增16s rrna编码基因的v4区域。简而言之,特异性于16s rrna基因的v4区域的条形码双索引引物扩增了dna。pcr条件如下:95℃ 2min,以下的30个循环:95℃ 20s,55℃ 15s,72℃ 5min,以及72℃ 10min。扩增子文库(~399bp)的大小由agilent bioanalyzer确认。然后根据制造商的说明,使用500循环miseq v2试剂盒(目录号ms-102-2003)在illumina miseq平台上对合并的扩增子文库进行测序,修改是添加到试剂盒中的具有自定义读取1/读取2的引物组和索引引物。将“preparing libraries for sequencing on the miseq”(部分15039740,rev.d)方案用于制备最终上样浓度为5.5pm并添加15%phix以在运行中产生多样性的文库。通过mothur处理了来自小鼠粪便收集物的微生物16s rrna基因测序数据。将
silva参考文件(第132版)用于比对序列,并以97%的序列同一性使用开放参考otu挑选方案。
[0201]
粪便ph和scfa测量
[0202]
在肿瘤接种和治疗后第20天收集小鼠的新鲜粪便团粒并称重。粪便团粒在di水中均质化,并以3000x g离心5min。用ph计检测上清液的ph。对于scfa测量,使用milli-q水从粪便团粒中提取scfa。将溶液在10000x g(4℃)下离心5min以沉淀细菌和其他固体。收集上清液,并经由在密歇根大学生物站中的离子色谱法测量scfa。使用外标法测定scfa的浓度。
[0203]
ifn-γ elispot测定
[0204]
从肿瘤接种的第7天开始,ct26荷瘤balb/c小鼠经由口服灌胃接受指定的样品每周五次。在第11天、第15天和第19天,还将动物i.p.给药α-pd-1抗体(100μg)。在第23天,将动物安乐死,并使用ifn-γelispot测定法分析它们的脾的抗肿瘤t细胞应答。将elispot板用捕获抗体包被24h,并用dmem+10%fbs封闭2h。将这些脾细胞以2
×
105个活细胞/孔的密度添加到96孔板中。同时,添加ah1肽(spsyvyhqf(seq id no.:1),20μg/ml)以刺激脾细胞。采用离子霉素和pma作为阳性对照。18h后,用生物素化检测抗体,随后用链霉亲和素-hrp和aec底物试剂盒检测ifn-γ斑点。在密歇根大学癌症中心免疫学核心(cancer center immunology core of university of michigan)测量了ifn-γ斑点的数量。对于mc38荷瘤c57bl/6小鼠中的ifn-γelispot测定,以类似方式进行。将第20天获得的pbmc用于ifn-γelispot测定。
[0205]
菊糖水凝胶在胃肠道系统中的保留
[0206]
使用fitc-菊糖凝胶测量菊糖凝胶在胃肠道系统中的保留。为了制备fitc标记的菊糖水凝胶,将47.5mg菊糖和12.5mg fitc-菊糖(sigma-aldrich)混合在200μl的di水中。对于菊糖的体内成像,小鼠接受fitc标记的菊糖或菊糖凝胶的口服灌胃,并在预设时间点进行安乐死。收获胃、小肠、盲肠、结肠和直肠,用pbs洗涤,之后用ivis光学成像系统进行荧光成像。为了检测粪便团粒中的菊糖含量,将fitc标记的菊糖或菊糖凝胶口服灌胃给小鼠,并在预设时间点收集粪便团粒。将粪便团粒称重并重悬浮在di水中。然后将样品溶液离心,并使用酶标仪测量上清液的荧光强度。将荧光强度相对于1mg/ml粪便样品进行归一化。为了检测结肠中的菊糖含量,将小鼠用菊糖或菊糖凝胶(60mg/剂)灌胃,并在灌胃后的预设时间点安乐死。收获、称重、均质并离心结肠中的粪便团粒。将上清液稀释20倍并用于菊糖检测。根据制造商的方案,经由picoprobetm菊糖测定试剂盒(biovision)检测菊糖。
[0207]
抗生素水处理
[0208]
小鼠在接种肿瘤前一周接受包含抗生素的无菌饮用水。肿瘤接种后,动物接受正常饮水5天,以避免抗生素对肿瘤植入和形成的直接影响。5天后,荷瘤小鼠接受了具有抗生素的饮用水,以提醒研究。更换包含氨苄青霉素(0.3mg/ml)、链霉素(2.5mg/ml)和黏菌素(0.3mg/ml)的抗生素饮用水每周两次。
[0209]
生物安全评价
[0210]
将ct26荷瘤小鼠用上述方案治疗。第29天,采集血液样品进行全血细胞计数(cbc)(包括嗜酸性粒细胞、淋巴细胞、单核细胞、血小板、红细胞、血红蛋白、平均血小板体积、红细胞分布宽度(rdw)和平均红细胞血红蛋白(mch))。血清样品用于生化分析,该血清样品包括丙氨酸转氨酶(alt)、谷草转氨酶(ast)、血尿素氮(bun)、葡萄糖、胆固醇和肌酸磷酸激酶
(cpk)。第29天对小鼠惊醒安乐死,并收集肺、肝脏、脾、心脏和肾脏用于h&e染色。
[0211]
统计分析
[0212]
随机化后进行动物研究。通过配对或非配对t检验或者单因素或双因素方差分析(anova)来分析数据,随后用prism 8.0(graphpad software)进行多重比较检验。p《0.05被认为是统计学显著的。
[0213]
实施例x.
[0214]
本实施例展示了使用菊糖凝胶制剂递送细菌和益生菌的方法。
[0215]
对结肠靶向的益生菌递送以改善健康益处有强烈的研究兴趣。开发了使用基于益生元的凝胶制剂共同递送细菌(益生菌)的新策略。作为概念验证,将大肠杆菌用作模型细菌生物,并使用前面描述的菊糖凝胶制剂来封装和递送大肠杆菌。
[0216]
将表达gfp的大肠杆菌用于评估菊糖凝胶制剂中大肠杆菌的包埋和生长。菊糖凝胶中的大肠杆菌表现出四个阶段的典型的细菌生长模式(图10)。细胞密度与到达静止期之前的gfp表达成比例。由于营养物耗尽和代谢物的生成,细胞数量在静止期保持不变并且在延迟期暴跌,而荧光逐渐积累。这表明菊糖凝胶可以用于捕获大肠杆菌并保持其生存力。
[0217]
将培养皿中大肠杆菌的生长与菊糖凝胶中的进行了比较。大肠杆菌在菊糖凝胶包埋组和pbs对照组(即培养皿)之间示出可比较的荧光强度。菊糖凝胶在gfp波长处发出可忽略不计的自发荧光。
[0218]
当通过cfu计数比较大肠杆菌的生存力时,观察到菊糖凝胶中包埋的大肠杆菌表现出增加的生存力(表1)。菊糖凝胶组计算的cfu是pbs中获得的数量的3倍高。这表明菊糖凝胶可以捕获并促进细菌的生长。这些结果与先前实施例中示出的结果相结合,表明设计用于结肠保留的菊糖凝胶可以用于捕获细菌(益生菌)并将其递送至结肠组织。
[0219]
表1.分别在pbs中孵育和菊糖凝胶包封24小时后通过cfu计数测定细胞生存力。
[0220]
大肠杆菌@pbs大肠杆菌@菊糖凝胶1.61
×
108cfu/ml5.25
×
108cfu/ml
[0221]
实施例xi.
[0222]
该实施例描述了实施例x中使用的材料和方法。
[0223]
大肠杆菌培养和cfu计数 将大肠杆菌在补充有100μg/ml氨苄青霉素的胰酶大豆肉汤(tsb)培养基中在37℃,200rpm下培养过夜。测量600nm处的光密度。对细胞培养物进行10倍系列稀释液,并将稀释液涂抹在tsb琼脂板上,在37℃下培养12小时。通过每个稀释因子的数量计算cfu。
[0224]
菊糖凝胶制备和大肠杆菌封装 使用涡旋将菊糖(330mg/ml)悬浮在无菌pbs缓冲液中。将悬浮液加热至70℃持续5min,并且然后在室温下冷却10min。将密度为7.5
×
109cfu/ml的大肠杆菌培养物以大肠杆菌:菊糖=1:9的比率加入冷却的悬浮液中,获得最终浓度为7.5
×
108cfu@300mg/ml的大肠杆菌凝胶。
[0225]
实施例xii.
[0226]
图1-10示出了在从杰克逊实验室获得的babl/c小鼠中生成的结果。由于已知来自不同动物供应商的小鼠具有不同的肠道微生物组,因此进行了旨在验证菊糖凝胶加α-pd-1联合疗法对从其他动物供应商获得的小鼠的治疗功效的实验。如图13a中示出,将获自查理士河(charles river)和塔科尼农场(taconic farm)babl/c小鼠接种ct26肿瘤细胞并用菊
糖凝胶加α-pd-1联合疗法进行治疗。菊糖凝胶加α-pd-1联合疗法在获自查理士河和塔科尼农场的babl/c小鼠中发挥了抗肿瘤功效(图13b-c),因此示出该联合疗法的抗肿瘤功效不是供应商的特定作用。
[0227]
除了babl/c小鼠中的ct26肿瘤模型外,还进行了试图在其他肿瘤模型中验证这些结果的实验。菊糖凝胶(60mg/剂)加α-pd-1联合疗法还在携带mc-38结肠癌或b16f10黑素瘤的c57bl/6小鼠(杰克逊实验室)中生成了强烈的cd8
+ t细胞应答与强大的抗肿瘤功效(图13d-e),因此示出了该策略在多个小鼠品系的多个肿瘤模型中的实用性。
[0228]
实施例xiii.
[0229]
为了了解菊糖凝胶的组成对体内结果的影响,进行了使用各种聚合度(dp)的菊糖合成各种菊糖凝胶制剂的实验。
[0230]
材料和方法
[0231]
菊糖样品购自now foods、swanson health products、sigma-aldrich和orafti。
[0232]1h-nmr。将每5mg菊糖粉末溶解在600μl d2o中以制备1h-nmr样品。样品在agilent/varian 400mhz nmr光谱仪上运行,该光谱仪配备5mm one探头,具有多核能力,由主机软件vnmrj 3.2操作。如先前所述,通过1h-nmr光谱计算dp(t.barkhatova,m.nazarenko,m.kozhukhova,i.khripko,foods and raw materials 2015,3)。
[0233]
maldi-tof-ms。将每个10mg菊糖样品溶解在1.00ml水、0.25ml甲醇和0.25ml乙腈中。然后将2μl样品溶液与基质溶液混合,并点样到目标板上。基质溶液是溶解在具有0.1%tfa的50/50乙腈/水中的浓度为4mg/ml的2,5-dhb。样品在bruker autoflex speed上以线性模式运行。将仪器用2,5-dhb基质中的牛胰岛素和细胞色素c的混合物进行质量校准。
[0234]
菊糖凝胶的制备。将期望重量的菊糖粉末溶解在1.0ml去离子水中。然后将菊糖溶液在70℃下与1000rpm振荡下加热5min,并在室温下保持过夜以用于糊化。
[0235]
流变测试。用于流变学测试的菊糖凝胶(样品3和5)如上所述制备,具有的浓度为300mg菊糖在1.0ml去离子水中。将菊糖(3)悬浮液以相同浓度制备,但没有加热和冷却程序。将菊糖凝胶(样品1)用相同的糊化步骤制备,但浓度为700mg菊糖在1.0ml去离子水中。在25℃下用由anton paar制造的配备有具有0.100mm间隙的平行pp60 ti板的mcr702 twindrive流变仪进行测量。所有测试均在1%的应变下进行,该应变在研究样品的线性粘弹性区域范围内。g'代表弹性模量,g”代表粘性模量。
[0236]
粪便样品中的菊糖含量。为了检测粪便样品中的菊糖含量,用菊糖凝胶(60mg/剂)对小鼠口服灌胃。并在灌胃后的预设时间点(0、2.5、5、7.5、10和12.5h)收集小鼠的新鲜粪便团粒并称重。将每个粪便团粒在800μl di水中均质化,并在20000rcf下离心10min。然后将上清液稀释25倍,用于根据制造商的说明用picoprobe
tm
菊糖测定试剂盒(biovision)定量菊糖含量。
[0237]
体内研究。将ct26荷瘤balb/c小鼠(雌性,jackson laboratory,6-8周龄)随机分配到不同组进行治疗。对小鼠灌胃菊糖凝胶(60mg/剂)每五天四次,并且经由腹腔内注射给药α-pd-1抗体(100μg/剂)每四天一次。从肿瘤接种后第5天开始,每隔一天测量肿瘤体积和小鼠体重。将肿瘤体积计算为(长度
×
宽度2)/2。
[0238]
统计分析。将graphpad prism 8用于分析统计数据。结果表示为平均值
±
sem。通过双因素anova与bonferroni多重比较检验分析组间差异。对于p值*p《0.05、**p《0.01
和***p《0.001,差异被认为是显著的。
[0239]
结果
[0240]
从不同的公司获得具有不同聚合度(dp)的菊糖样品,并通过1h-nmr进行分析(图14)。1h-nmr光谱分析揭示以下(图14)。菊糖样品#1具有平均dp≈7,mw≈1314da。菊糖样品#2具有平均dp≈10,mw≈1800da。菊糖样品#3具有平均dp≈23,mw≈3906da。菊糖样品#4具有平均dp≈26,mw≈4392da。菊糖样品#5具有平均dp≈28,mw≈4716da。
[0241]
此外,maldi-tof-ms分析揭示菊糖样品#1、#2、#3、#4和#5具有的摩尔质量在990至6336da之间(图15)。然而,在约990-2124da的峰强度的增加表明普遍存在5至12之间的较低dp菊糖链。可能的是,具有低dp的菊糖链较是更短的且更容易被激发而被检测到,而具有较高dp的长菊糖链链彼此紧密缠绕,并且不太可能从底物上被激发,从而导致maldi-tof-ms分析的信号强度较低。
[0242]
接下来进行实验,以使用具有各种dp的这些菊糖样品检查菊糖凝胶的形成。如图16中示出,与具有较高dp的菊糖样品(样品3-5)相比,具有dp 7和dp 10的菊糖样品(样品1和2)在加热前更易溶于水。对于在相同条件下的菊糖凝胶形成,与具有较高dp的其他四个菊糖样品相比,具有dp 7的菊糖样品1需要高的多的浓度的菊糖(700mg/g水)。具有最高dp 28的菊糖样品5在水中具有菊糖浓度甚至低至100mg/g也能够形成菊糖凝胶。这些结果示出,具有较高dp的菊糖在水中的溶解度较低,并且形成菊糖凝胶所需的浓度较低。
[0243]
菊糖的dp对凝胶的流变性也具有影响。在图17中,随着dp从7(样品1)上升到28(样品5),弹性模量(g')和粘性模量(g”)两者都增加至约10倍。与菊糖样品1和5相比,菊糖样品3呈现的g'和g”处于中间值。与游离菊糖溶液相比,由菊糖样品1、3和5形成的所有三种菊糖凝胶具有更大的g'和g”值。这些结果表明,这些样品更像固体而不是液体,证实了菊糖凝胶的成功形成。
[0244]
接下来进行了评价各种菊糖凝胶制剂在体内的结肠保留行为的实验。用具有各种dp的菊糖凝胶口服灌胃幼稚小鼠,并随着时间的推移分析粪便样品的菊糖含量。如图18中示出,具有较低dp的菊糖凝胶具有较早的峰值时间,菊糖样品1为灌胃后6.17h,菊糖样品2为灌胃后5.38h。并且对于具有较高dp的菊糖凝胶,观察到更长的峰值时间,菊糖样品3为7.73h,菊糖样品5为10.25h。此外,关于曲线下面积,随着dp的升高,粪便中的相对总菊糖含量逐渐下降。这些表明具有较高dp的菊糖凝胶延长了菊糖在胃肠道中的保留时间,这可能进一步增加肠道微生物区系对菊糖的利用。
[0245]
接下来进行了评估各种菊糖凝胶制剂(即用dp 7、10、23和28形成的菊糖凝胶)的治疗功效的实验。将携带s.c.侧腹ct26肿瘤的balb/c小鼠经口灌胃dp可变的菊糖凝胶(60mg/剂)加腹腔给药α-pd-1(100ug/剂)来治疗。每隔一天记录肿瘤体积和小鼠体重。尽管α-pd-1单独治疗组表现出中等的抗肿瘤功效,但α-pd-1治疗联合由dp 10或dp 23形成的菊糖凝胶表现出改善的抗肿瘤功效(图19)。值得注意的是,与具有dp 10或dp23的菊糖凝胶相比,具有dp 28的菊糖凝胶表现出显著增强的抗肿瘤功效(图19)。还观察到具有7的低dp的菊糖凝胶似乎降低了α-pd-1疗法的抗肿瘤功效。这些结果表明,菊糖凝胶的组成在α-pd-1疗法的抗肿瘤功效中起主要作用,并且具有较长dp的菊糖凝胶表现出优异的抗肿瘤功效,这可能是由于延长了在胃肠道中的保留时间,如图18中示出。在用各种菊糖凝胶制剂加α-pd-1疗法治疗的所有动物中,未观察到主要毒性或者动物体重的任何负面变化(图20),表
明菊糖凝胶加α-pd-1联合疗法的安全性。
[0246]
实施例xiv.
[0247]
接下来进行了检查菊糖浓度和温度对菊糖凝胶形成的影响的实验。首先将具有平均dp 23的菊糖(sigma)与水混合,得到15、20、25和30%w/v的期望浓度。将混合物分别加热至40、50、60、70℃持续5分钟。在室温下冷却过夜后,通过翻转eppendorf管来检查凝胶形成。对于给定dp 23的菊糖,较高的菊糖浓度导致菊糖凝胶形成(图21)。在凝胶化过程期间应用较高的温度会促进菊糖凝胶的形成(图21)。这些结果示出了菊糖凝胶形成的浓度和温度依赖性。
[0248]
实施例xv.
[0249]
接下来进行了使用马铃薯淀粉(另一种益生元天然纤维)检查凝胶形成的实验。检查了马铃薯淀粉浓度对凝胶形成的影响。将食品级马铃薯淀粉(bob's red mill)在水中以0.1、0.5、2.5和5%w/v的期望浓度预水合,随后在70℃下温和搅拌。图22示出了马铃薯淀粉凝胶。当溶胀完成时,马铃薯淀粉在高于5%w/v的浓度下立即糊化。
[0250]
实施例xvi.
[0251]
接下来进行的实验涉及通过将菊糖与其他天然膳食纤维或药物赋形剂联合形成新的纤维凝胶。简而言之,通过首先将23%w/w菊糖连同其他赋形剂(包括抗性马铃薯淀粉、果胶、瓜尔胶、豆胶、明胶或甘油)混合来制造菊糖凝胶。其他天然纤维将为共生微生物区系提供额外的营养来源,而其他赋形剂在这些制剂中充当增稠剂。然后将混合物在70℃加热5分钟,随后在室温下冷却过夜。在制造过程期间,基于在水中的单独溶解,利用预溶解和干共混两者来添加赋形剂。图23示出了#1菊糖凝胶、包含抗性马铃薯淀粉的#2菊糖凝胶、包含瓜尔胶的#3菊糖凝胶、包含果胶的#4菊糖凝胶以及包含豆胶的#5菊糖凝胶的凝胶化过程。首先将这些成分在水中混合(上图),在70℃加热5分钟(中图),随后在室温下冷却过夜,从而形成纤维凝胶(下图)(图23)。
[0252]
接下来进行以下实验,该实验改变添加到菊糖凝胶中的天然纤维和赋形剂的量,并确定用于形成纤维凝胶的理想组合物。如图24中示出,对于包含菊糖含量为23%w/w的菊糖凝胶,它们可以可靠地添加以下量的天然纤维或药物赋形剂:5%马铃薯淀粉、2%果胶、0.5%瓜尔胶、1.0%豆胶、5.0%明胶或50%甘油(w/w)。指示的值是可以添加到23%w/w菊糖凝胶而不破坏凝胶形成的每种成分的最大量。
[0253]
接下来进行了测量这些优化的纤维凝胶的流变性的实验。流变学测量是在25℃下使用配备有具有0.100mm间隙的平行40mm板的mcr702twindrive流变仪(anton paar,usa)进行的。所有频率扫描测量均在1%的应变下进行,该应变在所研究制剂的线性粘弹性区域范围内。g'代表弹性模量,g”代表粘性模量。获得流动曲线,其作为25℃下10-1
至102s-1
范围的剪切速率的函数。报告的结果是至少3次重复的平均值(图25)。与纯菊糖凝胶相比,如通过g'和g”的较低值所示出,所有测试的新纤维凝胶制剂都表现出较弱的凝胶强度。然而,菊糖凝胶联合马铃薯淀粉在粘度方面表现出增加至~10倍。
[0254]
通过援引并入
[0255]
本文提到的每份专利文件和科学文献的完整公开均通过援引并入本文用于所有目的。
[0256]
等同形式
[0257]
本发明可以在不背离其精神或本质特征下,以其他具体形式体现。因此,前述实施方式在所有方面均被认为是说明性的,而并非限制本文所述的本发明。因此,本发明的范围由所附权利要求书而不是上述说明书指明,并且在权利要求书的等价意义和范围内的所有改变均应包括在其中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1