用于治疗遗传性听力损失的腺相关病毒(AAV)系统的制作方法
用于治疗遗传性听力损失的腺相关病毒(aav)系统
1.相关申请的交叉引用
2.本技术根据35 u.s.c.
§
119(e)要求2019年9月30日提交的美国临时申请第62/907,834号的权益,该申请的内容通过引用以其整体并入本文。
3.序列表
4.本技术包括序列表,所述序列表已经以ascii格式电子提交并且在此通过引用以其整体并入。于2020年9月28日生成的所述ascii副本被命名为119561-01920_sl并且大小为31,079字节。
发明领域
5.本发明涉及基因疗法领域,包括用于在受试者或细胞中表达分离的多核苷酸的aav载体。本公开内容还涉及包含该多核苷酸的核酸构建体、启动子、载体和宿主细胞,以及将外源dna序列递送到靶细胞、组织、器官或生物体的方法,和用于治疗或预防遗传性听力损失的方法。
6.发明背景
7.基因疗法旨在改善遭受遗传突变或遭受基因表达谱中的畸变引起的获得性疾病的患者的临床结果。基因疗法包括治疗或预防由缺陷基因或者异常调控或表达(例如,表达不足或过表达)引起的医学状况,其可以导致紊乱、疾病、恶性肿瘤等。例如,由缺陷基因引起的疾病或紊乱可以通过向患者递送矫正性遗传物质来治疗、预防或改善,或者可以通过改变或沉默缺陷基因来治疗、预防或改善,例如,将矫正性遗传物质用于患者导致该遗传物质在该患者体内的治疗性表达。
8.基因疗法的基础是提供具有活性基因产物的转录盒(有时称为转基因或治疗性核酸),例如,该活性基因产物可以导致积极功能增益效应、负面功能损失效应或其他结果。这样的结果可归因于治疗性蛋白(诸如抗体、功能性酶或融合蛋白)的表达。基因疗法也可用于治疗由其他因素引起的疾病或恶性肿瘤。人类单基因紊乱可以通过向靶细胞递送和表达正常基因来治疗。矫正性基因在患者的靶细胞中的递送和表达可以经由多种方法进行,包括使用工程化病毒和病毒基因递送载体。
9.腺相关病毒(aav)属于细小病毒科(parvoviridae),并且更具体地属于依赖性细小病毒属(dependoparvovirus)。源自aav的载体(即,重组aav(ravv)或aav载体)在递送遗传物质方面具有吸引力,原因是(i)它们能够感染(转导)许多种非分裂和分裂细胞类型,包括肌细胞和神经元;(ii)它们缺少病毒结构基因,从而减弱宿主细胞对病毒感染的反应,例如,干扰素介导的反应;(iii)野生型病毒被认为在人类中是非致病性的;(iv)与能够整合到宿主细胞基因组中的野生型aav相比,复制缺陷型aav载体缺少rep基因并且通常以附加体(episome)的形式保持,从而限制插入性诱变或遗传毒性的风险;和(v)与其他载体系统相比,aav载体通常被认为是免疫原性相对较低并且因此不会触发严重的免疫应答(见ii),从而获得载体dna的持久性和潜在的治疗性转基因的长期表达。
10.非综合征性听力损失和耳聋(dfnb1;也称为间隙连接蛋白26耳聋)是常染色体隐
性的并且以先天性非进行性的轻度至严重的感觉神经性听力损伤为特征。gjb2基因编码间隙连接蛋白-26,它在耳蜗支持细胞中表达,形成控制钾稳态的间隙连接,这对于毛细胞的存活和功能以及正常听力是关键的。gjb2中的突变损害间隙连接和耳蜗稳态,导致毛细胞功能障碍和听力损失。
11.听力损失是最常见的遗传性感觉紊乱。在发达国家诸如美国,遗传突变是大多数幼儿听力损失的原因,据估计,在言语发育之前每500名儿童中就有1名受其影响(shearer等人,“hereditary hearing loss and deafness overview”,2017)。由于先天性听力损失是儿童中最普遍的慢性状况之一,因此常规进行新生儿筛查。在已检测到缺陷的那些病例中,通常随后进行遗传测试。
12.遗传测试可以用于通过鉴定gjb2中的双等位基因致病性变异来诊断dfnb1,该双等位基因致病性变异包括序列变异和改变间隙连接β-2蛋白(间隙连接蛋白26)表达的上游顺式调控元件中的变异。当在受影响的家庭成员中检测到引起dfnb1的gjb2致病性变异时,可以对有风险的亲属进行携带者测试、对风险增加的妊娠进行产前测试、以及进行植入前遗传诊断。smith&jones.nonsyndromic hearing loss and deafness,dfnb1.1998.在adam等人编著genereviews.university of washington,seattle;kemperman等人journal of the royal society of medicine 2002 95:171-177中。由于耳蜗是外科手术可及的并且局部应用于相对免疫保护的环境是可能的,因此使用病毒载体的基因疗法是用于治疗听力损失的有吸引力的方法。
13.然而,仍然需要有效的疗法来治疗感觉神经性听力损失。
14.发明概述
15.本文描述的技术涉及通过重组腺相关病毒(raav)载体表达间隙连接蛋白β2(gjb2)来治疗或预防听力损失的方法和组合物,其中该raav载体包含已经经过密码子优化的gjb2核酸序列。在一些实施方案中,raav载体包含已经经过密码子优化的gjb2核酸序列并组合了经测试gjb2表达最佳的启动子。因此,本公开内容涉及raav载体,通过该raav载体gjb2可以被包装用于靶向递送至罹患遗传性听力损失的患者,包括带有gjb2基因隐性或显性常染色体突变的患者。gjb2中的突变损害间隙连接和耳蜗的稳态,导致毛细胞功能障碍和听力损失。如本文描述的gjb2基因疗法的目标是恢复功能性间隙连接和保存毛细胞以改善听力。
16.根据一方面,本公开内容提供了包含编码gjb2的核酸序列的分离的多核苷酸。根据一些实施方案,核酸序列是非天然存在的序列。根据一些实施方案,核酸序列编码哺乳动物gjb2。根据一些实施方案,核酸序列编码人类gjb2、小鼠gjb2或大鼠gjb2。根据一些实施方案,核酸序列包含seq id no:10。根据一些实施方案,核酸序列是针对哺乳动物表达而经过密码子优化的。根据一些实施方案,核酸序列包含seq id no:11、seq id no:12或seq id no:13。
17.根据一些实施方案,核酸序列包含与seq id no:11至少85%相同的序列、与seq id no:12至少85%相同的序列、与seq id no:13至少85%相同的序列或与seq id no:18至少85%相同的序列。根据一些实施方案,核酸序列是针对在人类细胞、大鼠细胞或小鼠细胞中表达而经过密码子优化的。根据一些实施方案,核酸序列是cdna序列。根据一些实施方案,核酸序列还包含可操作地连接的血凝素(ha)c末端标签。根据一些实施方案,核酸序列
可操作地连接到启动子。根据一些实施方案,启动子是遍在活化性cba、小cba(smcba)、ef1a、casi启动子、耳蜗支持细胞启动子、gjb2表达特异性gfap启动子、小gjb2启动子、中gjb2启动子、大gjb2启动子或2-3个单独的gjb2表达特异性启动子的顺序组合。根据一些实施方案,启动子是经过优化的以驱动gjb2高表达。根据一些实施方案,核酸序列还包含含有土拨鼠肝炎病毒转录后调控元件(wpre)的可操作地连接的3’utr调控区。根据一些实施方案,核酸序列还包括可操作地连接的多腺苷酸化信号。根据一些实施方案,多腺苷酸化信号是sv40多腺苷酸化信号。根据一些实施方案,多腺苷酸化信号是人类生长激素(hgh)多腺苷酸化信号。根据一些实施方案,本文的任何方面和实施方案的多核苷酸还包含27个核苷酸的血凝素c末端标签;可操作地连接到经过优化以驱动gjb2高表达的以下启动子元件中的一个:(a)遍在活化性cba、小cba(smcba)、ef1a或casi启动子;(b)耳蜗支持细胞或gjb2表达特异性的1.68kb gfap、小/中/大gjb2启动子,或2-3个单独的gjb2表达特异性启动子的顺序组合;可操作地连接到包含土拨鼠肝炎病毒转录后调控元件(wpre)的3
’‑
utr调控区,随后是sv40或人类生长激素(hgh)多腺苷酸化信号。
18.根据另一方面,本公开内容提供了宿主细胞,该宿主细胞包含本文的任何方面或实施方案的多核苷酸。根据一些实施方案,宿主细胞是哺乳动物细胞。根据一些实施方案,宿主细胞是hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。根据一些实施方案,宿主细胞是bhk细胞。
19.根据另一方面,本公开内容提供了重组单纯疱疹病毒(rhsv),该重组单纯疱疹病毒(rhsv)包含本文的方面或实施方案中任一种中的多核苷酸。
20.根据另一方面,本公开内容提供了转基因表达盒,该转基因表达盒包含本文的方面和实施方案中任一种中的多核苷酸和最小调控元件。
21.根据另一方面,本公开内容提供了核酸载体,该核酸载体包含本文的任何方面或实施方案的表达盒。根据一些实施方案,该载体是腺相关病毒(aav)载体。
22.根据另一方面,本公开内容提供了宿主细胞,该宿主细胞包含本文的任何方面或实施方案的转基因表达盒。
23.根据另一方面,本公开内容提供了试剂盒,该试剂盒包含本文的任何方面或实施方案的表达载体和使用说明书。
24.表达载体,该表达载体包含本文的任何方面或实施方案的多核苷酸。根据一些实施方案,该载体是腺相关病毒(aav)载体。根据一些实施方案,所述aav载体的衣壳序列的血清型和itr的血清型独立地选自由以下组成的组:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11和aav12。
25.根据另一方面,本公开内容提供了重组腺相关(raav)表达载体,该重组腺相关(raav)表达载体包含本文的任何方面或实施方案的多核苷酸和aav基因组盒。根据一些实施方案,aav基因组盒的侧翼是两个序列调节的末端反向重复序列(sequence-modulated inverted terminal repeats),优选地长度约143个碱基。根据一些实施方案,aav基因组盒的侧翼是由两个反向相同重复序列组成的自我互补aav(scaav)基因组盒,两个反向相同重复序列优选地不长于2.4kb,由约113个碱基的使scaav可行的itr(scaav-enabling itr)(itrδtrs)隔开,并且在任一末端上侧翼是约143个碱基的序列调节的itr。根据一些实施方案,表达载体还包含最佳地适于耳蜗递送的蛋白衣壳变体。
26.根据另一方面,本公开内容提供了重组腺相关(raav)表达载体,该重组腺相关(raav)表达载体包含本文的任何方面或实施方案的多核苷酸,任选地包含具有或不具有血凝素c末端标签的密码子/序列优化的人类gjb2cdna,所述血凝素c末端标签优选地长度约27个核苷酸,所述密码子/序列优化的人类gjb2 cdna任选地尺寸约0.68千碱基(kb);可操作地连接到经过优化以驱动gjb2高表达的以下启动子元件中的一个:(a)遍在活化性cba,优选地尺寸约1.7kb;小cba(smcba),优选地尺寸约0.96kb;ef1a,优选地尺寸约0.81kb;或casi启动子,优选地尺寸约1.06kb;(b)耳蜗支持细胞或gjb2表达特异性gfap启动子,优选地尺寸约1.68kb;小gjb2启动子,优选地尺寸约0.13kb;中gjb2启动子,优选地尺寸约0.54kb;大gjb2启动子,优选地尺寸约1.0kb,或2-3个单独的gjb2表达特异性启动子的顺序组合;可操作地连接到包含土拨鼠肝炎病毒转录后调控元件(wpre)的0.9kb 3
’‑
utr调控区,随后是sv40或人类生长激素(hgh)多腺苷酸化信号,还包含aav基因组盒侧翼的两个约143个碱基的序列调节的末端反向重复序列(itr),或由两个反向相同重复序列组成的自我互补aav(scaav)基因组盒,优选地不长于2.4kb,由约113个碱基的使scaav可行的itr(itrδtrs)隔开,并且在任一末端上侧翼是约143个碱基的序列调节的itr;和适于靶向耳蜗递送的蛋白衣壳变体。根据一些实施方案,多腺苷酸化信号是sv40或人类生长激素(hgh)多腺苷酸化信号。根据一些实施方案,启动子是经过优化的以驱动gjb2高表达。根据一些实施方案,raav是选自由以下组成的组的血清型:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、rh-aav10、aav10、aav11和aav12。根据一些实施方案,raav是血清型aav1。根据一些实施方案,raav是血清型aav2。根据一些实施方案,raav是血清型aav3。根据一些实施方案,raav是血清型aav4。根据一些实施方案,raav是血清型aav5。根据一些实施方案,raav是血清型aav6。根据一些实施方案,raav是血清型aav7。根据一些实施方案,raav是血清型aav8。根据一些实施方案,raav是血清型aav9。根据一些实施方案,raav是血清型rh-aav10。根据一些实施方案,raav是血清型aav10。根据一些实施方案,raav是血清型aav11。根据一些实施方案,raav是血清型aav12。根据一些实施方案,raav包含在aav病毒粒子内。
27.根据另一方面,本公开内容提供了重组单纯疱疹病毒(rhsv),该重组单纯疱疹病毒(rhsv)包含本文的任何方面或实施方案中的表达载体。
28.根据另一方面,本公开内容提供了按以下顺序包含cba-gjb2(x)-ha-wpre-pa的多核苷酸,其中x包含与seq id no:18至少85%相同的核酸序列。根据另一方面,本公开内容提供了按以下顺序包含cba-gjb2(x)-ha-wpre-pa的多核苷酸,其中x包含与seq id no:18至少90%相同的核酸序列。根据另一方面,本公开内容提供了按以下顺序包含cba-gjb2(x)-ha-wpre-pa的多核苷酸,其中x包含与seq id no:18至少95%相同的核酸序列。根据另一方面,本公开内容提供了按以下顺序包含cba-gjb2(x)-ha-wpre-pa的多核苷酸,其中x包含由seq id no:18组成的核酸序列。
29.根据另一方面,本公开内容提供了宿主细胞,该宿主细胞包含本文的任何方面或实施方案中的表达载体。根据一些实施方案,宿主细胞是哺乳动物细胞。根据一些实施方案,宿主细胞是hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。根据一些实施方案,宿主细胞是bhk细胞。
30.根据另一方面,本公开内容提供了转基因表达盒,该转基因表达盒包含本文的方面或实施方案中任一种中的多核苷酸和最小调控元件。根据另一方面,本公开内容提供了
核酸载体,该核酸载体包含本文的任何方面和实施方案的表达盒。根据一些实施方案,该载体是腺相关病毒(aav)载体。
31.根据另一方面,本公开内容提供了试剂盒,该试剂盒包含本文的任何方面和实施方案的表达载体以及使用说明书。
32.根据另一方面,本公开内容提供了组合物,该组合物包含本文的任何方面和实施方案的多核苷酸。
33.根据另一方面,本公开内容提供了组合物,该组合物包含本文的任何方面和实施方案的宿主细胞。
34.根据另一方面,本公开内容提供了组合物,该组合物包含本文的任何方面和实施方案的重组单纯疱疹病毒(rhsv)。
35.根据另一方面,本公开内容提供了组合物,该组合物包含本文的任何方面和实施方案的转基因表达盒。
36.根据另一方面,本公开内容提供了组合物,该组合物包含本文的任何方面和实施方案的表达载体。根据一些实施方案中,组合物是药物组合物。
37.根据另一方面,本公开内容提供了治疗遗传性听力损失的方法,该方法包括向有相应需要的受试者施用本文的任何方面和实施方案中任一项的多核苷酸。
38.根据另一方面,本公开内容提供了预防遗传性听力损失的方法,该方法包括向有相应需要的受试者施用本文的任何方面和实施方案中任一项的多核苷酸。
39.根据另一方面,本公开内容提供了治疗或预防遗传性听力损失的方法,该方法包括向有相应需要的受试者施用本文的任何方面和实施方案的转基因表达盒。
40.根据另一方面,本公开内容提供了治疗或预防遗传性听力损失的方法,该方法包括向有相应需要的受试者施用本文的任何方面和实施方案的表达载体。
41.根据另一方面,本公开内容提供了治疗或预防遗传性听力损失的方法,该方法包括向有相应需要的受试者施用本文的任何方面和实施方案的重组腺相关(raav)表达载体。
42.根据另一方面,本公开内容提供了治疗或预防遗传性听力损失的方法,该方法包括向有相应需要的受试者施用包含本文的任何方面和实施方案的多核苷酸的重组腺相关(raav)病毒颗粒。根据一些实施方案,遗传性听力损失是dfnb1听力损失。根据一些实施方案,遗传性听力损失是由gjb2中的突变引起的。根据一些实施方案,遗传性听力损失是由常染色体隐性gjb2突变体(dfnb1)引起的。根据一些实施方案,遗传性听力损失是由常染色体显性gjb2突变体(dfna3a)引起的。根据一些实施方案,施用是向耳蜗施用。根据一些实施方案,施用是静脉内施用、脑室内施用、耳蜗内施用、鞘内施用或其组合。
43.根据本文的方面和实施方案中的一些实施方案,受试者是儿童。根据一些实施方案,受试者是婴儿。
44.根据另一方面,本公开内容提供了用于产生重组aav病毒颗粒的方法,该方法包括:用第一重组疱疹病毒和第二重组疱疹病毒共感染悬浮细胞,该第一重组疱疹病毒包含各自可操作地连接到启动子的编码aav rep基因和aav cap基因的核酸;该第二重组疱疹病毒包含gjb2基因和可操作地连接到所述基因的启动子;以及允许细胞产生重组aav病毒颗粒,从而产生重组aav病毒颗粒。根据一些实施方案,细胞是hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。根据一些实施方案,细胞以3和14之间的组合感
染复数(moi)被感染。根据一些实施方案,cap基因选自具有选自由以下组成的组的血清型的aav:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、rh-aav10、aav11和aav12。根据一些实施方案,第一疱疹病毒和第二疱疹病毒是选自由以下组成的组的病毒:巨细胞病毒(cmv)、单纯疱疹(hsv)和水痘带状疱疹(vzv)和爱泼斯坦-巴尔病毒(ebv)。根据一些实施方案,疱疹病毒是复制缺陷的。根据一些实施方案,共感染是同时的。
45.附图简述
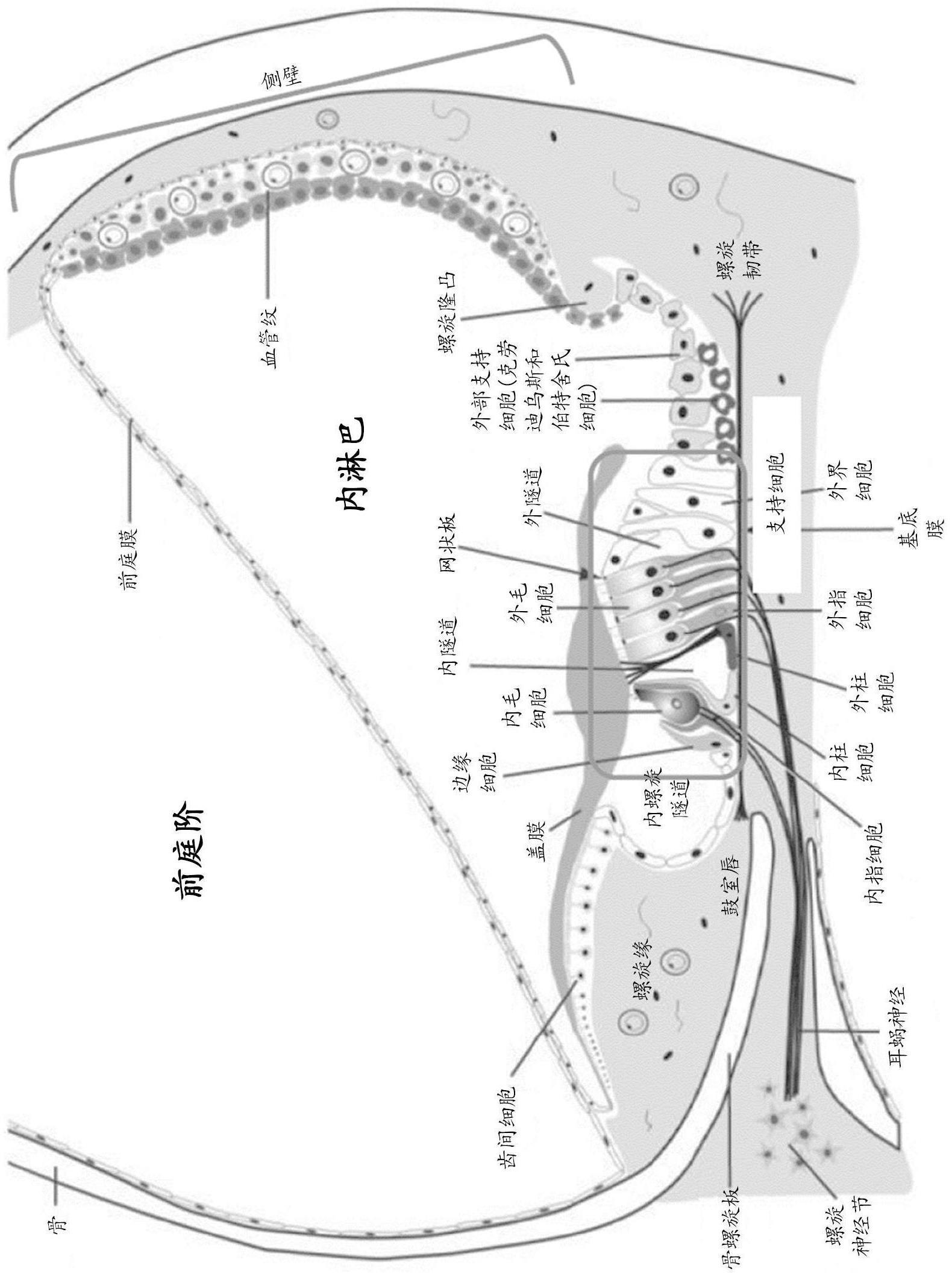
46.图1a是耳蜗解剖和细胞类型的示意图。
47.图1b示出支持细胞的特写。示出的是外毛细胞(01、02、03)、内毛细胞(ihc)、汉森细胞(h1、h2、h3、h4)、戴特斯细胞(d1、d2、d3)、柱细胞(p)、内指细胞(ipc)、外指细胞/边缘细胞(bc)。
48.图2示出gjb2载体(基因组)构建体单链(ss)aav-gjb2和自我互补scaav-gjb2的示意图。
49.图3示出cba启动子的核酸序列(seq id no.1)。
50.图4示出ef1a启动子的核酸序列(seq id no.2)。
51.图5示出casi启动子的核酸序列(seq id no.3)。
52.图6示出smcba启动子的核酸序列(seq id no.4)。
53.图7示出gfap启动子的核酸序列(seq id no.5)。
54.图8示出gjb2(1000)启动子的核酸序列(seq id no.6)。gjb2(128)加下划线,gjb2(539)为粗体。
55.图9示出以下itr(aav2)的核酸序列:5
’‑3’
:对于单链(ss)和自我互补(sc)aav基因组(seq id no.7);3
’‑5’
:仅对于单链(ss)aav基因组(seq id no.8);3
’‑5’
:仅对于自我互补(sc)aav基因组(seq id no.9)。
56.图10示出人类野生型gjb2(hgjb2wt)的核酸序列(seq id no.10)。
57.图11示出人类密码子优化的gjb2(hgjb2co3)的核酸序列(seq id no.11)。
58.图12示出人类密码子优化的gjb2(hgjb2co6)的核酸序列(seq id no.12)。
59.图13示出人类密码子优化的gjb2(hgjb2co9)的核酸序列(seq id no.13)。
60.图14示出血凝素(ha)标签的核酸序列(seq id no.14)。
61.图15示出土拨鼠肝炎病毒转录后调控元件(wpre)的核酸序列(seq id no.15)。
62.图16示出sv40多(a)的核酸序列(seq id no.16)。
63.图17示出sv40/bgh终止子序列的核酸序列(seq id no.17)。
64.图18a示出杂合密码子优化构建体(co369gjb2)的核酸序列(seq id no.18)。图18b示出杂合密码子优化构建体(co369gjb2)的氨基酸序列(seq id no.19)。
65.图19a示出对啮齿动物耳蜗中gfp转导的总结。
66.图19b示出对非人灵长类动物(nhp)耳蜗中gfp转导的总结。
67.图19c描绘了测试的各种aav2衣壳变体。图19c按照出现顺序分别公开了seq id no 20-32。
68.图20示出用paav-x-hgfp-pa载体转染的hek293细胞中的gfp表达,其中x为被测试的启动子,选自cba、smcba、casi、ef1a、gfap、gjb2(128)、gjb2(539)、gjb2(1000)。
69.图21示出用paav-x-hgfp-pa载体转染的rt4细胞中的gfp表达,其中x为被测试的
启动子,选自cba、smcba、casi、ef1a、gfap、gjb2(128)、gjb2(539)、gjb2(1000)。
70.图22描绘密码子优化的构建体(aav-cba-gjb2(x)-ha-wpre-pa)的示意图。
71.图23a和图23b是描绘当通过elisa进行测定时,各种gjb2密码子优化的构建体(aav-cba-gjb2(x)-ha-wpre-pa)与对照(wt)相比的gjb2和ha蛋白表达(分别)的变化倍数的图。
72.图24a是描绘在抗间隙连接蛋白26抗体(抗cx26)染色后通过绿色荧光蛋白(gfp)强度确定的免疫荧光定量的图。图24b是描绘在抗ha抗体后通过红色荧光蛋白(rfp)强度确定的免疫荧光定量的图。
73.图25示出hgjb2co9(seq id no:34)与wt(hgjb2)(seq id no:33)相比的序列比对。
74.图26示出gjb2 wt(seq id no:36)、co3(seq id no:37)、co6(seq id no:38)和co9(seq id no:39)序列之间的比对,根据比对确定的共有序列(seq id no:35),和co369杂合密码子优化序列。
75.图27a和图27b示出当通过elisa进行测定时,co9和co369密码子优化的构建体(aav-cba-gjb2(x)-ha-wpre-pa)与对照(wt)相比的gjb2和ha蛋白表达(分别)的变化倍数。
76.图28a和图28b示出使用抗间隙连接蛋白26(图28a)和抗ha(图28b)小鼠单克隆抗体对密码子优化的gjb2构建体进行蛋白印迹的结果。
77.图29示出使用co369作为感兴趣的基因进行3xflag添加的2步pcr的实例。图29按出现顺序分别公开了seq id no 40-43。
78.图30示出dna印迹分析结果,其中hgjb2wt和co369杂合构建体显示出预期的限制性消化片段条带。
79.图31a和图31b示出当通过elisa进行测定时,用抗间隙连接蛋白26(抗cx26;cx-1e8(33-5800))(图31a)或抗flag(图31b)抗体探查时,密码子优化的构建体在hela细胞中的表达。
80.图32是证实图31a和图31b中的elisa结果的蛋白印迹,展示了密码子优化的构建体在hek293细胞中表达。
81.图33a和图33b示出当通过elisa进行测定时,用抗间隙连接蛋白26(抗cx26;thermfisher 33-5800(1:500))(图33a)或抗flag(图33b)抗体探查时,构建体在hela细胞中的表达。
82.发明详述
83.定义
84.除非另外定义,否则本文使用的所有技术术语和科学术语具有本发明所属领域的技术人员通常理解的含义。以下参考文献为技术人员提供了本发明中使用的许多术语的一般定义。singleton等人dictionary of microbiology and molecular biology(第二版1994);the cambridge dictionary of science and technology(walker编著,1988);the glossary of genetics,第五版,r.rieger等人(编著),springer verlag(1991);和hale&marham,the harper collins dictionary of biology(1991)。如本文使用的,以下术语具有以下归于它们的含义,除非另外指明。
85.如本文使用的,术语“施用(administer)”、“施用(administering)”、“施用
(administration)”等意指用于实现将治疗剂或药物组合物递送到期望的生物学作用部位的方法。
86.如本文使用的,术语“aav病毒粒子(virion)”广义地意指完整的病毒颗粒,诸如例如野生型aav病毒粒子颗粒,其包含包装到aav衣壳蛋白中的单链基因组dna。单链核酸分子是有义链或反义链,因为两种链同样具有感染性。术语“raav病毒颗粒”是指重组aav病毒颗粒,即,有感染性但是复制缺陷的颗粒。raav病毒颗粒包含包装到aav衣壳蛋白中的单链基因组dna。
87.如本文使用的,术语“生物反应器”广义地意指可用于培养细胞的目的的任何装置。
88.如本文使用的,术语“运载体”意图包括任何和所有溶剂、分散介质、媒介物、包衣、稀释剂、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂、缓冲液、运载体溶液、悬浮液、胶体等。这样的介质和剂用于药学活性物质的用途是本领域熟知的。补充性活性成分也可以被掺入组合物中。措辞“药学上可接受”是指当施用至宿主时不产生毒性、过敏性或类似不良反应的分子实体和组合物。
89.如本文使用的,术语“基因”或“编码序列”广义地意指编码蛋白的dna区域(转录区域)。编码序列在位于适当的调控区诸如启动子的控制下时被转录(dna)并翻译(rna)为多肽。基因可以包含几个可操作地连接的片段,诸如启动子、5’前导序列、编码序列和3’非翻译序列,包含多腺苷酸化位点。措辞“基因的表达”是指其中基因被转录成rna和/或翻译成活性蛋白的过程。
90.术语“侧翼(flanking)”是指一个核酸序列相对于另一个核酸序列的相对位置。通常,在序列abc中,b的侧翼是a和c。对于排列axbxc也是如此。因此,侧翼序列(flanking sequence)在所侧接的序列(flanked sequence)之前或之后,但不需要与所侧接的序列相邻或紧邻。
91.如本文使用的,术语“基因的功能变体”包括具有微小变异的基因变体,诸如例如沉默突变、单核苷酸多态性、错义突变和其他不显著改变基因功能的突变或缺失。
92.如本文使用的,术语“基因递送”意指藉以将外来的dna转移至宿主细胞用于基因疗法应用的过程。
93.如本文使用的,术语“感兴趣的基因(goi)”广义地指引入到aav表达载体中的异源序列,并且通常指编码在人类或动物中有治疗性用途的蛋白的核酸序列。
94.如本文使用的,术语“听力损失”意指对受试者正常听到的声音的减弱的灵敏度。听力损失的严重程度根据在听者可以察觉之前通常必需的水平以上的音量增加来分类。根据一些实施方案,听力损失可以通过个体感知不同频率的音调的阈值音量的增加来表征。
95.如本文使用的,术语“疱疹病毒”或“疱疹病毒科(herpesviridae family)”广义地意指具有相对大的基因组的包膜的双链dna病毒的一般科。该科在广泛的脊椎动物和无脊椎动物宿主(在优选的实施方案中,哺乳动物宿主,例如在人类、马、牛、小鼠和猪中)的细胞核中复制。疱疹病毒科的示例性成员包括巨细胞病毒(cmv)、1型和2型单纯疱疹病毒(hsv1和hsv2)以及水痘带状疱疹(vzv)和爱泼斯坦-巴尔病毒(ebv)。
96.如本文使用的,术语“异源”意指源自与其所比较的或其被引入或掺入的其余实体的基因型不同的实体。例如,通过遗传工程化技术引入到不同细胞类型中的多核苷酸是异
源多核苷酸(并且,当表达时,可以编码异源多肽)。类似地,掺入到病毒载体中的细胞序列(例如,基因或其部分)相对于载体是异源核苷酸序列。
97.如本文使用的,术语“增加”、“增强”、“提高”(以及类似术语)通常指相对于自然的、预期的或平均的条件或者相对于对照条件直接或间接地增加浓度、水平、功能、活性或表现的行为。
98.如本文使用的,术语“感染”广义地意指通过病毒将异源dna递送到细胞中。如本文使用的术语“共感染”意指用两种或更多种病毒“同时感染”、“双重感染”、“多重感染”或“系列感染”。用两种(或更多种)病毒感染生产细胞将被称为“共感染”。术语“转染”是指通过物理或化学方法将异源dna递送到细胞的过程,诸如质粒dna,其通过电穿孔、磷酸钙沉淀方法或本领域熟知的其他方法被转移到细胞中。
99.如本文使用的,术语“内耳细胞”或“内耳的细胞”是指内毛细胞(ihc)和外毛细胞(ohc)、螺旋神经节神经元、前庭毛细胞、前庭神经节神经元、支持细胞和血管纹中的细胞。支持细胞是指耳内不可兴奋的细胞,例如,不是毛细胞或神经元的细胞。
100.如本文使用的,术语“末端反向重复序列(inverted terminal repeat)”或“itr”序列意指存在于病毒基因组末端的方向相反的相对短的序列。本领域充分理解的术语“aav末端反向重复序列(itr)”序列,是存在于天然单链aav基因组的两个末端的约145个核苷酸的序列。itr的最外侧核苷酸可以以两种可选方向中的任一种存在,导致不同aav基因组之间的异质性和单个aav基因组的两个末端之间的异质性。
[0101]“野生型itr”、“wt-itr”或“itr”是指aav或保留例如rep结合活性和rep切口能力的其他依赖病毒属(dependovirus)中天然存在的itr序列的序列。由于遗传密码的简并性或漂变,来自任何aav血清型的wt-itr的核苷酸序列可能与典型的天然存在的序列略有不同,并且因此本文使用所包括的wt-itr序列包括作为产生过程期间发生的天然发生的变化(例如,复制错误)的结果的wt-itr序列。根据一些实施方案,itr是wt aav2 itr。
[0102]
如本文使用的,术语“末端重复序列”或“tr”包括包含至少一个最小所需复制起点和包含回文发夹结构的区域的任何病毒末端重复序列或合成序列。rep结合序列(“rbs”)(也称为rbe(rep-结合元件))和末端分解位点(“trs”)共同构成“最小必需复制起点(minimal required origin of replication)”,并且因此tr包含至少一个rbs和至少一个trs。在特定的多核苷酸序列段内彼此为反向互补序列的tr通常各自被称为“末端反向重复序列”或“itr”。在病毒的上下文中,itr介导复制、病毒包装、整合和前病毒获救。
[0103]
术语“在体内”是指在生物体诸如多细胞动物中或内发生的测定或过程。在本文描述的一些方面中,当使用单细胞生物诸如细菌时,方法或用途可以称为“在体内”发生。术语“离体”是指使用在多细胞动物或植物体外的具有完整膜的活细胞(例如,外植体,培养的细胞,包括原代细胞和细胞系,转化的细胞系,和提取的组织或细胞,尤其包括血细胞)进行的方法和用途。术语“体外”是指不需要具有完整膜的细胞存在(诸如细胞提取物)的测定和方法,并且可以指在非细胞系统(诸如不包含细胞或细胞系统的培养基,诸如细胞提取物)中引入可编程的合成生物回路。
[0104]
如本文使用的,术语“分离的”分子(例如,分离的核酸或蛋白或细胞)意指它已经从其自然环境的组成部分中被鉴定和分离和/或回收。
[0105]
如本文使用的,术语“中耳”意指鼓膜和内耳之间的空间。
[0106]
如本文使用的,术语“最小调控元件”意指在靶细胞中有效表达基因所必需的并因此应被包含在转基因表达盒中的调控元件。这样的序列可以包括,例如,启动子或增强子序列,促进dna片段在质粒载体中插入的多接头序列,和负责mrna转录物的内含子剪接和多腺苷酸化的序列。
[0107]
如本文使用的,术语“最小化”、“减少”、“降低”和/或“抑制”(以及类似术语)通常指相对于自然的、预期的或平均的条件或相对于对照条件直接或间接地减少浓度、水平、功能、活性或表现的行为。
[0108]
如本文使用的,术语“非天然存在的”广义地意指自然界中不存在的蛋白、核酸、核糖核酸或病毒。例如,它可以是遗传修饰的变体,例如,cdna或密码子优化的核酸。
[0109]
如本文使用的,“核酸”或“核酸分子”意指由单体核苷酸链组成的分子,诸如例如dna分子(例如,cdna或基因组dna)。核酸可以编码,例如,启动子、gjb2基因或其部分或者调控元件。核酸分子可以是单链或双链的。“gjb2核酸”是指包含gjb2基因或其一部分或者gjb2基因或其一部分的功能变体的核酸。基因的功能变体包括基因的具有微小变异(诸如例如,沉默突变、单核苷酸多态性、错义突变、和其他不显著改变基因功能的突变或缺失)的变体。
[0110]
dna链和rna链的不对称末端被称为5’(五撇)和3’(三撇)末端,其中5’末端具有末端磷酸基团并且3’末端具有末端羟基基团。五撇(5’)末端在其末端处的脱氧核糖或核糖的糖环上具有第五个碳。核酸在体内以5’至3’方向合成,因为用于组装新链的聚合酶经由磷酸二酯键将每个新核苷酸附接到3’羟基(-oh)基团。
[0111]
如本文使用的术语“核酸构建体”是指从天然存在的基因中分离,或者是被修饰而以自然界中本来不存在的方式含有核酸区段,或者是合成的单链或双链的核酸分子。当核酸构建体含有表达本公开内容的编码序列所需的控制序列时,术语核酸构建体与术语“表达盒”同义。
[0112]“编码”特定gjb2蛋白的dna序列是被转录成特定rna和/或蛋白的核酸序列。dna多核苷酸可以编码被翻译成蛋白的rna(mrna),或者dna多核苷酸可以编码不被翻译成蛋白的rna(例如,trna、rrna或靶向dna的rna;也称为“非编码”rna或“ncrna”)。
[0113]
如本文使用的,术语“操作性地连接”或“可操作地连接”或“偶联”可以指遗传元件的并置,其中元件处于允许它们以预期方式操作的关系中。例如,如果启动子帮助启动编码序列的转录,则启动子可以操作性地连接到编码区。只要能维持这种功能关系,启动子和编码区之间可以存在间插残基。
[0114]
如本文使用的,相对于参考多肽或核酸序列的“序列同一性百分比(%)”被定义为在对齐序列和必要时引入空位以实现最大序列同一性百分比之后,候选序列中与参考多肽或核酸序列中的氨基酸残基或核苷酸相同的氨基酸残基或核苷酸的百分数,并且不考虑任何保守取代作为序列同一性的一部分。为了确定氨基酸或核酸序列同一性百分比的目的的比对可以通过本领域技术范围内的各种方式来实现,例如,使用公开可用的计算机软件程序,例如current protocols in molecular biology(ausubel等人,编著,1987),supp.30,第7.7.18节,表7.7.1中描述的那些,并且包括blast、blast-2、align或megalign(dnastar)软件。比对程序的实例是align plus(scientific and educational software,pennsylvania)。本领域技术人员可以确定用于测量比对的适当的参数,包括在被比较序列
的全长上实现最大对齐所需的任何算法。为了本文的目的,特定氨基酸序列a对、与或针对特定氨基酸序列b的氨基酸序列同一性%(其可替代地被表述为特定氨基酸序列a具有或包含对、与或针对特定氨基酸序列b的特定%的氨基酸序列同一性)计算如下:100乘以分数x/y,其中x是序列比对程序对a和b进行比对时,被该程序评分为相同匹配的氨基酸残基的数目,并且其中y是b中氨基酸残基的总数。应理解的是,在氨基酸序列a的长度不等于氨基酸序列b的长度的情况下,a与b的氨基酸序列同一性%将不等于b与a的氨基酸序列同一性%。为了本文的目的,特定核酸序列c对、与或针对特定核酸序列d的核酸序列同一性%(其可替代地被表述为特定核酸序列c具有或包含对、与或针对特定核酸序列d的特定%的核酸序列同一性)计算如下:100乘以分数w/z,其中w是序列比对程序对c和d进行比对时,被该程序评分为相同匹配的核苷酸的数目,并且其中z是d中核苷酸的总数。应理解的是,在核酸序列c的长度不等于核酸序列d的长度的情况下,c与d的核酸序列同一性%将不等于d与c的核酸序列同一性%。
[0115]
如本文使用的,术语“药物组合物”或“组合物”意指本文描述的组合物或剂(例如,重组腺相关(raav)表达载体),任选地与至少一种药学上可接受的化学组分(诸如但不限于运载体、稳定剂、稀释剂、分散剂、悬浮剂、增稠剂、赋形剂等)混合。
[0116]
如本文使用的,术语“多肽”和“蛋白”可互换地用于指氨基酸残基的聚合物,并且最小长度不限。这样的氨基酸残基聚合物可以含有天然或非天然氨基酸残基,并且包括但不限于肽、寡肽、氨基酸残基的二聚体、三聚体和多聚体。全长蛋白和其片段都包括在该定义中。该术语还包括多肽的后表达修饰,例如糖基化、唾液酸化、乙酰化、磷酸化等。此外,为了本公开内容的目的,“多肽”是指这样的蛋白,其包含对天然序列的修饰,诸如缺失、添加和取代(本质上通常是保守的),只要该蛋白维持期望的活性即可。这些修饰可以是有意的,如通过定点诱变,或者可以是偶然的,诸如通过产生蛋白的宿主的突变或由于pcr扩增引起的错误。
[0117]
如本文使用的,“启动子”意指促进特定基因转录的dna区域。作为转录过程的一部分,合成rna的酶,称为rna聚合酶,附着到基因附近的dna上。启动子含有特定的dna序列和响应元件,为rna聚合酶和募集rna聚合酶的转录因子提供起始结合位点。根据一些实施方案,启动子对于耳蜗中的支持细胞表达是高度特异性的。根据一些实施方案,启动子是内源性gjb2启动子。根据一些实施方案,启动子选自由以下组成的组:cba启动子、smcba启动子、casi启动子、gfap启动子和延伸因子-1α(ef1a)启动子。“鸡β-肌动蛋白(cba)启动子”是指源自鸡β-肌动蛋白基因的多核苷酸序列(例如,原鸡属(gallus)β肌动蛋白,由genbank entrez基因id 396526代表)。“smcba”启动子是指杂合cmv-鸡β-肌动蛋白启动子的小型形式。“casi”启动子是指包含cmv增强子的一部分、鸡β-肌动蛋白启动子的一部分和ubc增强子的一部分的启动子。
[0118]
如本文使用的术语“增强子”是指结合一种或更多种蛋白(例如,激活蛋白或转录因子)以增加核酸序列的转录活化的顺式作用调控序列(例如,50-1,500个碱基对)。增强子可以位于其调控的基因起始位点上游或基因起始位点下游最多1,000,000个碱基对。
[0119]
启动子可以称为驱动它所调控的核酸序列的表达或转录。措辞“可操作地连接”、“操作性地位于”、“操作性地连接”、“控制下”和“转录控制下”指示启动子相对于其调控的核酸序列处于正确的功能位置和/或方向,以控制该序列的转录起始和/或表达。如本文使
用的“反向启动子”是指其中核酸序列处于反向方向的启动子,使得原来的编码链现在是非编码链,且反之亦然。反向启动子序列可以在各种实施方案中用于调控开关的状态。此外,在各种实施方案中,启动子可与增强子结合使用。
[0120]
启动子可以是与基因或序列天然关联的启动子,如可以通过分离位于特定基因或序列的编码区段和/或外显子上游的5’非编码序列来获得。这样的启动子可以被称为是“内源的”。类似地,在一些实施方案中,增强子可以是与核酸序列天然关联的增强子,位于该序列的下游或上游。
[0121]
在一些实施方案中,编码核酸区段位于“重组启动子”或“异源启动子”的控制下,这两种启动子都是指在自然环境中通常不与其可操作地连接的编码核酸序列关联的启动子。重组或异源增强子是指在自然环境中通常不与特定核酸序列关联的增强子。这样的启动子或增强子可以包括其他基因的启动子或增强子;从任何其他原核细胞、病毒或真核细胞中分离的启动子或增强子;和非“天然存在”的合成启动子或增强子,即,包含不同转录调控区的不同元件和/或通过本领域已知的遗传工程化方法改变表达的突变。
[0122]
如本文使用的,术语“重组”可以指这样的生物分子,例如,基因或蛋白,其(1)已从其天然存在的环境中取出,(2)与自然界中发现该基因的多核苷酸的全部或部分不相关,(3)与自然界中该基因不连接的多核苷酸操作性地连接,或(4)在自然界中不存在。术语“重组”可以用于述及克隆的dna分离物、化学合成的多核苷酸类似物、或由异源系统生物合成的多核苷酸类似物、以及由这样的核酸编码的蛋白和/或mrna。
[0123]
如本文使用的,术语“重组hsv”、“rhsv”和“rhsv载体”广义地意指分离的、遗传修饰形式的1型单纯疱疹病毒(hsv),其含有掺入到病毒基因组中的异源基因。术语“rhsv-rep2cap2”或“rhsv-rep2cap1”意指其中来自aav血清型1或2的aav rep基因和cap基因已掺入到rhsv基因组中的rhsv,在某些实施方案中,编码感兴趣的治疗性基因的dna序列已掺入到病毒基因组中。
[0124]
如本文使用的,待通过本发明的方法治疗的“受试者”或“患者”或“个体”意指人类或非人类动物。“非人类动物”包括任何脊椎动物或无脊椎动物生物体。人类受试者可以是任何年龄、性别、种族或族裔群体,例如,白种人(白人)、亚洲人、非洲人、黑人、非裔美国人、非裔欧洲人、西班牙裔、中东人等。在一些实施方案中,受试者可以是患者或临床环境中的其他受试者。在一些实施方案中,受试者已经在进行治疗。在一些实施方案中,受试者是新生儿、婴儿、儿童、青少年或成人。
[0125]
如本文使用的,术语“治疗效果”是指结果被判断为是期望的和有益的治疗的结果。治疗效果可以包括直接或间接地停止、减少或消除疾病表现。治疗效果还可以包括直接或间接地停止、减少或消除疾病表现的进展。
[0126]
对于本文描述的任何治疗剂,治疗有效量可以根据初步体外研究和/或动物模型初始地确定。治疗有效剂量也可以根据人类数据确定。应用剂量可以基于施用化合物的相对生物利用度和效力进行调整。基于上述方法和其它熟知方法调整剂量以实现最大效力在普通技术人员的能力范围内。用于确定治疗有效性的一般原则(可见于goodman和gilman的the pharmacology basis of therapeutics,第10版,mcgraw-hill(new york)2001)的第1章,通过引用并入本文)在下文中总结。
[0127]
如本文使用的,术语“转基因”意指引入到细胞中,并且在适当条件下能够被转录
成rna,并任选地被翻译和/或表达的多核苷酸。在一些方面,它赋予引入它的细胞期望的特性,或以其他方式导致期望的治疗或诊断结果。
[0128]
如本文使用的,“转基因表达盒”或“表达盒”可互换使用,并指包含转基因(该转基因可操作地连接到一个或更多个启动子或足以指导该转基因转录的其他调控序列)的线性核酸段,但不包含编码衣壳的序列、其他载体序列或末端反向重复区。表达盒可以另外地包含一个或更多个顺式作用序列(例如,启动子、增强子或阻遏子(repressor))、一个或更多个内含子和一个或更多个转录后调控元件。
[0129]
如本文使用的,术语“治疗(treatment)”或“治疗(treating)”疾病或紊乱意指缓解疾病或紊乱的一个或更多个体征或症状、减轻疾病或紊乱的程度、使疾病或紊乱的状态稳定(例如,不恶化)、预防疾病或紊乱的传播、延迟或减缓疾病或紊乱的进展、改善或缓和疾病或紊乱的状态、以及缓解(无论是部分的还是完全的),无论是可检测到的还是检测不到的。例如,当gjb2以有效量(或剂量)表达时,足以预防、矫正异常生理反应和/或使异常生理反应正常化,例如,足以使疾病或紊乱的临床显著的特征减少至少约30%,更优选地至少50%,最优选地至少90%的治疗效果。“治疗(treatment)”还可指与如果不接受治疗预期的存活期相比延长的存活期。
[0130]
如本文使用的,术语“载体”意指包含待在体外或体内递送到宿主细胞中的核酸的重组质粒或病毒。
[0131]
如本文使用的,术语“表达载体”是指指导rna或多肽由载体上与转录调控序列连接的序列表达的载体。被表达的序列通常将(但不是必须)与细胞异源。表达载体可以包含另外的元件,例如,表达载体可以具有两种复制系统,因此允许其在两种生物体中(例如在用于表达的人类细胞中、和在用于克隆和扩增的原核宿主中)维持。术语“表达”是指参与产生rna和蛋白以及(如果适当的话)分泌蛋白的细胞过程,包括在适用的情况下,但不限于例如转录、转录物加工、翻译和蛋白折叠、修饰和加工。“表达产物”包括从基因转录的rna和通过从基因转录的mrna翻译所获得的多肽。术语“基因”意指当与适当的调控序列可操作地连接时,在体外或体内转录(dna)为rna的核酸序列。基因可以包括也可以不包括编码区之前和之后的区域,例如,5’非翻译(5’utr)序列或“前导”序列和3’utr序列或“尾随(trailer)”序列,以及单个编码区段(外显子)之间的间插序列(内含子)。
[0132]
如本文使用的,术语“重组病毒载体”意指包含一个或更多个异源序列(即,非病毒来源的核酸序列)的重组多核苷酸载体。在重组aav载体的情况下,重组核酸的侧翼是至少有一个末端反向重复序列(itr)。在一些实施方案中,重组核酸的侧翼是两个itr。
[0133]
如本文使用的,术语“重组aav载体(raav载体)”意指包含一个或更多个异源序列(即,非aav来源的核酸序列)的多核苷酸载体,该异源序列的侧翼是至少一个aav末端反向重复序列(itr)。当存在于已被合适的辅助病毒感染(或表达合适的辅助功能)并表达aav rep基因和cap基因产物(即aav rep蛋白和cap蛋白)的宿主细胞中时,这样的raav载体可以被复制并包装到感染性病毒颗粒中。当raav载体被掺入到较大的多核苷酸中(例如,在染色体中或在另一载体诸如用于克隆或转染的质粒中)时,则该raav载体可以被称为“前载体”,其在存在aav包装功能和合适的辅助功能的情况下可以通过复制和衣壳化而“获救”。raav载体可以是许多形式中的任何一种,包括但不限于质粒、线性人工染色体、与脂质复合、包封在脂质体内以及衣壳化为病毒颗粒例如aav颗粒。raav载体可以包装到aav病毒衣壳中以
产生“重组腺相关病毒颗粒(raav颗粒)”。
[0134]
如本文使用的,术语“raav病毒”或“raav病毒颗粒”意指包含至少一种aav衣壳蛋白和衣壳化的raav载体基因组的病毒颗粒。
[0135]
如本文使用的,“报告物”是指可用于提供可检测读出的蛋白。报告物通常产生可测量的信号,诸如荧光、颜色或发光。报告蛋白编码序列编码在细胞或生物体中的存在容易观察到的蛋白。例如,荧光蛋白使细胞在特定波长的光激发时发出荧光,萤光素酶使细胞催化产生光的反应,以及酶诸如β-半乳糖苷酶使底物转化为有色产物。可用于实验或诊断目的的示例性报告多肽包括但不限于β-内酰胺酶、β-半乳糖苷酶(lacz)、碱性磷酸酶(ap)、胸苷激酶(tk)、绿色荧光蛋白(gfp)和其他荧光蛋白、氯霉素乙酰转移酶(cat)、萤光素酶和其他本领域熟知的报告多肽。
[0136]
转录调控因子是指激活或阻遏感兴趣基因诸如gjb2的转录的转录激活因子和阻遏因子。启动子是启动特定基因转录的核酸区域。转录激活因子通常结合到转录启动子附近并募集rna聚合酶以直接启动转录。阻遏因子与转录启动子结合并在空间上阻碍rna聚合酶的转录启动。其他转录调控因子可以用作激活因子或阻遏因子,这取决于它们在哪里结合以及细胞和环境条件。转录调控因子类别的非限制性实例包括但不限于同源结构域蛋白、锌指蛋白、有翼螺旋(叉头)蛋白和亮氨酸拉链蛋白。
[0137]
如本文使用的,“阻遏蛋白”或“诱导蛋白”是与调控序列元件结合并分别阻遏或激活与调控序列元件操作性地连接的序列的转录的蛋白。如本文描述的优选的阻遏蛋白和诱导蛋白对至少一种输入剂或环境输入的存在或不存在敏感。如本文描述的优选蛋白在形式上是模块化的,包括例如可分离的dna结合和输入剂结合或响应元件或结构域。
[0138]
如本文使用的术语“包含(comprising)”或“包含(comprises)”用于述及组合物、方法及其各自的组成部分,这些组成部分对方法或组合物是必要的,但对未指明的要素(无论是否必要)的包括是开放的。
[0139]
如本文使用的术语“基本上由......组成”是指特定实施方案所需的那些要素。该术语允许存在不实质地影响该实施方案的基本的和新颖的或功能性的特征的要素。“包含”的使用表示包括而不是限制。
[0140]
术语“由......组成”是指如本文描述的组合物、方法和其各自的组成部分,所述组成部分不包括实施方案的描述中未列举的任何要素。
[0141]
如本文使用的术语“基本上由......组成”是指特定实施方案所需的那些要素。该术语允许存在不实质地影响本发明的实施方案的基本的和新颖的或功能性的特征的另外要素。
[0142]
术语“包括”在本文中用于意指措辞“包括但不限于”,并与措辞“包括但不限于”可互换地使用。
[0143]
术语“诸如”在本文中用于意指措辞“诸如但不限于”,并与措辞“诸如但不限于”可互换地使用。
[0144]
如本说明书和所附权利要求书中使用的,单数形式“一(a)”、“一(an)”和“该(the)”包括复数指示物,除非上下文另有明确指示。因此,例如,提及“该方法”包括本文描述的和/或对本领域技术人员而言在阅读本公开内容等后将是明显的一种或更多种类型的方法和/或步骤。类似地,词语“或”意图包括“和”,除非上下文另有明确指示。尽管与本文描
述的方法和材料相似或等同的方法和材料可以用于实践或测试本公开内容,但下文描述了合适的方法和材料。缩写“例如(e.g.)”源自拉丁文例如(exempli gratia),并且在本文中用于指示非限制性实例。因此,缩写“例如(e.g.)”与术语“例如(for example)”同义。
[0145]
本文公开的发明的可选要素或实施方案的分组不应解释为限制。每个组成员可以单独提及和要求保护,或者与该组的其他成员或本文中存在的其他要素以任何组合提及和要求保护。为了方便和/或专利性的原因,组的一个或更多个成员可以被包括于组中或从组中删除。当任何这样的包括或删除发生时,本说明书在本文中被认为含有作为修改的组,从而实现在所附权利要求书中使用的所有马库什组(markush group)的书面描述。
[0146]
在任何方面的一些实施方案中,本文描述的公开内容不涉及用于克隆人类的方法、用于修改人类生殖系遗传特性的方法、用于工业或商业目的的人类胚胎的用途、或用于修改动物的遗传特性的方法(这些方法可能导致动物遭受痛苦而对人或动物没有任何实质性的医学益处),并且也不涉及由这些方法得到的动物。
[0147]
本文在本发明的各方面的描述中定义了其他术语。
[0148]
本技术通篇引用的所有专利和其他出版物,包括文献参考、授权的专利、公布的专利申请和共同待决的专利申请,例如在这样的出版物中描述的可以与本文描述的技术结合使用的方法,为了描述和公开的目的通过引用明确并入本文。这些出版物仅为了其先于本技术的申请日期的公开内容被提供。就这一点而言,任何内容不应解释为承认本发明人没有资格借助在先发明或出于任何其他原因而先于这样的公开内容。所有关于日期的陈述或关于这些文件的内容的表述是基于对本技术人可用的信息,而不构成关于这些文件的日期或内容的正确性的任何承认。
[0149]
本公开内容的实施方案的描述并不旨在是穷尽性的或将本公开内容限制为所公开的精确形式。虽然本公开内容的特定实施方案和实例在本文中为了说明性目的被描述,但在本公开内容的范围内的各种等效修改是可能的,如相关领域的技术人员将认识到的那些。例如,虽然方法步骤或功能以特定的顺序呈现,但替代性实施方案可以以不同的顺序执行功能,或者可以基本上同时执行功能。本文提供的本公开内容的教导可以应用于其他程序或方法(如适当)。本文描述的各种实施方案可以被组合以提供另外的实施方案。如有必要,可以修改本公开内容的方面以采用上述参考文献和申请的组合、功能和概念来提供本公开内容的又另外的实施方案。此外,由于生物功能等效性的考虑,可以在不影响种类或量的方面的生物或化学作用的情况下对蛋白结构进行一些变化。可以根据详细描述对本公开内容进行这些和其他变化。所有这样的修改被意图包括于所附权利要求书的范围内。
[0150]
任何上述实施方案的特定要素可以被组合或被取代为其他实施方案中的要素。此外,虽然与本公开内容的某些实施方案相关的优点已经在这些实施方案的上下文中描述,但其他实施方案也可以表现出这样的优点,并且并非所有实施方案都必需表现出这样的优点才能落入本公开内容的范围。
[0151]
本文描述的技术通过下列实例进一步说明,这些实例不应以任何方式解释为进一步的限制。应当理解,本发明不限于本文描述的特定方法、方案和试剂等,并因此可变化。本文使用的术语仅为了描述特定实施方案的目的,并不意图限制本发明的范围,本发明的范围仅由权利要求书限定。
[0152]
核酸
[0153]
本文提供了对用于潜在治疗用途的核酸分子的表征和开发。如本文描述的,用于治疗用途的核酸编码gjb2蛋白,其中该核酸是密码子优化的。
[0154]
本公开内容提供了可用于治疗遗传性听力损伤的启动子、表达盒、载体、试剂盒和方法。本公开内容的某些方面涉及向受试者的内耳细胞递送异源核酸,包括施用重组腺相关病毒(raav)载体。根据一些方面,本公开内容提供治疗或预防遗传性听力损失的方法,该方法包括向受试者递送包含本文描述的raav载体的组合物,其中该raav载体包含异源核酸(例如,编码gjb2的核酸)。
[0155]
遗传性听力损伤(hi)的受试者中最常见的突变基因gjb2编码间隙连接蛋白-26(cx26)间隙连接通道蛋白,该蛋白是支持细胞之间的细胞间通信和耳蜗流体、内淋巴和外淋巴稳态的基础。gjb2位于13q12上的dfnb1基因座处。gjb2长度为5513bp,并含有两个外显子(长度分别为193bp和2141bp),由3179bp的内含子隔开(kiang等人,1997)。转录是从单起始位点启动的,并导致合成被认为是典型的2334个核苷酸的mrna(genbank nm_004004.5)。听力发病后,gjb2的损失引起内耳中各种细胞类型的大量细胞死亡。“gjb2核酸”是指包含gjb2基因或其一部分、或者gjb2基因或其一部分的功能变体的核酸。
[0156]
因此,在一些实施方案中,aav载体用于表达gjb2蛋白以恢复听力。
[0157]
根据一些实施方案,感兴趣的基因(例如,gjb2)是经过优化的以在表达(和/或功能)上优于野生型gjb2,并且还具有区别于(在dna/rna水平)野生型gjb2的能力。
[0158]
根据一些实施方案,本公开内容提供了gjb2治疗性蛋白或其片段(例如,功能性片段),其由密码子优化的核酸编码并在如本文描述的aav载体中和由其表达。本领域技术人员将理解,gjb2治疗性蛋白包括gjb2蛋白的所有剪接变体和种间同源物。gjb2治疗性蛋白包括完整的分子以及其截短的片段(例如,功能性片段)。
[0159]
图2示出gjb2载体(基因组)构建体单链(ss)aav-gjb2和自我互补scaav-gjb2的示意图。
[0160]
根据一些实施方案,本公开内容提供了编码野生型gjb2蛋白的核酸。根据一些实施方案,本公开内容提供了编码人类野生型gjb2蛋白的核酸。根据一些实施方案,编码人类野生型gjb2蛋白的核酸序列的长度为678bp。根据一种实施方案,编码人类野生型gjb2蛋白的核酸包含seq id no:10。根据一种实施方案,核酸与seq id no:10至少85%相同。根据一种实施方案,核酸与seq id no:10至少90%相同。根据一种实施方案,核酸与seq id no:10至少95%相同。根据一种实施方案,核酸与seq id no:10至少99%相同。根据一种实施方案,核酸由seq id no:10组成。
[0161]
图10示出人类野生型gjb2(hgjb2wt)的核酸序列(seq id no.10)。
[0162]
根据一些实施方案,本公开内容提供了编码gjb2蛋白的核酸,其中核酸序列是针对哺乳动物表达而经过密码子优化的。人类密码子优化的gjb2是编码正常听力所需的主要间隙连接蛋白的重要元件。进行密码子优化以增强gjb2的蛋白表达。
[0163]
如本文使用的,术语“密码子优化的”或“密码子优化”是指通过将至少一个、多于一个或大量的天然序列(例如,原核序列)的密码子替换为在感兴趣的脊椎动物(例如,小鼠或人类)基因中使用较频繁或最频繁的密码子,来修饰核酸序列以增强在该脊椎动物细胞中的表达的过程。不同的物种对特定氨基酸的某些密码子表现出特定的偏倚。通常,密码子优化不改变原始翻译蛋白的氨基酸序列。优化的密码子可以使用各种商业可用的平台(例
如,genscripts的optimumgene、atum的gene gps或blue heron biotech的密码子优化工具)或其他公开可用的数据库来确定。在一些实施方案中,编码gjb2蛋白的核酸是针对人类表达而经过优化的,和/或是人类gjb2或其功能片段。本文公开了示例性gjb2密码子优化序列。
[0164]
根据一些实施方案,本公开内容提供了编码人类密码子优化的gjb2蛋白的核酸。根据一些实施方案,所表达的gjb2治疗性蛋白对治疗遗传性听力损失包括治疗和/或预防dfnb1和dfna3a相关的先天性耳聋有作用。在一些实施方案中,gjb2治疗性蛋白不引起免疫系统反应。
[0165]
根据一些实施方案,编码人类密码子优化的gjb2蛋白的核酸序列的长度为678bp。根据一种实施方案,编码人类密码子优化的gjb2蛋白的核酸包含seq id no:11。根据一种实施方案,核酸与seq id no:11至少85%相同。根据一种实施方案,核酸与seq id no:11至少90%相同。根据一种实施方案,核酸与seq id no:11至少95%相同。根据一种实施方案,核酸与seq id no:11至少99%相同。根据一种实施方案,核酸由seq id no:11组成。
[0166]
图11示出人类密码子优化的gjb2(hgjb2co3)的核酸序列(seq id no.11)。
[0167]
根据一些实施方案,编码人类密码子优化的gjb2蛋白的核酸序列的长度为678bp。根据一种实施方案,编码人类密码子优化的gjb2蛋白的核酸包含seq id no:12。根据一种实施方案,核酸与seq id no:12至少85%相同。根据一种实施方案,核酸与seq id no:12至少90%相同。根据一种实施方案,核酸与seq id no:12至少95%相同。根据一种实施方案,核酸与seq id no:12至少99%相同。根据一种实施方案,核酸由seq id no:12组成。
[0168]
图12示出人类密码子优化的gjb2(hgjb2co6)的核酸序列(seq id no.12)。
[0169]
根据一些实施方案,编码人类密码子优化的gjb2蛋白的核酸序列的长度为678bp。根据一种实施方案,编码人类密码子优化的gjb2蛋白的核酸包含seq id no:13。根据一种实施方案,核酸与seq id no:13至少85%相同。根据一种实施方案,核酸与seq id no:13至少90%相同。根据一种实施方案,核酸与seq id no:13至少95%相同。根据一种实施方案,核酸与seq id no:13至少99%相同。根据一种实施方案,核酸由seq id no:13组成。
[0170]
图13示出人类密码子优化的gjb2(hgjb2co9)的核酸序列(seq id no.13)。
[0171]
根据一些实施方案,编码人类密码子优化的gjb2蛋白的核酸序列的长度为681bp。根据一种实施方案,编码人类密码子优化的gjb2蛋白的核酸包含seq id no:18。根据一种实施方案,核酸与seq id no:18至少85%相同。根据一种实施方案,核酸与seq id no:18至少90%相同。根据一种实施方案,核酸与seq id no:18至少95%相同。根据一种实施方案,核酸与seq id no:18至少99%相同。根据一种实施方案,核酸由seq id no:18组成。
[0172]
图18示出杂合密码子优化构建体(co369)的核酸序列(seq id no.18)。
[0173]
根据一些实施方案,编码人类密码子优化的gjb2蛋白的核酸序列的长度为678bp。根据一种实施方案,编码人类密码子优化的gjb2蛋白的核酸包含seq id no:13。根据一种实施方案,核酸与seq id no:13至少85%相同。根据一种实施方案,核酸与seq id no:13至少90%相同。根据一种实施方案,核酸与seq id no:13至少95%相同。根据一种实施方案,核酸与seq id no:13至少99%相同。根据一种实施方案,核酸由seq id no:13组成。
[0174]
根据本公开内容的实施方案,如本文描述的aav载体包含一个或更多个密码子优化的核酸序列,例如,编码gjb2治疗性蛋白或其功能片段的核酸序列。在一种实施方案中,
aav载体包含编码gjb2序列的密码子优化的核酸序列。在一些实施方案中,用于表达gjb2的aav载体可以具有编码全长gjb2蛋白的序列。在一些其他的实施方案中,用于表达gjb2的aav载体可以具有编码截短的gjb2蛋白的序列。
[0175]
根据一些实施方案,用于表达gjb2蛋白的aav载体还可以包含调控序列,诸如启动子、分泌信号、多a区域和增强子。
[0176]
启动子
[0177]
可以使用如本文描述的一种或更多种启动子在空间和时间上实现来自aav载体的gjb2治疗性蛋白或其片段的表达。
[0178]
用于表达gjb2蛋白的aav载体的表达盒可以包含启动子,该启动子可以影响整体表达水平。
[0179]
在本公开内容中设想使用各种启动子。
[0180]
根据一些实施方案,启动子是内源gjb2启动子。gjb2启动子是支持细胞特异性启动子,并且可以转导表达gjb2基因的内耳细胞;该启动子由于其长度短而可以用于产生scaav。根据一些实施方案,启动子包含seq id no:6。根据一些实施方案,启动子由seq id no:6组成。图8示出gjb2启动子的核酸序列(seq id no.6)。
[0181]
根据一些实施方案,启动子是cba启动子。cba启动子是可以转导内耳中多于一种细胞类型的强的遍在性启动子。根据一些实施方案,启动子包含seq id no:1。根据一些实施方案,启动子由seq id no:1组成。图3示出cba启动子的核酸序列(seq id no.1)。
[0182]
根据一些实施方案,启动子是ef1a启动子。ef1a启动子是可以转导内耳中多于一种细胞类型的哺乳动物来源的强遍在性启动子,并且由于其长度短而可以用于产生scaav。根据一些实施方案,启动子包含seq id no:2。根据一些实施方案,启动子由seq id no:2组成。图4示出ef1a启动子的核酸序列(seq id no.2)。
[0183]
根据一些实施方案,启动子是casi启动子。casi启动子是可以转导内耳中多于一种细胞类型的强遍在性启动子,并且由于其长度短而可以用于产生scaav。根据一些实施方案,启动子包含seq id no:3。根据一些实施方案,启动子由seq id no:3组成。图5示出casi启动子的核酸序列(seq id no.3)。
[0184]
根据一些实施方案,启动子是smcba启动子。smcba启动子是转导内耳中多于一种细胞类型的强遍在性启动子,并且由于其长度短而可以用于产生scaav。根据一些实施方案,启动子包含seq id no:4。根据一些实施方案,启动子由seq id no:4组成。图6示出smcba启动子的核酸序列(seq id no.4.)。
[0185]
根据一些实施方案,启动子是gfap启动子。gfap启动子是细胞特异性的并且在内耳支持细胞中具有活性。根据一些实施方案,启动子包含seq id no:5。根据一些实施方案,启动子由seq id no:5组成。图7示出gfap启动子的核酸序列(seq id no.5)。
[0186]
末端反向重复序列
[0187]
如本文描述的,用于表达gjb2蛋白的aav载体含有核酸,例如,位于两个末端反向重复(itr)序列之间的gjb2核酸序列(例如,密码子优化的gjb2核酸序列)。
[0188]
在一些实施方案中,itr序列可以来自细小病毒科,细小病毒亚科,依赖病毒属,其中包括腺相关病毒(aav),腺相关病毒通常感染人类(例如,血清型2、3a、3b、5和6)或灵长类动物(例如,血清型1和4)。有许多同源的血清型,例如aav2、aav4、aav6、aav8。
[0189]
根据一些实施方案,itr来自依赖病毒属诸如aav(例如,aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aavrh8、aavrh10、aav-dj和aav-dj8基因组)或者是嵌合itr或来自任何合成aav的itr。根据一些实施方案,aav载体的itr的血清型独立地选自由以下组成的组:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11和aav12。
[0190]
由于末端反向重复(itr)序列形成允许合成第二dna链的发夹结构的能力,因此末端反向重复(itr)序列是有效增加aav基因组所需的。scaav缩短的itr(trs)形成分子内双链dna模板,从而去除第二链合成的限速步骤。
[0191]
普通技术人员了解,itr序列具有双链霍利迪连接体(holliday junction)的共同结构,其典型地是t形或y形发夹结构,其中每个wt-itr由嵌入在较大的回文臂(a-a’)中的两个回文臂或环(b-b’和c-c’)和单链d序列形成,(其中这些回文序列的顺序定义了itr的翻转(flip或flop)方向)。参见,例如,来自不同aav血清型(aav1-aav6)的itr的结构分析和序列比较,并且在grimm等人,j.virology,2006;80(1);426-439;yan等人,j.virology,2005;364-379;duan等人,virology 1999;261;8-14中描述。本领域普通技术人员可以基于grimm等人,j.virology,2006;80(1);426-439中描述的来自不同aav血清型(aav1-aav6,以及禽aav(aaav)和牛aav(baav))的itr的序列比较,容易地确定用于aav载体的来自任何aav血清型的wt-itr序列;该文献显示了aav2的左itr与来自其他血清型的左itr的同一性%:aav-1(84%)、aav-3(86%)、aav-4(79%)、aav-5(58%)、aav-6(左itr)(100%)和aav-6(右itr)(82%)。
[0192]
图9示出以下itr(aav2)的核酸序列:5
’‑3’
:对于单链(ss)和自我互补(sc)aav基因组(seq id no.7);3
’‑5’
:仅对于单链(ss)aav基因组(seq id no.8);3
’‑5’
:仅对于自我互补(sc)aav基因组(seq id no.9)。
[0193]
在一些实施方案中,wt-itr序列的核苷酸序列可以被修饰(例如,通过修饰1个、2个、3个、4个或5个或更多个核苷酸或其中的任何范围的核苷酸),其中修饰是对互补核苷酸的取代,例如,g对c的取代并且反之亦然,以及t对a的取代并且反之亦然。因此,在一些实施方案中,使用基本上是wt的itr——即,该itr具有wt的基本环结构但有一些不改变或影响特性的保守核苷酸变化。
[0194]
用于遗传性听力损失的gjb2基因疗法
[0195]
本公开内容总体上提供了用于产生包含gjb2基因构建体的重组腺相关病毒(aav)病毒颗粒的方法及其在用于遗传性听力损失的基因疗法的方法中的用途。如本文描述的aav载体在向内耳细胞递送核酸(例如,gjb2基因构建体)方面特别有效。本文描述了构建、评价和利用能够有效地将gjb2递送到细胞中进行表达和随后分泌的重组腺相关病毒(raav)治疗性载体的方法。本文描述了用于遗传性听力损失的基于重组腺相关病毒(raav)的基因疗法的最佳修饰的gjb2/间隙连接蛋白26(cx26)cdna和相关遗传元件,该基因疗法包括治疗和/或预防dfnb1和dfna3a相关的先天性耳聋。
[0196]
重组腺相关病毒(raav)载体可以有效地容纳gjb2的靶基因和相关的遗传元件二者。此外,这样的载体可以被设计成在治疗上相关的耳蜗支持细胞中特异性表达gjb2。本公开内容描述了产生、评价和利用能够有效地向患者递送功能性gjb2基因的raav治疗性载体的方法。
[0197]
gjb2基因构建体可以包含:(1)具有或不具有27个核苷酸的血凝素(ha)c末端标签的密码子/序列优化的0.68kb人类gjb2 cdna;(2)经过优化以驱动gjb2高表达的以下启动子元件中的一个:(a)遍在活化性的1.7kb cba、0.96kb小cba(smcba)、0.81kb ef1a或1.06kb casi启动子;(b)耳蜗支持细胞或gjb2表达特异性的1.68kb gfap、0.13kb/0.54kb/1.0kb小/中/大gjb2启动子,或2-3个单独的gjb2表达特异性启动子的顺序组合;(3)包含土拨鼠肝炎病毒转录后调控元件(wpre)的0.9kb 3
’‑
utr调控区,随后是sv40或人类生长激素(hgh)多腺苷酸化信号;(4)aav基因组盒侧翼的两个143个碱基的序列调节的末端反向重复序列(itr),或由两个反向相同重复序列(每个不长于3.0kb)组成的自我互补aav(scaav)基因组盒,由113个碱基的使scaav可行的itr(itrδtrs)隔开,并且在任一末端上侧翼是143个碱基的序列调节的itr组成;和(5)最佳地适于耳蜗递送的蛋白衣壳变体。
[0198]
ha标签是人类流感血凝素,是在表达载体中用作通用表位标签的表面糖蛋白,有助于对感兴趣蛋白的检测。土拨鼠肝炎病毒转录后调控元件(wpre)是通过产生稳定其mrna的三级结构来增强感兴趣蛋白的表达的dna序列。多(a)序列是促进rna加工和转录物稳定性的重要元件。sv40/bgh序列是标志着转录单元结束的终止序列。
[0199]
根据一些实施方案,本文描述的aav载体特别适合于在耳蜗支持细胞中递送和表达glb2。根据一些实施方案,本文描述的aav载体特别适合于在外部支持细胞和/或科蒂器(organ of corti)支持细胞中的一种或更多种中递送和表达glb2。根据一些实施方案,本文描述的aav载体特别适于在外毛细胞、内毛细胞、汉森细胞、戴特斯细胞、柱细胞、内指细胞和/或外指细胞/边缘细胞中的一种或更多种中递送和表达glb2。
[0200]
腺相关病毒(aav)
[0201]
腺相关病毒(aav)是非致病性的单链dna细小病毒。aav具有约20nm的衣壳直径。单链dna基因组的每个末端含有末端反向重复序列(itr),它是基因组复制和包装所需的唯一顺式作用元件。aav基因组携带两个病毒基因:rep和cap。该病毒利用两个启动子和选择性剪接来产生复制所必需的四种蛋白(rep78、rep68、rep52和rep40)。第三启动子通过选择性剪接和选择性翻译起始密码子的组合产生三种结构病毒衣壳蛋白1、2和3(vp1、vp2和vp3)的转录物。berns&linden bioessays 1995;17:237-45。三种衣壳蛋白共有c末端533个氨基酸,而vp2和vp1分别含有另外的65个和202个氨基酸的n末端序列。aav病毒粒子以1:1:20的比含有总共60个拷贝的vp1、vp2和vp3,以t-1二十面体对称性排列。rose等人j virol.1971;8:766-70。aav需要腺病毒(ad)、单纯疱疹病毒(hsv)或其他病毒作为辅助病毒来完成其裂解生命周期。atchison等人science,1965;149:754-6;hoggan等人proc natl acad sci usa,1966;55:1467-74。在不存在辅助病毒的情况下,野生型aav通过itr与染色体的相互作用在rep蛋白的帮助下整合来建立潜伏期。berns&linden(1995)。
[0202]
aav血清型
[0203]
有许多不同的aav血清型,包括aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aavrh8、aavrh10、anc80l65及其变体或杂合体。体内研究显示,各种aav血清型表现出不同的组织或细胞向性。例如,aav1和aav6是对骨骼肌的转导有效的两种血清型。gao等人,proc natl acad sci usa,2002;99:11854-11859;xiao等人,j virol.1999;73:3994-4003;chao等人,mol ther.2000;2:619-623。aav-3显示对于巨核细胞的转导是优越的。handa等人,j gen virol.2000;81:2077-2084。aav5和aav6有效地感染
顶端气道细胞。zabner等人,j virol.2000;74:3852-3858;halbert等人,j virol.2001;75:6615-6624。aav2、aav4和aav5转导中枢神经系统中不同类型的细胞。davidson等人,proc natl acad sci usa.2000;97:3428-3432。aav8和aav5可以优于aav-2转导肝细胞。基于aav-5的载体以高于aav2的效率转导某些细胞类型(培养的气道上皮细胞、培养的横纹肌细胞和培养的人类脐静脉内皮细胞),而aav2和aav5二者显示出对nih 3t3、skbr3和t-47d细胞系的低转导效率。gao等人,proc natl acad sci usa.2002;99:11854-11859;mingozzi等人,j virol.2002;76:10497-10502.wo 99/61601。发现aav4转导大鼠视网膜的效率最高,aav5和aav1次之。rabinowitz等人,j virol.2002;76:791-801;weber等人,mol ther.2003;7:774-781。总之,aav1、aav2、aav4、aav5、aav8和aav9显示出对cns组织的向性。aav1、aav8和aav9显示出对心脏组织的向性。aav2表现出对肾组织的向性。aav7、aav8和aav9表现出对肝组织的向性。aav4、aav5、aav6和aav9表现出对肺组织的向性。aav8表现出对胰腺细胞的向性。aav3、aav5和aav8显示出对感光细胞的向性。aav1、aav2、aav4、aav5和aav8表现出对视网膜色素上皮(rpe)细胞的向性。aav1、aav6、aav7、aav8和aav9显示出对骨骼肌的向性。
[0204]
可以对病毒进行进一步的修饰以增强基因转移的效率,例如,通过改进每种血清型的向性。一种方法是将来自一种血清型衣壳的结构域交换到另一种,并从而从每个亲本创建具有期望的品质的杂合载体。由于病毒衣壳负责细胞受体结合,因此对病毒衣壳结构域(其对结合是关键的)的了解是重要的。在可获得晶体结构之前,对病毒衣壳(主要是对aav2)进行的突变研究主要是基于通过吸附外源部分、在随机位置插入肽或在氨基酸水平的详尽诱变进行的衣壳表面功能化。choi等人,curr gene ther.2005june;5(3):299-310,描述了用于杂合血清型的不同方法和考虑。
[0205]
来自其他aav血清型的衣壳在某些体内应用中提供优于基于aav2衣壳的raav载体的优点。首先,适当地使用具有特定血清型的raav载体可以增加将基因体内递送到基于aav2的载体感染较差或根本不感染的某些靶细胞的效率。其次,如果重新施用raav载体成为临床必需的,那么使用基于其他aav血清型的raav载体可以是有利的。已经展示重新施用具有相同衣壳的相同raav载体可能是无效的,可能是由于产生针对载体的中和抗体的产生。xiao等人,1999;halbert等人,1997。这个问题可以通过施用这样的raav颗粒来避免,该raav颗粒的衣壳由来自不同aav血清型的蛋白组成,不受针对第一种raav载体的中和抗体的存在的影响。xiao等人,1999。出于上述原因,使用来自包括aav2在内和除了aav2之外的血清型的cap基因构建的重组aav载体是期望的。将认识到,类似于rhsv但编码来自其他aav血清型(例如,aav1、aav2、aav3、aav5至aav9)的cap基因的重组hsv载体的构建可以使用本文描述的产生rhsv的方法来实现。在如本文描述的本发明的某些优选实施方案中,优选的是使用来自不同aav的cap基因构建的重组aav载体。与用于大规模产生raav的可选的方法相比,构建这些另外的rhsv载体的显著优点是容易和节省时间。特别是避免了为每种不同的衣壳血清型构建新的rep和cap可诱导细胞系的困难过程。
[0206]
制备重组aav(raav)载体
[0207]
本发明的raav载体的产生、纯化和表征可以使用本领域中已知的许多方法中的任何一种进行。对于实验室规模的产生方法的综述,参见,例如,clark rk,recent advances in recombinant adeno-associated virus vector production。kidney int.61s:9-15
(2002);choi vw等人,production of recombinant adeno-associated viral vectors for in vitro and in vivo use.current protocols in molecular biology 16.25.1-16.25.24(2007)(以下称为choi等人);grieger jc&samulski rj,adeno-associated virus as a gene therapy vector:vector development,production,and clinical applications.adv biochem engin/biotechnol 99:119-145(2005)(以下称为grieger&samulski);heilbronn r&weger s,viral vectors for gene transfer:current status of gene therapeutics,载于m.(编著),drug delivery,handbook of experimental pharmacology,197:143-170(2010)(以下称为heilbronn);howarth jl等人,using viral vectors as gene transfer tools.cell biol toxicol 26:1-10(2010)(以下称为howarth)。下面描述的产生方法意图作为非限制性实例。
[0208]
aav载体产生可以通过共转染包装质粒来完成。heilbronn。细胞系提供缺失的aav基因rep和cap以及所需的辅助病毒功能。在两个单独的质粒上或单个辅助构建体上将腺病毒辅助基因va-rna、e2a和e4与aav rep基因和cap基因一起转染。还转染重组aav载体质粒,其中aav衣壳基因被由itr括住的转基因表达盒(包含感兴趣的基因,例如,gjb2核酸、启动子和最小调控元件)替换。通常将这些包装质粒转染到293细胞中,293细胞是组成型表达剩余所需的ad辅助基因e1a和e1b的人类细胞系。这导致携带感兴趣基因的aav载体的扩增和包装。
[0209]
现在已经鉴定出多于一种血清型的aav,包括12种人类血清型和多于100种来自非人灵长类动物的血清型。howarth等人cell biol toxicol26:1-10(2010)。本发明的aav载体可以包含源自任何已知血清型aav的衣壳序列。如本文使用的,“已知血清型”包括可以使用本领域已知方法产生的衣壳突变体。这样的方法包括,例如,对病毒衣壳序列的遗传操作,不同血清型衣壳区暴露表面的结构域交换,以及使用诸如标记获救的技术产生aav嵌合体。参见bowles等人marker rescue of adeno-associated virus(aav)capsid mutants:a novel approach for chimeric aav production.journal of virology,77(1):423-432(2003)以及其中引用的参考文献。此外,本发明的aav载体可以包含源自任何已知血清型aav的itr。优选地,itr源自人类血清型aav1-aav12中的一种。在本发明的一些实施方案中,采用假分型(pseudotyping)方法,其中一种itr血清型的基因组被包装到不同的血清型衣壳中。
[0210]
根据一些实施方案,衣壳序列源自人类血清型aav1-aav12中的一种。根据一些实施方案,衣壳序列源自血清型aav2。根据一些实施方案,衣壳序列源自具有对靶向支持细胞(例如,外毛细胞、内毛细胞、汉森细胞、戴特斯细胞、柱细胞、内指细胞、外指细胞/边缘细胞)的高度向性的aav2变体。适用于该目的的衣壳包括aav2和aav2变体(包括aav2-tyf、aav2-meb、aav2-p2v2、aav2-mebtyftv、aav2-p2v6);以及aav5、aav8和anc80l65。
[0211]
根据一些实施方案,重组aav载体可以通过对病毒衣壳序列(特别是在aav三维结构的环出区域中)的遗传操作,或通过不同血清型衣壳区域暴露表面的结构域交换,或通过使用诸如标记获救的技术产生aav嵌合体而直接靶向。参见bowles等人marker rescue of adeno-associated virus(aav)capsid mutants:a novel approach for chimeric aav production.journal of virology,77(1):423-432(2003)以及其中引用的参考文献。
[0212]
choi等人中提供了一种用于产生、纯化和表征重组aav(raav)载体的可能方案。一
般来说,包括以下步骤:设计转基因表达盒,设计用于靶向特定受体的衣壳序列,产生无腺病毒的raav载体,纯化和滴定。这些步骤在以下总结并在choi等人中详细描述。
[0213]
转基因表达盒可以是单链aav(ssaav)载体或者包装成假双链转基因的“二聚体”或自我互补aav(scaav)载体。choi等人;howarth等人。由于需要将单链aav dna转化为双链dna,因此使用传统的ssaav载体通常导致基因表达的缓慢开始(从数天到数周直至达到转基因表达的平台期)。相反,scaav载体显示在静止细胞转导后数小时内开始基因表达,在数天内达到平台期。heilbronn。根据一些实施方案,使用scaav,其中与单链aav相比,scaav具有快速转导开始和增加的稳定性。可选地,转基因表达盒可以分为两个aav载体,这允许递送更长的构建体。参见例如,daya s.和berns,k.i.,gene therapy using adeno-associated virus vectors.clinical microbiology reviews,21(4):583-593(2008)(以下称为daya等人)。可以通过用限制性内切核酸酶消化适当的质粒(诸如例如,含有gjb2基因的质粒)以去除rep片段和cap片段,并凝胶纯化含有aavwt-itr的质粒骨架,来构建ssaav载体。choi等人。随后,可以将期望的转基因表达盒插入到适当的限制性位点之间以构建单链raav载体质粒。scaav载体可以如choi等人中描述的被构建。
[0214]
然后,raav载体和合适的aav辅助质粒和pxx6 ad辅助质粒的大规模质粒制备(至少1mg)可以通过双重cscl梯度分级来纯化。choi等人。合适的aav辅助质粒可以选自pxr系列pxr1-pxr5,它们分别允许将aav2 itr基因组交叉包装到aav血清型1至5的衣壳中。可以基于衣壳靶向感兴趣细胞的效率来选择适当的衣壳。可以采用改变基因组(即,转基因表达盒)长度和aav衣壳的已知方法来改进表达和/或基因向特定细胞类型(例如,视网膜锥细胞)的转移。参见,例如,yang gs,virus-mediated transduction of murine retina with adeno-associated virus:effects of viral capsid and genome size.journal of virology,76(15):7651-7660。
[0215]
接下来,用pxx6辅助质粒、raav载体质粒和aav辅助质粒转染293细胞。choi等人。随后,使分级的细胞裂解物经历多步raav纯化过程,然后进行cscl梯度纯化或肝素琼脂糖柱纯化。raav病毒粒子的产生和定量可以使用点印迹测定来确定。raav在细胞培养物中的体外转导可用于验证病毒的感染性和表达盒的功能性。
[0216]
除了choi等人中描述的方法之外,用于产生aav的各种其它转染方法可用于本发明的情况中。例如,瞬时转染方法是可用的,包括依赖于磷酸钙沉淀方案的方法。
[0217]
除了用于产生raav载体的实验室规模的方法之外,本发明可以利用生物反应器规模制备aav载体的领域中已知的技术,包括,例如,heilbronn;clement,n.等人large-scale adeno-associated viral vector production using a herpesvirus-based system enables manufacturing for clinical studies.human gene therapy,20:796-606.
[0218]
朝向实现可以产生大量临床级raav载体的可扩展生产系统的期望目标的进展,主要是在利用转染作为递送在细胞中产生raav所需的遗传元件的手段的生产系统中取得的。例如,通过用三质粒转染系统的质粒转染代替腺病毒感染而避免了对污染性腺病毒辅助物的去除,在所述三质粒转染系统中,第三质粒包含编码腺病毒辅助蛋白的核酸序列(xiao等人,1998)。双质粒转染系统中的改进也简化了产生过程并提高了raav载体的产生效率(grimm等人1998)。
[0219]
用于改进来自培养的哺乳动物细胞的raav产量的几种策略是基于通过遗传工程
化创建的专门生产细胞的开发。在一种方法中,大规模产生raav已通过使用遗传工程化的“前病毒”细胞系来实现的,在该细胞系中插入的aav基因组可以通过用辅助腺病毒或hsv感染细胞来“获救”。前病毒细胞系可以通过简单的腺病毒感染获救,相对于转染方案提供了增加的效率。
[0220]
第二种改进细胞的raav的产量的基于细胞的方法包括使用遗传工程化的“包装”细胞系,该遗传工程化的“包装”细胞系在其基因组中携带aav rep基因和cap基因之一,或者rep-cap二者以及感兴趣的itr-基因(qiao等人2002)。在前一种方法中,为了产生raav,包装细胞系被感染或转染使其具有辅助功能和具有aav itr-goi元件。后一种方法仅需要感染或转染细胞使其具有辅助功能。通常,使用包装细胞系的raav产生是通过用野生型腺病毒或重组腺病毒感染细胞来启动的。因为包装细胞包含rep基因和cap基因,所以不必外源提供这些元件。
[0221]
来自包装细胞系的raav产量已显示高于通过前病毒细胞系获救或转染方案获得的raav产量。
[0222]
使用基于递送辅助功能的方法实现了提高的raav产量,所述辅助功能来自利用重组单纯疱疹病毒(hsv)扩增子系统的hsv。尽管最初报道了每个细胞150-500个病毒基因组(vg)的量级的较低水平的raav载体产量(conway等人1997),但更近的基于rhsv扩增子的系统的改进提供了每个细胞raav v.g.和感染性颗粒(ip)的高得多的产量(feudner等人2002)。扩增子系统本来是复制缺陷的;然而,使用“内部破坏的(gutted)”载体(有复制能力的(rchsv)或复制缺陷的rhsv)仍然将免疫原性hsv组分引入到raav产生系统中。因此,必须实施对这些组分的适当测定和相应的纯化方案来去除它们。
[0223]
除了这些方法之外,本文描述了用于在哺乳动物细胞中产生重组aav病毒颗粒的方法,该方法包括用第一重组疱疹病毒和第二重组疱疹病毒共感染能够在悬浮液中生长的哺乳动物细胞,该第一重组疱疹病毒包含各自可操作地连接到启动子的编码aav rep基因和aav cap基因的核酸序列,该第二重组疱疹病毒包含gjb2基因和可操作地连接到所述gjb2基因的启动子,其两侧是aav末端反向重复序列,以促进感兴趣基因的包装,以及允许病毒感染哺乳动物细胞,从而在哺乳动物细胞中产生重组aav病毒颗粒。
[0224]
能够支持疱疹病毒复制的任何类型的哺乳动物细胞都适于根据本发明的方法使用,如本文描述的。因此,该哺乳动物细胞可以被认为是用于复制疱疹病毒的宿主细胞,如本文方法中描述的。本发明设想了用作宿主细胞的任何细胞类型,只要该细胞能够支持疱疹病毒的复制。合适的遗传上未修饰的哺乳动物细胞的实例包括但不限于诸如hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5的细胞系。
[0225]
在本发明的各种实施方案中使用的宿主细胞可以源自例如哺乳动物细胞,诸如人类胚胎肾细胞或灵长类动物细胞。其他细胞类型可以包括但不限于bhk细胞、vero细胞、cho细胞、或对其建立了组织培养技术的任何真核细胞,只要这些细胞是疱疹病毒允许性的。术语“疱疹病毒允许性(herpesvirus permissive)”意指疱疹病毒或疱疹病毒载体能够在细胞环境内完成整个细胞内病毒生命周期。在某些实施方案中,如描述的方法发生于在悬浮液中生长的哺乳动物细胞系bhk。宿主细胞可以源自现有的细胞系,例如,来自bhk细胞系,或者从头开发。
[0226]
用于产生本文描述的raav基因构建体的方法还包括通过以下方法在哺乳动物细
胞中产生的重组aav病毒颗粒,该方法包括用以下重组疱疹病毒共感染能够在悬浮液中生长的哺乳动物细胞:第一重组疱疹病毒,其包含各自可操作地连接到启动子的编码aav rep基因和aav cap基因的核酸;和(ii)第二重组疱疹病毒,其包含gjb2和可操作地连接到所述gjb2基因的启动子;以及允许病毒感染哺乳动物细胞,并从而在哺乳动物细胞中产生重组aav病毒颗粒。如本文描述的,疱疹病毒是选自由以下组成的组的病毒:巨细胞病毒(cmv)、单纯疱疹(hsv)和水痘带状疱疹(vzv)和爱泼斯坦-巴尔病毒(ebv)。重组疱疹病毒是复制缺陷的。根据一些实施方案,aav cap基因具有选自由以下组成的组的血清型:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aavrh8、aavrh10、anc80l65,包括变体或杂合体(例如,两种或更多种血清型的衣壳杂合体)。
[0227]
通过引用以其整体并入本文的美国专利申请公布第2007/0202587号描述了raav产生系统所需的元件。重组aav通过将基因构建体引入称为生产细胞的细胞在体外产生。用于产生raav的已知系统采用三个基础元件:(1)含有感兴趣基因的基因盒,(2)含有aav rep基因和cap基因的基因盒,和(3)“辅助”病毒蛋白的来源。
[0228]
第一基因盒是用侧翼是来自aav的末端反向重复序列(itr)的感兴趣基因构建的。itr的功能是指导感兴趣的基因向宿主细胞基因组中的整合,并且对重组基因组的衣壳化是必要的。hermonat和muzyczka,1984;samulski等人1983。第二基因盒含有编码raav复制和包装所需蛋白的aav基因rep和cap。rep基因编码dna复制所需的四种蛋白(rep 78、rep68、rep 52和rep 40)。cap基因编码构成病毒衣壳的三种结构蛋白(vp1、vp2和vp3)。muzyczka和berns,2001。
[0229]
需要第三元件,因为aav不能靠自己复制。辅助功能是来自产生有利于raav有效复制和包装的细胞环境的辅助dna病毒的蛋白产物。传统上,腺病毒(ad)被用来为raav提供辅助功能,但疱疹病毒也可以提供这些功能,如本文讨论的。
[0230]
用于基因疗法的raav载体的产生是使用合适的生产细胞系(诸如悬浮液中生长的bhk细胞)在体外进行的。适于在本发明中使用的其它细胞系包括hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。
[0231]
任何细胞类型都可以作为宿主细胞,只要该细胞能够支持疱疹病毒的复制。本领域技术人员将熟悉可用于从宿主细胞产生疱疹病毒的各种宿主细胞。合适的遗传上未修饰的哺乳动物宿主细胞的实例,例如,可以包括但不限于诸如hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5的细胞系。
[0232]
宿主细胞可以被改造以用于在悬浮培养中生长。宿主细胞可以是幼仓鼠肾(bhk)细胞。悬浮液中生长的bhk细胞系源自对贴壁性bhk细胞系的改造。这两种细胞系都是商业上可得的。
[0233]
一种用于递送raav产生所需的所有元件的策略利用了两种质粒和一种辅助病毒。这种方法依赖于用含有编码必需基因产物的基因盒的质粒转染生产细胞,以及用ad感染细胞以提供辅助功能。这种系统采用具有两种不同基因盒的质粒。第一种是编码待被包装为raav的重组dna的前病毒质粒。第二种是编码rep基因和cap基因的质粒。为了将这些不同的元件引入细胞,用ad感染细胞细胞,以及用这两种质粒转染细胞。由ad提供的基因产物由基因e1a、e1b、e2a、e4orf6和va编码。samulski等人1998;hauswirth等人2000;muzyczka和burns,2001。可选地,在更近的方案中,ad感染步骤可以用含有va、e2a和e4基因的腺病毒“辅助质粒”转染替换。xiao等人1998;matsushita等人1998。
[0234]
虽然ad常规地用作raav产生的辅助病毒,但也可以使用其他dna病毒,诸如1型单纯疱疹病毒(hsv-1)。已鉴定出aav2复制和包装所需的最少的hsv-1基因集,并且包括早期基因ul5、ul8、ul52和ul29。muzyczka和burns,2001。这些基因编码hsv-1核心复制机制的组分,即,解旋酶、引发酶、引发酶辅助蛋白和单链dna结合蛋白。knipe,1989;weller,1991。hsv-1的这种raav辅助特性已被用于设计和构建能够提供raav产生所需的辅助病毒基因产物的重组疱疹病毒载体。conway等人1999。
[0235]
用于基因疗法的raav载体的产生是使用合适的生产细胞系(诸如悬浮液中生长的bhk细胞)在体外进行的。适于在本发明中使用的其它细胞系包括hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。
[0236]
任何细胞类型都可以作为宿主细胞,只要该细胞能够支持疱疹病毒的复制。本领域技术人员将熟悉可用于从宿主细胞产生疱疹病毒的各种宿主细胞。合适的遗传上未修饰的哺乳动物宿主细胞的实例,例如,可以包括但不限于诸如hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5的细胞系。
[0237]
宿主细胞可以被改造以用于在悬浮培养中生长。在本发明的某些实施方案中,宿主细胞是幼仓鼠肾(bhk)细胞。悬浮液中生长的bhk细胞系源自对贴壁性bhk细胞系的改造。这两种细胞系都是商业上可得的。
[0238]
基于rhsv的raav制备方法
[0239]
本文描述了在悬浮液中生长的细胞中产生重组aav病毒颗粒的方法。来自连续建立的细胞系的悬浮或非锚定依赖性培养是大规模产生细胞和细胞产物的最广泛使用的手段。基于发酵技术的大规模悬浮培养对于制备哺乳动物细胞产物具有明显优点。可以在生物反应器中提供同质的条件,这允许精确地监测和控制温度、溶解氧和ph,并确保可以提取具有代表性的培养物样品。所使用的rhsv载体在组织培养瓶和生物反应器二者中都可以在允许的细胞系上容易地繁殖到高滴度,并提供适用于扩大规模到临床和市场生产所需的病毒生产水平的生产方案。
[0240]
搅拌罐生物反应器中的细胞培养提供非常高的体积比培养物表面积(volume-specific culture surface area),并已用于病毒疫苗的生产(griffiths,1986)。此外,搅拌罐生物反应器已在工业上证明是可扩展的。一种实例是多板cell cube细胞培养系统。产生感染性病毒载体的能力对制药工业越来越重要,尤其是在基因疗法的背景下。
[0241]
根据本文描述的方法细胞培养可以在允许大规模产生能够被本发明的疱疹载体感染的完全生物活性细胞的生物反应器中进行。生物反应器已被广泛应用于从悬浮和锚定依赖的动物细胞培养物二者产生生物产物。大多数大规模悬浮培养以分批过程或补料分批过程来操作,因为它们对于操作和扩大规模是最直接的。然而,基于恒化器或灌注原理的连续过程是可用的。生物反应器系统可以被设置为包括允许培养基交换的系统。例如,可以将过滤器并入到生物反应器系统中以允许从乏培养基(spent media)中分离细胞以辅助培养基交换。在用于制备疱疹病毒的本发明方法的一些实施方案中,培养基交换和灌注从细胞生长的某一天开始进行。例如,培养基交换和灌注可以在细胞生长的第3天开始。过滤器可以在生物反应器的外部,或在生物反应器的内部。
[0242]
用于产生重组aav病毒颗粒的方法可以包括:用第一重组疱疹病毒和第二重组疱
疹病毒共感染悬浮细胞,该第一重组疱疹病毒包含各自可操作地连接到启动子的编码aav rep基因和aav cap基因的核酸;该第二重组疱疹病毒包含gjb2基因构建体和可操作地连接到所述感兴趣基因的启动子;以及允许细胞产生重组aav病毒颗粒,从而产生重组aav病毒颗粒。细胞可以是hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。根据一些实施方案,cap基因可以选自具有选自由以下组成的组的血清型的aav:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aavrh8、aavrh10、anc80l65,包括其变体或杂合体(例如,两种或更多种血清型的衣壳杂合体)。细胞可以以3和14的之间的组合感染复数(moi)被感染。第一疱疹病毒和第二疱疹病毒可以是选自由以下组成的组的病毒:巨细胞病毒(cmv)、单纯疱疹(hsv)和水痘带状疱疹(vzv)和爱泼斯坦-巴尔病毒(ebv)。疱疹病毒可以是复制缺陷的。共感染可以是同时的。
[0243]
用于在哺乳动物细胞中产生重组aav病毒颗粒的方法可以包括用第一重组疱疹病毒和第二重组疱疹病毒共感染悬浮细胞,该第一重组疱疹病毒包含各自可操作地连接到启动子的编码aav rep基因和aav cap基因的核酸;该第二重组疱疹病毒包含gjb2基因构建体和可操作地连接到所述gjb2基因构建体的启动子;以及允许细胞繁殖,从而产生重组aav病毒颗粒,由此产生的病毒颗粒的数量等于或大于在贴壁条件下相等数量的细胞中生长的病毒颗粒的数量。细胞可以是hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。cap基因可以选自具有选自由以下组成的组的血清型的aav:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aavrh8、aavrh10、anc80l65,包括其变体或杂合体(例如,两种或更多种血清型的衣壳杂合体)。细胞可以以3和14的之间的组合感染复数(moi)被感染。第一疱疹病毒和第二疱疹病毒可以是选自由以下组成的组的病毒:巨细胞病毒(cmv)、单纯疱疹(hsv)和水痘带状疱疹(vzv)和爱泼斯坦-巴尔病毒(ebv)。疱疹病毒可以是复制缺陷的。共感染可以是同时的。
[0244]
用于将编码治疗性蛋白的核酸序列递送到悬浮细胞的方法包括:用第一重组疱疹病毒和第二疱疹病毒共感染bhk细胞,该第一重组疱疹病毒包含各自可操作地连接到启动子的编码aav rep基因和aav cap基因的核酸;该第二疱疹病毒包含gjb2基因构建体和可操作地连接到所述gjb2基因的启动子,其中感兴趣的基因包含治疗性蛋白编码序列;以及其中所述细胞以3和14之间的组合感染复数(moi)被感染;以及允许病毒感染细胞并表达治疗性蛋白,从而将编码治疗性蛋白的核酸序列递送到细胞。细胞可以是hek-293(293)、vero、rd、bhk-21、ht-1080、a549、cos-7、arpe-19和mrc-5。参见,例如,美国专利第9,783,826号。
[0245]
治疗方法
[0246]
aav与基因疗法
[0247]
基因疗法是指通过替换、改变或补充对疾病负责的基因来治疗遗传性或获得性疾病。它是通过将一个或更多个矫正性基因引入宿主细胞来实现的,通常是通过媒介物或载体手段来实现的。使用raav进行基因疗法对于许多疾病的治疗都有很大的前景。本文描述了产生重组腺相关病毒(raav),特别是产生大量重组aav以支持遗传性听力损失的治疗的方法。
[0248]
迄今为止,世界范围内已经进行了多于500项基因疗法临床试验。将raav作为基因疗法媒介物的努力为其作为人类疾病治疗的可应用性带来了前景。使用重组aav(raav)对引入到动物的细胞(包括临床上重要的脑、肝、骨骼肌和肺的非分裂细胞)中的基因进行递
送和长期表达,已在临床前取得了一些成功。在一些组织中,aav载体已显示整合到靶细胞的基因组中。hirata等人2000,j.of virology 74:4612-4620。
[0249]
raav的另一个优点是它在非分裂细胞类型(包括肝细胞、神经元和骨骼肌细胞)中执行这一功能的能力。raav已被成功地用作基因疗法媒介物以便实现促红细胞生成素在小鼠骨骼肌中的表达(kessler等人1996),酪氨酸羟化酶和芳族氨基酸脱羧酶在帕金森病猴模型cns中的表达(kaplitt等人1994)和因子ix在血友病动物模型的骨骼肌和肝中的表达。在临床水平,raav载体已用于人类临床试验以将cftr基因递送到囊性纤维化患者和将因子ix基因递送到血友病患者(flotte等人1998年;wagner等人1998)。此外,aav是辅助依赖的dna细小病毒,其与人类或哺乳动物中的疾病不相关(berns和bohensky,1987,advances in virus research,academic press inc,32:243-307)。因此,aav载体的最重要的属性之一是其在i期临床试验中的安全性谱。
[0250]
aav基因疗法已经在许多不同的病理环境中进行并治疗多种疾病和紊乱。例如,在i期研究中,将aav2-fix载体施用到8名血友病b受试者的骨骼肌中被证明是安全的,并在载体注射后至少10个月内实现因子ix的局部基因转移和表达(jiang等人mol ther.14(3):452-5 2006),先前已描述了将重组腺相关病毒α1-抗胰蛋白酶(raav2-cb-haat)基因载体肌内注射到aat缺陷成年人的i期试验(flotte等人hum gene ther.200415(1):93-128),并且在另一项临床试验中,对底丘脑核的aav-gad基因疗法已显示是安全的并且被患有晚期帕金森病的患者良好耐受(kaplitt等人lancet.200723;369(9579):2097-105)。
[0251]
gjb2 aav构建体提供了用于治疗dfnb1耳聋表型的基因疗法媒介物。本文描述的gjb2 aav基因疗法构建体和使用方法提供了用于dfnb1耳聋的疗法,该疗法有长期未满足的需求,因为对患者没有可用的基于基因疗法的治疗。
[0252]
gjb2/间隙连接蛋白26(cx26)与遗传性听力损失
[0253]
本文提供了可用于治疗受试者的听力紊乱或预防听力损失(或进一步的听力损失)的方法。将本文描述的一种或更多种核酸递送到内耳内的细胞(例如,在耳蜗(或耳蜗中的细胞或耳蜗细胞)中)可以用来治疗听力紊乱,听力紊乱通常被定义为部分听力损失或完全耳聋。
[0254]
根据一些实施方案,本文提供了采用基于gjb2 aav的基因疗法治疗以先天性非进行性轻度至严重感觉神经性听力损伤为特征的非综合征性听力损失和耳聋的方法。本文描述的gjb2 aav基因疗法构建体和使用方法提供了通过基因补充来矫正先天性耳聋的长期(例如,终身)疗法的首个且唯一的实例。重要的是,本文描述的gjb2 aav基因疗法构建体和使用方法将保留自然听力,而耳蜗移植不能。
[0255]
本文描述的允许在哺乳动物细胞中产生重组aav病毒颗粒的方法包括用第一重组疱疹病毒和第二重组疱疹病毒共感染能够在悬浮液中生长的哺乳动物细胞,该第二重组疱疹病毒包含在遗传性耳聋的治疗中具有治疗价值的gjb2基因构建体。
[0256]
gjb2编码主要的间隙连接蛋白间隙连接蛋白26(cx26),它与其他间隙连接蛋白一起提供了允许耳蜗中非感觉细胞之间的细胞间偶联的广泛网络。然而,gjb2突变如何引起遗传性听力损失的分子机制尚不完全清楚。已知听力发病后,gjb2的损失引起内耳中不同细胞类型的死亡,提示其在耳蜗发育过程中的相关性。此外,gjb2/cx26被假设为是通过维持科蒂器中的钾梯度稳态而形成正常听力所需的间隙连接网络所必要的。具有常染色体
pharmaceutical sciences(mack pub.co.,n.j.1991)中可得。
[0265]
根据一些实施方案,药物组合物包含bsst、pbs或bss中的一种或更多种。
[0266]
根据一些实施方案,药物组合物还包含组氨酸缓冲液。
[0267]
根据一些实施方案,药物组合物还包含泊洛沙姆缓冲液。
[0268]
根据一些实施方案,递送媒介物(例如,聚合物)可用于促进剂转移穿过鼓膜和/或通过圆窗,并且任何这样的递送媒介物可以用于递送本文描述的病毒。例如,参见arnold等人,2005,audiol.neurootol.,10:53-63,通过引用以其整体并入本文。
[0269]
尽管不是需要的,但组合物可以任选地以适于施用精确量的单位剂型提供。
[0270]
根据一些实施方案,在耳蜗植入之前向受试者施用组合物。
[0271]
施用方法
[0272]
通常,本文描述的组合物被配制用于施用到耳。根据一些实施方案,组合物被配制用于施用到耳蜗中的科蒂器(oc)中的细胞。oc中的细胞包括汉森细胞、戴特斯细胞、柱细胞、内指细胞和/或外指细胞/边缘细胞。oc包括两类感觉毛细胞:内毛细胞(ihc)和外毛细胞(ohc),内毛细胞将声音携带的机械信息转化为传送至神经元结构的电信号;外毛细胞用于放大和调节耳蜗反应,这是复杂听力功能所需的过程。根据一些实施方案,组合物被配制用于施用到ihc和/或ohc。
[0273]
向填充有高钾内淋巴流体的耳蜗管注射,可以提供直接进入毛细胞的途径。然而,这种精细的流体环境的改变可能破坏耳蜗内电位,提高注射相关毒性的风险。耳蜗管周围的外淋巴液填充的空间、鼓室阶和前庭阶,可以通过卵圆窗膜或圆窗膜从中耳进入。圆窗膜是唯一进入内耳的非骨性开口,在许多动物模型中相对容易接近,并且使用该途径施用病毒载体是良好耐受的。在人类中,耳蜗植入物替换通常依赖于通过圆窗膜的手术性电极插入。鼓室内注射治疗剂是将剂注射到鼓膜后的中耳和/或内耳中的技术。根据一些实施方案,组合物通过鼓室内注射到内耳和/或中耳中来施用。根据一些实施方案,组合物通过经由圆窗膜的注射施用。根据一些实施方案,组合物经由经鼓(transtympanic)注射直接施用到圆窗膜上。根据一些实施方案,组合物通过注射到鼓室阶或中间阶中来施用。根据一些实施方案,输送系统是能够刺穿鼓膜并直接接近圆窗膜的注射器和针头装置。根据一些实施方案,递送系统是滴耳器。根据一些实施方案,递送系统为表面(topical)制剂。根据一些实施方案,在手术程序中(例如在耳蜗开窗术(cochleostomy)过程中或管开窗术(canalostomy)过程中)施用组合物。对于一些施用途径,例如对于注射到内耳中和/或中耳中,可以使用持续释放系统。
[0274]
通过如本文描述的安全且有效地转导耳蜗细胞,本发明的方法可以用于治疗个体例如人类,其中转导的细胞产生的gjb2的量足以在延长的时间段(例如,数月,数年,数十年,终身)内恢复听力或前庭。
[0275]
根据本发明的治疗方法,可以基于接受治疗的受试者的特征(诸如受试者的年龄和待向其递送载体的区域的体积)来确定所递送的载体的体积。根据一些实施方案,所注射的组合物体积在约10μl至约1000μl之间,或在约100μl至约1000μl之间,或在约100μl至约500μl之间,或在约500μl至约1000μl之间。根据一些实施方案,所注射的组合物体积多于约1μl、2μl、3μl、4μl、5μl、6μl、7μl、8μl、9μl、10μl、15μl、20μl、25μl、50μl、75μl、100μl、200μl、300μl、400μl、500μl、600μl、700μl、800μl、900μl或1ml中的任何一种,或它们之间的任何
量。
[0276]
根据本公开内容的治疗方法,施用的载体浓度可以根据产生方法而不同,并且可以基于所确定对特定施用途径的治疗有效的浓度进行选择或优化。根据一些实施方案,每毫升载体基因组的浓度(vg/ml)选自由以下组成的组:约108vg/ml、约109vg/ml、约10
10
vg/ml、约10
11
vg/ml、约10
12
vg/ml、约10
13
vg/ml和约10
14
vg/ml。在优选的实施方案中,在约0.1ml、约0.2ml、约0.4ml、约0.6ml、约0.8ml和约1.0ml的体积中,浓度在10
10
vg/ml-10
13
vg/ml的范围内。
[0277]
本文描述的组合物的有效性可以通过几个标准来监测。例如,在使用本公开内容的方法在受试者中进行治疗之后,可以例如通过一个或更多个临床参数(包括本文描述的那些)评估受试者的疾病状态的一个或更多个体征或症状的进展的改善和/或稳定化和/或延迟。这样的测试的实例是本领域中已知的,并且包括客观以及主观的(例如,受试者报告的)测量。根据一些实施方案,这些测试可以包括但不限于听觉脑干反应(abr)测量、言语知觉、通信模式和主观评估听觉反应识别。
[0278]
根据一些实施方案,首先测试表现出非综合征性听力损失和耳聋(dfnb1)的受试者以确定他们在听觉范围内的阈值听力灵敏度。然后用本文描述的raav组合物治疗受试者。确定以db测量的阈值听力水平随频率的变化。根据一些实施方案,听力的改善被确定为至少一只耳在中频至高频处阈值听力灵敏度的10db至50db的改善。根据一些实施方案,听力的改善被确定为至少一只耳在中频至高频处阈值听力灵敏度的10db至30db的改善。根据一些实施方案,听力的改善被确定为至少一只耳在中频至高频处阈值听力灵敏度的10db至20db的改善。
[0279]
遗传性耳聋的体内小鼠模型
[0280]
根据一些实施方案,体内小鼠模型被用于评估本文描述的组合物的有效性。体内小鼠模型的一种实例是作为疾病模型的间隙连接蛋白26/gjb2敲除的转基因小鼠,诸如在takada等人,heiling research vol.309,2014中详细描述的实例,通过引用以其整体并入本文。
[0281]
本发明的另外的实施方案现在将参考以下实施例来描述。本文包含的实施例通过说明的方式而不是通过任何限制的方式被提供。
实施例
[0282]
实施例1.方法
[0283]
本发明使用但不限于以下方法进行。如本文描述的方法在2007年8月8日提交的名称为recombinant aav production in mammalian cells(哺乳动物细胞中重组aav产生)的pct申请第pct/us2007/017645号中阐述,该pct申请要求2007年8月14日提交的名称为recombinant aav production in mammalian cells(哺乳动物细胞中重组aav产生)的美国申请第11/503,775号的权益,该美国申请是2002年9月23日提交的名称为high titter recombinant aav production(高滴度重组aav产生)的美国申请序列第10/252,182号,现为2006年8月15日授权的美国专利第7,091,029号的部分继续申请。所有上述申请的内容在此通过引用以其整体并入。
[0284]
rhsv共感染方法
[0285]
用于重组腺相关病毒(raav)产生的rhsv共感染方法采用两种icp27缺陷的重组1型单纯疱疹病毒(rhsv-1)载体,一种携带aav rep基因和cap基因(rhsv-rep2capx,其中“capx”是指任何aav血清型),并且第二种携带感兴趣基因(goi)盒,其侧翼是aav末端反向重复序列(itr)。虽然该系统是用aav血清型2rep、cap和itr以及作为转基因的人源化绿色荧光蛋白基因(gfp)开发的,但该系统可以采用不同的转基因和血清型/假型元件。
[0286]
用rhsv载体感染哺乳动物细胞,提供所有顺式作用的和反式作用的raav组分以及生产性raav感染所需的辅助功能。用rhsv-rep2capx和rhsv-goi的混合物感染细胞。收获细胞并裂解以释放raav-goi,并通过下面描述的各种方法对所得的载体储备液进行滴定。
[0287]
doc-裂解
[0288]
在收获时,通过离心将细胞与培养基分离。留下培养基,同时使用2至3个冻融循环用含有0.5%(w/v)脱氧胆酸盐(doc)的裂解缓冲液(20mm tris-hcl、ph 8.0、150mm nacl)对细胞沉淀物进行提取,这提取细胞结合的raav。在一些情况下,将培养基和细胞结合的raav裂解物重新组合。
[0289]
原位裂解
[0290]
用于收获raav的替代方法是通过原位裂解。在收获时,将mgcl2添加到1mm的终浓度,将10%(v/v)triton x-100添加到1%(v/v)的终浓度,以及将benzonase添加到50单位/ml的终浓度。将该混合物在37℃摇动或搅拌2小时。
[0291]
定量实时pcr以确定drp产量
[0292]
dna酶抗性颗粒(drp)测定采用序列特异性的寡核苷酸引物和双重标记的杂交探针,使用实时定量聚合酶链式反应(qpcr)技术对扩增的dna序列进行检测和定量。在存在与dna杂交并发射拷贝依赖性的荧光的发荧光探针的情况下扩增靶序列。drp滴度(drp/ml)通过直接比较测试物与从携带相同dna序列的已知质粒稀释液产生的荧光信号的相对荧光单位(rfu)来计算。从该测定产生的数据反映包装的病毒dna序列的数量,而不指示序列完整性或颗粒感染性。
[0293]
绿色细胞感染性测定以确定感染性颗粒产量(仅raav-gfp)
[0294]
使用绿色细胞测定对raav-gfp储备液进行感染性颗粒(ip)滴定。用系列稀释的raav-gfp加饱和浓度的腺病毒(来为aav复制提供辅助功能)感染c12细胞(表达aav2 rep基因和cap基因的hela来源的细胞系——参见下文参考文献)。在2至3天的孵育后,对发绿色荧光的细胞(每个细胞代表一个感染事件)的数量计数并将其用于计算病毒样品的ip/ml滴度。
[0295]
clark kp等人在hum.gene ther.1995.6:1329-1341和gene ther.1996.3:1124-1132中描述了重组腺病毒产生,这两项均通过引用以其整体并入本文。
[0296]
tcid
50
以确定raav感染性
[0297]
含有感兴趣基因的raav颗粒(raav-goi)的感染性使用50%的组织培养感染性剂量(tcid
50
)测定来确定。在存在人类5型腺病毒的情况下对8种raav复制物进行系列稀释,并将其用于在96孔板中感染helarc32细胞(表达aav2 rep和cap的hela来源的细胞系,购自atcc)。在感染后3天,向每个孔中添加裂解缓冲液(终浓度1mm的tris-hcl ph 8.0、终浓度1mm的edta、终浓度0.25%(w/v)的脱氧胆酸盐、终浓度0.45%(v/v)的tween-20、终浓度0.1%(w/v)的十二烷基硫酸钠、终浓度0.3mg/ml的蛋白酶k),然后在37℃孵育1h,55℃孵育
id no.15)。图16示出sv40多(a)的核酸序列(seq id no.16)。图17示出asv40/bgh终止子序列的核酸序列(seq id no.17)。
[0310]
用星号(*)标记的元件也用于设计scaav载体构建体。
[0311]
实施例3.用于dfnb-1治疗的raav载体
[0312]
用于dfnb-1治疗的有效raav载体的组分包括:表现出耳蜗支持细胞向性的衣壳,驱动强遍在性或中等强度细胞类型特异性转基因表达的启动子,以及稳定编码间隙连接蛋白-26蛋白的转基因。
[0313]
衣壳选择
[0314]
图19a和图19b总结了从耳蜗向性研究中获得的数据,这些研究鉴定了用于在gjb2基因疗法中使用的aav2变体衣壳。这些先前的研究涉及五项独立的研究,两项在小鼠中,一项在豚鼠中,以及两项在非人灵长类动物(nhp)中。在啮齿类动物研究中,各自含有cba驱动的gfp报告物的aav衣壳初始组被耳蜗内施用到耳蜗中,用于组织分析并且然后2周后进行组织分析,以鉴定对各种治疗感兴趣的耳蜗组织有高向性(在这一情况中,对支持细胞有高向性)的候选物。从啮齿动物的数据中,选择了4种最终的衣壳,并与2种比较物衣壳一起在nhp中以与啮齿动物相似的方式进行测试(除了研究周期(in life)为12周而不是2周)。这些数据总结在图19a(对于啮齿动物)和图19b(对于nhp)中示出的表格中。选择p2v2是因为它显示出使其比其他衣壳更有利的积极特征的组合:这些特征包括优秀的支持细胞向性、相对较低的毛细胞向性和低炎性结果。
[0315]
图19c描绘了测试的各种aav2衣壳变体。根据本研究,将aav2-meb、aav2-p2v3、aav2-p2v2和aav-p2v6鉴定为用于dfnb治疗的raav载体中使用的顶尖候选物。
[0316]
启动子选择
[0317]
启动子的开发由对以下的鉴定组成:强遍在性启动子序列(cba、smcba、ef1a、casi)以及耳蜗支持细胞型特异性启动子(gfap和内源性哺乳动物gjb2启动子的不同长度形式,包括gjb2的128-bp长的基础启动子(gjb2(128))、gjb2(539)、gjb2(1000))。括号中的数字是碱基对(bp)长度,根据对gjb2基因的utr 5’的分析估计。虽然尚不精确知晓该启动子的真正内源性长度(即整个启动子还未界定),但这些长度是基于预测的启动子区域/基序选择的。1000bp长度的启动子估计含有较大gjb2启动子的所有已知功能区(主要是核心启动子加转录因子结合位点)。128bp长度的启动子代表最小“核心”启动子——任何进一步的截短都将完全消除启动子功能。539bp长度的启动子被选为这两者之间的中间体以推测地用作“中等强度”的启动子。这些启动子的序列由商业合成(genscript),随后进行内部pcr扩增和提取,得到具有相容的限制性位点区段的启动子区段,用于插入到独特的病毒包装载体中,该病毒包装载体含有氨苄青霉素选择盒、aav itr区段、hgfp报告基因和sv40多a(paav-x-hgfp-pa)。
[0318]
将启动子构建体转化到高效大肠杆菌细胞(sure2)中用于扩增,并选择克隆进行验证。进行sanger测序(genewiz)和限制性消化(用适当的限制性位点(kpni-mlui)检查启动子插入和itr完整性)来验证启动子质粒。选择每种启动子构建体的阳性克隆用于后续实验。经由体外转染hek-293(对照)或rt4(gjb2高表达细胞系)细胞来测试独特启动子构建体驱动hgfp表达的效力。
[0319]
简言之,将400μl培养基中的1e5个细胞接种在48孔板中。250ng dna以1:2的比用
genexplus进行转染。在48-72小时的时间点确定hgfp表达。图20示出用paav-x-hgfp-pa载体转染的hek293细胞中的gfp表达,其中x是启动子,选自cba、smcba、casi、ef1a、gfap、gjb2(128)、gjb2(539)、gjb2(1000),如指示的。图21示出用paav-x-hgfp-pa载体转染的rt4细胞中的gfp的表达,其中x是启动子,选自cba、smcba、casi、ef1a、gfap、gjb2(128)、gjb2(539)、gjb2(1000),如指示的。
[0320]
该数据表明cba和ef1a在两种细胞系中均驱动较强的gfp表达,而gjb2(1000)在rt4细胞中中度地驱动gfp表达并在hek293细胞中轻度地驱动gfp表达。这些结果表明cba和ef1a启动子为强启动子,而gjb2(1000)为中等强度的特异性启动子。
[0321]
实施例4.密码子优化的gjb2载体的设计与合成
[0322]
gjb2转基因优化由增强蛋白表达、稳定性和功能的工作组成。合成了密码子优化的gjb2变体,并评估了与野生型(wt)相比的蛋白表达的变化。产生了9种密码子优化的变体,各自含有27bp的c末端ha标签作为蛋白表达的可选测量以及相对于内源蛋白进行检测的手段。每个密码子优化的变体都含有独特优化(即,密码子使用、gc含量、5’mrna结构的稳定性、rna去稳定化序列的去除等),由不同的算法(genscript、atum和blueheron biotech)产生。
[0323]
进行内部pcr扩增和提取,得到具有相容的限制性位点(noti)的gjb2转基因区段用于插入到独特病毒包装载体中,该病毒包装载体含有氨苄青霉素选择盒和aav itr区段。完整合成后,将密码子优化的构建体转化到高效大肠杆菌细胞(sure2)中用于扩增,并选择克隆进行验证。进行sanger测序(genewiz)和限制性消化(用适当的限制性位点检查转基因插入和itr完整性)来验证密码子优化的gjb2质粒。
[0324]
图22描绘密码子优化的构建体(aav-cba-gjb2(x)-ha-wpre-pa)的示意图。
[0325]
选择每种密码子优化构建体的阳性克隆用于后续实验。为了确定最佳表达的密码子优化序列(称为hgjbco1
–
hgjbco9),进行转基因表达实验并经由细胞内elisa、免疫荧光和蛋白印迹进行分析。图23a和图23b示出当通过elisa进行测定时,各种gjb2密码子优化的构建体(aav-cba-gjb2(x)-ha-wpre-pa)与对照(wt)相比的gjb2和ha蛋白表达(分别)的变化倍数。如图23a中示出的,当用间隙连接蛋白26小鼠单克隆抗体(thermofisher scientific,cx-12h10)测定时,包含hgjbco3(co3)、hgjbco6(co6)和hgjbco9(co9)的构建体与wt相比显示出相当的蛋白表达。如图23b中示出的,当用ha小鼠单克隆抗体(thermofisher scientific,#26183)测定时,co9显示出显著更高的蛋白表达。蛋白印迹分析显示出,当用间隙连接蛋白26小鼠单克隆抗体测定时,co9具有与wt相当的表达,并且当用ha单克隆抗体测定时,co2、co3、co5、co6、co8和co9显示出与wt相当的表达(未示出)。当用gjb2和ha抗体测定时,免疫荧光数据显示出相当的结果,其中co3、co5、co6、co8和co9显示出与wt相比相当/更高的gjb2表达。在图24a中示出通过gfp强度确定的抗间隙连接蛋白26抗体(抗cx26)染色的免疫荧光研究的定量,并且图24b为通过rfp强度确定的抗ha染色的免疫荧光研究的定量。
[0326]
实施例5.密码子优化研究——第2代
[0327]
从实施例4中描述的结果中,选择密码子优化的gjb2#9(hgjb2co9)向前推进。hgjb2co9与wt(hgjb2)相比的序列同源性被确定为78%(图25)。制备更接近wt的密码子优化的变体以致力于改进蛋白的表达。用于设计变体的参数如下:如果co3/co6/co9位置中的
所有3个都对齐,则保留核苷酸变化。如果3个co3/co6/co9位置中的2个对齐,则保留核苷酸变化。从单独co3/co6或co9中去除单核苷酸变化。图26示出gjb2 wt、co3、co6和co9序列之间的比对,由该比对确定的共有序列和co369杂合密码子优化序列。测试对齐的核苷酸变化以确定它们如何改进蛋白表达。
[0328]
图27a和图27b示出当通过elisa进行测定(pierce比色细胞内elisa试剂盒(#62200))时,co9和co369密码子优化的构建体(aav-cba-gjb2(x)-ha-wpre-pa)与对照(wt)相比的gjb2和ha蛋白表达(分别)的变化倍数。进行詹纳斯绿染色来说明各孔中细胞数量的差异(a450值/a615值)。如图27a中示出的,间隙连接蛋白-26抗体(cx26;thermofisher scientific,cx-12h10)结果显示出wt、co9和co369的相似的蛋白表达。如图27a中示出的,在不存在wpre的情况下蛋白表达减少。如图27b中示出的,结果显示出co369-ha构建体(ha标签小鼠单克隆抗体(thermofisher scientific,#26183)的较高的平均蛋白表达。进行一式四份测量(4块板(n=4))。进行詹纳斯绿染色来说明各孔中细胞数量的差异(a450值/a615值)。
[0329]
当用间隙连接蛋白26小鼠单克隆抗体测定时,蛋白印迹分析示出杂合构建体co369是表达最高的载体之一(图28a)。当用抗ha小鼠单克隆抗体测定时,wt是表达最高的载体(图28b)。用β-肌动蛋白作为上样对照。
[0330]
总之,以上对蛋白表达的评估支持co369杂合体与wt gjb2构建体的可比性。elisa结果表明co369杂合体显示出最好的蛋白表达。蛋白印迹结果示出wt和co369杂合体显示出最好的蛋白表达。此外,免疫荧光数据将报告蛋白的正确定位(即,膜定位)。
[0331]
因此,从本文描述的研究中,选择具有aav2-p2v6衣壳、cba-hgfp启动子和gjb2co369杂合密码子优化转基因的构建体。
[0332]
实施例5.用含有gjb2基因组表达构建体的raav进行的体内研究
[0333]
设计了以下构建体以用于体内测试(术语cba和cb可互换使用以指cba启动子):
[0334]
ptr-cb-杂合gjb2(co369)-flag-wpre
[0335]
对照:ptr-cb-wtgjb2-flag-wpre
[0336]
进行用于将3xflag添加到相应的感兴趣基因的两步pcr方法来制备构建体。使用co369杂合体的实例在图29中示出。dna印迹分析示出wt和co369杂合flag构建体都显示出预期的限制性消化片段条带(图30)。
[0337]
图31a和图31b示出当通过elisa进行测定时,用抗间隙连接蛋白26(抗cx26;thermo,cx-1e8(33-5800))(图31a)或抗flag(图31b)抗体探查的密码子优化构建体在hek293细胞中的表达。当探查cx26和3xflag二者时,加标签的构建体在hek293中的表达显示出相当的表达。感兴趣的是,cx26探查似乎受到标签存在的影响。在蛋白印迹中也观察到该结果(图32)。进行詹纳斯绿染色来说明各孔中细胞数量的差异(a450值/a615值)。所有的组均以一式三份测试。
[0338]
图32是证实图31a和图31b中的elisa结果的蛋白印迹,展示了密码子优化的构建体在hek293细胞中表达。gapdh探针用于示出裂解物上样是相等的。裂解液上样是相等的(gapdh探针);观察到加标签的构建体在hek293中的表达如预期。
[0339]
图33a和图33b示出当通过elisa进行测定时,用抗间隙连接蛋白26(抗cx26;thermfisher 33-5800(1:500))(图33a)或抗flag(图33b)抗体探查的构建体在hela细胞中
的表达。当探查cx26和3xflag二者时,加标签的构建体在hela中的表达显示出相当的表达。cx26探查似乎受到标签存在的影响。总的来说,hela细胞中的结果与先前hek293细胞中的实验相当。蛋白印迹实验证实了elisa的结果(未示出)。
[0340]
在一组独立实验中,wt和co369杂合构建体二者都通过了质量控制测试(未示出)。
[0341]
将用含有gjb2基因组表达构建体的raav进行体内研究。收集的数据将包括用aav-gjb2先导候选物处理后来自小鼠组织的gjb2表达和耳蜗生物分布分析(通过如以上实施例中描述的体外研究确定)。收集的数据还将包括通过染料扩散和全细胞膜片钳测定对gjb2功能的评估。
[0342]
尽管为了清楚理解的目的已经通过说明和实例的方式在一些细节方面描述了本发明,但应当理解的是,在所附权利要求书的范围内可以实施某些变化和修改。对于基因疗法、分子生物学和/或相关领域的技术人员来说,根据上述公开内容将理解的或者通过本发明的常规实践或实施而变得明显的用于实施本发明的上述模式的修改被意图处于所附权利要求书的范围内。
[0343]
本说明书中提到的所有出版物(例如,非专利文献)、专利、专利申请公布和专利申请指示本发明所属领域技术人员的技术水平。所有这样的出版物(例如,非专利文献)、专利、专利申请公布和专利申请通过引用并入本文,其程度如同每一个单独的出版物、专利、专利申请公布或专利申请被具体和单独地指明通过引用并入。
[0344]
虽然已经结合该优选实施方案描述了上述发明,但它并不因此受到限制,而是仅受所附权利要求书的范围的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1