药物组合物及处置剂的制作方法
1.本发明涉及含有有效地抑制乙型肝炎病毒(hbv)基因表达的核酸分子和脂质的药物组合物及处置剂。
背景技术:
2.乙型肝炎病毒与丙型肝炎病毒一起为慢性肝炎的主要原因。在慢性乙型肝炎目前的治疗方法中,有干扰素(ifn)疗法和核酸类似物制剂疗法。ifn疗法的有效率停留在30~40%且伴有强烈的副作用。另一个核酸类似物制剂通过服用使肝炎静默而改善肝功能,但必须长期服用,由于停药在大部分的病例中肝炎会复发。因此,要求开发与目前的治疗方法不同的新的创新性治疗药(非专利文献1、2)。
3.非专利文献3中总结了慢性乙型肝炎治疗药可能的作用机制。其中,基于sirna的全病毒蛋白的翻译抑制可期待将作为hbv病毒的功能完全阻断。
4.核酸药物可以将在以往的低分子药物、抗体药物中无法考虑的mrna、mirna等分子作为创新药目标,其作为下一代药物被寄予厚望。
5.另一方面,由于已开发了能够将核酸递送至细胞的技术,因此核酸药物的开发活跃。作为核酸的递送技术之一,已知有将粒子(脂质体或脂质粒子)中内包有核酸的含核酸粒子进行给药的方法。在该技术中,使用具有氨基等且在低ph下成为阳离子的脂质来制备含核酸粒子,通过对粒子赋予适当的电荷而实现核酸的递送。例如,作为脂质粒子中含有的化合物,专利文献1中公开了具有酯基、缩醛基等作为连接脂肪族基团和氨基的连接基团的化合物。专利文献2中公开了具有乙烯基氧基、酰胺基、肟基等作为连接脂肪族基团和氨基的连接基团的化合物。需要说明的是,本说明书中,有时将具有氨基等且在低ph下成为阳离子的脂质称为阳离子性脂质。
6.此外,还对变更制造含核酸粒子时所使用的脂质化合物的种类及组成比进行了研究。专利文献3中记载了一种核酸-脂质粒子,其包含:(a)核酸;(b)构成粒子中存在的总脂质的约50mol%~约85mol%的阳离子性脂质;(c)构成粒子中存在的总脂质的约13mol%~约49.5mol%的非阳离子性脂质;和(d)构成粒子中存在的总脂质的约0.5mol%~约2mol%的抑制粒子凝聚的复合化脂质。专利文献4中记载了一种脂质制剂,其包含40~65%的特定结构的阳离子性脂质、5~10%的中性脂质、25~40%的甾醇、和0.5~10%的peg或peg修饰脂质。
7.现有技术文献
8.专利文献
9.专利文献1:国际公开公报2010/054401号小册子
10.专利文献2:国际公开公报2010/054405号小册子
11.专利文献3:国际公开公报2009/127060号小册子
12.专利文献4:国际公开公报2010/144740号小册子
13.非专利文献
14.非专利文献1:gastroenterology&hepatology 2016;12(11)679-689
15.非专利文献2:journal of hepatology 2016;64,s41-s48
16.非专利文献3:cold spring harb perspect med.2015;5(4)a021501
技术实现要素:
17.发明所要解决的课题
18.为了治疗乙型肝炎,期望能够强力地抑制乙型肝炎病毒增殖的核酸药物。
19.另一方面,利用具有氨基的脂质递送核酸的技术尚不充分,要求能够更高效地递送核酸的技术。
20.用于解决课题的手段
21.因此,本发明的目的在于提供药物组合物及处置剂,所述药物组合物组合有能够抑制乙型肝炎病毒基因表达的人工sirna和核酸递送优异的脂质,其中,人工sirna包含由下述序列a所示的碱基序列构成的核酸分子。
22.(序列a)5
’‑
cgucugugccuucucaucuucau-p-augaagaugagaaggcacagacggg-3’23.即,用于解决课题的手段如下。
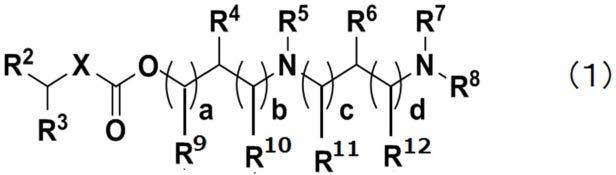
24.[1]一种药物组合物,其含有能够抑制乙型肝炎病毒基因表达的人工sirna、作为式(1)所示的化合物或其盐的脂质、胆固醇和具有聚乙二醇结构的脂质,其中,人工sirna包含由下述序列a所示的碱基序列构成的核酸分子。
[0025]
(序列a)
[0026]5’‑
cgucugugccuucucaucuucau-p-augaagaugagaaggcacagacggg-3’[0027]
式中,p表示:
[0028]
【化学式1】
[0029][0030]
【化学式2】
[0031][0032]
式中,x表示-nr
1-或-o-,
[0033]
r1表示氢原子、碳数为6~24的烃基、或r
21-l
1-r
22-所示的基团,r
21
表示碳数为1~24的烃基,l1表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0034]
【化学式3】
[0035][0036]r22
表示属于二价连接基团的碳数为1~18的烃连接基团,
[0037]
r2和r3分别独立地表示氢原子、碳数为3~24的烃基、或r
31-l
2-r
32-所示的基团,r
31
表示碳数为1~24的烃基,l2表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0038]
【化学式4】
[0039][0040]r32
表示属于二价连接基团的碳数为1~18的烃连接基团,
[0041]
r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
分别独立地表示氢原子或可以被取代的碳数为1~18的烷基,
[0042]
r4和r5、r
10
和r5、r5和r
12
、r4和r6、r5和r6、r6和r7、r6和r
10
、r
12
和r7、以及r7和r8中的任一组以上可相互连接形成可含有o原子的4~7元环,
[0043]
可以被取代的碳数为1~18的烷基上的取代基为羟基、羧基、-nr
45r46
所示的氨基、取代或未取代的芳基、取代或未取代的杂芳基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,
[0044]
取代或未取代的芳基、和取代或未取代的杂芳基上的取代基为碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,
[0045]
a、b、c和d分别独立地表示0~3的整数,其中,a+b为1以上,c+d为1以上。
[0046]
[2]根据[1]所述的药物组合物,其中,具有聚乙二醇结构的脂质为具有二酰基甘油结构和聚乙二醇结构的脂质。
[0047]
[3]根据[1]或[2]中任一项所述的药物组合物,其中,作为式(1)所示的化合物或其盐的脂质相对于总脂质的含量为40~70摩尔%。
[0048]
[4]根据[1]~[3]中任一项所述的药物组合物,其中,胆固醇相对于总脂质的含量为25~60摩尔%。
[0049]
[5]根据[1]~[4]中任一项所述的药物组合物,其中,具有聚乙二醇结构的脂质相对于总脂质的含量为0.5~10摩尔%。
[0050]
[6]根据[1]~[5]中任一项所述的药物组合物,其中,能够抑制乙型肝炎病毒基因表达的人工sirna相对于总脂质的含量为1~25质量%。
[0051]
[7]一种乙型肝炎的处置剂,其含有[1]~[6]中任一项所述的药物组合物。
[0052]
[8]一种肝硬化或肝癌的处置剂,其含有[1]~[6]中任一项所述的药物组合物。
[0053]
[a]一种对乙型肝炎进行处置的方法,其包含将[1]~[6]中任一项所述的药物组合物给药至对象的工序。
[0054]
[b]一种对肝硬化或肝癌进行处置的方法,其包含将[1]~[6]中任一项所述的药物组合物给药至对象的工序。
[0055]
[c]根据[1]~[6]中任一项所述的药物组合物,其在乙型肝炎的处置中使用。
[0056]
[d]根据[1]~[6]中任一项所述的药物组合物,其在肝硬化或肝癌的处置中使用。
[0057]
[e][1]~[6]中任一项所述的药物组合物用于制造乙型肝炎的处置剂的用途。
[0058]
[f][1]~[6]中任一项所述的药物组合物用于制造肝硬化或肝癌的处置剂的用途。
[0059]
发明效果
[0060]
通过使用本发明的药物组合物,能够抑制乙型肝炎病毒基因表达,能够对乙型肝炎和关联疾病有效地发挥治疗效果。
附图说明
[0061]
图1表示pxb细胞中的抗hbv分析试验的感染27天后的相对于无药剂添加孔的细胞活性(细胞活性)的相对值。
具体实施方式
[0062]
本发明的药物组合物含有能够抑制乙型肝炎病毒基因表达的人工sirn a(以下,有时称为人工sirna)、作为式(1)所示的化合物或其盐的脂质、非离子性脂质、和具有非离子性亲水性高分子结构的脂质,其中,人工si rna包含由序列a所示的碱基序列构成的核酸分子。
[0063]
本发明的药物组合物优选含有脂质粒子。脂质粒子是指由被分类为脂质的成分构成的粒子。
[0064]
作为脂质粒子的结构,可以考虑选自脂质凝聚而成的脂质凝聚体、胶束、脂质体中的任一种结构,但并不限定于此。
[0065]
在本发明的药物组合物含有脂质粒子的情况下,构成脂质粒子的脂质优选包含作为式(1)所示的化合物或其盐的脂质、非离子性脂质、和具有非离子性亲水性高分子结构的脂质。另外,人工sirna优选内包在脂质粒子中。
[0066]
脂质粒子的形态可以通过使用了电子显微镜观察或x射线的结构解析等来确认。例如,通过使用了cryo透射型电子显微镜观察(cryotem法)的方法,能够确认如脂质体那样脂质粒子为具有脂质双分子膜结构(层状结构)和内水层的结构、或具有在粒子内部具有电子密度高的核且填满了以脂质为代表的构成成分的结构等。通过小角x射线散射(saxs)测定,也能够确认脂质粒子有无脂质双分子膜结构(层状结构)。
[0067]
脂质粒子的粒径没有特别限定,优选为10~1000nm、更优选为30~500nm、进一步优选为50~250nm。脂质粒子的粒径可以通过通常的方法(例如动态光散射法、激光衍射法等)进行测定。
[0068]
本发明的药物组合物含有能够抑制乙型肝炎病毒基因表达的人工sirna。人工sirna包含由下述序列a所示的碱基序列构成的核酸分子。
[0069]
序列a:
[0070]5’‑
cgucugugccuucucaucuucau(序列号1)-p-augaagaugagaaggcacagacggg(序列号2)-3’[0071]
式中,p表示:
[0072]
【化学式5】
[0073][0074]
由序列a所示的碱基序列构成的核酸分子可基于亚磷酰胺法,通过市售的核酸合成机合成。作为rna酰胺化物(rna amidite),例如可以使用emm酰胺化物(国际公开第2013/027843号),酰胺化物的脱保护可以通过常规方法进行。p所示的连接分子可以通过使用下述的l-脯氨酸二酰胺酰胺化物导入至低聚物中。
[0075]
【化学式6】
[0076][0077]
在本发明的药物组合物中,人工sirna相对于总脂质的含量优选为1质量%~25质量%,更优选为1.5质量%~20质量%,进一步优选为2质量%~15质量%。
[0078]
本发明的药物组合物含有作为式(1)所示的化合物或其盐的脂质。
[0079]
【化学式7】
[0080][0081]
式中,x表示-nr
1-或-o-,
[0082]
r1表示氢原子、碳数为6~24的烃基、或r
21-l
1-r
22-所示的基团,r
21
表示碳数为1~24的烃基,l1表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0083]
【化学式8】
[0084][0085]r22
表示属于二价连接基团的碳数为1~18的烃连接基团,
[0086]
r2和r3分别独立地表示氢原子、碳数为3~24的烃基、或r
31-l
2-r
32-所示的基团,r
31
表示碳数为1~24的烃基,l2表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0087]
【化学式9】
[0088][0089]r32
表示属于二价连接基团的碳数为1~18的烃连接基团,
[0090]
r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
分别独立地表示氢原子或可以被取代的碳数为1~18的烷基,
[0091]
r4和r5、r
10
和r5、r5和r
12
、r4和r6、r5和r6、r6和r7、r6和r
10
、r
12
和r7、以及r7和r8中的任一组以上可相互连接形成可含有o原子的4~7元环,
[0092]
可以被取代的碳数为1~18的烷基上的取代基为羟基、羧基、-nr
45r46
所示的氨基、取代或未取代的芳基、取代或未取代的杂芳基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,
[0093]
取代或未取代的芳基、和取代或未取代的杂芳基的取代基为碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,
[0094]
a、b、c和d分别独立地表示0~3的整数,其中,a+b为1以上,c+d为1以上。
[0095]
作为r1中的碳数为6~24的烃基、以及r2和r3中的碳数为3~24的烃基,优选为烷基、烯基或炔基,更优选为烷基或烯基。碳数为6~24的烷基和碳数为3~24的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数为6~24的烷基优选为碳数为6~20的烷基,碳数为3~24的烷基更优选为碳数为6~20的烷基。具体而言,可举出己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、三甲基十二烷基(优选为3,7,11-三甲基十二烷基)、十四烷基、十五烷基、十六烷基、四甲基十六烷基(优选为3,7,11,15-四甲基十六烷基)、十七烷基、十八烷基、十九烷基、二十烷基等。碳数为6~24的烯基和碳数为3~24的烯基可以是直链也可以是支链,可以是链状也可以是环状。碳数为6~24的烯基优选为碳数为6~20的烯基,碳数为3~24的烯基更优选为碳数为6~20的烯基,具体而言,可举出己烯基、庚烯基、辛烯基、壬烯基、癸烯基、十一碳烯基、十二碳烯基、十二碳二烯基、十三碳烯基、十四碳烯基、十五碳烯基、十六碳烯基(优选为(z)-十六碳-9-烯基)、十六碳二烯基、十七碳烯基(优选为(z)-十七碳-8-烯基)、十七碳二烯基(优选为(8z,11z)-十七碳-8,11-二烯基)、十八碳烯基(优选为(z)-十八碳-9-烯基)、十八碳二烯基(优选为(9z,12z)-十八碳-9,12-二烯基)、十九碳烯基、二十碳烯基(优选为(z)-二十碳-11-烯基)、二十碳二烯基(优选为(11,14)-二十碳-11,14-二烯基)等。碳数为6~24的炔基优选为碳数为6~20的炔基,碳数为3~24的炔基更优选为碳数为6~20的炔基。具体而言,可举出己炔基、庚炔基、辛炔基、壬炔基、癸炔基、十一碳炔基、十二碳炔基、十四碳炔基、十五碳炔基、十六碳炔基、十七碳炔基、十八碳炔基等。优选上述烯基均具有1个或2个双键,优选炔基均具有1个或2个三键。
[0096]
作为r
21
和r
31
中的碳数为1~24的烃基,优选为碳数为10~24的烷基、碳数为10~24的烯基或碳数为10~24的炔基。碳数为10~24的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数为10~24的烷基优选为碳数为12~24的烷基。具体而言,可举出癸基、十一烷基、十二烷基、十三烷基、三甲基十二烷基(优选为3,7,11-三甲基十二烷基)、十四烷基、十五烷基、十六烷基、四甲基十六烷基(优选为3,7,11,15-四甲基十六烷基)、十七烷基、十八烷基、2-丁基己基、2-丁基辛基、1-戊基己基、2-戊基庚基、3-戊基辛基、1-己基庚
基、1-己基壬基、2-己基辛基、2-己基癸基、3-己基壬基、1-庚基辛基、2-庚基壬基、2-庚基十一烷基、3-庚基癸基、1-辛基壬基、2-辛基癸基、2-辛基十二烷基、3-辛基十一烷基、2-壬基十一烷基、3-壬基十二烷基、2-癸基十二烷基、2-癸基十四烷基、3-癸基十三烷基、2-(4,4-二甲基戊烷-2-基)-5,7,7-三甲基辛基等。碳数为10~24的烯基可以是直链也可以是支链,可以是链状也可以是环状。具体而言,可举出癸烯基、十一碳烯基、十二碳烯基、十二碳二烯基、十三碳烯基(优选为(z)-十三碳-8-烯基)、十四碳烯基(优选为十四碳-9-烯基)、十五碳烯基(优选为(z)-十五碳-8-烯基)、十六碳烯基(优选为(z)-十六碳-9-烯基)、十六碳二烯基、十七碳烯基(优选为(z)-十七碳-8-烯基)、十七碳二烯基(优选为(8z,11z)-十七碳-8,11-二烯基)、十八碳烯基(优选为(z)-十八碳-9-烯基)、十八碳二烯基(优选为(9z,12z)-十八碳-9,12-二烯基)等。碳数为10~24的炔基可以是直链也可以是支链,可以是链状也可以是环状。具体而言,可举出癸炔基、十一碳炔基、十二碳炔基、十四碳炔基、十五碳炔基、十六碳炔基、十七碳炔基、十八碳炔基等。优选上述烯基均具有1个或2个双键,优选炔基均具有1个或2个三键。
[0097]
作为r
22
和r
32
中的属于二价连接基团的碳数为1~18的烃连接基团,优选为碳数为1~18的亚烷基或碳数为2~18的亚烯基。碳数为1~18的亚烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为1~12、更优选为1~10、进一步优选为2~10。具体而言,可举出亚甲基、亚乙基、三亚甲基、四亚甲基、五亚甲基、六亚甲基、七亚甲基、八亚甲基、九亚甲基、十亚甲基、十一亚甲基、十二亚甲基等。碳数为2~18的亚烯基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为1~12、更优选为2~10。
[0098]
作为l1的优选范围,优选为-o(co)o-、-o(co)、或-(co)o-,更优选为-o(co)-或-(co)o-。
[0099]
作为l2的优选范围,优选为-o(co)o-、-o(co)、或-(co)o-,更优选为-o(co)-或-(co)o-。
[0100]
r4、r6、r9、r
10
、r
11
和r
12
中的可以被取代的碳数为1~18的烷基的碳数为1~18的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为1~12。具体而言,可举出甲基、乙基、丙基、异丙基、环丙基、丁基、异丁基、叔丁基、环丁基、戊基、环戊基、己基、环己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基等。烷基具有取代基时的取代基优选为羟基、羧基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
或-o-r
44
所示的基团,更优选为-o(co)-r
42
或-(co)o-r
43
所示的基团。
[0101]
r5、r7和r8中的可以被取代的碳数为1~18的烷基的碳数为1~18的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为1~12、更优选为1~8。具体而言,可举出甲基、乙基、丙基、异丙基、环丙基、丁基、异丁基、叔丁基、环丁基、戊基、环戊基、己基、环己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基等。烷基具有取代基时的取代基优选为羟基、羧基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
或-o-r
44
所示的基团,更优选为-o(co)-r
42
、-(co)o-r
43
或-o-r
44
所示的基团。
[0102]
作为可含有o原子的4~7元环,可举出氮杂环丁烷环、吡咯烷环、哌啶环、吗啉环、氮杂环庚烷环,优选为6元环,优选哌啶环、吗啉环。
[0103]
关于r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
,作为可以被取代的碳数为1~18的烷基中的取代基为取代或未取代的芳基时的芳基,优选碳数为6~22,更优选为6~18,进一步优选为
6~10。具体而言,可举出苯基、萘基、蒽基、菲基等。作为芳基上的取代基,优选碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,更优选羟基或羧基。作为取代芳基,具体而言,可举出羟基苯基、羧基苯基等。
[0104]
关于r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
,作为可以被取代的碳数为1~18的烷基中的取代基为取代或未取代的杂芳基时的杂芳基,优选碳数为1~12,更优选为1~6。具体而言,可举出吡啶基、吡唑基、咪唑基、苯并咪唑基、噻唑基、噁唑基等。作为杂芳基上的取代基,优选为碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,更优选为羟基或羧基。作为取代或未取代的杂芳基,具体而言可举出羟基吡啶基、羧基吡啶基、pyridonyl。
[0105]
作为r
41
、r
42
、r
43
、r
44
、r
45
和r
46
中的碳数为1~18的烃基,优选为碳数为1~18的烷基、碳数为2~18的烯基或碳数为2~18的炔基,更优选为碳数为1~18的烷基或碳数为2~18的烯基。碳数为1~18的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为3~18、更优选为5~18。具体而言,可举出丙基、异丙基、环丙基、丁基、异丁基、叔丁基、环丁基、戊基、环戊基、己基、环己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、三甲基十二烷基(优选为3,7,11-三甲基十二烷基)、十四烷基、十五烷基、十六烷基、十七烷基、十八烷基等。碳数为2~18的烯基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为3~18、更优选为5~18。具体而言,可举出烯丙基、异戊二烯基、戊烯基、己烯基、庚烯基、辛烯基、壬烯基(优选为(z)-2-壬烯基或(e)-2-壬烯基)、癸烯基、十一碳烯基、十二碳烯基、十二碳二烯基、十三碳烯基(优选为(z)-十三碳-8-烯基)、十四碳烯基(优选为十四碳-9-烯基)、十五碳烯基(优选为(z)-十五碳-8-烯基)、十六碳烯基(优选为(z)-十六碳-9-烯基)、十六碳二烯基、十七碳烯基(优选为(z)-十七碳-8-烯基)、十七碳二烯基(优选为(8z,11z)-十七碳-8,11-二烯基)、十八碳烯基(优选为(z)-十八碳-9-烯基)、十八碳二烯基(优选为(9z,12z)-十八碳-9,12-二烯基)等。碳数为2~18的炔基可以是直链也可以是支链,可以是链状也可以是环状。碳数优选为3~18、更优选为5~18。具体而言,可举出炔丙基、丁炔基、戊炔基、己炔基、庚炔基、辛炔基、壬炔基、癸炔基、十一碳炔基、十二碳炔基、十四碳炔基、十五碳炔基、十六碳炔基、十七碳炔基、十八碳炔基等。
[0106]
x表示-nr
1-时,r1优选表示碳数为6~24的烃基、或r
21-l
1-r
22-所示的基团。此时,优选r2和r3中的一个为氢原子;r2和r3中的另一个表示碳数为6~24的烃基、或r
31-l
2-r
32-所示的基团。
[0107]
当x表示-o-时,r2和r3分别独立地表示碳数为6~24的烃基或r
31-l
2-r
32-所示的基团。
[0108]
r4、r6、r9、r
10
、r
11
和r
12
优选为氢原子。
[0109]
r5优选为氢原子、碳数为1~18的烷基、可以被-o(co)-r
42
或-(co)o-r
43
取代的碳数为1~18的烷基、可以被芳基取代的碳数为1~18的烷基、可以被羟基取代的碳数为1~18的烷基,为烷基时可以与r4、r6、r
10
和r
12
相互连接形成可含有o原子的环。其中,优选为碳数为1~18的烷基、可以被-o(co)-r
42
或-(co)o-r
43
取代的碳数为1~18的烷基、可以被芳基取代的碳数为1~12的烷基、可以被羟基取代的碳数为1~8的烷基,更优选为碳数为1~18的烷基、可以被-o(co)-r
42
或-(co)o-r
43
取代的碳数为1~18的烷基。
[0110]
优选r7和r8分别独立地为氢原子、碳数为1~18的烃基、可以被-o(co)-r
42
或-(co)
o-r
43
取代的碳数为1~18的烷基、可以被芳基取代的碳数为1~8的烷基、或可以被羟基取代的碳数为1~8的烷基,或者r7和r8相互连接形成可含有o原子的4~7元环。
[0111]
r5与r7或r8不相互连接而不形成环。
[0112]
a+b优选为1或2,更优选为1。c+d优选为1或2,更优选为1。
[0113]
式(1)所示的化合物优选为下述式(1-1)所示的化合物。
[0114]
【化学式10】
[0115][0116]r24
表示氢原子、碳数为6~24的烃基、或r
21-l
1-r
22-所示的基团,r
21
表示碳数为1~24的烃基,l1表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0117]
【化学式11】
[0118][0119]r22
表示二价的连接基团碳数为1~18的烃连接基团。
[0120]r25
表示氢原子、碳数为3~24的烃基、或r
31-l
2-r
32-所示的基团,r
31
表示碳数为1~24的烃基,l2表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0121]
【化学式12】
[0122][0123]r32
表示二价的连接基团碳数为1~18的烃连接基团。
[0124]
r4、r5、r6、r7、r8、r
10
和r
12
分别独立地表示氢原子、或可以被取代的碳数为1~18的烷基,
[0125]
r4和r5、r
10
和r5、r5和r
12
、r4和r6、r5和r6、r6和r7、r6和r
10
、r
12
和r7、以及r7和r8中的任一组以上可相互连接形成可含有o原子的4~7元环。其中,优选r5与r7或r8不相互连接而不形成环。
[0126]
可以被取代的碳数为1~18的烷基上的取代基为羟基、羧基、-nr
45r46
所示的氨基、取代或未取代的芳基、取代或未取代的杂芳基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,取代或未取代的芳基、和取代或未取代的杂芳基上的取代基为碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基。
[0127]
式(1-1)中的r4、r5、r6、r7、r8、r
10
和r
12
的定义及优选的范围与式(1)中相同。
[0128]
式(1-1)的r
24
优选为碳数为6~24的烷基或烯基。碳数为6~24的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数为6~24的烷基优选为碳数为8~20的烷基。
具体而言,可举出辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、三甲基十二烷基(优选为3,7,11-三甲基十二烷基)、十四烷基、十五烷基、十六烷基、四甲基十六烷基(优选为3,7,11,15-四甲基十六烷基)、十七烷基、十八烷基、十九烷基、二十烷基等。碳数为6~24的烯基可以是直链也可以是支链,可以是链状也可以是环状。碳数为6~24的烯基优选为碳数为8~20的烯基。具体而言,可举出辛烯基、壬烯基、癸烯基、十一碳烯基、十二碳烯基、十二碳二烯基、十三碳烯基、十四碳烯基、十五碳烯基、十六碳烯基(优选为(z)-十六碳-9-烯基)、十六碳二烯基、十七碳烯基(优选为(z)-十七碳-8-烯基)、十七碳二烯基(优选为(8z,11z)-十七碳-8,11-二烯基)、十八碳烯基(优选为(z)-十八碳-9-烯基)、十八碳二烯基(优选为(9z,12z)-十八碳-9,12-二烯基)、十九碳烯基、二十碳烯基(优选为(z)-二十碳-11-烯基)、二十碳二烯基(优选为(11,14)-二十碳-11,14-二烯基)等。
[0129]
优选上述烯基均具有1个或2个双键。
[0130]
式(1-1)的r
25
优选为碳数为6~24的烷基或烯基。碳数为6~24的烷基可以是直链也可以是支链,可以是链状也可以是环状。碳数为6~24的烷基优选为碳数为7~20的烷基。具体而言,可举出己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、三甲基十二烷基(优选为3,7,11-三甲基十二烷基)、十四烷基、十五烷基、十六烷基、四甲基十六烷基(优选为3,7,11,15-四甲基十六烷基)、十七烷基、十八烷基等。碳数为6~24的烯基可以是直链也可以是支链,可以是链状也可以是环状。碳数为6~24的烯基优选为碳数为8~20的烯基。具体而言,可举出辛烯基、壬烯基、癸烯基、十一碳烯基、十二碳烯基、十二碳二烯基、十三碳烯基、十四碳烯基、十五碳烯基、十六碳烯基(优选为(z)-十六碳-9-烯基)、十六碳二烯基、十七碳烯基(优选为(z)-十七碳-8-烯基)、十七碳二烯基(优选为(8z,11z)-十七碳-8,11-二烯基)、十八碳烯基(优选为(z)-十八碳-9-烯基)、十八碳烯基(优选为(9z,12z)-十八碳-9,12-二烯基)、十九碳烯基、二十碳烯基(优选为(z)-二十碳-11-烯基)、二十碳二烯基(优选为(11,14)-二十碳-11,14-二烯基)等。
[0131]
优选上述烯基均具有1个或2个双键。
[0132]
在优选的方式中,
[0133]
x表示-o-;
[0134]
r2、r3、r
31
、l2和r
32
的定义与式(1)中的定义为同义,
[0135]
r4、r5、r6、r7、r8、r9、r
10
、r
11
、和r
12
分别独立地表示氢原子或可以被取代的碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基、以及取代或未取代的芳基、和取代或未取代的杂芳基上的取代基的定义与式(1)中的定义为同义,
[0136]
a+b为1,c+d为1或2。
[0137]
进一步优选的方式中,式(1)所示的化合物为下述式(2)所示的化合物。
[0138]
【化学式13】
[0139][0140]
式中,r2和r3分别独立地表示氢原子、碳数为3~24的烃基、或r
31-l
2-r
32-所示的基团,
[0141]r31
表示碳数为1~24的烃基,
[0142]
l2表示-o(co)o-、-o(co)-、-(co)o-、-o、或
[0143]
【化学式14】
[0144][0145]r32
表示属于二价连接基团的碳数为1~18的烃连接基团,
[0146]
r5表示氢原子、或可以被取代的碳数为1~18的烷基,
[0147]
r7和r8分别独立地表示氢原子、或可以被取代的碳数为1~18的烷基,
[0148]
可以被取代的碳数为1~18的烷基上的取代基为羟基、羧基、-nr
45r46
所示的氨基、取代或未取代的芳基、取代或未取代的杂芳基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,
[0149]r41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,取代或未取代的芳基、和取代或未取代的杂芳基上的取代基为碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,
[0150]r41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,e表示2或3。
[0151]
r2、r3、r5、r7和r8的定义与式(1)中的定义相同。
[0152]
式(2)中,优选r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,r5中的可以被取代的碳数为1~18的烷基上的取代基为羟基、取代或未取代的芳基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基,取代或未取代的芳基上的取代基为碳数为1~18的烷基、羟基、羧基、-nr
45r46
所示的氨基、-o(co)o-r
41
、-o(co)-r
42
、-(co)o-r
43
、或-o-r
44
所示的基团,r
41
、r
42
、r
43
、r
44
、r
45
和r
46
分别独立地表示碳数为1~18的烃基。
[0153]
式(2)中,进一步优选r2和r3分别独立地表示碳数为3~24的烃基、或r
31-l
2-r
32-所示的基团,l2表示-o(co)或-(co)o-,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基为未取代的芳基、-o(co)-r
42
、或-(co)o-r
43
,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0154]
式(2)中,进一步优选r2和r3分别独立地表示氢原子、或碳数为3~24的烃基,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基为未取代的芳基、-o(co)-r
42
、或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0155]
式(2)中,优选r2和r3中的至少一个表示r
31-l
2-r
32-所示的基团,l2表示-o(co)或-(co)o-,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基为未取代的芳基、-o(co)-r
42
、或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0156]
式(2)中,进一步优选r2和r3分别独立地表示r
31-l
2-r
32-所示的基团,l2表示-o(co)或-(co)o-,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基为未取代的芳基、-o(co)-r
42
、或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0157]
式(2)中,优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为3~24的烃基,l2表示-o(co)或-(co)o-,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基为未取代的芳基、-o(co)-r
42
或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0158]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为6的烃基,l2表示-o(co)或-(co)o-,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,可以被取代的碳数为1~18的烷基上的取代基为-o(co)-r
42
或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0159]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为6的烃基,l2表示-o(co)或-(co)o-,r5表示氢原子、或碳数为1~18的烷基,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基。
[0160]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为6的烃基,l2表示-o(co)或-(co)o-,r5表示氢原子、或碳数为1~18的烷基,r7和r8分别独立地表示氢原子或碳数为1~18的烷基,e表示2。
[0161]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为3~5的烃基,l2表示-o(co)或-(co)o-,r5表示氢原子、或碳数为1~18的烷基,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基。
[0162]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为3~5的烃基,l2表示-o(co)或-(co)o-,r5表示氢原子、或碳数为1~18的烷基,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,e表示2。
[0163]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为6的烃基,l2表示-o(co)或-(co)o-,r5表示氢原子、或被取代的碳数为1~18的烷基,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,被取代的碳数为1~18的烷基上的取代基为-o(co)-r
42
或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基。
[0164]
式(2)中,进一步优选r2和r3中的一个表示r
31-l
2-r
32-所示的基团,r2和r3中的另一个表示碳数为6的烃基,l2表示-o(co)或-(co)o-,r5表示氢原子、或被取代的碳数为1~18的烷基,r7和r8分别独立地表示氢原子、或碳数为1~18的烷基,被取代的碳数为1~18的烷基上的取代基为-o(co)-r
42
或-(co)o-r
43
所示的基团,r
42
和r
43
分别独立地表示碳数为1~18的烃基,e表示2。
[0165]
式(1)表示的化合物可以形成盐。
[0166]
作为碱性基团中的盐,例如可举出与盐酸、氢溴酸、硝酸及硫酸等无机酸的盐;与甲酸、乙酸、柠檬酸、草酸、富马酸、马来酸、琥珀酸、苹果酸、酒石酸、天冬氨酸、三氯乙酸和三氟乙酸等有机羧酸的盐;以及与甲磺酸、苯磺酸、对甲苯磺酸、均三甲苯磺酸和萘磺酸等磺酸的盐。
[0167]
作为酸性基团中的盐,例如可举出与钠和钾等碱金属的盐;与钙和镁等碱土金属的盐;铵盐;以及与三甲胺、三乙胺、三丁胺、吡啶、n,n-二甲基苯胺、n-甲基哌啶、n-甲基吗啉、二乙胺、二环己基胺、普鲁卡因、二苄基胺、n-苄基-β-苯乙基胺、1-二苯羟甲胺和n,n
’‑
二苄基乙二胺等含氮有机碱的盐等。
[0168]
在上述的盐中,作为优选的盐,可举出药理学上可接受的盐。
[0169]
对式(1)所示的化合物的制造方法进行说明。
[0170]
式(1)所示的化合物可以通过将公知的方法组合来制造,例如可以按照以下所示的制造方法来制造。
[0171]
[制造方法1]
[0172]
【化学式15】
[0173][0174]“式中,ra和rb表示离去基团;rc、rd和re表示氨基保护基或亚氨基保护基;r1、r2、r3、r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
具有与上述相同的含义;”作为离去基团,例如可举出氯基、氟基、溴基、三氯甲氧基、4-硝基-苯氧基、2,4-二硝基苯氧基、2,4,6-三氯苯氧基、五氟苯氧基、2,3,5,6-四氟苯氧基、咪唑基、三唑基、3,5-二氧代-4-甲基-1,2,4-噁二唑啶基、n-羟基琥珀酰亚胺基等。作为氨基保护基或亚氨基保护基,例如可举出叔丁氧基羰基、苄氧基羰基、2-硝基苯磺酰基、苄基等。
[0175]
(1-1)
[0176]
作为式[3]的化合物,例如已知氯甲酸4-硝基苯酯、1,1
’‑
羰基二咪唑、三光气和光气等。
[0177]
式[4]的化合物可以通过在碱的存在下使式[2]的化合物与式[3]的化合物反应来制造。
[0178]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类和芳香族烃类,这些溶剂可以混合使用。
[0179]
作为优选的溶剂,可举出醚类,更优选四氢呋喃。溶剂的用量没有特别限定,相对于式[2]的化合物为1~500倍量(v/w)即可。
[0180]
作为该反应中使用的碱,可举出无机碱或有机碱。碱优选为有机碱,具体而言,可举出三乙胺、n,n-二异丙基乙胺、4-甲基吗啉、吡啶、或n,n-二甲基氨基吡啶等。
[0181]
关于碱的用量,相对于式[2]的化合物为1~50倍摩尔、优选为1~10倍摩尔即可。
[0182]
式[3]的化合物的用量没有特别限定,相对于式[2]的化合物为0.3~10倍量(v/w)即可。
[0183]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0184]
(1-2)
[0185]
作为式[5]的化合物,例如已知有(9z,12z)-二((9z,12z)-十八碳-9,12-二烯-1-基)胺和二(十六烷基)胺等。
[0186]
式[6]的化合物可以通过在碱的存在下使式[4]的化合物与式[5]的化合物反应来制造。
[0187]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类和芳香族烃类,这些溶剂可以混合使用。
[0188]
作为优选的溶剂,可举出醚类,更优选四氢呋喃。溶剂的用量没有特别限定,相对于式[4]的化合物为1~500倍量(v/w)即可。
[0189]
作为该反应中使用的碱,可举出无机碱或有机碱。碱优选为有机碱,具体而言,可举出三乙胺、n,n-二异丙基乙胺、4-甲基吗啉、吡啶、或n,n-二甲基氨基吡啶等。
[0190]
关于碱的用量,相对于式[4]的化合物为1~50倍摩尔、优选为1~10倍摩尔即可。
[0191]
式[5]的化合物的用量没有特别限定,相对于式[4]的化合物为1~10倍量(v/w)即可。
[0192]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0193]
(1-3)
[0194]
作为式[2a]的化合物,例如已知叔丁基(2-((叔丁氧基羰基)氨基)乙基)(2-羟基乙基)氨基甲酸酯和叔丁基(2-((2-羟基乙基)(甲基)氨基)乙基)氨基甲酸酯等。
[0195]
式[6a]的化合物可以通过在碱的存在下使式[2a]的化合物与式[3]的化合物反应后,在碱的存在下使式[4a]的化合物与式[5]的化合物反应来制造。
[0196]
该反应按照制造方法(1-1)和(1-2)进行即可。
[0197]
(1-4)
[0198]
式[6]的化合物可以通过对式[6a]的化合物进行脱保护来制造。
[0199]
该反应例如按照t.w.greene等、protective groups in organic synt hesis第4版、第696~926页、2007年、john wiley&sons,inc.中记载的方法进行即可。
[0200]
[制造方法2]
[0201]
【化学式16】
[0202][0203]“式中,ra和rb表示离去基团;rc、rd和re表示氨基保护基或亚氨基保护基;r1、r2、r3、r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
具有与上述相同的含义“;作为离去基团,例如可举出氯基、氟基、溴基、三氯甲氧基、4-硝基-苯氧基、2,4-二硝基苯氧基、2,4,6-三氯苯氧基、五氟苯氧基、2,3,5,6-四氟苯氧基、咪唑基、三唑基、3,5-二氧代-4-甲基-1,2,4-噁二唑啶基、n-羟基
琥珀酰亚胺基等。作为氨基保护基或亚氨基保护基,例如可举出叔丁氧基羰基、苄氧基羰基、2-硝基苯磺酰基、苄基等。
[0204]
(2-1)
[0205]
作为式[3]的化合物,例如已知氯甲酸4-硝基苯酯、1,1
’‑
羰基二咪唑、三光气和光气等。
[0206]
式[8]的化合物可以通过在碱的存在下使式[7]的化合物与式[3]的化合物反应来制造。
[0207]
该反应按照制造方法(1-1)进行即可。
[0208]
(2-2)
[0209]
式[9]的化合物可以通过在碱的存在下使式[8]的化合物与式[2]的化合物反应来制造。
[0210]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类和芳香族烃类,这些溶剂可以混合使用。
[0211]
作为优选的溶剂,可举出醚类,更优选四氢呋喃。溶剂的用量没有特别限定,相对于式[8]的化合物为1~500倍量(v/w)即可。
[0212]
作为该反应中使用的碱,可举出无机碱或有机碱。碱优选为有机碱,具体而言,可举出三乙胺、n,n-二异丙基乙胺、4-甲基吗啉、吡啶、或n,n-二甲基氨基吡啶等。
[0213]
关于碱的用量,相对于式[8]的化合物为1~50倍摩尔、优选为1~10倍摩尔即可。
[0214]
式[2]的化合物的用量没有特别限定,相对于式[8]的化合物为1~10倍量(v/w)即可。
[0215]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0216]
(2-3)
[0217]
式[2a]的化合物例如已知叔丁基(2-((叔丁氧基羰基)氨基)乙基)(2-羟基乙基)氨基甲酸酯和叔丁基(2-((2-羟基乙基)(甲基)氨基)乙基)氨基甲酸酯等。
[0218]
式[9]的化合物可以通过在碱的存在下使式[8]的化合物与式[2a]的化合物反应后,在碱的存在下对式[9a]的化合物进行脱保护来制造。
[0219]
该反应按照制造方法(2-2)和(1-4)进行即可。
[0220]
[制造方法3]
[0221]
【化学式17】
[0222][0223]“式中,ra、rb和rg表示离去基团;rf表示碳数为1~18的烷基;r1、r2、r3、r4、r5、r6、r7、r8、r9、r
10
、r
11
、r
12
和r
42
具有与上述相同的含义;”作为离去基团,例如可举出氯基、氟基、溴基、三氯甲氧基、4-硝基-苯氧基、2,4-二硝基苯氧基、2,4,6-三氯苯氧基、五氟苯氧基、2,3,5,6-四氟苯氧基、咪唑基、三唑基、3,5-二氧代-4-甲基-1,2,4-噁二唑啶基、n-羟基琥珀酰亚胺基等。
[0224]
(3-1)
[0225]
作为式[3]的化合物,例如已知氯甲酸4-硝基苯酯、1,1
’‑
羰基二咪唑、三光气和光气等。
[0226]
式[8]的化合物可以通过在碱的存在下使式[7]的化合物与式[3]的化合物反应来制造。
[0227]
该反应按照制造方法(1-1)进行即可。
[0228]
(3-2)
[0229]
作为式[2b]的化合物,例如已知2,2
’‑
((2-(二乙基氨基)乙基)氮烷二基)双(乙烷-1-醇)和2,2
’‑
((3-(二乙基氨基)丙基)氮烷二基)双(乙烷-1-醇)等。
[0230]
式[9b]的化合物可以通过在碱的存在下使式[8]的化合物与式[2b]的化合物反应来制造。
[0231]
该反应按照制造方法(2-2)进行即可。
[0232]
(3-3)
[0233]
作为式[10a]的化合物,例如已知十二烷酸、癸酸、壬酸及辛酸等。
[0234]
式[9c]的化合物可以通过在缩合剂或酰卤化物的存在下、在碱的存在下使式[9b]的化合物与式[10a]的化合物反应来制造。
[0235]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类和芳香族烃类,这些溶剂可以混合使用。
[0236]
作为优选的溶剂,可举出醚类,更优选四氢呋喃。溶剂的用量没有特别限定,相对于式[9b]的化合物为1~500倍量(v/w)即可。
[0237]
作为该反应中使用的碱,可举出无机碱或有机碱。碱优选为有机碱,具体而言,可举出三乙胺、n,n-二异丙基乙胺、4-甲基吗啉、吡啶、或n,n-二甲基氨基吡啶等。
[0238]
关于碱的用量,相对于式[9b]的化合物为1~50倍摩尔,优选为1~10倍摩尔即可。
[0239]
作为该反应中使用的缩合剂,例如可举出n,n
’‑
二环己基碳二亚胺和1-乙基-3-(3-二甲基氨基丙基)碳二亚胺等碳二亚胺类;羰基二咪唑等羰基类;叠氮磷酸二苯酯等酸叠氮化物类;氰基磷酸二乙酯等酸氰化物类;2-乙氧基-1-乙氧基羰基-1,2-二氢喹啉;o-苯并三唑-1-基-1,1,3,3-四甲基脲鎓=六氟磷酸盐和o-(7-氮杂苯并三唑-1-基)-1,1,3,3-四甲基脲鎓=六氟磷酸盐等。
[0240]
作为该反应中使用的酰卤化物,例如可举出乙酰氯和三氟乙酰氯等羧酰卤化物类;甲磺酰氯和对甲苯磺酰氯等磺酰卤化物类;氯甲酸乙酯和氯甲酸异丁酯等氯甲酸酯类等。
[0241]
式[10a]的化合物的用量没有特别限定,相对于式[9b]的化合物为1~10倍量(v/w)即可。
[0242]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0243]
(3-4)
[0244]
作为式[10b]的化合物,例如已知十二烷酰氯、癸酰氯、壬酰氯及辛酰氯等。
[0245]
式[9c]的化合物可以通过在碱的存在下使式[9b]的化合物与式[10b]的化合物反应来制造。
[0246]
式[10b]的化合物可以通过使式[10a]的化合物与硫酰氯或草酰氯等反应来制造。
[0247]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类和芳香族烃类,这些溶剂可以混合使用。
[0248]
作为优选的溶剂,可举出醚类,更优选四氢呋喃。溶剂的用量没有特别限定,相对于式[9b]的化合物为1~500倍量(v/w)即可。
[0249]
作为该反应中使用的碱,可举出无机碱或有机碱。
[0250]
关于碱的用量,相对于式[9b]的化合物为1~50倍摩尔,优选为1~10倍摩尔即可。
[0251]
式[10b]的化合物的用量没有特别限定,相对于式[2b]的化合物为1~10倍量(v/w)即可。
[0252]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0253]
接着,对作为本发明化合物的制造原料的式[2]的化合物的合成进行说明。
[0254]
[制造方法4]
[0255]
【化学式18】
[0256][0257]“式中,rh和ri表示离去基团;r4、r5、r6、r7、r8、r9、r
10
、r
11
和r
12
具有与上述相同的含义;”作为离去基团,例如可举出氯基、溴基、碘基、甲磺酰基、4-甲苯磺酰基、氯甲烷磺酰基、三氟甲烷磺酰基等。
[0258]
(4-1)
[0259]
作为式[12]的化合物,例如已知2-氯-n,n-二甲基乙烷-1-胺、4-(2-氯乙基)吗啉和2-氯-n,n-二乙基乙烷-1-胺、2-溴-n,n-二乙基乙烷-1-胺、3-氯-n,n-二乙基乙烷-1-胺等。
[0260]
式[2]的化合物可以通过在碱的存在下或不存在下使式[11]的化合物与式[12]的化合物反应来制造。
[0261]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出醇类、卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类、芳香族烃类和水,这些溶剂可以混合使用。
[0262]
溶剂的用量没有特别限定,相对于式[11]的化合物为1~500倍量(v/w)即可。
[0263]
作为该反应中使用的碱,可举出无机碱或有机碱。关于碱的用量,相对于式[11]的化合物为1~10000倍摩尔、优选为1~5000倍摩尔即可。
[0264]
式[12]的化合物的用量没有特别限定,相对于式[11]的化合物为1~10倍量(v/w)即可。
[0265]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0266]
(4-2)
[0267]
作为式[14]的化合物,例如已知2-溴乙烷-1-醇和3-溴丙烷-1-醇等。
[0268]
式[2]的化合物可以通过在碱的存在下或不存在下使式[13]的化合物与式[14]的化合物反应来制造。
[0269]
该反应按照制造方法(4-1)进行即可。
[0270]
[制造方法5]
[0271]
【化学式19】
[0272][0273]“式中,rj表示离去基团;rk表示碳数为1~18的烷基;r4、r5、r6、r7、r8、r9、r
10
、r
11
、r
12
和r
43
具有与上述相同的含义;”作为离去基团,例如可举出氯基、溴基、碘基、甲磺酰基、4-甲苯磺酰基、氯甲烷磺酰基、三氟甲烷磺酰基等。
[0274]
(5-1)
[0275]
作为式[15a]的化合物,例如已知丙烯酸庚酯等。
[0276]
式[2]的化合物可以通过在碱的存在下或不存在下使式[2c]的化合物与式[15a]的化合物反应来制造。
[0277]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出醇类、卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类、芳香族烃类和水,这些溶剂可以混合使用。
[0278]
作为优选的溶剂,可举出醚类或腈类,更优选四氢呋喃或乙腈。
[0279]
溶剂的用量没有特别限定,相对于式[2c]的化合物为1~500倍量(v/w)即可。
[0280]
作为该反应中使用的碱,可举出无机碱或有机碱。
[0281]
关于碱的用量,相对于式[2c]的化合物为1~10000倍摩尔,优选为1~5000倍摩尔即可。
[0282]
式[15a]的化合物的用量没有特别限定,相对于式[13]的化合物为1~10倍量(v/w)即可。
[0283]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0284]
(5-2)
[0285]
作为式[15b]的化合物,例如已知3-氯丙酸庚酯等。
[0286]
式[2]的化合物可以通过在碱的存在下或不存在下使式[2c]的化合物与式[15b]的化合物反应来制造。
[0287]
该反应按照制造方法(4-1)进行即可。
[0288]
[制造方法6]
[0289]
【化学式20】
[0290][0291]“式中,rg和r
l
表示离去基团;rm表示碳数为1~18的烷基;r4、r5、r6、r7、r8、r9、r
10
、r
11
、r
12
和r
42
具有与上述相同的含义;”作为离去基团,例如可举出氯基、溴基、碘基、甲磺酰基、4-甲苯磺酰基、氯甲烷磺酰基、三氟甲烷磺酰基、三氯甲氧基、4-硝基-苯氧基、2,4-二硝基苯氧基、2,4,6-三氯苯氧基、五氟苯氧基、2,3,5,6-四氟苯氧基、咪唑基、三唑基、3,5-二氧代-4-甲基-1,2,4-噁二唑啶基、n-羟基琥珀酰亚胺基等。
[0292]
(6-1)
[0293]
作为式[10a]的化合物,例如已知十二烷酸、癸酸、壬酸和辛酸等。
[0294]
式[2]的化合物可以通过在缩合剂或酰卤化物的存在下、在碱的存在下使式[2b]的化合物与式[10a]的化合物反应来制造。
[0295]
该反应按照制造方法(3-3)进行即可。
[0296]
(6-2)
[0297]
作为式[10b]的化合物,例如已知十二烷酰氯、癸酰氯、壬酰氯及辛酰氯等。
[0298]
式[2]的化合物可以通过在碱的存在下使式[2b]的化合物与式[10b]的化合物反应来制造。
[0299]
该反应按照制造方法(3-4)进行即可。
[0300]
(6-3)
[0301]
作为式[16]的化合物,例如已知3-氯丙酸庚酯等。
[0302]
式[2]的化合物可以通过在碱的存在下或不存在下使式[2c]的化合物与式[16]的化合物反应来制造。
[0303]
该反应按照制造方法(4-1)进行即可。
[0304]
[制造方法7]
[0305]
【化学式21】
[0306][0307]“式中,rn、ro和r
p
表示碳数为1~17的烷基;r4、r5、r6、r7、r8、r9、r
10
、r
11
、r
12
、r
42
和r
43
具有与上述相同的含义。”[0308]
(7-1)
[0309]
作为式[17a]的化合物,例如已知甲醛、乙醛、丙醛、丁醛、戊醛、己醛、庚醛和辛醛等。
[0310]
式[2]的化合物可以通过在还原剂的存在下、在还原催化剂的存在下或不存在下、酸的存在下或不存在下,使式[2c]的化合物与式[17a]的化合物反应来制造。
[0311]
作为该反应中使用的溶剂,只要不对反应产生影响,就没有特别限定,例如可举出醇类、卤代烃类、醚类、酯类、酰胺类、腈类、亚砜类、芳香族烃类和水,这些溶剂可以混合使用。
[0312]
溶剂的用量没有特别限定,相对于式[2c]的化合物为1~500倍量(v/w)即可。
[0313]
作为该反应中使用的酸,可举出无机酸或有机酸。
[0314]
酸的用量相对于式[2c]的化合物,为0.01~10000倍摩尔,优选为0.05~100倍摩尔即可。
[0315]
作为该反应中使用的还原剂,例如可举出三乙酰氧基硼氢化钠、氰基硼氢化钠、2-甲基吡啶硼烷、甲酸和氢等。
[0316]
作为该反应中使用的还原催化剂,例如可举出钯-碳、氢氧化钯-碳、铂-碳、铑-碳和钌-碳等。
[0317]
式[17a]的化合物的用量没有特别限定,相对于式[13]的化合物为1~10倍量(v/w)即可。
[0318]
该反应在-30~150℃、优选0~100℃下实施5分钟~48小时即可。
[0319]
(7-2)
[0320]
作为式[17b]的化合物,例如已知2-氧代乙基辛酸酯和2-氧代乙基壬酸酯等。
[0321]
式[2]的化合物可以通过在还原剂的存在下、在还原催化剂的存在下或不存在下、酸的存在下或不存在下,使式[2c]的化合物与式[17b]的化合物反应来制造。
[0322]
该反应按照制造方法(7-1)进行即可。
[0323]
(7-3)
[0324]
作为式[17c]的化合物,例如已知3-氧代丙酸庚酯和3-氧代丙酸辛酯等。
[0325]
式[2]的化合物可以通过在还原剂的存在下、在还原催化剂的存在下或不存在下、酸的存在下或不存在下,使式[2c]的化合物与式[17c]的化合物反应来制造。
[0326]
该反应按照制造方法(7-1)进行即可。
[0327]
在上述的制造方法中使用的化合物中,在存在异构体(例如光学异构体、几何异构体及互变异构体等)的情况下,也可以使用这些异构体。另外,在存在溶剂化物、水合物和各种形状的晶体的情况下,也可以使用它们的溶剂化物、水合物和各种形状的晶体。
[0328]
在上述的制造方法中使用的化合物中,例如具有氨基、羟基或羧基等的化合物可以预先用通常的保护基保护这些基团,反应后,通过自身公知的方法使这些保护基脱离。
[0329]
通过上述的制造方法得到的化合物通过进行例如缩合、加成、氧化、还原、重排、取代、卤化、脱水或水解等自身公知的反应,或者通过将这些反应适当组合,可以衍生为其他化合物。
[0330]
在本发明的药物组合物中,作为式(1)所示的化合物或其盐的脂质相对于总脂质的含量优选为40摩尔%~70摩尔%,更优选为45摩尔%~65摩尔%,进一步优选为50摩尔%~60摩尔%。
[0331]
本发明的药物组合物含有胆固醇。
[0332]
通过含有胆固醇,能够使膜流动性降低,得到脂质粒子的稳定化效果。
[0333]
在本发明的药物组合物中,胆固醇相对于总脂质的含量优选为25摩尔%~60摩尔%,更优选为30摩尔%~55摩尔%,进一步优选为35摩尔%~55摩尔%,特别优选为40摩尔%~50摩尔%。
[0334]
本发明的药物组合物含有具有聚乙二醇结构的脂质。通过含有具有聚乙二醇结构的脂质,能够得到脂质粒子的分散稳定化效果。
[0335]
作为具有聚乙二醇结构的脂质,没有特别限定,可举出peg修饰磷酸乙醇胺、二酰基甘油peg衍生物、二烷基甘油peg衍生物、胆固醇peg衍生物、神经酰胺peg衍生物等。其中,优选二酰基甘油peg。即,作为具有聚乙二醇结构的脂质,优选为具有二酰基甘油结构和聚乙二醇结构的脂质,更优选为二酰基甘油结构的酰基为碳数为12~22的酰基。
[0336]
上述聚乙二醇衍生物的peg链的重均分子量优选为500~5000,更优选为750~3000。
[0337]
在本发明的药物组合物中,具有非离子性亲水性高分子的脂质相对于总脂质的含量优选为0.5摩尔%~10摩尔%,更优选为0.5摩尔%~5摩尔%,进一步优选为0.5摩尔%~3摩尔%,最优选为0.5摩尔%~2摩尔%。
[0338]
本发明的药物组合物可以含有两性离子性脂质。作为两性离子性脂质,优选磷脂。作为磷脂,没有特别限定,可举出磷脂酰胆碱、磷脂酰乙醇胺、鞘磷脂等,优选磷脂酰胆碱和磷脂酰乙醇胺。
[0339]
作为磷脂酰胆碱,没有特别限定,可举出大豆卵磷脂(spc)、氢化大豆卵磷脂(hspc)、蛋黄卵磷脂(epc)、氢化蛋黄卵磷脂(epc)、1,2-二肉豆蔻酰基-sn-甘油-3-磷酸胆碱(dmpc)、1,2-二棕榈酰基-sn-甘油-3-磷酸胆碱(dppc)、1,2-二硬脂酰基-sn-甘油-3-磷酸胆碱(dspc)、1-棕榈酰基-2-油酰基-sn-甘油-3-磷酸胆碱(popc)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(dopc)等。其中,优选二硬脂酰磷脂酰胆碱(dspc)、1,2-二棕榈酰基-sn-甘油-3-磷酸胆碱(dppc)、1,2-二肉豆蔻酰基-sn-甘油-3-磷酸胆碱(dmpc)。
[0340]
作为磷脂酰乙醇胺,没有特别限定,可举出1,2-二肉豆蔻酰基-sn-甘油-3-磷脂酰乙醇胺(dmpe)、1,2-二棕榈酰基-sn-甘油-3-磷脂酰乙醇胺(dpp e)、1,2-二硬脂酰基-sn-甘油-3-磷脂酰乙醇胺(dspe)、1,2-二油酰基-sn-甘油-3-磷脂酰乙醇胺(dope)、1,2-二亚油酰基-sn-甘油-3-磷脂酰乙醇胺(dlope)、1,2-二植烷酰基-sn-甘油-3-磷脂酰乙醇胺(d(phy)pe)、1-棕榈酰基-2-油酰基-sn-甘油-3-磷脂酰乙醇胺(pope)、1,2-二(十四烷基)-sn-甘油-3-磷脂酰乙醇胺、1,2-二(十六烷基)-sn-甘油-3-磷脂酰乙醇胺、1,2-二(十八烷
基)-sn-甘油-3-磷脂酰乙醇胺、1,2-二植烷基-sn-甘油-3-磷脂酰乙醇胺等。
[0341]
这些磷脂中,更优选二硬脂酰磷脂酰胆碱(dspc)、1,2-二棕榈酰基-sn-甘油-3-磷酰胆碱(dppc)、1,2-二肉豆蔻酰基-sn-甘油-3-磷酰胆碱(dmp c)、1,2-二油酰基-sn-甘油-3-磷脂酰乙醇胺(dope),进一步优选二硬脂酰磷脂酰胆碱(dspc)、1,2-二棕榈酰基-sn-甘油-3-磷酰胆碱(dppc),最优选二硬脂酰磷脂酰胆碱(dspc)。
[0342]
在本发明的药物组合物中,两性离子性脂质相对于总脂质的含量优选为0摩尔%~30摩尔%,更优选为0摩尔%~20摩尔%,进一步优选为0摩尔%~10摩尔%。
[0343]
对本发明的药物组合物的制造方法进行说明。
[0344]
药物组合物的制造方法没有限定,可以将作为式(1)所示的化合物或其盐的脂质、非离子性脂质、和具有非离子性亲水性高分子结构的脂质等分类为脂质的成分中的全部或一部分油溶性成分溶解于有机溶剂等而制成油相,使人工sirna等水溶性成分溶解于水中而制成水相,将油相和水相混合来制造。混合可以使用微混合器,也可以通过均化器等乳化机、超声波乳化机、高压喷射乳化机等来进行乳化。
[0345]
或者,也可以通过将含有脂质的溶液通过利用蒸发器等进行的减压干燥或利用喷雾干燥机等进行的喷雾干燥等来制备含有脂质的干燥的混合物,将该混合物添加到水系溶剂中,进一步利用前述的乳化机等进行乳化来制造。
[0346]
作为药物组合物的制造方法的一例,可举出包含下述工序的方法:
[0347]
将作为式(1)所示的化合物或其盐的脂质、非离子性脂质、和具有非离子性亲水性高分子结构的脂质等分类为脂质的成分溶解于有机溶剂而得到油相的工序(a);
[0348]
将工序(a)中得到的油相与含有人工sirna等水溶性成分的水相混合的工序(b);
[0349]
将工序(b)中得到的含有油相和水相的混合液稀释,得到脂质粒子的分散液的工序(c);
[0350]
从工序(c)中得到的脂质粒子的分散液中除去上述有机溶剂的工序(d);
[0351]
调节工序(d)中得到的脂质粒子的分散液的浓度的工序(e)。
[0352]
工序(a)中,包含将分类为脂质的构成成分溶解于有机溶剂(乙醇等醇或酯等)中的工序。溶解于有机溶剂后的总脂质浓度没有特别限定,通常为1mmol/l~100mmol/l,优选为5mmol/l~50mmol/l,更优选为10mm ol/l~30mmol/l。
[0353]
在工序(b)中,水相可以通过将人工sirna溶解于水或缓冲液中来得到。根据需要可以添加抗氧化剂等成分。将水相和油相混合的比率(质量比)优选为5:1~1:1,更优选为4:1~2:1。
[0354]
在工序(d)中,作为从脂质粒子的分散液中除去有机溶剂的方法,没有特别限定,可以使用通常的方法,例如可以通过使用磷酸缓冲生理盐水进行透析来除去有机溶剂。
[0355]
在工序(e)中,可以调整工序(d)中得到的分散液的浓度。在进行稀释的情况下,可以使用磷酸缓冲生理盐水、生理盐水等作为稀释液来稀释成适当的浓度。在进行浓缩的情况下,可以通过使用了超滤膜的超滤等将工序(d)中得到的分散液浓缩。也可以直接使用浓缩后的分散液,也可以在浓缩后使用上述稀释液将其调整为所期望的浓度。
[0356]
为了将本发明的脂质粒子的分散液制成药物组合物,优选进行无菌过滤。作为过滤的方法,可以使用中空纤维膜、反渗透膜、膜过滤器等从脂质粒子的分散液中除去不溶的物质。在本发明中,没有特别限定,优选通过能够进行灭菌的具有孔径的过滤器(优选为0.2
μm的过滤灭菌过滤器)进行过滤。另外,进行无菌过滤的工序优选在工序(c)或工序(d)之后。
[0357]
此外,根据需要可以对本发明的脂质粒子的分散液实施冷冻干燥。
[0358]
本发明的药物组合物可以添加包括药学上可接受的水溶液等介质、盐、防腐剂、缓冲剂等在内的添加剂。
[0359]
本发明的药物组合物可以用作处置剂。
[0360]
根据本发明,提供一种对乙型肝炎进行处置的方法,其包含将本发明的药物组合物给药至对象的工序。
[0361]
根据本发明,提供一种对肝硬化或肝癌进行处置的方法,其包含将本发明的药物组合物给药至对象的工序。
[0362]
根据本发明,提供用于在乙型肝炎的处置中使用的本发明的药物组合物。
[0363]
根据本发明,提供用于在肝硬化或肝癌的处置中使用的本发明的药物组合物。
[0364]
根据本发明,提供本发明的药物组合物用于制造乙型肝炎的处置剂的用途。
[0365]
根据本发明,提供本发明的药物组合物用于制造肝硬化或肝癌的处置剂的用途。
[0366]
处置剂的对象包括人和除人以外的哺乳动物。作为除人以外的哺乳动物,例如可举出猴、狗、猫、牛、马、小鼠、大鼠等。
[0367]
处置可以是实现所期望的治疗效果、例如状态进展的阻断或延缓的任意的处置和疗法,包括进展速度的降低、进展速度的停止、状态的好转、状态的治愈或缓解(无论是部分缓解还是完全缓解)、状态的1个或多个症状和/或征兆的预防、延缓、减轻或停止、或者对象或对象的生存比没有处置时所预测的延长。
[0368]
处置也包括预防。例如,通过对乙型肝炎、肝硬化或肝癌容易发病或复发或有其风险的对象进行处置,能够预防或延缓对象的乙型肝炎、肝硬化或肝癌的发病或复发。
[0369]
处置剂的对象疾病是乙型肝炎。另外,作为处置剂的对象疾病,也可以应用于作为乙型肝炎的关联疾病的肝硬化或肝癌。
[0370]
将本发明的药物组合物进行给药时的给药途径没有特别限定,可以通过任意的方法进行给药。作为给药方法,可举出经口给药、非经口给药(关节内给药、静脉内给药、动脉内给药、皮下给药、皮内给药、玻璃体内给药、腹腔内给药、肌肉内给药、阴道内给药、膀胱内给药、髓腔内给药、肺给药、直肠给药、结肠给药、颊给药、鼻给药、小脑延髓池内给药、吸入等),但优选非经口给药。作为非经口给药方法,优选静脉注射、皮下注射、皮内注射、腹腔内注射或肌肉内注射。
[0371]
作为给药量,例如对于一次给药,可以在对象的每1kg体重为0.01mg至100mg的范围内选择给药量。
[0372]
实施例
[0373]
在没有特别记载的情况下,通过柱色谱法进行的精制使用了自动精制装置isolera(biotage公司)或中压液体色谱仪yflc w-prep 2xy(山善株式会社)。
[0374]
在没有特别记载的情况下,硅胶柱色谱法中的载体使用了chro[实施例matorex q-pack si 50(富士silysia化学株式会社)、hi-flash colu mns w001、w002、w003、w004或w005(山善株式会社)。
[0375]
nh硅胶使用chromatorex q-pack nh 60(富士silysia化学株式会社)。
[0376]
nmr光谱使用四甲基硅烷作为内部基准,使用bruker av300(bruke r公司制)或bruker av400(bruker公司制)进行测定,用ppm表示总δ值。
[0377]
ms光谱使用acquity sqd lc/ms系统(waters公司制)进行测定。
[0378]
《化合物的合成》
[0379]
[制造例1]
[0380]
(1)
[0381]
【化学式22】
[0382][0383]
向2-(乙基氨基)乙烷-1-醇(4.0g)、2-溴-n,n-二乙基乙烷-1-胺氢溴酸盐(17.6g)和乙醇(80ml)的混合物中加入碳酸钾(18.6g),在加热回流下搅拌7小时。将反应混合物冷却至室温,滤去不溶物,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,得到淡黄色油状物的2-((2-(二乙基氨基)乙基)(乙基)氨基)乙烷-1-醇(6.5g)。
[0384]
msm/z(m+h):189.
[0385]
【化学式23】
[0386][0387]
在冰冷下向苯甲醛(30.0g)、6-溴己烷-1-醇(56.1g)、三乙基硅烷(67.5ml)、甲苯(300ml)的混合物中加入三氟化硼二乙醚络合物(46.2ml),在该温度下搅拌40分钟。向反应混合物中加入水,分取有机层,用饱和碳酸氢钠水溶液洗涤后,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到无色油状物的(((6-溴己基)氧基)甲基)苯(73.5g)。
[0388]1h-nmr(cdcl3)δ:7.38-7.23(5h,m),4.50(2h,s),3.47(2h,t,j=6.6hz),3.40(2h,t,j=6.6hz),1.92-1.81(2h,m),1.68-1.58(2h,m),1.52-1.35(4h,m).
[0389]
将(((6-溴己基)氧基)甲基)苯(66.7g)和四氢呋喃(200ml)的混合物滴加到镁(7.5g)和四氢呋喃(40ml)的混合物中,在室温下搅拌1小时。在冰冷下向反应混合物中加入甲酸乙酯(8.3g)和四氢呋喃(100ml)的混合物,在该温度下搅拌1小时。将反应混合物在冰冷下倒入10%硫酸水溶液(330ml)中后,加入己烷(300ml),分取有机层,用无水硫酸镁干燥后,减压下蒸馏除去溶剂。在得到的残留物中加入四氢呋喃(200ml)、乙醇(100ml)和10mol/
l氢氧化钾水溶液,在40℃下搅拌1小时。向反应混合物中加入己烷(200ml)和水(100ml),分取有机层后,用无水硫酸镁干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到无色油状物的1,13-双(苄氧基)三癸烷-7-醇(25.3g)。
[0390]1h-nmr(cdcl3)δ:7.36-7.24(10h,m),4.50(4h,s),3.61-3.54(1h,m),3.46(4h,t,j=6.6hz),1.68-1.56(4h,m),1.48-1.26(16h,m).
[0391]
将1,13-双(苄氧基)十三烷-7-醇(24.0g)、10%氢氧化钯-碳(10.0g)和甲醇(240ml)的混合物在氢气气氛下、50℃下搅拌3小时。将反应混合物冷却至室温,将不溶物用硅藻土过滤除去后,在减压下蒸馏除去溶剂。在得到的残留物中加入乙酸乙酯(40ml),滤取固态物,用乙酸乙酯洗涤后,在减压下使其干燥,得到白色固体的十三烷-1,7,13-三醇(11.7g)。
[0392]1h-nmr(cdcl3)δ:3.70-3.55(5h,m),1.64-1.24(20h,m).
[0393]
(3)
[0394]
【化学式24】
[0395][0396]
向十三烷-1,7,13-三醇、癸酸2-己酯、三乙胺、4-二甲基氨基吡啶和n,n-二甲基甲酰胺的混合物中加入1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐,在室温下搅拌15小时。向反应混合物中加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到无色油状物的7-羟基十三烷-1,13-二基双(2-己基癸酸酯)。
[0397]
向7-羟基十三烷-1,13-二基双(2-己基癸酸酯)、三乙胺和四氢呋喃的混合物中加入氯甲酸4-硝基苯酯,在室温下搅拌1小时。向反应混合物中加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到淡黄色油状物的7-(((4-硝基苯氧基)羰基)氧基)十三烷-1,13-二基双(2-己基癸酸酯)。
[0398]1h-nmr(cdcl3)δ:8.28(2h,dd,j=7.2h,2,1hz),7.39(2h,dd,j=7.2hz,2.1hz),4.86-4.76(1h,m),4.07(4h,t,j=6.6hz),2.36-2.25(2h,m),1.72-1.20(68h,m),0.87(12h,t,j=6.0hz).
[0399]
(4)
[0400]
【化学式25】
[0401][0402]
向7-(((4-硝基苯氧基)羰基)氧基)十三烷-1,13-二基双(2-己基癸酸酯)、2-((2-(二乙基氨基)乙基)(乙基)氨基)乙烷-1-醇、三乙胺和四氢呋喃的混合物中加入4-二甲基氨基吡啶,在加热回流下搅拌8小时。将反应混合物冷却至室温,加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(甲醇-乙酸乙酯)和硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,
得到无色油状物的7-(((2-((2-(二乙基氨基)乙基)(乙基)氨基)乙氧基)羰基)氧基)十三烷-1,13-二基双(2-己基癸酸酯)。
[0403]1h-nmr(cdcl3)δ:4.73-4.61(1h,m),4.17(2h,t,j=6.6hz),4.05(4h,t,j=6.6hz),2.76(2h,t,j=6.6hz),2.67-2.46(10h,m),2.36-2.23(2h,m),1.68-1.16(68h,m),1.09-0.97(9h,m),0.94-0.81(12h,m).msm/z(m+h):924.
[0404]
[制造例2]
[0405]
(1)
[0406]
【化学式26】
[0407][0408]
向2-(异丙基氨基)乙烷-1-醇(2.0g)、2-溴-n,n-二乙基乙烷-1-胺氢溴酸盐(7.6g)和乙醇(20ml)的混合物中加入碳酸钾(8.0g),在加热回流下搅拌7小时。将反应混合物冷却至室温,滤去不溶物,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,得到淡黄色油状物的2-((2-(二乙基氨基)乙基)(异丙基)氨基)乙烷-1-醇(3.5g)。
[0409]
msm/z(m+h):203.
[0410]
(2)
[0411]
【化学式27】
[0412][0413]
将10-乙氧基-10-氧代癸酸、亚硫酰氯及n,n-二甲基甲酰胺的混合物在加热回流下搅拌1小时30分钟。减压蒸馏除去溶剂,得到淡黄色油状物的10-氯-10-氧代癸酸乙酯作为粗产物。
[0414]
在-78℃下向氯化锌(ii)的四氢呋喃悬浮液中滴加1.0mol/l癸基溴化镁-二乙醚溶液,升温至0℃后,在该温度下搅拌30分钟。向反应混合物中加入四(三苯基膦)钯(0)和10-氯-10-氧代癸酸乙酯,在0℃下搅拌1小时。向反应混合物中加入1.0mol/l盐酸水溶液和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到褐色油状物的10-氧代二十烷酸乙酯。
[0415]
在10-氧代二十烷酸乙酯和2-丁基辛烷-1-醇的混合物中加入原钛酸四异丙酯,在
110℃下搅拌17小时。向反应混合物中加入水和乙酸乙酯,分取有机层,用无水硫酸钠干燥后,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到淡黄色固体的10-氧代二十烷酸2-丁基辛酯。
[0416]
在冰冷下向10-氧代二十烷酸2-丁基辛酯、甲醇和四氢呋喃的混合物中加入硼氢化钠,在室温下搅拌1小时。将反应混合物倒入冰和水的混合物中后,加入1.0mol/l盐酸水溶液,分取有机层,用无水硫酸钠干燥后,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到白色固体的10-羟基二十烷酸2-丁基辛酯。
[0417]
向10-羟基二十烷酸2-丁基辛酯、三乙胺和四氢呋喃的混合物中加入氯甲酸4-硝基苯酯,在室温下搅拌3小时。向反应混合物中加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用硫酸钠干燥,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到无色油状物的10-(((4-硝基苯氧基)羰基)氧基)二十烷酸2-丁基辛酯。
[0418]
向10-(((4-硝基苯氧基)羰基)氧基)二十烷酸2-丁基辛酯、2-((2-(二乙基氨基)乙基)(异丙基)氨基)乙烷-1-醇、三乙胺和四氢呋喃的混合物中加入4-二甲基氨基吡啶,在加热回流下搅拌。将反应混合物冷却至室温,加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(甲醇-乙酸乙酯)和硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,得到无色油状物的12-癸基-3-乙基-6-异丙基-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯。
[0419]1h-nmr(cdcl3)δ:4.73-4.61(1h,m),4.10(2h,t,j=6.6hz),3.97(2h,d,j=6.0hz),2.99-2.83(1h,m),2.68(2h,t,j=6.6hz),2.62-2.41(8h,m),2.29(2h,t,j=7.2hz),1.69-1.47(7h,m),1.40-1.19(42h,m),1.10-0.96(12h,m),0.94-0.83(9h,m).
[0420]
msm/z(m+h):726.
[0421]
[制造例3]
[0422]
(1)
[0423]
【化学式28】
[0424][0425]
向2,2
’‑
偶氮二基双(乙烷-1-醇)(2.0g)、2-溴-n,n-二乙基乙烷-1-胺氢溴酸盐(7.4g)和乙醇(40ml)的混合物中加入碳酸钾(7.9g),在加热回流下搅拌8小时。将反应混合物冷却至室温,滤去不溶物,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,得到淡黄色油状物的2,2
’‑
((2-(二乙基氨基)乙基)氮烷二基)双(乙烷-1-醇)(2.3g)。
[0426]
msm/z(m+h):205.
[0427]
(2)
[0428]
【化学式29】
[0429][0430]
将10-甲氧基-10-氧代癸酸、亚硫酰氯及n,n-二甲基甲酰胺的混合物在加热回流下搅拌1小时。减压蒸馏除去溶剂,得到褐色油状物的10-氯-10-氧代癸酸甲酯。
[0431]1h-nmr(cdcl3)δ:3.67(3h,s),2.88(2h,t,j=7.2hz),2.30(2h,t,j=7.2hz),1.75-1.57(4h,m),1.38-1.25(8h,m).
[0432]
在-78℃下向氯化锌(ii)的四氢呋喃悬浮液中滴加1.0mol/l己基溴化镁-二乙醚溶液,升温至0℃后,在该温度下搅拌30分钟。在冰冷下向反应混合物中加入四(三苯基膦)钯(0)后,在该温度下滴加10-氯-10-氧代癸酸甲酯,在该温度下搅拌1小时。向反应混合物中加入1.0mol/l盐酸水溶液和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到白色固体的10-氧代十六烷酸甲酯。
[0433]1h-nmr(cdcl3)δ:3.67(3h,s),2.38(4h,t,j=7.2hz),2.30(2h,t,7.2hz),1.65-1.49(6h,m),1.35-1.20(14h,m),0.88(3h,t,j=7.2hz).
[0434]
向10-氧代十六烷酸甲酯和2-丁基辛烷-1-醇的混合物中加入原钛酸四异丙酯,在110℃下搅拌1小时。向反应混合物中加入水,在室温下搅拌15分钟后,通过硅胶柱色谱法(乙酸乙酯-己烷)进行精制,得到无色油状物的10-氧代十六烷酸2-丁基辛酯。
[0435]1h-nmr(cdcl3)δ:3.97(2h,d,j=5.6hz),2.38(4h,t,j=7.6hz),2.29(2h,t,j=7.6hz),1.65-1.50(7h,m),1.35-1.20(30h,m),0.92-0.83(9h,m).
[0436]
在冰冷下向10-氧代十六烷酸2-丁基辛酯、甲醇和四氢呋喃的混合物中加入硼氢化钠,在该温度下搅拌30分钟。将反应混合物倒入冰和水的混合物中后,加入1.0mol/l盐酸水溶液和乙酸乙酯,分取有机层后,用饱和氯化钠水溶液洗涤,用无水硫酸钠干燥后,减压蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到无色油状物的10-羟基十六烷酸2-丁基辛酯。
[0437]1h-nmr(cdcl3)δ:3.97(2h,d,j=6.0hz),3.61-3.54(1h,m),2.30(2h,t,j=7.6hz),1.65-1.56(3h,m),1.48-1.22(38h,m),0.92-0.83(9h,m).
[0438]
向10-羟基十六烷酸2-丁基辛酯、三乙胺和四氢呋喃的混合物中加入氯甲酸4-硝基苯酯,在室温下搅拌4小时。向反应混合物中加入水和乙酸乙酯,分取有机层,用水洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(乙酸乙酯-己烷)精制,得到无色油状物的10-(((4-硝基苯氧基)羰基)氧基)十六烷酸2-丁基辛酯。
[0439]1h-nmr(cdcl3)δ:8.28(2h,dd,j=7.2hz,2.1hz),7.39(2h,dd,j=7.2hz,2.1hz),4.86-4.76(1h,m),3.97(2h,d,j=5.7hz),2.30(2h,t,j=7.2hz),1.74-1.20(41h,m),0.92-0.85(9h,m).
[0440]
(3)
[0441]
【化学式30】
[0442][0443]
向10-(((4-硝基苯氧基)羰基)氧基)十六烷酸2-丁基辛酯、2,2
’‑
((2-(二乙基氨基)乙基)氮烷二基)双(乙烷-1-醇)、三乙胺和四氢呋喃的混合物中加入4-二甲基氨基吡啶,在80℃下搅拌8小时。将反应混合物冷却至室温,加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(甲醇-乙酸乙酯)和硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,得到无色油状物的3-乙基-12-己基-6-(2-羟基乙基)-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯。
[0444]1h-nmr(cdcl3)δ:4.75-4.61(1h,m),4.21(2h,t,j=6.6hz),3.97(2h,d,j=5.7hz),3.55(2h,t,j=5.1hz),2.89(2h,t,j=6.6hz),2.76-2.65(4h,m),2.64-2.41(6h,m),2.30(2h,t,j=8.1hz),1.72-1.45(7h,m),1.40-1.20(34h,m),1.13-0.98(6h,m),0.96-0.81(9h,m).
[0445]
msm/z(m+h):672.
[0446]
(4)
[0447]
【化学式31】
[0448][0449]
向3-乙基-12-己基-6-(2-羟基乙基)-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯、辛酸、三乙胺、4-二甲基氨基吡啶和二氯甲烷的混合物中加入1-乙基-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐,在室温下搅拌6小时。向反应混合物中加入水和乙酸乙酯,分取有机层,用水洗涤后,用无水硫酸镁干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(甲醇-乙酸乙酯)和硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,由此得到无色油状物的3-乙基-12-己基-6-(2-(辛酰基氧基)乙基)-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯。
[0450]1h-nmr(cdcl3)δ:4.71-4.62(1h,m),4.20-4.08(4h,m),3.97(2h,d,j=5.6hz),2.89-2.77(4h,m),2.73-2.42(8h,m),2.29(4h,t,j=7.6hz),1.68-1.48(9h,m),1.39-1.18(42h,m),1.10-0.98(6h,m),0.94-0.81(12h,m).
[0451]
msm/z(m+h):798.
[0452]
[制造例4]
[0453]
(1)
[0454]
【化学式32】
[0455][0456]
使用2-己基癸烷-1-醇代替制造例3中所使用的2-丁基辛烷-1-醇,除此以外,通过与实施例3(2)同样的方法,得到无色油状物的10-(((4-硝基苯氧基)羰基)氧基)十六烷酸2-己基癸酯。
[0457]1h-nmr(cdcl3)δ:8.28(2h,dd,j=7.2hz,2.4hz),7.39(2h,dd,j=7.2hz,2.4hz),4.85-4.77(1h,m),3.97(2h,d,j=5.6hz),2.30(2h,t,j=7.6hz),1.72-1.20(49h,m),0.92-0.85(9h,m).
[0458]
(2)
[0459]
【化学式33】
[0460][0461]
向10-(((4-硝基苯氧基)羰基)氧基)十六烷酸2-己基癸酯、2-((2-(二乙基氨基)乙基)(异丙基)氨基)乙烷-1-醇、三乙胺和四氢呋喃的混合物中加入4-二甲基氨基吡啶,在80℃下搅拌8小时。将反应混合物冷却至室温,加入水和乙酸乙酯,分取有机层,用饱和氯化钠水溶液洗涤后,用无水硫酸钠干燥,减压下蒸馏除去溶剂。将得到的残留物通过硅胶柱色谱法(甲醇-乙酸乙酯)和硅胶柱色谱法(乙酸乙酯-己烷、nh硅胶)精制,得到无色油状物的3-乙基-12-己基-6-异丙基-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-己基癸基)酯。
[0462]1h-nmr(cdcl3)δ:4.72-4.61(1h,m),4.10(2h,t,j=6.6hz),3.97(2h,d,j=5.7hz),2.97-2.87(1h,m),2.68(2h,t,j=6.6hz),2.62-2.40(8h,m),2.29(2h,t,j=7.2hz),1.69-1.49(7h,m),1.40-1.19(42h,m),1.12-0.95(12h,m),0.93-0.82(9h,m).msm/z(m+h):726.
[0463]
《人工sirna的制作》
[0464]
[制造例5]
[0465]
(1)单链核酸分子的合成
[0466]
以下所示的单链核酸分子基于亚磷酰胺法,通过ab13900核酸合成机(商品名、applied biosystems)合成。上述合成中,作为rna酰胺化物,使用emm酰胺化物(国际公开第2013/027843号)(以下同样)。上述酰胺化物的脱保护按照常规方法进行。所合成的单链核酸分子通过hplc进行精制。
[0467]
作为单链核酸分子,分别如上述那样合成下述序列a和序列b所示的hbv基因表达抑制序列。在各单链核酸分子中,p为下式所示的连接分子,
[0468]
【化学式34】
[0469][0470]
【化学式35】
[0471][0472]
使用上式所示的l-脯氨酸二酰胺酰胺化物导入至低聚物中。在各序列中,下划线部分是基因表达抑制序列。
[0473]
(序列a)
[0474]5’‑
cgucugugccuucucaucuucau(序列号1)-p-augaagaugagaaggcacagacggg(序列号2)-3’[0475]
(序列b)
[0476]5’‑
cgucugugccuucucaucuuccc(序列号3)-p-gggaagaugagaaggcacagacggg(序列号4)-3’[0477]
1.体外(in vitro)试验
[0478]
《内包核酸的脂质粒子的制备》
[0479]
参考例101~103中作为阳离子性脂质使用了制造例1中制造的7-(((2-((2-(二乙基氨基)乙基)(乙基)氨基)乙氧基)羰基)氧基)十三烷-1,13-二基双(2-己基癸酸酯)、或制造例2中制造的12-癸基-3-乙基-6-异丙基-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯。
[0480]
比较例101中作为阳离子性脂质使用了通过专利文献4中记载的方法合成的具有以下结构的脂质(比较化合物a)。
[0481]
【化学式36】
[0482][0483]
将上述阳离子性脂质、作为磷脂的dspc(1,2-二硬脂酰基-sn-甘油-3-磷酸胆碱(1,2-distearoyl-sn-glycero-3-phosphocholine)、产品名:coatsome mc-8080;nof corporation)、胆固醇(产品名:cholesterol hp;日本精化株式会社)、作为peg脂质的dmg-peg2000(产品名:sunbright(r)gm-020;nof corporation)按照表1中记载的摩尔比溶解于
乙醇中,使总脂质浓度达到20mmol/l,得到油相。
[0484]
比较例101和102中将biomacromolecules 2013;14,3903-3915中记载的序列的luc2 sirna、比较例103和参考例101~103中将制造例5中制作的序列b的单链核酸(以下,称为sirna01)分别5mg溶解于灭菌水1ml中,用ph为4的10mmol/l乙酸缓冲液稀释,使核酸浓度达到19.7μmol/l,得到水相。接着,使用注射泵在微量混合器(参照日本专利第5288254号公报)中进行混合,使水相和油相的体积比达到水相:油相=3:1,将混合液用磷酸缓冲生理盐水(pbs)稀释2倍。进而,使用pbs进行透析除去乙醇,得到核酸脂质粒子的分散物。将得到的分散物用0.22μm直径的过滤器(sartorius公司制minisart 16534-k)过滤进行灭菌。将sirna相对于混合时的总脂质的质量比记载于表1。
[0485]
表1
[0486][0487]
《粒径和sirna内包率的测定》
[0488]
《粒径的测定》
[0489]
内包有sirna01的脂质粒子的粒径通过对脂质粒子分散液使用粒径测定系统els-z2(大塚电子)在原液的状态下进行测定。
[0490]
《sirna的内包率的评价》
[0491]
(总核酸浓度定量)
[0492]
通过向保持核酸的脂质粒子60μl中添加3mol/l乙酸钠水溶液30μl和糖原9μl,接着添加乙醇1.5ml,将脂质溶解,仅使核酸沉淀。然后,进行离心分离,除去上清液。风干15分钟以上后,加水使其再溶解,使用nan odrop nf1000(thermo fisher scientific)进行浓度测定,由此对总核酸浓度进行定量。
[0493]
(外水相中的核酸浓度的定量)
[0494]
使用quant-it ribogreen rna assay kit(thermo fisher scientific),按照方案进行定量。首先,将上述试剂盒中包含的20
×
te缓冲液用水稀释,制成1
×
te缓冲液。其中,te表示tris/edta(乙二胺四乙酸)。为了仅对外水相的核酸进行定量,用1
×
te缓冲液将保持核酸的脂质粒子分散液稀释至10000倍。
[0495]
将稀释至10000倍的脂质粒子分散液100μl加入96孔板中,接着向样品中加入用1
×
te缓冲液稀释至2000倍的ribogreen试剂(上述的quanti-it ribogreen rna assay kit中所包含的试剂)100μl,使用酶标仪infinitef200(tecan)测定荧光(激发波长:485nm,荧光波长:535nm),由此对外水相中的核酸浓度进行定量。
[0496]
(内包率的计算)
[0497]
使用上述工序中得到的总核酸浓度和外水相中的核酸浓度的定量结果,按照下述式算出核酸脂质粒子的核酸内包率。
[0498]
核酸内包率(%)=(总核酸浓度-外水相中的核酸浓度)
÷
总核酸浓度
×
100
[0499]
将结果示于表2。
[0500]
表2
[0501] 内包率(%)粒径(nm)比较例1016674比较例1028373比较例1038095参考例1019195参考例10210063参考例1038786
[0502]
《体外试验》
[0503]
使用本发明的内包核酸的脂质粒子分散物,如下进行pxb细胞中的抗hbv分析试验。
[0504]
(pxb-细胞中的抗hbv分析)
[0505]
使用从pxb小鼠(人肝细胞嵌合体小鼠)采集的新鲜人肝细胞(pxb细胞、phoenixbio公司制),按照以下的步骤评价抗hbv活性。
[0506]
作为培养基,使用以下的培养基。
[0507]
dmem(sigma公司制)+0.25μg/ml胰岛素(富士胶片和光纯药公司制)+1%青霉素/链霉素(sigma-aldrich公司制)+20mmol/l hepes(sigma-aldrich公司制)+15μg/ml l-脯氨酸(sigma-aldrich公司制)+50nmol/l地塞米松(sigma-aldrich公司制)+5ng/ml egf(peprotech公司制)+0.1mmol/l抗坏血酸2磷酸(富士胶片和光纯药公司制)+10%fbs+2%dmso
[0508]
然后,向上述培养基中分别加入用d-pbs(-)(富士胶片和光纯药公司制)调整成试验浓度的20倍浓度的药剂,制备各药剂的各种浓度的试验液。
[0509]
(1)将以7
×
104细胞/孔接种于96孔微量滴定板的pxb细胞用5%co2培养箱在37℃下孵育至感染日。
[0510]
(2)将pxb-细胞培养上清液来源的hbv(基因型c_jpnat)悬浮于含4%peg-8000的上述培养基中,加入到(1)的平板中,使其达到10copies/细胞,使其感染(100μl/孔),用5%co2培养箱在37℃下孵育1天。
[0511]
(3)除去感染后第1天的培养上清液,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃孵育1天。
[0512]
(4)除去感染后第2天的培养上清液,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育5天。
[0513]
(5)除去感染后第7天的培养上清液,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育5天。
[0514]
(6)除去感染后第12天的培养上清液,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育5天。
[0515]
(7)除去感染后第17天的培养上清液,将试验液加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育。在无药剂添加的对照中,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育。在试验液处理6小时后,除去培养上清液,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育5天。无药剂添加的对照也同样地实施培养基更换。
[0516]
(8)回收感染后第22天的培养上清液,将上述培养基加到平板(100μl/孔)中,用5%co2培养箱在37℃下孵育5天。无药剂添加的对照也同样地实施培养基更换。
[0517]
(9)回收感染后第27天的培养上清液。向剩余的细胞中添加用d-pbs(-)稀释了10倍的celltiter 96aqueous one solution cell proliferation assay(promega公司制)100μl/孔,用5%co2培养箱在37℃染色1~2小时后,测定490及655nm的吸光度,评价细胞活性。细胞活性的t/c%通过以下式所示的方法算出。
[0518]
【数学式1】
[0519][0520]
(10)将回收的感染后第22和27天的培养上清液中的hbsag用lumipulse(注册商标)hbsag-hq(富士rebio公司制)进行绝对定量。分别算出相对于无药剂添加的对照的相对值(%)。浓度用对数、相对值用实数作图,使用microsoft office excel 2007的forecast函数(1次回归法)算出药剂的ic
50
。
[0521]
将结果示于表3、图1。其中,图1中,将感染27天后的细胞活性用相对于无药剂添加孔的相对值表示。示出了3孔的平均值和标准偏差。
[0522]
表3
[0523][0524]
需要说明的是,参考例101~103中使用的序列b的单链核酸与序列a的单链核酸的结构虽不同但类似,与比较例101、102相比,在上述试验中得到了优异的效果。
[0525]
2.体内(in vivo)试验i
[0526]
《内包核酸的脂质粒子的制备》
[0527]
参考例201中作为阳离子性脂质使用了制造例1中制造的7-(((2-((2-(二乙基氨基)乙基)(乙基)氨基)乙氧基)羰基)氧基)十三烷-1,13-二基双(2-己基癸酸酯)、以及参考例202中使用了制造例2中制造的12-癸基-3-乙基-6-异丙基-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯。
[0528]
比较例201和比较例202中作为阳离子性脂质使用了通过专利文献4中记载的方法合成的具有以下结构的脂质(比较化合物a)。
[0529]
【化学式37】
[0530][0531]
将上述阳离子性脂质、作为磷脂的dspc(1,2-二硬脂酰基-sn-甘油-3-磷酸胆碱(1,2-distearoyl-sn-glycero-3-phosphocholine)、产品名:coatso me mc-8080;nof corporation)、胆固醇(产品名:cholesterol hp;日本精化株式会社)、作为peg脂质的dmg-peg2000(产品名:sunbright(r)gm-020;nof corporation)按照表4中记载的摩尔比溶解于乙醇中,使总脂质浓度达到20mmol/l,得到油相。
[0532]
比较例201中将下述所示的序列c的核酸、比较例202和参考例201、202中将制造例5中制作的sirna01 5mg溶解于灭菌水1ml中,用ph为4的10mmol/l乙酸缓冲液稀释,使核酸浓度达到19.7μmol/l,得到水相。接着,使用注射泵在微量混合器(参照日本专利第5288254号公报)中进行混合,使水相和油相的体积比达到水相:油相=3:1,将混合液用磷酸缓冲生理盐水(pbs)稀释2倍。进而,使用pbs进行透析除去乙醇,得到核酸脂质粒子的分散物。将得到的分散物用0.22μm直径的过滤器(sart orius公司制minisart 16534-k)过滤进行灭菌,使用amicon ultra离心式过滤器单元(merck公司制)通过超滤膜进行浓缩后,用pbs稀释至所期望的浓度,得到给药制剂。将sirna相对于混合时的总脂质的质量比示于表4。
[0533]
下述所示的序列c的核酸与制造例5同样地进行合成。
[0534]
(序列c)
[0535]
guaccgcacgucauucguauccc(序列号5)-p-gggauacgaaugacgugcgguacgu(序列号6)
[0536]
表4
[0537][0538]
通过上述方法,制作2次比较例201、202和参考例201、202中使用的制剂,将测定粒径和sirna内包率的结果示于表5。
[0539]
表5
[0540] 内包率(%)粒径(nm)比较例20180~8687~96比较例20271~8692~94参考例20174~8793~97参考例20281~89108~118
[0541]
《体内试验》
[0542]
(人肝细胞嵌合体小鼠的体内药效试验)
[0543]
将hbv基因型c感染后经过了10周的雄性、25周龄以上、体重为17g以上的pxb小鼠
(人肝细胞嵌合小鼠)分为5组(各2或3只)进行使用。
[0544]
将参考例201、参考例202、比较例202、阴性对照的比较例201的制剂分别以1mg/kg每周2次、4周进行静脉内给药。剩余1组作为对照组将磷酸缓冲液以每周2次、4周进行静脉内给药。将初次给药日记为第0天,在第2天、第6天、第13天和第20天时使用七氟醚麻醉,从眼窝静脉丛实施采血。进而,第25天时实施最终给药,给药后30分钟在七氟醚麻醉下打开腹腔,从下腔静脉实施采血。从采集的血液中分离血清,用qiaamp(注册商标)dna blood mini kit(qiagen公司制)精制。对得到的溶液中的hbv-dna量通过实时pcr法进行绝对定量。另外,对血清中的hbsag量分别通过使用了lumipulse(注册商标)hbsag-hq(富士rebio公司制)的化学发光酶免疫测定法进行绝对定量。将结果示于表6。
[0545]
表6
[0546]
血清中hbv-dna(copies/ml)
[0547][0548]
血清中hbsag(iu/ml)
[0549][0550]
nc:未计算(由于n=2,无法算出)
[0551]
通过制剂给药,血清中的hbv-dna和hbsag减少,在人肝细胞嵌合小鼠中也确认到药效。
[0552]
需要说明的是,参考例201、202中使用的序列b的单链核酸与序列a的单链核酸结构虽不同但类似,与比较例201、202相比,获得了优异的药效。
[0553]
3.体内试验ii
[0554]
《内包核酸的脂质粒子的制备》
[0555]
实施例301中作为阳离子性脂质使用了制造例4中制造的3-乙基-12-己基-6-异丙基-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-己基癸基)酯、实施例302中使用了制造例3中制造的3-乙基-12-己基-6-(2-(辛酰基氧基)乙基)-10-氧代-9,11-二氧杂-3,6-二氮杂二十一烷-21-(2-丁基辛基)酯。
[0556]
将上述阳离子性脂质、作为磷脂的dspc(1,2-二硬脂酰基-sn-甘油-3-磷酸胆碱(1,2-distearoyl-sn-glycero-3-phosphocholine)、产品名:coatso me mc-8080;nof corporation)、胆固醇(产品名:cholesterol hp;日本精化株式会社)、作为peg脂质的dmg-peg2000(产品名:sunbright(r)gm-020;nof corporation)按照表7中记载的摩尔比溶解于乙醇中,使总脂质浓度达到20mmol/l,得到油相。
[0557]
将制造例5中制作的序列a的单链核酸(以下称为sirna02)5mg溶解于灭菌水1ml中,实施例301中用ph为4的50mmol/l柠檬酸缓冲液、制造例302中用ph为4的10mmol/l乙酸缓冲液进行稀释,分别使核酸浓度达到19.7μmol/l,得到水相。接着,使用注射泵在微量混合器(参照日本专利第5288254号公报)中进行混合,使水相和油相的体积比达到水相:油相=3:1,将混合液用磷酸缓冲生理盐水(pbs)稀释2倍。进而,使用pbs进行透析除去乙醇,得到核酸脂质粒子的分散物。将得到的分散物用0.22μm直径的过滤器(sartorius公司制minisart 16534-k)过滤进行灭菌,使用amicon ultra离心式过滤器单元(merck公司制)通过超滤膜进行浓缩后,用pbs稀释至所期望的浓度,得到给药制剂。将sirna相对于混合时的总脂质的质量比示于表6。
[0558]
表7
[0559][0560]
《粒径和sirna内包率的测定》
[0561]
通过上述方法,制作3次实施例301、302中使用的制剂,将测定粒径和sirna内包率的结果示于表8。
[0562]
表8
[0563] 内包率(%)粒径(nm)实施例30188~93115~124实施例30289~94105~120
[0564]
《体内试验》
[0565]
(人肝细胞嵌合体小鼠中的体内药效试验)
[0566]
将hbv基因型c感染后经过了9周的雄性、26周龄以上、体重为15g以上的pxb小鼠(人肝细胞嵌合小鼠)分为3组(各3只)进行使用。
[0567]
将实施例301、实施例302的制剂分别以1mg/kg每周2次、6周进行静脉内给药。剩下1组作为对照组将磷酸缓冲液以每周2次、6周进行静脉内给药。将初次给药日记为第0天,在
第1天、第6天、第14天、第20天、第27天和第37天时使用七氟醚麻醉,从眼窝静脉丛实施采血。进而,第37天时实施最终给药,给药后30分钟在七氟醚麻醉下打开腹腔,从下腔静脉实施采血。从采集的血液中分离血清,用qiaamp(注册商标)dn a blood mini kit(qiagen公司制)精制。对得到的溶液中的hbv-dna量通过实时pcr法进行绝对定量。另外,对血清中的hbsag量分别通过使用了lumipulse(注册商标)hbsag-hq(富士rebio公司制)的化学发光酶免疫测定法进行绝对定量。将结果示于表9。
[0568]
表9
[0569]
血清中hbv-dna(copies/ml)
[0570][0571]
血清中hbsag(iu/ml)
[0572][0573]
通过本发明的制剂给药,血清中的hbv-dna和hbsag减少,在人肝细胞嵌合小鼠中也确认到药效。
[0574]
产业上的可利用性
[0575]
本发明的药物组合物能够高效地递送人工sirna,翻译抑制效果优异。因此,本发明的药物组合物作为药物是有用的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1