分散在聚合物基质中的吡唑化合物的药物组合物的制作方法
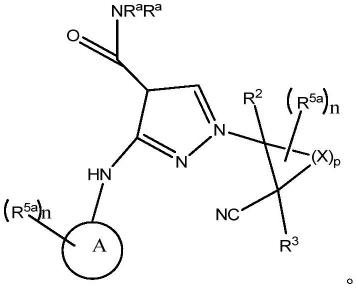
分散在聚合物基质中的吡唑化合物的药物组合物
背景技术:
1.wo 2018/108969公开了式i化合物,其为选择性janus激酶(jak)抑制剂,并且因此可用于治疗jak介导的疾病,例如特应性皮炎、关节炎和癌症。具体地,公开了1-[(3r,4s)-4-氰基四氢吡喃-3-基]-3-[(2-氟-6-甲氧基-4-吡啶基)氨基]吡唑-4-甲酰胺(i)。
[0002][0003]
在cil-31诱导的瘙痒研究中,相对于安慰剂,式(i)化合物显著抑制瘙痒,并且程度与奥拉替尼相似。是用于治疗狗的特应性皮炎的市售产品。还公开了通过口服施用化合物(i)治疗特应性皮炎的方法。
[0004]
wo 2013/041042公开了吡唑甲酰胺作为janus激酶抑制剂,其可用于治疗类风湿性关节炎、哮喘、慢性阻塞性肺病(copd)和癌症。该公开的化合物具有下式:
[0005][0006]
特应性皮炎(ad)是复发性瘙痒症和慢性炎症性皮肤病,其特征在于人的免疫系统失调和表皮屏障异常。特应性皮炎的病理学和免疫学属性已经成为广泛研究的主题[综述于rahman等,inflammation&allergy-drug target 10:486-496(2011)和harskamp等,seminar in cutaneous medicine and surgery 32:132-139(2013)]。特应性皮炎也是伴侣动物,尤其是狗中的常见病症,据估计其患病率为犬科动物群体的大约10-15%。狗和猫的特应性皮炎的发病机理[综述于nuttall等,veterinary records 172(8):201-207(2013)]显示出与人的特应性皮炎的发病机理明显的相似性,其中包括多种免疫细胞的皮肤浸润和cd4
+
th2极化细胞因子环境,包括占多数的il-4、il-13和il-31。此外,il-22涉及过度上皮增殖,导致特应性皮炎特有的表皮增生。
[0007]
申请人已发现,醋酸羟丙基甲基纤维素琥珀酸酯(hpmcas)聚合物基质中式(i)化合物的分散体导致式(i)化合物的生物利用度提高。
技术实现要素:
[0008]
本发明的一个实施方案是药物组合物,其包含分散在hpmcas聚合物基质中的药学上有效量的1-[(3r,4s)-4-氰基四氢吡喃-3-基]-3-[(2-氟-6-甲氧基-4-吡啶基)氨基]吡唑-4-甲酰胺;和药学上可接受的载体。
[0009]
本发明的另一个实施方案是治疗特应性皮炎的方法,其包括向有需要的动物口服施用有效量的上述药物组合物。
[0010]
另一个实施方案是制备药物组合物的方法。
附图说明
[0011]
图1-测定无定形固体分散体(asd)中存在的无定形化合物的量的粉末x射线衍射(pxrd)。
[0012]
图2
–
证实醋酸羟丙基甲基纤维素琥珀酸酯(hpmcas)中式(i)化合物的无定形固体分散体的生物利用度的药代动力学(pk)研究。
[0013]
图3-在体外筛选中评估几种抗成核聚合物维持式(i)化合物的能力。
[0014]
发明详述
[0015]
申请人已经开发了具有化学式(i)化合物1-[(3r,4s)-4-氰基四氢吡喃-3-基]-3-[(2-氟-6-甲氧基-4-吡啶基)氨基]吡唑-4-甲酰胺的制剂,式(i)化合物:
[0016][0017]
式(i)化合物是选择性janus激酶(jak)抑制剂,但是,式(i)化合物是水溶性差的化合物。通常,药物活性剂的水溶性差导致狗中的口服生物利用度差,并因此导致药物的生物学功效差。但是,式(i)化合物是水溶性差的化合物。水溶性差导致狗口服生物利用度差,通常低于50%。式(i)化合物的logp计算为1.25(excel的chemdraw和insight)。为了增强增溶作用和促进生物利用度,申请人已经将无定形状态的化合物作为无定形固体分散体(asd)的一部分给药。由于化合物的高熔点(》250℃)和在挥发性溶剂(如异丙醇、丙酮和二氯甲烷)中的低溶解度,生产asd的常规技术(如喷洒干燥和热熔挤出)不利于制备含有式(i)化合物的asd。因此,通过共沉淀或cpad(共沉淀的无定形分散体)制备asd。在该方法中,将化合物和聚合物溶解在溶剂中。然后在定转子均质机中,在高剪切下在反溶剂中快速沉淀化合物-聚合物溶液,形成化合物-聚合物无定形固体分散体。
[0018]
申请人现已发现,当与含有结晶形式的式(i)化合物的制剂相比时,使用无定形状态的式(i)化合物作为无定形固体分散体的一部分产生具有改善的生物利用度的制剂。
[0019]
基本上为无定形形式是指至少80%的化合物为无定形形式,优选至少90%或95%的化合物为无定形形式。通过pxrd或nmr测量无定形形式相对于结晶形式的百分比。
[0020]
片剂是具有或不具有合适的赋形剂的含有活性成分的固体剂型,并通过压制或模制制备。压制片剂是通过压制形成的片剂。
[0021]
固体分散体是药物在固体基质中的分散体,其中基质是小分子或聚合物。制备固
体分散体的方法是熔融挤出、喷雾干燥和共沉淀。参见huang等,acta pharmaceutica sinica b 2014;4(1),pp 18-25。当活性成分为无定形形式时,这被称为无定形固体分散体(asd)。
[0022]
在药物聚合物基质中,一些聚合物链物理地捕获药物分子。在理想的情况下,药物分子均匀分布在整个聚合物基质中。
[0023]
醋酸羟丙基甲基纤维素琥珀酸酯(hpmcas)聚合物(也称为醋酸羟丙甲纤维素琥珀酸酯)通常作为薄膜包衣以及用于片剂或颗粒剂的肠溶包衣材料被用于口服药物制剂中。这些聚合物是用于固体分散体制剂的溶解度增强剂。hpmcas聚合物已被用作通过喷雾干燥和熔融挤出制备的水溶性差的药物的无定形固体分散体的载体。醋酸羟丙基甲基纤维素琥珀酸酯聚合物是琥珀酸和羟丙基甲基纤维素的醋酸醚的混合物。hpmcas聚合物可以获得几种等级,其中乙酰基、琥珀酰基、甲氧基和羟丙基含量不同。例如,醋酸羟丙基甲基纤维素琥珀酸酯(ashland)的aquasolve
tm
品牌具有如下所示的三级。
[0024]
hpmcas等级乙酰含量琥珀酰基含量甲氧基含量羟丙基含量l5-9%14-18%20-24%5-9%m7-11%10-14%21-25%5-9%h10-14%4-8%22-26%6-10%
[0025]
在一个实施方案中,hpmcas聚合物为l级。在一个实施方案中,hpmcas聚合物为m级。在一个实施方案中,hpmcas聚合物为h级。在一个实施方案中,hpmcas聚合物是两种或更多种等级的混合物。
[0026]
在一个实施方案中,药物载体包括选自填充剂,润滑剂、粘合剂、抗成核剂和崩解剂的一种或多种赋形剂。
[0027]
药物组合物可包含一种或多种润滑剂。润滑剂减少了形成的片剂和用于形成片剂的模具壁之间的摩擦,由此使片剂更容易从模具中取出。润滑剂的示例是硬脂酸镁、滑石、氧化硅和硬脂富马酸钠。在一个实施方案中,润滑剂是硬脂酸镁。
[0028]
药物组合物可包含一种或多种助流剂。助流剂用于改善流动性。在一个实施方案中,助流剂是氧化硅、滑石或其混合物。
[0029]
药物组合物还可包含一种或多种填充剂/压缩助剂。填充剂/压制助剂用于增加具有低剂量活性成分的药物剂型的体积并增加剂型(例如片剂)的机械强度。填充剂的示例是微晶纤维素(mcc)(avicel ph102)、无水乳糖、乳糖一水合物(fast flo 316)、淀粉、多元醇(例如山梨糖醇、甘露糖醇、麦芽糖醇)、麦芽糖糊精、右旋糖、磷酸钙和硫酸钙。在一个实施方案中,填充剂是微晶纤维素、乳糖一水合物纤维素或其混合物。
[0030]
药物组合物还包含一种或多种崩解剂。一旦与液体接触,崩解剂有助于使片剂破碎成更小的片。崩解剂的实例是羟基乙酸淀粉钠(a型)、交联羧甲基纤维素钠和交聚维酮。在一个实施方案中,崩解剂是羟基乙酸淀粉钠(a型)。
[0031]
药物组合物还包含一种或多种粘合剂。粘合剂用于增加剂型(例如片剂)的机械强度。粘合剂也用于促进(湿或干)制粒过程中的颗粒形成。颗粒形成增加了最终共混物的(药物)含量均匀性和流动性。粘合剂的示例是pvp、羟丙基甲基纤维素(hpmc)和羟丙基纤维素(hpc)。在一个实施方案中,粘合剂是羟丙基纤维素(hpc)。
[0032]
药物组合物还包含一种或多种抗成核剂。抗成核剂抑制制剂的结晶。示例包括基
于纤维素的聚合物(例如甲基纤维素和羟丙基甲基纤维素)、泊洛沙姆(例如p68、p88、p98、p108、p125、p188、p237、p338和p407)、聚乙二醇、聚乙烯醇(pva)、乙烯基吡咯烷酮-乙酸乙烯酯共聚物(va64)、聚乙烯吡咯烷酮(pvp)、聚(乳酸-共-乙醇酸)(plga)、甲基纤维素a4c、羟丙基甲基纤维素e50和聚己酸内酯(pcl)。在一个实施方案中,抗成核剂是甲基纤维素a4c或羟丙基甲基纤维素e50。
[0033]
在本发明的一个实施方案中,制剂具有以下组成:
[0034][0035][0036]
在本发明的备选实施方案中,制剂的组分的浓度可以如下所示变化:
[0037][0038]
*微晶纤维素和乳糖一水合物的组合w/w百分比必须至少40%。
[0039]
在实施方案中,药物组合物是固体,优选片剂。
[0040]
本发明的一个实施方案是固体药物组合物,其包含:
[0041]
a)药学上有效量的分散于醋酸羟丙基甲基纤维素琥珀酸酯(hpmcas)聚合物基质中的式(i)化合物:
[0042]
以及
[0043]
b)药学上可接受的载体;
[0044]
其中式(i)化合物基本上以无定形形式存在;以及
[0045]
其中所述药物组合物为片剂。
[0046]
在一个实施方案中,分散体中聚合物与式(i)化合物的比例为约1:1至约20:1或约10:1至约5:1。
[0047]
在一个实施方案中,药物组合物中式(i)化合物的量为约0.5至约10%或约1.0至约5.0%或约2%(w/w)。
[0048]
在一个实施方案中,药物组合物中hpmcas-l聚合物的量为约10%至约30%或约15%至约25%或约20%(w/w)。
[0049]
制备无定形固体分散体(asd)制剂的方法
[0050]
在该方法中,将活性成分(api)和聚合物(i)溶解于溶剂中。然后,在反溶剂中快速沉淀api-聚合物溶液。洗涤沉淀并干燥。形成api和聚合物的无定形固体分散体并压制成片剂。
[0051]
在一个实施方案中,api是式(i)化合物。
[0052]
在一个实施方案中,聚合物是醋酸羟丙基甲基纤维素琥珀酸酯,l级。
[0053]
在一个实施方案中,溶剂是二甲基乙酰胺(dmac或dma)。dmac是具有式ch3c(o)n(ch3)2的有机化合物。
[0054]
在一个实施方案中,反溶剂是ph小于5的酸性水溶液,优选盐酸,优选0.1n hcl。
[0055]
在一个实施方案中,api-聚合物从溶剂中沉淀;在定转子均质机中在高剪切下进行反溶剂。
[0056]
在一个实施方案中,沉淀和洗涤条件为1:10的溶剂:反溶剂沉淀,接着10x浆液洗涤,接着5x置换洗涤。
[0057]
在一个实施方案中,在无定形固体分散体中,式(i)化合物与hpmcas-l聚合物的比例为10:1。
[0058]
在一个实施方案中,在无定形固体分散体中,式(i)化合物与hpmcas-l聚合物的比例为5:1。
[0059]
在一个实施方案中,在asd内部或之间加入表面活性剂、崩解剂和抗成核剂。在一个实施方案中,在asd形成并干燥后,将填充剂、粘合剂、润滑剂共混。
[0060]
本发明的一个实施方案是制备上述药物组合物的方法,所述药物组合物包含:
[0061]
i)将式(i)化合物和聚合物溶解在溶剂中;
[0062]
ii)将步骤i)的溶液与反溶剂混合以沉淀式(i)化合物在聚合物中的无定形固体分散体;
[0063]
iii)将步骤ii)的无定形固体分散体与药学上可接受的载体共混iv)将步骤iii)的产物压制成片剂以产生药物组合物;
[0064]
其中溶剂是二甲基乙酰胺(dmac),且反溶剂是ph小于5的酸性水溶液,优选盐酸溶液,更优选0.1n盐酸。
[0065]
在一个实施方案中,溶剂与反溶剂的比例为1:1至1:50或1:5至1:10。
[0066]
在一个实施方案中,用另外的反溶剂洗涤步骤ii)的沉淀物。
[0067]
在一个实施方案中,药学上可接受的载体包含填充剂、崩解剂、润滑剂、粘合剂和
抗成核剂中的一种或多种。
[0068]
在一个实施方案中,填充剂是微晶纤维素、乳糖或其混合物。
[0069]
在一个实施方案中,崩解剂是羟基乙酸淀粉钠。
[0070]
在一个实施方案中,润滑剂是硬脂酸镁。
[0071]
在一个实施方案中,粘合剂是羟丙基纤维素(hydroxypropylene cellulose)。
[0072]
在一个实施方案中,抗成核剂是甲基纤维素a4c或羟丙基甲基纤维素e50。
[0073]
本发明的一个实施方案是制备药物组合物的方法,所述方法包括:
[0074]
i)将式(i)化合物和聚合物溶解在溶剂中;
[0075]
ii)将步骤i)的溶液与反溶剂混合以沉淀式(i)化合物在聚合物中的分散体;
[0076]
iii)将步骤ii)的分散体与药学上可接受的载体共混;
[0077]
其中所述药物载体包括选自填充剂,润滑剂,粘合剂,抗成核剂和崩解剂的一种或多种赋形剂。
[0078]
治疗方法
[0079]
一种治疗特应性皮炎的方法,其包括向有需要的动物施用有效量的包含式(i)化合物和hpmcas聚合物的药物组合物。
[0080]
一种治疗特应性皮炎的方法,其包括向有需要的动物施用有效量的包含式(i)化合物和hpmcas聚合物的药物组合物,其中所述式(i)化合物的有效量为约0.1至约2.0mg/kg体重。
[0081]
所述药物组合物是口服施用的。
[0082]
在一个实施方案中,待治疗的动物是伴侣动物哺乳动物。在另一个实施方案中,伴侣动物是狗、猫或马。在另一个实施方案中,伴侣动物是狗。
[0083]
在本发明的一个实施方案中,施用于动物的活性成分的剂量为约0.1mg/kg至约2.0mg/kg,约0.2至约0.8mg/kg,约0.3至约0.7mg/kg、约0.5mg/kg、约1.0mg/kg。
[0084]
在一个实施方案中,组合物在没有食物的情况下施用。
[0085]
在一个实施方案中,组合物在进食状态施用。
[0086]
在一个实施方案中,组合物在禁食状态施用。
[0087]
在一个实施方案中,药物组合物每天施用一次,持续28天。
[0088]
在另一个实施方案中,药物组合物每天施用两次,持续14天,接着每天施用一次,持续14天。
[0089]
在其它实施方案中,药物组合物的施用是在上述给药方案之外每天施用,持续有医疗需要的时间,包括动物的存活时间。
[0090]
在一个实施方案中,药物组合物每天施用一次,持续有医疗需要的时间,包括动物的存活时间。
[0091]
在一个实施方案中,药物组合物每天施用两次,持续最多14天,然后每天施用一次,持续有医疗需要的时间,包括动物的存活时间。
[0092]
在一个实施方案中,药物组合物每天施用两次,持续一天、两天、三天、四天、五天、六天、七天、八天、九天、十天、十一天、十二天或十三天,然后每天施用一次,持续有医疗需要的时间,包括动物的存活时间。
[0093]
式(i)化合物的药物组合物可与抗组胺剂、抗生素、止痒剂和神经酰胺组合施用。
这些组合可以同时或依次施用。
实施例
[0094]
实施例1-聚合物基质选择。
[0095]
用多种聚合物(乙烯基吡咯烷酮-乙酸乙烯酯共聚物(va64)、羟丙基甲基纤维素(hpmc)和hpmcas)和挥发性溶剂(四氢呋喃(thf)、甲基乙基酮(mek)、甲基叔丁基醚(mtbe)和庚烷)与式(i)化合物一起进行初步试验。这些实验产生不利于下游加工(如研磨和压制)的溶液、半固体、含有结晶材料的固体或无定形固体。用于制备具有式(i)化合物的asd的多种溶剂和聚合物产生不能共混和压制的黏性材料。其它溶剂/聚合物组合产生极硬的材料,其不能通过常规研磨机研磨至均匀粒度。
[0096]
使用10ml规模的ika ultra-turrax tube drive以10ml规模制备以下列出的式(i)化合物的无定形固体分散体。产生的asd的特征也报道如下。
[0097]
聚合物溶剂反溶剂观察结果hpmcasdmacmtbe黏性hpmcasthfmtbe无定形相分离,高残留溶剂hpmcasmek庚烷无法研磨hpmcasmekmtbe无法研磨,高残留溶剂hpmcasthf庚烷无定形相分离,高残留溶剂hpmcdmacipa黏性hpmcdmac乙醇黏性va64dmacipa黏性va64dmac乙醇黏性
[0098]
接下来评估水溶剂系统,并且发现hpmcas与dmac:0.1n盐酸溶剂:反溶剂系统的组合成功。
[0099]
聚合物溶剂反溶剂观察结果hpmcasdmac0.1n hcl固体,无定形
[0100]
制备具有不同比例的hpmacas聚合物与活性成分(式(i)化合物)的无定形固体分散体(asd)的样品,并通过粉末x射线衍射(pxrd)分析以测定存在于asd中的无定形化合物的量。聚合物与化合物的比例为3:1的asd显示出少量的结晶度。但是,聚合物与化合物的比例为5:1和10:1的asd未显示出显著的结晶度。见图1。基线迹线是式(i)化合物的晶形。其它迹线显示具有api与聚合物的不同比例的一些asd的结晶度。具有3:1的聚合物与化合物比例的asd的迹线显示与结晶迹线最相似,并由此表明3:1的asd中存在大量式(i)化合物的结晶形式。具有5:1、7:1和10:1的聚合物与化合物的比例的asd的迹线显示与结晶迹线的相似性较小,由此表明这些asd的每一个中不存在大量式(i)化合物的结晶形式。
[0101]
实施例2-式(i)化合物和醋酸羟丙基甲基纤维素琥珀酸酯(hpmcas)的共沉淀制剂
[0102]
在此方法中,将式(i)化合物(即活性成分(api))和聚合物(醋酸羟丙基甲基纤维素琥珀酸酯,l级)溶解于溶剂(dmac)中。然后在定转子均质机中,在高剪切下在反溶剂(0.1n hcl)中快速沉淀api-聚合物溶液。使用1:10的溶剂:反溶剂比例实现沉淀和洗涤条件。沉淀后进行10x浆液洗涤,然后进行5x置换洗涤。形成化合物和聚合物的无定形固体分
散体并压制成片剂。
[0103]
通过将750mg化合物和7500mg hpmcas-l聚合物溶解于56.25ml dmac溶剂中形成hpmcas-l聚合物与式(i)化合物的比例为10:1的无定形固体分散体(asd)。搅拌该溶液过夜以确保完全溶解。接着,将500ml冷的0.1n hcl加入到1l烧杯中。将ika t25定转子均质机加入到烧杯中并转到20,000rpm。然后用注射器通过14g针将50ml化合物/聚合物溶液加入到转子定子混合器的高剪切区中。化合物/聚合物混合物快速沉淀并在冰上再混合2分钟。过滤所得悬浮液并将其加入至500ml新鲜的冷0.1n hcl中。将所得悬浮液再浆液洗涤2分钟,然后过滤。然后将250ml新鲜的冷0.1n hcl加入至所得滤饼的顶部并通过置换洗涤。然后将最终的滤饼在真空和氮气吹扫下干燥过夜。所得的干燥asd具有82.5%的测定值。为了制备片剂,将4850mg asd加入到3050mg微晶纤维素、1500mg乳糖一水合物和500mg羟基乙酸淀粉钠中,并用turbula混合器以49rpm混合15分钟。然后加入100mg硬脂酸镁,再混合5分钟。然后用卡弗压片机(carver press)以1500lbs压制5/16"圆形标准凹面片剂来制备片剂。
[0104]
通过将1500mg化合物和7500mg hpmcas-l聚合物溶解于56.25ml dmac溶剂中来形成hpmcas-l聚合物与式(i)化合物的比例为5:1的无定形固体分散体(asd)。搅拌溶液过夜以确保完全溶解。接着,将500ml冷的0.1n hcl加入到1l烧杯中。将ika t25定转子均质机加入至烧杯中并转到20,000rpm。然后用注射器通过14g针将50ml化合物/聚合物溶液加入至转子定子混合器的高剪切区中。化合物/聚合物混合物快速沉淀并在冰上再混合2分钟。过滤所得悬浮液并将其加入至500ml新鲜的冷0.1n hcl中。将所得悬浮液再浆液洗涤2分钟,然后过滤。然后将250ml新鲜的冷0.1n hcl加入至所得滤饼的顶部并通过置换洗涤。然后将最终的滤饼在真空和氮气吹扫下干燥过夜。所得asd具有93.3%的测定值为。将2150mg中间体加入至4750mg微晶纤维素、2500mg乳糖一水合物和500mg羟基乙酸淀粉钠中,并用turbula混合器以49rpm混合15分钟。然后加入100mg硬脂酸镁,再混合5分钟。然后用卡弗压片机以1500lbs压制5/16"圆形标准凹面片剂来制备片剂。
[0105]
通过用turbula混合器以49rpm将150mg化合物、3375mg微晶纤维素、3525mg乳糖一水合物和375mg羟基乙酸淀粉钠共混15分钟来制备含有结晶的式(i)化合物的片剂。然后用卡弗压片机以1500lbs压制5/16"圆形标准凹面片剂来制备片剂。
[0106]
实施例3-式(i)化合物的生物利用度
[0107]
上述asd和结晶制剂的药代动力学(pk)研究在进食和禁食的犬中进行。对于禁食组,动物在施用后4小时进食,然后禁食过夜。在喂养动物之前的时间点收集血样。在施用药物组合物前大约30分钟禁食过夜后,向进食的动物提供每日口粮。
[0108]
结果表明,在禁食状态下,具有hpmcas-l的无定形固体分散体(asd)制剂中含有式(i)化合物的制剂实现了生物利用度的显著改善。但是,在进食状态下,与用结晶式(i)化合物制备的制剂相比,生物利用度没有显著变化。见图2。
[0109]
实施例4-抗成核剂
[0110]
在提高以进食状态下施用的动物中式(i)化合物的生物利用度的尝试中,将抗成核剂加入至药物组合物以降低化合物结晶的可能性。在体外筛选中评估几种抗成核聚合物维持式(i)化合物的能力。在ph1.8的模拟胃液中制备各抗成核聚合物的0.5%溶液。将75ul的10mg/ml的api的dmso溶液加入至5ml的0.5%聚合物溶液中,并通过pion uv探针在272nm监测2小时。见图3。当使用抗成核聚合物甲基纤维素a4c(mc a4c)和羟丙基甲基纤维素e50
(hpmc e50)时,在整个2小时测试期间维持式(i)化合物的浓度。当使用其它聚合物时,式(i)化合物的浓度最初维持,但最终在2小时测试完成之前降低。这与仅具有模拟胃液(sgf)的对照样品相反,对照样品中式(i)化合物的浓度几乎立即下降。结果表明mca 4c和hpmc e50是改善进食状态下的生物利用度的合适的抗成核聚合物,因为与测试的其它聚合物相比,这些聚合物能够长期维持式(i)化合物的过饱和水平。
[0111]
实施例5-功效研究
[0112]
在被诊断为特应性皮炎的犬中,在一项隐蔽且随机化的概念验证研究中评价化合物。该研究的目的是评价化合物对客户拥有的犬的特应性皮炎的功效和耐受性。在两个剂量下评价化合物,并与安慰剂对照进行比较。犬将每天口服施用两次,持续长达14天、随后每天施用一次,持续长达28天、或每天施用一次,持续28天、并且将使用瘙痒视觉模拟量表(pvas)和犬特应性皮炎程度和严重程度指数(cadesi-4)评分工具分别评价瘙痒和皮肤病变。
[0113]
犬特应性皮炎程度和严重程度指数(cadesi-4)是用于在治疗患有特应性皮炎(ad)的犬的临床试验中分级皮肤病变的严重程度量表。在20个身体部位中的每一处对三种病变类型(红斑、苔藓样硬化和脱发/表皮脱落)进行从0至3的评分,最大评分为180,轻度、中度和重度ad皮肤病变的建议基准分别为10、35和60。cadesi-4:thierry,o.,manolis,s.,nuttall,t.,bensignor,e.,griffin,c.,hill,p.,for the international committee on allergic diseases of animals(icada)。犬特应性皮炎程度和严重程度指数(cadesi)-4的确认,用于评估犬中特应性皮炎的皮肤病变的简化严重程度量表。vet,dermatol.25:77-e25,2014。
[0114]
瘙痒视觉模拟量表(pvas)是包含瘙痒严重程度和瘙痒相关行为的特征的视觉模拟量表。在治疗患有ad的犬的临床试验中,它通常用于确定瘙痒的严重程度。pvas:hill,p.b.,lau,p.,和rybnicek,j.development of an owner-assessed scale to measure the severity of pruritus in dogs.vet.dermatol.18:301-308,2007。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1