包含旋覆花的中药组合物的抗疲劳制药用途
1.本发明属于医药领域,涉及包含旋覆花的中药组合物在制备抗疲 劳的药物中的用途。
背景技术:
2.疲劳是人体的一种主观感受,是机体防止发生过度机能衰竭而产 生的一种保护性反应,可分为生理性疲劳和病理性疲劳。生理性疲劳 主要以运动性疲劳为代表,病理性疲劳主要包括疾病伴发慢性疲劳、 慢性疲劳综合征和术后疲劳综合征等。病理性疲劳严重降低人们生活 能力和工作能力,严重者终生卧床,患者痛苦不堪,已经成为严重危 害人类健康的公共卫生问题。目前生理性疲劳治疗主要以特种营养补 充、睡眠调整和运动疗法等为主,病理性疲劳主要以适度运动和认知 心理疗法为主,辅以营养补充和对症药物治疗。
3.遗憾的是,现有干预措施抗疲劳作用并未取得一致性结论,且尚 无药物批准用于病理性疲劳的治疗。中医药对疲劳的认识具有极其悠 久的历史,结合传统中医理论和现代药理学研究,研发安全有效的抗 疲劳现代中药具有重要意义。
4.目前,尚需要开发新的抗疲劳手段特别是中医抗疲劳药手段。
技术实现要素:
5.本发明人经过深入的研究和创造性的劳动,惊奇地的发现,包含 旋覆花、代赭石、竹叶和淡豆豉的中药组合物或其提取物在多个模型 种具有抗疲劳作用,具有应用于制备抗疲劳药物的潜力。由此提供了 下述发明:
6.本发明的一个方面涉及选自如下的(1)
‑
(3)项中的任一项在制 备抗疲劳的药物中的用途:
7.(1)中药组合物,包括旋覆花、代赭石、竹叶和淡豆豉;
8.(2)提取物,其为第(1)项中的中药组合物的水提物和/或乙醇 溶液提取物;
9.(3)药物制剂,其包含第(2)项中的提取物,以及一种或多种 药学上可接受的辅料。
10.在本发明的一个或多个实施方式中,所述的用途,其中,所述疲 劳为生理性疲劳或病理性疲劳;
11.优选地,所述病理性疲劳为疾病伴发慢性疲劳、慢性疲劳综合征 或术后疲劳综合征。
12.在本发明的一个或多个实施方式中,所述的用途,其中,
13.所述中药组合物包括:旋覆花1
‑
3重量份、代赭石1
‑
3重量份、 竹叶0.5
‑
1.5重量份、淡豆豉0.5
‑
1.5重量份;
14.优选地,所述中药组合物包括:旋覆花1.5
‑
2.5重量份、代赭石 1.5
‑
2.5重量份、竹叶0.8
‑
1.2重量份、淡豆豉0.8
‑
1.2重量份;
15.优选地,所述中药组合物包括:旋覆花1.8
‑
2.2重量份、代赭石 1.8
‑
2.2重量份、竹
叶0.8
‑
1.2重量份、淡豆豉0.8
‑
1.2重量份;
16.优选地,所述中药组合物包括:旋覆花2重量份、代赭石2重量 份、竹叶1重量份、淡豆豉1重量份;
17.优选地,所述中药组合物由旋覆花、代赭石、竹叶和淡豆豉组成。
18.在本发明的一个或多个实施方式中,所述的用途,其中,第(1) 项中,所述提取物通过包括如下步骤的制备方法制得:
19.1)将第(1)项的中药组合物用50%
‑
95%(v/v)的乙醇溶液进 行回流提取,得到提取液;
20.2)将提取液过滤,将滤液减压浓缩后得到浸膏;
21.3)将浸膏用水分散得到悬浮液;
22.4)将悬浮液用有机溶剂萃取1次或多次,得到水层萃取产物,其 中,所述有机溶剂为选自石油醚、正己烷和环己烷中的一种或多种;
23.5)将水层萃取产物加水制得混悬液;离心,取上清液;
24.6)将上清液上样于弱极性或中等极性的大孔树脂柱,上样后以 1
‑
5倍柱体积的水洗脱,弃去水洗液,再以乙醇溶液洗脱,洗脱至洗 出液成淡黄色,收集洗脱液;
25.7)将洗脱液减压浓缩干燥,得到粉末。
26.在本发明的一个或多个实施方式中,所述的用途,其中,步骤1) 中,乙醇溶液的浓度为60%
‑
85%(v/v)、65%
‑
80%(v/v)、65%
‑
75% (v/v)或70%(v/v)。
27.在本发明的一个或多个实施方式中,所述的用途,其中,步骤1) 中,乙醇溶液的用量为8
‑
12倍体积、8
‑
12倍体积(例如8倍体积、9 倍体积、10倍体积、11倍体积或12倍体积)或10倍体积。
28.在本发明的一个或多个实施方式中,所述的用途,其中,步骤1) 中,乙醇溶液的浓度为65%(v/v)、66%(v/v)、67%(v/v)、68% (v/v)、69%(v/v)、70%(v/v)、71%(v/v)、72%(v/v)、73% (v/v)、74%(v/v)或75%(v/v)。
29.在本发明的一个或多个实施方式中,所述的用途,其中,步骤1) 中,提取时间为1
‑
10小时、1
‑
5小时、2
‑
3小时或2小时。
30.在本发明的一个或多个实施方式中,所述的用途,其中,步骤3) 中,浸膏与水的质量比为(1:5)
‑
(2:1)、(1:2)
‑
(2:1)、 (1:1.5)
‑
(1.5:1)或1:1。
31.在本发明的一个或多个实施方式中,所述的用途,其中,步骤4) 中,悬浮液与有机溶剂的体积比为(1:1)
‑
(1:4)、(1:1)
‑
(1: 2)或1:1。
32.在本发明的一个或多个实施方式中,所述的用途,其中,步骤6) 中,乙醇溶液的浓度为60%
‑
85%(v/v)、65%
‑
80%(v/v)、65%
‑
75% (v/v)或70%(v/v)。
33.在本发明的一个或多个实施方式中,所述的用途,其中,步骤6) 中,乙醇溶液的浓度为65%(v/v)、66%(v/v)、67%(v/v)、68% (v/v)、69%(v/v)、70%(v/v)、71%(v/v)、72%(v/v)、73%(v/v)、74%(v/v)或75%(v/v)。
34.在本发明的一个或多个实施方式中,所述的用途,其中,步骤6) 中,所述弱极性或中等极性大孔树脂柱选自ab
‑
8、hp20、i
‑
ipd400、 d4006和x
‑
5型树脂,优选为ab
‑
8型树脂。
35.在本发明的一个或多个实施方式中,所述的用途,其中,第(1) 项、第(2)项或第(3)项的单位剂量按照中药组合物的重量来计算, 为10
‑
100g、10
‑
90g、10
‑
80g、10
‑
70g、10
‑
60g、10
‑
50g、12
‑
60g、 12
‑
50g、12
‑
40g或12
‑
36g,例如12g、24g或36g。
36.在本发明的一个或多个实施方式中,所述的用途,其中,第(1) 项、第(2)项或第(3)项的给药剂量按照中药组合物的重量来计算, 为10
‑
100g/人、10
‑
90g/人、10
‑
80g/人、10
‑
70g/人、10
‑
60g/人、10
‑
50 g/人、12
‑
60g/人、12
‑
50g/人、12
‑
40g/人或12
‑
36g/人,例如12g/人、 24g/人或36g/人;
37.优选地,第(1)项、第(2)项或第(3)项的给药途径为口服给 药。
38.在本发明的一个或多个实施方式中,所述的用途,其中,第(3) 项中:
39.所述提取物为唯一活性成分;或者
40.所述药物制剂还包含一种或多种抗疲劳化合物例如咖啡因;
41.优选地,咖啡因的单位剂量为50
‑
100mg;
42.优选地,咖啡因的给药剂量为50
‑
100mg/人。
43.在本发明的一个或多个实施方式中,所述的用途,其中,第(3) 项中,所述药物制剂为口服制剂,例如片剂、胶囊剂、丸剂或颗粒剂。
44.本发明的另一方面涉及一种药物制剂,其包含本发明中任一项的 第(2)项中所述的提取物、一种或多种药学上可接受的辅料、以及一 种或多种抗疲劳化合物例如咖啡因;
45.优选地,提取物的单位剂量为300
‑
1500mg,优选为300
‑
1200mg、 300
‑
1000mg或300
‑
900mg;
46.优选地,咖啡因的单位剂量为50
‑
100mg;
47.优选地,所述药物制剂为口服制剂,例如片剂、胶囊剂、丸剂或 颗粒剂。
48.在本发明的一个或多个实施方式中,所述的药物制剂,其用于抗 疲劳;
49.优选地,所述疲劳为生理性疲劳或病理性疲劳;
50.优选地,所述病理性疲劳为疾病伴发慢性疲劳、慢性疲劳综合征 或术后疲劳综合征。
51.本发明的再一方面涉及一种组合药物产品,包括独立包装的第一 药物产品和第二药物产品,其中,
52.所述第一药物产品包含本发明中任一项的第(1)项中所述的中药 组合物、本发明中任一项的第(2)项中所述的提取物、或者本发明中 任一项的第(3)项中所述的药物制剂;
53.所述第二药物产品包含至少一种抗疲劳化合物例如咖啡因;可选 地,还包含一种或多种药学上可接受的辅料;
54.优选地,提取物的单位剂量为300
‑
1500mg,优选为300
‑
1200mg、 300
‑
1000mg或300
‑
900mg。
55.本发明的再一方面涉及一种抗疲劳的方法,包括给予有需求的受 试者以有效量的本发明中任一项的第(1)项中所述的中药组合物、本 发明中任一项的第(2)项中所述的提取物、或者本发明中任一项的第 (3)项中所述的药物制剂的步骤。
56.本发明中,
57.术语“辅料”在本申请中是指用以将主药给药的赋形剂或者媒介 物,其包括但不限于稀释剂、崩解剂、沉淀抑制剂、表面活性剂、助 流剂、粘合剂、润滑剂、包衣材料等。辅料在e.w.martin的
ꢀ“
remington's pharmaceutical sciences”中被一般性描述。辅料的实 例包括但不限于单硬脂酸铝、硬脂酸铝、羧甲基纤维素、羧甲基纤维 素钠、交聚维酮、异硬
脂酸甘油酯、单硬脂酸甘油酯、羟基乙基纤维 素、羟基甲基纤维素、羟基硬脂酸羟基二十八酯、羟基丙基纤维素、 羟基丙基甲基纤维素、乳糖、乳糖一水合物、硬脂酸镁、甘露醇、微 晶纤维素等。
58.取决于待治疗的疾病和患者以及给药途径,本发明的中药组合物 或者药物制剂可以以不同剂量每日一次或者多次给药。给药剂量取决 于许多因素,例如疲劳的严重程度,患者的性别、年龄、体重及个体 反应,给药途径及给药次数等。上述剂量可以单一剂量形式或分成几 个,例如二、三、四个剂量形式给药。
59.可改变本发明中药组合物或药物制剂中各主药的实际剂量水平, 以便能有效针对具体患者、组合物和给药方式得到所需的治疗反应。 剂量水平须根据给药途径、所治疗病况的严重程度以及待治疗患者的 病况和既往病史来选定。但是,本领域的做法是,给药剂量从低于为 得到所需治疗效果而要求的水平开始,逐渐增加剂量,直到得到所需 的效果。
60.术语“有效量”是指可在受试者中实现治疗、预防、减轻和/或缓 解疲劳的剂量。
61.本发明中,如果没有特别说明,乙醇溶液为乙醇的水溶液,其浓 度为体积百分比浓度(v/v)。
62.本发明中,如果没有特别说明,对于给药剂量涉及每人(/人)的 情形,是按照成年人体重60kg计算的,对于高于或低于体重60kg的 对象,可以将按照成年人体重60kg计算的剂量折合成每kg体重,再 乘以涉及实际体重的kg数来计算,或遵医嘱。
63.发明的有益效果
64.本发明中任一项的第(1)项中所述的中药组合物、本发明中任一 项的第(2)项中所述的提取物、或者本发明中任一项的第(3)项中 所述的药物制剂具有有效的抗疲劳作用。
附图说明
65.下面的附图中,如果没有特别说明:
66.veh表示溶剂对照组;
67.lps表示脂多糖;
68.caffeine表示咖啡因;
69.xbxt
‑
2表示实施例1中制得的小补心汤中药组合物提取物。
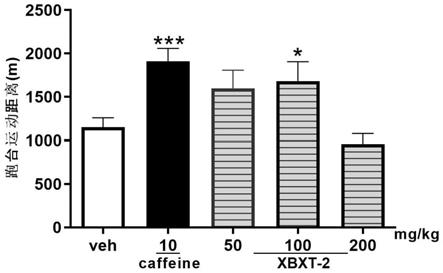
70.图1:xbxt
‑
2对正常小鼠跑台运动距离的影响。与溶剂对照组 相比(veh),*p<0.05****p<0.001。
71.图2:xbxt
‑
2对lps疲劳模型小鼠跑台运动距离的影响。与溶 剂对照组相比(veh),**p<0.01;与lps模型相比,#p<0.05##p<0.01 ###p<0.001####p<0.001。
72.图3:xbxt
‑
2对lps疲劳模型小鼠血糖的影响。与溶剂对照组 相比(veh),***p<0.001;与lps模型相比,#p<0.05。
73.图4:xbxt
‑
2对lps疲劳模型小鼠肝糖原的影响。与溶剂对照 组相比(veh),***p<0.001;与lps模型相比,##p<0.01####p<0.001。
74.图5:xbxt
‑
2对lps疲劳模型小鼠肌糖原的影响。与溶剂对照 组相比(veh),****p<0.001;与lps模型相比,#p<0.05####p<0.001。
具体实施方式
75.下面将结合实施例对本发明的实施方案进行详细描述,但是本领 域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限 定本发明的范围。实施例中未注明具体条件者,按照常规条件或制造 商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通 过市购获得的常规产品。
76.实施例1:xbxt
‑
2在正常小鼠上抗疲劳作用研究
77.实验动物:50只c57bl/6j小鼠,雄性,spf级,20
‑
22g,购自 斯贝福(北京)实验动物科技有限公司。
78.受试样品:中药组合物提取物(命名为xbxt
‑
2)和咖啡因。咖 啡因可商购或者自行合成。小补心汤中药组合物提取物的制备方法如 下:
79.旋覆花2kg、代赭石2kg、竹叶1kg、淡豆豉1kg,加入10倍量 (质量/体积,每kg药材加10l乙醇溶液)的70%(v/v)乙醇水溶 液加热回流提取2h,将提取液过滤,滤液减压浓缩后得到浸膏0.78 kg。浸膏以水分散(质量比1:1)为悬浮液,悬浮液以体积比为1:1 的石油醚(60℃
‑
90℃)萃取3遍(目的是除去大部分叶绿素和油脂), 取水层边搅拌边加入蒸馏水,得到总体积为6l的混悬液,将混悬液 在室温下离心(4000rpm,30min),弃去沉淀,上清液通过ab
‑
8 大孔吸附树脂(目的是吸附其中的黄酮类物质),上样后以2倍柱体 积的水洗脱,弃去水洗液,再以70%(v/v)乙醇洗脱,洗脱至洗出 液成淡黄色,收集洗脱液,将洗脱液减压浓缩干燥后得到黄色粉末约 142克,为提取物(命名为xbxt
‑
2)。该提取物以芦丁为标准品, 采用紫外分光光度法在510nm处测定,黄酮的粗含量不低于50%。
80.受试样品溶解:提取物xbxt
‑
2和咖啡因均分别以5%(v/v)的 dmso为溶剂进行溶解,浓度分别为2.5mg/ml、0.5mg/ml,供灌胃 (po)。
81.实验仪器:小鼠跑台。
82.实验方法:小鼠购入后适应性饲养3
‑
5天,按体重随机分为溶剂 对照组(veh)、阳性药组(咖啡因,caffeine,10mg/kg)、xbxt
‑
2 (50mg/kg、100mg/kg、200mg/kg)组,每组10只。各组小鼠按程 序进行3次跑台训练(速度从2m/s训练至14m/s),淘汰不合格小鼠。 各组小鼠单次灌胃给与溶剂对照、xbxt
‑
2和咖啡因1h后进行跑台 实验,记录小鼠跑步至力竭的运动距离,力竭判断标准为小鼠在跑道 后1/4处连续停留超过10s。跑台运动距离增加认为具有抗疲劳作用。
83.实验结果如图1所示。
84.结果显示:单次给与提取物(xbxt
‑
2)100mg/kg可显著增加正 常小鼠跑台运动距离,与溶剂对照组相比具有统计学差异(p<0.05), 表明提取物在正常动物模型上具有抗疲劳作用,具有抗生理性疲劳的 效果。
85.实施例2:xbxt
‑
2在脂多糖(lps)诱发病理疲劳模型上抗疲劳作用研究
86.实验动物:50只c57bl/6j小鼠,雄性,spf级,20
‑
22g,购自 斯贝福(北京)实验动物科技有限公司。
87.受试样品和溶解:同实施例1。
88.实验仪器:小鼠跑台。
89.实验方法:小鼠购入后适应性饲养3
‑
5天,按体重随机分为溶剂 对照组(veh)、lps疲劳模型组、阳性药组(咖啡因,caffeine,10mg/kg [折合成体重60kg的成人的用量相当于
76mg/人])、xbxt
‑
2(50mg/kg [折合成体重60kg的成人的用量相当于384mg/人]、100mg/kg、200 mg/kg)组,每组8
‑
9只。各组小鼠按程序进行3次跑台训练(速度从 2m/s训练至14m/s),淘汰不合格小鼠。除溶剂对照组,各组腹腔注 射lps(0.2mg/kg)12h后,单次灌胃给与溶剂对照、xbxt
‑
2和咖 啡因1h后进行跑台实验,记录小鼠跑步至力竭的运动距离,力竭判 断标准为小鼠在跑道后1/4处连续停留超过10s。跑台运动距离增加认 为具有抗疲劳作用。
[0090]
实验结果:见图2。
[0091]
结果显示:与溶剂对照组相比,lps可显著降低小鼠跑台运动距 离(p<0.01),模型成功;单次给与提取物(xbxt
‑
2)50mg/kg和 100mg/kg均可显著增加lps小鼠跑台运动距离,与lps模型组相比 具有统计学差异(p<0.05,p<0.001),表明提取物在病理疲劳模型特 别是lps诱发的病理疲劳模型上具有抗疲劳作用,具有抗病理性疲劳 的效果。
[0092]
实施例3:xbxt
‑
2对脂多糖诱发疲劳小鼠血清葡萄糖、肝糖原和肌糖原的影响
[0093]
实验动物:40只c57bl/6j小鼠,雄性,spf级,20
‑
22g,购自 斯贝福(北京)实验动物科技有限公司。
[0094]
受试样品和溶解:同实施例1。
[0095]
实验仪器:小动物血生化仪,酶标仪。
[0096]
实验方法:小鼠购入后适应性饲养3
‑
5天,按体重随机分为溶剂 对照组(veh)、lps疲劳模型组、阳性药组(咖啡因,caffeine,10 mg/kg)、xbxt
‑
2(100mg/kg)组,每组10只。各组小鼠按程序进行 3次跑台训练(速度从2m/s训练至14m/s),淘汰不合格小鼠。溶剂 对照组,各组腹腔注射lps(0.2mg/kg)12h后,单次灌胃给与溶剂 对照、xbxt
‑
2和咖啡因1h后进行跑台运动至力竭,然后立即断头 取血、肝脏组织和肌肉组织。全血于4℃静止4h后,3000r离心20min 取上清获得血清样本,于生化仪进行葡萄糖(glu)检测。肝脏和肌 肉组织采用肝/肌糖原试剂盒(南京建成生物工程研究所)按说明书操 作进行肝糖原和肌糖原检测。
[0097]
实验结如图3、图4和图5所示。
[0098]
结果显示:与溶剂对照组相比,lps可显著降低小鼠血糖 (p<0.001)、肝糖原(p<0.05)和肌糖原(p<0.001)含量,提示模型 成功;单次给与xbxt
‑
2 100mg/kg可显著增加lps模型小鼠血糖 (p<0.05)、肝糖原(p<0.001)和肌糖原(p<0.05),表明xbxt
‑
2 在病理疲劳模型特别是lps诱发的病理疲劳模型上的抗疲劳作用可 能是通过改善能源物质血糖和糖原耗竭发挥的。
[0099]
尽管本发明的具体实施方式已经得到详细的描述,本领域技术人 员将会理解。根据已经公开的所有教导,可以对那些细节进行各种修 改和替换,这些改变均在本发明的保护范围之内。本发明的全部范围 由所附权利要求及其任何等同物给出。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1