降低胆固醇的组合物及其制备方法与流程
1.本发明涉及一种组合物,具体涉及一种降低胆固醇的组合物及其 制备方法。
背景技术:
2.橙皮苷为柑橘类水果中的一种黄酮类化合物,其主要储存于柑橘 类水果的果皮中,且近年来有不少研究指出服用橙皮苷萃取物对于人 体具有降血压、降胆固醇和预防动脉硬化的效果,但却未见有人采用 发酵的方式使柑橘类水果中的橙皮苷含量增加,并使其功效不亚于橙 皮苷萃取物。
技术实现要素:
3.本发明的主要目的在于提供一种能降低胆固醇的组合物及其制 备方法。
4.技术方案:降低胆固醇的组合物,包括320~526μg/ml的橙皮 苷以及70~110μg/ml的阿魏酸。
5.降低胆固醇的组合物的制备方法,包括以下步骤:
6.(1)、将柠檬压榨成柠檬汁;
7.(2)、将步骤(1)得到的柠檬汁进行发酵,得到降低胆固醇的 组合物。
8.进一步地,步骤(1)中将连同果皮和种子的整颗柠檬压榨成柠 檬汁。
9.进一步地,步骤(2)中,直接将益生菌加入到步骤(1)得到的 柠檬汁内进行发酵,其中:
10.发酵的过程中温度控制在25℃~35℃并持续搅拌14到22天, 而在搅拌的过程中会不间断的通过搅拌设备将空气打入柠檬汁内,使 柠檬汁、益生菌以及空气能够充分的混合。
11.进一步地,所述益生菌包括胚芽乳酸杆菌(lactobacillus plantarum)以及季也蒙有孢汉逊酵母菌(hanseniaspora guilliermondii),其中:
12.所述胚芽乳酸杆菌与所述季也蒙有孢汉逊酵母菌的混合比例为 (1~6):(1~8)。
13.进一步地,所述柠檬汁和所述益生菌的混合比例为(1~2): (0.05~0.5)。
附图说明
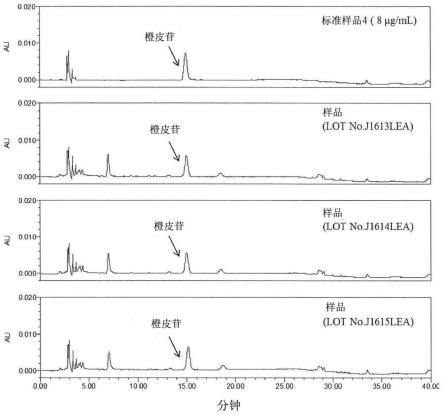
14.图1:本发明的橙皮苷的检测图谱;
15.图2:阿魏酸的标准图谱;
16.图3:本发明稀释10倍后的阿魏酸的检测图谱。
具体实施方式:
17.为了让本发明的目的、功效、特征及结构 能够有更为详尽的了解,下面借助较佳实施例 并配合附图说明如后。
18.本发明公开了降低胆固醇的组合物,其包 含有320~526μg/ml的橙皮苷以及70~
(laboratory autoclavable rodent diet5010),而对照组饲料则采用研究饮食 (research diets)的rd西方饮食(修改自 d12079b)(rd western diet(modify fromd12079b))高油脂高胆固醇饲料,正常组和对 照组的仓鼠均采自由摄食方式喂食。
42.饮水:将自来水经逆渗透处理机处理后装 入已灭菌的塑料瓶后供仓鼠自由饮用。
43.试验组别设计:详细的投予投喂量如下表 (一)所示,剂量推算系根据2005年美国食品药 物管理局所公告的实验出其估算方法,以60公 斤的成人为基准,使用高等实验动物进行试验 时,剂量的换算原则为人体每日每公斤体重的 建议摄取量的7.4倍为仓鼠1倍剂量。
[0044][0045]
表(一)
[0046]
试验物质的配制:将本发明以冷冻浓缩的 方式制备成3.7倍浓缩液,以灭菌水直接配制浓 缩液至投喂体积,以50ml的本发明为例,其经 浓缩处理后的体机为13.5ml,以人体与仓鼠的 剂量换算如下:
[0047]
低剂量对照组仓鼠投喂 的本发明;
[0048]
中剂量对照组仓鼠投喂 ml/kg/day的本发明;
[0049]
高剂量对照组仓鼠投喂高剂量对照组仓鼠投喂的本发明。
[0050]
投喂期间、方法:仓鼠于试验开始第一天 经口管喂食试验物质或对照物质连续6
周,投喂 剂量的计算系根据当日投喂前量测的体重为基 准,投喂的剂量如上所述,投喂的体积为 10ml/kg。
[0051]
临床症状观察:试验期间每日进行临床观 察,并记录仓鼠是否有异常临床症状或死亡, 并每周定时量测仓鼠体重变化及其饲料摄取 量。
[0052]
血清收集与血清制备:第6周以牺牲采血方 式收集血液样本,采取的血液放入生化管中并 于室温静置2小时后,再以2000
×
g离心15分钟收 集上层血清样本,检测血清中的总胆固醇 (total cholesterol,tc)、高密度脂蛋白胆固 醇(high density lipoprotein cholesterol, hdl-c)、低密度脂蛋白胆固醇(low densitylipoprotein cholesterol,hdl-c)。
[0053]
粪便收集:第6周牺牲前3天收集仓鼠粪便, 并去除沾黏于粪便的毛发等杂物,以热风干燥 后再磨成粉状,接着进行总胆固醇(tc)含量检 测分析。
[0054]
脏器采集:试验结束后以异氟醚 (isoflurane)将仓鼠麻醉牺牲后,采集肝脏秤 重以及检查是否有脂肪肝,并取其中最大叶于
ꢀ‑
70℃冰箱保存后进行总胆固醇(tc)含量检测 分析。
[0055]
血清生化指标测定:采用血清生化分析仪 检测血清中的总胆固醇(tc)、高密度脂蛋白胆 固醇(hdl-c)、低密度脂蛋白胆固醇(hdl-c), 并计算高密度脂蛋白胆固醇/低密度脂蛋白胆 固醇和总胆固醇/高密度脂蛋白胆固醇的比值。
[0056]
粪便总胆固醇的含量检测:依照福尔奇 (folch)法,将粉状的粪便粉末以筛子滤除 较大颗粒,再取一定量的粪便粉末加入20倍重 量的氯仿/甲醇混合溶液(混合比例为2:1),以 组织均质机均质后,接着以3000
×
g离心10分钟并 取出澄清液,接续依照卡尔森和戈德福德(carlson&goldford)法,将离心后的粪便 脂质均质液中加入0.2倍体积的0.9%生理食盐 水(saline)均匀混合,于室温下以1200
×
g离心5 分钟后去除上层液体,保留脂相层后置于95℃ 烘箱中待有机溶剂挥发后,以生化分析仪分析 粪便中总胆固醇。
[0057]
肝脏总胆固醇的含量检测:依照福尔奇 (folch)法,取一定量的肝脏加入20倍重量 的氯仿/甲醇混合溶液(混合比例为2:1),接续 依照卡尔森和戈德福德(carlson&goldford) 法,并以组织均质机均质后,接着以3000
×
g离心 10分钟并取出澄清液,将离心后的肝脏组织脂 质均质液加入0.2倍体积的0.9%生理食盐水 (saline)混合均匀,于室温下以1200
×
g离心5分 钟,去除上层液体并保留脂相层后置于95℃烘 箱中待有机溶剂挥发后,以脂溶液(tert-butylalcohol:tritonx-100:methanol=2:1: 1)溶解均匀混合,以生化分析仪分析粪便中总 胆固醇。
[0058]
在本次动物试验中,主要系探讨本发明对 于降低胆固醇的功效,并将试验分为正常组(给 予正常饲料以及灭菌水)、负对照组(给予高油 脂高胆固醇饲料以及灭菌水)、低剂量对照组 (给予高油脂高胆固醇饲料以及1倍相对人体剂 量的本发明)、中剂量对照组(给予高油脂高胆 固醇饲料以及2倍相对人体剂量的本发明)以及 高剂量对照组(给予高油脂高胆固醇饲料以及6 倍相对人体剂量的本发明),且每组均为10只试 验动物,经口服投喂6周后进行血液、粪便、肝 脏的胆固醇的相关检测,而检测结果以平均值 正负标准差表示,而检测数据以单因子变异数 分析(one-way anova)进行分析,并以邓肯多重 差距检定(duncan multiple range test)进行 事后检定,其结果如下列所示:
[0059]
首先,就各组仓鼠的每周平均摄食量的记 录如下表(二)所示。
[0060][0061][0062][0063]
表(二)
[0064]
由上表(二)可看出除了正常组之外,喂食 高油脂高胆固醇饲料的各个对照组的平均摄食 量皆无明显差别。
[0065]
接着,就各组仓鼠的每周平均体重变化以 及平均肝脏重量如下表(三)所示。
[0066]
[0067][0068]
[0069][0070]
表(三)
[0071]
由上表(三)可看出除了负对照组以外,其 余的组别在体重方面差异性并不大,而在肝脏 相对重量方面,由于负对照组喂养高油脂高胆 固醇饲料造成过多的脂肪在肝脏堆积,使负对 照组的肝脏相对重量明显大于正常组,且服用 不同剂量对照组的肝脏相对重量明显小于负对 照组,由此可看出服用本发明是能降低脂肪在 肝脏堆积的情况。
[0072]
接续,就各组仓鼠的第6周血清中总胆固 醇、高密度脂蛋白胆固醇(hdl-c)以及低密度脂 蛋白胆固醇(ldl-c)含量如下表(四)所示。
[0073][0074]
表(四)
[0075]
由上表(四)可知在6周试验结束后,各剂量 对照组的血清中的总胆固醇以及低密度脂蛋白 胆固醇含量与负对照组相比皆有显著降低,且 又以中剂量组对降低总胆固醇以及低密度脂蛋 白胆固醇的效果最为明显,而在高密度脂蛋白 胆固醇含量方面,各剂量对照组和负对照组并 无明显的差异。
[0076]
再来,就各组仓鼠的第6周试验结束前粪便 中总胆固醇含量如下表(五)所示。
[0077]
组别本发明剂量(ml/kg)总胆固醇(mg/dl)正常组无0.4601
±
0.189负对照组无3.325
±
0.807低剂量对照组6.24.490
±
1.559中剂量对照组12.34.377
±
1.009高剂量对照组37.04.489
±
0.736
[0078]
表(五)
[0079]
由上表(五)可看出各剂量对照组粪便中的 平均总胆固醇含量均明显高于负对照组。
[0080]
最后,就各组仓鼠的第6周肝脏中总胆固醇 含量如下表(六)所示。
[0081]
组别本发明剂量(ml/kg)总胆固醇(mg/dl)正常组无1.485
±
0.399负对照组无29.979
±
3.677低剂量对照组6.225.515
±
1.648中剂量对照组12.325.153
±
2.672
高剂量对照组37.023.701
±
4.718
[0082]
表(六)
[0083]
由上表(六)可看出各剂量对照组肝脏中的 总胆固醇含量是明显低于负对照组,且又以高 剂量对照组降低的幅度最为显著。
[0084]
续请参阅表(七)以及图1,表(七)为本 发明的橙皮苷含量检测结果,图1为本发明的橙 皮苷检测图谱。
[0085]
橙皮苷含量检测结果
[0086][0087]
表(七)
[0088]
再来,本发明更进一步的将组合物的成分 进行分析,并以此来检测本发明中的橙皮苷以 及阿魏酸含量和其图谱分析。
[0089]
接着,将取任意三组利用相同配比和制备 方法所制造出的本发明进行橙皮苷含量检测, 而其结果如表(七)所示,由表(七)中可看 出橙皮苷含量分别为491.39
±
2.89、485.96
±ꢀ
2.23、489.01
±
2.25μg/ml。
[0090]
再来如图1所示,图1由上而下分别为标准 的橙皮苷图谱以及三组本发明的图谱,且从图 谱中可看出三组送验的本发明在显示橙皮苷的 区段有产生峰值,且该峰值与标准的橙皮苷峰 值有所重叠,因此本发明中确实是含有橙皮苷。
[0091]
请继续参阅图2以及图3,图2为阿魏酸的标 准图谱,图3为本发明稀释10倍后的阿魏酸检测 图谱。
[0092]
接着,将图3所示的图谱与图2所示的图谱 相比,可发现本发明在显示阿魏酸的区段有产 生峰值,且该峰值与标准的阿魏酸峰值有所重 叠,因此本发明中确实是含有阿魏酸。
[0093]
综合上述表格可知仓鼠在服用了本发明的 后,是有助于降低其血清和肝脏中的胆固醇含 量。
[0094]
唯,但是以上所述者技术方案,仅系为本 发明的较佳实施例而已,举凡凡是应用本发明 说明书及申请专利范围所为的其它等效结构变 化者的技术方案,理应包含在本发明的申请专 利范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1