药物信息叠加扩增治疗系数的药物新制剂制备工艺与产品及用途的制作方法
1.本发明属于医药领域,具体涉及药物新制剂制备工艺与产品及用途。
背景技术:
2.药物制剂是按照一定形式制成的药物成品即药品。药物制剂解决了药品的用法和用量问题。药物的治疗指数即药物的治疗系数,是为了发挥药理作用,其药量必须在某一定阈值以上是必要的条件。通常用于治疗的量称作常用量(药用量),最大药用量称为极量,又有一次量及日摄的规定。呈现中毒症状的量为中毒量,导致动物死亡的量为致死量。据最近统计学计算方法,计算出50%有效量(ed50),50%致死的最小量(ld50),而治疗系数r=ld50/ed50表示,r值越大越安全。有很多药物新制剂发明,能够提高其药物治疗指数或治疗系数。但是,已有的提高药物治疗指数的新制剂发明技术,都是用改变药物结构或增加药物制剂组合物质工艺,其药物治疗指数的提高不够大(在个位数内),不改变药物结构或不增加药物制剂组合物质,能够提高药物治疗指数的制剂,且药物指数能够倍增提高的新制剂与工艺发明,迄今还没有。
技术实现要素:
3.本发明的技术方案,是在常规药物制剂工艺基础上,稀释药物药理活性成分浓度比例,同时增加药物信息叠加工艺,实现不改变药物结构比例组合成分大幅度扩增药物治疗系数。
4.本发明所述的药物是用以预防、治疗疾病的物质。是指凡能影响机体器官生理功能及细胞代谢活动的具有药理活性作用的化学单体物质及组合物质,植物及组合物质,生物物质。
5.本发明所述的药物制剂是按照一定形式制成的药品。常规药物制剂按形态分类有:1、液体剂型(如溶液剂、注射剂等),2、固体剂型(如片剂、胶囊剂等),3、半固体剂型(如软膏剂、凝胶剂等),4、气体剂型(如气雾剂、喷雾剂等)。按分散系统分类有:1、溶液型,2.、胶体溶液型,3、乳状液型,4、混悬液型,5、气体分散型,6、固体分散型。按给药途径分类有:1.经胃肠道给药的剂型,2.不经胃肠道给药的剂型包括(1)注射给药 如静脉注射、肌内注射、皮下注射和皮内注射等,(2)呼吸道给药 如吸入剂、喷雾剂、气雾剂等,(3)皮肤给药 如外用溶液剂、洗剂、搽剂、软膏剂、糊剂、贴剂等,(4)粘膜给药 如滴眼剂、滴鼻剂、含漱剂、舌下片剂、栓剂、膜剂等,以及直肠给药类,如灌肠剂、栓剂、直肠用胶囊栓等。
6.本发明所述的常规药物制剂工艺是以上药物制剂常规制备工艺。
7.本发明所述的药物信息是药物制剂中原料药物物质即药理活性物质(不含辅料物质)的信息。本发明发现药物包括其物质、能量、信息,药物信息与药物物质有联系又有区别,药物物质是药物信息的载体,药物信息是药物物质的一种属性但药物信息不是药物物质,药物信息就是药物信息,信息的本质是不确定性的辨析度,具有它的独特性。
8.本发明是根据本发明人发现的人体信息决定论原理,即对人体生命遗传、发育、生理功能、疾病与健康起决定作用的不是人体物质而是人体信息。人体物质是人体的物质基础,人体信息是人体的决定因素,因为组成人体物质元素相同的人,而形象、性格、与生理、疾病、健康等等却差异很大。这是人体生命系统与非人体生命系统的本质不同。根据人体信息决定论原理,药物对人体的药理活性作用包括药物物质对人体细胞物质受体的效应与药物信息对人体细胞信息受体的效应,即人体细胞通讯。本发明所述的药物信息是对人体细胞信息受体具有药理活性效应的信息,是人体细胞通讯信息,它遵循信息规律。
9.本发明所述的药物信息叠加工艺,是通过高强度药物信息的药物物质载体,对低强度药物信息的药物物质予以药物信息辐射,进行药物信息叠加,使低强度药物信息药物物质变为高强度药物信息药物物质。低强度的药物信息物质变为高强度的药物信息物质以后,可以提高药物的信息载荷,利用药物信息,通过信息换取能量,扩增其治疗系数。
10.本发明所述的药物信息强度与药物物质(药物信息辐射体)载体成比例相关,与药物治疗指数(系数)增加成比例相关。
11.本发明所述的药物信息辐射是在密封空间内一定距离微孔隔空实现,所述的密封空间是金属材料等高密度材料制备的不透气的药物信息辐射(反应)罐,所述的药物信息辐射(反应)罐高100-1000厘米,直径50-500厘米,内部结构包括上部药物信息辐射发生舱、下部药物信息辐射反应舱与中间隔空部,所述的上下部有可以开关的密封门,所述的隔空是通过中隔板隔开,高强度药物信息的物质载体与低强度药物信息物质不接触、不泄露,间隔一定空间进行信息辐射,其隔空距离1-30厘米;所述的间隔隔板是用微孔透气材料制作的间隔隔板,固体物质使用小于固体物质粒径直径的微孔透气材料、液体物质使用微孔防水透气材料制成,以保证间隔两边的物质可以微孔透气但不接触而隔空微孔辐射,通过所述的药物信息隔空微孔辐射实现药物信息叠加;所述的药物信息叠加是用药物信息辐射(反应)罐,在其发生舱装入高强度药物信息载体物质,在其反应舱装入低强度药物信息物质,关门密封进行药物信息微孔隔空辐射1-100小时的时间,即对反应舱的药物实现其药物信息叠加。
12.所述的高强度药物信息载体物质,是其药理活性成分比常规用药剂量高1-1万倍的物质;所述的低强度药物信息物质,是其药理活性成分比常规用药剂量低1-1万倍的物质。
13.所述的药物信息辐射每次操作时间是1-100小时。
14.所述的高强度药物信息载体物质对低强度药物信息物质药物信息辐射次数可以达到1-1万次。
15.本发明所述的高强度药物信息载体物质对低强度药物信息物质完成药物信息辐射即实现了对低强度药物信息物质的药物信息叠加,低强度药物信息物质可以具有高强度药物信息载体物质的有效作用功能量,赋能细胞信息通讯,扩增了其能量的功能信息,可以较小的能量发挥较大的功能作用;同时,低强度药物信息物质由于大幅度降低了药理活性成分浓度而大幅度降低其毒性,因此,治疗系数得到大幅度扩增,其扩增幅度可达1-1万倍。
16.本发明高强度药物信息载体物质可以由n种物质组合,对1种低强度药物信息物质实现药物信息叠加后,不仅大幅度扩增其治疗系数,还可以增加其临床新用途。
17.本发明可以使用n种剂量与成分组合方式,实现药物信息叠加,然后对实现药物信
息叠加的药物物质,用常规药物制剂工艺制备n种药品新制剂。
18.本发明所述的药物信息叠加新制剂包括:按形态分类有:1.液体剂型(如溶液剂、注射剂等),2.固体剂型(如片剂、胶囊剂等),3.半固体剂型(如软膏剂、凝胶剂等),4.气体剂型(如气雾剂、喷雾剂等。按分散系统分类有:1. 溶液型,2. 胶体溶液型,3. 乳状液型,4. 混悬液型,5. 气体分散型,6. 固体分散型。按给药途径分类有:1.经胃肠道给药的剂型,2.不经胃肠道给药的剂型包括(1)注射给药 ,如静脉注射、肌内注射、皮下注射和皮内注射等;(2)呼吸道给药 ,如吸入剂、喷雾剂、气雾剂等;(3)皮肤给药,如外用溶液剂、洗剂、搽剂、软膏剂、糊剂、贴剂等;(4)粘膜给药,如滴眼剂、滴鼻剂、含漱剂、舌下片剂、栓剂、膜剂等,以及直肠给药类,如灌肠剂、栓剂、直肠用胶囊栓等。
19.本发明药物信息叠加新制剂不仅大幅度扩增治疗系数增加其安全性,或者增加其新用途,还可以大幅度降低药物制剂生产成本,同时,也由于降低药物原料消耗有利于环境保护。
20.本发明药物信息叠加新制剂一种新用途是作为五脏开窍药品,用于五脏开窍,所述的五脏开窍是中医的肝开窍于目,肾开窍于耳,肺开窍于鼻,脾开窍于口,心开窍于舌。本发明用于五脏开窍部位喷雾人体头面部七窍(眼耳鼻口舌),开窍七窍,直通五脏,更大扩增治疗系数。
21.具体实施例本发明提供以下实施例进一步说明。但不限于这些实施例。
22.实施例1阿司匹林药物信息叠加药物新制剂。所述的阿司匹林〔aspirin,2-(乙酰氧基)苯甲酸,又名乙酰水杨酸〕是一种白色结晶或结晶性粉末,无臭或微带醋酸臭,微溶于水,易溶于乙醇,可溶于乙醚、氯仿,水溶液呈酸性。为水杨酸的衍生物,是百年经典的解热镇痛药,常用于感冒、流感等发热疾病的退热,以及一般疼痛镇痛。近年来发现阿司匹林对血小板聚集有抑制作用,能阻止血栓形成,临床上用于预防短暂脑缺血发作、心肌梗死、人工心脏瓣膜和静脉瘘或其他手术后血栓的形成。常规的阿司匹林制剂成年人日用量为每日2克。本实施例所述的新制剂,是用阿司匹林原料药物1克,加乙醇溶解充分后,加水至1000毫升,制成1号稀释液。另取阿司匹林原料1公斤,用防水透气材料包装制成药物信息辐射包,置于一个密封容器即药物信息辐射(反应)罐上部,再将所述的稀释液用敞口容器装好置于该密封容器下部,两者中间间隔10厘米,盖紧或关闭密封容器(门),进行药物信息辐射24小时,取出即制成阿司匹林药物信息叠加1号液新制剂。另外再用阿司匹林原料药物1克,加乙醇溶解充分后,加水至10000毫升,制成2号稀释液,再将所述的2号稀释液用敞口容器装好,替换1号稀释液置于前面所述的(置有药物信息辐射包)阿司匹林药物信息辐射罐密封容器下部,盖紧密封容器,进行药物信息辐射24小时,取出即制成阿司匹林药物信息叠加2号液新制剂。所述的药物信息辐射包可以在2年有效期内反复使用。所述的密封容器是特制的药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触)又可以透气或防水透气,实现微孔隔空阿司匹林药物信息辐射叠加。
23.本实施例所述的新制剂,与常规制剂阿司匹林泡腾片,进行了药效学比较实验,其
实验报告如下:1.1受试品及其剂量1号稀释叠加液:大鼠剂量:小剂量 5ml/kg、中剂量10ml/kg、大剂量15ml/kg。
24.2号稀释叠加液:大鼠剂量:小剂量5ml/kg、中剂量10ml/kg、大剂量15ml/kg。
25.1.2阿斯匹林阿斯匹林为经典的解热镇痛药西药,其解热镇痛作用稳定,其制剂选择阿斯匹林泡腾片(巴米尔),为阿斯利康制药有限公司生产,批号1901225。成人日用量为2克,按60kg/人,即人为0.033克/kg体重。按动物与人公斤体重等效剂量折算,大鼠用0.18g/kg体重,相当于临床等效日用剂量。
26.1.3动物sd大鼠232只,spf级,体重 160~180g,雌雄各半;均购自北京维通利华实验动物技术有限公司,许可证编号scxk(京) 2012-0001。饲养在屏障环境,实验动物使用许可证号syxk(京)2013-0035,适用范围为屏障级小鼠、大鼠、豚鼠、兔,有效期为2018年12月25日至2020年12月25日。动物饲料为spf大小鼠维持饲料,由北京科澳协力饲料有限公司提供,产品批号19103213,生产日期20191015,保质期为六个月。
27.1.4 试剂安琪高活性干酵母,安琪酵母(崇左)有限公司产品,生产日期22/08/2019,有效期至21/08/2020。冰醋酸,国药集团化学试剂有限公司产品,批号20150704。
28.1.5 仪器mc-347型电子体温计(肛温),欧姆龙有限公司生产。
29.2. 实验分组情况实验分为8组,分别为空白对照组、阿斯匹林组、1号稀释叠加液组高中低三个组、2号稀释叠加液高中低三个组。
30.3. 统计学处理实验数据采用均数
±
标准差(
±
sd)表示,用excel软件,采用t检验方法进行组间差异比较。
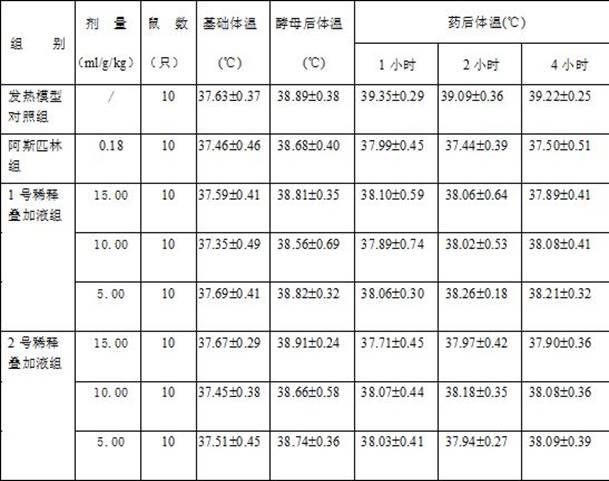
31.4. 实验方法和结果4.1对酵母致大鼠发热体温的影响取sd大鼠116只,雌雄各半,体重 160~180g。试验当日测动物肛温两次,以平均温度作为基础肛温。用15%的干酵母混悬液背部皮下注射(2ml/100g体重)致热,4.5小时后测肛温,取肛温升高0.8~2.0℃之间的动物用于试验。以肛温升高值随机分组,共8组,分别为空白对照组、阿斯匹林组(0.18g/kg)、1号稀释叠加液高中低三个组、2号稀释叠加液高中低三个组,每组10只,雌雄各半。灌胃给药,1ml/100g体重,对照组灌胃给予相同体积的蒸馏水。药后1、2、4小时各测肛温一次,记录不同时间点所测肛温值(℃),并与基础体温比较,推算其治疗系数变化。实验同法重复一次。结果见表1~2。
32.表1 1号稀释叠加液与2号稀释叠加液对酵母致大鼠发热体温的影响(
ꢀ±ꢀ
sd,第一次实验)
注:与对照组比较,p《0.01。
[0033] 表2 1号稀释叠加液与2号稀释叠加液对酵母致大鼠发热体温的影响(
ꢀ±ꢀ
sd,第二次实验)注:与对照组比较,p《0.01。
[0034]
由表1表2结果可见:发热模型对照组在酵母致热后体温明显高于基础体温1℃以上,且在药后(溶剂)1小时、2小时、4小时后体温维持在39℃以上,表明发热模型是成功的。阿司匹林传统制剂组解热作用具有有效性,1号稀释叠加液与2号稀释叠加液实验组解热作用也具有有效性,与对照组比较p《0.01。
[0035]
1号稀释叠加液实验阿司匹林含量是1mg/1ml(0.001g/ml),大剂量组15ml阿司匹林含量15mg/kg;中剂量组10ml阿司匹林含量10mg/kg;小剂量组5ml阿司匹林含量5mg/kg。常规阿司匹林制剂泡腾片实验剂量是180mg/kg。已知阿司匹林大鼠ld50(大鼠经口,医学百科记载)是1500mg/kg。计算得知阿司匹林泡腾片治疗系数是8.33。计算得知1号稀释叠加液大剂量组治疗系数是100,中剂量组治疗系数是150,小剂量组治疗系数是300.2号稀释叠加液实验阿司匹林含量是0.1mg/ml(0.0001g/ml),大剂量组15ml阿司匹林含量0.15mg/kg,中剂量组10ml阿司匹林含量0.1mg/kg,小剂量组5ml阿司匹林含量0.05mg/kg.计算得知2号稀释叠加液大剂量组治疗系数是1000,中剂量组治疗系数是1500,小剂量组治疗系数是3000。
[0036]
实施例2牛黄降压丸药物信息叠加新制剂喷雾剂制备工艺及产品,所述的牛黄降压丸是《中国药典》记载的中成药牛黄降压丸,所述的新制剂是中药组合物。按重量百分比,羚羊角(或山羊角)粉0.1-1%,优选0.7%;水牛角浓缩粉1-5%,优选3%;冰片0.1-1%,优选0.5%;党参10-30,优选22%;决明子8-20%,优选16%;黄芩提取物1-10%,优选0.8%;薄荷1-10,优选6%;珍珠0.1-1%,优选0.5%;人工牛黄0.1-1%,优选0.5%;黄芪10-30%,优选22%;川芎1-20%,优选9%;甘松1-15%优选9%;郁金1-20%,优选10%。所述的制备工艺是按所述的中药组合物配方称取中药材原料,先采用常规中药口服液制备工艺:中药材提取
→
中药提取液净化、浓缩
→
配制
→
过滤,制成与牛黄降压丸剂量一致的常规牛黄降压丸口服液,再将常规浓度的牛黄降压丸口服液稀释500倍,加入适量矫味剂、抑菌剂,制备成稀释液。然后制备牛黄降压药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入降压信息材料,所述的降压信息材料中药组合物用前述配伍,按常规口服液浓度使用的药物500倍装入,制成牛黄降压药物信息叠加辐射罐。再将所述的稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,取出将其液体灌装喷雾剂瓶,制成药物信息叠加牛黄降压丸喷雾剂。所述的喷雾剂治疗高血压,喷雾头部七窍(眼耳鼻口舌),每次10-15喷,每日2-3次,五脏开窍调治高血压。
[0037]
本实施例所述的新制剂产品(试验组即治疗组)与传统的牛黄降压(对照组),进行了临床应用比较实验,实验资料如下:试验采用分层区组随机、阳性平行对照试验设计。在某省中医药研究院附属医院进行临床试验,纳入对象为风阳上亢型高血压病(1-2级),停用西医降压药患者;主要观察指标为一般项目(受试者人口学资料及疾病相关指标)、疗效指标(如血压测量、症状体征)、不良事件/反应发生情况等。试验疗程为7天。计划入组72例受试者,试验组和对照组各36
例。
[0038]
本次临床试验共入组受试者72例,试验组(治疗组)和对照组各36例,试验中无脱落或剔除病例,实际完成病例数为72例。
[0039]
本次试验受试者均来源于门诊病例,受试者基本人口学资料(性别、婚况、年龄、身高、体重等)、一般生命指征(呼吸、心率、体温)、基本病情资料如高血压测量值及分级情况、体格检查情况、合并用药及合并疾病情况、药物过敏情况、中医证候积分及相关症状疗前分级情况等组间差异均无统计学意义(p》0.05),故可认为本次试验受试者基线资料均衡,具有较好的可比性。
[0040]
试验组(治疗组)治疗高血压的显效率为52.78%,总有效率为91.67%;对照组显效率为47.22%,有效率为91.67%,两组治疗高血压的疗效差异无统计学意义(p》0.05)。
[0041]
疗程结束后,试验组(治疗组)收缩压平均下降值为18.44
ꢀ±
8.37mmhg,舒张压下降值为13.95
ꢀ±
8.18 mmhg;对照组收缩压平均下降值为16.74
ꢀ±
10.37mmhg,舒张压下降值为16.13
ꢀ±
8.38mmhg,两组受试者治疗结束后血压均较疗前下降,差异有统计学意义(p《0.05),两组收缩压及舒张压下降幅度组间差异无统计学意义(p》0.05)。
[0042]
试验组(治疗组)中医证候疗效的显效率为83.33%,总有效率为100.0%,对照组显效率为66.67%,总有效率为100.0%,两组中医证候疗效差异无统计学意义(p》0.05)。疗程结束后两组中医证候积分均较疗前下降,差异有统计学意义(p《0.05),两组间下降幅度差异无统计学意义(p》0.05)。疗程结束后各症状体征如眩晕、头痛、烦躁易怒、面红、目赤、口干、口苦、便秘、溲赤等均得到有效改善,组间差异无统计学意义(》0.05)。
[0043]
试验产品及对照产品试验过程中均未发现有使用缺陷。
[0044]
试验中无不良事件/不良反应发生,使用安全。
[0045]
试验证明本发明试验组原料稀释500倍后药物信息辐射叠加工艺制备的新制剂,与传统制剂有效率基本一致,其显效率试验组高于对照组,治疗系数显著扩增。
[0046]
实施例3消渴丸药物信息叠加新制剂制备工艺及产品。所述的消渴丸是治疗糖尿病的中成药,广州第一中药厂生产品种。 所述的消渴丸药物信息叠加新制剂是用 新配制的消渴丸原料,所述的原料是指完成生产时间在3个月以内的消渴丸组合物原料,由以下重百分比的中药:地黄1-30%,葛根1-90%,黄芪1-30%,天花粉1-50%,山药1-30%,玉米须5-50%,用水提醇沉法或超临界萃取法或微波萃取法提取浓缩,再加入1-10%的格列本脲化合物(含量≥99%),充分混合而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规消渴丸剂量一致的常规浓度消渴丸口服液。再将常规浓度的消渴丸口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成消渴丸稀释液。然后制备消渴丸药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气实现药物信息微孔隔空辐射。在药物信息辐射发生舱装入降糖信息材料,所述的降糖信息材料有消渴丸中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成消渴丸药物信息叠加辐射罐。再将
所述的消渴丸稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成消渴丸药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成消渴丸药物信息叠加喷雾剂。
[0047]
实施例4参芪降糖片药物信息叠加新制剂制备工艺及产品。所述的参芪降糖片是治疗糖尿病的中成药,中国国家基本药物中成药品种。 所述的参芪降糖片药物信息叠加新制剂是用 新配制的参芪降糖片原料,所述的原料是指完成生产时间在3个月以内的参芪降糖片组合物原料,由以下重百分比的中药:五味子1-20%,地黄1-30%,黄芪5-30%,天花粉5-30%,山药5-30%,覆盆子1-20%,麦冬5-30,茯苓1-30,泽泻1-30,枸杞子5-50用水提醇沉法或超临界萃取法或微波萃取法提取浓缩,再加入1-10%的人参茎叶皂苷(含量≥90%),充分混合而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规参芪降糖片剂量一致的常规浓度参芪降糖片口服液。再将常规浓度的参芪降糖片口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成参芪降糖片稀释液。然后制备参芪降糖片药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气实现药物信息微孔隔空辐射。在药物信息辐射发生舱装入降糖信息材料,所述的降糖信息材料有参芪降糖片中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成参芪降糖片药物信息叠加辐射罐。再将所述的参芪降糖片稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成参芪降糖片药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成参芪降糖片药物信息叠加喷雾剂。
[0048]
实施例5风湿骨痛片药物信息叠加新制剂制备工艺及产品。所述的风湿骨痛片是治疗风湿关节病的中成药,中国国家基本药物中成药品种。 所述的风湿骨痛片药物信息叠加新制剂是用 新配制的风湿骨痛片原料,所述的原料是指完成生产时间在3个月以内的风湿骨痛片组合物原料,由以下重百分比的中药:麻黄1-10%,马钱子1-10%,制川乌1-10%,防风5-30%,独活5-30%,牛膝5-30%,桑寄生5-30%,防己5-30%,丹参1-30%,桂枝1-20%,续断1-30%,木瓜5-30%用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规风湿骨痛片剂量一致的常规浓度风湿骨痛片口服液。再将常规浓度的风湿骨痛片口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成风湿骨痛片稀释液。然后制备风湿骨痛片药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气实现药物信息微孔隔空辐射。在药物信息辐射发生舱装入风湿骨痛信息材料,所述的风湿骨痛信息材料有风湿骨痛片中药组合物,用前述配伍,按常
规口服液浓度剂量的药物原料粉末100-1000倍装入,制成风湿骨痛药物信息叠加辐射罐。再将所述的风湿骨痛片稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成风湿骨痛片药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成风湿骨痛片药物信息叠加喷雾剂。
[0049]
实施例6鼻炎康片药物信息叠加新制剂制备工艺及产品。所述的鼻炎康片是治疗鼻炎病的中成药,中国国家基本药物中成药品种。 所述的鼻炎康片药物信息叠加新制剂是用 新配制的鼻炎康片原料,所述的原料是指完成生产时间在3个月以内的鼻炎康片组合物原料,由以下重百分比的中药:广藿香1-20%、鹅不食草1-20%、野菊花5-30%、黄芩1-20%、薄荷油1-10%、苍耳子5-30%、麻黄1-20%、当归5-30%、猪胆粉1-20%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩,再加入马来酸氯苯那敏1-10%(含量≥99%),充分混合而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规鼻炎康片剂量一致的常规浓度鼻炎康片口服液。再将常规浓度的鼻炎康片口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成鼻炎康片稀释液。然后制备鼻炎康片药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入鼻炎信息材料,所述的鼻炎信息材料有鼻炎康片中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成鼻炎康片药物信息叠加辐射罐。再将所述的鼻炎康片稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成鼻炎康片药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成鼻炎康片药物信息叠加喷雾剂。
[0050]
实施例7颈复康颗粒药物信息叠加新制剂制备工艺及产品。所述的颈复康颗粒是治疗劲椎病的中成药,中国国家基本药物中成药品种。 所述的颈复康颗粒药物信息叠加新制剂是用 新配制的颈复康颗粒原料,所述的原料是指完成生产时间在3个月以内的颈复康颗粒组合物原料,由以下重百分比的中药:羌活1-20%,川芎1-20%,葛根5-30%,秦艽5-30%,威灵仙5-30%,苍术1-20%,丹参5-30%,白芍1-20%,地龙(酒制)1-20%,红花1-20%,乳香(制)1-10%,黄芪5-30%,党参5-30%,地黄1-20%,石决明1-20%,花蕊石(煅)1-20%,黄柏1-20%,王不留行(炒)1-20%,桃仁(去皮)1-20%,没药(制)1-10%,土鳖虫(酒制)1-10%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规颈复康颗粒剂量一致的常规浓度颈复康颗粒口服液。再将常规浓度的颈复康颗粒口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成颈复康颗粒稀释液。然后制备颈复康颗粒药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物
信息辐射发生舱装入劲椎病信息材料,所述的劲椎病信息材料有颈复康颗粒中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成颈复康颗粒药物信息叠加辐射罐。再将所述的颈复康颗粒稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成颈复康颗粒药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成颈复康颗粒药物信息叠加喷雾剂。
[0051]
实施例8金蝉止痒胶囊药物信息叠加新制剂制备工艺及产品。所述的金蝉止痒胶囊是治疗皮肤病的中成药,中国国家基本药物中成药品种。 所述的金蝉止痒胶囊药物信息叠加新制剂是用 新配制的金蝉止痒胶囊原料,所述的原料是指完成生产时间在3个月以内的金蝉止痒胶囊组合物原料,由以下重百分比的中药:金银花1-20%、栀子1-20%、黄芩1-20%、苦参1-20%、黄柏1-20%、龙胆5-30%、白芷5-30%、白鲜皮5-30%、蛇床子1-20%、蝉蜕5-30%、连翘1-20%、地肤子5-30、地黄1-20%、青蒿1-20%、广藿香1-10%、甘草1-10%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规金蝉止痒胶囊剂量一致的常规浓度金蝉止痒胶囊口服液。再将常规浓度的金蝉止痒胶囊口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成金蝉止痒胶囊稀释液。然后制备金蝉止痒胶囊药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入皮肤病信息材料,所述的皮肤病信息材料有金蝉止痒胶囊中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成金蝉止痒胶囊药物信息叠加辐射罐。再将所述的金蝉止痒胶囊稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成金蝉止痒胶囊药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成金蝉止痒胶囊药物信息叠加喷雾剂。
[0052]
实施例9平消片药物信息叠加新制剂制备工艺及产品。所述的平消片是治疗癌症的中成药,中国国家基本药物中成药品种。 所述的平消片药物信息叠加新制剂是用 新配制的平消片原料,所述的原料是指完成生产时间在3个月以内的平消片组合物原料,由以下重百分比的中药:郁金5-30%、马钱子粉1-20%、仙鹤草5-30%、五灵脂5-30%、白矾1-20%、硝石1-20%、干漆(制)1-10%、枳壳(麸炒)10-30%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规平消片剂量一致的常规浓度平消片口服液。再将常规浓度的平消片口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成平消片稀释液。然后制备平消片药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入抗癌信息材料,所述的抗癌信息材
料有平消片中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成平消片药物信息叠加辐射罐。再将所述的平消片稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成平消片药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成平消片药物信息叠加喷雾剂。
[0053]
实施例10珍珠明目滴眼液药物信息叠加新制剂制备工艺及产品。所述的珍珠明目滴眼液是治疗眼病的中成药,中国国家基本药物中成药品种。 所述的珍珠明目滴眼液药物信息叠加新制剂是用 新配制的珍珠明目滴眼液原料,所述的原料是指完成生产时间在3个月以内的珍珠明目滴眼液组合物原料,由以下重百分比的中药:珍珠30-80%,冰片20-70%。用水提醇沉法或超临界萃取法或微波萃取法提取,再加入辅料氯化钠、羟苯乙酯适量而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规滴眼液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规珍珠明目滴眼液剂量一致的常规浓度珍珠明目滴眼液。再将常规浓度的珍珠明目滴眼液稀释100-1000倍,加入适量抑菌剂,制备成珍珠明目滴眼液稀释液。然后制备珍珠明目滴眼液药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入明目信息材料,所述的明目信息材料有珍珠明目滴眼液中药组合物,用前述配伍,按常规滴眼液浓度剂量的药物原料粉末100-1000倍装入,制成珍珠明目滴眼液药物信息叠加辐射罐。再将所述的珍珠明目滴眼液稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成珍珠明目滴眼液药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成珍珠明目滴眼液药物信息叠加喷雾剂。
[0054]
实施例11仙灵骨葆胶囊药物信息叠加新制剂制备工艺及产品。所述的仙灵骨葆胶囊是治疗骨质疏松病的中成药,中国国家基本药物中成药品种。 所述的仙灵骨葆胶囊药物信息叠加新制剂是用 新配制的仙灵骨葆胶囊原料,所述的原料是指完成生产时间在3个月以内的仙灵骨葆胶囊组合物原料,由以下重百分比的中药:淫羊藿5-50%、续断3-30%、丹参3-30%、知母1-20%、补骨脂1-20%、地黄3-30%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规仙灵骨葆胶囊剂量一致的常规浓度仙灵骨葆胶囊口服液。再将常规浓度的仙灵骨葆胶囊口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成仙灵骨葆胶囊稀释液。然后制备仙灵骨葆胶囊药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入骨质疏松信息材料,所述的骨质疏松信息材料有仙灵骨葆胶囊中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成仙灵骨葆胶囊药物信息叠加辐
射罐。再将所述的仙灵骨葆胶囊稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成仙灵骨葆胶囊药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成仙灵骨葆胶囊药物信息叠加喷雾剂。
[0055]
实施例12接骨七厘片药物信息叠加新制剂制备工艺及产品。所述的接骨七厘片是治疗骨伤的中成药,中国国家基本药物中成药品种。 所述的接骨七厘片药物信息叠加新制剂是用 新配制的接骨七厘片原料,所述的原料是指完成生产时间在3个月以内的接骨七厘片组合物原料,由以下重百分比的中药:乳香(炒)1-10%、没药(炒)1-10%、当归3-30%、土鳖虫1-20%、骨碎补(烫)3-30%、硼砂1-10%、龙血竭1-20%、自然铜(煅)1-30%、大黄(酒炒)3-30%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规接骨七厘片剂量一致的常规浓度接骨七厘片口服液。再将常规浓度的接骨七厘片口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成接骨七厘片稀释液。然后制备接骨七厘片药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入接骨信息材料,所述的接骨信息材料有接骨七厘片中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成接骨七厘片药物信息叠加辐射罐。再将所述的接骨七厘片稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成接骨七厘片药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成接骨七厘片药物信息叠加喷雾剂。
[0056]
实施例13复方血栓通胶囊药物信息叠加新制剂制备工艺及产品。所述的复方血栓通胶囊是治疗血栓的中成药,中国国家基本药物中成药品种。 所述的复方血栓通胶囊药物信息叠加新制剂是用 新配制的复方血栓通胶囊原料,所述的原料是指完成生产时间在3个月以内的复方血栓通胶囊组合物原料,由以下重百分比的中药:三七5-50%,黄芪5-50%,丹参3-30%,玄参1-20%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规复方血栓通胶囊剂量一致的常规浓度复方血栓通胶囊口服液。再将常规浓度的复方血栓通胶囊口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成复方血栓通胶囊稀释液。然后制备复方血栓通胶囊药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入降血栓信息材料,所述的降血栓信息材料有复方血栓通胶囊中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成复方血栓通胶囊药物信息叠加辐射罐。再将所述的复方血栓通胶囊稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药
物信息辐射叠加48小时,制成复方血栓通胶囊药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成复方血栓通胶囊药物信息叠加喷雾剂。
[0057]
实施例14妇炎消胶囊药物信息叠加新制剂制备工艺及产品。所述的妇炎消胶囊是治疗妇科病的中成药,中国国家基本药物中成药品种。 所述的妇炎消胶囊药物信息叠加新制剂是用 新配制的妇炎消胶囊原料,所述的原料是指完成生产时间在3个月以内的妇炎消胶囊组合物原料,由以下重百分比的中药:醡浆草3-30% 败酱草5-50% 天花粉 2-20%大黄1-20% 牡丹皮1-20% 苍术 3-30%乌药1-10%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规妇炎消胶囊剂量一致的常规浓度妇炎消胶囊口服液。再将常规浓度的妇炎消胶囊口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成妇炎消胶囊稀释液。然后制备妇炎消胶囊药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入消炎信息材料,所述的消炎信息材料有妇炎消胶囊中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成妇炎消胶囊药物信息叠加辐射罐。再将所述的妇炎消胶囊稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成妇炎消胶囊药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成妇炎消胶囊药物信息叠加喷雾剂。
[0058]
实施例15尿毒清颗粒药物信息叠加新制剂制备工艺及产品。所述的尿毒清颗粒是治疗糖尿病的中成药,中国国家基本药物中成药品种。 所述的尿毒清颗粒药物信息叠加新制剂是用 新配制的尿毒清颗粒原料,所述的原料是指完成生产时间在3个月以内的尿毒清颗粒组合物原料,由以下重百分比的中药:大黄1-20%、黄芪3-30%、丹参3-30%、川芎1-20%、何首乌(制)1-20%、党参1-20%、白术3-30%、茯苓3-30%、桑白皮3-30%、苦参1-20%、车前草3-30%、半夏(姜制)1-10%、柴胡1-10%、菊花1-20%、白芍1-20%、甘草1-10%。用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规尿毒清颗粒剂量一致的常规浓度尿毒清颗粒口服液。再将常规浓度的尿毒清颗粒口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成尿毒清颗粒稀释液。然后制备尿毒清颗粒药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入尿毒清信息材料,所述的尿毒清信息材料有尿毒清颗粒中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成尿毒清颗粒药物信息叠加辐射罐。再将所述的尿毒清颗粒稀释液倒入敞口容器置于药物信息辐射反应舱,
关上门密封,进行药物信息辐射叠加48小时,制成尿毒清颗粒药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成尿毒清颗粒药物信息叠加喷雾剂。
[0059]
实施例16复方丹参片药物信息叠加新制剂制备工艺及产品。所述的复方丹参片是治疗心血管病的中成药,中国国家基本药物中成药品种。 所述的复方丹参片药物信息叠加新制剂是用 新配制的复方丹参片原料,所述的原料是指完成生产时间在3个月以内的复方丹参片组合物原料,由以下重百分比的中药:丹参10-50%,三七5-50%,冰片1-20%,用水提醇沉法或超临界萃取法或微波萃取法提取浓缩而成。所述的新制剂制备工艺是按所述的中药组合物配方称取所述的原料,先采用常规中药口服液制备工艺:配方称取原料
→
常规浓度加水配制
→
过滤
→
净化,制成与常规复方丹参片剂量一致的常规浓度复方丹参片口服液。再将常规浓度的复方丹参片口服液稀释100-1000倍,加入适量矫味剂、抑菌剂,制备成复方丹参片稀释液。然后制备复方丹参片药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入心血管信息材料,所述的心血管信息材料有复方丹参片中药组合物,用前述配伍,按常规口服液浓度剂量的药物原料粉末100-1000倍装入,制成复方丹参片药物信息叠加辐射罐。再将所述的复方丹参片稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成复方丹参片药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成复方丹参片药物信息叠加喷雾剂。
[0060]
实施例17紫杉醇药物信息叠加新制剂制备工艺及产品。所述的紫杉醇是一种天然抗癌药物,分子式为c47h51no14,在临床上已经广泛用于乳腺癌、卵巢癌和部分头颈癌和肺癌的治疗。紫杉醇作为一个具有抗癌活性的二萜生物碱类化合物,其新颖复杂的化学结构、广泛而显著的生物活性、全新独特的作用机制、奇缺的自然资源使其受到了植物学家、化学家、药理学家、分子生物学家的极大青睐,使其成为20世纪下半叶举世瞩目的抗癌明星和研究重点。 常规紫杉醇制剂有固体制剂与注射剂,所述的紫杉醇药物信息叠加新制剂制备工艺是按所述的常规制剂注射剂配方称取所述的紫杉醇原料,先采用常规注射剂制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规注射剂剂量一致的常规浓度紫杉醇注射液。再将常规浓度的紫杉醇注射液稀释100-1000倍,加入适量抑菌剂,制备成紫杉醇稀释液。然后制备紫杉醇药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入癌症信息材料,所述的癌症信息材料有紫杉醇原料,按常规注射剂浓度剂量的药物原料粉末100-1000倍装入,制成紫杉醇药物信息叠加辐射罐。再将所述的紫杉醇稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成紫杉醇药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成紫杉醇药物信息叠加喷雾剂。
[0061]
实施例18羟喜树碱药物信息叠加新制剂制备工艺及产品。所述的羟喜树碱是一种天然抗癌药物,羟喜树碱(hydroxycamptothecin)为从珙桐科落叶植物喜树的种子或根皮中提出额一种生物碱。喜树碱因泌尿系统毒性大,临床应用受到限制。本品为喜树碱的羟基衍生物,作用机制与喜树碱相似,但毒性较小。本品是dna合成抑制剂,实验研究表明主要作用于dna合成期(即s期),对g0期细胞没有作用,对g1、g2与m期细胞有轻微杀伤力。对多种动物肿瘤有抑制作用。作用机制为抑制dna拓扑异构酶ⅰ。与常用抗肿瘤药物无交叉耐药、动物实验显示其抗瘤谱广。对核酸特别是dna的合成有明显抑制作用。羟喜树碱在血液中的清除过程呈双相曲线,两相生物分别为4.5分钟和29分钟。给药后1小时,胆囊、小肠内容物维持浓度最高,其次为癌细胞,其他依次为骨髓、胃、肺等器官。静脉注射的羟喜树碱主要从胆汁排泄,通过粪便排出体外。24小时排出量胃39%,从粪便中排出29.6%,尿液中排出不到9%,癌细胞中24小时内保持稳定水平。 常规羟喜树碱制剂有注射剂,所述的羟喜树碱药物信息叠加新制剂制备工艺是按所述的常规制剂注射剂配方称取所述的羟喜树碱原料,先采用常规注射剂制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规注射剂剂量一致的常规浓度羟喜树碱注射液。再将常规浓度的羟喜树碱注射液稀释100-1000倍,加入适量抑菌剂,制备成羟喜树碱稀释液。然后制备羟喜树碱药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入癌症信息材料,所述的癌症信息材料有羟喜树碱原料,按常规注射剂浓度剂量的药物原料粉末100-1000倍装入,制成羟喜树碱药物信息叠加辐射罐。再将所述的羟喜树碱稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成羟喜树碱药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成羟喜树碱药物信息叠加喷雾剂。
[0062]
实施例19多柔比星药物信息叠加新制剂制备工艺及产品。所述的多柔比星是一种抗癌药物,又名阿霉素(英文名称:adriamycin),是一种抗生素类药物,分子式为c27h29no11。多柔比星抗瘤谱较广,适用于急性白血病(淋巴细胞性和粒细胞性)、恶性淋巴瘤、乳腺癌、支气管肺癌(未分化小细胞性和非小细胞性)、卵巢癌、软组织肉瘤、成骨肉瘤、横纹肌肉瘤、尤文肉瘤、母细胞瘤、神经母细胞瘤、膀胱癌、甲状腺癌、前列腺癌、头颈部鳞癌、睾丸癌、胃癌、肝癌等。所述的多柔比星是盐酸多柔比星。 常规多柔比星制剂有注射剂,所述的多柔比星药物信息叠加新制剂制备工艺是按所述的常规制剂注射剂配方称取所述的多柔比星原料,先采用常规注射剂制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规注射剂剂量一致的常规浓度多柔比星注射液。再将常规浓度的多柔比星注射液稀释100-1000倍,加入适量抑菌剂,制备成多柔比星稀释液。然后制备多柔比星药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入癌症信息材料,所述的癌症信息材料
有多柔比星原料,按常规注射剂浓度剂量的药物原料粉末100-1000倍装入,制成多柔比星药物信息叠加辐射罐。再将所述的多柔比星稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成多柔比星药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成多柔比星药物信息叠加喷雾剂。
[0063]
实施例20阿扎胞苷药物信息叠加新制剂制备工艺及产品。所述的阿扎胞苷是一种抗癌药物,中文别名:5-氮杂胞苷、5-氮杂胞嘧啶核苷、氮胞苷、氮杂胞苷,英文别名:5-azacytidine、ladakamycin,本品为胞嘧啶核苷类药物。能直接掺入dna中,抑制dna和rna合成,可杀伤处于s期的细胞。静注后血浆半衰期为3.5小时。临床治疗骨髓增生异常综合症(mds),急性非淋巴细胞性白血病。用于乳腺癌、肠癌、黑色素瘤等有一定疗效。 常规阿扎胞苷制剂有注射剂,所述的阿扎胞苷药物信息叠加新制剂制备工艺是按所述的常规制剂注射剂配方称取所述的阿扎胞苷原料,先采用常规注射剂制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规注射剂剂量一致的常规浓度阿扎胞苷注射液。再将常规浓度的阿扎胞苷注射液稀释100-1000倍,加入适量抑菌剂,制备成阿扎胞苷稀释液。然后制备阿扎胞苷药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入癌症信息材料,所述的癌症信息材料有阿扎胞苷原料,按常规注射剂浓度剂量的药物原料粉末100-1000倍装入,制成阿扎胞苷药物信息叠加辐射罐。再将所述的阿扎胞苷稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成阿扎胞苷药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成阿扎胞苷药物信息叠加喷雾剂。
[0064]
实施例21阿法替尼药物信息叠加新制剂制备工艺及产品。所述的阿法替尼是一种抗癌药物,所述的阿法替尼(afatinib)是表皮生长因子受体(egfr)和人表皮生长因子受体2(her2)酪氨酸激酶的强效、不可逆的双重抑制剂。适用于以下患者治疗:1具有表皮生长因子受体(egfr)基因敏感突变的局部晚期或转移性非小细胞肺癌 (nsclc),既往未接受过egfr酪氨酸激酶抑制剂(tki)治疗2含铂化疗期间或化疗后疾病进展的局部晚期或转移性鳞状组织学类型的非小细胞肺癌(nsclc)。 常规阿法替尼制剂有口服制剂,所述的阿法替尼药物信息叠加新制剂制备工艺是按所述的常规制配方称取所述的阿法替尼原料,先采用常规口服液制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规口服剂剂量一致的常规浓度阿法替尼口服液。再将常规浓度的阿法替尼口服液稀释100-1000倍,加入适量抑菌剂,制备成阿法替尼稀释液。然后制备阿法替尼药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入癌症信息材料,所述的癌症信息材料有阿法替尼原料,按常规口服剂量的药物原料粉末100-1000倍装入,制成阿法替尼药物信息叠加辐射罐。再将所述的阿法替尼稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密
封,进行药物信息辐射叠加48小时,制成阿法替尼药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成阿法替尼药物信息叠加喷雾剂。
[0065]
实施例22环磷酰胺药物信息叠加新制剂制备工艺及产品。所述的环磷酰胺是一种广谱抗癌药物,所述的环磷酰胺(cyclophosphamide,ctx)是进入人体内被肝脏或肿瘤内存在的过量的磷酰胺酶或磷酸酶水解,变为活化作用型的磷酰胺氮芥而起作用的氮芥类衍生物。抗瘤谱广,是第一个所谓“潜伏化”广谱抗肿瘤药,对白血病和实体瘤都有效。所述的环磷酰胺在体外无活性,主要通过肝脏p450酶水解成醛磷酰胺再运转到组织中形成磷酰胺氮芥而发挥作用。环磷酰胺可由脱氢酶转变为羧磷酰胺而失活,或以丙烯醛形式排出,导致泌尿道毒性。属于周期非特异性药,作用机制与氮芥相同。 常规环磷酰胺制剂有口服及注射剂,所述的环磷酰胺药物信息叠加新制剂制备工艺是按所述的常规制剂注射剂配方称取所述的环磷酰胺原料,先采用常规注射剂制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规注射剂剂量一致的常规浓度环磷酰胺注射液。再将常规浓度的环磷酰胺注射液稀释100-1000倍,加入适量抑菌剂,制备成环磷酰胺稀释液。然后制备环磷酰胺药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入癌症信息材料,所述的癌症信息材料有环磷酰胺原料,按常规注射剂浓度剂量的药物原料粉末100-1000倍装入,制成环磷酰胺药物信息叠加辐射罐。再将所述的环磷酰胺稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成环磷酰胺药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成环磷酰胺药物信息叠加喷雾剂。
[0066]
以上实施例所述的传统药品的药物信息叠加喷雾剂治疗其相关病症,喷雾头部七窍(眼耳鼻口舌),每次10-15喷,每日2-3次,五脏开窍调治。所述的新制剂扩增治疗系数100-1000倍后,其临床疗效与传统药品没有显著性差异。
[0067]
实施例23氨氯地平药物信息叠加新制剂制备工艺及产品。所述的氨氯地平(amlodipine),化学名为6-甲基-2-(2-氨基乙氧基)甲基-4-(2-氯苯基)-1,4-二氢-3,5-吡啶二甲酸甲乙酯,分子式为c20h25cln2o5,为一种治疗高血压及冠状动脉疾病的药物。 常规氨氯地平制剂有口服制剂,所述的氨氯地平药物信息叠加新制剂制备工艺是按所述的常规制剂配方称取所述的氨氯地平原料,先采用常规口服液制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规口服剂量一致的常规浓度氨氯地平口服液。再将常规浓度的氨氯地平口服液稀释100-1000倍,加入适量抑菌剂,制备成氨氯地平稀释液。然后制备氨氯地平药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入降压信息材料,所述的降压信息材料有氨氯地平原料,按常规口服剂量的药物原料粉末100-1000倍装入,制成氨氯地平药物信息叠加辐射罐。再将所述的氨氯地平稀释液倒入敞口容器置于药
物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成氨氯地平药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成氨氯地平药物信息叠加喷雾剂。所述的氨氯地平药物信息叠加喷雾剂治疗高血压,喷雾头部七窍(眼耳鼻口舌),每次10-15喷,每日2-3次,五脏开窍调治高血压症。
[0068]
实施例24阿卡波糖药物信息叠加新制剂制备工艺及产品。所述的阿卡波糖阿卡波糖(acarbose)为一种α-葡萄糖苷酶抑制剂,是复杂的低聚糖,其结构类似寡糖,这种非寡糖的“假寡糖”可在小肠上部细胞刷状缘处和寡糖竞争而与α-葡萄糖苷酶可逆地结合,抑制各种α-葡萄糖苷酶如麦芽糖酶、异麦芽糖酶、葡萄糖淀粉酶及蔗糖酶的活性,使淀粉分解成寡糖如麦芽糖(双糖)、麦芽三糖及糊精(低聚糖)进而分解成葡萄糖的速度减慢,使蔗糖分解成葡萄糖和果糖的速度减慢,因此造成肠道葡萄糖的吸收减缓,从而缓解餐后高血糖,达到降低血糖的作用。 常规阿卡波糖制剂有口服制剂,所述的阿卡波糖药物信息叠加新制剂制备工艺是按所述的常规制剂配方称取所述的阿卡波糖原料,先采用常规口服液制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规口服剂量一致的常规浓度阿卡波糖口服液。再将常规浓度的阿卡波糖口服液稀释100-1000倍,加入适量抑菌剂,制备成阿卡波糖稀释液。然后制备阿卡波糖药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入降糖信息材料,所述的降糖信息材料有阿卡波糖原料,按常规口服剂量的药物原料粉末100-1000倍装入,制成阿卡波糖药物信息叠加辐射罐。再将所述的阿卡波糖稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成阿卡波糖药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成阿卡波糖药物信息叠加喷雾剂。所述的阿卡波糖药物信息叠加喷雾剂治疗2型糖尿病,喷雾头部七窍(眼耳鼻口舌),每次10-15喷,每日2-3次,五脏开窍调治他那边。所述的新制剂扩增治疗系数100-1000倍后,其临床疗效与传统的阿卡波糖制剂没有显著性差异。
[0069]
实施例25氨溴索药物信息叠加新制剂制备工艺及产品。所述的氨溴索,英文名称:ambroxol,分子式:c13h18br2n2o,为溴己新在体内的活性代谢产物,为黏液溶解药,可用于用于急、慢性支气管炎及支气管哮喘、支气管扩张、肺气肿、肺结核、肺尘埃沉着病、手术后的咳嗽困难等。注射给药可用于术后肺部并发症的预防及早产儿、新生儿呼吸窘迫综合征的治疗。本品高剂量(每次250~500mg,一日2次)有降低血浆尿酸浓度和促进尿酸排泄的作用,可用于治疗痛风。 常规氨溴索制剂有口服制剂注射剂,所述的氨溴索药物信息叠加新制剂制备工艺是按所述的常规制剂配方称取所述的氨溴索原料,先采用常规口服液制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规口服剂量一致的常规浓度氨溴索口服液。再将常规浓度的氨溴索口服液稀释100-1000倍,加入适量抑菌剂,制备成氨溴索稀释液。然后制备氨溴索药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发
生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入信息材料,所述的信息材料有氨溴索原料,按常规口服剂量的药物原料粉末100-1000倍装入,制成氨溴索药物信息叠加辐射罐。再将所述的氨溴索稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成氨溴索药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成氨溴索药物信息叠加喷雾剂。所述的氨溴索药物信息叠加喷雾剂治疗咳嗽,喷雾头部七窍(眼耳鼻口舌),每次10-15喷,每日2-3次,五脏开窍调治咳嗽。所述的新制剂扩增治疗系数100-1000倍后,其临床疗效与传统的氨溴索片没有显著性差异。
[0070]
实施例26奥美拉唑药物信息叠加新制剂制备工艺及产品。所述的奥美拉唑,英文名称:(r)-omeprazole,英文别名:losec;mepral;gastrogard;omeprazole;loec;moprial;omeprazolum,分子式:c17h19n3o3s主要用于十二指肠溃疡和卓-艾综合征,也可用于胃溃疡和反流性食管炎;静脉注射可用于消化性溃疡急性出血的治疗。与阿莫西林和克林霉素或与甲硝唑与克拉霉素合用,以杀灭幽门螺杆菌。 常规奥美拉唑制剂有口服制剂注射剂,所述的奥美拉唑药物信息叠加新制剂制备工艺是按所述的常规制剂配方称取所述的奥美拉唑原料,先采用常规口服液制备工艺:配方称取原料
→
溶解配制
→
过滤
→
净化,制成与常规口服剂量一致的常规浓度奥美拉唑口服液。再将常规浓度的奥美拉唑口服液稀释100-1000倍,加入适量抑菌剂,制备成奥美拉唑稀释液。然后制备奥美拉唑药物信息叠加辐射(反应)罐,所述的辐射罐是金属密封罐,高1米,直径0.5米,结构分3层,上部是药物信息辐射发生舱,下部是药物信息辐射反应舱,中间是隔空层。发生舱与反应舱有可以开关的密封门。隔空层厚度1-10厘米,有若干微孔,可以使发生舱的物质与反应舱的物质保持隔空(不接触、不泄露)又可以透气或防水透气。在药物信息辐射发生舱装入信息材料,所述的信息材料有奥美拉唑原料,按常规口服剂量的药物原料粉末100-1000倍装入,制成奥美拉唑药物信息叠加辐射罐。再将所述的奥美拉唑稀释液倒入敞口容器置于药物信息辐射反应舱,关上门密封,进行药物信息辐射叠加48小时,制成奥美拉唑药物信息叠加液,取出将其液体灌装喷雾剂瓶,制成奥美拉唑药物信息叠加喷雾剂。所述的奥美拉唑药物信息叠加喷雾剂治疗胃及十二指肠溃疡病,喷雾头部七窍(眼耳鼻口舌),每次10-15喷,每日2-3次,五脏开窍调治胃及十二指肠溃疡病。所述的新制剂扩增治疗系数100-1000倍后,其临床疗效与传统的奥美拉唑没有显著性差异。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1