甘草异黄烷衍生物在制备预防、缓解或/和治疗瘙痒症药物中的应用
1.本发明涉及医药领域,涉及一种预防、缓解和/或治疗瘙痒症的药物或保健品,特别涉及一种中药甘草中的天然产物甘草异黄烷衍生物成分在预防、缓解和/或治疗瘙痒症药物或保健品中的应用。
背景技术:
2.甘草异黄烷类化合物是一类来源于传统中药甘草的天然产物,之前的研究揭示甘草具有广泛的药理作用,而具体到甘草异黄烷类化合物,已发现的作用包括抗菌、抗癌、抗氧化、抗炎等。在已有研究的基础上,进一步挖掘这类化合物新的作用及背后的分子机制具有重要的研究和应用价值。
3.瞬时受体电位通道(transient receptor potential ion channels,trps)是一类在许多组织器官中表达广泛并参与调控多种细胞功能的非选择性阳离子通道。依据氨基酸序列的同源性,trp通道分为7个亚家族:trpc(canonical)、trpv(vanilloid)、trpm(melastatin)、trpa(ankyrin)、trpn(nompc)、trpp(polycystin)和trpml(mucolipin)。通过介导胞内外阳离子的跨膜流动,trp通道在细胞钙离子的吸收、神经元生长锥的引导、角化细胞的生长与分化及感觉信号的传导等过程中发挥了关键作用。更为重要的是,一系列人类疾病,包括多囊性肾病、骨骼发育畸形、olmsted综合征等,都被证明是由trp通道的功能异常所引发。
4.对于trpv亚家族,自第一个成员trpv1在1997年被成功克隆开始,亚家族中的其它成员也陆续被发现和克隆。从分子序列和结构来看,trpv亚家族的六个成员序列高度同源,且都有着与经典的电压依赖钾通道类似的分子结构,即均为由4个亚基组装而成的四聚体,其中每个亚基包含6个穿膜区,以及位于胞内侧的包含锚蛋白重复序列结构的n端和包含“trp结构域”的c端。在第5和第6个穿膜区之间有一个环状结构,构建了离子通过的孔道,并被认为与通道的离子选择性有关。作为非选择性阳离子通道,trpv亚家族的成员均具有对二价阳离子更高的选择透过性,这其中尤以ca
2+
离子最为重要。由于trpv通道受到温度、ph值及一系列內源、外源性配体分子的调节,因此它们广泛参与机体感觉信息传递且具有调控胞内ca
2+
平衡等多种重要的生理功能。
5.trpv3通道于2002年首次被克隆,并被发现温热温度(31~39℃)即可将其激活。后续研究发现了更多可以激活trpv3的化合物,包括2-apb以及樟脑、薄荷醇、香芹酚等天然分子。trpv3通道在多种组织器官中广泛表达,其中尤以各种上皮组织最为重要,主要包括皮肤、口腔和胃肠道等的表皮。之前关于小鼠的研究发现,一方面,trpv3基因敲除小鼠可出现温觉障碍、毛发异常卷曲和皮肤屏障受损;而且敲除trpv3后,在多肽sligrl诱发的急性瘙痒,以及特应性皮炎模型和干皮症模型的慢性瘙痒中,小鼠的搔抓反应都显著降低了。另一方面,表达trpv3功能增强突变体(p.g573s)的转基因小鼠会出现严重的脱毛和皮肤红斑、水肿、糜烂、脱屑等,并伴有明显的自发瘙痒行为。更重要的是,我们之前的研究发现人
trpv3的功能增强突变会导致一种罕见的遗传性皮肤病——olmsted综合征,病人症状集中表现为手足皮肤的严重角化甚至进行性损毁,以及严重的脱发和疼痛瘙痒等。这些研究表明,trpv3在皮肤屏障、毛发发育、温度感受、炎症反应及痛痒觉传导等生理过程中均有重要作用;而作为一个重要的皮肤药物的靶点,特别是其所具有的治疗瘙痒的潜力,使trpv3已愈发成为目前最受关注的trp通道之一。然而由于一直缺乏有效的研究工具,包括特异性的激动剂和拮抗剂等,因此为解决更多有关trpv3的重要问题,寻找和开发更多调控trpv3的药物分子成为了大家共同关注的焦点。
6.对于离子通道的功能研究,要评估某一化合物对其的作用效果,传统上主要依赖于对电生理特性的检测。单细胞膜片钳记录技术因其直接、灵敏的优点成为了应用最广泛的电生理检测技术,具体而言,通过利用玻璃微电极与细胞膜表明形成的高阻抗封接,将细胞膜上表达的离子通道接入放大器、电极和浴液组成的环状电路,当外加不同刺激时,依据在一定的人工钳制细胞膜电位下所记录到的电路中电流变化,反映出离子通道的开闭状况。
7.瘙痒是一种可以诱发搔抓反应的常见令人不快的感觉,与疼痛相似却也有所区别,因为疼痛往往会促使人尽力避免触碰患处。痒觉的产生过程也与痛觉类似,依赖于初级传入神经元在外周器官如皮肤等的神经末梢对各种致痒分子的探测,外部的致痒原,或者由皮肤细胞、免疫细胞等分泌的內源性致痒分子,首先激活初级感觉神经元产生神经冲动,这些神经信号随即传入脊髓背角,经脊髓内部神经元接力后最终传导到大脑的感觉中枢产生痒觉。一般认为不同的致痒原会激活不同类群的感觉神经元,而依据对组胺这种最常见致痒原的反应,可把不同的致痒原诱发的瘙痒反应粗略分为组胺依赖性和非组胺依赖性两类。同时根据瘙痒感觉持续的时间长短,还可分为急性瘙痒和慢性瘙痒两大类,相对于急性瘙痒所具有的警示意义,持续不断且使人衰弱的慢性瘙痒,既可能伴随某些皮肤和系统性疾病而发生,又可以在身体无其他明显病患时发作,变成一种无明显生理意义而纯粹恼人的病症。
8.作为一种皮肤科常见的临床症状,瘙痒与多种疾病,如特应性皮炎、湿疹、银屑病等相伴而生,目前有关组胺依赖性和非组胺依赖性瘙痒的神经和分子机制已经逐步被揭示,据此也有不少治疗皮肤瘙痒的药物被开发出来,包括主要针对组胺依赖性瘙痒的抗组胺类药物和能短暂缓解瘙痒的清凉药物等,这些药物或者作用范围有限,或者有较大副作用,而且在临床上一直缺少针对非组胺依赖性急性瘙痒和慢性瘙痒的止痒药物,因此开发更多具有全新作用机制的止痒药物,将为饱受瘙痒困扰的人们带来新的希望。
技术实现要素:
9.本发明的目的是针对现有治疗瘙痒的药物存在的不足,尤其是针对非组胺依赖性急性瘙痒和慢性瘙痒的止痒药物及其在应用中存在的技术不足,提供一种甘草异黄烷衍生物在制备治疗瘙痒的药物中的应用,本发明的甘草异黄烷衍生物为trpv3的拮抗分子,以trpv3为靶点,治疗瘙痒,对非组胺依赖性急性瘙痒和慢性瘙痒的治疗效果显著。
10.为实现本发明的目的,本发明一方面提供一种甘草异黄烷衍生物在制备预防、缓解或/和治疗瘙痒症药物或保健品中的应用。
11.其中,所述甘草异黄烷衍生物为甘草异黄烷甲、甘草西定或以3-苯基色原烷为核
心的衍生物中的一种或多种,或其立体异构体及其在药学上可接受的盐和/或溶剂化物,优选为甘草异黄烷甲、甘草西定。
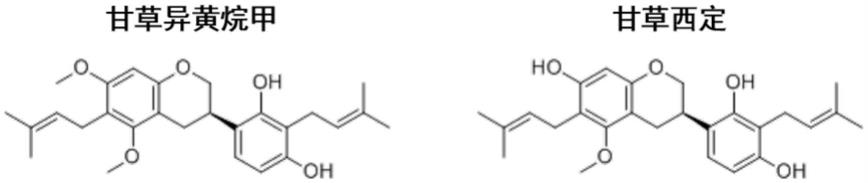
12.其中,甘草异黄烷甲和甘草西定的结构如下:
[0013][0014]
利用电生理膜片钳记录技术,在过表达trpv3通道的hek293t细胞系中,测试中药来源的天然产物化合物,筛选得到甘草异黄烷甲和甘草西定具有剂量依赖性地拮抗trpv3的能力。
[0015]
其中,所述药物由甘草异黄烷衍生物和药学上可接受的载体组成。
[0016]
特别是,所述的甘草异黄烷衍生物的纯度≥1%,优选为95%以上或95-100%纯物质。
[0017]
尤其是,药学上可接受的载体通常被保健专家认可用于这一目的且作为药剂的非活性成分。有关药学上可接受的载体的汇编可以在《药物赋形剂手册》(handbook of pharmaceutical excipients,第2版,由a.wade和p.j.weller编辑;american pharmaceutical association出版,washington and the pharmaceutical press,london,1994)等工具书中找到。
[0018]
其中,所述瘙痒症为组胺依赖性或/和非组胺依赖性瘙痒症,优选为非组胺依赖性瘙痒症。
[0019]
特别是,所述瘙痒症为急性瘙痒或/和慢性瘙痒。
[0020]
其中,所述药物以片剂、胶囊剂、丸剂、散剂、颗粒剂、糖浆剂、乳剂、注射剂、喷雾剂、凝胶剂、霜剂、巴布剂、橡胶贴膏剂形式存在。
[0021]
特别是,所述药物以片剂、胶囊剂、丸剂、散剂、颗粒剂、糖浆剂形式存在。
[0022]
本发明另一方面提供一种含有甘草异黄烷衍生物的用于预防、缓解或/和治疗瘙痒症的药物或保健品。
[0023]
其中,所述甘草异黄烷衍生物为甘草异黄烷甲、甘草西定或以3-苯基色原烷为核心的衍生物中的一种或多种,或其立体异构体及其在药学上可接受的盐和/或溶剂化物,优选为甘草异黄烷甲、甘草西定。
[0024]
特别是,所述甘草异黄烷衍生物的纯度≥1%,优选为95%以上或95-100%纯物质。
[0025]
尤其是,所述甘草异黄烷衍生物的重量与所述药物或保健品的总重量之比为(0.01-10):100,优选为(0.1-1):100。
[0026]
所述药物可以采用本领域公知的方法制成各种剂型,如片剂、胶囊剂、丸剂、散剂、颗粒剂、糖浆剂、溶液剂、注射剂、喷雾剂、气雾剂、凝胶型、霜剂、酊剂、巴布剂、橡胶贴膏剂或贴膏剂等。
[0027]
本发明还提供一种预防、缓解或/和治疗瘙痒症的方法,包括向瘙痒症给予治疗有效量的甘草异黄烷衍生物(甘草异黄烷甲、甘草西定),其治疗有效量为0.3~100mg/kg.d,
优选为1~20mg/kg.d,进一步优选为10mg/kg.d。
[0028]
除非另外说明,本发明中所用的术语“治疗有效量”为需要产生有效作用的药物的用量;“治疗有效量”是可以调整和变化的,最终由医务人员确定,其所考虑的因素包括给药途径和制剂的性质、接受者的体重、年龄等一般情况以及所治疗疾病的性质和严重程度。
[0029]
与现有技术相比,本发明具有如下的明显优点:
[0030]
1、本发明对已知化合物甘草异黄烷衍生物(甘草异黄烷甲、甘草西定)发掘了新的药用价值,将其用于预防、缓解、治疗瘙痒症,并可制备成预防、调理和/或治疗瘙痒症的药物或保健品,从而为中药材甘草、甘草中的天然产物化合物的应用开拓了一个新的领域。
[0031]
2、本发明的甘草异黄烷衍生物(甘草异黄烷甲、甘草西定)药理作用清楚,用于预防、缓解和治疗瘙痒症的功效显著,见效快、毒副作用小、安全性好,具有良好的药用前景。
[0032]
3、本发明的产品原料来源丰富、价廉、临床使用安全,制备工艺简单,可制成各种剂型,且服量小,使用方便,因此易于推广。
[0033]
4、本发明的甘草异黄烷衍生物(甘草异黄烷甲、甘草西定)是一类新的trpv3拮抗分子,可作为先导化合物,进一步用于trpv3相关疾病治疗药物的研发。
[0034]
本发明采用多肽sligrl诱导建立的非组胺依赖性急性瘙痒小鼠模型,通过统计30min内搔抓次数作为行为学检测指标,测试了甘草异黄烷甲和甘草西定抑制急性瘙痒的能力,结果表明它们均可以剂量依赖性地抑制sligrl诱发的急性瘙痒。
[0035]
采用钙泊三醇诱导建立的特应性皮炎慢性瘙痒小鼠模型,通过统计不同造模天数时每小时的搔抓次数作为检查指标,测试了甘草异黄烷甲和甘草西定抑制慢性瘙痒的能力,结果表明它们均可以在某种程度上抑制特应性皮炎模型小鼠的慢性瘙痒。
[0036]
本发明基于靶点分子trpv3筛选获得了一类新的拮抗分子,该类拮抗分子展示了抑制非组胺依赖性急性瘙痒和慢性瘙痒的活性,并可作为先导化合物,进一步用于瘙痒治疗药物的研发。
附图说明
[0037]
图1为不同浓度的甘草异黄烷甲对2-apb诱发的trpv3电流的拮抗效果图,其中a为在全细胞模式下记录trpv3电流变化的代表性曲线,包括单独给予100μm 2-apb刺激时,以及同时叠加多种浓度(30、100和300μm)的甘草异黄烷甲时的变化情况;b为甘草异黄烷甲拮抗trpv3通道的剂量效应关系图,由s型剂量效应曲线拟合计算得出,甘草异黄烷甲的ic
50
值为20.87μm(logic
50
=1.320
±
0.128,n=4-5),各浓度对应的数据均以平均值
±
sem表示;
[0038]
图2为不同浓度的甘草西定对2-apb诱发的trpv3电流的拮抗效果图,其中a为在全细胞模式下记录trpv3电流变化的代表性曲线,包括单独给予100μm 2-apb刺激时,以及同时叠加多种浓度(10、30和100μm)的甘草西定时的变化情况;b为甘草西定拮抗trpv3通道的剂量效应关系图,由s型剂量效应曲线拟合计算得出,甘草异黄烷甲的ic
50
值为15.24μm(logic
50
=1.183
±
0.120,n=5-8),各浓度对应的数据均以平均值
±
sem表示;
[0039]
图3为在膜内面向外模式下所记录的trpv3电流变化的代表性曲线,包括单独给予100μm 2-apb刺激时,以及同时叠加不同浓度的甘草异黄烷甲、甘草西定时的电流变化情况图,其中a为甘草异黄烷甲;b为甘草西定;最终10μm钌红可将trpv3电流完全阻断。
[0040]
图4为甘草异黄烷甲、甘草西定分别对于trpv1和trpa1通道的作用影响图;其中:
a、b为在全细胞模式下所记录的trpv1电流变化的代表性曲线,包括单独给予trpv1激动剂辣椒素时,以及同时叠加100μm的甘草异黄烷甲(a)或甘草西定(b)时的电流变化情况,最终非选择性trp通道拮抗剂钌红可将电流完全阻断;c、d为在全细胞模式下所记录的trpa1电流变化的代表性曲线,包括单独给予trpa1激动剂aitc时,以及同时叠加100μm的甘草异黄烷甲(c)或甘草西定(d)时的变化情况,最终非选择性trp通道拮抗剂钌红可将电流完全阻断;e、f:甘草异黄烷甲(e)和甘草西定(f)对trpv3、trpv1和trpa1的阻断能力比较图。采用未配对student's t检验,***p《0.001。以上各组数据均以平均值
±
sem表示,n=4-8。
[0041]
图5为甘草异黄烷甲对于sligrl所诱发急性瘙痒的抑制作用;其中a-c:分别为30、100及300μm甘草异黄烷甲作用的实验组与相应的不进行药物治疗的对照组小鼠按5min一个时间段统计搔抓次数的折线图,采用重复测量的方差分析,p》0.05(a-b),**p《0.01(c);d为30、100及300μm甘草异黄烷甲作用的实验组与相应的对照组小鼠30min内总搔抓次数的柱状图。采用配对的student's t检验,*p《0.05,**p《0.01,n.s.:p》0.05,以上各组数据均以平均值
±
sem表示,n=8;
[0042]
图6为甘草西定对于sligrl所诱发急性瘙痒的抑制作用;a-c:30、100及300μm甘草西定作用的实验组与相应的对照组小鼠按5min一个时间段统计搔抓次数的折线图,采用重复测量的方差分析,p》0.05(a-b),*p《0.05(c);d:30、100及300μm甘草西定作用的实验组与相应的对照组小鼠30min内总搔抓次数的柱状图。采用配对的student's t检验,**p《0.01,n.s.:p》0.05,以上各组数据均以平均值
±
sem表示,n=8;
[0043]
图7为不同浓度的甘草异黄烷甲和甘草西定对于sligrl所诱发急性瘙痒的抑制百分比,以及trpv3 ko小鼠的sligrl急性瘙痒相对于野生型的百分比对照图;柱状图分别为叠加30、100及300μm甘草异黄烷甲和甘草西定作用的实验组与相应的对照组小鼠30min内总搔抓次数的比值,以及trpv3 ko小鼠与野生小鼠30min内总搔抓次数的比值,以上各组数据均以平均值
±
sem表示,n=5-8。
[0044]
图8为用钙泊三醇诱导ad模型小鼠以及用trpv3拮抗剂进行治疗的操作流程示意图,时间线上方虚线箭头标示了用钙泊三醇给小鼠双耳造模的天数,下方黑色箭头标示了给小鼠双耳抹1
‰
的甘草异黄烷甲或甘草西定的天数,第0、4、7天时,在造模和给药前进行录像;
[0045]
图9为钙泊三醇诱导的ad模型小鼠在不同测试时间点的慢性瘙痒反应;其中:
[0046]
a,c,e:分别为第0、4、7天叠加1
‰
甘草异黄烷甲和甘草西定作用的实验组与作为对照的模型组小鼠按5min一个时间段统计搔抓次数的折线图;采用重复测量的方差分析,*p《0.05;
[0047]
b,d,f:分别为第0、4、7天叠加1
‰
甘草异黄烷甲和甘草西定作用的实验组与作为对照的模型组小鼠60min内总搔抓次数的柱状图;采用未配对的student's t检验与对照组进行比较,*p《0.05,n.s.:p》0.05。以上各组数据均以平均值
±
sem表示,n=7-8;
[0048]
图10为第0、4、7天叠加1
‰
甘草异黄烷甲和甘草西定作用的实验组与不进行药物治疗的模型组小鼠耳朵平均厚度的柱状图;采用未配对的student's t检验与对照组进行比较,**p《0.01,***p《0.001。以上各组数据均以平均值
±
sem表示,n=7-8;
[0049]
图11为不同处理后的hek293t细胞在荧光显微镜下观察的结果;每一行分别对应于左侧标注的条件下,于白光(明场)、绿色荧光(gfp)和红色荧光(pi染色)通道下拍摄典型
视野所得的图像。瞬时转染trpv3 g573s突变质粒后hek293t细胞出现gfp绿色荧光和很强的红色荧光信号(pi染色),具有正常形态的细胞数也变少了;若转染的同时添加20μm钌红,细胞的绿色荧光信号更强,但红色荧光信号却变得很微弱;而同时添加不同浓度(10和20μm)的甘草异黄烷甲和甘草西定,则红色荧光信号均较微弱,标尺为100μm;
[0050]
图12为同等条件下对hek293t细胞瞬时转染trpv3 g573s突变通道,并分别测试添加不同浓度(10和20μm)的甘草异黄烷甲、甘草西定和钌红,以及不添加任何拮抗剂条件下的细胞活力所得化学发光强度;采用未配对的student's t检验与不添加任何拮抗剂的对照组进行比较,**p《0.01,***p《0.001。以上各组数据均以平均值
±
sem表示,n=5。
具体实施方式
[0051]
下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随着描述而更为清楚。但这些实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
[0052]
以下通过试验例来进一步阐述本发明所述药物的有益效果,这些试验例包括了本发明药物的药效学试验。
[0053]
本发明所述甘草异黄烷甲为白色粉末,云南西力公司生产,经高效液相色谱两种检测器紫外检测器和蒸发光散射检测器面积归一化法测定,其纯度为97%。批号:bbp03331;
[0054]
甘草西定:白色粉末,云南西力公司生产,经高效液相色谱两种检测器紫外检测器和蒸发光散射检测器面积归一化法测定,其纯度为98%。批号:bbp03353。
[0055]
在本发明所述甘草异黄烷类分子的制备方法没有特别的限定,本领域技术人员可以根据本领域内的公知常识制备本发明所述的甘草异黄烷类分子,或者通过市售获得本发明所述的甘草异黄烷类分子(甘草异黄烷甲和甘草西定)。
[0056]
试验例1甘草异黄烷类化合物对trpv3的作用
[0057]
采用细胞膜片钳的方法评估化合物对过表达的人trpv3的作用。
[0058]
从美国atcc生物资源中心购得hek293t细胞系,将其复苏后接种在dmem完全培养基中,于饱和湿度且含5%co2的37℃恒温培养箱中进行培养。
[0059]
转染前,将hek293t细胞接种至6孔板中,在细胞密度达到50-70%时,使用lipofectamine 3000转染试剂,转染包含人源trpv3 cdna的真核表达质粒pcmv6-ac-gfp-trpv3(美国origene公司,货号rg211184)。
[0060]
电生理检测方法采用全细胞或膜内面向外(inside-out)记录模式,应用heka epc10型放大器及patchmaster记录软件,使用p-97型微电极拉制仪拉制的阻抗为3-5mω的电极,以
±
80mv方波电压记录电流(细胞钳制电位为0mv)。
[0061]
取转染trpv3质粒16-24h后的hek293t细胞,置于专门配制的浴液(130mm nacl,3mm hepes,0.3mm egta,ph=7.4)中,挑选状态较好、表面干净且有较强绿色荧光信号的细胞,然后将加入了内液(其组分同浴液)的电极缓慢移动至稍接触细胞膜表面,略稍施加负压,直至形成高阻封接后破膜,形成全细胞记录模式,或在形成高阻封接后直接将电极向上提,使电极尖端的膜片被撕下,形成膜内面向外式。
[0062]
1)在全细胞记录模式下,使用rsc-200快速交换给药系统重力灌流,先给予100μm2-apb激活trpv3通道,而后分别叠加不同浓度(300μm、100μm、30μm)的甘草异黄烷甲;或不同浓度(100μm、30μm、10μm)甘草西定,均可以观察到电流幅度明显减小。其中随着所叠加的甘草异黄烷甲浓度的增加,电流减小幅度不断扩大,直至最终几乎完全消失(如图1a);对于甘草西定的测试结果也是类似的,即在全细胞模式下,叠加甘草西定可降低2-apb诱发的电流,且电流减小的幅度呈现剂量依赖性(如图2a)。
[0063]
通过在多个浓度下测得甘草异黄烷甲、甘草西定对于trpv3电流的对应拮抗能力,并利用s型剂量效应曲线进行拟合,可得:甘草异黄烷甲的ic
50
值为20.87μm(如图1b),甘草西定的ic
50
值为15.24μm(如图2b)。
[0064]
2)在膜内面向外的记录模式下,即只记录单膜片上通道的电流,也同样观察到甘草异黄烷甲和甘草西定能够剂量依赖性地降低2-apb诱发的电流(如图3),说明它们抑制2-apb电流的能力并不依赖于胞内分子的辅助,而应该是直接作用于trpv3通道本身。
[0065]
试验例2甘草异黄烷类化合物对trpv1或trpa1的作用
[0066]
采用细胞膜片钳的方法评估化合物对过表达的人trpv1和trpa1的作用。
[0067]
从美国atcc生物资源中心购得hek293t细胞系,将其复苏后接种在dmem完全培养基中,于饱和湿度且含5%co2的37℃恒温培养箱中进行培养。
[0068]
转染前,将hek293t细胞接种至6孔板中,在细胞密度达到50-70%时,使用lipofectamine 3000转染试剂,转染包含人源trpv1 cdna的真核表达质粒pcmv6-ac-gfp-trpv1(美国origene公司,货号rg217653)或者转染包含人源trpa1cdna的真核表达质粒pcmv6-ac-gfp-trpa1(美国origene公司,货号rg219290)。
[0069]
电生理检测方法采用全细胞或膜内面向外记录模式,应用heka epc10型放大器及patchmaster记录软件,使用p-97型微电极拉制仪拉制的阻抗为3-5mω的电极,以
±
80mv方波电压记录电流(细胞钳制电位为0mv)。
[0070]
取转染trpv1或trpa1质粒16-24h后的hek293t细胞,置于专门配制的浴液(130mm nacl,3mm hepes,0.3mm egta,ph=7.4)中,挑选状态较好、表面干净且有较强绿色荧光信号的细胞,然后将加入了内液(其组分同浴液)的电极缓慢移动至稍接触细胞膜表面,略稍施加负压,直至形成高阻封接后破膜,形成全细胞记录模式。
[0071]
利用电生理的检测方法,通过在体外过表达trpv1或trpa1的hek293t细胞中记录100μm甘草异黄烷甲对trpv1激动剂辣椒素或trpa1激动剂aitc所诱发电流的作用,结果甘草异黄烷甲对于trpv1有较弱的阻断作用(阻断率为31.9%
±
6.6%,图4a),而对trpa1则几乎没有观察到拮抗作用(3.3%
±
15.5%,图4c),均显著低于其拮抗trpv3的效果(88.0%
±
7.5%,图4e),这些结果提示甘草异黄烷甲对trpv3通道有较好的作用特异性。利用类似的电生理测试方法也检测了100μm甘草西定对trpv1和trpa1电流的作用,甘草西定对于trpv1和trpa1的阻断程度(trpv1:52.2%
±
10.1%,图4b;trpa1:8.4%
±
10.8%,图4d)同样显著低于其拮抗trpv3的程度(93.3%
±
5.8%,图4f),说明甘草西定对trpv3通道也有一定的作用特异性。
[0072]
对于瘙痒的动物模型,标准的急性瘙痒模型采用在小鼠颈背部皮内注射致痒剂以产生瘙痒反应,并通过统计注射后一定时间内的搔抓次数来表征其瘙痒的程度,其中从小鼠后足抬起搔抓注射部位直至后足再次落地或放入嘴中舔舐记为一次搔抓行为。
[0073]
常见的致痒剂包括组胺、氯喹、5-羟色胺、化合物48/80以及多肽sligrl等。由于最新发表的研究表明,对于皮内注射par2的激活剂sligrl所诱发的急性瘙痒,敲除trpv3后小鼠的搔抓反应是显著降低的。因此,sligrl急性痒模型被选作评估trpv3拮抗分子在生理条件下抑制急性瘙痒作用效果的范例。
[0074]
试验例3甘草异黄烷甲对小鼠急性痒模型的作用
[0075]
将购买的8-10周龄(体重20-25g,雌雄各半)野生型c57bl/6j小鼠(斯贝福(北京)实验动物科技有限公司),选取其中的24只随机分成3组,即分成甘草异黄烷甲高剂量组(300μm)、中剂量组(100μm)、低剂量组(30μm),其中每组8只,至少提前2-3天剔除小鼠颈背部的毛发;
[0076]
正式实验当天,将小鼠分别放入(15cm
×
10cm
×
10cm)观察盒内进行适应性活动约5min;接着先在右耳后皮内预注射50μl含不同浓度(30μm、100μm、300μm)甘草异黄烷甲的生理盐水,30min后继续于同一位置注射50μl含50μg sligrl并叠加对应浓度甘草异黄烷甲的生理盐水(即生理盐水中既包括sligrl,同时也包含甘草异黄烷甲,其中甘草异黄烷甲的浓度分别与预注射时的浓度相对应,即sligrl+甘草异黄烷甲)以诱发急性瘙痒;立即将注射完毕的小鼠放入观察盒,保持安静的条件,用摄像头录像30min并事后回看录像,以5min为一个时间段进行搔抓行为的计数。
[0077]
隔天在左耳后皮内预注射50μl含0.1%dmso(溶剂)的生理盐水,作为对照组(不给药),30min后继续于同一位置注射50μl含50μg sligrl(同样含0.1%dmso)的生理盐水以诱发急性瘙痒;立即将注射完毕的小鼠放入观察盒,保持安静的条件,用摄像头录像30min并事后回看录像,以5min为一个时间段进行搔抓行为的计数。
[0078]
结果发现,叠加使用30、100或300μm甘草异黄烷甲的条件下,小鼠注射sligrl后30min内总搔抓次数相比于不给药的对照组(即在左耳一侧仅注射sligrl,即sligrl+dmso组)均有不同程度的下降(图5d)。
[0079]
不过30μm实验组和对照组的差异未达显著水平(p=0.1047),而随着作用浓度增加到100和300μm,实验组小鼠30min内总搔抓次数降低的水平就越来越显著了,这提示甘草异黄烷甲抑制sligrl诱发的急性瘙痒的能力随浓度的升高而增强。值得一提的是,分时段统计搔抓次数的折线图显示(如图5a-c):不同浓度的甘草异黄烷甲均使得实验组小鼠的搔抓次数随时间衰减更快,而当叠加的甘草异黄烷甲浓度足够高(300μm)时,实验组小鼠的搔抓次数从一开始便远低于不给药的对照组,且采用重复测量的方差分析所计算的p值也小于0.01,这从另一个侧面显示甘草异黄烷甲对于sligrl急性瘙痒确具有抑制作用。
[0080]
试验例4甘草西定对小鼠急性痒模型的作用
[0081]
将购买的8-10周龄(体重20-25g,雌雄各半)野生型c57bl/6j小鼠(斯贝福(北京)实验动物科技有限公司),选取其中的24只随机分成3组,即分成甘草西定高剂量组(300μm)、中剂量组(100μm)、低剂量组(30μm),其中每组8只,至少提前2-3天剔除小鼠颈背部的毛发;
[0082]
除了正式实验当天先在右耳后皮内预注射50μl含不同浓度(30μm、100μm、300μm)甘草西定的生理盐水,30min后继续于同一位置注射50μl含50μg sligrl并叠加对应浓度甘草西定的生理盐水(即生理盐水中既包括sligrl,同时也包含甘草西定,其中甘草西定的浓度分别与预注射时的浓度相对应,即sligrl+甘草西定)以诱发急性瘙痒之外,其余与试验
例3相同。
[0083]
结果发现,对于叠加使用30、100或300μm甘草西定的实验组小鼠,同样观察到30min内总搔抓次数相比于不给药的对照组(即在左耳一侧仅注射sligrl,即sligrl+dmso组)有不同程度的下降(图6d)。其中30μm实验组和对照组的差异未达显著水平(p=0.0523),但当作用浓度增加到100和300μm后,实验组小鼠30min内总搔抓次数便都显著低于对照组了,这意味着甘草西定具有与甘草异黄烷甲一样的效果,也可以有效抑制sligrl诱发的急性瘙痒反应。分时段统计的搔抓次数也得到了与甘草异黄烷甲类似的结果(如图6a-c):各实验组小鼠的搔抓次数都倾向于随时间更快衰减,而当叠加的甘草西定浓度增加到300μm后,两组之间的差异达到显著水平(p《0.05)。上述结果都证明了甘草西定同样能有效抑制sligrl诱发的急性瘙痒。
[0084]
通过计算不同实验组小鼠与各自对应的对照组小鼠在注射sligrl后30min内总的搔抓次数的比值,可观察到随着作用浓度的升高,甘草异黄烷甲和甘草西定的抑制效果均越来越强,呈现出相似的剂量依赖性(图7)。
[0085]
考虑到已有研究报道trpv3 ko小鼠(trpv3敲除小鼠)对于sligrl诱发的急性瘙痒显著低于野生型,作为另一方面的对照,也尝试在trpv3 ko小鼠(购自jackson实验室(jackson lab),美国)上注射了同样剂量的sligrl诱发急性瘙痒,结果其搔抓反应相对野生型小鼠的下降幅度与采用高浓度甘草异黄烷甲和甘草西定时的下降幅度相当。因此:甘草异黄烷甲和甘草西定在高浓度时已完全拮抗trpv3,从而在抑制sligrl急性瘙痒方面达到了与直接敲除trpv3几乎完全相同的效果。
[0086]
慢性瘙痒作为许多皮肤性和系统性疾病的重要并发症,在临床上已有的治疗手段颇为缺乏,甚至由于搔抓行为往往会加重皮肤损伤和炎症,从而陷入越痒越抓、越抓越痒的恶性循环,严重影响患者的正常生活和疾病康复进程。目前常见伴有慢性瘙痒的皮肤病包括:慢性湿疹、特应性皮炎(ad)、银屑病、干皮症和老年瘙痒症等。已有研究显示trpv3功能增强突变会导致小鼠出现与ad非常类似的皮炎症状;而最新发表的研究则证明,trpv3通过与par2受体蛋白相互作用在角质形成细胞中调控tslp等炎症因子的分泌,进而参与介导钙泊三醇诱导的ad模型小鼠的慢性瘙痒等症状。因此,选择钙泊三醇诱导的特应性皮炎模型作为对trpv3拮抗分子在生理条件下抑制慢性瘙痒能力进行评估的范例。
[0087]
试验例5甘草异黄烷类化合物对小鼠慢性痒模型的作用
[0088]
将购买的8-10周龄(体重20-25g,雌雄各半)野生型c57bl/6j小鼠(斯贝福(北京)实验动物科技有限公司),选取其中的22只随机分成3组,即分成甘草异黄烷甲组、甘草西定组和模型组,其中甘草异黄烷甲组、模型对照组各7只,甘草西定组8只;
[0089]
将钙泊三醇溶解于无水乙醇中,以100μm为工作浓度,使用20μl移液枪吸取钙泊三醇溶液滴在小鼠的两侧耳廓,每只耳朵20μl,每天1次,连续诱导7天进行特应性皮炎(ad)造模。
[0090]
为测试化合物通过拮抗trpv3而抑制慢性瘙痒的效果,在采用钙泊三醇诱导ad模型的同时,叠加(以凡士林作基质)质量分数为1
‰
的甘草异黄烷甲或甘草西定膏药进行治疗(即甘草异黄烷甲组、甘草西定组),而造模和给药处理的具体操作日程安排如图8所示:正式造模前5天开始,甘草异黄烷甲组、甘草西定组每天将1
‰
的甘草异黄烷甲或甘草西定膏药抹于小鼠双耳耳廓(约15mg每只耳朵)一次;模型组则每天将1
‰
的dmso膏药抹于小鼠
双耳耳廓(约15mg每只耳朵)一次;ad造模时,甘草异黄烷甲组、甘草西定组每天钙泊三醇给药半小时后继续抹药,模型组则在每天钙泊三醇给药半小时后涂膜凡士林基质,直到造模7天结束;其中第0、4、7天进行录像和测试双耳耳廓厚度。
[0091]
录像时将小鼠分别放入(15cm
×
10cm
×
10cm)观察盒内,进行适应性活动5min后,用摄像头录像60min,注意保持周围环境安静,事后回看录像,以5min为一个时间段进行搔抓行为的计数。
[0092]
结果在正式用钙泊三醇进行ad造模前(第0天),实验组(甘草异黄烷甲组、甘草西定组)与模型组60min内的总搔抓次数均非常低,且没有显著差异(图9a-b);造模4天后,小鼠出现明显的慢性瘙痒症状,此时1
‰
甘草异黄烷甲和甘草西定处理的实验组在60min内的总搔抓次数大约只有模型组的一半,且差异均具有显著性(图9c-d);而造模7天后,小鼠的慢性瘙痒症状已经非常严重,此时各实验组在60min内的总搔抓次数仍都低于模型组,不过仅1
‰
甘草西定处理的实验组降低的程度达到显著水平(图9e-f)。另外随着ad造模进程出现的,除了慢性瘙痒反应,还有小鼠耳朵炎症的不断加重,集中体现为耳廓厚度的不断增加,如图10所示,在第4、7天,1
‰
甘草异黄烷甲和甘草西定实验组小鼠耳朵的平均厚度均相比于模型组显著下降,提示甘草异黄烷甲和甘草西定同时具有一定的抗炎作用。值得注意的是,甘草异黄烷甲实验组小鼠耳朵的平均厚度相比于模型组差异的显著性随时间有降低的趋势,暗示了其抗炎作用可能较为有限而无法一直确保好的效果,与之相比,甘草西定的抗炎效果要更强一些。
[0093]
试验例6甘草异黄烷类化合物对trpv3功能增强突变体的作用
[0094]
本发明的甘草异黄烷类化合物不仅对于trpv3野生型有作用,而且对于trpv3的功能增强突变体也有阻断作用,从而拓展了其作用范围。
[0095]
1、定性试验
[0096]
在之前的研究中已经报道,trpv3的功能增强突变体(如g573s)可以诱发细胞死亡。为此,利用诺唯赞mut express ii fast mutagenesis kit试剂盒,依引物设计原则设计所需的定点突变引物如下:
[0097]
上游序列:5
’‑
gtccatgagcatgtacagcgtcatgatccagaagg-3’[0098]
下游序列:5
’‑
ctgtacatgctcatggactggaaaccccgcgta-3’[0099]
按照点突变试剂盒的推荐操作步骤对质粒pcmv6-ac-gfp-trpv3进行点突变,得到具有g573s突变的质粒。
[0100]
使用赛默飞lipofectamine 3000转染试剂盒,按照试剂盒推荐的操作方法进行转染处理。于hek293t细胞系中瞬时转染带gfp标签的trpv3 g573s突变通道质粒,在转染过程中,在添加转染液时,分别同时添加拮抗剂钌红(20μm)、甘草异黄烷甲(10μm或20μm)、甘草西定(10μm或20μm);在转染12h后弃掉细胞培养液,用pbs洗一次后用hoechst33342/pi细胞凋亡染色试剂盒进行染色,染色后在荧光显微镜下确实可观察到许多pi染色为阳性的细胞(图11),说明细胞大量死亡。
[0101]
由图11可知:在转染g573s突变质粒的同时添加了拮抗剂钌红(20μm)之后,pi染色为阳性的细胞数就变得非常少了(如图11),说明过表达的trpv3 g573s突变通道一旦为拮抗剂所阻断,就难以再诱导细胞死亡了;
[0102]
对转染时同时添加了10或20μm的甘草异黄烷甲和甘草西定的过表达g573s突变通
道的hek293t细胞进行pi染色,在荧光显微镜下也只能观察到较少的细胞带有红色荧光信号(如图11),说明过表达的trpv3 g573s突变通道为甘草异黄烷甲、甘草西定所阻断。
[0103]
2、定量试验
[0104]
为定量测试甘草异黄烷甲、甘草西定对于trpv3 g573s突变通道的作用,在hek293t细胞系中瞬时转染带gfp标签的trpv3 g573s突变通道质粒,并于转染过程中,分别添加拮抗剂钌红(10μm或20μm)、甘草异黄烷甲(10μm或20μm)、甘草西定(10μm或20μm),接着将混合了上述化合物及转染液的细胞悬液种至96孔板中进行培养。至少培养12h后,使用celltiter-glo luminescent cell viability assay试剂盒,以荧光素酶检测atp表征细胞活力的方法进行测试。
[0105]
测试时,每孔加入混合好的celltiter-glo测试溶液100μl,于摇床上混匀2min以裂解细胞;继续在室温至少放置10min以确保反应完全;之后使用多功能酶标仪,采用化学发光模式读数。
[0106]
结果发现与钌红的作用类似,在转染g573s突变质粒的同时添加10或20μm的这两种分子,都能显著提升表征细胞活力的化学发光强度(如图12)。上述定性和定量检测的结果一起,均说明甘草异黄烷甲和甘草西定对trpv3功能增强突变体亦有很强的阻断作用。
[0107]
实施例1甘草异黄烷甲软膏剂
[0108]
先将白凡士林240g,十八醇160g,单硬脂酸甘油酯40g,80℃水浴加热熔融,制成油相;
[0109]
十二烷基硫酸钠20g,甘油140g,4%羟苯乙酯4g,80℃加热溶于500ml蒸馏水中,制成水相;
[0110]
慢慢将水相加入油相中,边加边搅拌,冷凝成乳状基质,加入甘草异黄烷甲100g,灌装、灭菌,分装,制成软膏剂1000支,每支含甘草异黄烷甲100mg。
[0111]
加入的甘草异黄烷甲的量可以是1-200g,制成的软膏剂中每只含甘草异黄烷甲1-200mg。
[0112]
还可以用甘草西定替换甘草异黄烷甲,制成甘草西定软膏剂。
[0113]
实施例2甘草异黄烷甲软膏剂
[0114]
先将白凡士林300g(通常为10-500g),石蜡500(通常为50-1000g)g,液体石蜡2000g(通常为500-8000g),单硬脂酸甘油酯1000g(通常为100-2000g),司盘80 50g(通常为5-100g),80℃水浴加热熔融,制成油相;
[0115]
乳化剂op 50g(通常为5-100g),4%羟苯乙酯10g(通常为1-20g),80℃加热溶于1000ml(通常为100-2000ml)蒸馏水中,制成水相;
[0116]
慢慢将油相加入水相中,边加边搅拌,冷凝成乳状基质,加入甘草异黄烷甲100g,灌装、灭菌,封装,制成软膏剂1000支,每支含化合物甘草异黄烷甲1-200mg。
[0117]
加入的甘草异黄烷甲的量可以是1-200g,制成的软膏剂中每只含甘草异黄烷甲1-200mg。
[0118]
还可以用甘草西定替换甘草异黄烷甲,制成甘草西定软膏剂。
[0119]
实施例3甘草异黄烷甲软膏剂(油脂性基质软膏剂的制备)
[0120]
甘草异黄烷甲100g,加入3000g(通常为50-5000g)液体石蜡中搅拌成糊状,加入凡士林5000g(通常为100-8000g),研磨至均匀。灌装、灭菌,制成软膏剂1000支,每支含化合物
甘草异黄烷甲100mg。
[0121]
加入的甘草异黄烷甲的量可以是1-200g,制成的软膏剂中每只含甘草异黄烷甲1-200mg。
[0122]
还可以用甘草西定替换甘草异黄烷甲,制成甘草西定软膏剂。
[0123]
实施例4甘草异黄烷甲软膏剂(水性基质软膏剂的制备)
[0124]
cmc-na 200g(通常为30-300g)加入乙醇5000ml(通常为100-8000ml),研磨使湿润,再加甘油5000ml(通常为500-8000ml),继续研磨至均匀(无块状),继续加入苯甲酸钠水溶液200ml(通常为50-300ml)(含20g(通常为5-30g)苯甲酸钠)边加边研磨,混匀,溶胀得水溶性基质;加入甘草异黄烷甲100g,混匀,灌装,灭菌。制成软膏剂1000支,每支含化合物甘草异黄烷甲100mg。
[0125]
加入的甘草异黄烷甲的量可以是1-200g,制成的软膏剂中每只含甘草异黄烷甲1-200mg。
[0126]
还可以用甘草西定替换甘草异黄烷甲,制成甘草西定软膏剂。
[0127]
本发明上述实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1