一种多功能新型给药系统制剂的制备方法及应用
本发明涉及医药领域;尤其涉及一种多功能新型给药系统制剂的制备方法及应用。
背景技术:
肾缺血再灌注损伤(riri)是器官、组织部位缺血后再次血流而导致的缺血性受伤进一步加重的现象。肾脏作为高血流型器官,极容易发生缺血再灌注损伤。临床上因缺血再灌注损伤导致的急性肾功能衰竭十分常见,如器官移植、手术出血、严重烧伤等导致的肾部位血流量急剧减少,而此后恢复灌注可使肾功能损伤继续加重。riri的发病机制与以下因素有关,包括肾内皮细胞功能障碍、肾小管上皮细胞损伤和活性氧(ros)的增加。h2s具有促进血管舒张、抗增殖、预防炎症和白细胞粘附和抗氧化应激等作用,同时也具有促进血管重塑,促进肾小管细胞再生,减少肾脏部位的凋亡和自噬的作用。肾脏发生缺血再灌注损伤时,ros可引起氧化应激,通过激活caspase-3、nf-κb、凋亡信号激酶1、p53、蛋白激酶c等调节信号通路。目前,尚未有一种药物能全面的靶向治疗riri,仅为延缓疾病的进展。
技术实现要素:
本发明的目的是提供了一种多功能新型给药系统制剂的制备方法及应用。
本发明提供一种新型的基于cd44受体的ros敏感&h2s响应型新型给药系统,本发明通过合成透明质酸-烯丙基半胱氨酸-二茂铁甲酸(hfc),并包载雷帕霉素(rap),以期减少ros的浓度,增加h2s的产生,减少炎症因子的形成,降低对肾脏部位的损害。
本发明是通过以下技术方案实现的:
本发明涉及一种多功能新型给药系统制剂的制备方法;包括如下步骤:
步骤1,称取(cys)640mg,溶于1mldmso中;称取二茂铁甲酸(fe)230mg、nhs660mg和edc760mg,溶于1mldmso中进行活化;将cys溶液逐滴滴入到二茂铁甲酸溶液中,并反应12h;反应完成后,将反应生成的溶液通过h2o洗涤1次,然后加入0.2mol柠檬酸水溶液萃取,再依次通过h2o洗涤2次,饱和nacl溶液洗涤1次,最后加入无水na2so4,以除去其中的水分;50℃下烘箱烘干,得到纯化的fe-cys;
步骤2,称取fe-cys76.8mg、dmap33.3和edc76mg,溶于4ml甲酰胺中,置于磁力搅拌器中进行催化;称取ha41.7mg,溶于5ml甲酰胺中;将fe-cys反应溶液逐滴滴入到ha溶液中,并于40-50℃下磁力搅拌24h;待反应完成后,将反应溶液置于透析袋中,室温下透析;冻干,得到新型载体材料hfc;
对生成的hfc进行表征
通过ft-ir、1h-nmr对hfc的结构进行表征,以验证新型纳米胶束材料合成成功。
步骤3,称取30mghfc和6mgrap,溶于3mldmso中,通过自组装的方式将rap包埋于hfc中,得到hfc@rap。
优选地,步骤1中,所述活化的温度为30-40℃,活化的时间为1-2h。
优选地,步骤2中,所述催化的条件是:温度为30-40℃,时间为1-2h。
优选地,步骤2中,所述透析袋为mw=8000-14000的透析袋。
优选地,步骤2中,所述透析的时间为48h。
优选地,步骤3中,所述hfc和rap的质量比为10:2。
本发明的原理:本发明通过构建一种新型纳米胶束制剂hfc,使得其具有ros响应性、h2s缓慢释放特性以及巨噬细胞表面cd44受体的靶向性;通过引入ros敏感集团二茂铁甲酸,使得新型材料具有ros响应性,到达ros聚集区域,可快速断裂并释放rap;通过引入h2s供体烯丙基半胱氨酸,使得其在体内缓慢释放h2s,以促进肾小管细胞再生,减少肾脏部位的凋亡,并引起自噬;通过引入与cd44受体相结合的透明质酸(ha),使得新型制剂到达肾脏损伤部位时,可以锚定在肾脏部位聚集的巨噬细胞表面,最终达到以靶向治疗肾脏疾病的目的。
本发明具有以下优点:
(1)本发明通过化学键结合的方式合成了hfc新型载体,并通过1h-nmr、ft-ir对新型载体进行考察。
(2)本发明通过在不同浓度h2o2的体外释放实验,验证了本发明方法制备得到的hfc@rap的ros敏感效应;在低浓度的h2o2中,rap释放较慢,随着h2o2浓度的增加,药物能够快速的释放。
(3)本发明通过细胞毒性试验,验证了本发明方法制备得到的hfc@rap的安全性;通过对肾系膜细胞和巨噬细胞的毒性考察,验证了在不同浓度的hfc@rap在培养12h和24h后,细胞存活率均大于90%,药物对细胞的损伤极低,保障了用药的安全。
(4)本发明通过细胞摄取实验,验证了本发明方法制备得到的hfc@rap能顺利的进入肾系膜细胞和巨噬细胞,具有良好的生物相容性,并显示了新型给药系统的细胞摄取具有浓度依赖性和时间依赖性。
(5)本发明通过测定raw264.7细胞内h2o2及h2s,验证了本发明方法制备得到的hfc@rap能明显降低细胞内raw264.7细胞内h2o2的浓度,提高了h2s的浓度,达到了实验预期的目的。
附图说明
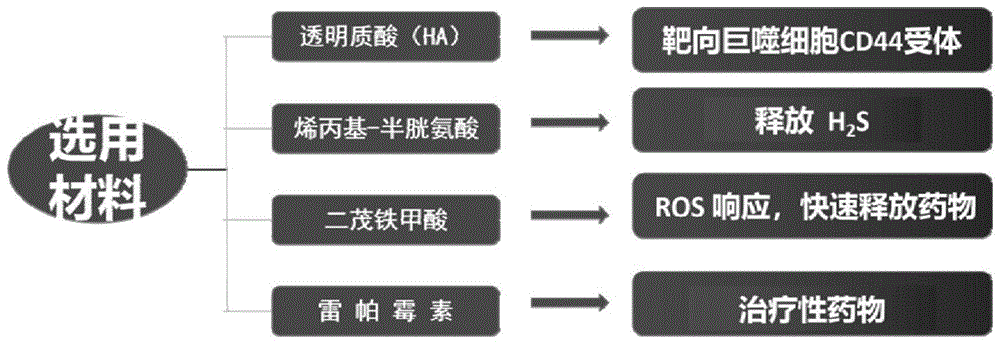
图1是本发明多功能新型给药系统制剂的制备方法所用原料及其作用图;
图2是本发明多功能新型给药系统制剂的制备方法的原理图;
图3是本发明多功能新型给药系统制剂的1h-nmr图;
图4是本发明多功能新型给药系统制剂的红外吸收光谱图;
图5是本发明多功能新型给药系统制剂的粒径、ζ电位、电镜图;
图6是在不同h2o2情况下的新型纳米制剂体外释放图;
图7是raw264.7不同时间细胞毒性图;
图8是肾系膜细胞不同时间细胞毒性图;
图9是raw264.7细胞的浓度依赖、时间依赖摄取图;
图10是肾系膜细胞的浓度依赖、时间依赖摄取图;
图11是raw264.7细胞内h2s浓度测定图
图12是raw264.7细胞内h2o2浓度测定图。
具体实施方式
下面结合具体实施例对本发明进行详细说明。应当指出的是,以下的实施实例只是对本发明的进一步说明,但本发明的保护范围并不限于以下实施例。
实施例
本实施例涉及一种多功能新型给药系统制剂的制备方法,见图1和图2所示:包括如下步骤:
步骤1,称取烯丙基半胱氨酸640mg,溶于1mldmso中。称取一定量的二茂铁甲酸230mg、nhs660mg和edc760mg,溶于1mlmso中,并在30-40℃下活化1-2h。将cys溶液逐滴滴入到二茂铁甲酸溶液中,并反应12h。反应完成后,将反应溶液通过h2o洗涤1次,然后加入0.2mol柠檬酸水溶液萃取,再依次通过h2o洗涤2次,饱和nacl溶液洗涤1次,最后加入无水na2so4,以除去其中的水分。50℃下烘箱烘干,得到纯化的fe-cys;
步骤2,称取适量的fe-cys76.8mg、dmap33.3和edc76mg,溶于4ml甲酰胺中,然后置于30-40℃磁力搅拌器中进行催化1-2h。称取ha41.7mg,溶于5ml甲酰胺中。将fe-cys反应溶液逐滴滴入到ha溶液中,并于40-50℃下磁力搅拌24h。反应完成后,将反应溶液置于mw=8000~14000的透析袋中,室温下透析48h。冻干后得到新型载体材料hfc。
对生成的hfc进行表征
通过ft-ir、1h-nmr对hfc的结构进行表征,以验证新型纳米胶束材料合成成功。图3显示,7.05ppm为二茂铁甲酸的c5h5质子吸收峰,6.85ppm的双峰为ch=ch2的质子吸收峰,2.99ppm为co-nh-ch2的质子吸收峰,2.66ppm为c-o-c的质子吸收峰;图4显示,3274.37cm-1为二茂铁中ch=ch-的伸缩振动吸收峰,1647.22cm-1为co-nh的伸缩振动吸收峰,1622.26cm-1为-ch2-ch=ch2的伸缩振动吸收峰,1314.28cm-1和1299.08cm-1为c-o-c的不对称伸缩振动吸收峰。红外图谱及核磁图谱共同证实了hfc的合成。
步骤3,hfc@rap的合成
称取30mghfc和6mgrap,溶于3mldmso中。通过自组装的方式将rap包埋于hfc中,得到hfc@rap。
对生成的hfc@rap进行表征
通过粒径仪对hfc@rap的粒径及ζ电位进行表征,见图5所示:通过电子透射电镜(tem)对纳米粒子的形态进行表征。
本实施例生成的hfc@rap进行体外释放实验
取一定量的hfc@rap,并置于mw=8000-12000的透析袋。将其置于20ml分别含有不同浓度h2o2(浓度分别为:0、0.05mm、5mm、5mm)的ph7.4pbs释放介质中,在37℃和120rpm的摇床中,进行体外药物释放,见图6所示。固定时间点用等量的新鲜介质置换各样品的释放介质,每次换取0.5ml。将得到的样品通过0.22μm的微孔滤膜过滤。然后计算累计释放量。
本实施例生成的hfc@rap的应用
细胞学研究
(1)细胞毒性研究。见图7和图8所示:将肾系膜细胞及raw264.7巨噬细胞接种于96孔板中,于37℃、5%co2以及饱和湿气下进行培养。并加入不同浓度的hfc@rap,在12h和24h后进行cck8实验,以验证hfc@rap对两种细胞的细胞毒性。
(2)细胞摄取研究。将肾系膜细胞及raw264.7巨噬细胞接种于96孔板中,并不同时间点考察两种细胞对不同浓度的hfc@rap摄取情况,见图9和图10所示:以验证是否具有浓度依赖性和时间依赖性。
(3)raw264.7细胞内h2o2及h2s浓度的测定,见图11和图12所示。将raw264.7巨噬细胞接种于6孔板,加入lps(1μg/ml)刺激后,按照h2o2及h2s检测试剂盒说明书进行检测及计算各组上清h2o2及h2s水平。
本发明通过构建一种新型纳米胶束制剂hfc,使得其具有ros响应性、h2s缓慢释放特性以及巨噬细胞表面cd44受体的靶向性;通过引入ros敏感集团二茂铁甲酸,使得新型材料具有ros响应性,到达ros聚集区域,可快速断裂并释放rap;通过引入h2s供体烯丙基半胱氨酸,使得其在体内缓慢释放h2s,以促进肾小管细胞再生,减少肾脏部位的凋亡,并引起自噬;通过引入与cd44受体相结合的透明质酸(ha),使得新型制剂到达肾脏损伤部位时,可以锚定在肾脏部位聚集的巨噬细胞表面,最终达到以靶向治疗肾脏疾病的目的。
以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变形或修改,这并不影响本发明的实质。
- 还没有人留言评论。精彩留言会获得点赞!