重组人sDR5-Fc融合蛋白在制备预防和/或治疗急性放射病的药物中的应用的制作方法
重组人sdr5-fc融合蛋白在制备预防和/或治疗急性放射病的药物中的应用
技术领域
1.本发明涉及辐射防护类蛋白药物及医药技术领域,具体涉及一种重组人sdr5-fc融合蛋白在制备预防和/或治疗急性放射病的药物中的应用。
背景技术:
2.急性放射病(acute radiation syndrome,ars)是机体在短时间内受到大剂量电离辐射后导致的全身性疾病。电离辐射是通过对生物体内结构分子的电离、激发和碰撞等直接作用或生成自由基和类自由基等活性分子间接作用,导致由辐射靶向的结构分子组成的生物体内物质结构损伤或者由于电离辐射而在生物体内产生的自由基会通过争夺附近细胞、血管、蛋白分子、脂肪化合物、dna分子中的电子,从而对正常组织造成损伤。这种电离辐射损伤通过分子-细胞-组织-系统不同层次进行传递,首先导致正常细胞功能紊乱和凋亡,进而引发正常组织、器官的损伤和功能紊乱,直到出现可见的临床效应。
3.研究表明,电离辐射诱导的细胞凋亡不同于化学药物(包括各类处方或非处方的化学药物、生物制剂、传统中药、天然药、保健品、膳食补充剂及其代谢产物和辅料等)和其他死亡刺激(例如自身免疫性炎性疾病)等诱导的细胞凋亡。电离辐射诱导的细胞凋亡与辐射剂量和细胞的辐射敏感性有关,并呈现不同细胞类型的异质性,其中主要涉及sapk/jnk(应激激活的蛋白激酶或c2jun氨基末端激酶)细胞凋亡信号通路、依赖于dna损伤的细胞凋亡信号通路、依赖于胞质电离损伤的细胞凋亡信号通路和依赖于质膜损伤的细胞凋亡信号通路。在这些电离辐射诱导的细胞凋亡信号通路中,线粒体可通过由bcl-2家族蛋白(例如具有抗细胞凋亡效应的bcl-2下调和促细胞凋亡的蛋白分子bax上调)诱导的线粒体膜通透性增加、释放cytc(细胞色素c)和激活半胱氨酸蛋白酶(caspases)或通过p53启动的细胞周期阻滞引起细胞凋亡而发挥中心调控作用,其中关键执行者是caspases。此外,电离辐射诱导的细胞凋亡还依赖于caspases的级联传递,caspases能够上调fas和/或fasl的表达,通过死亡受体途径介导正常细胞凋亡。因此,目前ars防治药物的研究主要围绕抗氧化、消除自由基、抗炎症、线粒体靶向制剂、促进造血、提高机体免疫力等方面开展,现有ars防治药物可分为含硫类、激素类、天然动植物类、细胞因子类、造血干细胞移植、线粒体靶向制剂等。
4.(1)含硫类
5.含硫类药物结构中含有自由巯基,代表性药物有氨磷汀(wr-2721)和n-乙酰半胱氨酸(nac)。这类化合物的还原特性使其具有良好的清除组织自由基、抗氧化等作用,是目前效果较好的一类电离辐射防护剂。然而,虽然这类药物对急性放射病的疗效确切,但这类合成药物的安全性是临床应用的主要隐患,例如wr-2721虽然具有很强的清除自由基和抗氧化活性,但其所需剂量较高,副作用较多,包括低血压、恶心呕吐、皮疹、发热或休克等;同时由于作用机制和药物特性,这类药物通常在受电离辐射前使用才有效。
6.(2)激素类
7.激素类药物主要是对骨髓有核细胞、造血干细胞和祖细胞都有明显的电离辐射防护作用,并能促进它们的恢复,代表性药物有“500”针剂、“523”片剂、雌三醇和褪黑素等。然而,激素类药物的主要问题是具有雌激素活性,应用后有一定副作用。
8.(3)天然动植物类
9.研究发现,多种药物组分及复方能通过其抗氧化、保护造血组织、改善微循环、促进细胞增殖等作用来发挥其电离辐射防护作用。如天然多糖类、酚类、生物碱类、黄酮类等活性成分对多种射线造成的氧化应激、骨髓抑制、免疫低下等都具有很好的防护作用。此外,某些天然药物复方对急性放射病也有一定治疗作用。
10.(4)细胞因子类
11.细胞因子的应用是多年来ars治疗中的常用手段,如重组人粒细胞集落刺激因子(rhgcsf)、il-12、重组人胰岛素样生长因子-i(rhigf-i)和重组人血小板生成素(rhtpo)等。临床上造血生长因子主要用于中度、重度和偏轻的极重度骨髓型病人治疗,此时病人的造血功能尚可自身恢复,对药物能有一定反应,如白细胞回升加快,最低至持续时间缩短等。
12.(5)造血干细胞移植
13.偏重的极重度骨髓型以上病人因病情严重而造血功能难以恢复或不能自身恢复,一般治疗难以奏效,此时需要实施造血干细胞移植,以重建造血功能。目前常用的有间充质干细胞(mscs)和人脐血干细胞等。
14.(6)线粒体靶向制剂
15.线粒体在电离辐射诱导的细胞凋亡信号通路中发挥中心调节作用,因此作用在于抑制细胞色素c从线粒体释放、抑制caspases的激活、下调p53蛋白表达等的线粒体靶向制剂也是有效抑制细胞凋亡的电离辐射防护剂。例如异氟西林(if)可以抑制细胞色素c从线粒体释放,降低电离辐射诱导的细胞内高ca
2+
,下调caspases-3的表达,减少fas外化和caspases-8激活等,从而抑制细胞凋亡;烯烃肽异位蛋白(jp4-039)、一氧化氮合酶抑制剂-合酶相关的烯烃肽(mcf201-89)和p53/mdm2/mdm4蛋白复合物抑制剂(beb55)等,均可减轻电离辐射损伤。
16.然而,虽然目前已有许多上述的多种类型的ars防治药物,但其多关注较小剂量电离辐射损伤的防护,而较少关注大剂量电离辐射损伤的预防和治疗,据统计受照电离辐射剂量<6gy的受照者病死率约为6.8%,≥6gy受照者的病死率则显著提高到90.0%,≥8gy的受照者无一例存活。随着当前核技术在军用和民用领域的广泛应用,提高对ars尤其是针对由于高剂量电离辐射导致的重型和极重型ars(例如极重度骨髓型、肠型、脑型等危重ars)的防治能力显得尤其重要。但迄今为止,国内外在对ars,尤其是重型和极重型ars的救治研究上均进展有限。
技术实现要素:
17.为了解决上述背景技术中所提出的问题,本发明的目的在于提供一种重组人sdr5-fc融合蛋白在制备预防和/或治疗急性放射病的药物中的应用,该重组人sdr5-fc融合蛋白可通过抑制电离辐射导致的过度正常细胞凋亡实现对急性放射病的预防和/或治疗作用。本发明创造性地将重组人sdr5-fc融合蛋白应用于防治由电离辐射所导致的ars,尤
其是大剂量电离辐射受照所导致的重型和极重型ars,令人惊讶地发现,重组人sdr5-fc融合蛋白确实能够防治电离辐射所导致的ars,尤其是大剂量电离辐射受照所导致的重型和极重型骨髓型ars,具体表现在该重组人sdr5-fc融合蛋白可提升电离辐射后外周血白细胞及血小板水平,促进骨髓造血干、祖细胞恢复。
18.为了达到上述目的,本发明所采用的技术方案为:一方面,本发明提供了一种重组人sdr5-fc融合蛋白在制备预防和/或治疗电离辐射诱导的急性放射病的药物中的应用。
19.进一步地,所述电离辐射诱导的急性放射病包括骨髓型急性放射病、肠型急性放射病和脑型急性放射病。
20.进一步地,所述电离辐射诱导的急性放射病可以为大剂量电离辐射诱导的急性放射病,所述大剂量电离辐射为≥6gy的电离辐射。
21.进一步地,所述重组人sdr5-fc融合蛋白通过阻断或封闭trail信号通路来阻断由电离辐射诱导的细胞凋亡预防电离辐射诱导的急性放射病。
22.进一步地,所述重组人sdr5-fc融合蛋白通过恢复急性放射病患者外周血中白细胞、血小板水平和淋巴细胞比例,以及恢复骨髓中lk和lsk细胞数量治疗急性放射病。
23.进一步地,所述重组人sdr5-fc融合蛋白的氨基酸序列如seq id no:1、seq id no:2、seq id no:3或seq id no:4所示。
24.另一方面,本发明提供了一种重组人sdr5-fc融合蛋白在制备阻断由电离辐射诱导的细胞凋亡的药物中的应用。
25.进一步地,所述重组人sdr5-fc融合蛋白可以用于制备阻断由大剂量电离辐射诱导的细胞凋亡的药物,所述大剂量电离辐射为≥6gy的电离辐射。
26.进一步地,所述重组人sdr5-fc融合蛋白通过阻断或封闭trail信号通路来阻断由电离辐射诱导的细胞凋亡。
27.进一步地,所述重组人sdr5-fc融合蛋白的氨基酸序列如seq id no:1、seq id no:2、seq id no:3或seq id no:4所示。
28.再一方面,重组人sdr5-fc融合蛋白在制备恢复急性放射病患者外周血中白细胞、血小板水平和淋巴细胞比例,以及恢复骨髓中lk和lsk细胞数量的药物中的应用。
29.进一步地,所述重组人sdr5-fc融合蛋白的氨基酸序列如seq id no:1、seq id no:2、seq id no:3或seq id no:4所示。
30.本发明的有益效果是:
31.本发明首次发现电离辐射导致生物体内正常组织细胞中dr5蛋白表达水平的上调,并且证明trail-dr5介导的细胞凋亡信号通路在电离辐射(包括高剂量电离辐射)导致的正常组织细胞凋亡中发挥重要作用。本发明首次提出重组人sdr5-fc融合蛋白在制备预防和/治疗急性放射病的药物中的应用,重组人sdr5-fc融合蛋白以trail-dr5系统为靶点,通过抑制trail-dr5的细胞凋亡信号通路,从而抑制由电离辐射导致的过度正常组织细胞凋亡,因此可有效用于对ars进行预防和/或治疗。
32.重组人sdr5-fc融合蛋白对造血免疫组织(骨髓型)急性放射病、肠型急性放射病和脑型急性放射病等具有很好的防护作用,具体表现在可提升电离辐射后小鼠外周血白细胞及血小板水平,促进骨髓造血干、祖细胞恢复,且显著提高大剂量电离辐射损伤后小鼠的生存率等;同时,由于sdr5本身是人体自身蛋白,具有毒性小、无免疫原性的优点,因此,
harbor)。
44.实施例中描述到的各种生物材料的取得途径仅是提供一种试验获取的途径以达到具体公开的目的,不应成为对本发明生物材料来源的限制。事实上,所用到的生物材料的来源是广泛的,任何不违反法律和道德伦理能够获取的生物材料都可以按照实施例中的提示替换使用。
45.以下实施例中使用的实验动物、试剂和仪器及其来源:
46.1)实验动物
47.balb/c小鼠,雄性,6~8周龄,体重19~21g,购于北京维通利华实验动物技术有限公司,动物质量合格证号:scxk-(京)2016-0006。
48.2)试剂和仪器
49.sdr5-fc融合蛋白:seq id no:4,试验代码as1501,25mg/瓶,来自深圳市中科艾深医药有限公司;
50.电子分析天平:me235s型,购自德国sartorius公司;
51.电子天平:eps-2001型,购自长沙湘平科技发展有限公司;
52.宝灵曼全自动血液分析仪:型号bm860,购自北京宝灵曼阳光科技有限公司。
53.实施例1:电离辐射诱导的细胞凋亡中dr5蛋白表达水平检测
54.本实施例中利用电离辐射照射实验小鼠,以检测受照小鼠免疫器官(例如胸腺)中dr5蛋白水平的表达情况,并初步检验sdr5-fc融合蛋白(as1501)对电离辐射诱导的细胞凋亡的抑制情况,具体包括以下步骤。
55.1.1、对balb/c小鼠单次全身60coγ射线照射,照射剂量为6.0gy,照射剂量率为68.7cgy/min,照射距离均为90cm;
56.1.2、将经照射后的balb/c小鼠随机分为正常对照组(未照射组)、模型对照组和as1501给药组,照射后当天、第一天、第二天和第三天,as1501给药组连续每天尾静脉给药10mg/kg;模型对照组给予生理盐水空白溶剂;
57.1.3、给药后24小时,将各组小鼠脱颈安乐死,取胸腺组织,制作切片,免疫组化tunnel法检测细胞凋亡率,同时荧光标记dr5抗体检测dr5蛋白表达水平的变化。
58.结果如图1所示,为60coγ射线单次全身照射balb/c小鼠后胸腺组织切片的tunnel-dr5免疫荧光图像,其中a-c:tunnel-dr5抗体双标记叠加图;d-f:dr5抗体标记检测的dr5蛋白表达水平;g-i:tunnel检测的细胞凋亡率。可见,balb/c小鼠经单次全身60coγ射线6.0gy照射后,其胸腺组织中dr5蛋白表达水平及细胞凋亡水平均有明显增高,表明小鼠经大剂量电离辐射后正常组织的dr5蛋白水平显著上调,并且也证实trail-dr5介导的细胞凋亡在电离辐射损伤的致伤机制中具有重要作用。另一方面,小鼠经60coγ射线单次全身照射后,相对于模型对照组,as1501给药组中电离辐射损伤小鼠胸腺组织的dr5蛋白表达水平无明显变化,但细胞凋亡数量有所降低,进一步证明trail-dr5介导的细胞凋亡信号通路在电离辐射诱导的细胞凋亡中发挥着重要作用,也初步证明sdr5-fc融合蛋白确实可抑制电离辐射损伤引起的小鼠胸腺细胞过度凋亡。
59.实施例2:sdr5-fc融合蛋白对大剂量电离辐射后小鼠生存率的影响
60.该实施例利用sdr5-fc融合蛋白对大剂量电离辐射后小鼠进行给药处理,并对给药后小鼠的生存率进行统计分析,以检测sdr5-fc融合蛋白对大剂量电离辐射后小鼠生存
率的影响,具体包括以下步骤。
61.2.1、将balb/c小鼠随机分为辐射模型对照组、氨磷汀(作为阳性药物)组、as1501高、中、低剂量组以及正常对照组,共6组,每组9只,其中:
62.辐射模型对照组:辐射后当天及第1-3天,每天尾静脉注射给予生理盐水空白溶剂对照;
63.氨磷汀组:辐射前30分钟,给予氨磷汀150mg/kg腹腔注射;
64.as1501高剂量组:辐射后当天及第1-3天,每天尾静脉注射给予15mg/kg剂量的as1501溶液;
65.as1501中剂量组:辐射后当天及第1-3天,每天尾静脉注射给予10mg/kg剂量的as1501溶液;
66.as1501低剂量组:辐射后当天及第1-3天,每天尾静脉注射给予5mg/kg剂量的as1501溶液;
67.正常对照组:未接受辐射的正常balb/c小鼠。
68.2.2、辐射剂量:辐射模型对照组、氨磷汀组和as1501高、中、低剂量组小鼠均接受60coγ射线一次全身照射,照射剂量8.5gy,照射剂量率为68.68cgy/min,照射距离均为90cm。
69.2.3、指标检测:不同实验组小鼠辐射给药后,观察小鼠的死亡数据,绘制给药后不同时间生存曲线图。
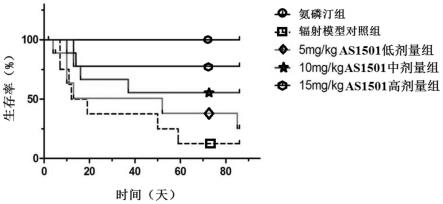
70.结果如图2所示,为不同实验组小鼠的生存曲线,可见相对于辐射模型对照组(ns),经8.5gy单次全身60coγ射线电离辐射后的balb/c小鼠经连续尾静脉注射给予高中低不同剂量sdr5-fc融合蛋白后,均可显著提升电离辐射后小鼠生存率,并且呈明显剂量依赖性,表明sdr5-fc融合蛋白具有显著提升电离辐射损伤小鼠生存率的作用,正常对照组小鼠生存状态良好,生存率100%,生存曲线未在图2中标示。
71.实施例3:sdr5-fc融合蛋白对电离辐射损伤小鼠外周血象的影响
72.该实施例利用sdr5-fc融合蛋白对电离辐射后小鼠进行给药处理,并对给药后小鼠外周血象进行测定,以检测sdr5-fc融合蛋白对电离辐射损伤小鼠外周血象的影响,具体包括以下步骤。
73.3.1、将balb/c小鼠随机分为正常对照组、生理盐水对照组和sdr5-fc融合蛋白给药组,其中:
74.生理盐水对照组:辐射后当天及第1-3天,每天尾静脉注射给予生理盐水空白溶剂对照;
75.sdr5-fc融合蛋白给药组:辐射后当天及第1-3天,每天尾静脉注射给予5mg/kg剂量的as1501溶液;
76.正常对照组:未接受辐射的正常balb/c小鼠。
77.3.2、辐射剂量:生理盐水对照组和sdr5-fc融合蛋白给药组小鼠均接受60coγ射线一次全身照射,照射剂量6gy,照射剂量率为68.7cgy/min,照射距离均为90cm。
78.3.3、样本采集:辐射后当天及辐射后第1、3、5、7、11、15、19、24、30d,分别从正常对照组、生理盐水对照组和sdr5-fc融合蛋白给药组中随机取3只小鼠,眼眶静脉丛取血30μl于抗凝管中,利用全自动血液分析仪检测外周血象,具体包括外周血象中白细胞(wbc)水
平、血小板(plt)水平和淋巴细胞比例(lym%)。
79.对各组小鼠外周血象中白细胞水平的检测结果如图3所示,可见,相对于正常对照组小鼠,6.0gy辐射后,sdr5-fc融合蛋白给药组和生理盐水对照组小鼠外周血中wbc均显著下降,在辐射后3-7天最明显,表明电离辐射在诱导细胞凋亡过程中可导致小鼠外周血中wbc水平下降。sdr5-fc融合蛋白给药组小鼠在照射后进行as1501给药处理,相对于生理盐水对照组小鼠,在第7-13天,外周血中白细胞的水平显著较高(*p<0.05),表明sdr5-fc融合蛋白在电离辐射诱导损伤后早期具有促进外周血中白细胞水平恢复的趋势。
80.对各组小鼠外周血象中血小板水平的检测结果如图4所示,可见,相对于正常对照组小鼠,6.0gy辐射后,sdr5-fc融合蛋白给药组和生理盐水对照组小鼠外周血中plt均显著下降,在辐射后7天左右最明显,表明电离辐射在诱导细胞凋亡过程中可导致外周血中plt水平下降。sdr5-fc融合蛋白给药组小鼠在照射后进行as1501给药处理,相对于生理盐水对照组小鼠,在照射后2-4周显示出较明显的促进血小板水平恢复功能,快速达到正常对照组小鼠的外周血中血小板水平,表明sdr5-fc融合蛋白在电离辐射诱导损伤后能够有效促进外周血中血小板水平的快速恢复。
81.对各组小鼠外周血象中淋巴细胞比例的检测结果如图5所示,可见,相对于正常对照组小鼠,6.0gy辐射后,sdr5-fc融合蛋白给药组和生理盐水对照组小鼠淋巴细胞比例均显著降低,表明电离辐射在诱导细胞凋亡过程中可导致外周血中淋巴细胞比例明显下降。sdr5-fc融合蛋白给药组小鼠在照射后进行as1501给药处理,相对于生理盐水对照组小鼠,可较显著增加淋巴细胞水平,表明sdr5-fc融合蛋白在电离辐射诱导损伤后能够有效恢复淋巴细胞水平。
82.实施例4:sdr5-fc融合蛋白对电离辐射损伤小鼠骨髓造血功能的影响
83.该实施例利用sdr5-fc融合蛋白对电离辐射后小鼠进行给药处理,并对给药后小鼠骨髓造血功能进行检测,以检测sdr5-fc融合蛋白对电离辐射损伤小鼠骨髓造血功能的影响,具体包括以下步骤。
84.4.1、将balb/c小鼠随机分为正常对照组、生理盐水对照组和sdr5-fc融合蛋白给药组,其中:
85.生理盐水对照组:辐射后当天及第1-3天,每天尾静脉注射给予生理盐水空白溶剂对照;
86.sdr5-fc融合蛋白给药组:辐射后当天及第1-3天,每天尾静脉注射给予10mg/kg剂量的as1501溶液;
87.正常对照组:未接受辐射的正常balb/c小鼠。
88.4.2、辐射剂量:生理盐水对照组和sdr5-fc融合蛋白给药组小鼠均接受60coγ射线一次全身照射,照射剂量4gy,照射剂量率为68.7cgy/min,照射距离均为90cm。
89.4.3、样本采集:辐射后当天(2h)及辐射后第1、4、7、11、14、19d,分别从正常对照组、生理盐水对照组和sdr5-fc融合蛋白给药组中随机取3只小鼠,分别麻醉处死小鼠,分离小鼠骨髓细胞并计数,用cd16/32抗体孵育后,1%bsa封闭;再用lineage抗体、sca-1抗体和c-kit在4℃标记30min。0.4%多聚甲醛固定后用流式细胞仪检测骨髓有核细胞中的linsca-1-c-kit+(lk)和lin-sca-1+c-kit+(lsk)细胞百分比并计算细胞数。
90.对各组小鼠骨髓lk细胞和lsk细胞数量的检测结果分别如图6和图7所示,可见,
4.0gy辐射后,sdr5-fc融合蛋白给药组和生理盐水对照组小鼠骨髓lk和lsk细胞数量均显著降低,表明电离辐射在诱导细胞凋亡过程中可导致骨髓lk和lsk细胞数量明显下降。与生理盐水对照组比较,sdr5-fc融合蛋白给药组在多个时间点均可较显著增加骨髓lk和lsk细胞水平,表明sdr5-fc融合蛋白在电离辐射损伤的治疗中具有一定促进骨髓造血功能修复作用。
91.综上实施例结果可知,电离辐射能够引起正常组织细胞的凋亡,并且在电离辐射诱导的正常组织(例如免疫器官、造血系统等)细胞凋亡时,检测到组织中dr5蛋白表达水平显著上调,并且基于sdr5-fc融合蛋白可有效降低细胞凋亡率的结果证明trail-dr5介导的细胞凋亡信号通路在电离辐射诱导的细胞凋亡中发挥着重要作用,至少会诱导外周血中的白细胞、血小板和淋巴细胞,以及造血系统如骨髓中lk和lsk细胞的凋亡,造成血象平衡状态改变和造血干、祖细胞数量的下降,进而引发严重的急性放射病ars。基于此,发明人创造性地将sdr5-fc融合蛋白用于预防和/或治疗由电离辐射导致的ars中,利用sdr5-fc融合蛋白可阻断trail-dr5介导的细胞凋亡信号通路的原理,有效保护电离辐射过程中正常组织细胞不受辐射影响并促进电离辐射损伤后正常组织中细胞水平的恢复,具体可表现为可显著提升电离辐射损伤后外周血中血象关键指标白细胞、血小板和淋巴细胞水平,促进其快速恢复至正常状态,并可促进骨髓造血干、祖细胞恢复。因此,sdr5-fc融合蛋白可在由电离辐射导致的重度或极重度ars,尤其是极重度骨髓型ars等的预防和/或治疗中具有良好应用前景,为ars的治疗提供了新的方法。
92.氨基酸序列如seq id no:1、seq id no:2、seq id no:3所示的sdr5-fc融合蛋白具有与氨基酸序列如seq id no:4所示的sdr5-fc融合蛋白相似的效果。
93.最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1