一种抗菌抗凝血涂层、制备方法及其应用
1.本发明涉及医用材料技术领域,具体而言,涉及一种抗菌抗凝血涂层、制备方法及其应用。
背景技术:
2.血液接触类生物材料是一类应用于临床的植入性材料,具有治疗、替换或增进组织功能等作用。其中,血液接触植/介入器械及体外血液循环设备在临床应用中一直面临着术后感染和血栓栓塞等并发症,这些并发症不仅会影响器械寿命,更为严重的是并发症还会对患者造成极大的伤害。
3.目前,临床应对这些问题的主要策略是通过系统给药方式进行抗生素和抗凝药物辅助治疗,但是长期使用抗生素和抗凝药物则不可避免地会引起一系列副作用。例如抗生素耐药性和血小板减少症等、甚至会导致出血。
4.然而,目前报道的大多数表面改性方法存在工艺复杂、需要繁复的表面预处理、涉及到有毒化学试剂等问题。
5.鉴于此,特提出本发明。
技术实现要素:
6.本发明的目的在于提供一种抗菌抗凝血涂层、制备方法及其应用以解决上述技术问题。本发明提供了新的策略从而减少上述并发症的发生,这对于在设备和血液之间提供安全的生物相容性界面是至关重要的,有利于提高血液接触类生物器材的表面性能。
7.本发明是这样实现的:
8.本发明提供了一种抗菌抗凝血涂层,其包括内涂层和外涂层,内涂层带有酚羟基、伯氨基和金属离子;外涂层由如下方法制得:通过酰胺键将带有nhs活化羧基的烯烃化合物接枝于内涂层表面,在含有自由基引发剂的刺激响应型聚合物单体溶液中通过自由基聚合反应共聚制得。
9.在本发明应用较佳的实施方式中,上述内涂层由儿茶酚结构化合物、多元氨基化合物和金属离子沉积而成;
10.优选地,儿茶酚结构化合物的酚羟基与金属离子通过配位键结合,多元氨基化合物具有能与儿茶酚结构化合物反应的伯氨基。
11.在本发明应用较佳的实施方式中,上述内涂层是将待处理基材置于含儿茶酚结构化合物、多元氨基化合物和金属离子的混合溶液中制得,其中,儿茶酚结构化合物浓度为0.1
‑
1000mg/ml,多元氨基化合物浓度为1
‑
10mg/ml,金属离子浓度为0.05
‑
1mg/ml;
12.优选地,儿茶酚结构化合物浓度为0.1
‑
2mg/ml,多元氨基化合物浓度为2
‑
5mg/ml,金属离子浓度为0.1
‑
0.3mg/ml。
13.在本发明应用较佳的实施方式中,上述儿茶酚结构化合物为邻苯二酚及其衍生物;多元氨基化合物为己二胺、聚烯丙胺及其盐酸盐、聚赖氨酸、壳聚糖、聚乙烯亚胺及其衍
生物、乙二胺中的至少一种;金属离子为二价金属离子;
14.优选地,邻苯二酚衍生物包括黄酮醇类、花色素类、花色苷类或花青素类、邻羟基苯甲酸酯类、黄酮类、羟基茋类、3,4
‑
二羟基苯丙氨酸及其衍生物、2,3
‑
二羟基苯丙氨酸及其衍生物、4,5
‑
二羟基苯丙氨酸及其衍生物、二羟基肉桂酸酯类、邻多羟基香豆素类、邻多羟基异香豆素类、邻多羟基香豆酮类、邻多羟基异香豆酮类、邻多羟基查耳酮类、邻多羟基色酮类、邻多羟基醌类、邻羟基氧杂蒽酮类、1,2二羟基苯及其衍生物、1,2,4
‑
三羟基苯及其衍生物、1,2,3
‑
三羟基苯及其衍生物、2,4,5
‑
三羟基甲苯及其衍生物、原花色素类原花色苷类、单宁酸、鞣花酸、3,4,5
‑
三羟基苯甲酸、去甲基肾上腺素、多巴胺中的至少一种;
15.优选地,邻苯二酚衍生物包括多巴胺、3,4,5
‑
三羟基苯甲酸、单宁酸、去甲基肾上腺素、3,4
‑
二羟基苯丙氨酸及其衍生物、2,3
‑
二羟基苯丙氨酸及其衍生物、4,5
‑
二羟基苯丙氨酸及其衍生物中的至少一种;
16.优选地,二价金属离子为铜离子、锌离子和镁离子中的至少一种。
17.在本发明应用较佳的实施方式中,上述带有nhs活化羧基的烯烃化合物通过酰胺反应接枝于所述内涂层表面;
18.优选地,为n
‑
羟基琥珀酰亚胺丙烯酸酯、丙烯酸酯peg
‑
n羟基琥珀酰亚胺酯中的至少一种;
19.优选地,浓度为1
‑
10mg/ml;
20.优选地,浓度为3
‑
5mg/ml。
21.在本发明应用较佳的实施方式中,上述刺激响应型聚合物单体为能被自由基引发聚合生成具有亲疏水性与温度或光照相关的特性的聚合物;
22.优选地,刺激响应型聚合物单体为n
‑
异丙基丙烯酰胺、2
‑
螺吡喃丙基甲基丙烯酸甲酯、n
‑
乙烯基己内酰胺、n,n
‑
二乙基丙烯酰胺、n
‑
异丙基甲基丙烯酰胺、甲基丙烯酸、甲基丙烯酸二甲氨基乙酯、3
‑
(二甲基(4
‑
乙烯基苄基铵)丙基磺酸盐、3
‑
(1
‑
(4
‑
乙烯基苄基)
‑
1h
‑
咪唑
‑3‑
鎓)丙烷
‑1‑
磺酸盐中的至少一种;
23.优选地,刺激响应型聚合物单体浓度为50
‑
1000mg/ml;
24.优选地,刺激响应型聚合物单体浓度为100
‑
300mg/ml;
25.在本发明应用较佳的实施方式中,上述引发剂为过硫酸钠、过硫酸铵和过硫酸钾的至少一种;
26.优选地,引发剂的浓度为0.1
‑
10mg/ml;
27.优选地,引发剂的浓度为1
‑
3mg/ml。
28.本发明还提供了一种抗菌抗凝血涂层的制备方法,其包括如下步骤:在待处理基材的表面制备带有酚羟基、伯氨基和金属离子的内涂层,然后将表面具有内涂层的基材置于含有nhs活化羧基的烯烃化合物中反应,再置于含有引发剂的刺激响应型聚合物单体溶液中共聚制得外涂层。
29.在本发明应用较佳的实施方式中,上述内涂层的制备是将待处理基材置于含儿茶酚结构化合物、多元氨基化合物和金属离子的弱碱性水溶液中进行,优选地,弱碱性水溶液为tris缓冲溶液、pbs缓冲溶液、becine缓冲溶液、氢氧化钠溶液和氢氧化钾溶液的至少一种;优选地,内涂层制备时的反应温度为1
‑
100℃,反应时间为1
‑
24小时;优选地,反应时间为10
‑
15h;
30.优选地,将表面具有内涂层的基材置于含有羧基的烯烃化合物中反应的温度为1
‑
100℃,反应时间为1
‑
24h;优选地,反应的温度为37℃,反应时间为2
‑
8h;
31.共聚反应的温度为1
‑
100℃,共聚反应的时间为12
‑
72h;优选地,共聚反应的时间为24
‑
48h。
32.本发明还提供了一种如抗菌抗凝血涂层或抗菌抗凝血涂层的制备方法制得的抗菌抗凝血涂层在制备医用材料表面涂层中的应用,医用材料为血液接触类器械。
33.本发明具有以下有益效果:
34.本发明通过先制备具有酚羟基、伯氨基和金属离子的内涂层,一方面,金属离子具有杀菌功能而赋予涂层抗菌性能,另一方面金属离子能催化体内的rsno(亚硝基硫醇化合物)产生no,从而赋予涂层持久的no释放功能。而外涂层为刺激响应性聚合物,通过外界的刺激,如温度和光照的变化,通过改变构象使得表面微生物被释放,从而洗脱黏附在涂层外表面的微生物,即外涂层具有抑制生物膜形成的功能。因此,本发明提供的抗菌抗凝涂层综合了抗菌、抗凝和抑制生物膜形成的三种功能。
35.此外,本申请还提供了抗菌抗凝涂层的制备方法,具有中间步骤少,简单易行的优势。制备获得的抗菌抗凝抑制生物膜形成涂层可广泛应用于血液接触类器械的表面改性。
附图说明
36.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
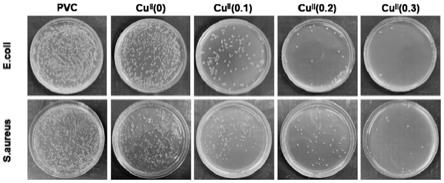
37.图1为不同铜离子浓度(0
‑
300μg/ml)的抗菌抗凝抑制生物膜形成涂层的抗菌效果图;
38.图2为血液凝固结果示意图。
具体实施方式
39.现将详细地提供本发明实施方式的参考,其一个或多个实例描述于下文。提供每一实例作为解释而非限制本发明。实际上,对本领域技术人员而言,显而易见的是,可以对本发明进行多种修改和变化而不背离本发明的范围或精神。例如,作为一个实施方式的部分而说明或描述的特征可以用于另一实施方式中,来产生更进一步的实施方式。
40.本发明提供了一种抗菌抗凝血涂层,其包括内涂层和外涂层,内涂层带有酚羟基、伯氨基和金属离子;外涂层由如下方法制得:通过酰胺键将带有nhs活化羧基的烯烃化合物接枝于内涂层表面,在含有自由基引发剂的刺激响应型聚合物单体溶液中通过自由基聚合反应共聚制得。
41.经发明人研究发现,内涂层中螯合的金属离子可以杀死细菌赋予涂层优异的抗菌效果,并且金属离子可通过催化内源性s
‑
亚硝基硫醇的分解,赋予涂层持久的no释放能力。此外,内涂层表面接枝的刺激响应型聚合物可以通过控制外界环境的变化,如温度和光照,可以改变构象使得表面微生物被释放,从而洗脱涂层表面黏附的微生物,赋予抗菌抗凝血涂层抑制生物膜形成的功能。因此,这三种功能的结合,使得经由抗菌抗凝涂层改性过的血
液接触类器械表现出优异的抗菌抗凝抑制生物膜形成的功能,有效地解决了血液接触类器械术后感染问题和血栓栓塞等并发症问题。
42.在本发明应用较佳的实施方式中,上述内涂层由儿茶酚结构化合物、多元氨基化合物和金属离子沉积而成。在一种实施方式中,是将待处理基材置于儿茶酚结构化合物、多元氨基化合物和金属离子的混合液中,反应后在待处理基材的表面制备内涂层。
43.在一种实施方式中,儿茶酚结构化合物的酚羟基与金属离子通过配位键结合,多元氨基化合物具有能与儿茶酚结构化合物反应的伯氨基。通过共价键以实现儿茶酚结构化合物、多元氨基化合物以及金属离子的结合。
44.在本发明应用较佳的实施方式中,上述内涂层是将待处理基材置于含儿茶酚结构化合物、多元氨基化合物和金属离子的混合溶液中制得,其中,儿茶酚结构化合物浓度为0.1
‑
1000mg/ml,多元氨基化合物浓度为1
‑
10mg/ml,金属离子浓度为0.05
‑
1mg/ml。
45.在一种实施方式中,儿茶酚结构化合物浓度为0.1
‑
2mg/ml,多元氨基化合物浓度为2
‑
5mg/ml,金属离子浓度为0.1
‑
0.3mg/ml。
46.在一种实施方式中,儿茶酚结构化合物浓度为0.1mg/ml、0.2mg/ml、0.5mg/ml、0.8mg/ml、1mg/ml、1.2mg/ml、1.5mg/ml、1.8mg/ml或2mg/ml。
47.多元氨基化合物浓度为2mg/ml、3mg/ml、4mg/ml或5mg/ml,金属离子浓度为0.1mg/ml、0.2mg/ml或0.3mg/ml。
48.需要说明的是,上述所列举的浓度数值仅为发明人列举的几种情形,在其他实施方式中,上述反应物的浓度并不限于上述列举的具体值范围内。可选为母液或者稀释液。
49.在本发明应用较佳的实施方式中,上述儿茶酚结构化合物为邻苯二酚及其衍生物;多元氨基化合物为己二胺、聚烯丙胺及其盐酸盐、聚赖氨酸、壳聚糖、聚乙烯亚胺及其衍生物、乙二胺中的至少一种;金属离子为二价金属离子。
50.在一种实施方式中,邻苯二酚衍生物包括黄酮醇类、花色素类、花色苷类或花青素类、邻羟基苯甲酸酯类、黄酮类、羟基茋类、3,4
‑
二羟基苯丙氨酸及其衍生物、2,3
‑
二羟基苯丙氨酸及其衍生物、4,5
‑
二羟基苯丙氨酸及其衍生物、二羟基肉桂酸酯类、邻多羟基香豆素类、邻多羟基异香豆素类、邻多羟基香豆酮类、邻多羟基异香豆酮类、邻多羟基查耳酮类、邻多羟基色酮类、邻多羟基醌类、邻羟基氧杂蒽酮类、1,2二羟基苯及其衍生物、1,2,4
‑
三羟基苯及其衍生物、1,2,3
‑
三羟基苯及其衍生物、2,4,5
‑
三羟基甲苯及其衍生物、原花色素类原花色苷类、单宁酸、鞣花酸、3,4,5
‑
三羟基苯甲酸、去甲基肾上腺素、多巴胺中的至少一种;
51.在一种实施方式中,邻苯二酚衍生物包括多巴胺、3,4,5
‑
三羟基苯甲酸、单宁酸、去甲基肾上腺素、3,4
‑
二羟基苯丙氨酸及其衍生物、2,3
‑
二羟基苯丙氨酸及其衍生物、4,5
‑
二羟基苯丙氨酸及其衍生物中的至少一种。
52.在一种实施方式中,上述邻苯二酚衍生物是具有芳环的邻苯二酚,芳环选自:苯、萘、四氢化萘、二氢化茚、茚、蒽、菲、异吲哚、二氢吲哚、异二氢吲哚、苯并呋喃、二氢苯并呋喃、苯并二氢吡喃、异苯并二氢吡喃、苯并吡喃、异苯并吡喃、喹啉、四氢喹啉以及异喹啉,芳环包含由芳环的两个相邻碳原子携带的至少两个羟基基团。
53.在一种实施方式中,上述的邻苯二酚衍生物可以选自儿茶素、槲皮素、巴西木素(braziline)、血色素、苏木精、绿原酸、咖啡酸、没食子酸、儿茶酚、没食子酸、l
‑
dopa、花葵素、矢车菊素、(
‑
)
‑
表儿茶素、(
‑
)
‑
表没食子儿茶素、(
‑
)
‑
表没食子儿茶素3
‑
没食子酸酯
(egcg)、(+)
‑
儿茶素、异槲皮素、橙桑黄酮、七叶亭、6,7
‑
二羟基
‑3‑
(3
‑
羟基
‑
2,4
‑
二甲氧基苯基)香豆素、紫檀素ac、芒果苷、紫铆因、海生菊苷、硫黄菊素、刺槐因、甜菜素、3,4
‑
二氢
‑
6,7
‑
二羟基
‑
1(2h)
‑
异喹啉酮(pericampylinon a)、茶黄素、原花色素a2、原花色素b2、原花色素c1、原矢车菊素dp4
‑
8、单宁酸、红棓酚、5,6
‑
二羟基
‑2‑
甲基
‑
1,4
‑
萘醌、茜素、蟛蜞菊内酯、(3,3',4,4'
‑
普耳文酸)(variegatic acid)、钉菇酸(gomphidic acid)、地衣酸(xerocomic acid)、鼠尾草酚,以及含有它们的天然提取物。
54.在一种实施方式中,上述的邻苯二酚衍生物也可以为天然的邻苯二酚衍生物,例如选自动物、细菌、真菌、藻类、植物以及果实提取物。
55.上述的二价金属离子为铜离子、锌离子和镁离子中的至少一种。
56.在本发明应用较佳的实施方式中,上述带有nhs活化羧基的烯烃化合物通过酰胺反应接枝于所述内涂层表面。
57.在一种实施方式中,为n
‑
羟基琥珀酰亚胺丙烯酸酯、丙烯酸酯peg
‑
n羟基琥珀酰亚胺酯中的至少一种;
58.在一种实施方式中,浓度为1
‑
10mg/ml。例如1mg/ml、2mg/ml、3mg/ml、4mg/ml、5mg/ml、6mg/ml、7mg/ml、8mg/ml、9mg/ml或10mg/ml。
59.在一种实施方式中,浓度为3
‑
5mg/ml。
60.在本发明应用较佳的实施方式中,上述刺激响应型聚合物单体为能被自由基引发聚合生成具有亲疏水性与温度或光照相关的特性的聚合物;
61.在一种实施方式中,刺激响应型聚合物单体为n
‑
异丙基丙烯酰胺、2
‑
螺吡喃丙基甲基丙烯酸甲酯、n
‑
乙烯基己内酰胺、n,n
‑
二乙基丙烯酰胺、n
‑
异丙基甲基丙烯酰胺、甲基丙烯酸、甲基丙烯酸二甲氨基乙酯、3
‑
(二甲基(4
‑
乙烯基苄基铵)丙基磺酸盐、3
‑
(1
‑
(4
‑
乙烯基苄基)
‑
1h
‑
咪唑
‑3‑
鎓)丙烷
‑1‑
磺酸盐中的至少一种;
62.在一种实施方式中,刺激响应型聚合物单体浓度为50
‑
1000mg/ml;例如:100mg/ml、200mg/ml、300mg/ml、400mg/ml、500mg/ml、600mg/ml、700mg/ml、800mg/ml、900mg/ml或1000mg/ml。
63.在一种实施方式中,刺激响应型聚合物单体浓度为100
‑
300mg/ml。
64.在本发明应用较佳的实施方式中,上述引发剂为过硫酸钠、过硫酸铵和过硫酸钾的至少一种。在其他实施方式中,上述引发剂的类型可以根据需要进行自适应调整,并不限于上述限定的几种引发剂的种类。
65.在一种实施方式中,引发剂的浓度为0.1
‑
10mg/ml;例如:0.1mg/ml、0.5mg/ml、1mg/ml、2mg/ml、3mg/ml、4mg/ml、5mg/ml、6mg/ml、7mg/ml、8mg/ml、9mg/ml或10mg/ml。
66.在一种实施方式中,引发剂的浓度为1
‑
3mg/ml。
67.本发明还提供了一种抗菌抗凝血涂层的制备方法,其包括如下步骤:在待处理基材的表面制备带有酚羟基、伯氨基和金属离子的内涂层,然后将表面具有内涂层的基材置于含有nhs活化羧基的烯烃化合物中反应,再置于含有引发剂的刺激响应型聚合物单体溶液中共聚制得外涂层。
68.在本发明应用较佳的实施方式中,上述内涂层的制备是将待处理基材置于含儿茶酚结构化合物、多元氨基化合物和金属离子的弱碱性水溶液中进行,在一种实施方式中,弱碱性水溶液为tris缓冲溶液、pbs缓冲溶液、becine缓冲溶液、氢氧化钠溶液和氢氧化钾溶
液的至少一种;在一种实施方式中,内涂层制备时的反应温度为1
‑
100℃,反应时间为1
‑
24小时;在一种实施方式中,反应时间为10
‑
15h;
69.在一种实施方式中,将表面具有内涂层的基材置于含有羧基的烯烃化合物中反应的温度为1
‑
100℃,反应时间为1
‑
24h;在一种实施方式中,反应的温度为37℃,反应时间为2
‑
8h;
70.共聚反应的温度为1
‑
100℃,共聚反应的时间为12
‑
72h;在一种实施方式中,共聚反应的时间为24
‑
48h。
71.本发明还提供了一种如抗菌抗凝血涂层或抗菌抗凝血涂层的制备方法制得的抗菌抗凝血涂层在制备医用材料表面涂层中的应用,医用材料为血液接触类器械。血液接触类器械包括不限于一二三类器械。
72.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
73.以下结合实施例对本发明的特征和性能作进一步的详细描述。
74.实施例1
75.1mg多巴胺、2mg己二胺和0.4mg氯化铜溶解在4ml tris溶液中,混合均匀后,将pvc置于反应液中,反应12小时后。用去离子水清洗三次后用n2吹干即可制得内涂层。
76.将5mg的n
‑
羟基琥珀酰亚胺丙烯酸酯溶于5ml的pbs溶液中,混合均匀后,将沉积有内涂层的材料置于反应液中,反应6小时后。用去离子水清洗三次后用n2吹干,然后置于用15mg过硫酸钠、800mgn
‑
异丙基丙烯酰胺和8ml去离子水的均匀混合溶液中反应48小时,用去离子水清洗三次后用n2吹干,制得抗菌抗凝抑制生物膜形成涂层。
77.实施例2
78.1mg多巴胺、2mg己二胺和0.6mg氯化铜溶解在4ml tris溶液中,混合均匀后,将pvc置于反应液中,反应12小时后。用去离子水清洗三次后用n2吹干即可制得内涂层。
79.将5mg的n
‑
羟基琥珀酰亚胺丙烯酸酯溶于2.5ml的pbs溶液中,混合均匀后,将沉积有内涂层的材料置于反应液中,反应6小时后。用去离子水清洗三次后用n2吹干,然后置于用15mg过硫酸钠、1600mgn
‑
异丙基丙烯酰胺和8ml去离子水的均匀混合溶液中反应48小时,用去离子水清洗三次后用n2吹干,制得抗菌抗凝抑制生物膜形成涂层。
80.实施例3
81.2mg多巴胺、2mg己二胺和0.4mg氯化铜溶解在4ml tris溶液中,混合均匀后,将pvc置于反应液中,反应12小时后。用去离子水清洗三次后用n2吹干即可制得内涂层。
82.将5mg的n
‑
羟基琥珀酰亚胺丙烯酸酯溶于2.5ml的pbs溶液中,混合均匀后,将沉积有内涂层的材料置于反应液中,反应12小时后。用去离子水清洗三次后用n2吹干,然后置于用15mg过硫酸钠、800mgn
‑
异丙基丙烯酰胺和8ml去离子水的均匀混合溶液中反应48小时,用去离子水清洗三次后用n2吹干,制得抗菌抗凝抑制生物膜形成涂层。
83.实施例4
84.1mg多巴胺、4mg己二胺和0.6mg氯化铜溶解在4ml tris溶液中,混合均匀后,将pvc置于反应液中,反应12小时后。用去离子水清洗三次后用n2吹干即可制得内涂层。
85.将5mg的n
‑
羟基琥珀酰亚胺丙烯酸酯溶于5ml的pbs溶液中,混合均匀后,将沉积有内涂层的材料置于反应液中,反应6小时后。用去离子水清洗三次后用n2吹干,然后置于用30mg过硫酸钠、800mgn
‑
异丙基丙烯酰胺和8ml去离子水的均匀混合溶液中反应48小时,用去离子水清洗三次后用n2吹干,制得抗菌抗凝抑制生物膜形成涂层。
86.实施例5
87.与实施例1相比,区别仅在于刺激响应型聚合物单体为2
‑
螺吡喃丙基甲基丙烯酸甲酯,带有nhs活化羧基的烯烃化合物为丙烯酸酯peg
‑
n羟基琥珀酰亚胺酯其余的制备方法和条件相同。
88.实施例6
89.与实施例1相比,区别仅在于刺激响应型聚合物单体为n
‑
乙烯基己内酰胺。其余的制备方法和条件相同。
90.实施例7
91.与实施例1相比,区别仅在于刺激响应型聚合物单体为n,n
‑
二乙基丙烯酰胺。其余的制备方法和条件相同。
92.实施例8
93.与实施例1相比,区别仅在于:邻苯二酚衍生物为3,4,5
‑
三羟基苯甲酸,二价金属离子来源为硫化锌,多元氨基化合物为聚烯丙胺,其余的制备方法和条件相同。
94.实施例9
95.与实施例1相比,区别仅在于:邻苯二酚衍生物为去甲基肾上腺素,二价金属离子来源为硫化镁,多元氨基化合物为聚乙烯亚胺,其余的制备方法和条件相同。
96.实施例10
97.与实施例1相比,区别仅在于:邻苯二酚衍生物为3,4
‑
二羟基苯丙氨酸,二价金属离子来源为硫化镁,多元氨基化合物为乙二胺,其余的制备方法和条件相同。
98.实施例11
99.1mg多巴胺、2mg己二胺和0.4mg硫化铜溶解在4ml pbs缓冲溶液中,混合均匀后,将pvc置于反应液中,反应2小时后。用去离子水清洗三次后用n2吹干即可制得内涂层。
100.将5mg的n
‑
羟基琥珀酰亚胺丙烯酸酯溶于5ml的pbs溶液中,混合均匀后,将沉积有内涂层的材料置于反应液中,反应18小时后,反应温度为25℃。用去离子水清洗三次后用n2吹干,然后置于用15mg过硫酸钠、8mgn
‑
异丙基丙烯酰胺和8ml去离子水的均匀混合溶液中反应15小时,用去离子水清洗三次后用n2吹干,制得抗菌抗凝抑制生物膜形成涂层。
101.实验例1
102.抗菌实验。
103.检测样品的制备包括如下步骤:按照实施例1提供的涂层制备方法分别以不同浓度的氯化铜制备抗菌抗凝抑制生物膜形成涂层,与实施例1相比,区别仅在于氯化铜的浓度不同,分别为0、0.1mg/ml、0.2mg/ml和0.3mg/ml,其余的制备方法和条件均相同,制得四种含有涂层的pvc,具体记为:cuⅱ(0)、cuⅱ(0.1)、cuⅱ(0.2)以及cuⅱ(0.3)。不含有涂层的pvc作为对照样品组。
104.菌种:革兰氏阳性菌(金黄色葡萄球菌,s.aureus)和革兰氏阴性菌(大肠杆菌)。
105.具体过程如下:
106.(1)菌种保藏:将菌种分别接种于营养琼脂(na)斜面上,37
±
1℃条件下培养24h后,在0~5℃条件下保存不超过30天;
107.(2)菌种活化:将步骤(1)中保藏的斜面菌种转接到平板营养琼脂培养基上,在37
±
1℃条件下培养24h,每天转接一次,不超过两周。本实验采用连续转接2次后的新鲜细菌培养物(24h之内转接的);
108.(3)检测样品的紫外灭菌:检测样品和覆盖膜正反面都在超净台上进行紫外灭菌,先反面紫外照射60min,再正面照射30min。覆盖膜不分正反面均在紫外下照射60min;
109.(4)菌悬液制备:用接种环从步骤(2)中转接后的培养基上取少量(1~3环)新鲜细菌,加入培养液(营养肉汤/生理盐水。大肠杆菌选用浓度为1/500的营养肉汤稀释液,金黄色葡萄球菌为1/100的营养肉汤稀释液)中,并依次做10倍递增稀释,连续稀释五次后的实验接种物作为试验用菌悬液(接种环上的细菌稀释到1ml培养液为单倍菌液,继续稀释1000倍为实验菌液);
110.将上述灭菌后的检测样品接种上述步骤(4)制备的菌悬液:分别取实验用菌悬液100μl滴加在检测样品(2.5cm
×
2.5cm)表面,每个样品三个平行。用灭菌镊子夹起灭菌覆盖膜(2.2cm
×
2.2cm,0.05~0.10mm厚)分别覆盖在检测样品上,铺平,使其中没有气泡,菌液均匀接触样品。置于无菌培养皿中,并在培养皿中放入一团无菌水润湿的棉花。将培养皿置于37
±
1℃、相对湿度大于90%的条件下培养24h。
111.菌落计数前的菌落培养:取出培养皿放在超净工作台上,取出培养皿中的棉花团,然后分别在每个样品的培养皿中加入10ml洗脱液,反复吹打清洗样品正面和覆盖膜,充分混匀后取100μl接种于提前凝固好的营养琼脂培养基上,立马均匀地推开。最后置于37
±
1℃下培养24h后计数。
112.检测结果参见图1。根据图1可知,可以得知,不管是金黄色葡萄球菌抗菌实验还是大肠杆菌抗菌实验,在含有铜离子样品上的菌落数明显低于pvc空白对照样上的菌落数,而且不含有铜离子的涂层样品表面的细菌数也略少于pvc空白对照样;随着加入的铜离子浓度增加,菌落数目降低。说明加入的铜离子浓度越大,涂层的抗菌性能越好。
113.实验例2
114.本实验例进行半体内动物实验。
115.检测样品的制备:
116.检测样品1的制备,与实施例1相比,区别仅在于氯化铜浓度为0mg/ml,其余的制备方法和条件与实施例1相同,由该制备方法制得的导管样品。
117.检测样品的编号如下:不含涂层的pvc导管、检测样品1、聚(n
‑
异丙基丙烯酰胺)(pnipam)以及实施例1的导管样品,具体记为:pvc、cuⅱ、pnipam、cuⅱ+pnipam。
118.具体过程如下:
119.(1)将上述样品与半体内循环导管装置相连接组装,向其中灌入生理盐水,轻弹样品管与三通管连接处以确保气泡完全排出,并在两端用止血钳夹住;
120.(2)耳缘注射30mg/ml的戊巴比妥钠溶液麻醉新西兰大白兔,划开颈部皮肤并小心剥离出兔左颈动脉和右颈静脉,使血管裸露。随后在兔耳缘静脉注射10μm no供体;
121.(3)取出用生理盐水浸润后的留置针并穿刺插入兔颈动脉和颈静脉,随后将组装好的样品与兔颈动脉和静脉相连。取下止血钳后,使血液流回心脏形成半体内血液循环回
路。并记录实验开始时间。在实验过程中不断观察导管中血液颜色的变化,并每隔30min进行一次检流,检查导管是否堵塞,同时每隔60min补充一次供体;
122.(4)循环3h后实验停止,取下实验装置,并用生理盐水对其进行冲洗。随后拍摄样品照片和导管横截面,参见图2,通过实验导管的横截面图片评价抗凝血功能。
123.根据图2可知,不含有涂层的pvc样品和不含有铜离子涂层样品完全堵塞,而含有铜离子的样品,无论是否接枝了pnipam,均未堵塞,证明了铜离子催化no供体释放no,赋予了样品优异的抗凝血功能。
124.以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1