一种基于心电单极导联V2、V5推衍导联V3、V4的方法及设备与流程
本发明涉及心电导联技术领域,尤其涉及一种基于心电单极导联v2、v5推衍导联v3、v4的方法及设备。
背景技术:
动态心电图是通过动态心电图仪在患者日常生活状态下连续24小时或更长时间记录其心电活动的全过程,并借助计算机进行分析处理,以发现在常规体表心电图检查时不易发现的心律失常和心肌缺血等,为临床诊断、治疗及判断疗效提供重要的客观依据。动态心电图仪又称holter心电图,已由单导、双导发展为12导联、18导联全记录。
随着导联增加,心电数据更加全面,利于心脏诊断。然而,导联增加,导联电极数量增加,且患者需要佩戴24小时或更长时间,不利于患者活动,且舒适性降低。因此,在现有的心电算法中,一般采用推衍导联的方式,以减少动态心电图实际所需的导联电极数量。
导联电极及安放位置如下:v1,电极安放于胸骨右缘第四肋间;v2,电极安放于胸骨左缘第四肋间;v3,电极安放于v2~v4连接线的中间位置;v4,电极安放于左锁骨中线与第五肋间相交处;v5,电极安放于左腋前线和v4同一水平的位置。
目前,已有心电算法较少能推衍或准确推衍v3和v4。
技术实现要素:
本发明实施例的主要目的在于提供一种基于心电单极导联v2、v5推衍导联v3、v4的方法及设备,旨在推衍特别是准确推衍v3和v4,以进一步减少导联电极。
本发明实施例提供了一种基于心电单极导联v2、v5推衍导联v3、v4的方法,所述方法包括以下步骤:获取心电单极导联v2的临床数据v2和心电单极导联v5的临床数据v5;对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行基于临近单极导联线性相关的推衍处理,得到导联v3的推衍数据v′3和导联v4的推衍数据v′4;对所述导联v3的推衍数据v′3和所述导联v4的推衍数据v′4分别进行幅值转化处理,得到所述导联v3的合成数据v3和所述导联v4的合成数据v4,以便利用所述导联v3的合成数据v3和所述导联v4的合成数据v4进行心电图分析。
优选地,所述对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行基于临近单极导联线性相关的推衍处理,得到所述导联v3的推衍数据v′3和所述导联v4的推衍数据v′4包括:利用用于推衍所述导联v3的第一线性回归方程,对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行推衍处理,得到所述导联v3的推衍数据v′3,其中,所述第一线性回归方程为v′3=β31*v2+β32*v5+β30,所述β31,β32,β30是所述第一线性回归方程的参数;利用用于推衍所述导联v4的第二线性回归方程,对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行推衍处理,得到所述导联v4的推衍数据v′4,其中,所述第二线性回归方程为v′4=β41*v2+β42*v5+β40,其中,β41,β42,β40是所述第二线性回归方程的参数。
优选地,所述第一线性回归方程的参数β31、β32、β30的参数值通过以下步骤得到:获取第一时间段内所述心电单极导联v2的已有临床数据、所述心电单极导联v3的已有临床数据和所述心电单极导联v5的已有临床数据;利用所述第一时间段内的所述心电单极导联v2的已有临床数据、所述心电单极导联v3的已有临床数据和所述心电单极导联v5的已有临床数据,确定所述第一线性回归方程的参数β31、β32、β30的初始的参数值;对所述第一线性回归方程的参数β31、β32、β30的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β31、β32、β30的最终的参数值。
优选地,所述对所述第一线性回归方程的参数β31、β32、β30的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β31、β32、β30的最终的参数值包括:根据所述第一时间段内所述心电单极导联v2的已有临床数据,确定所述心电单极导联v2的已有临床数据平均值v2amp;根据所述第一时间段内所述心电单极导联v5的已有临床数据,确定所述心电单极导联v5的已有临床数据平均值v5amp;利用所述心电单极导联v2的已有临床数据平均值v2amp和所述心电单极导联v5的已有临床数据平均值v5amp,对所述第一线性回归方程的参数β31、β32、β30的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β31、β32、β30的最终的参数值。
优选地,所述第二线性回归方程的参数β41、β42、β40的参数值通过以下步骤得到:获取第二时间段内所述心电单极导联v2的已有临床数据、所述心电单极导联v4的已有临床数据和所述心电单极导联v5的已有临床数据;利用所述第二时间段内的所述心电单极导联v2的已有临床数据、所述心电单极导联v4的已有临床数据和所述心电单极导联v5的已有临床数据,确定所述第二线性回归方程的参数β41、β42、β40的初始的参数值;对所述第二线性回归方程的参数β41、β42、β40的初始参的数值进行归一化处理,得到所述第二线性回归方程的参数β41、β42、β40的最终的参数值。
优选地,所述对所述第一线性回归方程的参数β41、β42、β40的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β41、β42、β40的最终的参数值包括:根据所述第二时间段内所述心电单极导联v2的已有临床数据,确定所述心电单极导联v2的已有临床数据平均值v2amp;根据所述第二时间段内所述心电单极导联v5的已有临床数据,确定所述心电单极导联v5的已有临床数据平均值v5amp;利用所述心电单极导联v2的已有临床数据平均值v2amp和所述心电单极导联v5的已有临床数据平均值v5amp,对所述第一线性回归方程的参数β41、β42、β40的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β41、β42、β40的最终的参数值。
优选地,所述对所述导联v3的推衍数据v′3和所述导联v4的推衍数据v′4分别进行幅值转化处理,得到所述导联v3的合成数据v3和所述导联v4的合成数据v4包括:获取推衍时间段内所述心电单极导联v2的临床数据,并根据所述推衍时间段内的所述心电单极导联v2的临床数据,确定所述推衍时间段内所述心电单极导联v2的临床数据平均值v2amp;获取所述推衍时间段内所述心电单极导联v5的临床数据,并根据所述推衍时间段内的所述心电单极导联v5的临床数据,确定所述推衍时间段内所述心电单极导联v5的临床数据平均值v5amp;利用所述推衍时间段内所述心电单极导联v2的临床数据平均值v2amp和所述心电单极导联v5的临床数据平均值v5amp,对所述推衍时间段内所述导联v3的推衍数据v′3进行幅值转化处理,得到所述导联v3的合成数据v3;利用所述推衍时间段内所述心电单极导联v2的临床数据平均值v2amp和所述心电单极导联v5的临床数据平均值v5amp,对所述推衍时间段内所述导联v4的推衍数据v′4进行幅值转化处理,得到所述导联v4的合成数据v4。
本发明实施例还提供了一种基于心电单极导联v2、v5推衍导联v3、v4的设备,所述设备包括存储器、处理器以及存储在所述存储器上并可在所述处理器上运行的程序,所述程序被所述处理器执行时实现上述的基于心电单极导联v2、v5推衍导联v3、v4的方法的步骤。
本发明提供的一种基于心电单极导联v2、v5推衍导联v3、v4的方法及设备,其通过心电单极导联v2的临床数据v1和心电单极导联v5的临床数据v5,得到导联v3、v4的合成数据,减少了导联电极数量,且合成数据的准确性高。
附图说明
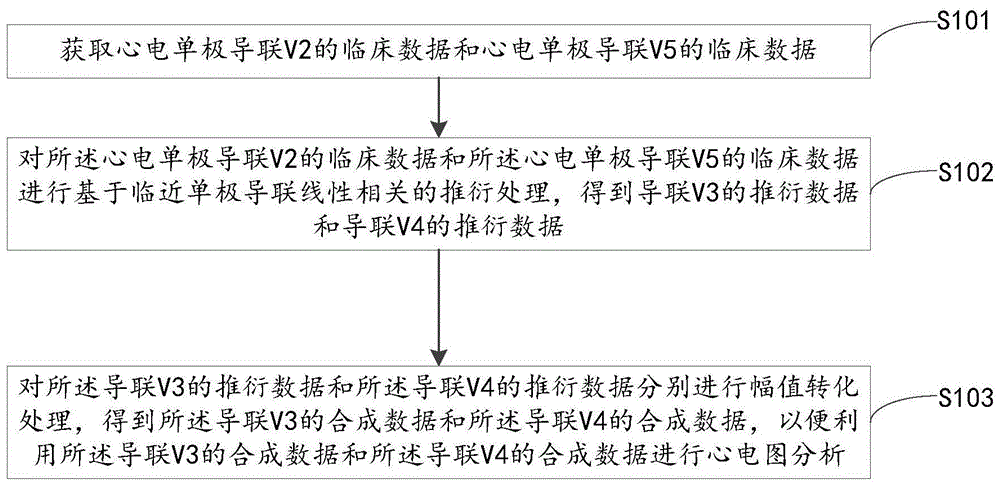
图1是本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的方法的流程图;
图2是本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的详细流程图;
图3a和图3b分别是本发明提供的v2原始数据、v5原始数据对应的波形图以及v3原始数据、v3合成数据对应的波形图;
图4a和图4b分别是本发明提供的v2原始数据、v5原始数据对应的波形图以及v4原始数据、v4合成数据对应的波形图;
图5是本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的设备的结构框图。
具体实施方式
应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
在后续的描述中,使用用于表示元件的诸如“模块”、“部件”或“单元”的后缀仅为了有利于本发明的说明,其本身没有特有的意义。因此,“模块”、“部件”或“单元”可以混合地使用。
图1是本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的方法的流程图,如图1所示,该方法可以包括以下步骤:
步骤s101:获取心电单极导联v2的临床数据v2和心电单极导联v5的临床数据v5。
心电单极导联v2的临床数据v2是安放于胸骨右缘第四肋间的电极采集的心电数据,心电单极导联v5的临床数据v5是安放于左腋前线和v4同一水平的位置电极采集的心电数据,其中,v4对应的电极安放于左锁骨中线与第五肋间相交处。
本发明旨在利用心电单极导联v2的临床数据v2和心电单极导联v5的临床数据v5。准确地推衍出导联v3的数据和导联v4的数据,以下通过步骤s102和步骤s103进行具体说明。
步骤s102:对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行基于临近单极导联线性相关的推衍处理,得到导联v3的推衍数据v′3和导联v4的推衍数据v′4。
具体地,通过以下步骤得到所述导联v3的推衍数据v′3:利用用于推衍所述导联v3的第一线性回归方程,对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行推衍处理,得到所述导联v3的推衍数据v′3,其中,所述第一线性回归方程为v′3=β31*v2+β32*v5+β30,所述β31,β32,β30是所述第一线性回归方程的参数。
上述β31,β32,β30的参数值可以通过以下步骤得到:获取第一时间段内所述心电单极导联v2的已有临床数据、所述心电单极导联v3的已有临床数据和所述心电单极导联v5的已有临床数据;利用所述第一时间段内的所述心电单极导联v2的已有临床数据、所述心电单极导联v3的已有临床数据和所述心电单极导联v5的已有临床数据,确定所述第一线性回归方程的参数β31、β32、β30的初始的参数值;对所述第一线性回归方程的参数β31、β32、β30的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β31、β32、β30的最终的参数值。具体地说,根据所述第一时间段内所述心电单极导联v2的已有临床数据,确定所述心电单极导联v2的已有临床数据平均值v2amp,根据所述第一时间段内所述心电单极导联v5的已有临床数据,确定所述心电单极导联v5的已有临床数据平均值v5amp,然后利用所述心电单极导联v2的已有临床数据平均值v2amp和所述心电单极导联v5的已有临床数据平均值v5amp,对所述第一线性回归方程的参数β31、β32、β30的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β31、β32、β30的最终的参数值,例如,先计算v2amp与v5amp之和的一半,得到调整系数,将参数β31、β32、β30的初始的参数值除以该调整系数,得到参数β31、β32、β30的最终的参数值。
同样地,通过以下步骤得到所述导联v4的推衍数据v′4:利用用于推衍所述导联v4的第二线性回归方程,对所述心电单极导联v2的临床数据v2和所述心电单极导联v5的临床数据v5进行推衍处理,得到所述导联v4的推衍数据v′4,其中,所述第二线性回归方程为v′4=β41*v2+β42*v5+β40,其中,β41,β42,β40是所述第二线性回归方程的参数。
上述β41,β42,β40的参数值可以通过以下步骤得到:获取第二时间段内所述心电单极导联v2的已有临床数据、所述心电单极导联v4的已有临床数据和所述心电单极导联v5的已有临床数据;利用所述第二时间段内的所述心电单极导联v2的已有临床数据、所述心电单极导联v4的已有临床数据和所述心电单极导联v5的已有临床数据,确定所述第二线性回归方程的参数β41、β42、β40的初始的参数值;对所述第二线性回归方程的参数β41、β42、β40的初始参的数值进行归一化处理,得到所述第二线性回归方程的参数β41、β42、β40的最终的参数值。具体地说,根据所述第二时间段内所述心电单极导联v2的已有临床数据,确定所述心电单极导联v2的已有临床数据平均值v2amp,根据所述第二时间段内所述心电单极导联v5的已有临床数据,确定所述心电单极导联v5的已有临床数据平均值v5amp,然后利用所述心电单极导联v2的已有临床数据平均值v2amp和所述心电单极导联v5的已有临床数据平均值v5amp,对所述第一线性回归方程的参数β41、β42、β40的初始的参数值进行归一化处理,得到所述第一线性回归方程的参数β41、β42、β40的最终的参数值。例如,先计算v2amp与v5amp之和的一半,得到调整系数,将参数β41、β42、β40的初始的参数值除以该调整系数,得到参数β31、β32、β30的最终的参数值。
需要指出的是,上述第一时间段和第二时间段可以是同一时间段,也可以是不同时间段。上述心电单极导联v2的已有临床数据、心电单极导联v3的已有临床数据、心电单极导联v4的已有临床数据和心电单极导联v5的已有临床数据为历史数据,用于确定上述各个参数的参数值。确定参数值时,可以利用上述第一/第二时间段的全部数据,确定一组参数值,也可以将上述第一/第二时间段划分成若干个子时间段,然后利用各个子时间段的数据,确定回归效果较好的一组或多组参数值,当存在回归效果较好的多组参数值时,可以选取回归效果最好的一组参数值作为最终参数值,也可以对回归效果较好的多组参数值进行求平均处理,并将参数平均值作为最终参数值。这样,在确定上述各个参数的最终参数值后,基于步骤s101获取的临床数据,通过步骤s102和步骤s103的处理即可得到导联v3的数据和导联v4的数据。
步骤s103:对所述导联v3的推衍数据v′3和所述导联v4的推衍数据v′4分别进行幅值转化处理,得到所述导联v3的合成数据v3和所述导联v4的合成数据v4,以便利用所述导联v3的合成数据v3和所述导联v4的合成数据v4进行心电图分析。
具体地,步骤s103包括:获取推衍时间段内所述心电单极导联v2的临床数据,并根据所述推衍时间段内的所述心电单极导联v2的临床数据,确定所述推衍时间段内所述心电单极导联v2的临床数据平均值v2amp;获取所述推衍时间段内所述心电单极导联v5的临床数据,并根据所述推衍时间段内的所述心电单极导联v5的临床数据,确定所述推衍时间段内所述心电单极导联v5的临床数据平均值v5amp;利用所述推衍时间段内所述心电单极导联v2的临床数据平均值v2amp和所述心电单极导联v5的临床数据平均值v5amp,对所述导联v3的推衍数据v′3进行幅值转化处理,得到所述导联v3的合成数据v3;利用所述推衍时间段内所述心电单极导联v2的临床数据平均值v2amp和所述心电单极导联v5的临床数据平均值v5amp,对所述导联v4的推衍数据v′4进行幅值转化处理,得到所述导联v4的合成数据v4。其中,推衍时间段是需要进行推衍合成的导联v3、v4的数据的时间段。
本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的方法,通过心电单极导联v2的临床数据v2和心电单极导联v5的临床数据v5,得到导联v3、v4的合成数据,减少了导联电极数量,且合成数据的准确性高。
在本领域中,还可以提供一种计算机可读存储介质,该计算机可读存储介质存储有程序,该程序可被处理器执行,以实现上述基于心电单极导联v2、v5推衍导联v3、v4的方法的各个步骤。
图2是本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的详细流程图,如图2所示,推衍导联v3的步骤可以包括:
步骤s201:设线性回归方程。
对心电单极导联v2、v3、v5的数据v2、v″3、v5进行多元线性回归分析,设方程为:
v″3=β1*v2+β2*v5+β0
用最小二乘法计算出公式中对应的β1、β2、β0三个参数;
其中,
步骤s202:对已有的临床数据进行测试,得到多组β1、β2、β0的值,选取其中回归效果较好的几组进行分析。
将利用一组参数值推导出来的心电单极导联v3的数据与实际测试得到的心电单极导联v3的数据比较,若两者相似度高于预设相似度阈值,则认为该组参数值的回归效果较好,可以选取该组参数。实施时,可以将最高相似度对应的一组阈值应用于后续计算步骤,也可以对回归效果较好的几组参数值进行求平均处理,并将平均值应用于后续计算步骤。
步骤s203:因为不同的心电数据的幅值不同,为了计算统一需要对参数进行归一化处理:
β31=β1/((v2amp+v5amp)*0.5)
β32=β2/((v2amp+v5amp)*0.5)
β30=β0/((v2amp+v5amp)*0.5)
v2amp是求参数时对应心电数据v2导联幅值的平均值,v5amp是求参数时对应心电数据v5导联幅值的平均值。
将已测得的参数和数据进行综合分析,得出最终的参数值,例如,得到的最终参数值分别为:β31=0.072;β32=0.107;β30=0.077。
步骤s204:测试数据时,在归一化的方程上乘以一定的倍数。
对待测数据进行幅值转化,即在归一化后的方程上乘以v2和v5导联幅值的平均值相加的一半,具体如下:
v3=(v2amp+v5amp)*0.5*(β31*v2+β32*v5+β30)
其中,v2amp是待测心电数据中v2导联幅值的平均值,v5amp是待测心电数据中v5导联幅值的平均值。
步骤s205:计算出导联v3的最终数据。
即,获取v2和v5,并根据v2和v5,计算v′3=β31*v2+β32*v5+β30,然后乘以(v2amp+v5amp)*0.5,得到导联v3的合成数据v3。
如图3a和图3b所示,心电单极导联v3的原始波形与由心电单极导联v2和v5合成的导联v3的合成波形相似度高,两者基本一致。
推衍导联v4与推衍导联v3的方法基本相同,如图2所示,可以包括如下步骤:
步骤s201:设线性回归方程。
1.对心电单极导联v2、v4和v5的数据v2、v″4、v5进行多元线性回归分析,设方程为:
v″4=β1*v2+β2*v5+β0
用最小二乘法计算出公式中对应的β1、β2、β0三个参数;
其中,
步骤s202:对已有的临床数据进行测试,得到多组β1、β2、β0的值,选取其中回归效果较好的几组进行分析。
将利用一组参数值推导出来的心电单极导联v4的数据与实际测试得到的心电单极导联v4的数据比较,若两者相似度高于预设相似度阈值,则认为该组参数值的回归效果较好,可以选取该组参数。实施时,可以将最高相似度对应的一组阈值应用于后续计算步骤,也可以对回归效果较好的几组参数值进行求平均处理,并将平均值应用于后续计算步骤。
步骤s203:因为不同的心电数据的幅值不同,为了计算统一需要对参数进行归一化处理:
β41=β1/((v2amp+v5amp)*0.5)
β42=β2/((v2amp+v5amp)*0.5)
β40=β0/((v2amp+v5amp)*0.5)
v2amp是求参数时对应心电数据v2导联幅值的平均值,v5amp是求参数时对应心电数据v5导联幅值的平均值。
将已测得的参数和数据进行综合分析,得出最终的参数值,例如,得到的最终参数值分别为:β41=0.019;β42=0.166;β40=0.077。
步骤s204:测试数据时,在归一化的方程上乘以一定的倍数。
对待测数据进行幅值转化,即在归一化后的方程上乘以v2和v5导联幅值的平均值相加的一半,具体如下:
v4=(v2amp+v5amp)*0.5*(β41*v2+β42*v5r+β40)
其中,v2amp是待测心电数据中v2导联幅值的平均值,v5amp是待测心电数据中v5导联幅值的平均值。
步骤s205:计算出导联v4的最终数据。
即,获取v2和v5,并根据v2和v5,计算v′4=β41*v2+β42*v5r+β40,然后乘以(v2amp+v5amp)*0.5,得到导联v4的合成数据v4。
如图4a和图4b所示,心电单极导联v4的原始波形与由心电单极导联v2和v5合成的导联v4的合成波形基本一致。
在现有的心电算法中,所有的推衍导联都是基于双极的,如基于wilson推导的肢体导联,或基于fank的正交心电图的导联,本发明提出了一种基于心电单极导联以及利用临近心电单极导联之间线性相关推衍出对应导联的方法,提高了人体在扭转运动等不同姿态时导联重建的准确性。另外,传统心电图的判别标准都是基于wilson导联体系的,本发明的基于心电单极导联的推衍方法使重建后的波形更加接近wilson导联,便于心电图的判读,同时减少了电极数量。
图5是本发明提供的基于心电单级导联v2、v5推衍导联v3、v4的设备的结构框图,如图5所示,所述设备20包括存储器21、处理器22以及存储在所述存储器21上并可在所述处理器22上运行的程序,所述程序被所述处理器22执行时实现上述的基于心电单级导联v2、v5推衍导联v3、v4的方法的步骤。
本发明提供的基于心电单极导联v2、v5推衍导联v3、v4的设备,通过心电单极导联v2的临床数据v2和心电单极导联v5的临床数据v5,得到导联v3、v4的合成数据,减少了导联电极数量,且合成数据的准确性高。
以上参照附图说明了本发明的优选实施例,并非因此局限本发明的权利范围。本领域技术人员不脱离本发明的范围和实质内所作的任何修改、等同替换和改进,均应在本发明的权利范围之内。
- 还没有人留言评论。精彩留言会获得点赞!