一种用于治疗冠状病毒感染的植物凝集素succ-ConA及应用的制作方法
本发明属于医药技术领域,具体地,涉及一种植物凝集素succ-cona,更具体地,涉及一种用于治疗冠状病毒感染的植物凝集素succ-cona及应用。
背景技术:
新型冠状病毒(2019-ncov)于2020年2月12日被国际病毒分类委员会正式分类命名为严重急性呼吸综合征冠状病毒2(severeacuterespiratorysyndromecoronavirus2,sars-cov-2),世界卫生组织(who)于同日将sars-cov-2导致的疾病正式命名为covid-19。sars-cov-2属于β属冠状病毒,是一种正链rna病毒,其核酸序列与sars-cov有79.5%一致性,而与蝙蝠冠状病毒batcovratg13株的一致性高达96.2%,其与蝙蝠体内检测到的β冠状病毒更为相似,sars-cov-2是感染人类的冠状病毒家族的第七个成员(zhun,zhangd,wangw,etal.anovelcoronavirusfrompatientswithpneumoniainchina,2019[j].newenglandjournalofmedicine,2020.)。
sars-cov-2、sars-cov及mers-cov均属于β属冠状病毒,外覆包膜,因棘突蛋白呈现皇冠状而得名,其基因组为单股、正链rna,大小约30kb,表达4个结构蛋白和数个非结构蛋白,结构蛋白包括表面棘突(s)蛋白、包膜(e)蛋白、膜(m)蛋白、核衣壳(n)蛋白。冠状病毒的细胞内增殖过程主要包括病毒颗粒侵入、病毒rna复制和转录、病毒蛋白翻译、内质网-高尔基体内的病毒组装及病毒颗粒释放。其中,侵入过程包括病毒颗粒与细胞表面受体结合、受体介导的内吞、经内体运输以及蛋白酶依赖的s蛋白裂解,最终导致病毒胞膜与内体膜融合,进而将病毒颗粒释放入胞质中。
sars-cov和sars-cov-2的细胞受体均为ace2,mers-cov的受体为dpp4。虽然sars-cov-2s蛋白中与ace2蛋白结合的5个关键氨基酸中有4个发生了变化,但变化后的氨基酸却没有影响sars-covs蛋白与ace2蛋白互作的构象,与sars-covs蛋白相比,sars-cov-2s蛋白结构与ace2蛋白相互作用能力,由于丢失的少数氢键有所下降,但仍然达到很强的结合自由能,说明sars-cov-2是通过s蛋白与人ace2相互作用机制感染人的呼吸道上皮细胞(xux,chenp,wangj,etal.evolutionofthenovelcoronavirusfromtheongoingwuhanoutbreakandmodelingofitsspikeproteinforriskofhumantransmission[j].sciencechinalifesciences,2020,63(3):457-460.)。
随着冠状病毒的不断传播,其基因组也在不断发生变异,相关研究表明突变株d614g已经在全球范围内广泛流行,到2020年12月,98%以上的序列都含有d614g突变(korberb,fischerwm,gnanakarans,etal.trackingchangesinsars-cov-2spike:evidencethatd614gincreasesinfectivityofthecovid-19virus[j].cell,2020,182(4):812-827.e19.),在n501y突变株的基础上进化出来的英国突变株和南非突变株,目前主要在英国和南非流行,虽然不断有其它国家报道发现了两个突变株,但是还没有在英国和南非之外的区域形成主要流行株,除这些突变株外,还包括一些和其他突变位点联合的突变株,如d614g+i472v、d614g+a435s、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g。
在当前冠状病毒不断发生变异的情况下,开发同时针对sars-cov-2及sars-cov-2突变株、sars-cov、mers-cov冠状病毒毒株的广谱抗病毒药物对于预防和治疗冠状病毒的感染至关重要。
技术实现要素:
本发明的目的是提供一种用于治疗冠状病毒感染的植物凝集素succ-cona及应用。
为了实现上述目的,本发明采用如下技术方案:
根据本发明的一个方面,本发明提供了植物凝集素succ-cona在制备病毒抑制剂中的应用。
进一步,所述病毒为冠状病毒、弹状病毒;
优选地,所述冠状病毒选自hcov-229e、hcov-oc43、hcov-nl63、hcov-hku、sars-cov、mers-cov、sars-cov-2、及其突变株中的任意一种或多种;
更优选地,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及其突变株;
最优选地,所述突变株包括d614g+i472v、d614g+a435s、a222v、k417n、s477n、e484k、n501y、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g、b.1.1.7、b.1.351、p.1;
最优选地,所述突变株为b.1.1.7、b.1.351、p.1;
优选地,所述弹状病毒为水疱性口炎病毒、狂犬病病毒;
更优选地,所述弹状病毒为水疱性口炎病毒。
本发明中所述的“植物凝集素succ-cona”,是指琥珀酰-伴刀豆球蛋白a(succinylatedconcanavalina,succ-cona),是在天然的刀豆球蛋白a(cona)的基础上,对其进行琥珀酰化修饰得到的植物凝集素,succ-cona是活性二聚体(二价)形式,不会重新聚集形成ph5.6以上的四聚体,这种琥珀酰化修饰一定程度上降低了其凝集活性,但保留了其与甘露糖或葡萄糖残基的反应性。
本发明中所述的“水疱性口炎病毒(vesicularstomatitisvirus,vsv)”,是一种弹状病毒科、水疱病毒属的病毒之一,vsv基因组为不分节段的单股负链rna(ssrna)病毒,长约11kb。从3’端到5’端依次排列着n、ns、m、g、l5个不重叠的基因,分别编码核(n)蛋白、磷酸(p)蛋白、基质(m)蛋白、糖(g)蛋白、及rna聚合酶(l)蛋白等5种不同的主要蛋白,vsv在大多数脊椎动物、鸟类、爬行动物、鱼类及昆虫的细胞培养上可以生长,一般来说,vsv属的病毒在感染脊椎动物细胞后,可以很快引起明显的细胞病变。
根据本发明的另一方面,本发明提供了植物凝集素succ-cona在制备用于预防和/或治疗病毒感染的药物组合物中的应用。
进一步,所述病毒为冠状病毒、弹状病毒;
优选地,所述冠状病毒选自hcov-229e、hcov-oc43、hcov-nl63、hcov-hku、sars-cov、mers-cov、sars-cov-2、及其突变株中的任意一种或多种;
更优选地,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及其突变株;
最优选地,所述突变株包括d614g+i472v、d614g+a435s、a222v、k417n、s477n、e484k、n501y、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g、b.1.1.7、b.1.351、p.1;
最优选地,所述突变株为b.1.1.7、b.1.351、p.1;
优选地,所述弹状病毒为水疱性口炎病毒、狂犬病病毒;
更优选地,所述弹状病毒为水疱性口炎病毒。
进一步,本发明还包括植物凝集素succ-cona在制备用于预防和/或治疗病毒感染所致疾病的药物组合物中的应用。
在本发明的实施例中,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及sars-cov-2突变株,所述sars-cov-2突变株优选为b.1.1.7、b.1.351、p.1。
在本发明的实施例中,所述弹状病毒优选为水疱性口炎病毒。
根据本发明的又一方面,本发明提供了一种病毒抑制剂。
进一步,所述抑制剂包含有效量的植物凝集素succ-cona;
进一步,所述抑制剂为冠状病毒、弹状病毒抑制剂;
优选地,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及其突变株;
更优选地,所述突变株包括d614g+i472v、d614g+a435s、a222v、k417n、s477n、e484k、n501y、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g、b.1.1.7、b.1.351、p.1;
最优选地,所述突变株为b.1.1.7、b.1.351、p.1;
优选地,所述弹状病毒为水疱性口炎病毒、狂犬病病毒;
更优选地,所述弹状病毒为水疱性口炎病毒。
根据本发明的又一方面,本发明提供了一种用于预防和/或治疗病毒感染的药物组合物。
进一步,所述药物组合物包含有效量的植物凝集素succ-cona;
优选地,所述病毒为冠状病毒、弹状病毒;
更优选地,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及其突变株;
最优选地,所述突变株包括d614g+i472v、d614g+a435s、a222v、k417n、s477n、e484k、n501y、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g、b.1.1.7、b.1.351、p.1;
最优选地,所述突变株为b.1.1.7、b.1.351、p.1;
更优选地,所述弹状病毒为水疱性口炎病毒、狂犬病病毒;
最优选地,所述弹状病毒为水疱性口炎病毒。
进一步,所述药物组合物还包含药学上可接受的载体和/或辅料;
优选地,所述药物组合物还可包含其他抗病毒的药物和/或化合物;
优选地,所述药物组合物的剂型选自溶液、混悬液、乳剂、浸膏、酏剂、粉剂、颗粒剂、片剂、胶囊中的任意一种。
本发明所述“药学上可接受的载体”,是指本领域认可的并且包括例如参与从身体的一个器官或部分携带或运输任何主题组合物至身体的另一个器官或部分的药学上可接受的材料、组合物或赋形剂,如液体或固体填充剂、稀释剂、溶剂或包囊材料。每种载体必须在与主题组合物的其他成分相容的意义上是“可接受的”并且对患者无害。可以用作药学上可接受的载体的材料的一些例子包括:(1)淀粉,如玉米淀粉和马铃薯淀粉;(2)糖,如乳糖、葡萄糖和蔗糖;(3)麦芽;(4)明胶;(5)滑石粉;(6)纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;(7)粉末状黄蓍胶;(8)可可脂和栓剂蜡;(9)油,如花生油、棉籽油、葵花籽油、芝麻油、橄榄油、玉米油和大豆油;(10)二醇,如丙二醇;(11)多元醇,如甘油、山梨醇、甘露糖醇和聚乙二醇;(12)酯,如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,如氢氧化镁和氢氧化铝;(15)海藻酸;(16)无热原的水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)磷酸盐缓冲液;(21)药物制剂中使用的其他无毒的相容物质。
进一步,本发明所述的药物组合物的施用途径不受限制,只要它能发挥期望的治疗效果或预防效果即可,包括(但不限于):静脉内、腹膜内、眼内、动脉内、肺内、口服、小泡内、肌肉内、气管内、皮下的、通过皮肤、通过胸膜、局部的、吸入、通过粘膜、皮肤、肠胃、关节内、心室内、直肠、阴道、颅骨内、尿道内、肝内、瘤内,在某些情况下,可以系统地给药,在某些情况下可以局部地给药。
进一步,本发明所述的药物组合物的剂量不受限制,只要获得期望的治疗效果或者预防效果即可,可以依据症状、性别、年龄等来恰当的确定,本发明的治疗药物组合物或预防药物组合物的剂量可以使用例如对疾病的治疗效果或者预防效果作为指标来确定。
进一步,本发明所述的药物组合物可以作为医药单独施用或与其它药物一起施用,可以与本发明的药物组合物一起施用的其它药物不受限制,只要它不损害本发明的治疗性或预防性药物组合物的效果即可。
根据本发明的又一方面,本发明提供了前面所述的抑制剂在如下任一方面的应用:
(1)在抑制病毒核酸增殖中的应用;
(2)在抑制病毒进入细胞中的应用;
(3)在制备用于预防和/或治疗病毒感染的药物中的应用;
优选地,所述病毒为冠状病毒、弹状病毒;
更优选地,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及其突变株;
最优选地,所述突变株包括d614g+i472v、d614g+a435s、a222v、k417n、s477n、e484k、n501y、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g、b.1.1.7、b.1.351、p.1;
最优选地,所述突变株为b.1.1.7、b.1.351、p.1;
更优选地,所述弹状病毒为水疱性口炎病毒、狂犬病病毒;
最优选地,所述弹状病毒为水疱性口炎病毒。
本发明中所述的病毒抑制剂具有抑制病毒的作用,因此,其可应用于预防和/或治疗病毒感染的药物制备中,同时也可应用于预防和/或治疗病毒感染所致疾病的药物制备中。
根据本发明的又一方面,本发明提供了前面所述的药物组合物在如下任一方面的应用:
(1)在预防和/或治疗病毒感染中的应用;
(2)在预防和/或治疗病毒感染所致疾病中的应用;
优选地,所述病毒为冠状病毒、弹状病毒;
更优选地,所述冠状病毒为sars-cov、mers-cov、sars-cov-2、及其突变株;
最优选地,所述突变株包括d614g+i472v、d614g+a435s、a222v、k417n、s477n、e484k、n501y、a222v+d614g、k417n+d614g、s477n+d614g、e484k+d614g、n501y+d614g、b.1.1.7、b.1.351、p.1;
最优选地,所述突变株为b.1.1.7、b.1.351、p.1;
更优选地,所述弹状病毒为水疱性口炎病毒、狂犬病病毒;
最优选地,所述弹状病毒为水疱性口炎病毒。
本发明中所述的“治疗”,是本领域公知的,并且包括预防疾病、失调或病症在可能有出现疾病、失调和/或病症的倾向但还没有被诊断患有所述疾病、失调和/或病症的动物中发生;抑制疾病、失调或病症,例如,阻碍其进展;并缓解疾病、失调或病症,例如,引起疾病、失调和/或病症的消退。治疗疾病或病状包括改善特定疾病或病状的至少一种症状,即便基础病理生理学不受影响,如通过施用药剂治疗受试者的神经系统病状如多发性硬化和与氧化应激相关的其他疾病如肾脏疾病,尽管这种药剂不治疗该病状的病因。
相对于现有技术,本发明具有以下有益效果:
本发明首次发现植物凝集素succ-cona同时针对sars-cov-2及sars-cov-2突变株、sars-cov、mers-cov冠状病毒毒株具有广谱抗病毒的作用,可用作广谱抗病毒的制剂或药物活性成分,为预防和治疗冠状病毒的感染提供了新思路,为临床试验的开展提供了理论基础,具有重要的医学研究价值。
附图说明
以下,结合附图来详细说明本发明的实施方案,其中:
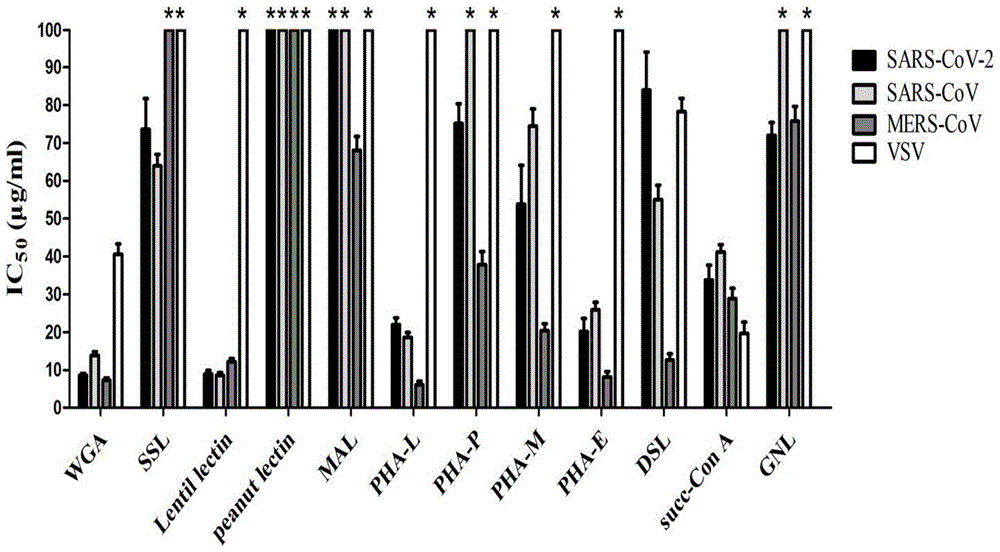
图1是采用假病毒中和实验检测不同的植物凝集素对sars-cov-2、sars-cov、mers-cov和vsv的抗病毒活性的结果统计图;
图2是sars-cov-2s蛋白突变株和流行性突变株对不同的植物凝集素的中和敏感性的结果图;
图3是不同的植物凝集素对3种流行性突变株的抗病毒活性的结果图,其中,a图:b.1.1.7,b图:b.1.351,c图:p.1;
图4是植物凝集素的血细胞凝集活性的实验结果图;
图5是小扁豆凝集素对balb/c小鼠体重增加的影响结果统计图;
图6是小扁豆凝集素在早期阶段抑制sars-cov-2感染的结果图,其中,a图:小扁豆凝集素在处理前后抑制假病毒感染的结果图,b图:cpe抑制实验的结果图;
图7是小扁豆凝集素的碳水化合物特异性及其对sars-cov-2s蛋白的反应结果图,其中,a图:cy3标记的小扁豆凝集素聚糖阵列结果图;b图:l-阿拉伯糖、d-半乳糖、d-葡萄糖、n-乙酰-d-葡萄糖胺(d-glcnac)、甲基α-d-甘露醇苷和d-glcnac与甲基α-d-甘露醇苷的摩尔混合物对小扁豆凝集素中和活性的竞争性抑制结果图,c图:小扁豆凝集素对ace2-s三聚体结合的竞争性抑制结果图;
图8是小扁豆凝集素的碳水化合物特异性及其对sars-cov-2s蛋白的反应结果图,其中,a图:n165的n-聚糖图谱,b图:n234的n-聚糖图谱,c图:n343的n-聚糖图谱,d图:sars-cov-2糖蛋白三聚体(wuhan-hu-1,genbank:mn908947,pdbid6vsb)预融合结构上的代表聚糖n165(紫色)、n234(黄色)和n343(红色),其中一个rbd为“上”构象,另外两个rbd为“下”构象,ace2受体结合位点用淡蓝色表示,e图:n165、n234和n343能与小扁豆凝集素结合的n-聚糖比例的饼状结果图。
具体实施方式
下面结合具体实施例,进一步阐述本发明,仅用于解释本发明,而不能理解为对本发明的限制。本领域的普通技术人员可以理解为:在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照厂商所建议的条件实施检测。
实施例1植物凝集素对sars-cov-2s蛋白结合活性及抗病毒活性的检测
1、实验材料
小扁豆凝集素(lentillectin)、麦胚芽凝集素(wga)、无梗接骨木凝集素(ssl)、花生凝集素(peanutlectin)、怀槐凝集素(mal)均购自于wako(japan);曼陀罗凝集素(dsl)、琥珀酰-伴刀豆球蛋白a(succ-cona)、雪花莲凝集素(gnl)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、来源于红芸豆的植物凝集素-m(pha-m)和植物凝集素-p(pha-p)均购自于sigmaaldrich;hek293细胞表达的sars-cov-2s三聚体购自于acrobiosystems公司(中国,北京);293t细胞由美国典型培养物保藏中心(atcc)提供;huh7细胞由日本研究生物资源保藏中心(jcrb)提供;构建了sars-cov-2spike(wuhan-hu-1,mn908947;hcov-19/southafrica/krisp-k007869/2020,b.1.351,epi_isl_860630;hcov-19/england/qeuh-f56f0f/2021,b.1.1.7,epi_isl_852526;hcov-19/brazil/am-991/2020,p.1,epi_isl_833171)、sars-covspike(genbank:ay278491)、mers-covspike(genbank:afs88936.1)、vsvglycoprotein(genbank:m27165)表达质粒,其中,wuhan-hu-1spike表达质粒用作诱变的模板。
2、假病毒的制备、滴定和抗病毒的分析
首先进行假病毒的制备和滴定,在假病毒制备滴定完成后,采用基于假病毒感染huh7细胞的抗病毒实验进行检测,将100μl系列稀释的凝集素制剂稀释液添加到96孔板中,然后加入50μl假病毒(1300tcid50/ml),并在37℃的条件下孵育1小时。然后,加入100μlhuh7细胞(2×105cells/ml),并在37℃、5%co2的湿化环境中孵育,孵育24小时后进行化学发光检测,采用reed-muench法计算各凝集素的ic50。
3、表面等离子体共振(spr)方法检测凝集素与sars-cov-2s蛋白的结合活性
spr检测在biacoret200仪器(biacore,cytiva)上进行,采用胺偶联法将sars-cov-2s蛋白三聚体固定在cm5芯片的第二流通池上,首先将400mmn-n-(3-二甲基氨基丙基)-碳二亚胺盐酸盐与100mmn-羟基琥珀酰亚胺的1:1混合物激活传感器芯片表面,将s三聚体稀释至25μg/ml的浓度,采用10mm醋酸钠溶液(ph5.0)稀释,并注入活化的表面,用1.0m乙醇胺/盐酸(ph8.5)溶液以10μl/min的速度阻断残留的反应表面封闭7min,达到约1000个响应单元(ru)的固定化水平。采用类似胺偶联剂处理流通池1,但不注射任何配体,作为空白对照。
采用0.01mhepes、0.05%聚山梨酯20、150mmnacl和3mmedta缓冲液对凝集素进行系列稀释,将稀释后的凝集素以30μl/min的速度注入芯片上2min,然后解离150s,用甘氨酸1.5(cytiva)以20μl/min的浓度再生表面30s,以去除结合凝集素。
4、采用sec-mals测定蛋白质的分子量
通过体积排阻色谱法将凝集素流过tskg3000swxl色谱柱(tosohbiosciencellc,kingofprussia,pa,usa),并通过三角光散射检测器(dawn)和示差折光检测器(optilabt-rex,wyatttechnology,santabarbara,california)进行检测,采用astra7进行数据分析,计算蛋白质的分子量(mw)。
5、实验结果
实验结果显示,小扁豆凝集素、麦胚芽凝集素(wga)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、琥珀酰-伴刀豆球蛋白a(succ-cona)对sars-cov-2s蛋白均具有较强的结合活性(见表1),而花生凝集素和怀槐凝集素(mal)对sars-cov-2s蛋白对sars-cov-2s蛋白则没有结合活性;
假病毒中和实验的结果显示,小扁豆凝集素、麦胚芽凝集素(wga)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、琥珀酰-伴刀豆球蛋白a(succ-cona)对sars-cov-2、sars-cov和mers-cov假病毒均具有较强的抑制活性,5种凝集素对sars-cov-2的ic50在8.5~33.8μg/ml之间,其中,小扁豆凝集素和麦胚芽凝集素(wga)对sars-cov-2的抑制活性最强。麦胚芽凝集素(wga)、琥珀酰-伴刀豆球蛋白a(succ-cona)对水疱性口炎病毒vsv也显示出较强的抑制活性,无梗接骨木凝集素(ssl)虽然对sars-cov和sars-cov-2均有一定的抑制作用,但对mers-cov无抑制作用,花生凝集素未表现出病毒抑制作用,怀槐凝集素(mal)对sars-cov-2s蛋白无明显的结合活性,对sars-cov-2也无抗病毒活性,仅对mers-cov有不显著的抗病毒活性(见表1和图1),结果表明了5种植物凝集素(小扁豆凝集素、麦胚芽凝集素(wga)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、琥珀酰-伴刀豆球蛋白a(succ-cona))对sars-cov-2s蛋白具有较强的结合活性,且同时对sars-cov-2、sars-cov、mers-cov均有较强的抗病毒活性。
表1不同的植物凝集素对sars-cov-2的抗病毒活性的结果
实施例2植物凝集素对sars-cov-2s蛋白突变株和sars-cov-2流行性突变株感染的抑制作用检测
本实施例分别检测了各种植物凝集素对sars-cov-2s蛋白突变株和sars-cov-2流行性突变株感染的抑制作用,所述突变株包括英国流行突变株b.1.1.7、南非流行突变株b.1.351、巴西流行突变株p.1、组合突变株d614g+i472v、组合突变株d614g+a435s、a222v、k417n、s477n、e484k、n501y、组合突变株a222v+d614g、组合突变株k417n+d614g、组合突变株s477n+d614g、组合突变株e484k+d614g、组合突变株n501y+d614g等突变株;
凝集素主要针对糖蛋白的糖基部分,在本实施例中,发明人研究了sars-cov-2s蛋白的糖化位点的变化是否会影响其对凝集素的中和敏感性,共构建28个n-连接糖基化位点缺失(22个位点,24个突变体)或o-连接糖基化位点缺失(4个预测位点,4个突变体)的人工突变体。
1、基于假病毒(sars-cov-2s蛋白突变株)的中和敏感性实验
分别检测了28个糖基化突变体以及各种组合突变株对各植物凝集素的敏感性,具体实验方法如下:
采用基于假病毒感染huh7细胞的抗病毒实验进行检测,将100μl系列稀释的凝集素制剂稀释液添加到96孔板中,然后加入50μl假病毒(1300tcid50/ml),并在37℃的条件下孵育1小时。然后,加入100μlhuh7细胞(2×105cells/ml),并在37℃、5%co2的湿化环境中孵育,孵育24小时后进行化学发光检测,采用reed-muench法计算各凝集素的ic50。
2、植物凝集素的抗病毒活性检测实验
分别检测了各种植物凝集素对sars-cov-2流行性突变株b.1.1.7、b.1.351和p.1的抗病毒活性,具体实验方法如下:
采用基于假病毒感染huh7细胞的抗病毒实验进行检测,将100μl系列稀释的凝集素制剂稀释液添加到96孔板中,然后加入50μl假病毒(1300tcid50/ml),并在37℃的条件下孵育1小时。然后,加入100μlhuh7细胞(2×105cells/ml),并在37℃、5%co2的湿化环境中孵育,孵育24小时后进行化学发光检测,采用reed-muench法计算各凝集素的ic50。
3、实验结果
中和敏感性的实验结果显示,小扁豆凝集素对28个糖基化突变体的抗病毒活性(中和敏感性)均未受影响,ic50的倍数变化均在4.0以下(见图2),n122q和n801q对gnl的敏感性降低了4倍,n343q对dsl和gnl的敏感性降低了4倍,而n709q和位于近端膜c端的三个突变(n1098q、n1134q和n1173q)对pha-l、pha-e的敏感性增加了4-10倍,n1098q对wga的敏感性增加了6倍(见图2),表明了5种植物凝集素(小扁豆凝集素、麦胚芽凝集素(wga)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、琥珀酰-伴刀豆球蛋白a(succ-cona))可以对28个糖基化突变体高效中和;
抗病毒活性检测的结果显示,小扁豆凝集素、麦胚芽凝集素(wga)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、琥珀酰-伴刀豆球蛋白a(succ-cona)对流行性突变株b.1.1.7、b.1.351和p.1的抗病毒活性与对sars-cov-2的抗病毒活性相似,均表现出一定的抗病毒活性,其中,小扁豆凝集素和wga对3种流行性突变株的抗病毒活性最强(见图3a-c),进一步证明了5种植物凝集素(小扁豆凝集素、麦胚芽凝集素(wga)、植物凝集素(pha-e)、白细胞凝集素(pha-l)、琥珀酰-伴刀豆球蛋白a(succ-cona))对sars-cov-2及其流行性突变株均具有抗病毒活性。
实施例3植物凝集素的血细胞凝集活性和细胞毒性的检测
由于许多的天然凝集素都会引起血细胞凝集,因此,在本实施例中发明人研究了不同植物凝集素的血细胞凝集活性,并对huh7和293t细胞的细胞毒性进行了研究。
1、植物凝集素的血细胞凝集活性的检测
采用鸡血标本检测植物凝集素的血细胞凝集活性,用pbs洗涤公鸡红细胞,并以1%(v/v)的终浓度重悬,将50μl2倍系列稀释的植物凝集素溶液与等体积的红细胞溶液在96孔圆底板中混合,将流感抗原(b/maryland/15/2016,nibsc-uk-en63qg,nibsc代码:18/104,ha:69μg/ml)进行2倍系列稀释,并作为阳性对照,pbs溶液用作阴性对照,将板在室温条件下孵育1小时,并通过目测确定各种植物凝集素的血细胞凝集活性。
2、植物凝集素的细胞毒性的检测
采用huh7和293t细胞对各种植物凝集素的细胞毒性进行检测,植物凝集素对huh7和293t细胞的细胞毒性活性以cc50(50%细胞毒浓度)表示;
此外,采用balb/c小鼠对小扁豆凝集素在体内的影响进行了验证,在第0天,对小鼠腹膜内注射20mg/kg的小扁豆凝集素(n=6)或pbs(n=6),其中,pbs为阴性对照,并在注射后每天测量小鼠的体重并记录,以balb/c小鼠的体重增加作为机体健康状况的指标。
3、实验结果
血细胞凝集活性检测的实验结果显示,pbs没有显示出任何血凝活性,已知的血凝剂流感血凝剂ha在浓度高于0.03μg/ml时显示出血凝活性,小扁豆凝集素在最高浓度为1mg/ml时才会表现出较弱的凝集活性,琥珀酰-伴刀豆球蛋白a(succ-cona)在1mg/ml时也未表现出血凝活性(见图4),表明了小扁豆凝集素和琥珀酰-伴刀豆球蛋白a(succ-cona)均具有较弱的血凝活性;
细胞毒性检测的实验结果显示,所有的植物凝集素在500μg/ml时均未表现出细胞毒性(见表1),证明了本发明所述的植物凝集素不具有细胞毒性,进一步采用动物实验验证小扁豆凝集素在体内的影响的结果表明,在20mg/kg的注射量下,并未出现balb/c小鼠的体重下降,进一步证明了所述的植物凝集素不具有细胞毒性(见图5)。
实施例4小扁豆凝集素抗sars-cov-2感染的机制研究
为了研究小扁豆凝集素对sars-cov-2感染的抑制作用的机制,本发明对其体外作用模式进行了研究,具体实施方式如下:
1、对小扁豆凝集素的抗病毒活性进行检测
首先用小扁豆凝集素分别对huh7细胞或假病毒进行预处理和后处理,并检测其抗病毒活性。小扁豆凝集素预处理:用系列稀释的凝集素溶液在37℃的条件下与huh7细胞共孵育1h,pbs洗涤5次后(此洗涤步骤也可省略),用sars-cov-2假病毒感染细胞;小扁豆凝集素后处理:将sars-cov-2假病毒分别在37℃的条件下感染huh7细胞0、1、2、4、6、8和24h后,再加入系列稀释的小扁豆凝集素,检测小扁豆凝集素对病毒感染的影响。
2、基于sars-cov-2活病毒的细胞病变抑制实验(cpe抑制实验)
首先将梯度稀释的小扁豆凝集素和100tcid50的sars-cov-2活病毒等体积混合,并在37℃的条件下孵育1小时,然后将混合物转移至铺有veroe6细胞的96孔培养板中,37℃培养3天后,采用显微镜观察细胞的形态和状态,并记录相关数据,根据所得数据计算cpe抑制率,评估小扁豆凝集素对sars-cov-2活病毒的抗病毒作用。
3、聚糖阵列分析
用cy3标记植物凝集素,并用基于假病毒的抗病毒测定实验检测其生物活性,用封闭缓冲液封闭n-glycan微阵列载玻片(creativebiochip,南京,中国)30分钟,然后用pbst(pbs缓冲液,0.05%tween20)洗涤,加入1~8μg/ml凝集素-cy3,37℃孵育2小时,洗涤以去除未结合的凝集素,然后对微阵列载玻片进行扫描和分析。
4、基于spr的ace2竞争性结合测定
小扁豆凝集素对ace2-s三聚体结合的竞争性分析是采用biacoret200系统(biacore,cytiva)在25℃的条件下进行分析的,通过抗人igg(fc)抗体(cat.no.br100530,cytiva)以5μg/ml的浓度将人ace2-hfc标签捕获到s系列传感器芯片cm5的第二个流通池中,注射时间为30s,流速为10μl/min,以产生350ru的响应,在运行缓冲液(1×hepes、0.005%tween-20)中制备400nmsars-cov-2s蛋白的测定溶液,其中含有浓度为0nm、0.5nm、5nm、20nm、50nm的小扁豆凝集素,流速为30μl/min,缔合时间为60s,解离时间为90s,检测对人ace2结合的反应,用3mmgcl2再生人ace2和抗人igg(fc)抗体的表面,结合动力学参数采用
5、实验结果
抗病毒活性检测的实验结果显示,在处理0、1和2h后,以及用小扁豆凝集素预孵育假病毒1h后,观察到小扁豆凝集素对病毒感染性的显著抑制作用(见图6a);用小扁豆凝集素预孵育huh7细胞后,用大量pbs洗涤细胞以清除残留的凝集素,结果显示没有抑制作用,而不使用pbs洗涤的预孵育导致了显著的剂量依赖性的感染抑制作用;随着添加小扁豆凝集素时间的延长,抑制作用逐渐减弱,4h后无病毒抑制,表明了小扁豆凝集素在病毒感染的早期阶段发挥作用,且直接与sars-cov-2的s蛋白反应;
cpe抑制实验的结果显示,与sars-cov-2活病毒预孵育的小扁豆凝集素显示出了较强的抑制作用,ic50为60.26μg/ml(1.2μm)(见图6b),进一步表明了小扁豆凝集素在病毒感染的早期阶段与sars-cov-2直接反应发挥抗病毒的作用;
聚糖阵列分析的结果显示,小扁豆凝集素与两种类型的n糖的结合效果最佳:从man-5到man-9的高甘露糖型n糖,以及非还原端含有glcnac的n糖(见图7a),高甘露糖型man-8和man-9的结合亲和力最高,非还原端含有glcnac的n-聚糖可以是单天线复杂型n-聚糖(n020)、双天线复杂型n-聚糖(n000)或杂合型n-聚糖(n010)。凝集素分别与甲基α-d-甘露醇苷、n-乙酰-d-葡萄糖胺(d-glcnac)和d-葡萄糖孵育后,抑制了小扁豆凝集素的抗病毒活性,其中α-d-甘露醇苷的抑制作用最强(见图7b),表明小扁豆凝集素的抗病毒活性直接依赖于其高甘露糖型/glcnac结合功能;
基于spr的竞争性结合测定的结果显示,50nm的小扁豆凝集素可有效地阻断ace2受体和s三聚体蛋白的结合,从而在病毒感染的早期发挥抗病毒的作用。糖基化位点n165、n234和n343位于s蛋白受体结合位点周围(见图8d),n234的n-聚糖是高甘露糖型,由man-8(53.2%)、man-9(40.3%)、man-7(3.4%)、man-6(1.5%)和man-5(1.5%)组成,在n165和n343中,n-聚糖以复杂型为主,在n165中也发现了约20%的高甘露糖型聚糖man-5和少量的杂合型聚糖(见图8a-c),小扁豆凝集素与各糖基化位点特异性结合聚糖的比例见图8e,n234、n165和n343位点的大多数聚糖可与小扁豆凝集素结合,表明了小扁豆凝集素可与n234、n165和n343位点的n-聚糖结合,并阻断ace2与rbd的结合,从而抑制sars-cov-2感染,发挥抗病毒的作用。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!