一种锰离子-CpG寡核苷酸纳米颗粒的制备方法及应用
一种锰离子
‑
cpg寡核苷酸纳米颗粒的制备方法及应用
技术领域
1.本发明涉及生物医学技术领域,具体涉及一种锰离子
‑
cpg寡核苷酸纳米颗粒的制备方法及应用。
背景技术:
2.锰元素是机体所必需的微量元素之一。最新的研究发现,锰离子可以通过传递病毒入侵的信号来激活固有免疫系统中的各个环节,协助机体抵抗病毒的入侵。在机体固有免疫应答中起到“传令兵”的作用。研究表面,小鼠缺乏锰离子后对于肿瘤的抵抗能力明显减弱,证明锰元素在对肿瘤的免疫监视中具有重要的作用。
3.cpg odn(cpg oligonucleotide,cpg寡脱氧核苷酸)是人工合成的含有非甲基化的胞嘧啶鸟嘌呤二核苷酸(cpg)的寡脱氧核苷酸(odn),可激活多种免疫细胞,促进肿瘤抗原呈递,诱导th1免疫反应,促进抗原特异性抗体的产生和cd8
+
t细胞的细胞毒性。在肿瘤微环境中,cpg odn可激活免疫系统,打破免疫抑制状态,从而抑制肿瘤生长。cpg odn作为单药已在黑色素瘤、胶质母细胞瘤、肾细胞癌、t细胞淋巴瘤等患者中进行了评估,并证明了其抗肿瘤活性。作为单独的治疗药物,cpg odn临床试验全身给药的效果较差,所以目前多为瘤内注射,一定程度上限制了其在实体瘤上的应用。同时对于已建立的肿瘤来说,cpg odn诱导的免疫反应通常不足以完全清除肿瘤,因此,cpg odn与其他疗法联合的治疗方案仍在探索中,特别是联合那些可能削弱肿瘤使其更易受到免疫介导性攻击的疗法。
4.近年来,纳米材料在生命科学领域的研究及应用备受关注。纳米颗粒进入人体和细胞之后,可直接诱导产生多种生物学效应,例如激活机体免疫应答反应、促进细胞凋亡等。由于肿瘤微环境的复杂性,大多数功能性试剂(如小分子化疗药物)递送到肿瘤细胞内的浓度有限,治疗效果也不佳,甚至产生不良副作用和毒性问题。与正常组织血管相比,纳米颗粒在肿瘤血管具有更强的渗透性,会蓄积在肿瘤部位。针对肿瘤微环境特性,构建纳米平台用于癌症诊断和肿瘤治疗被认为是改善癌症治疗的有效方法。基于纳米颗粒的药物载体作为癌症诊断和治疗工具,已被证明可增强抗肿瘤效率并降低副作用。
技术实现要素:
5.针对现有技术的不足,本发明旨在提供一种锰离子
‑
cpg寡核苷酸纳米颗粒的制备方法及应用。
6.为了实现上述目的,本发明采用如下技术方案:
7.一种锰离子
‑
cpg寡核苷酸纳米颗粒的制备方法,包括以下步骤:
8.s1、用去离子水溶解无水氯化锰得到氯化锰溶液待用;
9.s2、用去离子水将cpg寡脱氧核苷酸cpg odn溶解得到cpg odn溶液待用;
10.s3、将步骤s1所配制的氯化锰溶液与步骤s2所配制的cpg odn溶液混合于无菌生理盐水中,振荡混匀,即得到锰离子
‑
cpg寡核苷酸纳米颗粒。
11.进一步地,步骤s1中,所述氯化锰溶液的浓度为100mg/ml。
12.进一步地,步骤s2中,所述cpg odn溶液的浓度为2.5mg/ml。
13.进一步地,步骤s3中,所述无菌生理盐水:氯化锰溶液:cpg odn溶液的体积比例为5:1:4。
14.上述制备方法制备得到的锰离子
‑
cpg寡核苷酸纳米颗粒可应用于制备治疗肿瘤药物。所述肿瘤为肺癌、肝癌、胃癌、结肠癌、乳腺癌、卵巢癌、子宫颈癌、胰腺癌、胆管癌、皮肤癌、恶性黑色素瘤中的一种。
15.本发明的有益效果在于:相比于单独使用氯化锰或cpg odn,本发明方法制备得到的锰离子
‑
cpg寡核苷酸纳米颗粒能够显著的促进肿瘤细胞坏死,抑制肿瘤细胞的生长,同时能够使脾脏中nkt细胞的数量增加,使脾脏中cd4
+
t、cd8
+
t细胞的增殖能力显著增强,显示出了良好的抗肿瘤作用。并且,该纳米颗粒的原料成本较低,且制备工艺简单,生物安全性较高。在肿瘤免疫治疗中有良好的应用前景。
附图说明
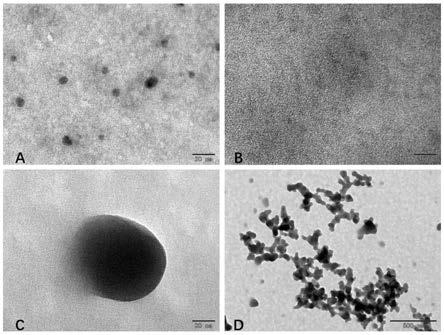
16.图1为本发明实施例1中的透射电镜扫描图片,其中a是氯化锰的透射电镜成像图,b是cpg寡核苷酸的透射电镜成像图,c是20纳米的锰离子
‑
cpg寡核苷酸纳米颗粒的透射电镜成像图,d是500纳米的锰离子
‑
cpg寡核苷酸纳米颗粒的透射电镜成像图。
17.图2为本发明实施例2中给予c57/b6小鼠接种llc(小鼠肺癌细胞)后分别经pbs(对照组)、mncl2、cpg以及锰离子
‑
cpg寡核苷酸纳米颗粒治疗后的小鼠肿瘤生长曲线示意图;
18.图3为本发明实施例2中在给予c57/b6小鼠接种llc(小鼠肺癌细胞)后分别经pbs(对照组)、mncl2、cpg以及锰离子
‑
cpg寡核苷酸纳米颗粒治疗后25天,摘取小鼠肿瘤后观察其重量变化。
19.图4为本发明实施例2中在给予c57/b6小鼠接种llc(小鼠肺癌细胞)后分别经pbs(对照组)、mncl2、cpg以及锰离子
‑
cpg寡核苷酸纳米颗粒治疗后25天,摘取小鼠肿瘤的图片;
20.图5为本发明实施例3中给予c57/b6小鼠接种llc(小鼠肺癌细胞)后分别经pbs(对照组)、mncl2、cpg以及锰离子
‑
cpg寡核苷酸纳米颗粒治疗后25天,分析小鼠脾脏中cd4
+
t细胞、cd8
+
t细胞的增殖能力变化。
21.图6为本发明实施例3中给予c57/b6小鼠接种llc(小鼠肺癌细胞)后分别经pbs(对照组)、mncl2、cpg以及锰离子
‑
cpg寡核苷酸纳米颗粒治疗后25天,分析小鼠脾脏中nkt细胞的变化。
22.图7为本发明实施例3中给予c57/b6小鼠接种llc(小鼠肺癌细胞)后分别经pbs(对照组)、mncl2、cpg以及锰离子
‑
cpg寡核苷酸纳米颗粒治疗后25天,分析小鼠脾脏中cd4
+
t细胞、cd8
+
t细胞的增殖能力以及nkt细胞变化的统计图。
具体实施方式
23.以下将结合附图对本发明作进一步的描述,需要说明的是,本实施例以本技术方案为前提,给出了详细的实施方式和具体的操作过程,但本发明的保护范围并不限于本实施例。
24.实施例1
25.本实施例提供一种锰离子
‑
cpg寡核苷酸纳米颗粒的制备方法,包括以下步骤:
26.s1、用去离子水溶解无水氯化锰得到100mg/ml的氯化锰溶液待用;氯化锰的透射电镜成像图如图1中的a所示。
27.s2、用去离子水将cpg寡脱氧核苷酸(cpg odn)溶解得到2.5mg/ml的cpg odn溶液待用;cpg寡核苷酸的透射电镜成像图如图1中的b所示。
28.在本实施例中,cpg寡脱氧核苷酸由苏州泓迅生物科技股份有限公司合成,所述cpg寡脱氧核苷酸的序列如表1所示。
29.表1
30.primer namesequence(5
’→3′
)cpg odn 1826t*c*c*a*t**g*a*c*g*t*t*c*c*t*g*a*c*g*t*t
31.s3、将步骤s1所配制的氯化锰溶液与步骤s2所配制的cpg odn溶液混合于无菌生理盐水中,振荡混匀,即得到锰离子
‑
cpg寡核苷酸纳米颗粒。在本实施例中,所述无菌生理盐水∶氯化锰溶液∶cpg odn溶液的体积比例为5∶1∶4。
32.所得到的锰离子
‑
cpg寡核苷酸纳米颗粒的透射电镜成像如图1中的c、d所示,其中图1的c为20纳米图像,d为500纳米图像。
33.实施例2
34.本实施例通过实验对实施例1所制得的锰离子
‑
cpg寡核苷酸纳米颗粒的抗肿瘤作用进行研究,具体操作过程如下:
35.在给予c57/b6小鼠腹股沟接种llc(小鼠肺癌细胞,5*105/只)后,将实施例1制得的锰离子
‑
cpg寡核苷酸纳米颗粒对小鼠进行滴鼻免疫。动态监测小鼠肿瘤体积变化情况,结果表明,与分别给与mncl2、cpg odn滴鼻免疫的小鼠相比,接受锰离子
‑
cpg寡核苷酸纳米颗粒滴鼻免疫的小鼠体内的肿瘤体积更小,如图2、图4所示。在接种肿瘤细胞25天以后取出肿瘤组织进行称重,同样发现接受锰离子
‑
cpg寡核苷酸纳米颗粒滴鼻免疫的小鼠体内的肿瘤更轻,如图3所示。这说明,通过锰离子
‑
cpg寡核苷酸纳米颗粒治疗,能够更好的抑制肿瘤细胞的生长来发挥抗肿瘤作用。
36.实施例3
37.本实施例通过实验研究锰离子
‑
cpg寡核苷酸纳米颗粒对体内免疫细胞的影响,具体操作过程如下:
38.将接种llc的c57/b6小鼠在接种25天后处死,取出脾脏后将其放入含有ⅳ型胶原酶的6孔板中;用剪刀将脾脏剪碎后放入37℃细胞培养箱消化40min;40min后加macs buffer使其消化终止;然后将40μm的筛网放在离心管上,将组织及所有液体经筛网转移至离心管中,在此过程中用注射器针芯平头不断研磨组织,研磨时要用macs buffer反复冲洗。之后将离心管放入离心机用1800r/min,4℃离心5min;离心后弃上清,然后加入2ml的红细胞裂解液,室温放置2min;2min后加入20ml的macs buffer来终止反应,继续放入离心机用1800r/min,4℃离心5min;弃上清后加2ml macs buffer重悬细胞,用30μm滤网过滤至离心管中制成单细胞悬液,用台盼蓝染色测细胞活力并对细胞进行计数;放入离心机用1800r/min,4℃离心5min;弃上清后根据计数结果及实验需要将制好的单细胞悬液定容至合适的体积。
39.将脾脏单细胞悬液根据细胞数(细胞数约为5
×
106个,定容100μl/孔)加入96孔圆
底板;每孔按照体积1:100的比例加入2.4g2封闭液1μl,封闭5min后每孔加200μl的macs buffer,放入离心机用1800r/min,4℃离心2min;弃上清后,按照每种抗体浓度加入适当比例的荧光抗体,避光反应15min;之后每孔加200μl的macs buffer,放入离心机用1800r/min,4℃离心2min;弃上清后,每孔加入100μl的a700染液染死细胞,避光反应15min;之后每孔加200μl的macs buffer,放入离心机用1800r/min,4℃离心2min;弃上清后,每孔用200μl的macs buffer重悬细胞,之后用流式细胞仪上机检测。可以发现,如图7所示,锰离子
‑
cpg寡核苷酸纳米颗粒治疗能够使脾脏中的nkt细胞的数量增加(图6),且能够更好的促进脾脏中cd4
+
t细胞和cd8
+
t细胞的增殖(图5)来发挥抗肿瘤作用。
40.对于本领域的技术人员来说,可以根据以上的技术方案和构思,给出各种相应的改变和变形,而所有的这些改变和变形,都应该包括在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1