一种藜麦提取物的组合物及其制备方法和用途与流程
本发明属于天然药物技术领域,具体涉及一种藜麦提取物的组合物及其制备方法和用途,以及含有该藜麦提取物的组合物的药物组合物。
背景技术:
对肿瘤患者进行化疗虽然能够产生一定的疗效,但是化疗后大部分患者会出现不同程度的副作用。化疗相关性腹泻就是近代临床医学治疗所派生的副产物,严重影响化疗的进程。临床上引起化疗相关性腹泻的常见药物有5-氟尿嘧啶、伊立替康、希罗达、托泊替康等,其中5-氟尿嘧啶和伊立替康联合用药时,有50%-80%的患者出现该症状,超过30%的患者引起iii至iv级的腹泻。然而目前国际上对于化疗相关性腹泻尚无满意的治疗方案,主要以对症处理为主,包括(1)使用止泻药以减少胃肠道蠕动,常用药物有易蒙停、复方苯乙哌啶、颠茄西丁等;使用思密达以提高粘膜屏障对攻击因子的防御作用;(2)抗感染治疗,主要针对大肠杆菌感染,可选用氨基糖苷类、喹诺酮类药物;(3)进食高蛋白、高热量、低残渣食物,避免对胃肠道有刺激的饮食;(4)补充足够的营养,维持水及电解质平衡,尤其要防止低钾血症的发生;(5)最近认为奥曲肽对控制化疗相关性重度腹泻和类癌综合征相关的腹泻有效。
化疗药物如5-fu为一种嘧啶类氟化物,是临床恶性肿瘤(如结肠癌和乳腺癌)的常用化疗抗代谢药物,在细胞内转化为有效的氟尿嘧啶脱氧核苷酸后,通过阻断脱氧核糖尿苷酸被细胞内胸苷酸合成酶转化为胸苷酸,从而干扰dna的合成。然而5-fu在体内被磷酸化为5-fdump或者5-fump后,对增殖的小肠细胞较敏感,能导致小肠粘膜损伤,并干扰肠细胞分裂,引起肠壁细胞坏死及肠壁的广泛炎症,造成吸收和分泌细胞数量之间的平衡发生变化,从而导致腹泻。5-fu具有的显著毒性限制了它的使用剂量,引起了许多副反应并威胁着化疗的有效性。其中约50%-80%的病人使用5-fu引起肠粘膜炎,导致胃肠道溃疡,而出现腹胀、呕吐和腹泻的临床反应。
以食品为原料开发对化疗相关性腹泻有治疗作用的产品目前尚属空白。藜麦(chenopodiumquinoawilld.)富含多种营养成分,包括蛋白质、脂肪、维生素以及微量元素等,其营养价值超过任何一种传统的粮食作物,是联合国粮农组织(fao)推荐的唯一单体植物即可满足人体基本营养需求的完美全营养食品。藜麦所含氨基酸种类丰富,含有人类必须的9种必须氨基酸,有利于人体蛋白质的吸收利用,同时还含有许多非必须氨基酸,特别是富含多数作物没有的赖氨酸。藜麦已被美国国家研究委员会和美国国家航空航天局评估为一种极富营养特性的食物,将其列为人类未来移民外太空的理想“太空粮食”。我国藜麦发展时间较晚,于2008年开始藜麦的规模化种植,目前在山西、甘肃、青海等地区推广种植,目前我国市面上还鲜有成熟的藜麦相关产品。藜麦作为一种营养价值突出的功能性健康食品,不仅富含多酚、黄酮、皂苷、多糖、多肽、蜕皮激素等活性成分,还含有丰富的维生素、必需氨基酸、矿物质(k、p、mg、ca、zn、fe)等营养物质,具有均衡补充营养、增强机体功能等生理活性。
技术实现要素:
本发明的目的是针对目前临床上缺少针对化疗相关性腹泻的满意治疗方案的问题,提供一种治疗化疗相关性腹泻的藜麦提取物的组合物及其制备方法、用途和药物组合物,从而能够有效地治疗由于抗肿瘤的化疗所引发的腹泻,以及降低化疗药物对胃肠道的毒副作用。
本发明的目的是通过以下技术方案实现的:
一方面,本发明提供了一种藜麦提取物的组合物,其包含重量比为1:10到10:1的藜麦总皂苷和藜麦总多糖。优选地,所述藜麦总皂苷与藜麦总多糖的重量比为1:5到5:1;更优选地,所述藜麦总皂苷与所述藜麦总多糖的重量比为1:1。
优选地,所述藜麦总皂苷主要包含:藜麦皂苷1~9、齐墩果-油酸-葡萄吡喃糖苷、脱氧美商陆酸吡喃葡萄糖酯、常春藤皂苷等;所述藜麦总多糖主要包含淀粉类多糖和非淀粉类多糖;所述非淀粉类多糖主要包含纤维素、半纤维素多糖和果胶聚糖;所述纤维素由半乳糖醛酸、半乳糖、木糖和葡萄糖组成。
另一方面,本发明还提供了所述藜麦提取物的组合物的制备方法,其包括以下步骤:
(1)将藜麦用水加热提取,得到藜麦水提取液;
(2)将藜麦水提取液上样至大孔吸附树脂进行吸附,先用水洗脱,收集水洗脱液,除去水得到藜麦总多糖;再用乙醇水溶液洗脱,收集乙醇水溶液洗脱液,除去乙醇和水得到藜麦总皂苷;
(3)将藜麦总多糖和藜麦总皂苷混合。
在上述制备方法的步骤(1)中,优选地,所述水加热提取的条件为:藜麦与水的体积比为1:10-1:15,优选为1:12;提取时间为15-30min,优选20min;提取次数为1-3次,优选2次。
在上述制备方法的步骤(2)中,优选地,所述上样的流速为1-3bv/h,优选为2bv/h。
在上述制备方法的步骤(2)中,优选地,收集的水洗脱液的体积为柱体积的2-4倍,优选为3倍。
在上述制备方法的步骤(2)中,优选地,所述乙醇水溶液的浓度按体积比计为70-95%,优选为75-90%,最优选为90%。
在上述制备方法的步骤(2)中,优选地,收集的乙醇水洗脱液的体积为柱体积的2-4倍,优选为3倍。
进一步优选地,上述制备方法包括以下步骤:
(1)将藜麦用水加热提取,得到藜麦水提取液,过滤,离心并浓缩,得到藜麦浓缩液;
(2)将藜麦浓缩液上样至大孔吸附树脂进行吸附,先用水洗脱,收集水洗脱液,经浓缩和干燥除去水得到藜麦总多糖;再用乙醇水溶液洗脱,收集乙醇水溶液洗脱液,经浓缩并干燥除去乙醇和水得到藜麦总皂苷;其中所述大孔吸附树脂可以选自ab-8、d101、dm130、hpd100、hpd300、hpd450、hpd600、hpd826或nka-9中的一种或多种。
(3)将藜麦总多糖和藜麦总皂苷混合。
在上述制备方法的步骤(1)中,优选地,所述离心的转速为6000-10000rpm/min,优选为8000rpm/min;离心时间为3-8min,优选为5min。
在上述制备方法的步骤(1)中,优选地,所述浓缩的料液比为1:1-1:4(g/ml),优选为1:2(g/ml)。
根据本发明的一个具体实施方案,所述制备方法包括以下步骤:
(1)将藜麦与蒸馏水按体积比1:12混合加热至沸,保持微沸状态提取20min,提取2次,合并提取液,冷却后滤除滤渣,以8000rpm/min离心5min,取上清,浓缩至料液比1:2(g/ml),得到藜麦浓缩液;
(2)将藜麦浓缩液上样至大孔吸附树脂进行吸附,上样流速为2bv/h,上样结束后先用蒸馏水洗脱,收集3倍柱体积的蒸馏水洗脱液,旋转蒸发浓缩成浸膏后真空干燥除去水得到藜麦总多糖粉末;再用体积比为90%的乙醇水溶液进行洗脱,收集3倍柱体积的乙醇水溶液洗脱液,旋转蒸发浓缩成浸膏后真空干燥得到藜麦总皂苷粉末。
(3)将藜麦总多糖和藜麦总皂苷混合。
再一方面,本发明提供了一种用于治疗化疗相关性腹泻的药物组合物,其包含所述藜麦提取物的组合物。
优选地,本发明的用于治疗化疗相关性腹泻的药物组合物为包含100-350mg所述藜麦提取物的组合物的单位制剂。
本发明还提供了一种用于抗肿瘤的药物组合物,其包含所述藜麦提取物的组合物和抗肿瘤药物。
优选地,所述抗肿瘤药物选自5-氟尿嘧啶、紫衫烷类、羟基喜树碱、伊立替康、卡培他滨和/或托泊替康中的一种或多种,更优选为5-氟尿嘧啶。
优选地,所述藜麦提取物的组合物与抗肿瘤药物的重量之比为1:1。
优选地,本发明的药物组合物还包含药学上可接受的载体、稀释剂和/或赋形剂。进一步优选地,所述药学上可接受的载体、稀释剂和/或赋形剂选自淀粉、微晶纤维素、乳糖、蔗糖、糖粉、糊精、纤维素衍生物、羧甲基淀粉钠、低取代羟丙基纤维素、硬脂酸及其盐或滑石粉中的一种或多种。
优选地,本发明的药物组合物为口服制剂;更优选地,所述药物组合物为片剂、胶囊剂、滴丸剂、缓释制剂或控释制剂;进一步优选地,所述药物组合物为片剂或胶囊剂。
又一方面,本发明提供了所述藜麦提取物的组合物或所述用于治疗化疗相关性腹泻药物组合物在制备用于治疗化疗相关性腹泻的药物中的用途。优选地,所述化疗相关性腹泻是肿瘤患者在化疗期间所产生的相关性腹泻;更优选地,所述化疗相关性腹泻是由5-氟尿嘧啶、紫衫烷类、羟基喜树碱、伊立替康、卡培他滨和/或托泊替康引起的肿瘤患者在化疗期间所产生的相关性腹泻。
本发明还提供了所述用于抗肿瘤的药物组合物在制备用于治疗肿瘤的药物中的用途。优选地,所述肿瘤选自肠癌、胃癌、肝癌、胰腺癌、食管癌,更优选为结肠癌。
与现有技术相比,本发明提供的藜麦提取物的组合物及其药物组合物具有以下优点:
1.本发明的藜麦提取物的组合物在5-fu导致的小鼠腹泻模型中的研究结果表明:其对于5-fu所致的小鼠腹泻有明显的对抗作用。
2.本发明的藜麦提取物的组合物能增强化疗药物对肿瘤的抑制作用,在小鼠肿瘤模型中观察到其与5-fu联合应用后产生协同抗肿瘤作用,显著抑制肿瘤生长。
3.本发明人首次将藜麦总皂苷及藜麦总多糖按照一定比例进行混合,并通过大量实验明确了两种组分之间的最佳用量配比,使该组合物发挥了更好的协同作用。
4.本发明的组合物中的藜麦总皂苷和藜麦总多糖可以通过常规的技术手段获得,具有操作获得方便、成本较低的特点。
附图说明
以下,结合附图来详细说明本发明的实施方案,其中:
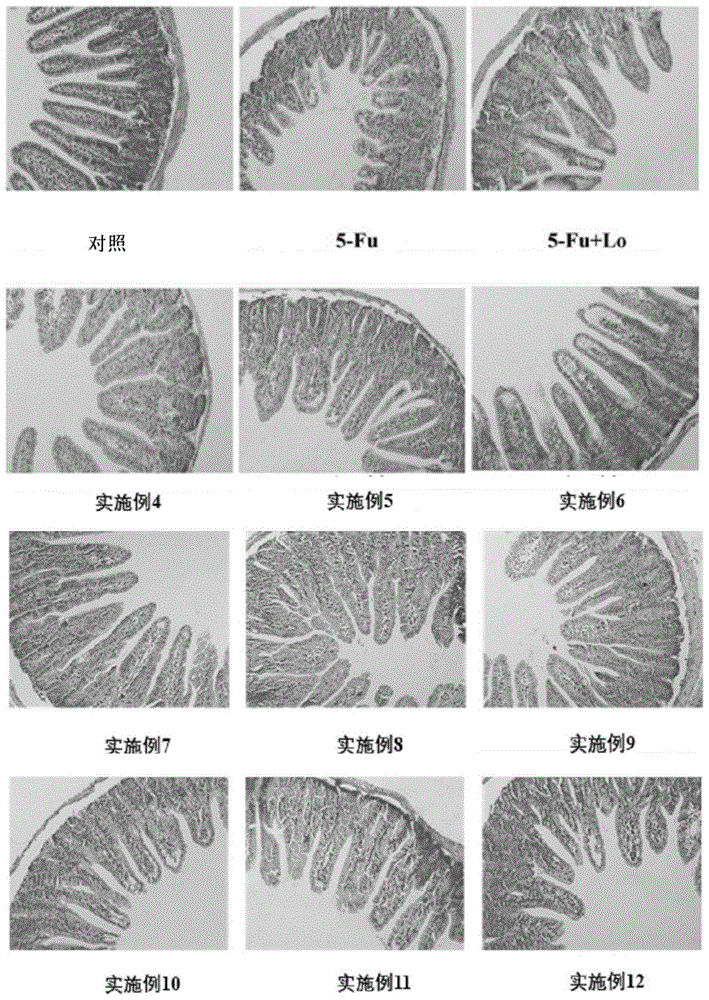
图1显示了组合物实施例4-12、盐酸洛哌丁胺给药后化疗药(5-fu)所致的肠粘膜损伤模型的病理切片h&e染色结果(100×)。
图2显示组合物与5-fu联合对ct-26结肠癌小鼠的肿瘤生长具有协同抑制作用。
具体实施方式
下面结合具体实施例对本发明作进一步的说明,本发明的实施例及试验例是为了使本领域的技术人员能够更好地理解本发明,但并不对本发明作任何限制。下面通过实施例进一步阐述本发明的组合物及其制备,以及其在抗化疗相关性腹泻和抗肿瘤中的实验效果。
实施例1
(1)藜麦前处理:取藜麦与蒸馏水按体积比1:10混合加热至沸,保持微沸状态提取15min,提取2次,合并提取液,冷却后滤除滤渣,离心(8000rpm/min,5min),取上清,浓缩至料液比1:1(g/ml),得藜麦浓缩液。
(2)藜麦浓缩液以大孔吸附树脂进行纯化,上样流速为2bv/h,上样结束后用蒸馏水洗脱,收集2倍蒸馏水洗脱液,旋转蒸发浓缩成浸膏后真空干燥得粉末,即为藜麦总多糖;再用75%(体积比)乙醇水溶液进行洗脱,收集2倍乙醇水溶液洗脱液,旋转蒸发浓缩成浸膏后真空干燥得粉末,即为藜麦总皂苷。
实施例2
(1)藜麦前处理:取藜麦与蒸馏水按体积比1:12混合加热至沸,保持微沸状态提取25min,提取2次,合并提取液,冷却后滤除滤渣,离心(8000rpm/min,5min),取上清,浓缩至料液比1:2(g/ml),得藜麦浓缩液。
(2)藜麦浓缩液以大孔吸附树脂进行纯化,上样流速为2bv/h,上样结束后用蒸馏水洗脱,收集3倍蒸馏水洗脱液,旋转蒸发浓缩成浸膏后真空干燥得粉末,即为藜麦总多糖;再用85%(体积比)乙醇水溶液进行洗脱,收集3倍乙醇水溶液洗脱液,旋转蒸发浓缩成浸膏后真空干燥得粉末,即为藜麦总皂苷。
实施例3
(1)藜麦前处理:取藜麦与蒸馏水按体积比1:10混合加热至沸,保持微沸状态提取15min,提取2次,合并提取液,冷却后滤除滤渣,离心(8000rpm/min,5min),取上清,浓缩至料液比1:4(g/ml),得藜麦浓缩液。
(2)藜麦浓缩液以大孔吸附树脂进行纯化,上样流速为2bv/h,上样结束后用蒸馏水洗脱,收集4倍蒸馏水洗脱液,旋转蒸发浓缩成浸膏后真空干燥得粉末,即为藜麦总多糖;再用95%(体积比)乙醇水溶液进行洗脱,收集4倍乙醇水溶液洗脱液,旋转蒸发浓缩成浸膏后真空干燥得粉末,即为藜麦总皂苷。
实施例4
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖1份、实施例1制备的藜麦总皂苷5份组成。
实施例5
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖1份、实施例2制备的藜麦总皂苷5份组成。
实施例6
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖1份、实施例3制备的藜麦总皂苷5份组成。
实施例7
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖5份、实施例1制备的藜麦总皂苷1份组成。
实施例8
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖5份、实施例2制备的藜麦总皂苷1份组成。
实施例9
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖5份、实施例3制备的藜麦总皂苷1份组成。
实施例10
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖1份、实施例1制备的藜麦总皂苷1份组成。
实施例11
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖1份、实施例2制备的藜麦总皂苷1份组成。
实施例12
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖1份、实施例3制备的藜麦总皂苷1份组成。
实施例13
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖5份、实施例1制备的藜麦总皂苷0份组成。
实施例14
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖5份、实施例2制备的藜麦总皂苷0份组成。
实施例15
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖5份、实施例3制备的藜麦总皂苷0份组成。
实施例16
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖0份、实施例1制备的藜麦总皂苷5份组成。
实施例17
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖0份、实施例2制备的藜麦总皂苷5份组成。
实施例18
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖0份、实施例3制备的藜麦总皂苷5份组成。
实施例19
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖8份、实施例1制备的藜麦总皂苷1份组成。
实施例20
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖8份、实施例2制备的藜麦总皂苷1份组成。
实施例21
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖8份、实施例3制备的藜麦总皂苷1份组成。
实施例22
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖1份、实施例1制备的藜麦总皂苷8份组成。
实施例23
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖1份、实施例2制备的藜麦总皂苷8份组成。
实施例24
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖1份、实施例3制备的藜麦总皂苷8份组成。
实施例25
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖10份、实施例1制备的藜麦总皂苷1份组成。
实施例26
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖10份、实施例2制备的藜麦总皂苷1份组成。
实施例27
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖10份、实施例3制备的藜麦总皂苷1份组成。
实施例28
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例1制备的藜麦总多糖1份、实施例1制备的藜麦总皂苷10份组成。
实施例29
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例2制备的藜麦总多糖1份、实施例2制备的藜麦总皂苷10份组成。
实施例30
一种治疗化疗相关性腹泻的藜麦提取物组合物,按重量份计由实施例3制备的藜麦总多糖1份、实施例3制备的藜麦总皂苷10份组成。
药效学评价
在下述试验例中,组合物为不同重量比的藜麦总皂苷及藜麦总多糖的混合物。本发明人对上述两种成分用量比例在1:10-10:1之间的多种配伍比例的组合物进行化疗相关性腹泻的治疗效果的评价,发现在本发明的用量比例范围内的组合物能够获得良好的协同作用,其中上述两种成分用量比例在1:5-5:1之间的组合物的效果最佳。以下为各实施例的组合物获得的药效学试验结果。
试验例1
1.试验材料
试验动物
健康昆明种小鼠,体重18g-22g,雌雄各半,由中国医学科学院放射医学研究所实验动物中心提供并饲养,二级清洁,许可证号:scxh(军)2012-0004,动物合格证编号:0042643。
试验仪器
低温冰箱(sanyoultralow,日本sanyo公司);低温离心机(labofuge400r,德国heraeus公司);微量移液器(美国dragonlab公司);leicatp1020脱水机(德国);leicarm2016轮转式切片机(德国)。
中性福尔马林固定液及pbs的配制
中性福尔马林:40%甲醛100ml,酸性磷酸钠(或无水磷酸二氢钾)4.0g,磷酸氢二钠6.5g,蒸馏水900ml加入容量瓶中封存。
2.试验方法
2.1试验动物及分组
雄性昆明小鼠常规适应性饲养一周,按体重分层完全随机分组。空白组(对照)、多次模型组(模型)、阳性对照盐酸洛哌丁胺组(洛哌丁胺)、组合物实施例4-30,每组16只各组同时进入实验。采用苦味酸标记动物。
2.2试验动物腹腔注射和灌胃
空白组腹腔注射生理盐水1ml/kg,d1-4天,其余各组小鼠每天上午腹腔注射5-fu60mg/kg1-4天,阳性对照组和lm组在注射5-fu前,分别灌胃给药盐酸洛哌丁胺组(4mg/kg)、组合物实施例4-30。空白组和模型组组灌胃给予0.5%羧甲基纤维素钠(1ml/kg)。
2.3试验动物取材
实验第6天分别对每组各16只动物进行取材。处死小鼠,解剖,迅速取一段回肠,浸泡于10%中性福尔马林液中固定,石蜡包埋,常规制片,h&e染色,光镜下观察肝组织形态学变化。
2.4组合物对化疗相关性腹泻模型小鼠胃排空和肠推进的影响
取小鼠雌雄各半,随机分组,空白组(对照)、5-fu模型组(模型)、阳性对照盐酸洛哌丁胺组(洛哌丁胺)、组合物实施例4-30。每组12只,各组同时进入实验。采用苦味酸标记动物。连续给药6天,末次给药前禁食24h,末次给药后30min,除空白组外其余各组分别腹腔注射5-fu300mg/kg,15min后,各组灌胃给药0.05%酚红溶液0.3ml/只,20min后,颈椎脱颈法处死,取贲门至直肠末端胃肠,自幽门括约肌处取胃,将其放入25ml0.1mol/lnaoh溶液中切碎搅匀,室温下静置1h,取4ml的上清液加入0.5ml33%三氯乙酸除去蛋白,1600g30min离心,上清液中加入1ml2mol/lnaoh溶液,在560nm处测吸光度(a值)为胃内酚红的残留量,并另外取6只小鼠,给予0.05%的酚红后立即处死,取胃,测其吸光度为酚红的基准吸光度。
胃排空率%=(1-a胃内酚红/a基准酚红)×100%。
取出小肠分离肠系膜,剪取幽门至回盲肠部的肠管,置于托盘上,轻轻将小肠拉成直线,测量酚红前进的距离。
小肠推进率%=酚红前进的距离/小肠的全长×100%。
2.5观察指标
2.5.1小鼠体重
每天上午用电子称对小鼠进行体重测量并记录。
2.5.2腹泻情况
每天记录小鼠粪便数,观察小鼠皮肤被粪便污染程度并对腹泻情况进行评分。腹泻评分标准:正常粪便0分;软便1分;湿便2分;湿便,肛门周围轻度沾染3分;湿便,肛门周围中度或严重沾染4分。
2.5.3小鼠回肠组织病理形态学--h&e染色
取小鼠下回肠约5cm;将所取小肠组织置于甲醛固定液中固定48h,甲醛液不少于标本的10倍体积;固定期间,不断轻轻摇动容器,以利于固定液渗入;小肠组织固定48小时后,弃掉固定液并取出组织;剪裁至长度为1cm左右,放进包埋框,先用pbs冲洗去掉未与组织结合的固定液和沉淀物;再将已固定的组织经脱水机进行脱水,脱水程序设定依次为:70%乙醇3h,80%乙醇2h,95%乙醇i50min,95%乙醇ii50min,无水乙醇i50min,无水乙醇ii50min,二甲苯:乙醇(1:1)20min,二甲苯i10min,二甲苯ii10min,石蜡i(48-50℃)1h,石蜡ii(54-56℃)1h,石蜡iii(58-60℃)1h,然后将组织迅速用包埋蜡(58-60℃)注入包埋模具中,用石蜡切片机将已包埋的组织块切成7μm厚的薄片;将切妥的切片置于温水中铺展平整后,多聚赖氨酸载玻片捞起并附贴其上,晾干后再用烤片机烤片,使得牢固附着;h&e染色:组织切片采用苏木素染液、伊红染液染色后中性树胶封片;在光镜下观察小肠组织的病理形态学改变。
2.6协同抗肿瘤作用研究
2.6.1荷瘤鼠模型复制
在无菌条件下,收集对数生长期的ct-26结肠癌细胞,用生理盐水洗涤两次,调整细胞密度为5×106个细胞/ml,小鼠皮肤消毒后用1ml注射器于每只裸鼠右腋皮下接种0.1ml的细胞悬液。本实验接种成功率100%。接种后继续在spf级条件下的层流架中饲养。每日观察试验动物的营养状况、活动状态,每2-3天用游标卡尺测量皮下肿瘤直径,待肿瘤平均直径为5-6mm时,选择无出血、无坏死、无感染的小鼠进行实验。
2.6.2实验动物分组和治疗方案
将建模成功后荷瘤鼠随机组,每组10只,各组用药情况如下:生理盐水阴性对照组;lm组合物给药组;化疗药物给药组;联合给药组。实验期间所有试验动物均自由采食、饮水。给药期间注意观察试验鼠饮食、体重等一般情况,每2天用游标卡尺测量一次瘤块的长径(a)和短径(b),按公式v=1/2×a×b2计算肿瘤体积。
2.6.3联用对移植荷瘤鼠结肠癌的抑制作用
末次给药24h后,将各处理组荷瘤鼠颈椎脱臼处死,立即完整剥离瘤块,称量离体瘤块重量,计算各组平均瘤重,依据下列公式计算抑瘤率。抑瘤率(%)=(对照组平均瘤重-给药组平均瘤重)/对照组平均瘤重×100%
3.试验结果
3.1组合物缓解5-fu给药后所致的体重急剧下降
从体重变化曲线可以看出,空白组小鼠在实验过程中一直在上升,而模型组和给药组的体重呈现下降趋势。比较模型组和给药组,模型组下降的较快,从第四天开始,给药组下降较明显,但无显著性差异。不同剂量组合物比较,组合物实施例4-12以及19-30下降缓慢,实施例4-12下降更明显。结果见表1。
表1.组合物对5-fu引起的化疗相关性胃肠不适及肠粘膜损伤所致的体重急剧下降的缓解作用
*p<0.01,**p<0.01(相比于5-fu模型组)。
3.2组合物5-fu给药后所致的严重腹泻现象
从腹泻评分看(表2),阳性药盐酸洛哌丁胺组、组合物实施例4-12和模型组(5-fu60mg/kg/天)比较,对腹泻具有明显的抑制作用,且具有显著性差异。组合物实施例4-12给药组对腹泻的抑制作用呈现趋势剂量依赖性,表明了组合物实施例4-12能有效抑制化疗药物5-fu引起的腹泻。组合物实施例13-18给药组没有明显的抑制作用,组合物实施例19-30给药组的抑制作用明显高于模型组,略微高于实施例13-18给药组,但低于组合物实施例4-12给药组。
表2组合物对5-fu引起的化疗相关性胃肠不适及肠粘膜损伤所致的严重腹泻的抑制作用
*p<0.01,**p<0.01(相比于5-fu模型组)。
3.3病理切片
进一步的对小鼠回肠进行病理切片观察,由图1我们可以看出,5-fu模型组的小鼠回肠组织表现出严重广泛的炎性病变:隐窝急剧破损,固有层纤维化,慢性炎症因子浸润,粘膜下层水肿。然而,组合物实施例4-12给药组回肠的隐窝和绒毛长度显著增加。回肠组织绒毛有轻微的炎症浸润,固有层显示不完整的中性粒细胞浸润,且扩展到粘膜下层。结果表明了组合物实施例4-12给药后能逆转5-fu造成的肠道毒性。组合物实施例13-30给药组未见明显变化。
3.4组合物对5-fu引起的腹泻的抑制作用
5-fu能显著增加酚红在肠段中的运动,呈现亢进状态,组合物实施例4-12对5-fu引起的腹泻模型小鼠均具有抑制胃排空的作用。如表3所示,组合物实施例4-12对胃排空的抑制率高达63.38%(p<0.01)。组合物实施例4-12对5-fu引起的肠运动功能亢进亦具有抑制作用;组合物实施例13-18对5-fu引起的肠运动功能亢进未见显著的调节作用;组合物实施例19-30对5-fu引起的肠运动功能亢进未见显著的调节作用略高于组合物实施例13-18,但差异不明显。
表3组合物实施例对5-fu模型小鼠的胃排空和肠推进的作用
相较于模型组:*p<0.05,**p<0.01。
3.5组合物与5-fu联合抗肿瘤作用
组合物协同化疗药5-fu治疗结肠癌后起到了减毒增效的作用。两者联合后抑瘤率有显著的提高,说明组合物实施例10-12协同化疗药5-fu后起到了增效的作用;联合用药后改善了小鼠常规生理指标,使小鼠的饮水饮食量和精神状态有了明显的改善,脾指数和胸腺指数都有所提高,组合物实施例10-12给药后能逆转5-fu造成的肠道毒性,因此说明了组合物协同化疗药5-fu治疗结肠癌后起到了减毒的作用,结果如表4和图2所示。
表4组合物与5-fu的协同抗肿瘤作用
- 还没有人留言评论。精彩留言会获得点赞!