5-十四烷氧基-2-呋喃甲酸在制备用于治疗银屑病样皮炎的药物中的用途
1.本发明涉及医药技术领域,更具体涉及一种用于治疗银屑病样皮炎的药物及其应用。
背景技术:
2.银屑病,俗称“牛皮癣”,世卫组织(who)将之列入世界十大顽症。中国银屑病发病率为0.3~0.5%,患者约1000万,呈逐年上升趋势。
3.银屑病是一种常见的慢性系统性炎症性疾病,主要累及皮肤和关节,严重影响患者的身心健康,给社会带来沉重的经济负担。银屑病是一种复杂的、多基因影响的免疫介导疾病,由感染、药物、外伤和情绪压力等环境因素所引发。银屑病的免疫发病机制以树突状细胞(dendritic cells,dc)所调控的t淋巴细胞分化为中心,并以白细胞介素(interleukin,il)-23/il-17所介导的炎症轴为主。表皮朗格汉斯细胞(langerhanscells,lc)作为表皮中的唯一dc亚群,在银屑病的发病机制中发挥重要作用。
4.众所周知,银屑病与代谢综合征相关,包括高血压、血脂异常、胰岛素抵抗、肥胖和心血管疾病。涉及循环系统和不同皮肤层次的脂质紊乱与银屑病的疾病严重程度有关。联合转录组分析也揭示了银屑病皮损中脂质途径发生了重大变化,表明异常脂质代谢在银屑病发病机制中发挥了关键作用。然而,针对异常脂质代谢的治疗方法确未被尝试。
5.目前尚无治愈银屑病的治疗方法,已有的治疗措施存在着各自有效性和安全性方面的局限,例如环孢素a、甾族化合物、甲氨蝶呤以及光化学疗法均有免疫抑制作用,但由于副作用,这些治疗并非理想。
6.因此,本领域中,进一步深入研究银屑病的发病机理,继而开发靶向性强、远期疗效好、安全性高、价格低廉的新一代治疗银屑病新药及治疗方法势在必行。
技术实现要素:
7.本发明的主要目的在于提供了一种用于治疗银屑病样皮炎的药物及其应用,以解决现有技术中常见的治疗银屑病样皮炎药物疗效较差且毒副作用较多的问题。
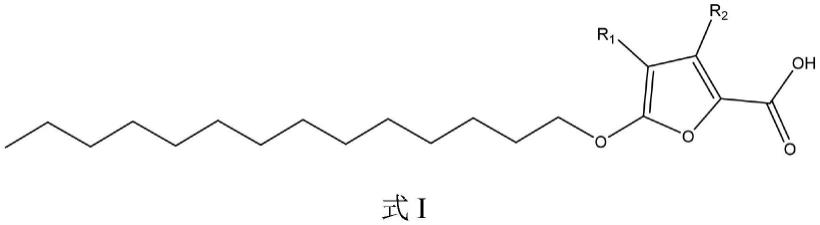
8.为了实现上述目的,根据本发明的一个方面,提供了一种下式i所示的化合物或其可药用盐、氘代物、溶剂化物、代谢产物或前药在制备用于治疗银屑病样皮炎的药物中的用途,
9.10.其中,r1和r2相同或不同且为氢、卤素、羟基、c
1-12
烷基或c
1-12
烷氧基。
11.根据本发明的另一方面,提供了一种包括下式i所示的化合物或其可药用盐、氘代物、溶剂化物、代谢产物或前药的药物组合物在制备用于治疗银屑病样皮炎的药物中的用途,
[0012][0013]
其中,r1和r2相同或不同且为氢、卤素、羟基、c
1-12
烷基或c
1-12
烷氧基。
[0014]
根据本发明的另一方面,提供了一种包括下式i所示的化合物或其可药用盐、氘代物、溶剂化物、代谢产物或前药的药物制剂在制备用于治疗银屑病样皮炎的药物中的用途,
[0015][0016]
其中,r1和r2相同或不同且为氢、卤素、羟基、c
1-12
烷基或c
1-12
烷氧基。
[0017]
进一步地,该药物制剂进一步包括药学上可接受的药用辅料。
[0018]
进一步地,该药物制剂为固体片剂、口服液、胶囊、滴丸、软膏剂、凝胶制剂、透皮贴剂、微乳制剂或气雾剂。
[0019]
进一步地,该药物制剂为软膏剂、凝胶制剂、透皮贴剂、微乳制剂或气雾剂。
[0020]
进一步地,该药用辅料包括基质材料、保湿剂、ph调节剂、表面活性剂、防腐剂、螯合剂和稳定剂中的一种或多种。
[0021]
进一步地,该药物组合物或该药物制剂进一步包括甲氨蝶呤、维甲酸、环孢素a、依那西普、英夫利昔单抗、阿达木单抗和乌司奴单抗中的一种或多种。
[0022]
进一步地,r1和r2相同或不同且为氢、羟基、c
1-6
烷基或c
1-6
烷氧基;
[0023]
进一步地,r1和r2相同或不同且氢、羟基、甲基或甲氧基;
[0024]
进一步地,该化合物为5-十四烷氧基-2-呋喃甲酸。
[0025]
进一步地,该化合物通过抑制抑制表皮朗格汉斯细胞免疫功能以治疗银屑病样皮炎。
[0026]
进一步地,该化合物通过下调表皮朗格汉斯细胞的中性脂质水平,抑制表皮朗格汉斯细胞成熟、抗原吞噬及il-23p19分泌以治疗银屑病样皮炎。
[0027]
进一步地,该银屑病样皮炎为咪喹莫特诱导的银屑病样皮炎。
[0028]
本发明的有益效果:
[0029]
通过皮下注射5-十四烷氧基-2-呋喃甲酸能够减轻咪喹莫特(imiquimod,imq)诱
导的银屑病样皮肤炎症,其中5-十四烷氧基-2-呋喃甲酸下调表皮朗格汉斯细胞的中性脂质水平,抑制其成熟、抗原吞噬及il-23p19分泌。
附图说明
[0030]
为了更清楚地说明本技术实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的一些实施例,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的附图,而并不超出本技术要求保护的范围。
[0031]
图1为5-十四烷氧基-2-呋喃甲酸(5-tetradecyloxy-2-furoicacid,tofa)化学结构式示意图。
[0032]
图2为皮下注射tofa治疗imq诱导银屑病样皮肤炎症的实验流程图。
[0033]
图3为皮下注射tofa减轻imq诱导银屑病样皮肤炎症的组织病理图片。
[0034]
图4为皮下注射tofa降低imq诱导银屑病样皮肤炎症的pasi评分图。
[0035]
图5为皮下注射tofa减少imq诱导银屑病样皮肤炎症所导致的皮肤增厚实验结果图。
[0036]
图6为皮下注射tofa使得imq诱导小鼠表皮朗格汉斯细胞的中性脂质含量变化趋势图。
[0037]
图7为皮下注射tofa下调表皮朗格汉斯细胞的中性脂质含量流式细胞技术(facs)结果示意图。
[0038]
图8为皮下注射tofa下调表皮朗格汉斯细胞的mhc-ii表达流式细胞技术(facs)结果示意图。
[0039]
图9为皮下注射tofa下调表皮朗格汉斯细胞的cd80表达流式细胞技术(facs)结果示意图。
[0040]
图10为皮下注射tofa抑制表皮朗格汉斯细胞吞噬抗原的能力流式细胞技术(facs)结果示意图。
[0041]
图11为皮下注射tofa抑制表皮朗格汉斯细胞分泌il-23的能力流式细胞技术(facs)结果示意图。
具体实施方式
[0042]
下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
[0043]
需要说明的是,在不冲突的情况下,本技术中的实施例及实施例中的特征可以相互组合。下面将结合实施例来详细说明本发明。
[0044]
以下结合具体实施例对本发明作进一步详细描述,这些实施例不能理解为限制本技术所要求保护的范围。
[0045]
正如背景技术部分所描述的,现有的治疗银屑病样皮炎药物疗效较差且毒副作用较多的问题。为了解决上述问题,本发明提供了一种下式i所示的化合物或其可药用盐、氘
代物、溶剂化物、代谢产物或前药在制备用于治疗银屑病样皮炎的药物中的用途,
[0046][0047]
其中,r1和r2相同或不同且为氢、卤素、羟基、c
1-12
烷基或c
1-12
烷氧基。
[0048]
根据本发明的另一方面,提供了一种包括下式i所示的化合物或其可药用盐、氘代物、溶剂化物、代谢产物或前药的药物组合物在制备用于治疗银屑病样皮炎的药物中的用途,
[0049][0050]
其中,r1和r2相同或不同且为氢、卤素、羟基、c
1-12
烷基或c
1-12
烷氧基。
[0051]
根据本发明的另一方面,提供了一种包括下式i所示的化合物或其可药用盐、氘代物、溶剂化物、代谢产物或前药的药物制剂在制备用于治疗银屑病样皮炎的药物中的用途,
[0052][0053]
其中,r1和r2相同或不同且为氢、卤素、羟基、c
1-12
烷基或c
1-12
烷氧基。
[0054]
如本文所用,短语“可药用盐”包括碱金属盐,如钠盐、钾盐、锂盐等;碱土金属盐,如钙盐、镁盐等;其他金属盐,如铁盐、铜盐、钴盐等;有机碱盐,如铵盐、三乙胺盐、吡啶盐、甲基吡啶盐、2,6-二甲基吡啶盐、乙醇胺盐、二乙醇胺盐、三乙醇胺盐、环己胺盐、乙二胺盐、胍盐、异丙基胺盐、三甲基胺盐、三丙基胺盐、三乙醇胺盐、二乙醇胺盐、乙醇胺盐、二甲基乙醇胺盐、二环己基胺盐、咖啡碱盐、普鲁卡因盐、胆碱盐、甜菜碱盐、苯明青霉素盐、葡萄糖胺盐、n-甲基葡糖胺盐、可可碱盐、氨丁三醇盐、嘌呤盐、哌嗪盐、吗啉盐、哌啶盐、n-乙基哌啶盐、四甲基胺盐、二苄基胺盐和苯基甘氨酸烷基酯盐等;氢卤酸盐,如氢氟酸盐、盐酸盐、氢碘酸盐、氢溴酸盐等;无机酸盐,如盐酸盐、硝酸盐、硫酸盐、高氯酸盐、磷酸盐等;低级烷磺酸盐,如甲磺酸盐、三氟甲磺酸盐、乙磺酸盐等;芳基磺酸盐,如苯磺酸盐、对甲苯磺酸盐等;有机酸盐,如乙酸盐、苯甲酸盐、富马酸盐、甲酸盐、三氟乙酸盐、糠酸盐、葡萄糖酸盐、谷氨酸盐、乙醇酸盐、羟乙磺酸盐、乳酸盐、马来酸盐、苹果酸盐、扁桃酸盐、粘液酸盐、双羟萘酸
盐、泛酸盐、硬脂酸盐、琥珀酸盐、磺胺酸盐、酒石酸盐、丙二酸盐、2-羟基丙酸盐、柠檬酸盐、水杨酸盐、草酸盐、羟乙酸盐、葡萄糖醛酸盐、半乳糖醛酸盐、枸橼酸盐、赖氨酸盐、精氨酸盐、门冬氨酸盐、肉桂酸盐等。
[0055]
如本文所用,短语“氘代物”是指式i化合物基团中的一个或多个氢被氘所取代所生成的含氘化合物。
[0056]
如本文所用,短语“溶剂化物”指本发明化合物或其盐,它们还包括以分子间非共价力结合的化学计量或非化学计量的溶剂。当溶剂为水时,则为水合物。
[0057]
如本文所用,短语“代谢产物”是指具体的化合物或其盐在体内通过代谢作用所得到的产物。一个化合物的代谢产物可以通过所属领域公知的技术来进行鉴定,其活性可以通过如本发明所描述的那样采用试验的方法进行表征。这样的产物可以是通过给药化合物经过氧化,还原,水解,酰氨化,脱酰氨作用,酯化,脱脂作用,酶裂解等等方法得到。相应地,本发明包括化合物的代谢产物,包括将本发明的化合物与哺乳动物充分接触一段时间所产生的代谢产物。
[0058]
如本文所用,短语“前药”,代表一个化合物在体内转化为式i所示的化合物。这样的转化受前体药物在血液中水解或在血液或组织中经酶转化为母体结构的影响。本发明前体药物类化合物可以是酯,在现有的发明中酯可以作为前体药物的有苯酯类,脂肪族(c
1-24
)酯类,酰氧基甲基酯类,碳酸酯,氨基甲酸酯类和氨基酸酯类。
[0059]
如本文所用,术语“烷基”指饱和的、单价的、非支链或支链的烃链。烷基的例子包括,但不限于:(c
1-c3)烷基,如甲基、乙基、丙基、异丙基,和(c
4-c8)烷基,如2-甲基-l-丙基、2-甲基-2-丙基、2-甲基-l-丁基、3-甲基-l-丁基、2-甲基-3-丁基、2,2-二甲基-l-丁基、2-甲基-戊基、3-甲基-1-戊基、4-甲基-1-戊基、2-甲基-2-戊基、3-甲基-2-戊基、4-甲基-2-戊基、2,2-二甲基-l-丁基、3,3-二甲基-1-丁基、2-乙基-l-丁基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、己基、庚基、辛基等等。任何烷基可以是未取代的或被一个或多个适当的取代基取代。
[0060]
如本文所用,术语“烷氧基”指烷基的氧醚基团。烷氧基的例子包括,但不限于:甲氧基、乙氧基、正-丙氧基、仲丁氧基、叔-丁氧基、正-乙氧基等等。烷氧基可以是未取代的或被一个或多个适当的取代基取代。
[0061]
如本文所用,术语“卤素”是指氟、氯、溴或碘。相应地,术语“卤代”是指氟代、氯代、溴代和碘代。
[0062]
在本发明中,术语“治疗”也包括“预防”,除非存在与此相反的具体说明。术语“治疗(的)”和“治疗(地)”应该作相应的理解。
[0063]
本发明的上述药物、药物组合物以及药物制剂针对银屑病的脂质代谢紊乱进行治疗,从代谢层面直接抑制炎症,通过抑制过度脂质合成,从而减轻银屑病样皮肤炎症。
[0064]
本发明还提供治疗银屑病样皮炎的方法,该方法包括给予所述患者治疗有效量的上文定义的药物、药物组合物以及药物制剂。
[0065]
达到成功治疗的药量当然取决于患者及银屑病样皮炎的严重性。剂量可由熟练的药师便利地确定。
[0066]
在本文中,术语“治疗有效量”和“有效量”表示所述物质和物质的量对于预防、减轻或改善疾病或病症的一种或多种症状,和/或延长接受治疗的对象的存活是有效的。
[0067]
在一种优选的实施方式中,该药物制剂进一步包括药学上可接受的药用辅料。
[0068]
在一种优选的实施方式中,本发明的药物制剂中的式i的化合物以1至20%的范围的浓度存在,以整个组合物的重量计。
[0069]
在一种优选的实施方式中,本发明的药物制剂中的式i的化合物以1至10%的范围的浓度存在,以整个组合物的重量计。
[0070]
在一种优选的实施方式中,本发明的药物制剂中的式i的化合物以2至8%的范围的浓度存在,以整个组合物的重量计。
[0071]
在一种优选的实施方式中,该药物制剂为固体片剂、口服液、胶囊、滴丸、软膏剂、凝胶制剂、透皮贴剂、微乳制剂或气雾剂。
[0072]
在一种优选的实施方式中,该药物制剂为软膏剂、凝胶制剂、透皮贴剂、微乳制剂或气雾剂。
[0073]
在一种优选的实施方式中,使用用于化妆品制剂的常规赋形剂(特别是凡士林、液体石蜡和羊毛脂)所配制的微乳制剂或软膏剂。
[0074]
在一种优选的实施方式中,该药用辅料包括基质材料、保湿剂、ph调节剂、表面活性剂、防腐剂、螯合剂和稳定剂中的一种或多种。
[0075]
在一些实施方式中,该基质材料选自卡波姆、交联羧甲基纤维素钠、海藻酸钠、壳聚糖、凡士林、石蜡、蜂蜡、硬脂酸、羊毛脂、聚乙二醇、单硬脂酸甘油酯中的一种或者至少两种的混合物。
[0076]
在一种优选的实施方式中,该保湿剂是滋润和软化皮肤的物质。该保湿剂可以选自甘油、山梨醇、丙二醇、丙二醇、聚乙二醇及其混合物。
[0077]
在一种优选的实施方式中,该ph调节剂将组合物的ph设定和/或保持在所需值。该ph调节剂可以选自三乙醇胺、柠檬酸、乙酸、磷酸、丙酸、乳酸、碳酸、铵/氨、氢氧化钠及其混合物。
[0078]
在一种优选的实施方式中,该表面活性剂为脂肪酸皂、十二烷基硫酸钠、月桂醇聚氧乙烯醚硫酸钠、十六烷基聚氧乙烯醚磷酸钠、大豆磷脂(卵磷脂)、高碳烷基的伯、仲、叔胺和季铵盐如十八烷基三甲基氯化铵、c
12-14
烷基二甲基苄基氯化铵、双十八烷基二甲基氯化钠、椰油酰胺基丙基甜菜碱、咪唑啉、失水山梨醇单水桂酸脂、环氧乙烷加成物、月桂醇聚氧乙烯醚、椰油酸二乙醇酰胺、油酸单甘油酯、聚氧乙烯蓖麻油和聚氧乙烯羊毛脂中的一种或一种以上的组合。
[0079]
在一种优选的实施方式中,该防腐剂阻止或最小化由于存在不同类型的微生物引起的制剂组分的劣化。该防腐剂可以选自苯氧基乙醇、托酚酮、氯苯甘醚、乙基己基甘油、异噻唑烷酮(isothiazolidone)、二唑烷基脲、咪唑烷基脲和对羟基苯甲酸酯以及它们的混合物。
[0080]
在一种优选的实施方式中,该螯合剂络合并中和可能影响药物制剂的稳定性和/或外观的金属离子。该螯合剂可以是单原子螯合配体和多齿螯合配体。该螯合剂可选自乙二胺四乙酸(edta)、次氮基三乙酸(nta)、羟乙基乙二胺三乙酸(heedta)、二乙烯三胺五乙酸(dtpa)、二乙醇甘氨酸(deg)、乙醇二甘氨酸(edg)、柠檬酸、磷酸、酒石酸,或其盐,以及它们的混合物。
[0081]
在一些实施方式中,该稳定剂选自依地酸二钠、亚硫酸钠、尼泊金酯中的一种或多
种。
[0082]
本发明的化合物可与用于所述目的地其它已知药物组合使用用于治疗银屑病样皮炎,这构成了本发明的另一方面。在一种优选的实施方式中,该药物组合物或该药物制剂进一步包括甲氨蝶呤、维甲酸、环孢素a、依那西普、英夫利昔单抗、阿达木单抗和乌司奴单抗中的一种或多种。
[0083]
在一种优选的实施方式中,r1和r2相同或不同且为氢、羟基、c
1-6
烷基或c
1-6
烷氧基;
[0084]
在一种优选的实施方式中,r1和r2相同或不同且氢、羟基、甲基或甲氧基;
[0085]
在一种优选的实施方式中,该化合物为5-十四烷氧基-2-呋喃甲酸。化学结构式如图1所示。
[0086]
在一种优选的实施方式中,该化合物通过抑制抑制表皮朗格汉斯细胞免疫功能以治疗银屑病样皮炎。
[0087]
其中,朗格汉斯细胞(langerhanscell,简称“lc”)为表皮非角质形成细胞的一种,数量极少散在分布于表皮中。朗格汉斯细胞具有树枝状突起,散布于棘层细胞间。细胞核不规则,高尔基复合体发达,溶酶体较多。还有一种特殊的网球拍形小颗粒,称为伯贝克颗粒,其功能是参与免疫应答。朗格汉斯细胞能获捕和处理侵入皮肤的抗原,并传递给t细胞,所以是一种抗原呈递细胞。
[0088]
在一种优选的实施方式中,该化合物通过下调表皮朗格汉斯细胞的中性脂质水平,抑制表皮朗格汉斯细胞成熟、抗原吞噬及il-23p19分泌以治疗银屑病样皮炎。
[0089]
在一种优选的实施方式中,该银屑病样皮炎为咪喹莫特(imiquimod,imq)诱导的银屑病样皮炎。
[0090]
其中,咪喹莫特是toll样受体(tolllikereceptor,tlr)7/8的特异性激活剂,可以特异性与浆细胞样树突状细胞(plasmacytoid dendriticcells,pdc)内涵体tlr7结合,诱导pdc分泌大量的干扰素(interferon,ifn)-α。imq应用于有银屑病倾向的患者会诱发和加重病情。
[0091]
实验方法:
[0092]
8~10周龄的野生型c57bl/6小鼠背部脱毛后,连续5天局部涂抹62.5mg咪喹莫特(imiquimod,imq)乳膏(5%,#h20030128,四川医药),以诱导银屑病样皮损;健康对照组涂抹同等剂量的凡士林(vaseline,vas,#180102,山东名德)。从涂药前一天开始,连续6天于小鼠背部皮下注射体积为100μl的剂量为5mg/kg体重的乙酰辅酶a羧化酶的变构抑制剂tofa(#t6575,sigma)或磷酸盐缓冲盐水(phosphatebuffersaline,pbs)。实验进程如图2所示。
[0093]
使用银屑病面积和严重程度指数(psoriasisareaandseverityindex,pasi)评价小鼠皮损的严重程度,其由红斑指数(0~4)、浸润指数(0~4)和鳞屑指数(0~4)所组成。皮肤厚度用游标卡尺测量。制备石蜡包埋皮肤组织标本,进行苏木精-伊红染色。
[0094]
获取小鼠背部皮肤,真表皮分离后制备表皮单细胞悬液,使用完全培养基重悬后于37℃体外培养,同时添加或者不添加tofa(10μg/ml,#t6575,sigma)。
[0095]
为了确定lcs吞噬外来抗原的能力,新鲜分离的表皮细胞与葡聚糖-异硫氰酸荧光素(dextran-fitc,0.025%,#fd4,sigma),于37℃或4℃下共同孵育45分钟,其后使用pbs冲洗细胞。
[0096]
流式细胞术分析:使用抗cd16/cd32抗体(2.4g2,#553141,bd biosciences)预处理后,使用固定活性染色剂(#564406,bdbiosciences)染色10分钟以区分细胞的死活,使用抗小鼠i-a/i-e抗体(m5/114,#562363,bdbiosciences)、抗小鼠cd45.2抗体(104,#109832,biolegend)和抗小鼠cd80抗体(16-10a1,#104708,biolegend)进行表面标记。细胞内染色用bd-cytofix/cytoperm(#51-2090kz,bd-biosciences)固定和渗透细胞,用抗小鼠il-23p19抗体(n71-1183,#565317,bdbiosciences)于4℃下培养30分钟。最后,使用bd-lsrfortessa细胞仪检测细胞,并用flowjo软件分析。
[0097]
实验结果如下所示:
[0098]
1、pasi评分显示皮下注射tofa减轻了imq诱导的银屑病样皮肤炎症(pasi评分下调),下调皮肤厚度,改善组织病理特征(图3-图5)。相较于健康对照组,imq诱导小鼠表皮lc中的中性脂质含量增高;应用tofa后,imq诱导小鼠表皮lcs中的脂质呈下降趋势(图6,bodipy
tm
493/503染色)。该结果提示,表皮lc中的脂质水平在调控imq诱导银屑病样皮炎中可能发挥重要作用。
[0099]
2、为了探索脂质含量对lc免疫功能的影响,我们使用tofa减少表皮lcs中脂肪酸的合成(图7所示,制备野生型c57bl/6小鼠表皮单细胞悬液,同时添加或者不添加tofa(10μg/ml)于37℃持续18小时,最后4小时添加bdgolgistop
tm
蛋白转运抑制剂。使用抗mhc
‑ⅱ
、cd45.2、cd80抗体和bodipy
tm
493/503进行染色并进行流式分析)。tofa显著降低了体外培养的lcs中的中性脂质水平,其细胞表面成熟标记物mhc-ii和cd80的表达、对于葡聚糖-fitc的吞噬能力和il-23的分泌均随之显著下降(图8-11所示,制备野生型c57bl/6小鼠表皮单细胞悬液,同时添加或者不添加tofa(10μg/ml)于37℃持续18小时,最后4小时添加bdgolgistop
tm
蛋白转运抑制剂。使用抗mhc
‑ⅱ
、cd45.2、cd80抗体和bodipy
tm
493/503进行染色并进行流式分析),表明表皮lcs中性脂质含量与其免疫功能高度相关,进一步提示脂质代谢紊乱可能通过影响表皮lc的免疫功能从而影响银屑病的发生发展。
[0100]
以上所述的仅是本发明的实施例,方案中公知的具体技术及特性等常识在此未作过多描述。应当指出,对于本领域的技术人员来说,在不脱离本发明的前提下,还可以作出若干变形和改进,这些也应该视为本发明的保护范围,这些都不会影响本发明实施的效果和专利的实用性。本技术要求的保护范围应当以其权利要求的内容为准,说明书中的具体实施方式等记载可以用于解释权利要求的内容。
[0101]
以上对本发明实施例进行了详细介绍,本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明仅用于帮助理解本发明的方法及其核心思想。同时,本领域技术人员依据本发明的思想,基于本发明的具体实施方式及应用范围上做出的改变或变形之处,都属于本发明保护的范围。综上所述,本说明书内容不应理解为对本发明的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1