口服降糖肽TSME在制备抗神经退行性疾病药物方面的应用
口服降糖肽tsme在制备抗神经退行性疾病药物方面的应用
技术领域
1.本发明涉及口服降糖肽tsme在制备抗神经退行性疾病药物方面的应用,属于生物医药技术领域。
背景技术:
2.神经退行性疾病是一类以异常神经元死亡丢失为特征的疾病,如阿尔茨海默病、帕金森病、亨廷顿舞蹈症等。阿尔茨海默病是最常见的神经退行性疾病,主要临床表现为认知功能和学习障碍、记忆力衰退等。随着人口老龄化不断加速,近年阿尔茨海默病患病人数正在急剧增加,其导致的社会负担也日益加剧,尤其在中国,阿尔茨海默病患者人数已居世界第一,防治阿尔茨海默病药物市场需求巨大。
3.帕金森病是最常见的神经退行性疾病之一,多发于老年人群体。帕金森病最主要的病理改变包括中脑黑质多巴胺能神经元异常退化,及其导致的纹状体多巴胺显著减少和路易小体的形成,临床表现为静止性震颤、运动迟缓、肌强直和姿势步态异常等运动障碍,甚至出现认知障碍等非运动症状。中国帕金森病患者在全球帕金森病高发国家中约占一半,且随着人口老龄化不断加速,帕金森病导致的社会负担也日益加剧。
4.用于阿尔茨海默病临床治疗的药物主要包括胆碱酯酶抑制剂和nmda受体拮抗剂等,这些药物虽能在一定程度上缓解临床症状,但疗效有限,难以逆转疾病的发生发展。近年,生物药物的研制进入高速发展阶段,2021年6月fda批准生物药物aducanumab作为阿尔茨海默病疗法,这也是自2003年以来,fda批准的首款抗阿尔茨海默病新药,显示了生物药物应用于神经退行性疾病领域的巨大潜力。但由于在胃肠道中易被酶解失活,大多数生物药物包括多肽、蛋白及抗体等需要长期注射给药,可能会给病人带来诸多不便,降低了病人长期用药的依从性。
5.因此,开发非注射途径给药的生物药物具有重要的临床意义。口服给药方式应用广泛、使用方便,也是多肽、蛋白质等生物药物的理想给药方式。
6.发明人在本领域已经获得了一些研究成果,先于2013年12月17日申请专利号cn201310694475.0、授权公告号cn103665148b的中国发明专利,再于2019年08月14日申请专利号cn201910747519.9、授权公告号cn110437329b的中国发明专利,已在前期研究中获得了系列具有可口服给药潜力的多肽,在此基础上发明人进行了大量探索、实验及研究工作,目前已取得进一步研究成果。
技术实现要素:
7.本发明的目的在于:根据发明人新近研究成果,针对现有技术存在的问题,提出口服降糖肽tsme在制备抗神经退行性疾病药物方面的应用,尤其是制备抗阿尔茨海默病或帕金森病药物方面的应用。
8.本发明解决其技术问题的技术方案如下:
9.一种口服降糖肽的用途,其特征是,所述用途为用于制备治疗或预防神经退行性
疾病的药物;
10.所述口服降糖肽的氨基酸序列为:
11.his
‑
gly
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
leu
‑
ser
‑
met
‑
gln
‑
met
‑
glu
‑
glu
‑
glu
‑
ala
‑
val
‑
leu
‑
leu
‑
phe
‑
ile
‑
glu
‑
trp
‑
leu
‑
met
‑
asn
‑
gly
‑
gly
‑
pro
‑
ser
‑
ser
‑
gly
‑
ala
‑
pro
‑
pro
‑
pro
‑
ser
‑
cys。
12.优选地,所述神经退行性疾病包括阿尔茨海默病。
13.优选地,所述神经退行性疾病包括帕金森病。
14.优选地,所述药物的剂型为口服给药剂型。
15.优选地,所述药物的剂型为非口服给药剂型。
16.一种药物组合物的用途,其特征是,所述用途为用于制备治疗或预防神经退行性疾病的药物制剂;
17.所述药物组合物含有口服降糖肽,所述口服降糖肽的氨基酸序列为:
18.his
‑
gly
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
leu
‑
ser
‑
met
‑
gln
‑
met
‑
glu
‑
glu
‑
glu
‑
ala
‑
val
‑
leu
‑
leu
‑
phe
‑
ile
‑
glu
‑
trp
‑
leu
‑
met
‑
asn
‑
gly
‑
gly
‑
pro
‑
ser
‑
ser
‑
gly
‑
ala
‑
pro
‑
pro
‑
pro
‑
ser
‑
cys。
19.优选地,所述神经退行性疾病包括阿尔茨海默病。
20.优选地,所述神经退行性疾病包括帕金森病。
21.优选地,所述药物的剂型为口服给药剂型。
22.优选地,所述药物的剂型为非口服给药剂型。
23.本发明涉及的口服降糖肽为专利号cn201310694475.0、授权公告号cn103665148b的中国发明专利中具体实施方式记载的多肽tsme1。本发明的发明人在对该多肽做进一步研究后发现,该多肽能缓解β
‑
淀粉样蛋白诱导阿尔茨海默病样模型神经细胞死亡,能缓解mpp
+
诱导帕金森病样模型神经细胞死亡,能对β
‑
淀粉样蛋白诱导阿尔茨海默病动物模型认知能力和记忆功能退化起到缓解作用,且口服给药有效,因此该多肽可作为治疗或预防神经退行性疾病的候选分子,具有良好的应用前景。
附图说明
24.图1为本发明实施例1的结果示意图,纵坐标为相对细胞存活率。
25.图2为本发明实施例2的结果示意图,其中a图为小鼠定位航行实验第5天轨迹图
‑
学习能力的考察结果图,b图为小鼠空间探索实验轨迹图
‑
空间记忆能力的考察结果图。
26.图3为本发明实施例3的结果示意图,纵坐标为相对细胞存活率。
具体实施方式
27.下面参照附图并结合实施例对本发明作进一步详细描述。但是本发明不限于所给出的例子。各实施例中,所用方法如无特别说明均为常规方法,所用试剂和材料如无特别说明均为市售品。
28.各实施例中提及的tsme1即本发明采用的口服降糖肽,其氨基酸序列为:his
‑
gly
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
leu
‑
ser
‑
met
‑
gln
‑
met
‑
glu
‑
glu
‑
glu
‑
ala
‑
val
‑
leu
‑
leu
‑
phe
‑
ile
‑
glu
‑
trp
‑
leu
‑
met
‑
asn
‑
gly
‑
gly
‑
pro
‑
ser
‑
ser
‑
gly
‑
ala
‑
pro
‑
pro
‑
pro
‑
ser
‑
cys。
29.各实施例中若有提到对比多肽tsme4,则该多肽是指cn103665148b中记载的多肽tsme4,其氨基酸序列为:his
‑
gly
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
leu
‑
ser
‑
glu
‑
gln
‑
met
‑
glu
‑
glu
‑
glu
‑
ala
‑
val
‑
thr
‑
leu
‑
phe
‑
ile
‑
glu
‑
trp
‑
leu
‑
ser
‑
asn
‑
gly
‑
gly
‑
pro
‑
ser
‑
ser
‑
gly
‑
ala
‑
pro
‑
pro
‑
pro
‑
ser
‑
cys。
30.各实施例中采用的多肽均由吉尔生化(上海)公司用固相合成法进行合成。
31.实施例1
32.本实施例为检测多肽tsme1对β
‑
淀粉样蛋白诱导阿尔茨海默病样模型神经细胞死亡的缓解作用。
33.具体过程如下:
34.待测多肽tsme1实验组:选择处于复苏后10代以内且处于对数生长期的sh
‑
sy5y神经细胞,接种于96孔板中,每个孔100μl培养基,在细胞培养箱(37℃、5%co2)中培养24h,加入0.5μm的aβ
25
‑
35
(β
‑
淀粉样蛋白片段),并加入待测多肽tsme1。24h后,加入10%培养基体积的mtt溶液(终浓度为0.5mg/ml),于细胞培养箱中继续孵育4h,弃去上清液,每孔加入150μl二甲基亚砜后于摇板器上以500rpm振荡5min,振荡结束后置于酶标仪中以570nm为检测波长,630nm为参比波长,测定各孔的od值,并计算细胞存活情况。
35.与上述待测多肽实验组相比,阴性对照组不加入aβ
25
‑
35
和待测多肽tsme1,模型组不加入待测多肽tsme1。
36.结果如图1所示,与模型组相比,多肽tsme1能缓解β
‑
淀粉样蛋白诱导阿尔茨海默病样模型sh
‑
sy5y细胞死亡,且存在浓度依赖性,浓度越高,sh
‑
sy5y细胞的存活率越高。
37.实施例2
38.本实施例为检测多肽tsme1对β
‑
淀粉样蛋白诱导阿尔茨海默病小鼠模型认知能力和记忆功能退化的缓解作用。
39.具体过程如下:
40.实验动物饲养于温度为25℃
±
2℃的动物房中,自由饮食和水,每日光照12h。选用c57雄性小鼠(20
±
1.5g)作为实验对象,随机分为空白对照组和侧脑室注射aβ
25
‑
35
实验组,以侧脑室注射aβ
25
‑
35
建立阿尔茨海默病动物模型,具体造模操作如下:麻醉动物,剪去头顶多余毛发,并将其固定在脑立体定位仪上;常规消毒后,于头顶正中纵向剪开皮肤,钝性分离粘膜等组织,暴露出前囟;根据小鼠脑立体定位图谱定位;小鼠在前囟后0.8mm,矢状缝两侧各1.2mm处分别用0.5mm钻头钻破颅骨,微量进样器注射给药,深度为3.0mm,每侧缓慢注射4μl的aβ
25
‑
35
溶液(注射速度为1μl/min,注射完留针10min);缓慢退针,缝合伤口,涂抹青霉素粉末预防感染。
41.侧脑室注射aβ
25
‑
35
实验组的小鼠随机分组,每组9只,分别为模型组(皮下注射生理盐水)、模型组(灌胃生理盐水)、tsme1(1.06mg/kg/day)灌胃给药组、tsme1(2.12mg/kg/day)灌胃给药组、tsme1(4.24mg/kg/day)灌胃给药组、tsme1(0.1mg/kg/day)皮下给药组、tsme4(0.1mg/kg/day)皮下给药组、tsme4(4.24mg/kg/day)灌胃给药组;连续给药14天。
42.本实施例采用morris水迷宫评价实验动物的空间学习和记忆能力。
43.在第9天开始对实验动物进行定位航行实验,为期5天,定位航行实验用于评价动物的空间学习能力。将实验动物面向池壁放入池内,训练开始。如果小鼠在60s内找到平台并在平台上停留5s,训练停止;如果小鼠在60s内没有找到平台,则需引导小鼠到达平台并
在平台上停留10s。每次实验结束后,将小鼠吹干,放回笼内。系统将会记录小鼠的游泳轨迹和逃避潜伏期等数据。
44.空间探索实验于第14天进行,用于评价动物的空间记忆能力。第14天将平台从池中撤出,而后将小鼠从离平台所在象限最远的象限中面向池壁放入水中,让其在水中游泳60s。系统将会记录小鼠的游泳轨迹,在原平台所在象限停留的时间及穿越原平台所在位置的次数。
45.小鼠morris水迷宫实验结果如表1a和1b、图2a和图2b所示。
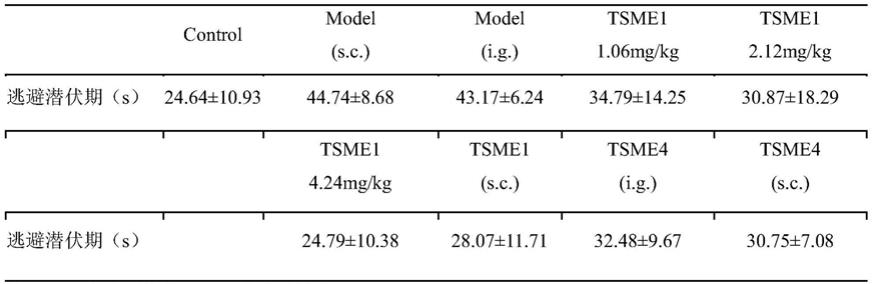
46.表1a、小鼠定位航行实验第5天的逃避潜伏期
[0047][0048]
注:(s.c.)为皮下给药,(i.g.)为灌胃给药
[0049]
表1b、小鼠空间探索实验
[0050][0051]
注:(s.c.)为皮下给药,(i.g.)为灌胃给药
[0052]
与模型组相比,tsme1(4.24mg/kg/day)灌胃给药组、tsme1(0.1mg/kg/day)皮下给药组中小鼠逃避潜伏期显著缩短,而其在原平台所在象限停留时间及穿越原平台所在位置的次数则明显增加,表明待测多肽tsme1对β
‑
淀粉样蛋白诱导阿尔茨海默病小鼠模型认知能力和记忆功能退化具有缓解作用,且口服给药有效。
[0053]
与tsme4灌胃给药组和皮下给药组相比,相同浓度、相同给药方式的tsme1给药组小鼠逃离潜伏期均显著缩短,而其在原平台所在象限停留时间及穿越原平台所在位置的次数则明显增加,表明多肽tsme1在缓解阿尔茨海默病小鼠模型的认知能力和记忆功能退化
方面明显优于tsme4。由此可知,虽然tsme1与tsme4同为exendin
‑
4类似物,且属于同系列口服降糖肽,但是在本实施例中tsme1明显优于tsme4。
[0054]
实施例3
[0055]
本实施例为检测多肽tsme1对mpp
+
诱导帕金森病样模型神经细胞死亡的缓解作用。
[0056]
具体过程如下:
[0057]
待测多肽tsme1实验组:sh
‑
sy5y细胞经过10μm维甲酸诱导分化6天后,选择处于对数生长期的分化后sh
‑
sy5y细胞,以3
×
104个/ml的密度接种于96孔板(每孔100μl),在37℃、5%co2细胞培养箱中培养。培养24h后,每孔加入1μm的mpp
+
,并加入待测多肽tsme1。24h后,加入10%培养基体积的mtt溶液(终浓度为0.5mg/ml),于细胞培养箱中继续孵育4h,弃去上清液,每孔加入150μl二甲基亚砜后于摇板器上以500rpm振荡5min,振荡结束后置于酶标仪中以570nm为检测波长,630nm为参比波长,测定各孔的od值,并计算细胞存活情况。
[0058]
与上述待测多肽实验组相比,阴性对照组不加入mpp
+
和待测多肽tsme1,模型组不加入待测多肽tsme1。
[0059]
结果如图3所示,与模型组相比,多肽tsme1能缓解mpp
+
诱导帕金森病样模型sh
‑
sy5y细胞死亡,且存在浓度依赖性,浓度越高,sh
‑
sy5y细胞的存活率越高。
[0060]
除上述实施例外,本发明还可以有其他实施方式。凡采用等同替换或等效变换形成的技术方案,均落在本发明要求的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1