可注射温敏水凝胶及其制备方法与流程
1.本发明涉及生物医用材料,具体而言,涉及一种可注射温敏水凝胶及其制备方法。
背景技术:
2.创面修复及伤口治疗是生物医用材料着眼的一个基本医疗问题。目前为止,已经有多种生物材料来促进创面的愈合,如静电纺丝纤维、多孔泡沫及功能化水凝胶等。其中,水凝胶敷料类材料具备优异的软湿特性及生物相容相似性,可作为生物活性因子或细胞的良好载体,也可更好的模拟皮肤细胞外基质结构。可注射性水凝胶可在外界刺激条件下实现原位凝胶化,在创面病灶处与组织相贴合,最大限度填充不规则创面且不对周围组织造成伤害。其中温敏性交联的水凝胶主要是通过温度的改变发生“溶胶
‑
凝胶”的转变,其温和的凝胶化条件可最大程度上维持目标细胞或药物的生物活性。基于此,这类温敏凝胶材料在伤口敷料材料领域具有重要的应用前景。
3.但是,传统的温敏性水凝胶存在制备过程复杂、生物相容性差、难降解等问题。
技术实现要素:
4.本发明的目的包括,例如,提供了一种可注射温敏水凝胶的制备方法,其能够提供一种低成本的可注射温敏水凝胶制备方法。
5.本发明的目的还包括,提供了一种可注射温敏水凝胶,其能够提供一种低成本的可注射温敏水凝。
6.本发明的实施例可以这样实现:
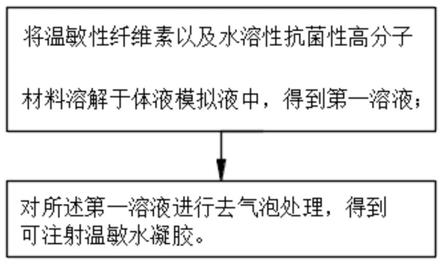
7.本发明的实施例提供了一种可注射温敏水凝胶的制备方法,包括:
8.将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液;
9.对所述第一溶液进行去气泡处理,得到可注射温敏水凝胶。
10.另外,本发明的实施例提供的可注射温敏水凝胶的制备方法还可以具有如下附加的技术特征:
11.可选地,所述温敏性纤维素为甲基纤维素、羟丙基纤维素或者羟丙基甲基纤维素中任意一种。
12.可选地,所述水溶性抗菌性高分子材料为季铵盐壳聚糖或者聚赖氨酸。
13.可选地,所述体液模拟液为磷酸缓冲盐溶液或者模拟体液。
14.可选地,所述温敏性纤维素的质量占比为6
‑
10%。
15.可选地,所述水溶性抗菌性高分子材料的质量占比为0.1
‑
2%。
16.可选地,所述将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液的步骤包括:
17.将所述水溶性抗菌性高分子材料溶解于所述体液模拟液,得到第一混合液;
18.将所述温敏性纤维素溶解于所述第一混合液,得到所述第一溶液。
19.可选地,所述将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液的步骤包括:
20.将所述温敏性纤维素溶解于所述体液模拟液,得到第二混合液;
21.将所述水溶性抗菌性高分子材料溶解于所述第二混合液,得到所述第一溶液。
22.可选地,所述将所述温敏性纤维素溶解于所述体液模拟液,得到第二混合液的步骤包括:
23.将所述温敏性纤维素加入所述体液模拟液中,并在50
‑
60℃温度进行搅拌混合,得到所述第二混合液。
24.本发明的实施例还提供了一种可注射温敏水凝胶。所述可注射温敏水凝胶由可注射温敏水凝胶的制备方法获得。
25.本发明实施例的可注射温敏水凝胶及其制备方法的有益效果包括,例如:
26.可注射温敏水凝胶的制备方法,将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液;对第一溶液进行去气泡处理,得到可注射温敏水凝胶。温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液的混合顺序不受限制,制备方法简单;原料来源广泛,价格低廉;得到的可注射温敏水凝胶具有非常好的生物相容性以及生物降解性,还具有抗菌性。提供了一种低成本的可注射温敏水凝胶制备方法。
27.可注射温敏水凝胶,由上述的可注射温敏水凝胶的制备方法获得,温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液的混合顺序不受限制,制备方法简单。原料来源广泛,价格低廉。
附图说明
28.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
29.图1为本发明实施例提供的可注射温敏水凝胶的制备方法的流程图;
30.图2为本发明实施例提供的可注射温敏水凝胶的制备方法的其中一个实施方式的流程图;
31.图3为本发明实施例提供的可注射温敏水凝胶的第一种成分的转变温度曲线图;
32.图4为本发明实施例提供的可注射温敏水凝胶的第二种成分的转变温度曲线图。
具体实施方式
33.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。通常在此处附图中描述和示出的本发明实施例的组件可以以各种不同的配置来布置和设计。
34.因此,以下对在附图中提供的本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范
围。
35.应注意到:相似的标号和字母在下面的附图中表示类似项,因此,一旦某一项在一个附图中被定义,则在随后的附图中不需要对其进行进一步定义和解释。
36.在本发明的描述中,需要说明的是,若出现术语“上”、“下”、“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,或者是该发明产品使用时惯常摆放的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。
37.此外,若出现术语“第一”、“第二”等仅用于区分描述,而不能理解为指示或暗示相对重要性。
38.需要说明的是,在不冲突的情况下,本发明的实施例中的特征可以相互结合。
39.下面结合图1至图2对本实施例提供的可注射温敏水凝胶的制备方法进行详细描述。
40.请参照图1,本发明的实施例提供了一种可注射温敏水凝胶的制备方法,包括:将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液;对第一溶液进行去气泡处理,得到可注射温敏水凝胶。具体地,可以通过在4℃的环境下静置6
‑
12小时进行气泡处理,得到可注射温敏水凝胶。
41.本实施例中,以温敏性纤维素为温敏型载体,以水溶性抗菌性高分子材料作为抗菌组分与凝胶组分,体液模拟液作为溶剂与助凝胶剂制备得到可注射温敏水凝胶。
42.温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液的混合顺序不受限制,制备方法简单。采用温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液,原料来源广泛,价格低廉,制备工艺简单。纤维素作为大分子多糖,易于降解,可注射温敏水凝胶具有非常好的生物相容性以及生物降解性,当温敏水凝胶注射至创面处,凝胶能够粘附于创面,可以很好的贴合伤口并释放药物;具备抗菌性能;具有优秀的温度敏感性,当温度处于30
‑
37℃之间时可迅速形成白色凝胶,且该过程可逆。效果好,成本低。
43.本实施例中,温敏性纤维素的质量占比为6
‑
10%。具体地,质量占比可以为6%、7%、8%、9%、10%。
44.本实施例中,水溶性抗菌性高分子材料的质量占比为0.1
‑
2%。具体地,质量占比为0.1%、0.5%、0.8%、1%、1.2%、2%。
45.本实施例中,温敏性纤维素为甲基纤维素、羟丙基纤维素或者羟丙基甲基纤维素中任意一种。
46.甲基纤维素是纤维素的甲基醚,是纤维素醚类中最简单的形式,具有良好的生物相容性。在甲基纤维素溶液状态,甲基纤维素分子被水化,分子间只是存在简单的链缠绕作用;当温度升高后,由于甲氧基的疏水作用导致凝胶的形成。
47.本实施例中,水溶性抗菌性高分子材料为季铵盐壳聚糖或者聚赖氨酸。
48.本实施例中,体液模拟液为磷酸缓冲盐溶液或者模拟体液。
49.本实施例中,将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液的步骤包括:
50.将水溶性抗菌性高分子材料溶解于体液模拟液,得到第一混合液;
51.将温敏性纤维素溶解于第一混合液,得到第一溶液。
52.具体地,先将水溶性抗菌性高分子材料加入体液模拟液,搅拌混合得到第一混合液;然后将温敏性纤维素加入第一混合液,在50
‑
60℃温度进行搅拌混合,得到第一溶液。温度可以是50℃、51℃、52℃、55℃、56℃、60℃。
53.在其他实施例中,将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液的步骤包括:
54.将温敏性纤维素溶解于体液模拟液,得到第二混合液;
55.将水溶性抗菌性高分子材料溶解于第二混合液,得到第一溶液。
56.具体地,先将温敏性纤维素加入体液模拟液中,并在50
‑
60℃温度进行搅拌混合,得到第二混合液。再将水溶性抗菌性高分子材料溶解于第二混合液,得到第一溶液。
57.具体地,参照图2,将6
‑
10wt%甲基纤维素溶解于磷酸缓冲盐溶液,得到第二混合液;将0.1
‑
2wt%季铵盐壳聚糖溶解于第二混合液,得到第一溶液;对第一溶液进行去气泡,得到可注射温敏水凝胶。
58.在其他实施例中,将温敏性纤维素以及水溶性抗菌性高分子材料溶解于体液模拟液中,得到第一溶液的步骤包括:
59.将温敏性纤维素以及水溶性抗菌性高分子材料先后加入体液模拟液,并在在50
‑
60℃温度进行搅拌混合,得到第一溶液。
60.承上述,温敏性纤维素、水溶性抗菌性高分子材料加入体液模拟液的顺序不分先后。其中,温敏性纤维素溶解于体液模拟液都需要在50
‑
60℃温度下进行,可以是温敏性纤维素加入体液模拟液后即进行加热,也可以在温敏性纤维素、水溶性抗菌性高分子材料均加入体液模拟液后再进行加热。
61.本实施例中,对第一溶液进行去气泡处理,得到可注射温敏水凝胶的步骤包括:对第一溶液进行超声、离心或4℃静置等方式去气泡处理,得到可注射温敏水凝胶。去气泡的方式不限于超声、离心或4℃静置等方式。
62.实施例1
63.配置磷酸缓冲盐溶液标准溶液作为凝胶的溶剂与助凝胶剂;
64.取一定量的磷酸缓冲盐溶液于烧杯中,在其中加入6
‑
10wt%的甲基纤维素(粘度15mpas),在室温下初步搅拌成黏稠溶液;
65.再加入0.1
‑
2wt%的季铵盐壳聚糖;将烧杯封口,进一步在50
‑
60℃温度下充分搅拌均匀,得到白色粘稠液体;
66.冷却至室温后,通过超声等方式除去气泡后,得到可注射温敏水凝胶。
67.该水凝胶的溶胶凝胶转变温度为30
‑
37℃。其中,图3示出了7%甲基纤维素、1%季铵盐壳聚糖的水凝胶的溶胶
‑
凝胶转变温度曲线图,转变温度在36.7℃。图4示出了10%甲基纤维素、1%季铵盐壳聚糖水凝胶的溶胶
‑
凝胶转变温度曲线图,转变温度在31.9℃。
68.实施例2
69.取9.2g磷酸缓冲盐溶液标准溶液于烧杯中,在其中加入0.7g甲基纤维素后,在室温初步搅拌;
70.再加入0.1g季铵盐壳聚糖,利用保鲜膜封口,置于60℃水浴中,磁力搅拌至完全溶解,得到白色黏稠溶液;
71.冷却至室温后,通过离心除去其中的气泡,得到可注射温敏水凝胶。
72.该水凝胶的溶胶凝胶转变温度为36.5℃。
73.实施例3
74.取9.2g磷酸缓冲盐溶液标准溶液于烧杯中,在其中加入0.2g的季铵盐壳聚糖,在室温初步搅拌;
75.再加入0.7g的甲基纤维素,在50℃温度下充分搅拌均匀,得到白色粘稠液体;
76.通过4℃静置除去其中的气泡,得到可注射温敏水凝胶。
77.该水凝胶的溶胶凝胶转变温度为35.4℃。
78.实施例4
79.取10g磷酸缓冲盐溶液标准溶液于烧杯中,在其中加入0.5g的聚赖氨酸,在室温初步搅拌;
80.再加入0.8g的羟丙基纤维素,在60℃温度下充分搅拌均匀,得到白色粘稠液体;
81.通过超声除去其中的气泡,得到可注射温敏水凝胶。
82.该水凝胶的溶胶凝胶转变温度为34.3℃。
83.实施例5
84.取10g磷酸缓冲盐溶液标准溶液于烧杯中,在其中加入0.8g的聚赖氨酸以及0.8g的羟丙基甲基纤维素,在55℃温度下充分搅拌均匀,得到白色粘稠液体;
85.通过离心除去其中的气泡,得到可注射温敏水凝胶。
86.该水凝胶的溶胶凝胶转变温度为33.1℃。
87.本实施例提供的一种可注射温敏水凝胶的制备方法至少具有以下优点:
88.温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液的混合顺序不受限制,制备方法简单。
89.温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液为原材料,价格低廉易于获得。
90.具有非常好的生物相容性以及生物降解性,当温敏凝胶注射至创面处,凝胶能够粘附于创面,可以很好的贴合伤口并释放药物。
91.具有优秀的温度敏感性,当温度处于30
‑
37℃之间时可迅速形成白色凝胶,且过程可逆。
92.本发明的实施例还提供了一种可注射温敏水凝胶。可注射温敏水凝胶由可注射温敏水凝胶的制备方法获得。温敏性纤维素、水溶性抗菌性高分子材料以及体液模拟液的混合顺序不受限制,制备方法简单。原料来源广泛,价格低廉。
93.以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以所述权利要求的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1