改善的柔性球囊导管的制作方法
1.本发明整体涉及用于在血管内医学治疗期间从血管中移除急性堵塞物的装置和方法。更具体地,本发明涉及用于在此类手术期间闭塞目标血管的部分的球囊引导导管。
背景技术:
2.球囊引导导管可用于标准动脉性或缺血性中风手术中,以充当诊断和治疗装置的管道,同时还提供流动阻止、流动控制和/或流动反转,以助于从患者体内安全取出凝块。该种流动控制提供了远端血管保护,这对于使栓塞迁移和其他程序并发症的风险最小化很重要,特别是在中风患者小而脆弱的脑通道中。另外,由这些导管提供的近端流动控制已示出与更好的血管造影和临床结果相关联。这些导管可用于减少动脉内机械性血栓切除手术的再通过程期间的手术时间和精力。例如,它们可限制缺血性中风期间所需的凝块取出尝试次数,同时还减少远端栓塞的发生率。
3.球囊引导导管必须足够柔性,同时还具有轴向刚度以通过曲折脉管系统平稳地递送至目标部位(通常为颈内动脉并进入缺血性中风患者的脑脉管系统中)。将球囊引导导管设计成具有适当的柔性可能由于需要包括膨胀管腔以使球囊引导导管的球囊膨胀而变得复杂。
4.这些装置还必须被设计成尽可能地无创伤,同时仍递送较高水平的性能。一旦获得进入目标的通路并展开球囊,引导导管必须相当稳固以在通过管腔推进、操纵和撤回其他装置的同时在该位置保持稳定。管腔本身必须具有对于这些装置足够大的直径,同时还引导在手术期间移除血液和血栓物质所需的更有效的抽吸。然而,管腔尺寸必须通过需要尽可能小型的外径来平衡,以使一旦导管从患者移除就必须闭合的入口孔的尺寸最小化。将球囊引导导管设计成具有最佳尺寸的管腔也可能由于需要包括膨胀管腔以使球囊引导导管的球囊膨胀而变得复杂。
技术实现要素:
5.本发明的一个目的是提供除了导管的中心管腔之外还具有小直径膨胀管腔管的球囊引导导管。膨胀管腔管可定位在导管的中心管腔内或导管的主体外部,使得膨胀管腔管可使球囊独立于中心管腔膨胀。
6.示例性球囊引导导管可包括基本上管状的主体、膨胀管腔和球囊。管状主体可包括内部中空管腔和管状主体远侧端部。膨胀管腔可包括膨胀管腔远侧端部和近侧节段,所述膨胀管腔远侧端部靠近管状主体远侧端部与管状主体连接,所述近侧节段延伸管状主体的长度的大部分。近侧节段能够相对于管状主体运动。球囊可与膨胀管腔远侧端部流体连通。
7.膨胀管腔可具有小于内部中空管腔的管腔直径的膨胀直径。
8.球囊可靠近管状主体远侧端部附连。
9.管状主体远侧端部可具有从第一位置处的较宽厚度渐缩至第二位置处的较窄厚
度的壁厚。第一位置可在球囊的近侧方向上,并且第二位置可在球囊下方。
10.管状主体远侧端部可包括被设置在球囊下方的柔性部分。柔性部分可比管状主体的靠近球囊的部分更具柔性并且在球囊的近侧方向上。
11.膨胀管腔可位于内部中空管腔中。当膨胀管腔位于内部中空管腔中时,膨胀直径可小于内部中空管腔的管腔直径。膨胀管腔可至少部分地偏心于管状主体。
12.膨胀管腔可位于管状主体的外部。
13.所公开的技术还包括导管,该导管包括具有内部中空管腔的基本上管状的主体、限定延伸穿过所述导管的内部中空管腔的内表面、延伸管状主体的长度的大部分的流体管腔、以及围绕管状主体和流体管腔的外部套管。外部套管可延伸管状主体的长度的大部分。外部套管可足以将流体管腔沿管状主体的长度的大部分固定到管状主体。
14.管状主体可包括外表面,并且流体管腔可被设置在管状主体的外表面上。
15.流体管腔可被设置在外表面的一侧上。
16.导管可进一步包括附连到管状主体的远侧端部的球囊。球囊可与流体管腔流体连通。
17.流体管腔可具有基本上新月形的横截面。
18.流体管腔可包括聚合物,诸如pet。
19.管状主体可包括至少一个增强编织物或线圈。
20.所公开的技术还可包括用于展开球囊引导导管的方法。该方法可包括将球囊引导导管推进到患者的脉管系统中。球囊引导导管可包括管状主体、膨胀管腔和球囊,该管状主体具有远侧端部、内部中空管腔,该膨胀管腔具有靠近管状主体的远侧端部附连到管状主体的远侧端部并且延伸管状主体的长度的大部分。该方法可包括在导管被推进穿过脉管系统时使膨胀管腔独立于管状主体挠曲以有利于导管的柔性运动以及使球囊通过膨胀管腔膨胀。
21.该方法可进一步包括将中间导管通过球囊引导导管推进至目标位置并且抽吸闭塞性血栓。
22.该方法可进一步包括将微导管和凝块取出装置通过所述球囊引导导管推进至目标位置,并且展开所述凝块取出装置以捕获闭塞性血栓并在抽吸下取出所述血栓。
23.该方法可进一步包括将中间导管、微导管和凝块取出装置通过所述球囊引导导管推进至目标位置,并且展开所述凝块取出装置以捕获闭塞性血栓并在抽吸下取出所述血栓。
附图说明
24.将参考下面的描述并结合附图进一步讨论本发明的上述方面和另外的方面,在这些附图中,类似的编号指示各种图中类似的结构组件和特征部。附图未必按比例绘制,相反,将重点放在示出本发明的原理。附图仅以举例方式而非限制方式描绘了本发明装置的一种或多种具体实施。
25.图1为根据本发明的各方面的球囊引导导管的图示;
26.图2a为根据本发明的各方面的图1中示出的球囊引导导管的导管末端的图;
27.图2b为根据本发明的各方面的图2a中示出的球囊引导导管的导管末端的侧视横
截面图;
28.图3为根据本发明的各方面的具有外部膨胀管腔的另一个示例性球囊引导导管的图示;
29.图4a为根据本发明的各方面的图3中示出的球囊引导导管的导管末端的图;
30.图4b为根据本发明的各方面的具有外部膨胀管腔的球囊引导导管的导管末端的透视图;
31.图5a为根据本发明的各方面的处于收缩状态的具有流体管腔的另一个球囊引导导管的横截面图;
32.图5b为根据本发明的各方面的具有处于膨胀状态的球囊的图5a中所示球囊引导导管的透视图;
33.图5c为根据本发明的各方面的图5b中示出的球囊引导导管的横截面图;
34.图6a示出根据本发明的各方面的与中间导管、微导管和凝块取出装置一起使用以捕获血管中的目标栓塞的球囊引导导管;
35.图6b示出根据本发明的各方面的具有微导管和凝块取出装置的球囊引导导管;并且
36.图7为概述了根据本发明的各方面的用于展开球囊引导导管的步骤的流程图。
具体实施方式
37.球囊引导导管必须足够柔性,同时还具有轴向刚度以通过曲折脉管系统平稳地递送至目标部位。为了实现期望的柔性,可提供与球囊引导导管的中心管腔相比具有小直径的膨胀管腔。膨胀管腔可定位在导管的管状主体的中心管腔内。另选地,膨胀管腔可定位在管状主体的外部。通过从管状主体的外层内移除膨胀管腔,可改善球囊引导导管的柔性,从而允许有效地递送至目标部位。
38.尽管本文详细解释了所公开技术的示例实施方案,但是应当理解可以设想其他实施方案。因此,并不意图将所公开技术的范围限制在以下描述中阐述的或附图中所示的部件的构造和布置的细节。所公开技术能够具有其他实施方案并且能够以各种方式实践或实施。
39.还应该注意的是,除非上下文清楚地指明,否则本说明书和所附权利要求中所用的单数形式“一个/一种”和“所述/该”包括复数指代物。所谓“包含”或“含有”或“包括”是指至少命名的化合物、元素、颗粒或方法步骤存在于组合物或制品或方法中,但不排除存在其他化合物、材料、颗粒、方法步骤,即使其他此类化合物、材料、颗粒、方法步骤具有与命名的那些相同的功能。
40.在描述示例实施方案时,为了清楚起见,将采用术语。旨在使每个术语设想其本领域技术人员理解的最广泛的含义,并且包括以类似方式操作以实现类似目的的所有技术等同物。还应当理解,提到方法的一个或多个步骤不排除存在附加的方法步骤或在那些明确标识的步骤之间的中间方法步骤。在不脱离所公开技术的范围的情况下,可以与本文所述的顺序不同的顺序执行方法的步骤。类似地,还应当理解,提到装置或系统中的一个或多个部件不排除存在附加的部件或在那些明确标识的部件之间的中间部件。
41.如本文所讨论的,脉管系统可为任何“受试者”或“患者”(包括任何人或动物)的脉
管系统。应当理解,动物可为各种任何适用的类型,包括但不限于哺乳动物、兽医动物、家畜动物或宠物类动物等。例如,动物可为专门选择具有与人类相似的某些特征的实验动物(例如,大鼠、狗、猪、猴等)。应当理解,受试者可为例如任何适用的人类患者。
42.如本文所讨论的,针对任何数值或范围的术语“约”或“大约”指示允许零件或部件的集合实现其如本文所述的预期目的的合适的尺寸公差。更具体地,“约”或“大约”可是指列举值的值
±
20%的范围,例如“约90%”可是指71%至99%的值范围。
43.附图示出了根据本发明的大致中空或管状的结构。当在本文中使用时,术语“管状”和“管”应广义地理解,并且不限于为正圆柱体的或横截面为完全圆周的或在其整个长度上具有均匀横截面的结构。例如,管状结构或系统通常被示出为基本上呈正圆柱体的结构。然而,在不脱离本发明范围的情况下,管状系统可具有锥形或弯曲外表面。
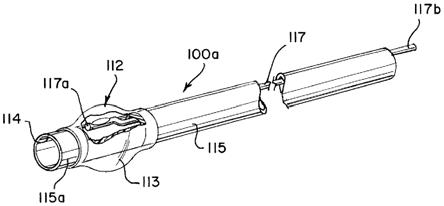
44.现在参见附图,图1和图2a示出了示例性球囊引导导管100a。球囊引导导管100a可包括导管末端112、基本上管状的主体115、膨胀管腔117和球囊113。出于说明的目的,管状主体115被示出为透明的,但在实践中不需要是透明的。
45.管状主体115可为薄的、细长的中空管。管状主体115可包括海波管。常用的海波管材料包括镍钛诺和不锈钢合金。管状主体115可在其整个长度上具有均匀的刚度,或沿长度变化的刚度。管状主体115的刚度分布变化可通过激光切割特征部产生,诸如周向狭槽沟槽和/或纵向或轴向偏移的图案化脊或凹陷部。另选地,管状主体115可为聚合物管。在一些情况下,聚合物管的外表面可包括脊和/或凹陷部以提供增强的扭矩、推动和可跟踪特征。管状主体115的刚度分布的变化可通过利用沿管状主体115具有不同长度和刚度的聚合物材料层来实现。
46.管状主体115的内表面和外表面两者均可由润滑的低摩擦材料(诸如ptfe)制成,或者涂覆有润滑的低摩擦材料。这可有利于导航球囊引导导管100a通过脉管系统,对于沿到达目标部位的路径接触内血管壁而言存在平滑的非研磨性表面。
47.管状主体115可包括内部中空管腔114。内部中空管腔114可用于将其他导管和辅助装置递送到目标部位。在一些示例中,内部中空管腔114还可提供用于抽吸和造影剂注射的通道。管状主体115可具有相对薄的壁,使得内部中空管腔114可具有较大截面面积以用于抽吸和使其他装置通过。内部中空管腔114的尺寸可基于目标部位而变化,或者可使用大约0.087"的标准引导导管内径。如图2a中所示,内部中空管腔114可限定纵向轴线111。
48.膨胀管腔117可为基本上管状的,并且可被设置在内部中空管腔114内。膨胀管腔117可具有远侧端部117a和近侧节段117b。近侧节段117b可沿管状主体115的长度的大部分延伸穿过内部中空管腔114。在一些实施方案中,近侧节段117b可沿管状主体115的整个长度延伸穿过内部中空管腔114。如图2a中所示,膨胀管腔117的近侧节段117b可基本上平行于纵向轴线111延伸,使得膨胀管腔117至少部分地与管状主体115偏心。另选地,膨胀管腔117可被设置成靠近管状主体115的内壁,使得膨胀管腔117偏离纵向轴线111。膨胀管腔117的至少一部分能够相对于管状主体115运动,从而提供增加的球囊引导导管100a柔性。在一些示例中,膨胀管腔117的连杆的大部分能够相对于管状主体运动。例如,当通过脉管系统操纵球囊引导导管100a时,内部中空管腔114内的膨胀管腔117的长度的一些或全部可与管状主体115对准地运动。除此之外或另选地,膨胀管腔117的长度的一些或全部可独立于管状主体115运动。
49.在许多治疗中,希望球囊引导导管100a的远侧长度具有更大的柔性以导航脉管系统,同时球囊引导导管100a的近侧长度具有更大的刚度以被推动。因此,在一些示例中,膨胀管腔117能够相对于管状主体115在整个远侧长度的大部分上运动,并且在整个近侧长度的大部分上附连到管状主体115,使得内部中空管腔114在近侧长度上与内部中空管腔114对准地运动。
50.如图2a中所示,膨胀管腔117可被设置在内部中空管腔114内,使得膨胀管腔117的远侧端部117a终止于管状主体115的远侧端部115a近侧。在该构型中,膨胀管腔117的远侧端部117a和球囊113可流体连通。膨胀管腔117可注射流体和/或其他膨胀介质以使球囊113膨胀。当膨胀时,球囊113可紧贴血管的内壁。膨胀球囊113可具有卵形或锥形形状,具有用于与脉管系统壁界面接触的无创伤的大的扩张式曲率半径。
51.球囊113可靠近管状主体115的远侧端部115a安装。在一些实施方案中,球囊113可被安装到管状主体115的远侧端部115a的外表面,使得球囊113和管状主体115彼此齐平。因为膨胀管腔117完全在内部中空管腔114内,所以球囊113可沿管状主体115的整个圆周与管状主体115的远侧端部115a的外表面齐平地被安装。齐平安置可为球囊引导导管100a提供平滑的递送轮廓。球囊113可通过机械构件(诸如环形扎绞带或条带)安装到远侧端部115a的外表面,或者其可通过其他方式压接、焊接或附接。在一个示例中,球囊使用合适的粘合剂方式(诸如环氧树脂或氰基丙烯酸酯)附接。
52.管状主体115的远侧端部115a可被修改,以便增加球囊引导导管100a的柔性。以举例的方式,与从远侧端部115a延伸的管状主体115的壁相比,远侧端部115a的壁可具有减小的厚度。在这种意义上,管状主体115可具有从第一位置处的较宽厚度渐缩至第二位置处的较窄厚度的壁厚。第一位置可相对于球囊113在近侧。第二位置可在球囊113下方。另选地或除此之外,柔性材料可被设置在管状主体115的远侧端部115a处,使得柔性材料被设置在球囊113下方。以举例的方式,柔性材料可包括弹性体材料,包括但不限于具有介于大约25d和大约40d之间的硬度的弹性体以及弹性体在相同硬度范围内的共混物。柔性材料可为与管状主体115不同的材料。柔性材料可比管状主体115的材料更具柔性。对管状主体115的远侧端部115a的这些修改可增加球囊引导导管100a的远侧端部115a处的柔性,同时还沿导管100a的长度的大部分保持轴向刚度,使得球囊引导导管100a可安全且有效地操纵穿过患者的脉管系统至目标部位。
53.球囊113可由多种材料中的任一种构造,诸如氯丁二烯、聚氨酯、尼龙、pbx或任何其它热塑性弹性体。这些材料使得球囊113耐用且薄。球囊113可为气体可渗透的。另选地,球囊113可为气体不可渗透的。就无创伤润滑性而言,球囊113的外表面可涂覆有亲水性涂层,并且球囊113可被成形为使得在膨胀时存在最小的血管壁收缩。
54.图2b示出了图2a中所示球囊引导导管100a的导管末端112的侧视横截面图。管状主体115可包括内部中空管腔114。膨胀管腔117可被设置在内部中空管腔114内。在一些情况下,膨胀管腔117被设置在内部中空管腔114内并且靠近管状主体115的顶部内表面,如图2b中所示。在一些情况下,膨胀管腔117可被设置在内部中空管腔114内并且靠近管状主体115的侧视内表面或底部内表面。在一些情况下,膨胀管腔117可被设置成基本上偏心于内部中空管腔114和管状主体115。在导管100a弯曲时,膨胀管腔117的所示部分相对于内部中空管腔114自由运动。
55.膨胀管腔117可具有第一直径d1,并且内部中空管腔114可具有第二直径d2。第一直径d1可小于第二直径d2。在一些实施方案中,第一直径d1可为第二直径d2的大约四分之一。在一些实施方案中,第一直径d1可为第二直径d2的大约一半。第一直径d1可小于第二直径d2,因为球囊膨胀所需的膨胀介质的体积通常不是很大。
56.图3至图4b示出了相对于管状主体115具有外部膨胀管腔117的球囊引导导管100b。膨胀管腔117可具有远侧端部117a和近侧节段117b。近侧节段117b可从远侧端部117a延伸并且可延伸管状主体115的长度的大部分。远侧端部117a可靠近管状主体115的远侧端部115a。球囊113可接合到管状主体115的远侧端部115a的外表面的至少一部分和膨胀管腔117的远侧端部117a的至少一部分,使得膨胀管腔117可与球囊113流体连通。球囊113可使用任何附接机构接合到管状主体115的外表面和膨胀管腔117的远侧端部117a的外表面,所述附接机构包括但不限于环形扎绞带或条带、粘合剂、压接或焊接。
57.如图4a中所示,膨胀管腔117可相对于纵向轴线111平行于管状主体115延伸。膨胀管腔117被示出为相对于管状主体115和内部中空管腔114径向向下或“6点钟”取向。尽管在膨胀管腔117平行于管状主体115延伸时,膨胀管腔117的外表面和管状主体115的外表面可在膨胀管腔117的长度的一些或全部上彼此接触,膨胀管腔117的外表面不附连到管状主体115的外表面,使得膨胀管腔117可在未附连长度上不独立或独立于管状主体115运动和/或操纵。如此构造时,与膨胀管腔117附连到管状主体115的导管100b的柔性相比,在球囊引导导管100b通过其中膨胀管腔117未附连到管状主体115的脉管系统操纵时,导管100b可具有增加的柔性。该增加的柔性可有利于球囊引导导管100b至血管内的目标位置的有效递送。
58.图4b示出了具有外部膨胀管腔117的球囊引导导管100b。膨胀管腔117被示出为相对于管状主体115和内部中空管腔114径向向上或大致处于“12点钟”取向。球囊113可接合到管状主体115的远侧端部115a的外表面的至少一部分和膨胀管腔117的远侧端部117a的至少一部分,使得膨胀管腔117可与球囊113流体连通。球囊113可使用任何附接机构接合到管状主体115的远侧端部115a的外表面和膨胀管腔117的远侧端部117a的外表面,所述附接机构包括但不限于环形扎绞带或条带、粘合剂、压接或焊接。
59.因为膨胀管腔117的第一直径d1可相对较小,因此膨胀管腔117基本上不影响管状主体115的外部轮廓。在这种意义上,球囊引导导管100b可被有效地操纵穿过脉管系统。
60.通过将膨胀管腔117定位在内部中空管腔114内或直接沿管状主体115的外表面定位,如图1至图4b中所示,球囊引导导管100可表现出与在管状主体的外层内包括膨胀管腔的其他现有球囊引导导管相比改善的柔性。改善的柔性可有利于球囊引导导管100在脉管系统内的安全且有效的导航和定位。
61.图5a至图5c示出了具有流体管腔118的球囊引导导管200。图5a示出了处于收缩状态的球囊引导导管200的横截面图,其中该横截面相对于球囊113在近侧方向上截取,作为与图5c的横截面类似的位置,如图5b中所示。球囊引导导管200可包括基本上管状的主体115。管状主体115可具有内表面116和外表面124。内表面116可限定内部中空管腔114并且可延伸管状主体115的长度。内部中空管腔114可用于将其他导管和辅助装置递送至目标部位,并且还作为用于抽吸和注射造影剂的通道。
62.球囊引导导管200可包括被设置在管状主体115的外表面124的侧面126上的流体管腔118。流体管腔118可延伸管状主体115的长度的大部分。在一些实施方案中,流体管腔
118可延伸管状主体115的整个长度。
63.流体管腔118可具有多种横截面形状。以举例的方式,流体管腔118可具有基本上新月形的横截面,如图5a至图5c中所示。另选地,流体管腔118可具有基本上圆形、椭圆形或三角形或多边形的横截面。
64.流体管腔118可基本上由薄的、非适形的材料制成。流体管腔118可基本上由一种或多种热塑性聚合物制成,包括但不限于聚对苯二甲酸乙二醇酯(pet)、聚四氟乙烯(ptfe)、聚乙烯(pe)、氟化乙烯丙烯(fep)等。
65.外部套管120可围绕管状主体115的外表面124和流体管腔118。外部套管120可延伸管状主体115的长度的大部分。在一些实施方案中,外部套管120可延伸管状主体115的整个长度。外部套管120可提供结构稳定性并且可沿管状主体115的长度的大部分将流体管腔118固定到管状主体115。外部套管120可基本上由弹性材料制成,并且可提供外表面润滑性而不会由于弹性材料的柔软性而显着增加刚度。以举例的方式,弹性材料可为高密度聚乙烯。
66.特别是推进穿过曲折脉管系统可导致球囊引导导管200和膨胀管腔117和/或内部中空管腔114扭结或卷曲。内部中空管腔114的扭结可导致导丝或其他装置上的束缚。扭结的膨胀管腔117可抑制往返于球囊引导导管200的球囊113的流动。在一些极端情况下,扭结的膨胀管腔117可导致球囊完全失效或者丧失使球囊113膨胀或收缩的能力。这可能在治疗期间引起并发症,因为可能需要移除非功能性球囊引导导管,医师可能需要在不阻止血流的情况下进行手术,或者一些其他装置可能需要通过膨胀管腔插入以使球囊收缩。
67.为了使扭结最小化,管状主体115可包括支撑结构122。支撑结构122可被设置在管状主体115的内表面116和管状主体115的外表面124之间。支撑结构122可为至少一个加强组件。加强组件可为加强编织物和/或线材线圈。支撑结构122可包括任何数量的加强组件。可以调节和操纵编织物和/或线圈的密度或其构造中所用的材料以改变球囊引导导管200的轴向刚度分布。例如,改变编织物和/或线圈的密度、材料或构型可增加管状主体115的远侧端部115a的柔性,同时仍然最小化膨胀管腔117扭结的可能性。
68.图5b和图5c示出了处于膨胀状态的球囊引导导管200。球囊113可接合到管状主体115的远侧端部115a的外表面124和外部套管120,使得流体管腔118与球囊113流体连通。因为球囊在最远侧端部处接合到管状主体115并且在另一端部处接合到外部套管,所以球囊113未被安装成与管状主体115齐平。
69.流体管腔118可被用作注射膨胀介质以使球囊113膨胀的导管。如图5a至图5c中所示,流体管腔118与内部中空管腔114分开且不同,使得流体管腔118可独立于内部中空管腔114使球囊113膨胀。图5c示出了处于膨胀状态的球囊引导导管200的横截面图。如图5c中所示,当流体管腔118注射膨胀介质时,流体管腔118可膨胀。将图5a与图5c进行比较,当膨胀时(图5c),流体管腔118可具有相比于未膨胀时(图5a)更大的横截面积。因此,外部套管120可被配置为当流体管腔118膨胀时允许流体管腔118的形状改变。当导管200弯曲或以其他方式操纵时,外部套管120可进一步允许流体管腔118的形状改变。
70.尽管图5a至图5c示出了包括支撑结构122的管状主体115,可以设想的是,球囊引导导管200可包括没有支撑结构122的管状主体115。通过不包括支撑结构122,球囊引导导管200可沿管状主体115的整个长度具有增加的柔性。
71.如关于球囊引导导管100所述,可修改管状的远侧端部115a,以便增加球囊引导导管200的远侧端部115a处的柔性,同时还沿导管200的长度的大部分保持足够的轴向刚度。与从远侧端部115a延伸的管状主体115的壁相比,远侧端部115a的壁可具有减小的厚度。另选地或除此之外,柔性材料可被设置在管状主体115的远侧端部115a处,使得柔性材料被设置在球囊113下方。
72.图6a和图6b示出了与其他机械血栓切除设备结合使用的球囊引导导管100、200。参见图6a,球囊引导导管100、200可通过目标血管20推进到闭塞凝块40的近侧的部位。可使球囊113膨胀以阻止血管20中的近侧流动。进入导管,诸如中间导管35或抽吸导管可被推进通过并超过球囊引导导管100、200的远侧端部到达目标。容纳凝块取出装置60的微导管70可被进一步推进通过中间导管35和球囊引导导管100、200,并且被展开以捕获凝块40,同时通过导管中的一个或多个抽吸。在捕获凝块40后,可将凝块取出装置60撤回到中间导管35中,中间导管可压缩凝块取出装置60的结构并且增强在取出期间施加到凝块上的夹持力。凝块取出装置60、微导管70、中间导管35和凝块40可然后撤回经过球囊引导导管100、200并且从患者体内完全移除。
73.如图6b中所示,球囊引导导管100、200可通过目标血管(包括颈内动脉)操纵到目标位置,并且球囊113可膨胀。膨胀球囊113可阻挡目标位置近侧的血液,从而防止血液干扰凝块的捕获。微导管70和凝块取出装置60可被推进穿过内部中空管腔114并且直接从管状主体115的远侧端部115a展开。凝块取出装置60可包括装置轴64,使得凝块取出装置60可有效地到达并捕获凝块。可通过球囊引导导管100、200的内部中空管腔114施加抽吸,以防止碎片或残片从目标部位向远侧迁移。尽管膨胀管腔117可阻挡内部中空管腔114的横截面的一部分,但抽吸在一些治疗和特定装置构型中仍然可能是有效的。作为膨胀管腔117的位置造成的任何潜在缺点的折衷,潜在优点是,与在球囊引导导管的外层内具有膨胀管腔的球囊引导导管相比,球囊引导导管100a的远侧端部可具有更大的柔性。改善的柔性可有利于将球囊引导导管100a导航到凝块40并成功地取出凝块40。如果需要附加的取出尝试来清除血管,则可将微导管70和凝块取出装置60迅速递送回目标部位。
74.凝块取出装置60可为任何数量的可商购获得的产品。一些凝块取出装置可在捕获时压缩凝块以获得牢固的夹持,然而,这可使凝块更紧实或“更粘”,从而使取出复杂化。其他凝块取出装置可在凝块和血管之间膨胀,以使压缩最小化,同时使凝块从血管壁松开。凝块取出装置可基本上由镍钛诺或具有足够弹性应变能力的其它形状记忆材料制成,使得当凝块取出装置在微导管内处于收缩构型时不超过弹性极限。该弹性应变能力允许装置在微导管内有效地“弹簧加载”,使得当展开时,其能够自膨胀以接合凝块。
75.手术期间球囊引导导管100、200的放置可通过添加射线不可透的标记物来辅助。此类标记物可包括射线不可透的合金元素,诸如钯、铂、金等。例如,射线不可透的标记物可在管状主体115的远侧端部115a处放置在球囊113的远侧。
76.图7示出了概述展开球囊引导导管的方法700的流程图。该方法700可包括以非特定顺序呈现的以下步骤中的一个或多个。示例性方法700可包括如相关领域中技术人员了解和理解的附加步骤。示例性方法可通过如本文所公开的示例性球囊引导导管、其变型或如本领域普通技术人员了解和理解的其另选方案来执行。
77.在步骤710中,球囊引导导管被推进到患者的脉管系统中。球囊引导导管可包括管
状主体、膨胀管腔和球囊,该管状主体具有远侧端部、内部中空管腔,该膨胀管腔具有靠近管状主体的远侧端部附连到管状主体的远侧端部并且延伸管状主体的长度的大部分。
78.在步骤720中,在导管被推进穿过脉管系统时,独立于管状主体的膨胀管腔可挠曲以有利于导管的柔性运动。
79.在步骤730中,球囊可通过膨胀管腔膨胀。
80.除了将球囊引导导管推进至患者的脉管系统中之外,方法700还可包括将中间导管通过球囊引导导管推进至目标位置。在适当地将中间导管定位在目标位置处时,可抽吸闭塞性血栓。
81.方法700还可包括将微导管和凝块取出装置通过球囊引导导管推进至目标位置。一旦将微导管适当地定位在目标位置处,就可展开凝块取出装置以捕获闭塞性血栓。然后可在抽吸下取出所捕获的血栓。
82.方法700还可包括将中间导管、微导管和凝块取出装置通过球囊引导导管推进至目标位置。可展开凝块取出装置以捕获闭塞性血栓。然后可在抽吸下取出所捕获的血栓。
83.本文所包含的描述是本发明的实施方案的示例,并且不旨在以任何方式限制本发明的范围。虽然描述了本发明的具体示例,但在不脱离本发明的范围和实质的前提下,可对装置和方法进行各种修改。例如,虽然本文所述的示例涉及特定部件,但本发明包括利用部件的各种组合实现所述功能、利用另选的材料实现所述功能、组合各个示例的部件、将各个示例的部件与已知部件组合等的其它示例。本发明设想用其它熟知的和可商购获得的产品替换本文所示的组成部件。对于本发明所涉及的领域内的普通技术人员而言,这些修改通常是显而易见的并且旨在落入以下权利要求书的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1