包含C-O-P键的衍生物在患有肾功能衰竭的患者中的用途的制作方法
包含c-o-p键的衍生物在患有肾功能衰竭的患者中的用途
1.本技术是申请日为2014年3月14日、申请号为201480021589.1、发明名称为“包含c-o-p键的衍生物在患有肾功能衰竭的患者中的用途”的发明专利申请的分案申请。
技术领域
2.本发明涉及长效形式的包含c-o-p键的化合物用于治疗患有肾功能衰竭的患者的疾病中的用途,而不管该化合物是否进行其他的治疗。
背景技术:
3.肾功能衰竭(也称为肾功能损害或肾脏疾病)为导致肾脏功能进程性损失的疾病,并伴有肾小球率过滤(gfr)或指数降低。尽管肾脏损伤的初始阶段可以是无临床症状的,但是随着疾病的进展,则呈现尿毒症。尿毒症是描述由于肾脏不正确地过滤和排除毒素而导致血液污染的概念。
4.肾脏疾病可以分类为:
[0005]-急性肾损伤:肾脏功能的进程性损失,其通常导致少尿以及流体和电解质失衡。必须通过透析进行治疗,直至病因可以被确认并治疗。
[0006]-慢性肾脏病(ckd):肾脏功能经历几个月或几年而更缓慢地损失。根据肾脏功能的程度,基于gfr来定义ckd的5个阶段:
[0007]
ο阶段1:正常或较高的gfr(》90ml/min)
[0008]
ο阶段2:轻微的ckd。gfr=60-89ml/min
[0009]
ο阶段3:中等的ckd。gfr=30-59ml/min
[0010]
ο阶段4:炎症的ckd。gfr=15-29ml/min
[0011]
ο阶段5:晚期ckd。gfr《15ml/min。需要透析或肾脏移植来保持健康状态。
[0012]
此外,急性肾功能衰竭可以伴有ckd发生,其称为慢加急性肾脏衰竭。
[0013]
使用不同的治疗备选方案来治疗遭受所述状况的患者。在其他的功能中,肾脏与肝脏一起负责活化维生素d(vitd),其在钙的动态平衡中起重要的作用。患有肾脏损害的患者因此呈现vitd缺乏,结果这是第一待引入的药理学治疗。
[0014]
肾脏损害与疾病的治疗一起导致高钙血症和高磷血症。因此,使用一种或多种磷结合剂来治疗患有肾功能衰竭的患者,从而降低血液中的磷的浓度,并且使用拟钙剂通过控制甲状旁腺激素(pth)的水平来控制血浆中钙的水平。本文所述的一种或多种磷结合剂包括司维拉姆,以及镧、铁、钙及其他金属的多种盐。主要的拟钙剂为西那卡塞和kai-4169。此外,还存在其他类型的辅助药剂,其在肾脏损害中给药,用于调节血压、胆固醇、利尿用途、硫代硫酸钠或二磷酸盐。
[0015]
高钙血症和高磷血症可以导致心血管钙化,但是抑制因子(例如基质 gla蛋白、骨桥蛋白、胎球蛋白、维生素k)缺乏或促进因子(维生素d、 fgf23、炎性细胞因子、脂质沉积、凋亡小体、核复合物等)失衡可以延迟或加速所述的过程。患有肾脏损害的患者通常描述为患有ckd-mbd的患者(慢性肾脏疾病-骨矿物质病),因为改变的肾脏功能会激起作用级联,
这些作用还会影响骨重塑。
[0016]
已经显示,冠状动脉钙化的程度与较低的存活以及更大量的心血管事件有关(rs shantouf,mj budoff,n ahmadi,a ghaffari,f flores,a gopal,nnoori,j jing,cp kovesdy,k kalantar-zadeh.total and individual coronaryartery calcium scores as independent predictors of mortality in hemodialysispatients.am j nephrol 2010;31:419-425)。
[0017]
具体而言,已经显示,未患有可测量的冠状动脉钙化的患者(cac=0) 呈现出较低百分率的心血管事件以及较低的死亡率。当cac得分升高时,心血管事件的数量也增加,但是存活减少。
[0018]
此外,russo等人(d russo,s corrao,y battaglia,m andreucci,acaiazza,a carlomagno,m lamberti,n pezone,a pota,l russo,m sacco,bscognamiglio.progression of coronary artery calcification and cardiac eventsin patients with chronic renal disease not receiving dialysis.kidney int 2011;80:112-118)证明,血管钙化更快速地进展与较低的存活以及更高风险的心血管意外事件有关。
[0019]
如此,心血管事件(包括死亡)与2个参数有关:
[0020]-血管钙化的程度。
[0021]-所述的血管钙化的进展的速度。
[0022]
目前,还没有被批准的能够证明在透析患者中具有较高的存活或较低的心血管意外事件的治疗,并且仍需要治疗与肾脏损害有关的不同疾病 (由肌体的钙化过程和骨重塑失衡所导致)。
[0023]
已经报道其结构包含磷的多种化合物(焦磷酸盐、二磷酸盐、肌醇磷酸盐、六偏磷酸盐等)能够抑制含钙晶体的形成。已经发现,在包含c-o-p 键的这种大家族中,一些化合物能够抑制多种类型的钙化,但是还尚未证明这些治疗可用于存在的肾脏损害,因为已知的研究或者与正常肾脏功能有关,或者在尿毒症的情况下,未发现所述的化合物是有效的。
[0024]
发明概述
[0025]
意想不到的是,本发明的发明人发现了在患有肾功能衰竭的个体中用于长效给药的形式,其允许式i所示的化合物的效力被再建,其中所述的式i所示的化合物在其他形式下在患有尿毒症的个体中是无效的。所述的长效给药与团注或短期输注类型的给药相反,并允许足够水平的这些化合物被保持,或者甚至在足的时期内在血液中再建。结果,在所述的疾病的早期或者当此类疾病已经建立时,预防、治疗、抑制和/或缓和肾脏损害有关的疾病,或者预防它们的进展。
[0026]
因此,本发明的一个实施方案涉及式i所示的至少一种化合物及其药物可接受的盐用于制备治疗患有肾功能衰竭的受试对象中的肾功能衰竭相关疾病的药剂的用途,其中所述的肾功能衰竭可表征为以长效形式给药所述的药剂:
[0027][0028]
其中:
[0029]
r1至r
12
均独立地表示h,-x,-ox,-nhx,-nx2,-sx,-oso3hx,-oso3x2或式ii所示的化合物:
[0030][0031]
其中各个x独立地表示h,c
1-30
烷基,c
2-30
烯基,c
2-30
炔基或cy1,其中c
1-30
烷基,c
2-30
烯基和c
2-30
炔基独立地可任选地被一个或多个r
14
取代,并且其中cy1可任选地被一个或多个r
15
取代;cy1表示碳环的或杂环的3至10 元环,其可以是饱和的,部分不饱和的或芳香族的,其中所述的杂环具有选自o、s和n的1个至4个杂原子,其中所述的环可以通过任何可利用的c原子与所述的分子的剩余部分键合,并且其中cy1可任选地与1个至 4个5元或6元环稠合,每个环是饱和的、部分不饱和的或芳香族的碳环或杂环,并且其中所述的稠合的杂环可以包含选自o、n和s的1个或2 个杂原子;
[0032]
各个r
13
独立地表示h,c
1-30
烷基,-nh2,-nhc
1-30
烷基或n(c
1-30
烷基)2,其中各个c
1-30
烷基独立地可任选地被一个或多个卤素,-oh,-cn和-no2基团取代;以及
[0033]
各个r
14
和r
15
独立地表示-oh,c
1-30
烷氧基,c
1-30
烷基亚硫酰基,c
1-30
酰氧基,磷酸盐,卤素,三卤化c
1-30
烷基,腈或叠氮化物,前体条件是r1至r
12
的至少一者独立地表示式ii所示的化合物。
[0034]
在另一个实施方案中,本发明涉及上文定义的用途,其中:各个x优选地独立地表示h,c
1-30
烷基或cy1,其中c
1-30
烷基可任选地被一个或多个 r
14
取代,并且其中cy1可任选地被一个或多个r
15
取代;并且每个r
14
和 r
15
独立地表示-oh,c
1-30
烷氧基,c
1-30
烷基亚硫酰基,c
1-30
酰氧基,磷酸盐, 卤素,三卤化c
1-30
烷基,腈或叠氮化物。
[0035]
在另一个实施方案中,本发明涉及上文定义的用途,其中:各个x表示h,c
1-30
烷基或cy1。
[0036]
在另一个实施方案中,本发明涉及上文定义的用途,其中:各个x表示h。
[0037]
在另一个实施方案中,本发明涉及上文定义的用途,其中:自由基r1, r3,r5,r7,r9和r
11
的至少一者独立地表示式ii所示的化合物:
[0038][0039]
各个r
13
独立地表示h,c
1-30
烷基,-nh2,-nhc
1-30
烷基或-n(c
1-30
烷基)2,其中各个c
1-30
烷基独立地可任选地被一个或多个卤素,-oh,-cn和-no2基团取代;并且r2,r4,r6,r8,r
10
和r
12
独立地表示h。
[0040]
在另一个实施方案中,本发明涉及上文定义的用途,其中:r1,r3,r5, r7,r9和r
11
独立地表示式ii所示的化合物:
[0041][0042]
各个r
13
独立地表示h或c
1-30
烷基,其中各个c
1-30
烷基独立地可任选地被一个或多个卤素,-oh,-cn和-no2基团取代;并且r2,r4,r6,r8,r
10
和r
12
独立地表示h。
[0043]
在另一个实施方案中,本发明涉及上文定义的用途,其中:r1,r3,r5, r7,r9和r
11
独立地表示式ii所示的化合物:
[0044][0045]
各个r
13
独立表示h或c
1-30
烷基;并且r2,r4,r6,r8,r
10
和r
12
独立地表示h。
[0046]
在另一个实施方案中,本发明涉及上文定义的用途,其中:r1,r3,r5, r7,r9和r
11
独立地表示式ii所示的化合物:
[0047][0048]
各个r
13
独立表示h;并且r2,r4,r6,r8,r
10
和r
12
独立地表示h。
[0049]
在本发明的另一个实施方案中,涉及上文定义的用途,其中式i所示的化合物为肌醇六磷酸盐(ip6)。
[0050]
肌醇磷酸盐可以通过在体内的脱磷酸作用而形成其他的肌醇磷酸盐 (ip5,ip4,ip3,ip2,ip1或肌醇)。假设肌醇是指该分子的任何异构体形式。
[0051]
式i所示的所有化合物包含c-o-p键。所述的键为所述的化合物提供对含钙晶体的
亲和性以及体内水解的足够不稳定的键,由此抑制含钙晶体(例如羟磷灰石(hap))在骨中的不可逆的结合,这种结合对骨重塑具有不利的影响,当使用二磷酸盐进行长期给药时,情况便是如此,因为这些化合物包含不能被肌体水解的p-c-p键。
[0052]
其他特别的情况是不包含所述的c-o-p键的磷酸化化合物,例如焦磷酸盐,其p-o-p键意味着它们在肠内非常容易被水解,因此意味着胃肠外给药是可行的。
[0053]
本发明的化合物(具有c-o-p键)表示足够的中点(由于其效力)并表示以下事实:所述的肌体代表了用于排除所述的化合物的机制,由此降低了副作用的风险。
[0054]
就此而言,本发明人证明所述的化合物快速地与其受体结合,从而允许该化合物在相对短的时间内取得最大的结合,并且所述的结合是可逆的,由此意味着所述的化合物在经过合理的时间后可以由受体的表面上排除。该事实表明关于具有p-c-p键的化合物具有巨大的差异,其在体内在它们受体(例如在骨中)的表面上可以呈现几个月的半衰期,从而影响骨重塑。
[0055]
在另一个实施方案中,本发明涉及上文定义的用途,其还包括选自以下的化合物:拟钙化合物;维生素b,维生素d和维生素k;磷的(磷)螯合剂;硫代硫酸盐,利尿剂,优选为噻嗪化物或吲达帕胺;二磷酸盐或其药物可接受的盐;焦磷酸盐;柠檬酸盐,抗高血压和抗胆固醇试剂。
[0056]
利尿化合物优选包括噻嗪化物或吲达帕胺。
[0057]
在另一个实施方案中,本发明涉及上文定义的用途,其还包括微生物 d和/或k。
[0058]
在整个本发明中,术语“c
1-30
烷基”作为基团或基团的一部分是指包含1至30个碳原子的线性或支化的链烷基团,包括除了其他以外的甲基, 乙基,丙基,异丙基,丁基,异丁基,仲丁基,叔丁基,戊基,己基,癸基和十二烷基基团。
[0059]
术语“c
2-30
烯基”是指包含2至30个碳原子的线性或支化的烷基链,并且还包含一个或多个双键。其实例包含除了其他以外的乙烯基,1-丙烯基, 2-丙烯基,异丙烯基,1-丁烯基,2-丁烯基,3-丁烯基和1,3-丁二烯基。
[0060]
术语“c
2-30
炔基”是指包含2至30个碳原子的线性或支化的烷基链,并且还包含一个或多个三键。其实例包括除了其他以外的乙炔基,1-炔丙基, 2-炔丙基,1-炔丁基,2-炔丁基,3-炔丁基和1,3-丁二炔基。
[0061]
cy1基团涉及3元至10元的碳环或杂环,其可以是饱和的、部分不饱和的或芳香族的,并且其通过任何可利用的c原子与所述的分子的剩余部分键合。当cy1基团为杂环时,cy1包含选自n、o和s的1个至4个杂原子。此外,cy1可以可任选地与至多4元、5元或6元碳环或杂环稠合,所述的cy1可以是饱和的、部分不饱和的或芳香族的。如果稠环为杂环,则所述的环包含选自n、o和s的1个或2个杂原子。cy1的实例包括除了其他以外的苯基,萘基,噻吩基,呋喃基,吡咯基,噻唑基,异噻唑基, 咪唑基,吡唑基,1,2,3-三唑基,1,2,4-三唑基,四唑基,1,3,4-噻二唑基,1,2,4
‑ꢀ
噻二唑基,吡啶基,吡嗪基,嘧啶基,哒嗪基,苯并咪唑基,苯并呋喃基, 异苯并呋喃基,吲哚基,异吲哚基,苯并噻吩苯基,苯并噻唑基,环丙基, 环丁基,环戊基,环己基,环庚基,吖丁啶基和氮丙啶基。
[0062]c1-30
烷氧基作为基团或基团的一部分是指-oc
1-30
烷基,其中c
1-30
烷基部分具有上文相同的含义。其实例包括甲氧基,乙氧基,丙氧基,异丙氧基基,丁氧基,异丁氧基,仲丁氧基和叔丁氧基。
[0063]c1-30
烷基亚硫酰基作为基团或基团的一部分是指-soc
1-30
烷基,其中 c
1-30
烷基部分具有上文相同的含义,其实例包括甲基亚硫酰基,乙基亚硫酰基,丙基亚硫酰基,异丙基亚硫酰基,丁基亚硫酰基,异丁基亚硫酰基, 仲丁基亚硫酰基和叔丁基亚硫酰基。
[0064]c1-30
酰氧基作为基团或基团的一部分是指-coc
1-30
烷基,其中c
1-30
烷基部分具有上文相同的含义。其实例包括乙酰基(acetyl),乙酰基 (ethanoyl),丙酰基和2,2-二异丙基戊酰基。
[0065]
卤素自由基或其卤素简称是指氟、氯、溴和碘。
[0066]
三卤化c
1-30
烷基表示c
1-30
烷基的3个氢原子被上文所定义的3个卤素自由基所取代而得到的基团。其实例包括除了其他以外的三氟甲基,三溴甲基,三氯甲基,三碘甲基,三氟乙基,三溴乙基,三氯乙基,三碘乙基, 三溴丙基,三氯丙基和三碘丙基。
[0067]-nhc
1-30
烷基表示-nh2基的1个氢原子被上文所定义的c
1-30
烷基所取代而得到的基团。其实例包括除了其他以外的甲基胺,乙基胺,丙基胺,丁基胺和戊基胺。
[0068]-n(c
1-30
烷基)2表示-nh2基的2个氢原子被上文所定义的c
1-30
烷基所取代而得到的基团。其实例包括其他以外的二甲基胺,二乙基胺,二异丙基胺,二丁基胺和二异丁基胺。
[0069]
表达“可任选地被一个或多个
……
取代”表示这样的可能性:基团可以被一个或多个取代基取代,优选为1、2、3或4个取代基,更优选为1、 2或3个取代基,甚至更优选为1或2个取代基,前提条件是所述的取代基具有足够取代可利用的位置。如果存在取代基,则所述的取代基可以是相同的或不同的,并且可以位于任何可利用的位置。
[0070]
本发明的另一个方面涉及组合物的用途,其中所述的组合物包含上文所述的通式i所示的至少一种化合物、以及另一种活性物质和/或药物可接受的媒介物。
[0071]
所述的活性物质选自拟钙剂、维生素、磷结合剂、硫代硫酸盐、二磷酸盐、焦磷酸盐、柠檬酸盐、利尿剂、抗高血压试剂和抗胆固醇试剂,其用于制备在患有肾功能衰竭的受试对象中用于治疗和/或预防肾功能衰竭相关疾病的药剂,其中所述的肾功能衰竭可表征为以长效形式给药所述的药剂。
[0072]
所述的化合物通常用于治疗肾脏损害相关的疾病。ckd-mbd总是具有钙和磷的代谢失衡,这导致高钙血症和高磷血症,这是潜在的问题并且在骨(其主要由hap(磷酸钙)组成)不能再作为血液中过量的钙和磷的缓冲剂时便进入上述阶段,由此意味着含钙晶体沉积在肌体中不同的组织和器官中。结果,上述段落中所述的不同药品在不同的水平下发挥作用,但都具有单一的目的,即,帮助控制所述的钙和磷的代谢失衡。
[0073]
作为活性物质描述的多种化合物通过修改含钙晶体的结构中存在的离子浓度而改变结晶过程的热力学,其中所述的含钙晶体直接或间接导致肾功能衰竭相关的疾病。该亚组包括拟钙剂、磷结合剂、硫代硫酸盐、vitd 和利尿剂。
[0074]
拟钙剂允许通过调节血液pth水平来控制钙和磷的浓度。所述的化合物包括西那卡塞,nps r-467,nps r-568,kai-4169。
[0075]
硫代硫酸盐为减少血液中游离钙浓度的螯合剂。
[0076]
尽管具有不同的作用机制,但是vitd具有相似的效果。vitd优选选自钙化醇(calciferol),维生素d2(vit d2),维生素d3(vit d3),度骨化醇,帕立骨化醇,阿尔法罗或α-骨化二醇,骨化二醇,骨化三醇,或者它们的衍生物或药物可接受的盐。
[0077]
磷结合剂在磷酸盐被吸附之前通过扣留磷酸盐而在胃肠道起作用,由此降低其在
血液中的系统浓度。磷酸盐结合剂可以包含金属或者是不含金属的。不含金属的螯合剂包括司维拉姆。含金属的螯合剂包括多种钙、铁、镧、铝和镁盐。
[0078]
此外,利尿剂还通过改变体积而改变钙和磷的浓度,从而影响热力学。利尿剂优选为噻嗪化物,噻嗪化物类(吲达帕胺,氯噻酮,美托拉宗等),袢利尿剂(布美他尼,依他尼酸,呋塞米,托塞米等),碳酸酐酶抑制剂,渗压性利尿剂,留钾利尿剂等。噻嗪化物优选为氯塞嗪,依匹噻嗪,苄氟甲噻嗪或氢氯苯噻。
[0079]
其余的化合物(焦磷酸盐、柠檬酸盐、二磷酸盐、抗高血压试剂、抗胆固醇试剂、vit b、vit k)通过试图终止结晶过程以动力学的方式针对改变的钙和磷的代谢、或者通过增加抑制因子(焦磷酸盐、柠檬酸盐、vit b、 vit k、二磷酸盐)的量或减少促进因子(在抗高血压试剂的情况下为坏疽的残留物或有机物质,或者在抗胆固醇试剂的情况下为脂质沉积物)的数量而改变骨代谢,从而发挥作用。
[0080]
二磷酸盐可以包含氮或不包含氮。所述的二磷酸盐优选选自依替膦酸盐,阿仑膦酸盐,利塞膦酸盐,唑来膦酸盐,替鲁膦酸盐,帕米膦酸盐, monidronate,奈立膦酸盐,帕米膦酸盐,奥帕膦酸盐,氯膦酸盐,伊班膦酸盐。
[0081]
抗高血压试剂优选为抗利尿剂(上文列出的那些),肾上腺素能神经阻断剂(β阻断剂,α阻断剂,混合的阻断剂),钙通道阻断剂(二氢吡啶或非二氢吡啶),肾素抑制剂,血管紧张素转化酶抑制剂,血管紧张素ii受体拮抗剂,醛固酮拮抗剂,血管扩张剂,α-2激动剂或血压疫苗。
[0082]
抗胆固醇试剂优选为斯达汀,贝特类药物,尼克酸,胆汁酸螯合剂, 依替米贝,洛美他派,植物固醇或奥利斯特。
[0083]
在另一个实施方案中,本发明涉及用于治疗患有肾功能衰竭的患者的组合的组合物,其包含上文所定义的式i所示的至少一种化合物,以及单独、同时或依次使用的一种或多种有用的药品,优选地,其中所述的有用的药品由以下列举物中选择:拟钙剂,维生素b、维生素d和维生素k,磷酸盐结合剂、利尿剂等,例如二磷酸盐或其药物可接受的盐、焦磷酸盐、柠檬酸盐、抗高血压试剂或抗胆固醇试剂。
[0084]
在本报告中,术语“组合的制备物”或“并置物”表示组合的制备物的成分不必一起存在于(例如)组合物中,这样所述的成分可以分开或依次用于应用中。因此,表达“并置的”含义是根据多种成分的物理分离,所述的制备物不必是真正的组合。
[0085]
此外,本发明的药物组合物还可以包含一种或多种赋形剂。
[0086]
术语“赋形剂”是指以下物质,其帮助本发明的药物组合物的元素被吸附、稳定所述的元素、活化或帮助组合物的制备(就赋予顺应性或提供使得所述的组合物更宜人的风味而言)。因此,赋形剂可以具有保持所组合的组分(例如淀粉、糖或纤维素,例如作为甜味剂,作为着色剂)、保护所述的组合物(例如将其与空气和/或水分隔离,作为片剂、胶囊或任何其他呈现形式的填料,作为分解剂以确保多种成分被溶解并使其在肠内吸收)的作用,不排除本段中未提及的任何其他类型的赋形剂。
[0087]
如同赋形剂的情况,“药物可接受的媒介物”为组合物中使用的用于将其中所包含的任何成分稀释成预定的体积或重量的物质。药物可接受的赋形剂为惰性物质或者使得包含本发明的药物组合物的任何元素具有类似作用的物质。所述的媒介物的作用是允许引入其他的元素,允许更好地制定剂量和给药,或者为所述的组合物提供顺应性和形状。
[0088]
本发明的另一方面涉及用于治疗患有肾功能衰竭的患者的方法,其包括给药长效(非团注的)形式的治疗有效量的式i所示的化合物或其药物可接受的盐。
[0089]
在本发明中,术语“肾功能衰竭有关的疾病”是指在患有肾脏损害的个体中多种自然的疾病过程,并且可以指但不限于与钙或钙代谢紊乱有关的任何疾病,例如肾石病,心血管钙化,心血管病,骨质疏松症,骨癌,足痛风,钙化性肌腱炎,皮肤钙质沉着症,类风湿关节炎,骨矿物质病,骨软症,动力缺失性骨病,钙过敏。
[0090]
其他的肾功能衰竭的相关疾病可以为心血管类型,例如但不限于冠心病,心力衰竭,心脏病,动脉粥样硬化,动脉硬化,血栓症,高血压,心肌梗死,动脉瘤,心绞痛,周围性血管疾病和脑血管疾病。患有肾脏损害的患者可以遭受心血管意外事件、事件或疾病(缺血,心律失常,心肌梗死,中风等)。
[0091]
一个重要的概念是多种紊乱(包括上述段落中列出的那些)在存在尿毒症的情况下可以通过预防、减少、减慢或终止钙化的进展来治疗。与钙紊乱有关的疾病或者由所述的疾病诱导的钙化在开始给药时可以已经存在,从而减少或终止疾病的进展;或者尚未存在,从而预防疾病的出现或发作。
[0092]
在本发明中,术语“肾功能衰竭”或“肾脏损害”是指肾脏功能减退(gfr)为阶段1至阶段5的任何阶段、急性肾功能损伤或慢加急肾脏衰竭的受试对象。
[0093]
在本发明中,术语个体或受试对象是指任何动物物种,包括人类。
[0094]
在本发明中,术语“长效”、缓释、非团注是指给药形式,其将所述的化合物缓慢地释放至血流中,由此比“团注型”给药更长时间地在血浆中保持较高的水平。团注型给药包括快速静脉注射,例如小于10秒,或者在经历不到大约3分钟的时间内静脉输注。
[0095]
在本发明的实施方案中,长效可以使治疗足够的水平在血液中保持至少30分钟。在肌醇磷酸盐的情况下,所述的足够的水平优选为高于0.15 微摩尔(μm),更优选为高于0.3μm,甚至更优选为高于0.6μm。
[0096]
本发明人意外地发现,并经过比较测试,当受试对象呈现肾脏损害(尿毒症)时,对于血管钙化可以取得在正常肾脏功能状况下的治疗效力。因此,首次描述了可以取得足够的治疗水平并将所述的水平保持足够长时间的非团注型给药是特别有用的,并且还使得副作用降低,由此改善了产品的安全性。所述的非团注给药可以在24小时的时间内、优选为在4小时的时间内、更优选为在20分钟的时间内、甚至更优选为在5分钟的时间内给药。在任何情况下,尽管在经历短时间内进行给药,但是最重要的方面在于非团注型的化合物被释放至血液中的时间被延长,并且可以使治疗水平在血液中保持至少30分钟、优选为超过1小时、更优选为超过3小时、甚至更优选为超过4小时。
[0097]
本发明的重要方面由治疗患有肾脏损害的受试对象从而预防或治疗钙紊乱相关的疾病组成。尽管已经描述具有c-o-p键的化合物能够抑制含钙盐的结晶,但是其在患有肾脏损害的受试对象中使用并且作为非团注型给药是新型的。例如已经描述六磷酸肌醇(ip6)在具有正常肾脏功能的大鼠中用于治疗肾结石(f grases,b isern,p sanchis,jj torres,a costa-bauz
à
,a. phytate acts as an inhibitor of renal calculi.front biosci 2001;12:2580-2587),但是从未证明其在患有肾脏损害的受试对象中对肾结石的作用,所以所述的用途完全是新型的。证明在尿毒症存在下此类化合物在钙紊乱相关的疾病中的效力的多个近期的尝试是失败的,导致本领域的技术人员得出结论,此类化合物在
肾脏损害存在下不能用于治疗所述的疾病。
[0098]
本发明人意外地发现当式i所示的包含c-o-p键的化合物给药患有尿毒症的动物时,在血液中得到更低的水平并保持更短的时间。该发现与本领域技术人员的理解完全相反。当在肾脏损害的状况下给药所述的化合物时,肾脏排出所述的化合物比正常肾脏功能的情况时减少,并且更严重的肾功能不全导致所述的化合物更慢地排出。因此,本领域的技术人员预计当将所述的化合物给药患有肾脏损害的受试对象时,与具有正常肾脏功能的受试对象相比,可以在更长的时间内在血液中获得更高水平的所述的化合物。
[0099]
意想不到的是,本发明人发现式i所示的化合物的行为是完全相对的。近期研发的足够的分析工具允许这种惊人的行为被发现(perello j, maraschiello c,lentheric i,mendoza p,tur f,tur e,encabo m,martin e, benito m,isern b.method for the direct detection and/or quantification of atleast one compound with a molecular weight of at least 200. pct/ep2012/069878),而之前的方法不能使此类化合物在生物基质(例如血液)中被正确地定量。
[0100]
当将式i所示的化合物给药受试对象时,在血液或血浆中得到较低水平的所述的化合物,并且在一些情况下,所述的水平是不可检测的。通过相同的给药途径将相同的剂量给药具有正常肾脏功能的受试对象可以在更长的时间内在血液中具有更高的水平。
[0101]
本发明人发现优化在尿毒症存在下由于所述的化合物的更快地代谢,所以更快地排出所述的化合物。该发现解释了在尿毒症存在下当所述的化合物被迅速破坏(代谢)时,证明此类化合物的效力的多种尝试的失败的原因,在正常肾脏功能的状况下更是如此,并且不能对特定的受体和疾病发挥治疗作用,换言之,更高的代谢速率防止达到治疗水平,以及保持能够证明其效力的足够的时间。
[0102]
本发明的化合物或组合物可以通过能够激发非团注型释放或效果的任何合适的方法来给药,例如血管内(例如静脉内)输注,其他胃肠外(皮下, 皮下储库,腹膜内,肌肉内,皮内,鞘内,硬膜外,脊柱或本领域技术人员已知的其他方式),局部(鼻内,吸入,叶鞘内,经皮或本领域技术人员已知的其他方式),肠内(口服,舌下,直肠等)给药,口服,脊柱,腹膜内制备物或本领域技术人员已知的其他方式。
[0103]
在口服给药的具体情况下,传递技术可以用于在血液中取得更高的水平,或者将所述的水平保持更长的时间,以便得到或增强长效(非团注) 的效果。例如所述的传递技术可以包括使用脂质体、有机聚合物、形成结合或离子对(例如季铵盐)。此外,传递技术可以延迟或调控所述的化合物的吸附,和/或保护所述的化合物在达到血流和/或相应受体之前在胃肠道或肝脏首过效应过程中免于被代谢,这可以有助于保持暴露一定的时间。
[0104]
在使用透析治疗的患者的具体情况下,非常合适的给药方法由通过透析仪器非团注型给药所述的化合物组成(替代将所述的化合物以静脉方式直接注入患者中)。因此,当血液离开患者并通过透析回路循环时,可以使用所述的化合物治疗血液,并且当包含所述的化合物的血液返回至肌体时,所述的化合物以呈现一系列优点的方式引入至血液中。
[0105]
这种给药方法被意外地发现并作为貌似备选的方式。本领域的技术人员无疑地认为通过透析仪器给药是不可行的,因为这些具有相对低分子量的化合物在通过透析膜时容易损失。因此,当血液在肌体外时通过透析系统给药所述的化合物并非是备选的,因为所述的化合物在再次达到受试对象的肌体之前在通过过滤器(透析膜)时会损失(透析掉)。例如
在ip6 的情况下,本发明人以外地发现所述的化合物未损失,因为发现ip6与蛋白质的结合范围为70-90%,因此意味着仅10-30%的化合物可以被透析掉。但是,此外,化合物的高的负电荷产生了静电排斥,这防止它们以显著的方式通过过滤器。
[0106]
此外,本发明人显示所述的化合物,优选为肌醇磷酸盐,可以螯合(扣留)血流中游离的或离子钙,由此降低其浓度,这对于所述的钙是必须的,从而发挥其生物作用。因此,当达到某种血液浓度时,钙的螯合便成问题。非团注型给药是更合适的,因为所述的给药避免了浓度峰,并消除了对钙螯合的影响。
[0107]
此外,在透析患者的情况下,通过透析仪器给药使得血液在返回至肌体前与透析液平衡,因此,尽管包含c-o-p键的化合物可以扣留离子钙,但是当血液通过透析过滤器时,上述事实被抵消,从而消除了所述的副作用并显著改善安全性。
[0108]
如本发明所用,术语“治疗”是指抵制在受试对象(优选为哺乳动物,更优选为人类)中所关注的疾病或病理学状况所导致的作用,包括:
[0109]
(i)抑制疾病或病理学状况,换言之,减缓或终止其发展或进程;
[0110]
(ii)减轻疾病或病理学状况,换言之,使得所述的疾病或病理学状况、或者其症状消退;
[0111]
(iii)稳定疾病或病理学状况。
[0112]
在本发明的实施方案中,意外地观察到式i所示的化合物与用于肾脏损害的选自列表的其他治疗之间的协同作用,已经观察到当把式i所示的化合物与修改含钙晶体生成的热力学的另一种物质组合时,发生协同作用。此外,已经观察到将式i所示的化合物与修改所述的过程的动力学(减少促进因子或增加抑制因子)的另一种物质组合物时,也会产生所述的协同。
[0113]
通常,所给予的本发明的化合物的有效数量取决于所关注的化合物的相对效力、待治疗的紊乱的严重性以及受试对象的体重。给药可以为每天一次至每周一次,每月一次、2个月一次或本领域的技术人员已知的任何其他的频率。
[0114]
如在整个说明书和权利要求书中所用,词语“包含”及其变体无意于排除其他的技术特征、添加剂、成分或步骤。对于本领域的技术人员而言,本发明的其他主题、优点和特征部分得自于说明书,部分得自于本发明的实践。以下实施例和附图仅以举例说明的方式提供,并且无意于限定本发明。
[0115]
附图简述
[0116]
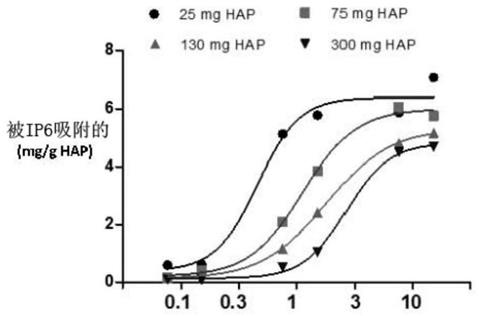
图1示出在37℃、ph7.4下温育8h后,ip6对不同浓度的hap晶体的吸附。
[0117]
图2示出ip6对hap晶体的吸附。在130mg hap存在下,将ip6(7.6 μm)在37℃、ph7.4下温育5分钟至8小时。
[0118]
图3示出由hap表面上释放ip6的动力学。在130mg hap存在下温育ip6(7.6μm),以及在不同时间点直至48小时时ip6的释放。
[0119]
图4示出在正常和尿毒症大鼠中,在s.c.给药10mg/kg后ip6的pk 概况。
[0120]
图5示出在正常和尿毒症大鼠中,在静脉输注10和50mg/kg后,在 4h中ip6的pk概况。
[0121]
图6示出在大鼠的维生素d诱导的心血管钙化模型(5x75,000iu/kg) 中,在静脉给药ip6后在主动脉(a)和心脏(b)中的钙含量。剂量表示为 mg/k;c=对照组。
[0122]
图7示出在大鼠的维生素d诱导的心血管钙化模型(3x300,000iu/kg) 中,在s.c.给药ip6后在主动脉中的钙含量。
[0123]
图8示出在第5天至第14天,在使用10和60mg/kg ip6进行s.c.治疗后,心脏钙化的进展(a)以及对该钙化进展的抑制(b)。在第1、2和3天给药100,000iu/kg维生素d。
[0124]
图9示出在第5天至第14天,在使用10和60mg/kg ip6进行s.c.治疗后,肾脏钙化的进展(a)以及对该钙化进展的抑制(b)。在第1、2和3天给药100,000iu/kg维生素d。
[0125]
图10示出ip6对离子钙的螯合。将浓度增加的ip6加入至处于0.15m nacl,ph 7.4中的2.5mm钙的溶液中,并测量离子钙的水平。
[0126]
图11示出在团注和非团注型给药ip6后,qtc间期的增加。
[0127]
图12示出通过透析回路给药20分钟后,人类血液中的ip6的浓度。
[0128]
图13示出通过透析回路给药ip6达20分钟后,人类血液中的离子钙的浓度。
[0129]
图14示出了ip6与西那卡塞(a)和司维拉姆(b)的作用之间的协同。
实施例
[0130]
下文中将通过本发明人实施的多个测试来说明本发明,其中所述的测试强调了所述的治疗方法的特异性和效力。
[0131]
实施例1.ip6与用于肾脏损害的其他治疗的相容的组合。
[0132]
目的:用于评价ip6与用于肾脏损害的其他治疗的相容性。
[0133]
试验:使用ip6(皮下,s.c.),ip6(s.c.)+司维拉姆(oral),ip6(s.c.)+西那卡塞(oral),ip6(s.c.)+vit d(s.c.),ip6(s.c.)+硫代硫酸钠(s.c.),ip6(s.c.) +伊班膦酸盐(s.c.)治疗wistar大鼠。
[0134]
结果与讨论:在单独给药ip6或者伴有另一种治疗之间未观察到明显的差异。得到的结论是,伴随给药ip6以及用于肾脏损害的其他治疗未表明相容性问题。
[0135]
实施例2.体外测定ip6对羟磷灰石(hap)的亲和性。
[0136]
目的:本研究的目的在于分析ip6对其靶物的亲和性,由此得到ip6 对hap的亲和性的曲线。
[0137]
试验:在37℃,ph 7.4下,将4种不同数量的hap与浓度增加的ip6 温育4小时,同时持续搅拌。对与靶物(hap)表面结合的ip6的总数量进行定量。
[0138]
结果:得到剂量依赖的吸附曲线,并且在浓度为7.6μm或更高下达到饱和。ip6在hap表面上的最大吸附为在使用300mg靶物时吸附4.8mg 至当使用25mg hap时吸附6.42mg,并且该最大吸附是在7.6μm ip6存在下经历8小时而取得的。为了表征ip6的结合行为,计算其吸附在hap 上的ec
50
和e
max
。使用非线性回归模型来进行计算(log[激动剂]与应答
‑ꢀ
斜率变量;graphpad prism软件)。计算的ec
50
值为0.46μm(25mg hap), 0.96μm(75mg hap),1.22μm(130mg hap)和2.09μm(300mg hap)。在 6.42mg/g值下,e
max
达到饱和。结果示于图1中。
[0139]
结论:ip6对hap具有高亲和性,并且其在hap晶体上的吸附线性增加直至7.6μm ip6,在该点处,hap表面上的吸附位点达到饱和。
[0140]
实施例3.体外测定ip6与hap的结合动力学。
[0141]
目的:分析ip6与hap的结合速率。
[0142]
试验:在37℃,ph 7.4下,将130mg hap与7.6μm ip6温育(3个重复)不同的时间区
间,同时持续搅拌。
[0143]
结果与讨论:观察到ip6与hap快速结合(图2),并且在60分钟时达到吸附最大值。在5分钟后取得最大结合的大约80%。
[0144]
实施例4.ip6与hap的体外亲和性。释放研究。
[0145]
目的:分析ip6由hap上的释放速率。
[0146]
试验:在37℃,ph 7.4下,将130mg hap与7.6μm ip6温育不同的时间区间,同时持续搅拌。随后,将具有吸附的ip6的hap放置于不含ip6 的溶液中,并且在不同的时间点评价由hap表面上释放的ip6的量。
[0147]
结果与讨论:观察到ip6由hap的表面上相对缓慢地释放(图3)。在温育2天后,80%的ip6保持与hap的表面结合。
[0148]
实施例5.向具有正常肾脏功能和具有肾脏功能减退的大鼠皮下给药 (s.c.)ip6的药代动力学(pk)概况。
[0149]
目的:评价具有正常肾脏功能和肾脏损害的大鼠的pk概况。
[0150]
试验:向具有正常肾脏功能的大鼠给药单一s.c.剂量(10mg/kg)。在不同的时间点直至60分钟获得血浆样品。不同组的wistar大鼠在10天内接受600mg/kg(p.o.)腺嘌呤的口服治疗,从而诱导肾脏损害。在第11天和第 13天给药α-骨化二醇(300ng/kg),并且在第14天在不同的时间点直至60 分钟收集血浆样品。对2个组的血浆ip6浓度进行定量。
[0151]
结果与讨论:正常的wistar大鼠在至少30分钟内呈现可测量的水平,并且在给药后的15分钟具有峰值浓度7.4μm。尿毒症小鼠显示更低的暴露,其在所有的时间点都具有更低的水平,并且在给药后的5分钟具有峰值浓度1.8μm(图4)。检测低级肌醇磷酸盐(ip5,ip4,ip3,ip2,ip1)和肌醇作为代谢物。
[0152]
结论:在尿毒症动物中ip6的暴露低于正常动物,并且在更短的时间内达到较低的峰值浓度。该作用是由于在尿毒症存在下较高的代谢速率。
[0153]
实施例6.通过延长输注向具有正常肾脏功能和具有肾脏损害(尿毒症)的大鼠给药ip6的药代动力学(pk)概况。
[0154]
目的:评价通过静脉输注向具有正常肾脏功能和具有肾脏损害的非透析大鼠给予ip6的pk概况。
[0155]
试验:每天,使用剂量为10或50mg/kg ip6通过静脉输注(经过4h) 来治疗具有正常肾脏功能的wister大鼠。在第0天,在不同时间点至4小时时获得血浆样品。然后,使用600mg/kg(p.o.)腺嘌呤在10天内口服治疗所述的动物,从而诱导肾脏损害。在第11天和第13天,使用α-骨化二醇 (300ng/kg)治疗所述的动物,并在第14天,在不同的时间点至4小时时收集血浆样品。对2个组的血浆ip6水平进行定量。
[0156]
结果:正常大鼠在剂量为10和50mg/kg下分别显示峰值血浆浓度8.4 和68.4μm。但是,当使大鼠形成尿毒症时,在30分钟时在10mg/kg下取得的峰值浓度为2.8μm,但是所述的值由于高的代谢速率在4小时后降低至1.2μm。在50mg/kg下可以部分客服代谢作用,并且在4小时时取得峰值血浆浓度为24.6μm,而且在30分钟后未观察到血浆浓度降低,因此使得大致恒定的浓度保持3小时(第1小时至第4小时)(图5)。尽管最终血浆浓度低于正常大鼠,但是暴露保持明显并且潜在地是足够有效的,如下一实施例中说明的那样。
[0157]
结论:在尿毒症动物中ip6的暴露低于正常动物,并且在4小时后达到较低的浓度。
但是如果所述的剂量足够高,则延长的输注可以在延长的时间内取得显著的水平,从而部分客服了由于高的代谢速率而产生的作用。
[0158]
实施例7.在具有正常肾脏功能的动物中ip6在钙相关疾病中的效力。
[0159]
7.a.通过静脉给药ip6来抑制vitd诱导(75,000iu/kg x 5)的心血管钙化
[0160]
目的:评价在大鼠中静脉ip6在抑制维生素d诱导的心血管钙化中的效力。
[0161]
试验:将雄性sprague dawley(sd)大鼠分成7组,并且在14天中每天静脉给药剂量为0,0.05,0.1,0.5,1,5和10mg/kg的ip6。通过在第3天至第7天口服给药75,000iu/kg维生素d的处理来诱导钙化。收集样品。在第14天,收集动物的主动脉和心脏来定量钙化。
[0162]
结果与讨论:给药维生素d诱导主动脉和心脏的钙化显著增加。静脉给药0.05至0.5mg/kg ip6不会影响主动脉和心脏的矿物质含量。但是,给药剂量为1至10mg/kg会减少2种组织中的钙化,在主动脉中最多减少 60%,而在心脏中最多减少68%(图6)。
[0163]
7.b.通过s.c.ip6来抑制vitd诱导(300,000iu/kg x 3)的心血管钙化。
[0164]
目的:评价在大鼠中s.c.ip6用于抑制vitd诱导的心血管钙化的效力。
[0165]
试验:将雄性sd大鼠分成9组。其中的2组(假治疗组和对照组) s.c.接受2ml/kg生理盐水;6组s.c.接受剂量为0.1,1,10,60和100mg/kg(2 ml/kg)的ip6,并且另一个组s.c.接受35mg/kg焦磷酸钠ppi(2ml/kg)。1 个组使用加载有200mg/ml ip6的s.c.alzet泵来进行治疗。从治疗第3天开始,在3天内口服给药300,000iu/kg维生素d(2ml/kg)来诱导钙化。不采取治疗组是使用生理盐水按照相似的方式处理的。在治疗7天后,测定心脏、主动脉和肾脏中的钙含量。
[0166]
结果与讨论:s.c.ip6抑制钙化,并得到剂量应答的行为。产生明显作用的最低剂量为10mg/kg,其与28mg/kg焦磷酸盐产生相同的作用,并且 ip6展现更高的潜能。60和100mg/kg的剂量展现大约60%的潜能。使用 alzet泵通过延长给药进行治疗使得钙化降低85%(图7)。
[0167]
结论:s.c.ip6以剂量应答的方式来抑制主动脉的钙化,并且ec
50
为 3.75mg/kg,而e
max
为65.5%。ppi展现出良好的效力,但是比ip6的剂量更高。使用alzet泵的延长给药使得效力显著增加。
[0168]
7.c.评价在大鼠模型中,在2周内ip6(s.c.)对维生素d诱导的血管钙化(100,000iu/kg x 3)的进展的作用。
[0169]
目的:评价ip6对血管钙化进展的药理学概况。
[0170]
试验:使用维生素d(s.c.100,000iu/kg)对48sd大鼠进行x3处理,从而诱导组织钙化。使得钙化进展5天,并从第5天直至第14天,s.c.给予0,10或60mg/kg ip6的治疗。评价肾脏和心脏的钙化。
[0171]
结果与讨论:从第5天至第14天,组织钙化明显进展。使用ip6进行治疗100%地抑制了心脏钙化的进展(图8)并且在最高剂量下,95%地抑制了肾脏的钙化。这些发现首次表明ip6在体内可以抑制钙的生长,甚至在所述的结石已经形成并沉积在组织中时也是如此。
[0172]
实施例8.在患有肾脏损害(尿毒症)的动物中ip6对钙紊乱的效力。
[0173]
8.a.肾切除术与通过i.v.团注模型给药ip6。
[0174]
目的:测定静脉ip6在慢性肾脏损害模型(5/6肾切除的大鼠)中在预防组织钙化中的效力。
[0175]
试验:通过完整的右侧肾切除术和2/3左肾部分切除术将48只sd大鼠的5/6肾切除。使用2ml/kg生理盐水、1mg/kg ip6或5mg/kg ip6静脉 (团注)16只动物/组。动物接受包含20%乳糖的富含磷酸盐的饮食(1%ca, 1.2%p)。8周后,收集主动脉、心脏和剩余的1/3肾脏,并测定组织的钙含量。
[0176]
结果与结论:当使用ip6治疗动物时,未观察到钙化抑制的证据。尽管所述的模型呈现高度的变化性,但是由于仅较低百分率的对照动物呈现出钙化,并且手术过程不可能是非常一致的,所以尿毒症动物中高的代谢速率是效力缺乏的原因。
[0177]
8.b.腺嘌呤与团注型s.c.给药模型。
[0178]
目的:测定在慢性肾脏损害的动物模型(尿毒症)中ip6在预防组织钙化中的效力。
[0179]
试验:在10天中,每天通过使用腺嘌呤(600mg/kg/day)口服(p.o.)处理 4组(n=12)雄性wistar大鼠来诱导ckd。在使用腺嘌呤处理后,大鼠接受剂量为300ng/kg(3x/周,p.o.)α-骨化二醇直至第28天。从第0天直至处死(第 28天),使用2ml/kg s.c.团注0,3,10和30mg/kg ip6来治疗所述的动物。在各治疗中,将3只额外的动物包含在内,用于评价ip6的pl。在28天后,收集主动脉、心脏和右肾,并测定组织钙含量。
[0180]
结果与结论:在任何组织中均未观察到钙化抑制的证据。尽管所述的模型是可重复的,并具有一致的组织钙化,但是尿毒症动物中ip6的高的代谢速率是效力缺乏的原因。
[0181]
8.c.腺嘌呤与非团注型血管内给药模型。
[0182]
目的:测定在尿毒症动物中以非团注型给药ip6在预防组织钙化中的效力。
[0183]
试验:在10天中,每天通过使用腺嘌呤(600mg/kg/day)口服(p.o.)处理 2组(n=12)雄性wistar大鼠来诱导ckd。在使用腺嘌呤处理后,大鼠接受剂量为300ng/kg(3x/周,p.o.)α-骨化二醇直至第28天。从第0天直至处死(第 28天),在4小时内使用血管内输注50mg/kg ip6或生理盐水来处理动物。在28天后,收集主动脉、心脏和右肾,并测定组织钙含量。
[0184]
结果与结论:使用ip6进行治疗使得主动脉和心脏的平均钙化分别降低80%和85%。尽管高代谢速率(其在试验结束时时血浆ip6的水平降低 90%),但是延长的非团注型给药使得代谢作用被补偿并且在尿毒症状况下在钙疾病中首次证明ip6的效力。
[0185]
实施例9.ip6的体外钙螯合。
[0186]
目的:评价ip6的离子钙螯合潜能
[0187]
试验:与浓度增加的ip6一起,移取处于nacl 0.15m,ph 7.40中的 2.5mm钙。使用钙选择性电极和电位计以电位方式测量游离离子钙的量。
[0188]
结果与结论:ip6在379μm以上展现出明显的离子钙螯合能力。剂量应答曲线(图10)的半对数表示显示出sigmoid概况,在3788μm下饱和,并且ec
50
为539μm。这些结果示于图10中。所述的浓度与体内研究中所观察到的水平一致,并且解释了ip6的副作用与低血钙症(离子钙被螯合) 有关的原因。
[0189]
实施例10.ip6的体内钙螯合。
[0190]
10.1.在有意识的狗中在2小时的血管内输注后通过遥测来测定ip6 对心血管功能的作用。
[0191]
目的:测定非团注型给药ip6对心电图(ecg)和血清离子钙浓度的作用。
[0192]
试验:在latin方设计中,通过在2h内输注3,10和30mg/kg ip6来治疗4只雄性狗。
在各剂量之间实施1周的清除期。在输注前1h和20分钟以及输注后5,15,30,45分钟、1,2,6和24h遥测ecg。在第二阶段,在相同的剂量下,在输注前20分钟以及输注后1,1.5,2,3和6h,取得血液样品用于pk。在这种情况下,各剂量之间的清除期为2天。此外,还测量血液样品中的总钙和游离的钙。
[0193]
结果:在2h内输注任何剂量的ip6后,健康状态、体重、心肺功能、 ecg、体温以及血液中的总钙和游离钙相对未受影响。此外,平均血液离子钙浓度也未受影响。在3,10和30mg/kg下,所发现ip6的峰值水平分别为27,150和482μm。
[0194]
结论:在所述的试验状况下,2h内输注剂量为3,10和30mg/kg的ip 对狗不具有不利的作用。
[0195]
10.2.在有意识的狗中在团注型静脉给药后通过遥测来测定ip6对心血管功能的作用。
[0196]
目的:检验在狗中团注型给药ip6对血清离子钙、ecg和临床迹象的作用。
[0197]
试验:向4只雄狗(2只/剂量)输注10,15和30mg/kg。在不同的剂量之间引入2天的清除期。以遥测方式记录ecg。针对ecg测量,在不同天测定血液钙离子浓度。
[0198]
结果与结论:在10mg/kg剂量下,ip6对ecg参数或离子钙浓度不具有明显的作用。在15mg/kg意识观察到轻微的心动过速和延长的qtc 间期,在30mg/kg以上变得显著(图11)。这种作用与离子钙减少30%有关。低血钙症是导致延长的qtc间期的原因。这些发现以及在之前的实施例中经过2h输注的那些发现一起证明由于ip6可以螯合离子钙,所以根据血浆ip6的峰值浓度,ip6影响了低血钙症并延长qtc间期。所述的作用可以与通过非团注型给药的方式来增加给药时间有关。
[0199]
实施例11.通过透析系统给药ip6。
[0200]
目的:使用真实的透析系统在人类血液中建立ip6的透析能力以及其对钙螯合的作用。
[0201]
试验:由进行放血治疗的患者得到的1升人类血液引入至受者中,从而形成封闭的透析环路,由此模拟真实的透析。进行2个试验(透析前给药和透析后给药,均以旁路模式和透析模式),在受者(其模拟了动物或人类的肌体)的外部时在20分钟内将ip6给予人类血液,并通过透析回路循环。在37℃的受控的温度下将包含1升全血的受者与透析仪器连接,从而形成封闭的回路。透析仪器将连接1小时(透析液流速为500ml/min,血液流速为350ml/min)。在不同的时间收集血液样品,从而测定ip6和离子钙的浓度。
[0202]
结果与结论:使用标准的透析仪器,在20分钟内通过透析线路给药 ip6(模拟了标准的临床过程)显示通过透析膜,ip6未损失(图12)。
[0203]
此外,证明ip6螯合(扣留)了游离的钙(仪器,以旁路模式),但是当所述的仪器设置于透析模式时,由于透析液供入的钙的结果,使得离子钙的水平得以恢复,所以这种不利的螯合作用被克服(图13),从而允许这种通过透析系统的新模式的非团注或长效型给药(其适用于产品的效力,如上述实施例中说明的那样),并改善ip6所建立的安全性。
[0204]
实施例12.ip6与用于肾脏损害的其他治疗的协同作用。
[0205]
目的:评价ip6的作用与用于肾脏损害的其他治疗的作用之间的潜在协同作用。
[0206]
试验:在ph 7.4下通过将合适浓度的钙与磷酸盐混合使羟磷灰石(hap)结晶。通过适当地修改钙和磷的浓度来模拟西那卡塞和司维拉姆的作用。诱导期(hap开始结晶所需的
时间)记录为分析信号。
[0207]
结果与结论:用于对照试验的诱导期为8分钟。当加入ip6时,对于 11.4μm的浓度而言,诱导时间逐渐增加至28分钟。随后,将范围为0-11.4 μm的不同浓度的ip6与恒定模拟浓度的西那卡塞和司维拉姆结合,从而适当地修改了钙和磷的浓度。当模拟西那卡塞和司维拉姆的作用时,诱导时间(未加入ip6)分别为14和15分钟。如图14可见,当加入ip6时,发现明显的协同作用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1