超声脑中小微动/静脉血管微泡造影灌注功能定量分类成像方法
1.本发明属于超声成像领域,涉及一种脑中、小、微动/静脉血管微泡造影灌注功能定量分类成像方法。
背景技术:
2.目前磁共振成像(mri)、正电子发射型计算机断层显像(pet)等成像技术在脑内成像方面的应用主要是进行脑内组织、血管结构成像,并在向脑内功能成像发展,例如联合特定造影剂进行血流动力学特征分析,但这些成像技术的缺点是时间分辨率、空间分辨率差,以及无法获得局部细微、或脑小微血管的灌注特征。
3.超声成像与其他医学影像技术相比具有非侵入、使用方便、成本低、对人体损害小等优点,目前在脑部成像中已有经颅多普勒成像技术得到临床应用,具备时间分辨率和床边检查以及无辐射等优势。但是,只能对颅脑内的大、中血管进行成像,以反映脑大中血管的血流流速变化,无法实现对局部细微或脑小微血管的灌注特征的辨识。同时,由于颅骨声遮挡和衰减效应,使得脑部超声成像,例如经颅多普勒成像的灵敏度、分辨率差,实时性与深度相互制约。
4.nakagami回波统计模型具有声学参数独立性的优势,可以恢复或减弱声场变化导致的回波幅度变化,以反映固有的散射子超声回波特征。而颅骨声遮挡和衰减效应本质上是改变颅内声压及声场分布。因此,理论上nakagami参数具有改善颅骨声遮挡和衰减效应的可能性,但结合nakagami回波统计模型进行超声局部细微或脑小微血管功能实时成像,从而为脑部提供多层次和多参量定征,仍然是目前亟待解决的技术难题。
技术实现要素:
5.本发明的目的在于提供一种超声脑中小微动/静脉血管微泡造影灌注功能定量分类成像方法。
6.为实现上述目的,本发明采用了以下技术方案:
7.1)利用超声波探头经颞窗采集脑部超声回波信号;
8.2)对步骤1)采集的超声回波信号依据经颅衰减的微泡母小波进行微泡小波解相关全频域检测,然后进行nakagami回波统计参数成像,得到脑血管三维(3d)回波统计参数造影图像序列矩阵;
9.3)沿着时间序列对脑血管三维回波统计参数造影图像序列矩阵进行重构,然后通过机器学习进行成分分析并定征灌注成分,对获得的多个灌注成分的时间变化曲线建立脑中、小、微血管灌注区域的关联,并分别分离脑中、小、微血管分布;
10.4)根据脑中、小、微血管分布分别提取灌注特征,然后计算脑中、小、微血管的时间类、强度类及比值类灌注参量;
11.5)对脑中、小、微血管分布中的脑血管根据各灌注参量分别进行编码成像以及动
脉与静脉的分离。
12.优选的,所述步骤1)具体包括以下步骤:
13.1.1)将声透镜置入一侧与颞骨表面契合的封装体中,将低频超声相控阵探头由另一侧伸入封装体并通过封装体内部的耦合剂与声透镜对接;
14.1.2)采用低频超声相控阵探头,经颞窗外侧的声透镜(声透镜通过封装体定位)向脑部发射超声波,并利用该低频超声相控阵探头接收和采集超声回波信号,得到原始射频数据。
15.优选的,所述步骤2)中,经颅衰减的微泡母小波是依据颅骨声衰减声场分布,并通过构造声场驱动的脑血管微泡母小波而得到的。
16.优选的,所述步骤2)中,nakagami回波统计参数成像具体包括以下步骤:对上述原始射频数据在经过逐扫描线进行微泡小波解相关全频域检测后所得脑血管微泡小波解相关数据,以不同倍数的基准窗长为窗长大小,分别在每个窗长大小下估计脑血管微泡造影回波统计参数,其中,基准窗长为低频超声相控阵探头发射的超声波的波长的n倍,n=1,3,5
…
9;对脑血管微泡造影回波统计参数进行编码成像。
17.优选的,所述步骤3)具体包括以下步骤:
18.3.1)将获得的脑血管三维回波统计参数造影图像序列矩阵按照时间序列进行二维线性变换,得到重构的二维(2d)矩阵;
19.3.2)对步骤3.1)得到的二维矩阵进行主成分分析,获得多个灌注成分;主成分分析过程中,假设二维矩阵中各元素的值为主成分向量矩阵和空间权重矩阵的线性组合;
20.3.3)分别对不同灌注成分计算时间变化曲线,然后根据各灌注成分时间变化曲线差异,分别与脑中、小、微血管灌注区域建立关联。
21.优选的,所述步骤4)具体包括以下步骤:
22.4.1)对脑中、小、微血管的灌注区域分层处理,每层以a
×
a像素为窗长大小,以单像素为窗间移动步长,分别提取脑中、小、微血管灌注时间强度曲线,其中,a=1~9;
23.4.2)根据步骤4.1)提取的灌注时间强度曲线,计算得到脑中、小、微血管的时间类、强度类及比值类灌注参量;
24.优选的,所述时间类灌注参量为冲入时间、冲出时间、达峰时间中的一种或多种;强度类灌注参量为峰值、曲线下面积中的一种或多种;比值类灌注参量为冲入率、冲出率中的一种或多种。
25.优选的,所述步骤5)具体包括以下步骤:
26.依据造影微泡在动静脉中的灌注特征差异以及时间类、强度类及比值类灌注参量的数值,分别进行伪彩色编码,采用强度双阈值法并通过调节伪彩色编码图像的上阈值及下阈值,对脑中、小、微血管进行动静脉分离。
27.本发明的有益效果体现在:
28.本发明对原始射频数据进行微泡小波解相关全频域检测和nakagami回波统计参数成像后,利用脑血管三维图像矩阵进行灌注成分定征,并分离脑中、小、微血管分布,从而能够通过脑中、小、微血管各自的时间类、强度类与比值类灌注参量,对颅脑动静脉分层次进行灌注参量成像,可以为脑部病变提供多层次、多参量定征。
29.进一步的,本发明采用带有颞窗耦合配件(包括封装体、声透镜)的相控阵探头获
取原始射频数据,相较于未使用该颞窗耦合配件,能够增加超声波经颅传播,并且获得更多的颅内超声波回波信号,提高颅内超声成像分辨率。
附图说明
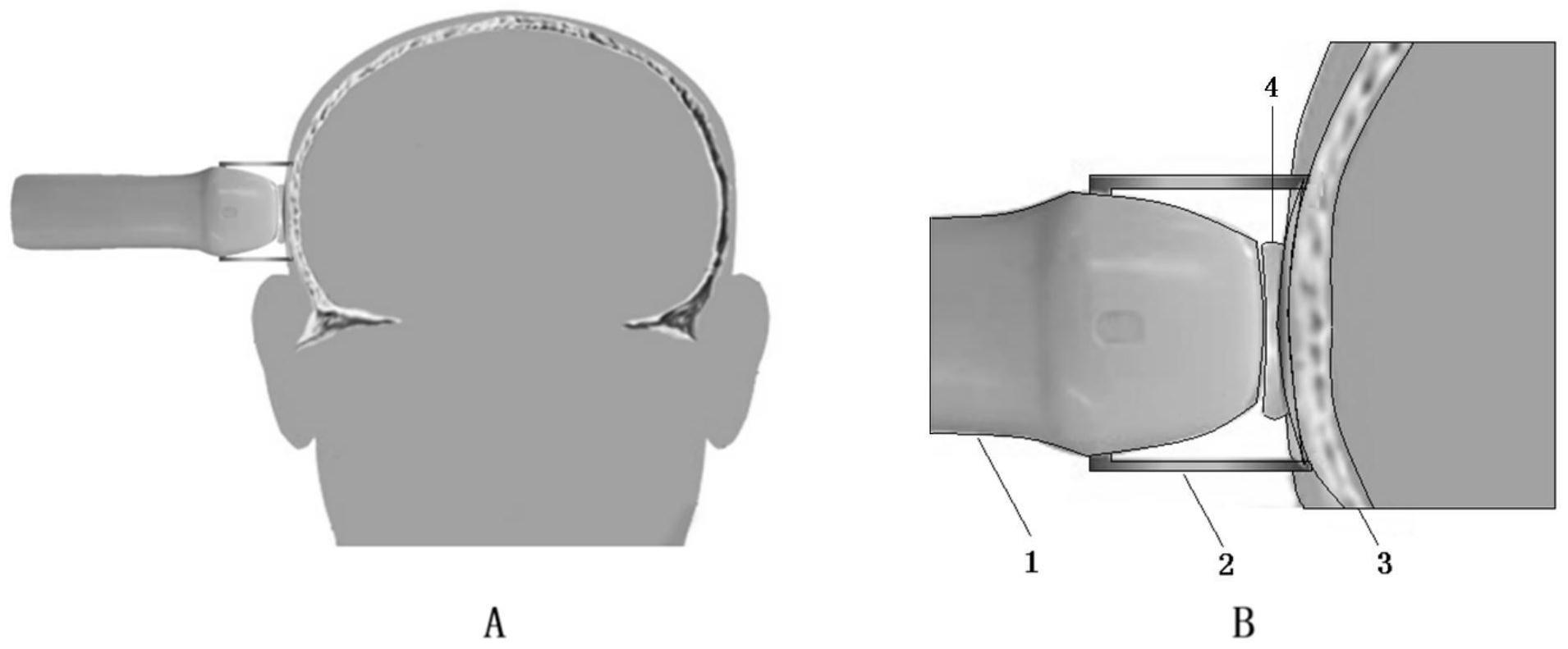
30.图1为本发明实施例中超声探头发射超声波及采集回波信号的示意图;其中:(a)低频超声相控阵探头与颞窗的耦合示意图;(b)利用声透镜构建的耦合配件示意图;1-相控阵探头,2-封装体,3-颞骨,4-声透镜。
31.图2为本发明实施例中超声脑中小微动/静脉血管微泡造影灌注功能定量分类成像的流程框图。
具体实施方式
32.下面结合附图和实施例对本发明作进一步详细说明。所述实施例仅用于解释本发明,而非对本发明保护范围的限制。
33.本发明提供一种超声脑中小微动/静脉血管微泡造影灌注功能定量分类成像方法。该成像方法基于超声灌注功能成像原理,使用带有颞窗耦合配件的低频颅脑超声相控阵探头发射超声波,然后采集回波信号;接着对获得的原始射频数据进行微泡小波解相关全频域检测和回波统计参数成像,不仅解决了颅骨引起的超声信号衰减问题,而且还获得了脑血管(含颅脑中、小、微血管)三维(3d)回波统计参数造影图像序列矩阵。然后将该造影图像序列矩阵按照时间序列重构,并利用机器学习方法进行成分分析与定征分离,接着分离颅脑中、小、微血管分布。最后分别提取颅脑中、小、微血管灌注时间强度曲线,计算得到各自的时间类、强度类与比值类参量,并对颅脑动静脉进行编码成像和血流动力学分析。
34.参见图2,上述超声脑中小微动/静脉血管微泡造影灌注功能定量分类成像方法具体包括以下步骤:
35.步骤一 将相控阵探头与颞窗声透镜装置耦合,经颞窗进行脑血管微泡造影成像的超声回波信号接收和采集。
36.(1.1)构建颞窗声透镜装置(作为探头的颞窗耦合配件,图1):设计一个沿低频超声相控阵探头1阵列厚度方向呈凹面的声透镜4,将该声透镜4置入一具有与颞骨3相契合表面的封装体2中,封装体2内部装满超声耦合剂;封装体2的制作材料与低频超声相控阵探头1声窗材料一致,例如采用硅胶材料制作,以增强超声经过颞窗的声透效率。
37.(1.2)将低频超声相控阵探头1耦合进颞窗声透镜装置,使声透镜4一侧为低频超声相控阵探头1声窗,另一侧为封装体2与颞骨3相契合表面;低频超声相控阵探头1经颞窗发射超声波,并接收和采集超声回波信号,得到脑内组织-血管原始射频数据。其中,低频超声相控阵探头1的中心频率为2.0~3.0mhz。
38.步骤二 设计经颅骨衰减的微泡母小波,对相控阵探头获得的脑内组织-血管原始射频数据进行微泡小波解相关全频域检测和回波统计参数成像,获得脑血管三维(3d)回波统计参数造影图像序列矩阵。
39.(2.1)依据颅骨声衰减声场分布,构造该声场驱动的脑内血管中的微泡母小波,对获得的脑内组织-血管原始射频数据逐扫描线进行多尺度下微泡小波解相关全频域检测(ultrasound med biol,37(2011),pp.1292-1305),从而抑制脑组织回波,以及提高脑血管
回波对比度。其中,全频域由超声波探头的带宽决定,即低频超声相控阵探头1的全部接收频率范围。
40.(2.2)对通过步骤(2.1)检测得到的脑血管微泡小波解相关数据,以3倍波长为矩形窗的基准窗长,改变窗长大小(窗长大小为奇数),以单像素作为相应窗长大小的矩形窗的移动步长,逐窗移动并估计该尺度窗内的脑血管微泡造影nakagami回波统计参数,并返回给窗中心位置像素(相当于对图像进行平滑处理)。
41.(2.3)对脑血管微泡造影回波统计参数进行编码成像,恢复被颅骨遮挡衰减的脑血管回波信号,获得脑血管3d回波统计参数造影图像序列矩阵。
42.步骤三 沿着时间序列重构脑血管3d回波统计参数造影图像序列矩阵,进行机器学习成分分析与定征分离,将获得的多个灌注成分的时间变化曲线与颅脑中、小、微血管的灌注特征关联,并分离颅脑中、小、微血管分布。
43.(3.1)将获得脑血管3d回波统计参数造影图像序列矩阵按照时间序列(i=[
…it
…
]),进行二维线性变换,重构为二维(2d)矩阵(ω=[
…dt
…
]),具体变换过程如下:
[0044][0045]dt
=[(x1)
t
…
(xm)
t
]
t
,1≤t≤t
[0046]
t、m和n分别是脑血管3d回波统计参数造影图像序列矩阵的帧数、单帧图像像素列数和单帧图像像素行数。上标t表示转置。i
t
表示在t时间段内t时刻的造影图像。xm表示在t时刻时造影图像的第m列向量。d
t
表示在t时刻时造影图像每个像素的数值矩阵。x
nm
表示造影图像最后一行最后一列的像素点的像素值。
[0047]
(3.2)对得到的二维矩阵ω进行主成分分析,获得多个灌注成分,主成分分析过程如下:
[0048]
在模型假设中,二维(2d)矩阵(ω)中各元素的值为主成分向量矩阵u和空间权重矩阵v的线性组合:
[0049]
ωk×
t
=uk×
fvf
×
t
+ε
[0050]
k=m
×
n,表示矩阵ω中所有像素;f表示主成分分量的阶数,当f大于等于4时,ε可省略(ε是指残差)。因此,主成分向量矩阵u的计算方法如下:
[0051][0052]
根据以上公式,在计算得到u后,确定与灌注参量对应的主成分(具体实验确定),即灌注成分。
[0053]
(3.3)分别对不同灌注成分计算时间变化曲线,然后根据各灌注成分时间变化曲线差异,分别与脑中、小、微血管灌注区域建立关联(实验建立的关联)。
[0054]
(3.4)根据灌注成分关联结果,分离得到脑中、小、微血管分布。
[0055]
步骤四 对颅脑中、小、微血管的灌注区域进行分层处理,分别提取颅脑中、小、微血管灌注时间强度曲线,并计算得到各自的时间类、强度类与比值类参量。
[0056]
(4.1)对脑中、小、微血管的灌注区域(超声得到的视频图像区域)分层处理(分层处理就是按照中、小、微血管分布分别处理),每层以3
×
3像素为窗长大小,以单像素为窗间移动步长,分别逐窗提取脑中、小、微血管灌注时间强度曲线。
[0057]
(4.2)根据获得的脑中、小、微血管灌注时间强度曲线,计算得到各自的时间类、强度类与比值类参量;其中,时间类参量包括:冲入时间、冲出时间、达峰时间;强度类参量包括:峰值、曲线下面积;比值类参量包括:冲入率、冲出率。时间类参量用于实现对颅脑动脉、静脉分别进行血流动力学分析。
[0058]
步骤五 对颅脑动静脉进行血流动力学分析及编码成像。
[0059]
(5.1)依据造影剂在血液循环系统中存在的“动脉血管先到先离、静脉后到后离”的灌注特征差异,以及时间类参量对造影剂冲入时间、达峰时间和冲出时间的表征,根据不同时间类参量数值范围,可以对颅脑中、小、微动脉与静脉进行分离。
[0060]
(5.2)根据各类参量的数值,进行伪彩色编码成像;采用强度双阈值法并通过调节伪彩色编码图像的上阈值及下阈值,对脑中、小、微血管进行动静脉分离,获得颅脑中、小、微血管分层的动脉/静脉多参量灌注参量成像。
[0061]
本发明的优点如下:
[0062]
1.利用经颅骨衰减的微泡母小波,能在全频域对相控阵探头获得的脑组织-血管信号进行微泡小波解相关检测,提高微泡检出灵敏度和对比度。
[0063]
2.对脑血管内的造影微泡信号进行回波统计参数编码和成像,可以恢复因颅骨声遮挡和衰减效应导致的造影微泡信号低估和成像对比度差等系列问题。
[0064]
3.提供了多种灌注成分的时间变化曲线,分离得到脑中、小、微血管的灌注参量信息。
[0065]
4.依据时间类灌注参量可以用于对颅脑动、静脉进行血流动力学分析并分别编码成像。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1