维拉帕米在制备促使骨代谢进入低转换以防治骨质疏松的产品中的应用
1.本发明涉及医药领域,具体地涉及维拉帕米的促使骨代谢进入低转换以防治骨质疏松的用途。
背景技术:
2.骨质疏松症是一种以骨量降低、骨组织的微结构破坏,导致骨脆性增加和易发生骨折的一种全身性疾病。目前研究普遍认为,其是一种常见的年龄相关疾病,由遗传因素和环境因素共同作用,且峰值骨量、骨质疏松症具有遗传倾向。通过对双胞胎研究发现,与骨密度相关的50%-90%的变异可被遗传;父母有骨质疏松性骨折史,其子女发生骨质疏松性骨折的遗传相关风险为1.30-4.24。
3.随着大型单核苷酸多态性基因分型技术的发展,极大地促进了骨密度的全基因组关联研究,目前已成功地识别了一系列骨质疏松症的常见遗传变异,但仍很大一部分骨质疏松相关的遗传变异有待进一步研究发现。2017年nature genetics通过全基因组关联性研究,分析了英国生物样本库中超过14万名参与者,结合患者足跟超声骨密度,发现了153个和骨密度相关的基因位点,这些基因位点在遗传性疾病的发病因素中占到了12%的比例。2018年nature genetics的研究,通过对英国生物样本库中超过42.6万人进行研究,鉴定出了518个与骨密度相关的基因组位点(其中301个位点是新发现的),能够解释与骨质疏松症相关的20%的遗传突变,有望帮助研究人员开发出新型靶向性疗法来治疗骨质疏松症并降低人群骨折的风险。但是,骨质疏松相关的遗传变异,仍需进一步研究。
4.在前期的基础研究中发现骨质疏松病理生理过程中骨代谢状态的改变尤为明显,因此影响成骨细胞、破骨细胞的代谢、分化成熟以及功能的基因则是研究骨质疏松防治的关键点。因此,研究临床可以应用的针对相关基因以促使骨代谢转变的药物对骨质疏松的防治具有非常重要的临床诊疗和基础科研价值。
技术实现要素:
5.本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种安全且有效的维拉帕米在制备促使骨代谢进入低转换以防治骨质疏松的产品中的应用。
6.本发明的目的可以通过以下技术方案来实现:
7.一种维拉帕米在制备促使骨代谢进入低转换以防治骨质疏松的产品中的应用,所述产品为含有维拉帕米、或其光学异构体、或其药学上可接受的盐的组合物或制剂。
8.进一步地,所述的促使骨代谢进入低转换以防治骨质疏松包括如下任一项:
9.(i)减少成骨细胞内txnip表达水平;
10.(ii)减少破骨细胞内txnip表达水平;
11.(iii)抑制破骨细胞的分化、吸收,成骨细胞的分化、矿化,从而具有促使骨代谢进入低转换的状态;
12.(iv)促使骨代谢进入低转换,以防止骨质疏松造成的骨丢失;
13.(v)促使骨代谢进入低转换,以治疗骨质疏松造成的骨丢失;
14.(vi)提高骨质疏松病理状态下的骨修复能力。
15.上述成骨细胞或破骨细胞为体细胞,选自:骨髓间充质干细胞、骨祖细胞、成骨前体细胞、成骨细胞、骨髓来源的巨噬细胞、破骨前体细胞、破骨细胞、软骨祖细胞、软骨细胞或其组合。
16.进一步地,所述的组合物或制剂中维拉帕米的含量为0.001-99wt%,较佳地为 0.01-90wt%,按组合物或制剂的总重量计,进一步优选地,组合物或制剂中含有有效维拉帕米的量为10~60wt%。
17.进一步地,所述的组合物为药物组合物、化妆品组合物、膳食补充剂、食品组合物或保健品组合物。
18.更进一步地,所述的药物组合物含有(a)维拉帕米或其药学上可接受的盐作为活性成分;和(b)药学上可接受的载体或赋形剂。
19.更进一步地,所述的药物组合物还含有额外的防治骨质疏松活成分。
20.更进一步地,所述的额外防治骨质疏松活成分为:如可降低txnip水平的褪黑素,如可降低txnip水平的鲁斯可皂苷元(ruscogenin),如可降低txnip水平的sbi-477,如可降低txnip水平的sbi993等。
21.更进一步地,所述的药物组合物的形式包括:片剂、胶囊剂、颗粒剂、混悬剂、丸剂、溶液剂、糖浆剂、或注射剂。
22.所述的组合物或制剂被施用于哺乳动物,所述的哺乳动物包括:灵长动物;更佳地所述的哺乳动物为人。
23.所述的促使骨代谢进入低转换以防治骨质疏松包括皮肤促使骨代谢进入低转换以防治骨质疏松。
24.在本发明的第二方面,提供了一种保健品组合物,所述保健品组合物含有维拉帕米作为促使骨代谢进入低转换以防治骨质疏松的有效成分。所述保健品组合物为对维拉帕米为没有负面影响的保健品组合物,如不含激素的维丁钙片、钙尔奇d,不含激素的口服钙剂等。
25.在本发明的第三方面,提供了一种化妆品组合物,化妆品组合物含有维拉帕米作为促使骨代谢进入低转换以防治骨质疏松的有效成分。就是将维拉帕米、或其光学异构体、或其药学上可接受的盐加入化妆品中,经皮给药。所述化妆品为对维拉帕米为没有负面影响的化妆品,如不含类固醇激素的护手霜,不含重金属的保湿水等
26.在本发明的第四方面,提供了一种维拉帕米在体外非治疗性的减少txnip蛋白表达量中的应用,向细胞培养体系中加入维拉帕米或其盐,从而减少所述细胞中 txnip蛋白的表达量;
27.或者在维拉帕米或其盐存在下,培养细胞,从而减少所述细胞中txnip蛋白的表达量。
28.培养体系中,维拉帕米的浓度为0.01-100μm,较佳地0.05-75μm,更佳地 0.1-50μm,最佳地0.5-25μm。
29.所述的细胞为真核细胞。
interactingprotein,txnip)。txnip是细胞内硫氧还蛋白(thioredoxin,txn)氧化还原系统的重要生理抑制剂,在多种器官和组织中表达,发挥着调节细胞内氧化还原反应的作用。 txnip除了在氧化还原调控中发挥重要作用外还参与炎症反应、糖代谢等多种重要生理过程。
59.如本文所用,术语“骨代谢”指骨的细胞在不停地进行着细胞代谢,不仅骨的细胞之间会相互作用,还存在骨髓中的红细胞生成细胞、基质细胞相互作用,以进行骨的改建和重建。
60.如本文所用,骨质疏松(osteoporosis)是是由于多种原因导致的骨密度和骨质量下降,骨微结构破坏,造成骨脆性增加,从而容易发生骨折的全身性骨病。
61.如本文所用,“促使骨代谢进入低转换以防治骨质疏松”是指延缓、阻滞、减少、停止和/或逆转骨量丢失的进程。
62.骨质疏松病理生理过程中骨代谢状态的改变尤为明显,因此影响成骨细胞、破骨细胞的代谢、分化成熟以及功能的基因则是研究骨质疏松防治的关键点。
63.小鼠成骨细胞(bmsc)
64.bmsc细胞是由小鼠内外骨膜和骨髓中基质内的间充质始祖细胞分化而来,能特异性分泌多种生物活性物质,调节并影响骨的形成和重建过程。
65.小鼠破骨细胞(bmms)
66.bmms细胞数小鼠骨吸收的主要功能细胞,在骨发育、生长、修复、重建中具有重要的作用。破骨细胞起源于血系单核-巨噬细胞系统,是一种特殊的终末分化细胞,它可由其单核前体细胞通过多种方式融合形成巨大的多核细胞。
67.小鼠双侧卵巢切除模型(ovx模型)
68.手术构建小鼠双侧卵巢切除(ovariectomy,ovx)模型已被广泛用于骨质疏松的机理研究。
69.活性成分
70.本发明的促使骨代谢进入低转换以防治骨质疏松活性成分是维拉帕米或其药学上可接受的盐。
71.维拉帕米(verapamil)是一类苯烷基胺型钙通道阻滞剂,临床上用于治疗高血压、心律失常和心绞痛。化学式:c27h38n2o4,分子量:454.6110。结构式如式所示:
[0072][0073]
在本发明中,一种优选的活性成分是维拉帕米的药学上可接受的盐,一种典型的药学上可接受的盐是盐酸盐,即盐酸维拉帕米(b1867)。常用的盐酸维拉帕米是 1当量的维拉帕米与1当量盐酸形成的盐酸盐。
[0074]
维拉帕米为钙通道阻滞剂(钙拮抗剂)。由于抑制钙内流可降低心脏舒张期自动去
极化速率,而使窦房结的发放冲动减慢,也可减慢传导。可减慢前向传导,因而可以消除房室结折返。对外周血管有扩张作用,使血压下降,但较弱,一般可引起心率减慢,但也可因血压下降而反射性心率加快。对冠状动脉有舒张作用,可增加冠脉流量,改善心肌供氧。
[0075]
药物组合物及施用方法
[0076]
本发明还提供了含有本发明活性成分的组合物或制剂或产品,所述组合物或制剂或产品可用于促使骨代谢进入低转换以防治骨质疏松。代表性的组合物或制剂或产品包括促使骨代谢进入低转换以防治骨质疏松的药物、保健品。
[0077]
一种优选的组合物是药物组合物,它含有有效量的维拉帕米或其药学上可接受的盐和药学上可接受的载体。
[0078]
如本文所用,术语“有效量”或“有效剂量”是指可对人和/或动物产生功能或活性(即保护软骨细胞缓解骨关节炎功能)的且可被人和/或动物所接受的量。
[0079]
如本文所用,术语“药学上可接受的”的成分是适用于人和/或哺乳动物而无过度不良副反应(如毒性、刺激和变态反应)的,即具有合理的效益/风险比的物质。术语“药学上可接受的载体”指用于治疗剂给药的载体,包括各种赋形剂和稀释剂。
[0080]
本发明的药物组合物含有安全有效量的本发明的活性成分以及药学上可接受的载体。这类载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、凝胶及其组合。通常药物制剂应与给药方式相匹配,本发明的药物组合物的剂型为注射剂、口服制剂(片剂、胶囊、口服液)、透皮剂、缓释剂。例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。所述的药物组合物宜在无菌条件下制造。
[0081]
本发明所述的活性成分的有效量可随给药的模式和待治疗的疾病的严重程度等而变化。优选的有效量的选择可以由本领域普通技术人员根据各种因素来确定 (例如通过临床试验)。所述的因素包括但不限于:所述的活性成分的药代动力学参数例如生物利用率、代谢、半衰期等;患者所要治疗的疾病的严重程度、患者的体重、患者的免疫状况、给药的途径等。通常,当本发明的活性成分每天以约 0.01mg-50mg/kg动物体重(较佳的0.1mg-10mg/kg动物体重)的剂量给予,能得到令人满意的效果。例如,由治疗状况的迫切要求,可每天给予若干次分开的剂量,或将剂量按比例地减少。
[0082]
典型地,当以局部关节内注射方式给予维拉帕米时,一个60kg体重的对象(人),日平均剂量通常为0.6-3000mg,较佳地6-600mg,更佳地45-90mg。
[0083]
本发明所述的药学上可接受的载体包括(但不限于):水、盐水、脂质体、脂质、肽类物质、纤维素、纳米凝胶、或其组合。载体的选择应与给药方式相匹配,这些都是本领域的普通技术人员所熟知的。
[0084]
促使骨代谢进入低转换以防治骨质疏松的方法
[0085]
本发明提供了一种促使骨代谢进入低转换以防治骨质疏松的方法(包括治疗性方法、或体外非治疗性方法),以及抑制txnip蛋白表达和/或活性的方法。
[0086]
典型地,该方法包括:向培养的细胞体系内加入本发明药物组合物或本发明活性成分,从而延缓和/或逆转骨量丢失的病理进程;或减少txnnip蛋白表达量。
[0087]
在另一优选例中,所述的细胞为bmsc、bmms细胞,尤其是正常的体细胞。
[0088]
本发明还提供了一种促使骨代谢进入低转换以防治骨质疏松方法,包括步骤:给需要的对象施用维拉帕米、或其光学异构体、或其药学上可接受的盐作为促使骨代谢进入
低转换以防治骨质疏松活性成分。
[0089]
优选地,所述的促使骨代谢进入低转换以防治骨质疏松方法为给所述对象施用 (或施涂)含维拉帕米或其盐的保健品。
[0090]
在本发明中,代表性的化妆品的剂型可选自下组(但并不限于):固体剂型、半固体剂型、液体剂型、或其组合,如溶液、凝胶、膏霜、乳液、精华、透皮贴、面膜等。
[0091]
本发明的主要优点包括:
[0092]
(a)首次证实了维拉帕米可以有效地降低成骨、破骨细胞内txnip水平,抑制成骨、破骨细胞分化。
[0093]
(b)维拉帕米通过抑制成骨、破骨细胞分化促使骨代谢进入低转换,以防治骨质疏松,延缓骨松相关疾病的发展。
[0094]
(c)通过便捷的给药方式,维拉帕米展现出有利于推广、应用的防治骨质疏松的潜在前景,避免创伤性治疗造成的影响。
[0095]
(d)维拉帕米作为一种已上市的老药,具有较高的使用安全性。
[0096]
因此,本发明的活性成分维拉帕米(或含维拉帕米的组合物和产品)可应用于促使骨代谢进入低转换以防治骨质疏松,延缓骨松相关疾病发病率等多方面。
[0097]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
[0098]
实施例1.
[0099]
一、维拉帕米的体外细胞实验
[0100]
1.1方法
[0101]
盐酸维拉帕米(b1867),购自apexbio公司;bmms、bmsc细胞提自c57bl/6 小鼠骨髓,实验在上海交通大学附属第九人民医院骨科实验室完成。
[0102]
经cck8测定verapamil(txnip抑制剂)的ic50值。100um药物浓度下向培养基中按浓度梯度添加verapamil(txnip抑制剂)溶液体外刺激小鼠原代细胞 bmsc,观察细胞增殖分化及凋亡情况。药物刺激后利用pcr检测txnip在rna 水平的变化、wb检测txnip在蛋白水平的变化。通过成骨诱导液诱导bmsc向成骨细胞分化,诱导7天时,进行alp染色,观察分化细胞百分比来验证verapamil (txnip抑制剂)对成骨细胞分化的影响。通过成骨诱导液诱导bmsc向成骨细胞分化,诱导28天时,进行alizarin red染色,观察矿化结节百分比来验证verapamil (txnip抑制剂)对成骨细胞矿化的影响。通过成骨诱导液诱导bmsc向成骨细胞分化,诱导7天时,提取rna进行pcr实验,验证verapamil(txnip抑制剂) 对成骨相关基因的影响。
[0103]
经cck8测定verapamil(txnip抑制剂)的ic50值。100um药物浓度下向培养基中按浓度梯度添加verapamil(txnip抑制剂)溶液体外刺激小鼠原代细胞 bmms,观察细胞增殖分化及凋亡情况。药物刺激后利用pcr检测txnip在rna 水平的变化、wb检测txnip在蛋白水平的变化。通过mcsf和rankl诱导bmms 向破骨细胞分化,直至出现明显融合的多核空泡样破骨细胞时,进行trap染色,观察破骨细胞数目、面积来验证verapamil(txnip抑制剂)对破骨细胞分化的影响。通过mcsf和rankl在骨吸收板上诱导bmms向破骨细胞分化,出现明显融
合的多核空泡样破骨细胞后,继续诱导4天,随后洗去细胞,观察骨吸收百分比来验证verapamil(txnip抑制剂)对破骨细胞骨吸收能力的影响。通过mcsf和 rankl诱导bmms向破骨细胞分化,诱导5天时,提取rna进行pcr实验,验证verapamil(txnip抑制剂)对破骨相关基因的影响。
[0104]
1.2结果
[0105]
实验数据如图1、2所示。
[0106]
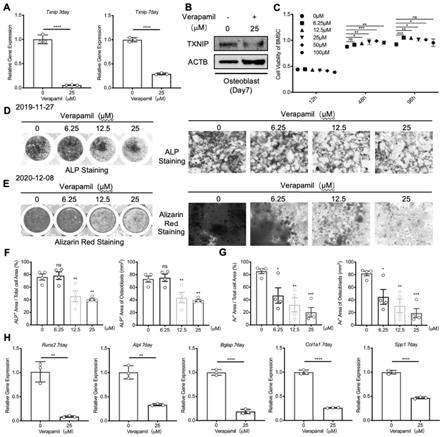
图1为体外小鼠原代成骨细胞实验结果图。
[0107]
其中:
[0108]
a.为体外小鼠原代细胞bmsc向成骨细胞分化的过程中添加txnip抑制剂 25μm(verapamil,pbs配置成溶液)刺激后的实时荧光定量pcr(quantitativereal-time pcr)图,结果显示verapamil抑制成骨细胞内txnip在rna层面的表达。
[0109]
b.为体外小鼠原代细胞bmsc向成骨细胞分化的过程中添加txnip抑制剂 25μm(verapamil,pbs配置成溶液)刺激后的蛋白质免疫印迹(western blot,wb)图,结果显示verapamil抑制成骨细胞内txnip在蛋白层面的表达。
[0110]
c.为向体外小鼠原代细胞bmsc中添加不同浓度txnip抑制剂(verapamil) 刺激后的细胞活性(cell counting kit-8,cck8)图,结果显示verapamil在100nm 及其以下浓度不影响bmsc的增殖。
[0111]
d.为体外小鼠原代细胞bmsc向成骨细胞分化的过程中添加不同浓度txnip 抑制剂(verapamil)刺激后碱性磷酸酶染色(alp染色)图,结果显示verapamil 浓度依赖性抑制成骨细胞的分化。
[0112]
e.为体外小鼠原代细胞bmsc向成骨细胞分化的过程中添加不同浓度txnip 抑制剂(verapamil)刺激后茜素红染色(alizarin red染色)图,结果显示verapamil 浓度依赖性抑制成骨细胞的矿化。
[0113]
f.为碱性磷酸酶染色(alp染色)结果的统计图,可以看出维拉帕米浓度依赖性的抑制小鼠原代细胞bmsc向成骨细胞分化。
[0114]
g.为茜素红染色(alizarin red染色)结果的统计图,可以看出维拉帕米浓度依赖性的抑制小鼠成骨细胞矿化产生钙结节。
[0115]
h.为体外小鼠原代细胞bmsc向成骨细胞分化的过程中添加txnip抑制剂 (verapamil)刺激后的实时荧光定量pcr(quantitative real-time pcr)图,结果显示25nm的verapamil抑制成骨相关基因的表达。
[0116]
图2为体外小鼠原代破骨细胞实验结果图。
[0117]
其中:
[0118]
a.为体外小鼠原代细胞bmms向破骨细胞分化的过程中添加txnip抑制剂 25μm(verapamil,pbs配置成溶液)刺激后的实时荧光定量pcr(quantitativereal-time pcr)图,结果显示verapamil抑制破骨细胞内txnip在rna层面的表达。
[0119]
b.为体外小鼠原代细胞bmms向破骨细胞分化的过程中添加txnip抑制剂 25μm(verapamil,pbs配置成溶液)刺激后的蛋白质免疫印迹(western blot, wb)图,结果显示verapamil抑制破骨细胞内txnip在蛋白层面的表达。
[0120]
c.为向体外小鼠原代细胞bmms中添加不同浓度txnip抑制剂(verapamil) 刺激后
的细胞活性(cell counting kit-8,cck8)图,结果显示verapamil在50nm 及其以下浓度不影响bmms的增殖。
[0121]
d.为体外小鼠原代细胞bmms向破骨细胞分化的过程中添加不同浓度txnip 抑制剂(verapamil)刺激后抗酒石酸磷酸酶染色(trap染色)图,结果显示verapamil 浓度依赖性抑制破骨细胞的分化。
[0122]
e.为抗酒石酸磷酸酶染色(trap染色)结果的统计图,可以看出维拉帕米浓度依赖性的抑制小鼠原代细胞bmms向破骨细胞分化。
[0123]
f.为在骨吸收板上进行体外小鼠原代细胞bmms向破骨细胞分化的过程中添加不同浓度txnip抑制剂(verapamil)刺激后破骨细胞骨吸收的光镜图,结果显示verapamil浓度依赖性抑制破骨细胞的骨吸收。
[0124]
g.为破骨细胞骨吸收结果的统计图,可以看出维拉帕米浓度依赖性的抑制小鼠破骨细胞的骨吸收功能。
[0125]
h.为体外小鼠原代细胞bmms向破骨细胞分化的过程中添加txnip抑制剂 (verapamil)刺激后的实时荧光定量pcr(quantitative real-time pcr)图,结果显示25nm的verapamil抑制破骨相关基因的表达。(*表示p《0.05。**表示p《0.01。 ***表示p《0.001)
[0126]
二、小鼠ovx骨质疏松模型研究
[0127]
2.1方法
[0128]
选取成年(9周龄)野生型小鼠分为空白对照组,手术对照组,低浓 (verapamil-0.7mg/kg,pbs配置成溶液)以及高浓(verapamil-1.4mg/kg,pbs 配置成溶液)度组各6只建立ovx骨质疏松模型,在建模后的6周内持续每周2 次的腹腔注射给药,并在第4周腹腔注射钙黄绿素、第5周腹腔注射茜素红,于术后第6周取材,进行小鼠胫骨骨量分析,以及骨组织学染色,通过h&e染色、 vonkussa染色、trap染色、荧光双标观察骨组织表型。
[0129]
2.2结果
[0130]
实验结果如图3所示。
[0131]
图3.为小鼠ovx骨质疏松模型verapamil腹腔注射给药研究结果图(每周2 次,腹腔注射给药,共给药6周后)。
[0132]
其中:
[0133]
a.小鼠胫骨microct检查皮质骨及松质骨图片,分别为空白对照组(假手术组),手术对照组(ovx手术+pbs),低浓(ovx+verapamil-0.7mg/kg)以及高浓(ovx+verapamil-1.4mg/kg)度组。
[0134]
b.小鼠胫骨microct检查统计图,结果显示:与空白对照组相比,手术对照组胫骨骨量明显降低,骨小梁数目、厚度减少,骨小梁间距增加;verapamil治疗组 (低浓和高浓)部分挽救了ovx导致的骨丢失,胫骨骨量相较手术对照组有所增加,骨小梁数目、厚度增加,骨小梁间距减少。以上结果证实verapamil对小鼠骨质疏松具有防治作用。
[0135]
c.小鼠骨组织切片h&e染色,结果显示空白对照组小鼠胫骨近端组织结构完整,形态规则,生长板平滑和平坦,骨小梁数目正常;手术对照组骨小梁数目减少; verapamil治疗组(低浓和高浓)骨小梁数目较手术对照组有所增加。小鼠骨组织切片vonkussa染色,结果显示空白对照组小鼠胫骨近端组织结构完整,形态规则,生长板平滑和平坦,骨小梁数目正常;手术对照组骨小梁数目减少;verapamil治疗组(低浓和高浓)骨小梁数目较手术对照
组有所增加。小鼠骨组织切片荧光双标,结果显示空白对照组两次荧光染料在小鼠骨小梁上沉积的间距尚可,骨形成速率正常;手术对照组两次染料沉积的间距减少,骨形成速率下降;verapamil治疗组(低浓和高浓)两次染料沉积的间距进一步减少,骨形成速率进一步下降。
[0136]
d.小鼠骨组织切片trap染色,结果显示空白对照组小鼠骨小梁上破骨细胞数目正常;手术对照组小鼠骨小梁上破骨细胞数目增加;verapamil治疗组(低浓和高浓)小鼠骨小梁上破骨细胞数目较手术对照组有所降低,以上结果证实 verapamil治疗,在体内同时抑制了成骨、破骨细胞促使骨代谢进入低转换以防治骨质疏松。
[0137]
e.为vonkussa染色结果的统计图,可以看出verapamil治疗组(低浓和高浓) 挽救了手术对照组导致的骨量减少,verapamil治疗组(低浓和高浓)较手术对照组骨量有所增加。
[0138]
f.为荧光双标提示的骨形成速率的统计图,可以看出verapamil治疗组(低浓和高浓)进一步降低了手术对照组导致的骨形成速率下降,verapamil治疗组(低浓和高浓)较手术对照组骨形成速率进一步下降。
[0139]
g.为trap染色结果的统计图,可以看出verapamil治疗组(低浓和高浓)逆转了手术对照组导致的破骨细胞数目增加,verapamil治疗组(低浓和高浓)较手术对照组破骨细胞数目有所下降。
[0140]
(*表示p《0.05。**表示p《0.01。***表示p《0.001) 。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1