具有ATP-柠檬酸裂解酶抑制活性化合物的用途
具有atp-柠檬酸裂解酶抑制活性化合物的用途
技术领域
1.本发明涉及生物医药领域,具体涉及具有柠檬酸裂解酶抑制活性化合物的用途。
背景技术:
2.心血管疾病(cvd)是全球发病率和致死率最高的疾病。血脂异常作为心血管疾病重要的病理基础,目前临床常用他汀类药物进行治疗,通过抑制3-羟基-3-甲基戊二酸单酰辅酶a(hmg-coa)还原酶达到降低胆固醇合成的目的。虽然他汀类降脂药物能够减少心血管事件的发生,但存在一些不良反应,如肌毒性和肝毒性等,降低患者的依从性。因此临床上仍然需要疗效更好副作用更小的药物。
3.atp-柠檬酸裂解酶(atp-citrate lyase,acly)是连接葡萄糖分解代谢和胆固醇、脂肪酸合成代谢过程中的主要酶,在atp和辅酶a(coa)存在下催化柠檬酸生成乙酰辅酶a和草酰乙酸,为胆固醇和脂肪酸从头合成提供原料,并支持组蛋白和与代谢相关的酶的乙酰化。简单过程如下:
4.柠檬酸+atp+coa
→
乙酰辅酶a+草酰乙酸+adp
5.acly含有1101个氨基酸,是由4个相同亚基组成的同源四聚体,可分为6个结构域,在不同位点结合coa,atp及柠檬酸。acly在组织中普遍表达,尤其是脂肪产量高的组织,包括肝、肾和胰岛β细胞等,并在多种癌症细胞中表达增加,例如乳腺癌,膀胱癌和结肠癌等。acly是抗肿瘤和降脂的重要靶点,抑制acly表达可以抑制乙酰辅酶a产生,从而减少脂质的内源性合成,达到降脂和抑制肿瘤细胞生长的目的,改善高脂血症、动脉硬化性心血管疾病、肥胖症、糖尿病、胰岛素抵抗、脂肪肝和癌症等疾病。自1990年就开始开发acly抑制剂,目前仅有用于治疗高胆固醇血症的bempedoic acid(etc-1002)上市,并且其对于acly仅有弱抑制活性,半抑制浓度(ic
50
)为29μm。因此,亟需找到有效的小分子作为acly的高亲和力抑制剂,用以治疗高脂血症、动脉粥样硬化性心血管疾病、糖尿病等代谢类疾病和癌症。
技术实现要素:
6.发明目的:针对现有技术存在的问题,本发明提供具有acly抑制活性的化合物,用于制备atp-柠檬酸裂解酶抑制剂,进一步用于有效治疗高脂血症、动脉粥样硬化性心血管疾病、糖尿病等代谢类疾病和癌症。
7.本发明还提供所述化合物的药物组合物。
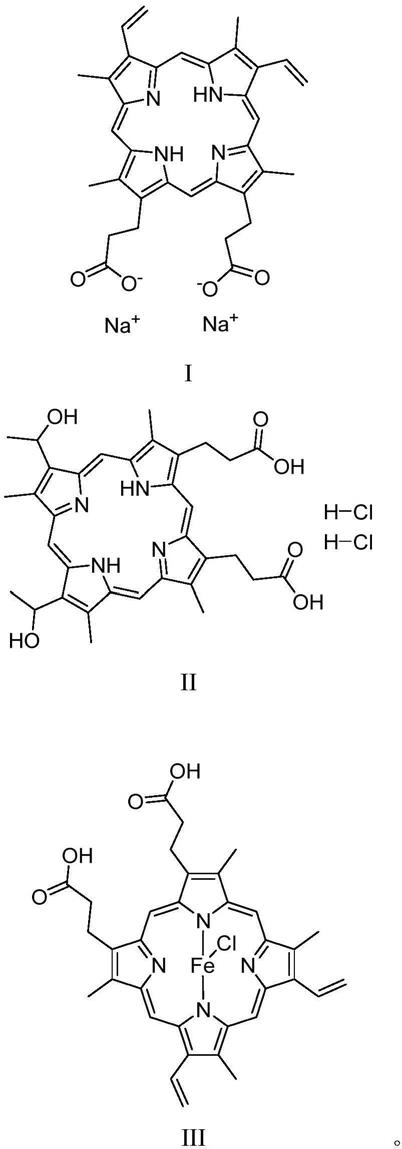
8.技术方案:为了实现以上目的,本发明提供如下式i-iii任一所示的化合物或其药学上可接受的盐或溶剂化合物在制备atp-柠檬酸裂解酶抑制剂中的用途:
[0009][0010]
作为优选,所述式i-iii任一所示的化合物或其药学上可接受的盐或溶剂化合物在制备以atp-柠檬酸裂解酶为靶点的小分子抑制剂中的用途。
[0011]
本发明所述的式i-iii任一所示的化合物或其药学上可接受的盐或溶剂化合物在制备预防和治疗atp-柠檬酸裂解酶介导的疾病的药物中的用途。
[0012]
进一步地,所述atp-柠檬酸裂解酶介导的疾病包括高脂血症、动脉硬化性心血管疾病、肥胖症、糖尿病、胰岛素抵抗、脂肪肝和癌症。
[0013]
其中,所述式i-iii化合物可作为药用盐使用或者溶剂化物组成的药物组合物,所述盐为化合物与金属离子或药学上可接受的胺或铵离子形成的盐。
[0014]
其中,所述金属离子包括钠、钾或钙离子,所述胺包括乙二胺或氨丁三醇。
[0015]
本发明所述的预防和/或治疗atp-柠檬酸裂解酶介导的疾病的药物组合物,其包
含式i-iii任意一种或多种化合物或其药学上可接受的盐或溶剂化物作为活性成分和药学上可接受的载体。
[0016]
其中,所述atp-柠檬酸裂解酶介导的疾病包括高脂血症、动脉硬化性心血管疾病、肥胖症、糖尿病、胰岛素抵抗、脂肪肝和癌症。
[0017]
其中,所述化合物与载体的组合物是胶囊剂、散剂、片剂、颗粒剂、丸剂、注射剂、糖浆剂、口服液、吸入剂、软膏剂、栓剂或贴剂。
[0018]
本发明运用还原型烟酰胺腺嘌呤二核苷酸(nadh)连续监测法对化合物库进行高通量筛选,筛选出化合物库中具有潜在活性的候选分子,选择活性较好的化合物进行深入研究,待测化合物库购自topscience公司上市药物库(l1000)。
[0019]
本发明运用nadh连续监测法建立acly抑制剂高通量筛选模型,进行初筛,复测,得到具有明确acly抑制活性的候选药物。具体步骤如下:
[0020]
步骤一:构建含acly蛋白表达序列的质粒。
[0021]
步骤二:转化质粒至bl21菌株,经裂解,镍柱及分子筛纯化得试验所用acly蛋白。
[0022]
步骤三:nadh连续监测法条件测试。
[0023]
步骤四:采用nadh连续监测法最佳测试条件对化合物进行高通量筛选,得到有活性的化合物。
[0024]
步骤五:采用adp-glo
tm
激酶检测法测定优选化合物对adp生成量的影响,明确acly抑制作用。
[0025]
最终本发明在筛选topscience公司的上市药物库(l1000)的过程中惊奇地发现原卟啉钠,血卟啉二盐酸盐,氯化血红素具有明确的acly抑制作用,并且活性较强。实验结果表明,式i化合物(原卟啉钠,cas:50865-01-5)、式ii化合物(血卟啉二盐酸盐,cas:17696-69-4)、式iii化合物(氯化血红素,cas:16009-13-5)能够抑制acly蛋白,例如使用nadh连续监测法,式i-iii化合物能够抑制acly蛋白参与的反应过程(ic
50
值分别为554nm,381nm,282nm)。进一步使用adp-glo
tm
激酶检测法证明,式i-iii化合物对acly蛋白的抑制活性呈现剂量依赖性(ic
50
值分别为2138nm,162nm,173nm)。上述研究结果表明,式i-iii化合物具有明确的acly抑制作用。本发明的化合物有望用于预防或治疗acly介导的高脂血症、动脉粥样硬化性心血管疾病、糖尿病等代谢类疾病和癌症。
[0026]
有益效果:与现有技术相比,本发明具有如下优点:
[0027]
本发明提供了一类具有atp-柠檬酸裂解酶抑制活性的化合物,首次提出了式i-iii所示的化合物或其药学上可接受的盐或溶剂化合物在atp-柠檬酸裂解酶抑制剂中的用途,本发明化合物可以与acly结合,能够抑制acly催化柠檬酸生成乙酰辅酶a,从而发挥降脂作用,可进一步用于降血脂药物的开发,用于制备预防或治疗acly介导的高脂血症、动脉粥样硬化性心血管疾病、糖尿病等代谢类疾病和癌症。本发明发现的acly小分子抑制剂,活性明确,为开发具有临床治疗价值的药物奠定基础。
附图说明
[0028]
图1为化合物库初筛结果;
[0029]
图2为nadh连续监测法测定优选化合物所得量效关系曲线;
[0030]
图3为adp-glo
tm
激酶检测法测定优选化合物所得量效关系曲线。
具体实施方式
[0031]
下面通过实施例具体说明本发明的内容。在本发明中,以下所述的实施例是为了更好地阐述本发明,并不是用来限制本发明的范围。
[0032]
实施例1
[0033]
采用nadh连续监测法,主要依靠acly催化柠檬酸生成乙酰辅酶a和草酰乙酸,草酰乙酸在苹果酸脱氢酶(mdh)的催化作用下与nadh发生反应生成氧化型烟酰胺腺嘌呤二核苷酸(nad
+)
,nadh消耗使340nm处吸收值减少,其呈现的斜率即代表acly催化反应的速率,简单过程如下:
[0034]
acly催化过程:柠檬酸+atp+coa
→
乙酰辅酶a+草酰乙酸+adp
[0035]
mdh催化过程:草酰乙酸+nadh
→
苹果酸+nad
+
[0036]
当抑制剂存在时,acly催化反应不能发生,nadh在340nm处吸收值变化减小,即可反映出化合物对于acly活性的抑制作用。
[0037]
本发明运用nadh连续监测法建立acly抑制剂高通量筛选模型,进行初筛,复测,得到具有明确acly抑制活性的候选药物。
[0038]
实验设计如表1所示:
[0039]
表1实验组别设计
[0040][0041][0042]
表1所用acly蛋白为参考文献(nature,2019,566-570)表达纯化所得,其余试剂均为配制所得。缓冲液由4-羟乙基哌嗪乙磺酸(50mm),氯化镁(10mm),月桂醇聚氧乙烯醚(0.01%),二硫代苏糖醇(4mm)组成。操作时每孔反应体系中溶剂二甲亚砜(dmso)的终浓度为0.1%,acly蛋白的反应终浓度为3nm,mdh蛋白(购自上海源叶生物)的反应终浓度为10u/ml。化合物初筛浓度为10μm。
[0043]
操作步骤如下:
[0044]
(1)分别稀释acly蛋白至6nm,稀释mdh蛋白至20u/ml;
[0045]
(2)从化合物库中取10mm母液配制为10μm;
[0046]
(3)每孔加入20μl蛋白溶液及20μl化合物溶液;
[0047]
(4)室温静置孵育30min;
[0048]
(5)每孔加入1.6μl柠檬酸盐,atp,coa及nadh等体积混合液;
[0049]
(6)使用酶标仪进行连续读数30次,每次相隔15s;
[0050]
(7)计算每孔斜率:
[0051]
以酶标仪读数为y轴,以连续读数次数为x轴,进行线性回归,得到方程y=kx+b,其中k即为所求斜率。
[0052]
(8)计算acly蛋白活力(%),拟合曲线计算半数抑制率(ic
50
值):
[0053]
acly蛋白活力(%)=(样品孔斜率-阴性对照孔斜率)/(阳性对照孔斜率-阴性对照孔斜率)*100%
[0054]
初筛与复测过程相同,初筛只选用一个浓度对化合物库进行初步筛选,复测选择初筛中活性较好的化合物以50μm为初始浓度,3倍浓度梯度稀释至12个浓度,并进行活性测试。
[0055]
初筛结果见图1。10μm浓度化合物acly蛋白活力在50%以下为活性较好化合物,从中得到优选化合物。
[0056]
优选化合物结构如下:
[0057]
[0058][0059]
复测优选化合物的量效曲线见图2。得到优选化合物的ic
50
值。
[0060]
复测优选化合物的ic
50
值如表2所示,其中bms-303141为阳性对照,选自参考文献(bioorg.med.chem.lett,2007,3208-3211)。
[0061]
表2复测优选化合物对acly蛋白的的ic
50
值
[0062][0063]
实施例2
[0064]
采用adp-glo
tm
激酶检测法测定不同浓度原卟啉钠,血卟啉二盐酸盐,氯化血红素
参与反应时对adp生成量的影响。adp-glo
tm
激酶检测试剂盒(promega)识别反应中所形成的adp,将adp转化为atp,并与萤光素酶偶联产生检测信号。简单过程如下:
[0065]
acly催化过程:柠檬酸+atp+coa
→
乙酰辅酶a+草酰乙酸+adp
[0066]
adp-glo
tm
激酶检测法:adp
→
atp
→
atp+荧光素酶
[0067]
当抑制剂存在时,反应产生adp减少,荧光信号减弱,利用荧光信号强弱,即可反映出化合物对于acly的抑制效果。
[0068]
实验设计如表3所示:
[0069]
表3实验组别设计
[0070][0071]
表3所用acly蛋白为表达纯化所得,其余试剂均为配制所得。缓冲液由4-羟乙基哌嗪乙磺酸(50mm),氯化镁(10mm),月桂醇聚氧乙烯醚(0.01%),二硫代苏糖醇(4mm)组成。操作时每孔反应体系中acly蛋白的反应终浓度为1nm。
[0072]
操作步骤如下:
[0073]
(1)稀释acly蛋白至1nm;
[0074]
(2)用缓冲液稀释化合物至30μm,并依次3倍稀释至12孔;
[0075]
(3)每孔加入40μl蛋白溶液及40μl化合物溶液;
[0076]
(4)室温静置孵育15min;
[0077]
(5)每孔加入0.8μl柠檬酸盐,atp,coa等体积混合液;
[0078]
(6)室温静置孵育60min;
[0079]
(7)取出5μl反应液置于黑色384孔板;
[0080]
(8)每孔加入5μl adp-glo试剂;
[0081]
(9)室温静置孵育40min;
[0082]
(10)每孔加入10μl激酶检测试剂;
[0083]
(11)室温静置孵育30min;
[0084]
(12)酶标仪读数,计算acly蛋白活力(%),拟合曲线计算半数抑制率(ic
50
值):
[0085]
acly蛋白活力(%)=(样品孔数值-阴性对照孔数值)/(阳性对照孔数值-阴性对照孔数值)*100%
[0086]
adp-glo
tm
激酶检测法测定优选化合物所得量效曲线图见图3。
[0087]
adp-glo
tm
激酶检测法测定优选化合物的ic
50
值如表4所示,其中ndi-091143为阳性对照。
[0088]
表4 adp-glo
tm
激酶检测法测定优选化合物的ic
50
值
[0089][0090]
实施例2的活性测试结果显示,使用nadh连续监测法,式i-iii化合物能够抑制acly蛋白参与的反应过程(ic50值分别为554nm,381nm,282nm)。进一步使用adp-glo
tm
激酶检测法证明,式i-iii化合物对acly蛋白的抑制活性呈现剂量依赖性(ic50值分别为2138nm,162nm,173nm);其活性明显强于阳性药bms-303141。
[0091]
以上结果表明,本发明化合物具有较好的acly抑制活性,通过抑制acly进而限制乙酰辅酶a的生物合成治疗肿瘤;也可以有效阻止胆固醇和脂肪酸的从头合成,治疗血脂异常,降低心血管疾病的风险等;可以如同现有药物bempedoic acid(etc-1002)通过抑制acly治疗高胆固醇血症,本发明提出的化合物可以用于制备预防和治疗atp-柠檬酸裂解酶介导的疾病的药物,包括高脂血症、动脉硬化性心血管疾病、肥胖症、糖尿病、胰岛素抵抗、脂肪肝和癌症等。
[0092]
实施例3
[0093]
剂型制备
[0094]
片剂:式iii化合物(50g)、羟丙甲基纤维素e(150g)、淀粉(200g)、聚维酮k30适量和硬脂酸镁(1g)混合,制粒,压片。
[0095]
其他剂型:根据药典2015版常规制剂法,将式i-iii化合物与不同的药物辅料混合,制成胶囊剂、散剂、颗粒剂、丸剂、注射剂、糖浆剂、口服液、吸入剂、软膏剂、栓剂或贴剂等。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1