导丝跨瓣器及介入器械的引导系统的制作方法
1.本技术涉及医疗设备领域,特别是涉及一种导丝跨瓣器及介入器械的引导系统。
背景技术:
2.介入手术对人体造成的创伤小,侵害性少,是现如今常用的医疗技术,通常需要专门的输送系统将诊疗器械、植入器械等输送至病变部位进行相应的治疗或辅助治疗操作。
3.一般输送系统主要包括鞘管、位于鞘管内的鞘芯,鞘管和鞘芯两者的近端延伸至操作手柄。以介入主动脉瓣膜置换手术为例,手术时预先经股动脉穿入较细的导丝,导丝的前端经主动脉瓣后进入左心室,之后将送装载有主动脉瓣膜的鞘管沿导丝送入,直至到达主动脉瓣处,再后撤鞘管释放支架。
4.主动脉瓣在钙化或病变时,主动脉瓣的内径会缩小,在手术中导丝跨过较为狭窄的主动脉瓣时有一定的操作困难,可能会影响手术的成功率。
技术实现要素:
5.为了解决上述技术问题,本技术公开了导丝跨瓣器,包括:
6.导管,所述导管具有相对的远端和近端,所述导管内带有多个副通道以及用于供导丝穿设的主通道,各副通道的侧壁在临近导管的远端位置带有开放区;
7.多根支撑丝,各支撑丝穿设于对应的副通道内,并由导管的近端延伸固定至导管的远端,各支撑丝在导管的远端位置具有:
8.处在副通道内的收纳状态;
9.以及经由开放区延伸出副通道的展开状态,展开状态下,各支撑丝沿主通道径向向外扩张为三维结构。
10.以下还提供了若干可选方式,但并不作为对上述总体方案的额外限定,仅仅是进一步的增补或优选,在没有技术或逻辑矛盾的前提下,各可选方式可单独针对上述总体方案进行组合,还可以是多个可选方式之间进行组合。
11.可选的,所述导管为多腔管,所述多腔管的各腔分别与各通道相对应。
12.可选的,各副通道绕主通道的周向间隔布置。
13.可选的,沿导管的径向,各开放区均位于所述导管的外侧壁、并沿导管的周向布置;
14.所述开放区所在副通道对应的圆心角为大于120度。
15.可选的,沿导管的轴向,所述开放区的长度为4mm-10mm;
16.所述支撑丝采用熔融、焊接、胶粘或紧固件的方式与所述导管远端的固定。
17.可选的,各支撑丝在导管的远端带有预定型段,该预定型段在展开状态下自膨成所述三维结构。
18.可选的,展开状态下,各支撑丝弯曲的辐射分布以形成三维的网笼结构,并限定所述网笼结构的外轮廓;
19.所述支撑丝的数量为3~8根。
20.可选的,展开状态下,在网笼结构的周向上,各支撑丝等距分布。
21.可选的,展开状态下,网笼结构的外轮廓大致为旋转体,各支撑丝对应所述旋转体的母线;
22.所述母线为光滑的曲线。
23.可选的,所述导丝跨瓣器还包括手柄,所述手柄与所述导管的近端固定连接;
24.所述手柄内滑动安装有驱动件,所述驱动件与各支撑丝的近端固定连接。
25.可选的,所述支撑体设置有指示所述驱动件相对位置的刻度标识。
26.本技术还提供如下技术方案:
27.介入器械的引导系统,包括导丝以及采用以上任一项所述的导丝跨瓣器,所述导丝活动穿设于所述主通道。
28.本技术公开的导丝跨瓣器在自身周向上与周边组织之间至少有三处支撑点,以确保主通道的远端开口处于或临近周边组织的几何中心处,导丝能够藉由主通道到达主动脉瓣膜处时,能够便于导丝穿过主动脉瓣。
29.具体的有益技术效果将在具体实施方式中结合具体结构或步骤进一步阐释。
附图说明
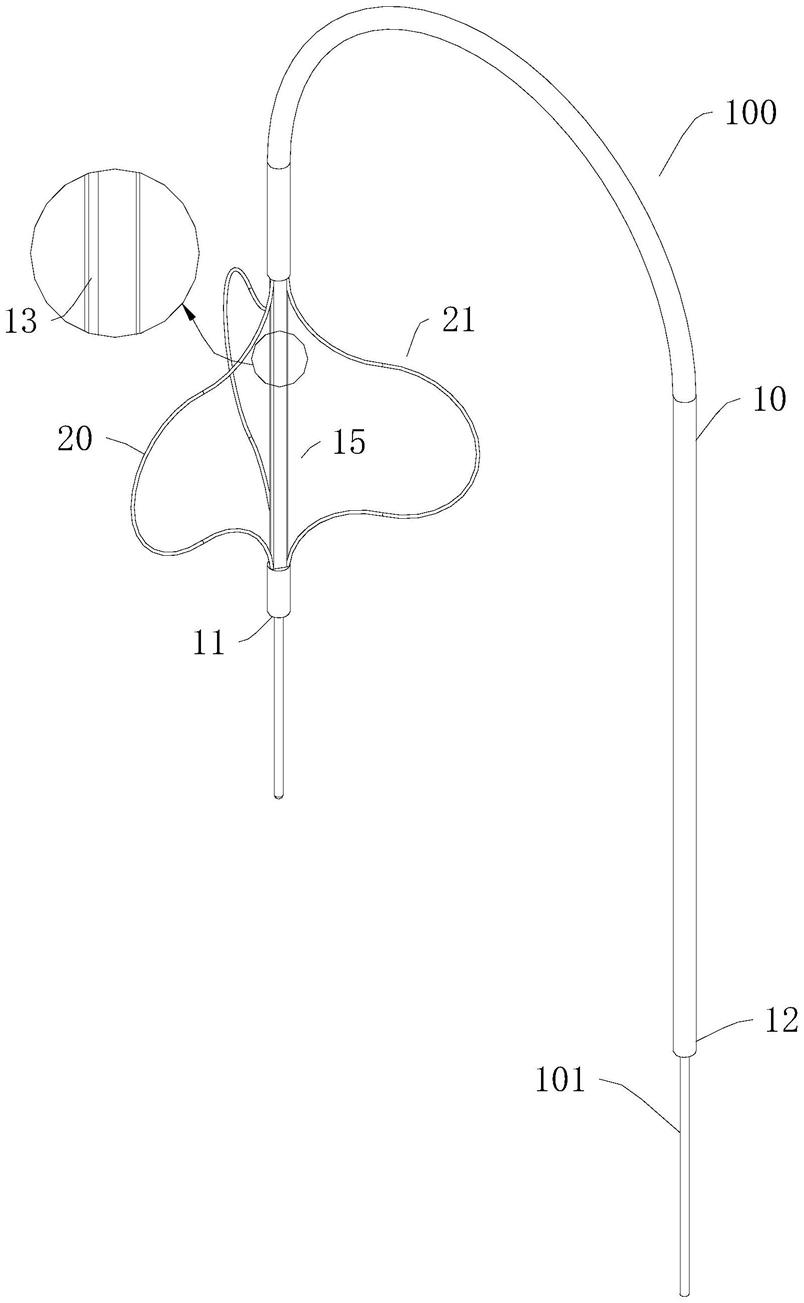
30.图1为本技术提供的一实施例中导丝跨瓣器的结构示意图;
31.图2为本技术提供的一实施例中导丝跨瓣器的结构示意图;
32.图3为图1中导管的截面结构示意图;
33.图4为本技术一实施例的导丝跨瓣器在周边组织的使用状态视图。
34.图中附图标记说明如下:
35.100、导丝跨瓣器;101、导丝;
36.10、导管;11、远端;12、近端;13、副通道;14、主通道;15、开放区;
37.20、支撑丝;21、三维结构;
38.30、周边组织;31、主动脉瓣;32、右冠状动脉;33、左冠状动脉。
具体实施方式
39.下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
40.需要说明的是,当组件被称为与另一个组件“连接”时,它可以直接与另一个组件连接或者也可以存在居中的组件。当一个组件被认为是“设置于”另一个组件,它可以是直接设置在另一个组件上或者可能同时存在居中组件。
41.除非另有定义,本文所使用的所有的技术和科学术语与属于本技术的技术领域的技术人员通常理解的含义相同。本文中在本技术的说明书中所使用的术语只是为了描述具体的实施例的目的,不是在于限制本技术。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
42.参考附图1至附图3所示,本技术公开了导丝跨瓣器100,包括:
43.导管10,导管10具有相对的远端11和近端12,导管10内带有多个副通道13以及用于供导丝101穿设的主通道14,各副通道13的侧壁在临近导管10的远端11位置带有开放区15;
44.多根支撑丝20,各支撑丝20穿设于对应的副通道13内,并由导管10的近端12延伸固定至导管10的远端11,各支撑丝20在导管10的远端11位置具有:
45.处在副通道13内的收纳状态;
46.以及经由开放区15延伸出副通道13的展开状态,展开状态下,各支撑丝20沿主通道14径向向外扩张为三维结构21。
47.以下实施例为便于叙述以应用在介入主动脉瓣膜置换手术为例,当然也适合其他场景(例如二尖瓣、三尖瓣等位置同理),尤其导丝101的远端需要穿过瓣膜的情况。
48.其中在未作特殊说明的情况下,本实施例及下述实施例中的“远端”指靠近病灶即远离操作者一端,“近端”反之。
49.在介入手术中,导管10的远端11预先到达主动脉瓣31处,然后各支撑丝20在导管10经由开放区15向外扩张、直至处于展开状态,各支撑丝20在展开状态下形成三维结构21。为了避免安全隐患,三维结构21的外轮廓大致呈弧形面,使用时三维结构21抵靠周边组织(例如血管)。
50.三维结构21在自身周向上与周边组织之间至少有三处支撑点,以确保主通道14的远端开口处于或临近主动脉瓣31的几何中心处(在忽略周边组织的横截面为不规则的情况下,周边组织的几何中心为周边组织横截面的圆心),导丝101能够藉由主通道14到达主动脉瓣31处时,能够便于导丝101穿过主动脉瓣31。
51.其中,细长的导管10由弹性材料制成,以使导管10能够沿周边组织穿行,导管10内的主通道14以及各副通道13均并行设置。支撑丝20的长度长于副通道13的长度,并暴露在导管10的近端12,以便于术者操控各支撑丝20。收纳状态下,沿导管10的轴向,各支撑丝20在开放区15的长度与开放区15的长度等长设置。
52.当然,在其他一些实施例中,导丝101也可以预先到达主动脉瓣31处,导管10能够藉由导丝101沿周边组织到达主动脉瓣31处,然后各支撑丝20在导管10的经由开放区15向外扩张、直至处于展开状态,在三维结构21抵靠周边组织的内壁后,以确保导丝101的远端处于或临近周边组织的几何中心处,然后推动导丝101、使导丝101穿过主动脉瓣31。
53.导管10具有一腔体,腔体内穿设有多根管件,各管件均带有一腔体,各管件的腔体与各通道相对应,为了保证各支撑丝20稳定的由开放区15延伸出副通道13,需要将各管件与导管10相对固定,会造成导丝跨瓣器100加工工艺复杂。为了解决该技术问题,参考附图3,在本实施例中,导管10为多腔管,多腔管的各腔分别与各通道相对应。导管10在加工时连通主通道14与副通道13一体成型,不仅可以降低各通道的加工工艺的难度,同时还能够保证各通道之间的相对位置不变。
54.其中,多腔管的腔体均由导管10的远端11延伸至近端12,并分别在导管10的两端开放。腔体的数量与通道的数量相同,此处的通道是指主通道14和副通道13。
55.参考附图1至附图3,在本实施例中,各副通道13绕主通道14的周向间隔布置。同时推动各支撑丝20,以使各支撑丝20同步沿主通道14径向向外扩张,以降低导丝跨瓣器100的
操作难度。各副通道13呈环形阵列布置在主通道14的周向,且环形阵列的圆心与主通道14的轴线相重合。
56.为了确保各支撑丝20沿主通道14径向向外扩张,参考附图1,参考其中一实施例中,沿导管10的径向,各开放区15均位于导管10的外侧壁、并沿导管10的周向布置;开放区15所在副通道13对应的圆心角为大于120度。优选地,开放区15所在副通道13对应的大于150度。例如图中3中,开放区15所在副通道13对应的圆心角为180度。
57.三维结构21沿导管10轴向的长度过短时,可能会造成三维结构21不能抵持周边组织,影响主通道14的远端的位置;三维结构21沿导管10轴向的长度过长时,三维结构21与周边组织相接触的点具主动脉瓣31的距离过长,此处的周边组织在轴向发生弯曲时,同样可能会影响主通道14的远端位置。沿导管10的轴向,开放区15的两端限定三维结构21的长度,因此开放区15的长度直接影响三维结构21的长度,参考其中一实施例中,沿导管10的轴向,开放区15的长度为4mm-10mm,开放区15沿导管10轴向长度受限于根据周边组织的管径、导管10管径等因素。优选地,开放区15的长度为4mm-10mm。
58.支撑丝20的远端与导管10的固定方式上,参考其中一实施例,支撑丝20采用熔融、焊接、胶粘或紧固件的方式与导管10远端11的固定。
59.支撑丝20固定在导管10远端11时,支撑丝20的远端置于副通道13的远端内,以降低导管10在径向的上尺寸,以使导丝跨瓣器100结构紧凑。例如:支撑丝20通过熔融的方式固定在导管10远端11时,至少导管10的材质为医用塑料材质,支撑丝20的远端置于副通道13的远端内,然后通过副通道13的内壁通过熔融的方式将支撑丝20箍紧,以能够将支撑丝20固定在导管10远端11。
60.为了使各支撑丝20在导管10的远端11形成三维结构21,参考其中一实施例,各支撑丝20在导管10的远端11带有预定型段,该预定型段在展开状态下自膨成三维结构21。各支撑丝20可以通过热定型成预想的初始形状,支撑丝20在体内的环境下恢复到初始形状,可以减少在术中人为干涉三维结构21的形成,以使三维结构21的形成更加精准。参考一实施例中,支撑丝20采用记忆合金,例如镍钛丝。
61.当然,在其它实施例中,各支撑丝20在对应的副通道13内同步运行,并在导管10的近端12相对固定。导丝跨瓣器100在运动至预定位置后,操作者可以通过推动各支撑丝20,各支撑丝20在导管10的开放区15释放,并形成三维结构21。通过推动各支撑丝20的距离,可以根据周边组织内径对调整三维结构21在导管10径向的大小,以增大导丝跨瓣器100的应用场景;导丝跨瓣器100在回收的时,只拉动各支撑丝20,直至各支撑丝20处于收拢状态即可。
62.各支撑丝20在导管10的近端12相对固定可以保证个支撑丝20的同步运行。其中,各支撑丝20同步运动是指:各支撑丝20的运动速度以及运动距离相同。各支撑丝20同步能够保证三维结构21在导管10径向上的尺寸保持一致,避免三维结构21在导管10径向上出现突变,以影响主通道14的远端开口的位置。
63.为了能够使各支撑丝20运动,术者可以直接或间接的驱动各支撑丝20。关于驱动各支撑丝20运动详见下文中关于手柄的具体描述,在此不予以展开。
64.在本实施例中,各支撑丝20由一根金属管切割而成。其中,金属管沿自身长度方向包括切割段以及未切割段,在切割段上进行切割形成各支撑丝20。各支撑丝20分别伸入到
对应的副通道13内后,未切割段暴露于导管10的近端12,以便于与外部手柄相连接。
65.在本实施例中,展开状态下,各支撑丝20弯曲的辐射分布以形成三维的网笼结构,并限定网笼结构的外轮廓。
66.网笼结构具有与导管10延伸方向一致的轴向,展开状态下所有支撑丝20在网笼结构轴向的两端分别聚拢。展开状态下,各支撑丝20处于开放区15的部分通过自身弯曲限定网笼结构的外轮廓。支撑丝20弯曲的部分呈弧形设置,且同根支撑丝20的各部分均处于同一平面,从而使各支撑丝20弯曲时呈辐射分布。
67.在本实施例中,支撑丝20的数量为3~8根。三维结构21与周边组织形成至少3处支撑点,以增加导丝跨瓣器100与周边组织的支撑点,以能够分散导丝跨瓣器100作用在周边组织的应力,减少对周边组织的损害,同时还能够限制网笼结构的沿周边组织径向的窜动。优选地,支撑丝20的数量为三根,副通道13的数量为三个,相应开放区15的数量为三个。
68.在本实施例中,展开状态下,在网笼结构的周向上,各支撑丝20等距分布。展开状态下,各支撑丝20抵靠周边组织时,各支撑丝20的受力均匀,且受到的作用力均指向网笼结构的轴向,以使网笼结构不易变形。为了保证网笼结构在轴向两端上的各支撑丝20等距分布,各副通道13沿导管10周向等距分布。参考其中一实施例中,沿网笼轴向,各支撑丝20在网笼结构的周向上均等距分布。
69.在本实施例中,展开状态下,网笼结构的外轮廓大致为旋转体,各支撑丝20对应旋转体的母线;母线为光滑的曲线。
70.沿导管10的周向,相邻的各支撑丝20之间具有一定的间隙,在忽略该间隙的情况下,网笼结构可以看作是一个支撑丝20绕导管10轴向旋转的旋转体。旋转体具有与导管10延伸方向一致的轴向,各支撑丝20的延伸方向为旋转体的母线,光滑的曲线避免戳伤周边组织并且能够很好的贴合周边组织。参考其中一实施例中,网笼结构的两端均平滑处理方便收纳入导管10内。
71.在本实施例中,导丝跨瓣器100还包括手柄,手柄与导管10的近端12固定连接;手柄内滑动安装有驱动件,驱动件与各支撑丝20的近端连接。
72.导丝跨瓣器100送入人体内部并移动至动脉瓣膜附近后,通过手柄上的驱动件控制各支撑丝20同步运动,完成支撑丝20展开状态;在导丝101穿过动脉瓣膜后,需要对导丝跨瓣器100进行回收时,需要通过手柄上的驱动件拉动各支撑丝20恢复至收拢状态。
73.手柄能够对各部件(例如导管10、驱动件以及支撑丝20)提供支撑,同时还能够为操作人员提供握持的空间,因此对手柄的具体形状和具体结构并没有严格限制,例如可以采用筒状结构或框架式结构,一般原则是至少应有足够的力学强度,并保证与各部件(例如导管10、驱动件以及支撑丝20)之间的牢固连接。就手柄自身而言可以使一体结构或可拆卸的分体结构,为了便于拆卸,可以采用螺栓、销钉等方式连接。
74.驱动件主要是为了带动多根支撑丝20沿导管10轴向运做往复运动,为了实现基本功能可以在现有技术中选取电机、气缸、液压缸甚至是手动驱动部件,当驱动件直接输出的运动方式与各支撑丝20的运动方式不一致时,可以利用适当的传动部件对运动形式进行转行和传递。参考其中一实施例,驱动件为手动驱动部件,驱动件的部分伸入手柄并与各支撑丝20相连,部分裸露在手柄外供操作人员推拨。
75.导丝跨瓣器100在回收的过程中,各支撑丝20均处于收纳状态后,如果驱动件持续
带动各支撑丝20运动,此时会发生导管10的管壁发生堆叠的现象,会造成导管10的径向尺寸变大,以影响导丝跨瓣器100的回收,造成安全隐患;同样的,导丝跨瓣器100在放置的过程中,各支撑丝20均处于展开状态后,如果驱动件持续带动各支撑丝20运动,此时会发生三维结构21的径向持续增大,会造成安全隐患。为了解决该技术问题,参考其中一实施例,支撑体设置有指示驱动件相对位置的刻度标识。
76.刻度标识方便操作人员快速读取驱动件的滑动距离,进而判断各支撑丝20的展开状态与收纳状态。其中,刻度标识通过开槽、激光刻印或者喷漆等方法刻印在驱动件的附近,并沿驱动件的滑动方向布置。
77.参考附图1,本技术一实施例还提供一种介入器械的引导系统,包括导丝101以及提供以上各实施例的导丝跨瓣器100,导丝101活动穿设于主通道14。在介入手术中,导管10的远端11预先到达主动脉瓣31处,然后各支撑丝20在导管10经由开放区15向外扩张、直至处于展开状态,各支撑丝20在展开状态下形成三维结构21,三维结构21在自身周向上与周边组织之间至少有三处支撑点,以确保主通道14的远端开口处于或临近主动脉瓣31的几何中心处,导丝101能够藉由主通道14到达主动脉瓣31处时,能够便于导丝101穿过主动脉瓣。
78.参考附图4,下面阐述导丝跨瓣器100应用在主动脉瓣膜31置换手术:
79.导管10的远端11预先到达主动脉瓣31处,然后三根支撑丝20在展开状态下分锚定在右冠状动脉窦32、左冠状动脉窦33以及无冠状动脉窦底,以使导管10上的主通道14的远端开口处于主动脉瓣31的几何中心处,导丝101能够藉由主通道14到达主动脉瓣膜31处时,便于导丝101穿过主动脉瓣31。
80.以上实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。不同实施例中的技术特征体现在同一附图中时,可视为该附图也同时披露了所涉及的各个实施例的组合例。
81.以上实施例仅表达了本技术的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对申请专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本技术构思的前提下,还可以做出若干变形和改进,这些都属于本技术的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1