一种基于血卟啉单甲醚糖基缀合物的光化一体载药纳米胶束及其制备方法和应用
1.本发明属于载药纳米胶束及光化一体载药纳米粒技术领域,具体涉及一种基于血卟啉单甲醚糖基缀合物的光化一体载药纳米胶束及其制备方法和应用。
背景技术:
2.光动力治疗(photodynamictherapy,pdt)的抗肿瘤机制是当光敏剂在肿瘤部位被特定波长的激光激发后,将能量传递给周围的氧气等物质而产生活性氧(ros),活性氧能诱导肿瘤细胞的凋亡和坏死。光动力治疗具有肿瘤传统治疗手段无法替代的独特优势:(1)无耐药性产生,可重复多次使用;(2)不产生免疫力损害;(3)可在手术、化疗和放疗后或同时使用,具有良好的兼容性;(4)仅在光照时才发生作用,其副作用小且较易控制。因此,光动力治疗被认为是一种更安全且具有选择性的癌症治疗策略,已成为肿瘤防治科学中极为活跃的研究领域。特别是随着激光技术、光导纤维和医学光照设备的不断进步和发展,光动力治疗在癌症治疗领域的应用日益广泛。
3.恶性肿瘤是一类多病因、多阶段、多结局的全身系统性慢性疾病,单一的治疗方式往往疗效有限,联合化疗和光动力治疗显示出强大的抗肿瘤效果。化疗与光动力治疗的联合应用能显著提高抗肿瘤效果,其具有以下优势:(1)增加肿瘤细胞对化疗药的敏感性,提高化疗效果;(2)减少化疗药的剂量,降低毒副作用;(3)多种作用机制促进肿瘤细胞的凋亡和坏死,克服肿瘤的多药耐药,发挥高效的协同抗肿瘤作用。因此,化疗与光动力治疗的联合应用具有良好的临床应用前景。
4.然而,因化疗药和光敏剂在理化性质和药动学性质上存在显著差异,如何实现二者的高效同步递药仍是一个亟待解决的难题。纳米药物递送系统是通过包封或者吸附等手段,将药物小分子整合于纳米材料中,形成药物纳米颗粒,可以实现有效的递送。但由于ddss的载药量低、载体毒性、合成操作复杂等原因,都严重限制了这些高效的纳米药物递送系统在临床中的转化与应用。无载体纳米药物在不使用或者在使用少量聚合物材料的情况下,基于纯活性物质制备而成纳米自递送药物体系能够克服载体递药系统的诸多缺点。因此,如何基于光敏剂构建肿瘤微环境响应的纳米自递送系统,同时作为载体负载抗肿瘤化药紫杉醇,实现光动力治疗与化疗相结合的治疗具有重要意义。
技术实现要素:
5.本发明解决的技术问题是提供了一种基于血卟啉单甲醚糖基缀合物的光化一体载药纳米胶束及其制备方法,该方法将光敏剂血卟啉单甲醚与单糖相连合成环状小分子两亲性糖基缀合物,再自组装形成纳米载药胶束,进一步通过共载化疗药紫杉醇实现化疗药和光敏剂的高效共载和同步递送,最终构建肿瘤微环境响应的载药纳米胶束,实现对肿瘤无载体光化一体治疗,该光化一体载药纳米胶束能够用于制备治疗抗肿瘤药物。
6.本发明为解决上述技术问题采用如下技术方案,一种基于血卟啉单甲醚糖基缀合
物的光化一体载药纳米胶束,其特征在于:该光化一体载药纳米胶束由具有环状结构的血卟啉单甲醚糖基缀合物自组装形成纳米胶束并共载化疗药物形成,其中具有环状结构的血卟啉单甲醚糖基缀合物的结构式为:
[0007][0008]
进一步限定,所述化疗药物为抗肿瘤药物,优选为脂溶性的紫杉醇。
[0009]
本发明所述的基于血卟啉单甲醚糖基缀合物的光化一体载药纳米胶束的制备方法,其特征在于具体过程为:将具有环状结构的血卟啉单甲醚糖基缀合物和化疗药物溶于氯仿/甲醇的混合溶液中,于37℃旋转蒸发去除氯仿直至形成薄膜,真空干燥,再加入ph7.4的hepes缓冲溶液,置于摇床中于37℃水化,然后在冰浴条件下探头超声得到光化一体载药纳米胶束。
[0010]
进一步限定,所述具有环状结构的血卟啉单甲醚糖基缀合物的具体制备步骤为:
[0011]
步骤s1:将单糖在碱性化合物的作用下与醋酸酐反应得到全乙酰单糖化合物1,其中单糖为葡萄糖、半乳糖或甘露糖,碱性化合物为甲醇钠、吡啶或醋酸钠;
[0012]
步骤s2:将全乙酰单糖化合物1在酸性化合物的作用下与炔丙醇反应生成丙炔糖化合物2,其中酸性化合物为乙酸、盐酸或三氟化硼乙醚;
[0013]
步骤s3:将丙炔糖化合物2在碱性化合物的作用下脱乙酰基保护并在碱性条件下与对甲苯磺酰氯反应得到化合物3,其中碱性化合物为甲醇钠、碳酸钾、氢氧化钠或氢氧化钾;
[0014]
步骤s4:将化合物3与硫代乙酸钾反应得到化合物4;
[0015]
步骤s5:将血卟啉单甲醚与3-叠氮基丙胺在dcc和dipea的作用下反应生成叠氮修饰的血卟啉单甲醚化合物5;
[0016]
步骤s6:将化合物4和化合物5在抗坏血酸钠和铜盐的作用下反应得到化合物6,其中铜盐为无水硫酸铜、氯化亚铜或碘化亚铜;
[0017]
步骤s7:将化合物6在碱性化合物的作用下脱保护得到目标化合物具有环状结构的血卟啉单甲醚糖缀合物,其中甲醇钠、碳酸钾、氢氧化钠或氢氧化钾;
[0018]
制备过程的合成路线为:
[0019]
[0020][0021]
本发明所述的基于血卟啉单甲醚糖基缀合物的光化一体载药纳米胶束在制备抗肿瘤药物中的应用,该光化一体载药纳米胶束能够显著提高光敏剂和化疗药物的协同抗肿瘤效果。
[0022]
本发明中具有环状结构的血卟啉单甲醚糖基缀合物具有两亲性,可以自组装形成胶束,本发明采用薄膜蒸发-探头超声的方法制备胶束,血卟啉单甲醚是脂溶性的核,糖基部分是亲水性的壳,脂溶性的化疗药物紫杉醇可以包裹在脂溶性的核中,进而实现化疗药物无载体递送。
[0023]
本发明具有以下优点和有益效果:本发明中具有环状结构的血卟啉单甲醚糖缀合物合成路线简洁,反应条件温和;纳米胶束制备工艺简单,粒径小且均一;通过改变亲水性单糖即可发散式获得大量的具有环状结构的血卟啉单甲醚糖缀合物,以到达靶向不同肿瘤细胞的作用;载药纳米胶束在肿瘤微环境中,特异性响应,协同触发药物在肿瘤部位的选择性释放。本发明设计的基于无载体递送的光化一体小分子自组装纳米递药系统能够显著提高光敏剂和化疗药的协同抗肿瘤效果。
附图说明
[0024]
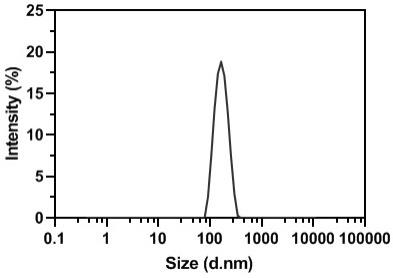
图1是实施例制得的光化一体载药纳米胶束的粒径分布图;
[0025]
图2是实施例制得的光化一体载药纳米胶束的电位图;
[0026]
图3是实施例制得的光化一体载药纳米胶束的透射电子显微镜图。
具体实施方式
[0027]
以下通过实施例对本发明的上述内容做进一步详细说明,但不应该将此理解为本发明上述主题的范围仅限于以下的实施例,凡基于本发明上述内容实现的技术均属于本发明的范围。
[0028][0029]
以下提供本发明的实施例以如上化合物hmme-gal为例:
[0030]
实施例
[0031]
hmme-gal的合成
[0032]
1,2,3,4,6-五-o-乙酰基-β-d-吡喃半乳糖的合成:
[0033][0034]
取350ml乙酸酐和干燥无水半乳糖(50g)置于2l烧瓶中,并将反应混合物加热至50℃。加入无水乙酸钠(25g)并将混合物搅拌,直至获得澄清的溶液。将温度升高至90℃,将反应混合物在此温度下持续反应2.5h,然后将其冷却并倒入搅拌的冰水中。3h后,将结晶物质过滤并在热的甲醇中结晶。将产物通过重结晶进一步纯化得到化合物1b。
[0035][0036]
取1,2,3,4,6-五-o-乙酰基-β-d-吡喃葡萄糖(2.0mmol)溶解于干燥二氯甲烷中,氮气保护,0℃加入炔丙醇(3.0mmol),然后缓慢滴加三氟化硼乙醚(3.6mmol),室温反应过夜。待反应结束,加入碳酸钾(200mg)搅拌30min淬灭反应,过滤,滤液加水,二氯甲烷萃取3次,无水硫酸钠干燥,减压蒸馏除去溶剂。浓缩物经柱层析分离得到目标化合物2b,白色固体,产率为88%。m.p.122-124℃.1h nmr(600mhz,cdcl3)δ5.40(s,1h),5.22(t,j=9.2hz,
1h),5.06(d,j=10.2hz,1h),4.74(d,j=8.4hz,1h),4.38(s,2h),4.22-4.16(m,1h),4.14-4.11(m,1h),3.94(t,j=6.6hz,1h),2.46(s,1h),2.15(s,3h),2.07(s,3h),2.05(s,3h),1.99(s,3h).hrms(esi),m/z calcd.for c
17h23o10
([m+h]
+
)387.1286,found:387.1290。
[0037][0038]
取化合物2b(1.52mmol)于圆底烧瓶中用甲醇溶解,加入甲醇钠溶液调节ph为8-9,室温搅拌。tlc监测原料反应完全,加入酸性树脂调节ph约为7,过滤,旋干滤液后真空干燥做下一步。取真空干燥后的油状物于圆底烧瓶中,吡啶溶解后在冰浴下缓慢加入对甲苯磺酰氯的吡啶溶液(3.04mmol),再加入4-二甲氨基吡啶(0.76mmol),室温搅拌。tlc监测原料反应完全后,冰浴下滴加苯甲酰氯(6.08mmol),室温搅拌至反应完全。旋干吡啶,用柱色谱进行分离即可得到白色固体化合物3b。1h nmr(400mhz,cdcl3)δ7.95(d,j=8.4hz,2h),7.75(m,4h),7.61-7.51(m,2h),7.54(s,1h),7.43-7.37(m,7h),7.23-7.19(m,4h),5.40(s,1h),5.22(t,j=9.2hz,1h),5.03(d,j=10.2hz,1h),4.64(d,j=8.4hz,1h),4.38(s,2h),4.19-4.16(m,1h),4.12-4.11(m,1h),3.90(t,j=6.6hz,1h),2.47(s,1h)。
[0039][0040]
取化合物3b(0.77mmol)于圆底烧瓶中,丙酮溶解,加入硫代乙酸钾(3.09mmol)和四丁基碘化铵(0.08mmol),于65℃回流搅拌。tlc监测原料反应完全后,冷却至室温,旋干丙酮,柱色谱分离(石油醚:乙酸乙酯=6:1,v/v)即可得到黄色固体化合物4b。1h nmr(400mhz,cdcl3)δ7.98-7.92(m,4h),7.81(d,j=7.2hz,2h),7.51(t,j=7.2hz,2h),7.45-7.34(m,5h),7.27(t,j=8.0hz,2h),5.40(s,1h),5.22(t,j=9.2hz,1h),5.03(d,j=10.2hz,1h),4.64(d,j=8.4hz,1h),4.38(s,2h),4.19-4.16(m,1h),4.12-4.11(m,1h),3.90(t,j=6.6hz,1h),2.47(s,1h),2.30(s,3h)。
[0041][0042]
取血卟啉单甲醚(1mmol)溶解于干燥二氯甲烷中,加入适量分子筛,0℃搅拌30min。在另一个圆底烧瓶中取3-叠氮基丙胺(2.6mmol)和dcc(2.5mmol)溶解于二氯甲烷中(2ml),然后加入dipea(2.5mmol)。接下来将其缓慢滴加于血卟啉单甲醚溶液中。反应室温搅拌过夜。待反应完全,过滤除去分子筛,滤液减压蒸馏得到浓缩物,浓缩物用用色谱柱
分离得到目标化合物5。1h nmr(400mhz,cdcl3)δppm:10.24,10.04,9.89,9.94(s,4h),7.70(s,2h),6.36(d,j=7.0hz,2h,),4.70(m,4h),3.75-3.67(m,12h),3.66-3.63(m,12h),3.02(s,2h),2.40-2.05(m,14h)。
[0043][0044]
化合物4b(0.5mmol)和化合物5(0.2mmol)溶解于水和四氢呋喃(1:1,v/v,10ml)的混合溶剂中,加入抗坏血酸钠(0.2mmol)和五水硫酸铜(0.1mmol),避光65℃搅拌4h。待反应结束,减压蒸馏除去四氢呋喃,然后加入乙酸乙酯萃取3次,合并有机相,无水硫酸钠干燥,减压蒸馏除去溶剂,浓缩物经柱层析分离得到目标化合物6。1h nmr(400mhz,cdcl3)δppm:10.24,10.04,9.89,9.94(s,4h),7.96-7.90(m,8h),7.88(d,j=7.6hz,2h),7.75(d,j=8.4hz,4h),7.70(s,2h),7.67(s,2h),7.60(t,j=8.0hz,2h),7.54(s,2h),7.53-7.49(m,4h),7.48-7.31(m,12h),7.26(t,j=8.0hz,4h),6.36(d,j=7.0hz,2h,),5.40(s,1h),5.22(t,j=9.2hz,1h),5.03(d,j=10.2hz,1h),4.64(d,j=8.4hz,1h),4.70(m,4h),4.38(s,2h),4.19-4.16(m,1h),4.12-4.11(m,1h),3.90(t,j=6.6hz,1h),3.75-3.67(m,12h),3.66-3.63(m,12h),3.02(s,2h),2.40-2.05(m,14h),2.30(s,3h)。
[0045][0046]
取化合物6于圆底烧瓶中,加入10ml甲醇溶解,室温条件下滴加1mol/l的甲醇钠溶液调节ph为8-9。tlc监测原料反应完全后,加入酸性树脂调节ph约为7,过滤,旋干溶剂后真空干燥得到化合物7。1h nmr(400mhz,cd3od)δppm:10.24,10.04,9.89,9.94(s,4h),8.03(s,2h),5.40(s,1h),5.22(t,j=9.2hz,1h),5.03(d,j=10.2hz,1h),4.76-4.69(m,4h),4.68(d,j=8.4hz,1h),4.38(s,2h),4.19-4.16(m,1h),4.12-4.11(m,1h),3.90(t,j=6.6hz,1h),3.75-3.67(m,12h),3.66-3.63(m,12h),3.02(s,2h),2.40-2.05(m,14h),2.30(s,3h)。
[0047]
ptx@hmme-gal纳米胶束的制备
[0048]
采用薄膜分散-探头超声法制备ptx@hmme-gal纳米胶束,取hmme-gal和ptx溶于氯
仿/甲醇的混合溶液中,于37℃旋转蒸发除去氯仿直至形成薄膜,真空干燥过夜;加入10mmol
·
l-1
的hepes缓冲溶液(ph 7.4)1ml,放入摇床中,于37℃水化30min,在冰浴条件下探头超声得到ptx@hmme-gal纳米胶束。利用透射电镜观察ptx@hmme-gal纳米胶束的形貌。ptx@hmme-gal纳米胶束表面光滑,呈球形,粒径120nm左右。动态光散射(dls)分析表明(图2),ptx@hmme-gal纳米胶束的平均粒径和多分散性指数(pdi)分别为157.4
±
7.69nm和0.074,揭示出ptx@hmme-gal纳米胶束在水溶液中分散性良好并没有显著的聚合。
[0049]
以上显示和描述了本发明的基本原理,主要特征和优点,在不脱离本发明精神和范围的前提下,本发明还有各种变化和改进,这些变化和改进都落入要求保护的本发明的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1