大环寡肽与κ阿片样物质受体配体组合用于MS疗法
kor,最近被提出参与ms的发病机理(du,nat commun 7,2016,11120;mei,j neurosci,2016,36(30),7925-35)。阿片受体的缺失可以部分解释通常在ms患者中观察到的中枢神经性疼痛(baron,nat clin pract neurol 2(2),2006,95-106)。据报道,孕妇表达较高水平的内源性阿片样物质(akil,annu rev neurosci 7,1984,223-55)。妊娠ms患者经历疾病的缓解,并且较少复发。然而,分娩后三个月,这些妇女表现出复发率的显著增加,与内源性阿片样物质水平的降低相反(roullet,j neurol neurosurg psychiatry 56(10),1993,1062-5;lutton,exp biol med(maywood)229(1),2004,12-20)。此外,最近的研究表明,kor的基因缺失诱导了明显更严重的eae表型(du,同前;mei,nat med 20(8),2014,954-960;mei,2016,同前)。kor不影响t细胞的分化和功能,相反,其在opc向有髓少突神经胶质细胞(myelinating oligodendrocytes)(ol)的分化中起关键作用(du同前)。因此,通过激动剂诸如u50,488靶向kor促进opc分化和髓鞘再生,而kor敲除阻止激动剂介导的有益作用(du,同前;mei,2014,同前;mei,2016,同前)。几项研究报道了髓磷脂对维持轴突完整性的必要作用,推测是通过向轴突提供物理和代谢支持来维持轴突完整性(lee,nature,2012,487(7408),443-8;mei,2014,同前)。最近利用高通量筛选的努力已鉴定了大量有利于髓鞘再生的化合物(mei,2014,同前;najm,nature,2015,522(7555),216-20)。在wo 2019/171333中,预示了kor激动剂纳呋拉啡(nalfurafine)在治疗脱髓鞘疾病中的用途。鉴于纳呋拉啡在cns脱髓鞘疾病模型中减少神经炎症和促进髓鞘再生,denny(clinical&translational immunology 10(1),e1234,2021,1-19)讨论了纳呋拉啡在ms治疗中的临床应用前景。另外,tangherlini(j.med.chem.62,2019,893-907)描述了用于治疗神经炎症的基于喹喔啉的kor激动剂的开发。此外,已显示[t20k]kalata b1结合并激活hkor(muratspahic和gruber,2018,“nature-derived peptides as molecular tools to study gpcr signaling”journal of peptide science 24,s137-s137,2018)。
[0006]
然而,由于有害的副作用和脱靶受体,kor激动剂诸如u50,488的临床潜力受到限制。特别地,存在kor激动剂,诸如u50,488,其在所需的药物有效剂量/浓度显示出诸如烦躁不安、镇静、多尿和/或幻觉等副作用(lalanne,front psychiatry,2014,5,170)。已知胞质溶胶蛋白beta-抑制蛋白2(β-抑制蛋白2)的募集是这方面的相关机制(lalanne同前)。因此,迫切需要在ms和相关疾病/缺陷/症状的治疗中与减少的副作用和提高的效力相关联的新型化合物的连续鉴定。另外,尽管有多种可用的ms药物,但仍存在未满足的临床需求,即开发在预防ms患者的失能进展方面具有提高的功效的新ms药物。
[0007]
因此,本发明基本的问题是提供用于ms和相关疾病、缺陷和/或症状的改进的医学干预,特别是用于ms和相关疾病、缺陷和/或症状的医学干预且不具有副作用、具有较少或改善的副作用的工具和方法。
[0008]
该技术问题通过提供权利要求中表征的实施方案来解决。
[0009]
本发明涉及脱髓鞘疾病、神经病学病症和/或神经相关疾病(如ms)以及相关疾病、缺陷和/或症状的组合治疗,所述组合治疗包含大环寡肽和kor的配体的施用/医学使用。在本说明书中还设想了神经炎症的治疗。
[0010]
本发明涉及ms和相关疾病、缺陷和/或症状的组合治疗,所述组合治疗包含大环寡肽和kor的配体的施用/医学使用。
[0011]
本发明还涉及一种药物组合物,其包含
[0012]
(a)大环寡肽;和
[0013]
(b)kor的配体,
[0014]
或(a)和(b)的组合,
[0015]
用于以下的用途
[0016]
(i)治疗ms(例如通过疗法或预防性(prophylactic)/防治性(preventive)治疗进行治疗);
[0017]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生,和/或改善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0018]
(iii)预防或减少脱髓鞘(特别是少突神经质细胞的脱髓鞘)和/或预防(新的)cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0019]
(iv)治疗(例如通过疗法治疗或预防性/防治治疗)疼痛,特别是神经性疼痛(例如中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0020]
本发明还涉及一种药物组合物,其包含
[0021]
(a)大环寡肽;和
[0022]
(b)kor的配体,
[0023]
或(a)和(b)的组合,
[0024]
用于以下的用途
[0025]
(v)治疗cns损伤;和/或
[0026]
(vi)治疗脱髓鞘疾病、神经病学病症和/或神经相关疾病。
[0027]
本发明还涉及在上述(i)、(ii)、(iii)、(iv)、(v)和/或(vi)中与kor的配体(包含其的药物组合物)组合使用的大环寡肽(包含其的药物组合物)。
[0028]
本发明还涉及在上述(i)、(ii)、(iii)、(iv)、(v)和/或(vi)中与大环寡肽(包含其的化合物)组合使用的kor的配体(包含其的药物组合物)。
[0029]
本发明还涉及用于以下方面的方法:
[0030]
(i)治疗ms(例如通过疗法或预防性/防治性治疗进行治疗);
[0031]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生,和/或改善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0032]
(iii)预防或减少脱髓鞘(特别是少突神经质细胞的脱髓鞘)和/或预防(新的)cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0033]
(iv)治疗(例如通过疗法治疗或预防性/防治性治疗)疼痛,特别是神经性疼痛(例如中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛,
[0034]
所述方法包含向有此需要的受试者施用药学有效量的
[0035]
(a)大环寡肽;和
[0036]
(b)kor的配体,
[0037]
或(a)和(b)的组合,或包含(a)和(b)的药物组合物,或所述组合的步骤。
[0038]
本发明还涉及用于以下方面的方法:
[0039]
(v)治疗cns损伤;和/或
[0040]
(vi)治疗脱髓鞘疾病、神经病学病症和/或神经相关疾病。
[0041]
所述方法包含向有此需要的受试者施用药学有效量的
[0042]
(a)大环寡肽;和
[0043]
(b)kor的配体,
[0044]
或(a)和(b)的组合,或包含(a)和(b)的药物组合物,或所述组合的步骤。
[0045]
本发明解决了上文鉴定的技术问题,因为如下文和所附实施例中所述,令人惊讶地发现大环寡肽能够与kor结合,特别是能够充当kor的配体。
[0046]
在第一实验中(关于详细内容参见所附实施例),来自几种植物物种的富含肽的级分显示出对kor的亲和力。重要的是,从吐根苦荽(carapichea ipecacuanha)和三色堇中分离的大环寡肽能够以在低μm范围内的亲和力与kor结合。值得注意的是,突变体大环寡肽[t20k]-kalata b1(在本文中也称为“t20k”、“[t20k]”或“t20k本身/自身;最初在白花蛇舌草(oldenlandia affinis)中鉴定的;参见例如wo2013/093045)在本文中显示为能够结合并完全活化kor,并充当正构kor的配体。另外,重要的是,在本发明的说明书显示了[t20k]-kalata b1充当kor的变构调节剂,从而增强(作为正变构调节剂,pam)确定的(其它)正构kor的配体的功效/效力。特别地,在本发明的说明书中显示了[t20k]-kalata b1能够影响kor的配体诸如强啡肽a 1-13和u50,488的效力/功效。此外,在本发明的说明书令人惊讶地显示了[t20k]-kalata b1本身不募集β-抑制蛋白2,甚至降低kor的配体如u50,488募集β-抑制蛋白2的功效。因此,在本发明的说明书中提供了可靠的证据:即大环寡肽可以没有kor依赖性和中枢介导的副作用,甚至具有降低kor激动剂诸如强啡肽a 1-13和u50,488的此类作用的潜力。
[0047]
因此,在本发明的说明书中,令人惊讶地证明了大环寡肽,特别是[t20k]-kalata b1,可以在kor处表现出双位作用模式(bitopic mode of action),因为它们充当变构配体以及变构调节剂,并且它们的一种或多种作用伴随着降低的kor依赖性和中枢介导的副作用。换句话说,在本发明的说明书中,令人惊讶地证明了大环寡肽,特别是[t20k]-kalata b1,不仅可以是kor上的正构配体,还可以充当能够以变构方式与kor接合的双位配体。
[0048]
最后,在eae模型中[t20k]-kalata b1穿透cns的能力在本文和所附实施例中得到证实。
[0049]
因此,在本发明的说明书中提供的证据表明,通过(a)一种或多种大环寡肽(特别是[t20k]-kalata b1)与(a)一种或多种kor的配体(特别是(an)一种或多种正构kor激动剂(如强啡肽a 1-13或u50,488))的组合靶向kor,在脱髓鞘疾病、神经病学病症和/或神经相关疾病的治疗中具有很高的潜力,所述治疗是如髓鞘再生和/或疼痛治疗,更具体地为ms(髓鞘再生和/或疼痛)疗法,此外,所述疗法还有望产生有益的免疫抑制作用。此外,当与kor的配体组合时,它们的序列多样性使大环寡肽成为脱髓鞘疾病、神经病学病症和/或神经相关疾病的理想候选疗法,如髓鞘再生和/或疼痛疗法,更具体地,ms(髓鞘再生和/或疼痛)疗法(也参考附图6a、附图6b和附图6c)。
[0050]
在本发明的说明书中应用的治疗,特别是ms治疗和相关疾病、缺陷和/或症状的治疗,可以包括或导致ms发作的复发率和/或频率的降低和/或(相关患者的)失能进展的预防或减退。
[0051]
另外,在本发明的说明书中应用的治疗,特别是ms和相关疾病、缺陷和/或症状的治疗可以包括或导致
[0052]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生,和/或改
善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0053]
(iii)预防或减少脱髓鞘(特别是少突神经胶质细胞的脱髓鞘)和/或预防cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0054]
(iv)治疗(例如通过疗法治疗或预防性/防治治疗)疼痛,特别是神经性疼痛(例如中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0055]
另外,在本发明的治疗,特别是ms和相关疾病、缺陷和/或症状的治疗的上下文中,
[0056]
(i)将诱导或增加髓鞘再生,特别是少突神经胶质细胞的髓鞘再生,和/或将改善(例如减少或治愈/愈合)cns损伤(例如脑部损伤);
[0057]
(ii)将预防或减少脱髓鞘,特别是少突神经胶质细胞的脱髓鞘,和/或将预防cns损伤(例如脑损伤)的形成,和/或减少现存cns损伤(例如脑损伤);和/或
[0058]
(iii)将治疗疼痛,特别是神经性疼痛(例如中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0059]
在本发明的说明书中,治疗,特别是ms相关疾病、缺陷和/或症状的治疗,例如,被设想为意指(新的)cns损伤(例如脑损伤)(的形成)、(少突神经胶质细胞的)脱髓鞘、(中枢或外周)神经性疼痛、由ms引起/伴随ms的疼痛、失能(的进展)等。
[0060]
所述治疗,特别是ms和相关疾病、缺陷和/或症状的治疗,还可以包括或导致促进opc分化、髓鞘再生和/或(随后的)神经元功能恢复。
[0061]
脱髓鞘疾病、神经病学病症和/或神经相关疾病,特别是ms和相关疾病、缺陷和症状的含义是技术人员所公知的。例如,在ciccarelli(同前)和sospedra(同前)中描述了它们。
[0062]
根据本发明治疗的脱髓鞘疾病、神经病学病症和/或神经相关疾病的实例选自由以下组成的组:ms、视神经炎、德维克氏病、炎性脱髓鞘疾病、中枢神经系统神经病、脊髓病(如脊髓痨)、脑白质病和脑白质营养不良症,或者选自由以下组成的组:格林-巴利综合征及其慢性对应疾病、慢性炎性脱髓鞘性多神经病、抗mag(髓磷脂相关糖蛋白)外周神经病、夏-马-图三氏(cmt)病、铜缺乏症和进行性炎性神经病。
[0063]
在本发明的一个方面的上下文中,将减少/改善或避免副作用,特别是(中枢介导的或外周介导的)kor依赖性副作用,更特别是由β-抑制蛋白2募集引起的副作用。此类副作用是,例如,阿片样物质危险(opioid crisis)/耐受性和/或烦躁不安、镇静、多尿和/或幻觉(或与其相关的副作用)(参考lalanne同前)。因此,在根据本发明的ms和相关疾病、缺陷和/或症状的治疗的一个方面的上下文中,将减少/改善或避免一种或多种此类副作用。
[0064]
优选地,在本发明的说明书中被靶向的kor是人kor(hkor)。因此,优选kor的配体是hkor的配体。通常,优选地,被靶向的kor是待治疗患者的kor。例如,如果待治疗的患者是人,那么被靶向的kor优选是hkor。
[0065]
kor,特别是hkor,在本领域中是公知的,例如描述于lalanne(同前)和du(同前)中。hkor的详细表征,特别是氨基酸序列信息,可从数据库条目https://www.uniprot.org/uniprot/p41145中获得。
[0066]“(h)kor的配体/激动剂”和“(h)kor的配体/激动剂”的含义在本领域是已知的,并且在本文中相应地使用了各自的术语(例如https://www.guidetopharmacology.org/grac/objectdisplayforward?objectid=318&familyid=50&familytype=gpcr)。
[0067]
在本发明的说明书中,kor的配体可以是kor的激动剂(kor的“无偏”配体和“无偏”激动剂)、kor的部分激动剂或kor的偏向性激动剂。
[0068]
在本发明的说明书中,分别地作为kor的“激动剂”和对kor表现出“激动”功能,意味着kor被激活,即其一种或多种相关生物功能被诱导或增强。特别地,分别地作为kor的“激动剂”和对kor表现出“激动”功能,在本发明的说明书中意指kor对阿片样物质刺激的反应(例如细胞内camp减少)被诱导或增强,导致raf/mek
1/2
/erk
1/2
或jak2/stat3信号传导级联的激活(https://pubmed.ncbi.nlm.nih.gov/27881770-enhancing-remyelination-through-a-novel-opioid-receptor-pathway/?from_single_result=borniger+and+hesp;borniger,j neurosci 36(47),2016,3)。用于测试kor的相关生物学功能的测定在本领域中是已知的,并且例如描述于https://pubmed.ncbi.nlm.nih.gov/27881770-enhancing-remyelination-through-a-novel-opioid-receptor-pathway/?from_single_result=borniger+and+hesp中。另外,在所附实施例(例如实施例2和3)中描述了这种测定。
[0069]
kor的多种激动剂是本领域已知的(https://www.guidetopharmacology.org/grac/objectdisplayforward?objectid=318&familyid=50&familytype=gpcr)。kor激动剂的几个非限制性实例在附表6中给出。
[0070]
通常,kor的激动剂是完全配体/激动剂,即“无偏”配体/激动剂。这意味着它们完全激活kor信号传导途径,例如任一特定途径,即g蛋白途径和/或抑制蛋白途径。例如,在本发明的说明书中,kor的“无偏”配体/激动剂是,特别地在相关的内源浓度/剂量或药学上有效的浓度/剂量,诱导或能够诱导抑制蛋白募集,特别是β-抑制蛋白2募集的配体/激动剂,或增强或能够增强抑制蛋白募集,特别是β-抑制蛋白2募集的配体/激动剂。不受理论的束缚,抑制蛋白募集,特别是β-抑制蛋白2募集,可能与kor的更高(和/或更快)的内化相关联。反过来,这可增加例如耐受性的机会(参见阿片样物质危险)。由于抑制蛋白募集,特别是β-抑制蛋白2募集,与副作用(诸如阿片样物质危险/耐受性和/或烦躁不安、镇静、多尿和/或幻觉相关联(lalanne同前),因此完全激动性、“无偏”kor的配体,特别是在所需的药物有效浓度/剂量,通常显示副作用,诸如阿片样物质危险/耐受性和/或烦躁不安、镇静、多尿和/或幻觉(lalanne同前)。
[0071]
本领域已知多种完全激动性“无偏”kor的配体。此类kor激动剂的几个非限制性实例在附表6中给出,并简称为“激动剂”。
[0072]
除了完全激动性、“无偏”kor的配体/激动剂以外,kor的配体/激动剂也可以是“偏向性”配体/激动剂。这意味着它们不(或在较低程度上)激活kor信号传导途径,例如特定途径,即g蛋白途径,或抑制蛋白途径。例如,在本发明的说明书中,kor的“偏向性”配体/激动剂是,特别地在相关的内源浓度/剂量或药学上有效的浓度/剂量,不(或在较低程度上)诱导,或不(或在较低程度上)能够诱导抑制蛋白募集,特别是β-抑制蛋白2募集的配体/激动剂,或不(或在较低程度上)增强,或不(或在较低程度上)能够增强抑制蛋白募集,特别是β-抑制蛋白2募集的配体/激动剂。在本发明的说明书中,“偏向性”kor的配体/激动剂,特别是在所需的药物有效浓度/剂量,显示出较少副作用或无副作用,诸如阿片样物质危险/耐受性和/或烦躁不安、镇静、多尿和/或幻觉。例如,在本发明的说明书中,g蛋白偏向性配体/激动剂显示出减少的副作用。
[0073]
多种“偏向性”kor的配体/激动剂是本领域已知的。此类kor激动剂的几个非限制性实例在附表6中给出,并被称为“偏向性激动剂”。
[0074]
本领域技术人员将理解,kor的配体/激动剂的“偏向”和它们的“偏向因子(bias factor)”分别不是绝对的特征且可以在一定范围内变化。特别地,从“无偏”kor的配体/激动剂到“偏向性”kor的配体/激动剂存在“平稳的过渡”。
[0075]
然而,就kor信号传导途径而言,存在典型的“偏向性”kor的配体/激动剂。典型的“偏向性”kor的配体/激动剂的例子是本领域已知的,并在附表6(“偏向性激动剂”)中给出。优选地,“偏向性”kor的配体/激动剂是天然存在的“偏向性”kor的配体/激动剂。根据本发明使用的典型“偏向性”kor的配体/激动剂的具体非限制性实例是collybolide(蘑菇斑盖金钱菌(collybia maculate))、降伊波加因碱(noribogaine)(植物依波加(iboga)的代谢物)、b-64(salvinorin a衍生物)、纳呋拉啡(吗啡衍生物)、三唑1.1、6-gnti、hs666、hs665和甲磺酰基salvinorin b。
[0076]
同样,对于kor信号传导途径,存在典型的“无偏”kor的配体/激动剂。典型的“无偏”kor的配体/激动剂的实例是本领域已知的,并在附表6(“激动剂”)中给出。根据本发明使用的典型“无偏”kor的配体/激动剂的具体非限制性实例是强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u50488、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林(difelikefalin)(cr845,fe-202845)、也称为d-phe-d-phe-d-leu-d-lys-[γ-(4-n-哌啶基)氨基羧酸)、强啡肽、纳布啡、pentasozin、哌替啶和舒芬太尼。
[0077]
技术人员知道或至少能够容易地测试给定kor的配体/激动剂的“偏向因子”。相应的测定描述于所附的实施例中,并且是本领域已知的(参见,例如,https://www.ncbi.nlm.nih.gov/pmc/articles/pmc3868907(white,mol pharmacol 85(1),2014,83-90)和https://www.ncbi.nlm.nih.gov/pubmed/25320048(white,j pharmacol exp ther 352(1),2015,98-109))。
[0078]
除了完全激动性、“无偏”kor的配体/激动剂以外,kor的配体/激动剂也可以是“部分”配体/激动剂。作为“部分”kor的配体/激动剂意味着配体/激动剂与内源比较/标准配体相比,(对于给定的途径,例如g蛋白或抑制蛋白或其它途径;通常对于g蛋白途径)具有较低的功效。作为非限制性说明,emax减少了1%至99%;0%是拮抗剂,100%是内源性完全激动剂。实际上,“部分”kor的配体/激动剂的功效可具有约20%-80%的内源性完全配体/激动剂的功效。
[0079]
多种“部分”kor的配体/激动剂是本领域已知的。此类kor激动剂的几个非限制性实例在附表6中给出,并被称为“部分激动剂”。典型的“部分”kor的配体/激动剂的具体非限制性实例是强啡肽b、damgo和内吗啡肽-1-amo2。
[0080]
通常,根据本发明使用的kor的配体可以是kor的小分子配体或肽配体,例如kor的内源性肽配体。相应的配体在本领域是已知的。相应的实例在附表6中给出,并分别称为“小分子”、“肽”或“内源性的”。作为kor的配体(特别是激动剂)的小分子的具体但非限制性实例也描述于tangherlini(同前)、bourgeois(j.med.chem.57,2014,6845-60)、molenveld(bioorg.med.chem.lett.25,2015,5326-30)和soeberdt(j.med.chem.60,2017,2526-51)中。一方面,可根据本发明使用基于喹喔啉的kor激动剂(如tangherlini(同前)、bourgeois((同前)、molenveld(同前)中所描述的那些)。此类基于喹喔啉的kor激动剂的实例是化合
物12和化合物14(如,例如,tangherlini(同前)中所描述的;参见其第4.2.1节和第4.2.3节,另见下文的表6)。
[0081]
在本发明的说明书中使用的kor的配体的具体非限制性实例是u50,488或强啡肽a-(1-13)。
[0082]
优选地,要使用的(h)kor配体/激动剂是正构(h)kor配体/激动剂。这意味着其与内源性配体结合(h)kor的相同位点或者是内源性配体。
[0083]
在本发明的说明书中,设想了要使用的(h)kor配体/激动剂((b)项)不是要使用的大环寡肽((a)项)。因此,要所用的(h)kor配体/激动剂被设想为(在本发明的药物组合物、试剂盒或组合等中)不同的附加活性成分。优选地,要使用的(h)kor配体/激动剂根本不是大环寡肽。
[0084]
通常,术语“大环寡肽”的含义是本领域已知的,并且在本文中相应地使用术语“大环寡肽”(参见,例如,http://www.cybase.org.au/index.php上的cybase)。特别地,如本发明的说明书中所用的“大环寡肽”是头尾相接的环化肽,所述大环寡肽链包含六个保守的半胱氨酸残基,所述六个半胱氨酸残基能够形成以环状胱氨酸结(cck)基序排列的三个二硫键(大环寡肽链;参考图7)。大环寡肽的半胱氨酸间(inter-cysteine)序列可以耐受大范围的残基取代(参见,例如,clark,2006,biochem j,394,85-93以及图6和图7)。一方面,本文使用的术语“大环寡肽”是指如craik(1999,j mol biol,294,1327-1336)、clark(2006,同前)和特别地us 7,592,533 b1中所述的大环寡肽。
[0085]
本发明的说明书中使用的“大环寡肽”可以包括环1中典型的glu(e)残基(参考图7)。然而,也可以使用其它“大环寡肽”。例如,caripe型的一些大环寡肽不含有环1中的典型e(参考fahradpour front pharmacol 8,2017,616)。然而,它们被设想为由根据本发明的术语“大环寡肽”所涵盖。术语“大环寡肽”的含义还涵盖“环状打结蛋白(cyclic knottins)”,如不含有环1中的典型e的所述caripe型环状打结蛋白。
[0086]
特别地,要在本发明的说明书中使用的大环寡肽包含能够形成环状骨架的氨基酸序列,其中所述环状骨架包含结构(式i):
[0087]
环状(c[x1…
xa]c[x
i1
…
x
ib
]c[x
ii1
…
x
iic
]c[x
iii1
…
x
iiid
]c[x
iv1
…
x
ive
]c[x
v1
…
x
vf
])
[0088]
其中
[0089]
(i)c为半胱氨酸;
[0090]
(ii)[x1…
xa],[x
i1
…
x
ib
],[x
ii1
…
x
iic
],[x
iii1
…
x
iiid
],[x
iv1
…
x
ive
],和[x
v1
…
x
vf
]中的每一种代表一个或多个氨基酸残基,其中序列残基内或之间的每个一个或多个氨基酸残基可以相同或不同;以及
[0091]
(iii)a、b、c、d、e和f代表各自序列中氨基酸残基的数量,a至f中的每一个可以相同或不同,范围为1至约20。
[0092]
优选地,a为3至6,b为4至8,c为3至10,d为1,e为4至8,和/或f为5至13。
[0093]
可在本发明的说明书中使用/施用的特定大环寡肽是kalata型大环寡肽(例如kalata b型大环寡肽,如kalata b1或其突变体或kalata b2或其突变体;也参见表3和图6a)、caripe型大环寡肽(例如任何caripel至caripe13或其突变体或psyle e或其突变体;也参见表4和图6b)或堇菜型大环寡肽(例如表5中所列的任何堇菜型大环寡肽或其突变体,特别是在本发明的说明书中已经鉴定的新型“vitri”大环寡肽(也称为“vitri肽100”)(gd
pipcgetcftgkcysetigctcewpictkn)或其突变体;另见表5和图6c)。
[0094]
另外,要根据本发明使用/施用的特定大环寡肽可来源于或可包含于白花蛇舌草、三色堇、吐根苦荽、psychotria solitudinum、香堇菜、苦瓜或甜菜。白花蛇舌草、三色堇和吐根苦荽的提取物是优选的)。
[0095]
表3和图6a中描述了kalata b型大环寡肽的非限制性实例。表4和图6b中描述了caripe型大环寡肽的非限制性实例。表5和图6c中描述了堇菜型大环寡肽的非限制性实例。
[0096]
kalata b型大环寡肽是本领域已知的,并且例如描述于wo2013/093045、gr
ü
ndemann(jnatprot 75(2),2012,167-74;2013同前),hellinger(j ethnopharmacol 151(1),2014,299-306)和thell(同前)中。caripe型大环寡肽是本领域已知的,并且例如描述于fahradpour(同前)中。堇菜型大环寡肽在本领域中也是已知的,并且例如描述于hellinger(j proteome res 14(11),2015,4851-62)中。
[0097]
要在本发明的说明书中使用/施用的大环寡肽,特别是kalata b型大环寡肽,可以包含式ii的氨基酸区段(seq id no.17)
[0098]
xxx
1-leu-pro-val-cys-gly-glu-xxx
2-cys-xxx
3-gly-gly-thr-cys-asn-thr-pro-xxx
1-cys-xxx
1-cys-xxx
1-trp-pro-xxx
1-cys-thr-arg-xxx1(ii)。
[0099]
xxx1、xxx2和xxx3可以是任意氨基酸、非天然氨基酸或肽模拟物,优选为脂族氨基酸。特别地,xxx2可以是任意氨基酸、非天然氨基酸或肽模拟物,但不是lys,和/或xxx3可以是任意氨基酸、非天然氨基酸或肽模拟物,但不是ala或lys。优选地,式ii的xxx2和/或xxx3根本没有突变。更具体地,xxx1可以是gly、thr、ser、val、ile、asn、asp或优选为lys,xxx2可以是thr,和/或xxx3可以是val或phe。甚至更具体地,式ii的位置1处的xxx1可以是gly,式ii的位置18处的xxx1可以是lys或优选为gly,式ii的位置20处的xxx1可以是thr、ser或优选为lys,式ii的位置22处的xxx1可以是ser或thr,式ii的位置25处的xxx1可以是val或ile,式ii的位置29处的xxx1可以是asn、asp或优选为lys,式ii的xxx2可以是thr和/或式ii的xxx3可以是val或phe。
[0100]
具体定义的式ii的氨基酸残基也可以根据特定的(类型的)大环寡肽而变化。因此,关于xxx1、xxx2和/或xxx3的描述不仅适用于式ii,也适用于不包含式ii的特定氨基酸区段的其它大环寡肽的相应氨基酸残基。在本说明书中,“对应的”特别地意指一个或多个相同或相似位置处的氨基酸残基。更具体地,“对应的”意指是同源的。其它大环寡肽的实例是本文定义的caripe型大环寡肽,特别是下面定义的包含式iii的氨基酸区段(seq id no.18)的大环寡肽;和本文定义的堇菜型大环寡肽,特别是下面定义的包含式iiii的氨基酸区段(seq id no.19)的大环寡肽。
[0101]
在本发明的说明书中使用/施用的大环寡肽,特别是caripe型大环寡肽,可以包含式iii的氨基酸区段(seq id no.18)
[0102]
gly-xxx
1-ile-pro-cys-xxx
2-xxx
3-xxx
4-cys-xxx
5-xxx
6-xxx
7-xxx
8-cys-xxx
9-xxx
10-xxx
11-ala-xxx
12-xxx
13-xxx
14-cys-xxx
15-cys-xxx
16或-xxx
17-xxx
18-xxx
19-cys-tyr-xxx
20-xxx
21
(seq id no.18)
[0103]
xxx1至xxx
21
中的任一个或全部可以是任何氨基酸、非天然氨基酸或肽模拟物。特别地,xxx1可以是val、ala或leu,xxx2可以是gly、ser或thr,xxx3可以是glu、gly或ser,xxx4可以是ser或thr,xxx5可以是val、leu或phe,xxx6可以是phe或arg,xxx7可以是ile或asn,
id no:7、5、4或6中所示的任一氨基酸序列携带相同的一个或多个突变,或者分别在对应于seq id no:7、5、4或6中所示的任一氨基酸序列中已被突变的一个或多个氨基酸位置的一个或多个氨基酸位置处携带一个或多个突变;
[0114]
(iii)大环寡肽,其包含头尾相接的环化形式的表3、表4或表5所示的大环寡肽的氨基酸序列或由头尾相接的环化形式的表3、表4或表5所示的大环寡肽的氨基酸序列组成,其中所述氨基酸序列分别与seq id no:7、5、4或6中所示的任一氨基酸序列携带相同的一个或多个突变,或者分别在对应于seq id no:7、5、4或6中所示的任一氨基酸序列中已被突变的一个或多个氨基酸位置的一个或多个氨基酸位置处携带一个或多个突变;
[0115]
(iv)大环寡肽,其包含头尾相接的环化形式的与seq id no:7、5、4、6或155中的任一个中所示的(或如表3、表4和表5中任一个表中所示的)氨基酸序列具有至少70%,优选至少80%,更优选到至少90%,甚至更优选至少95%,甚至更优选至少98%和甚至更优选至少99%同一性的氨基酸序列,或由头尾相接的环化形式的与seq id no:7、5、4、6或155中的任一个中所示的(或如表3、表4和表5中任一个表中所示的)氨基酸序列具有至少70%,优选至少80%,更优选到至少90%,甚至更优选至少95%,甚至更优选至少98%和甚至更优选至少99%同一性的氨基酸序列组成,其中所述氨基酸序列分别与seq id no:7、5、4或6中所示的任一氨基酸序列携带相同的一个或多个突变,或者分别在对应于seq id no:7、5、4或6中所示的任一氨基酸序列中已被突变的一个或多个氨基酸位置的一个或多个氨基酸位置处携带一个或多个突变;和
[0116]
(v)大环寡肽,其包含头尾相接的环化形式的以下氨基酸序列或由头尾相接的环化形式的以下氨基酸序列组成:
[0117]
氨基酸序列
[0118]
xxx
1-leu-pro-val-cys-gly-glu-xxx
2-cys-xxx
3-gly-gly-thr-cys-asn-thr-pro-xxx
1-cys-xxx
1-cys-xxx
1-trp-pro-xxx
1-cys-thr-arg-xxx1[0119]
(式ii;seq id no.17),
[0120]
其中xxx1是任意氨基酸、非天然氨基酸或肽模拟物;xxx2是任意氨基酸、非天然氨基酸或肽模拟物,优选为thr;xxx3是任意氨基酸、非天然氨基酸或肽模拟物,优选为val或phe;或者
[0121]
氨基酸序列
[0122]
gly-xxx
1-ile-pro-cys-xxx
2-xxx
3-xxx
4-cys-xxx
5-xxx
6-xxx
7-xxx
8-cys-xxx
9-xxx
10-xxx
11-ala-xxx
12-xxx
13-xxx
14-cys-xxx
15-cys-xxx
16-xxx
17-xxx
18-xxx
19-cys-tyr-xxx
20-xxx
21
(式iii;seq id no.18),
[0123]
其中xxx1是val、ala或leu,xxx2是gly、ser或thr,xxx3是glu、gly或ser,xxx4是ser或thr,xxx5是val、leu或phe,xxx6是phe或arg,xxx7是ile或asn,xxx8是pro或arg,xxx9是ile、phe、thr或leu,xxx
10
是ser、thr、ile或val,xxx
11
是thr、ser、ala、arg或pro,xxx
12
是val、leu或ala,xxx
13
是ile、leu、phe或val,xxx
14
是gly或arg,xxx
15
是ser或thr,xxx
16
是lys、ser或arg,xxx
17
是asn、asp、his或lys,xxx
18
是lys、asn、his或tyr,xxx
19
是val或ile,xxx
20
是arg、leu、lys或asn和/或xxx
21
是asn或asp;
[0124]
或
[0125]
氨基酸序列
[0126]
gly-xxx
1-xxx
2-xxx
3-cys-gly-glu-xxx
4-cys-xxx
5-xxx
6-xxx
7-xxx
8-cys-xxx
9-xxx
10-xxx
11-xxx
12-cys-xxx
13-cys-xxx
14-xxx
15-xxx
16-xxx
17-cys-xxx
18-xxx
19-xxx
20
(式iiii;seq id no.19),
[0127]
其中xxx1至xxx
20
中的任一个或全部可以是任意氨基酸、非天然氨基酸或肽模拟物,优选地,xxx1至xxx
20
中的任一个或全部可以是:eq id no.155中所示的“vitri”大环寡肽的一个或多个相应氨基酸残基的一个或多个保守氨基酸交换,
[0128]
并且其中所述氨基酸序列分别与seq id no:7、5、4或6中所示的任一氨基酸序列携带相同的一个或多个突变,或者分别在对应于seq id no:7、5、4或6中所示的任一氨基酸序列中已被突变的一个或多个氨基酸位置的一个或多个氨基酸位置处携带一个或多个突变。
[0129]
此外,在该方面的上下文中,优选的大环寡肽是携带至lys(k)的突变的大环寡肽,特别是在对应于(例如同源于)t20k大环寡肽的位置20的位置,更特别是t20k突变本身或相应突变。
[0130]
在本发明的说明书中使用/施用的大环寡肽的优选但非限制性实例是由上文(i)至(v)中任一项所定义的头尾相接的环化形式的氨基酸序列组成的大环寡肽。
[0131]
在优选实施方案中,在本发明的说明书中使用/施用的大环寡肽是kalata b型大环寡肽。kalata b型大环寡肽可以是kalata b2或kalata b2型大环寡肽,或者更优选为kalata b1或kalata b1型大环寡肽。大环寡肽kalata b1和b2只有5个氨基酸位置不同(参考seq id no:1及2;wo2013/093045的图6;附表3),即kalata b2中的val至phe(环2)以及thr至ser(环4)、ser至thr(环5)、val至ile(环5)和asn至asp(环6)的保守替换。这些取代没有显著的结构后果(有显著的结构后果(参见wo2013/093045的图6),并且这两种肽具有相似的生物活性特征谱(gruber,toxicon 49,2007,561-575)。然而,在本发明的说明书中使用/施用的最优选大环寡肽是t20k本身(seq id no:7)。
[0132]
在本发明的说明书中使用/施用的大环寡肽的具体的非限制性实例是这样的大环寡肽,其包含头尾相接的环化形式的seq id no:7、5、4、6或155中所示的氨基酸序列或由头尾相接的环化形式的seq id no:7、5、4、6或155中所示的氨基酸序列组成。
[0133]
在本发明的说明书中,设想了要使用的大环寡肽是非接枝的,即非接枝大环寡肽。
[0134]
术语“非接枝的”或“非接枝大环寡肽”意指大环寡肽不包括另一种/另外的(药物)活性组分,如(药物)活性肽或肽表位,所述肽或肽表位已经作为接枝模板或接枝框架被接枝到大环寡肽支架中。
[0135]
因此,最优选的是,在本发明的说明书中使用/施用的大环寡肽是(天然存在的、天然的或突变的)非接枝大环寡肽,即“本身”/“自身”不含一种或多种任何另外的(药物)活性组分的大环寡肽。
[0136]
在本领域中已知,大环寡肽可以充当其它(药物)活性组分如其它治疗性肽的支架(参见,例如,gunasekera,2008,j med chem,51,7697-704;wang,acs chemical biology 9,2014,156-63;us2010/0298528)。此类接枝大环寡肽,在本领域中也称为“大环寡肽的接枝类似物”(例如gunasekera同前)、“生物工程环肽”(例如wang2014同前),等等,即包含另外的(药物)活性组分的大环寡肽,在本发明的说明书中是不太优选的。已知接枝大环寡肽的特定实例是两个半胱氨酸残基之间的至少一个(+/-完整)环被另外的(药物)活性组分替
代的大环寡肽(参见,例如gunasekera同前;wang 2014同前;us2010/0298528)。接枝大环寡肽的“另外的(药物)活性组分”在本领域中也称为“生物活性序列”(例如gunasekera同前)、
““
生物活性”表位”/”(肽)表位”(gunasekera同前)、“(潜在)治疗性氨基酸序列”(wang2014同前)、“(抗原性)肽”(wang 2014同前)、“接枝”(us2010/0298528)等。这种“其它(药物)活性组分”的实例是mog
35-55
表位(wang 2014同前)、rgd表位(us2010/0298528)以及在例如us2010/0298528或gunasekera(同前)的上下文中已被接枝到大环寡肽支架上的其它表位。
[0137]
这将与本发明的说明书中优选使用的大环寡肽和大环寡肽突变体/变体形成对比。具体而言,本发明的说明书中使用的大环寡肽突变体/变体被设想为突变的,使得不再引入另外的(药物)活性组分,即接枝。
[0138]
因此,在本发明的说明书中,术语“大环寡肽”特别被设想为指大环寡肽本身或突变的大环寡肽本身,即非接枝大环寡肽或非接枝突变的大环寡肽,但不包括大环寡肽的接枝类似物、生物工程环肽等,即接枝大环寡肽。术语“大环寡肽”也相应地用于本领域。
[0139]
对于在本发明的说明书中使用/施用的大环寡肽突变体/变体,两个半胱氨酸残基之间的一个或多个(+/-完整)环可能被(一段)另外的氨基酸残基替代,只要没有引入另外的(药物)活性成分。本领域技术人能够容易地分别区分接枝大环寡肽与非接枝大环寡肽,以及接枝大环寡肽与非接枝大环寡肽突变体/变体。
[0140]
然而,原则上,在本发明的说明书中也可以使用/施用接枝大环寡肽。例如,接枝大环寡肽可以与公开的kor配体和/或非接枝大环寡肽组合使用/施用。
[0141]
应当理解,对于在本发明的说明书中使用/施用的各种大环寡肽,一级序列,即氨基酸序列主链中一定的灵活性和可变性是可能的,只要确保由至少一些固定的氨基酸残基和它们的空间排列定义的各个肽的总体二级和三级结构(参见,例如,上文的式i、ii、iii和iiii)。
[0142]
基于本文提供的教导,一方面,本领域技术人员能够容易地找到/鉴定根据本发明起作用的大环寡肽的相应突变体/变体。另一方面,技术人员能够测试给定的大环寡肽突变体/变体是否仍然具有期望的功能,例如至少一种本文别处描述的功能。此类测试的相应实验指导,即各自的测定,在本领域是已知的,并在本文和所附实例中示例性地提供和描述。
[0143]
因此,一方面,本发明还涉及本文中定义的(天然)大环寡肽的突变体或变体形式的使用/施用,特别是表3、表4和表5中所示的大环寡肽的突变体或变体形式的使用/施用,更特别是kalata b2或优选kalata b1的突变体或变体形式的使用/施用。突变体或变体形式可以被(合成地)优化,即,与它们的非突变体/非变体形式相比,它们可以更好地适用于治疗ms和相关疾病和/或症状。大环寡肽的突变体/变体形式的非限制性实例是表3、表4和表5中所示的环状肽,其中已经进行了一个或多个与seq id no:4至7中的任一个相同的突变,或者已经在对应于(例如同源于)seq id no:4至7中的任一个中已被突变的氨基酸位置的氨基酸位置处进行了一个或多个相应的(例如同源的)突变。
[0144]
如果没有不同地提及,当在本文使用时,术语“大环寡肽”被设想为也涵盖“一个或多个大环寡肽突变体/变体”。
[0145]
根据本发明的突变的/变异的/经修饰的大环寡肽的非限制性实例在上文第(iv)节中给出,或者是由上文第(iv)节中定义的头尾相接的环化形式的氨基酸序列组成的大环寡肽。突变的/变异的/经修饰的大环寡肽的其它实例是包含选自由seq id no:4至7组成的
组的氨基酸序列的大环寡肽,或由头尾相接的环化形式的选自由seq id no:4至7组成的组的氨基酸序列组成的大环寡肽。
[0146]
至于大环寡肽的突变体/变体,例如,设想相应的天然存在的肽或天然肽的一个或多个氨基酸分别被其它一个或多个天然存在的或合成的氨基酸替换。在这种情况下,优选的是,这种/这些氨基酸交换是一个或多个保守氨基酸交换,即一个或多个替换氨基酸与待替换的一个或多个氨基酸属于相同的氨基酸类别。例如,酸性氨基酸可以被另一种酸性氨基酸替换,碱性氨基酸可以被另一种碱性氨基酸替换,脂肪族氨基酸可以被另一种脂肪族氨基酸替换,和/或极性氨基酸可以被另一种极性氨基酸替换。
[0147]
特别设想的是,导致所公开的大环寡肽的突变体/变体的氨基酸交换使得所得突变体/变体的三级结构内的极性和电荷模式仍然(基本上)模拟/对应于相应大环寡肽的三维结构。
[0148]
突变体或变体环状肽的另外的实例是kalata b型大环寡肽(例如kalata b1或其突变体/变体或kalata b2或其突变体;也参见表3);或caripe型大环寡肽(例如caripe 1-13或其突变体/变体或psyle e或其突变体/变体中的任一种;也参见表4);或堇菜型大环寡肽(例如表5所示的任何堇菜型大环寡肽或其突变体/变体;也参见表5);或由seq id no:1或2的氨基酸序列或seq id no:20-187中的任一个的氨基酸序列的头尾相接的环化形式组成的大环寡肽,
[0149]
(i)其至少1个、2个、3个、4个、5个、6个、7个、8个、9个或10个酸性氨基酸残基分别被1个、2个、3个、4个、5个、6个、7个、8个、9个或10个选自由酸性氨基酸残基组成的组的不同氨基酸残基替换;
[0150]
(ii)其至少1个、2个、3个、4个、5个、6个、7个、8个、9个或10个碱性氨基酸残基分别被1个、2个、3个、4个、5个、6个、7个、8个、9个或10个选自由碱性氨基酸残基组成的组的不同氨基酸残基替换;和/或
[0151]
(iii)其至少1个、2个、3个、4个、5个、6个、7个、8个、9个或10个脂肪族氨基酸残基分别被1个、2个、3个、4个、5个、6个、7个、8个、9个或10个选自由脂肪族氨基酸残基组成的组的不同氨基酸残基替换。
[0152]
其它突变的/变异的大环寡肽包含式ii、iii或iiii的氨基酸区段,但所述氨基酸区段的
[0153]
(i)至少1个、2个、3个、4个、5个、6个、7个、8个、9个或10个(其余特定的)酸性氨基酸残基分别被1个、2个、3个、4个、5个、6个、7个、8个、9个或10个选自由酸性氨基酸残基组成的组的不同氨基酸残基替换;
[0154]
(ii)至少1个、2个、3个、4个、5个、6个、7个、8个、9个或10个(其余特定的)碱性氨基酸残基分别被1个、2个、3个、4个、5个、6个、7个、8个、9个或10个选自由碱性氨基酸残基组成的组的不同氨基酸残基替换;和/或
[0155]
(iii)至少1个、2个、3个、4个、5个、6个、7个、8个、9个或10个(其余特定的)脂肪族氨基酸残基分别被1个、2个、3个、4个、5个、6个、7个、8个、9个或10个选自由脂肪族氨基酸残基组成的组的不同氨基酸残基替换。
[0156]
通常,术语“氨基酸”或“氨基酸残基”的含义是本领域已知的,并相应地用于本文中。因此,值得注意的是,当“氨基酸”是肽/蛋白质的组分时,术语“氨基酸”在本文中以与“氨基酸残基”相同的意义使用。
[0157]
特别地,本文所提及的“氨基酸”或“氨基酸残基”被设想为天然存在的氨基酸,更优选是天然存在的l-氨基酸。然而,尽管不太优选,但本发明的说明书中的“氨基酸”或“氨基酸残基”也可以是d-氨基酸或非天然存在的(即合成的)氨基酸,例如正亮氨酸、β-丙氨酸或硒代半胱氨酸。
[0158]
术语“一个或多个酸性氨基酸”、“一个或多个碱性氨基酸”、“一个或多个脂肪族氨基酸”和“一个或多个极性氨基酸”的含义在本领域也是已知的(参见,例如,stryer,biochemie,spectrum akad.verlag,1991,item i.2.)。这些术语相应地用于整个本发明中。因此,本文给出的关于本发明的大环寡肽的特定条件也适用。
[0159]
特别地,本文使用的术语“一种或多种酸性氨基酸”旨在指选自包含asp、asn、glu和gln的组的氨基酸,本文使用的术语“一种或多种碱性氨基酸”旨在指选自包含arg、lys和his的组的氨基酸,本文使用的术语“脂肪族氨基酸”旨在指选自包含gly、ala、ser、thr、val、leu、ile、asp、asn、glu、gln、arg、lys、cys和met的组的任意氨基酸,本文使用的术语“极性氨基酸”旨在指选自包含cys、met、ser、tyr、gln、asn和trp的组的任意氨基酸。
[0160]
在优选实施方案中,根据本发明使用/施用的大环寡肽和突变的/变异的大环寡肽是这样的大环寡肽,其对应于(例如同源于)式ii的xxx1,优选对应于(例如同源于)式ii的位置20和/或29处的xxx1的氨基酸残基中的至少一个被一个或多个不同的氨基酸残基替换。同样地,根据本发明使用/施用的大环寡肽和突变的/变异的大环寡肽也可以是这样的大环寡肽,其对应于(例如同源于)氨基酸位置1、18、20、22、25和/或29,优选对应于氨基酸位置20和/或29的氨基酸残基中的至少一个被一个或多个不同的氨基酸残基替换。在本文中,“对应于”特别是指一个或多个相同的氨基酸残基和/或在一个或多个相同或相似的位置上。更具体地,“对应的”意指是同源的。例如,这种一个或多个不同的氨基酸残基可用于标记相应的突变的/变异的大环寡肽。这种一个或多个不同的氨基酸残基的非限制性实例是lys。相应的突变的/变异的大环寡肽的非限制性实例是包含(头尾相接的环化形式的)seq id no:4至7的氨基酸序列或由所述(头尾相接的环化形式的)seq id no:4至7的氨基酸序列组成的突变的/变异的大环寡肽,其中seq id no.5或7是优选的;seq id no.7是最优选的。
[0161]
在具体的方面,根据本发明使用的突变的/变异的大环寡肽是位于“第一”与“第二”cys(分别对应于“第一”和“第二”cys,如上文式i所述)之间和/或“第二”与“第三”cys(分别对应于“第二”和“第三”cys,如上文式i所述)之间的一个或多个其氨基酸残基未被替换的大环寡肽。
[0162]
优选地,在此类突变的/变异的大环寡肽中,“第二”cys侧翼的氨基酸残基,特别是在式i的n-末端方向上与“第二”cys相邻的氨基酸残基和在式i的c-末端方向上与“第二”cys相邻的氨基酸残基都不被另一个氨基酸残基替换,特别是不被lys或ala残基替换。
[0163]
优选地,所使用/施用的大环寡肽及其突变体/变体缺乏对水解或切割蛋白酶(例如血清蛋白酶)敏感的位点。术语“水解”和“(血清)蛋白酶”以及位点的结构的含义是本领域公知的。
[0164]
在优选方面,在根据本发明使用/施用的突变的/变异的大环寡肽中,特别是在本文别处更具体定义的突变的/变异的大环寡肽(例如,上文第(iv)项和第(i)至(iii)项,或
下文第(i)至(v)项中定义的突变的/变异的大环寡肽)中,(六个)cys残基均未被另一种氨基酸残基替换。
[0165]
然而,关于大环寡肽的突变体/变体,(六个)cys残基(特别是本文定义的cys)中的一个或多个,也可以被一个或多个其它氨基酸替换,只要该替换仍然导致大环寡肽内的单个分子内键联,如二硫键的键联,即导致天然大环寡肽的正确折叠/模拟。这种氨基酸除其它以外可以是非天然存在的氨基酸,如具有能够形成二硫键的-sh基团的非天然存在的氨基酸。然而,本文中优选的是,cys,特别是上面式i中给出的cys,是天然存在的氨基酸,优选为cys本身。
[0166]
本领域技术人员还将认识到,可以修饰根据本发明使用的形成大环寡肽的氨基酸中的一个或多个。据此,本文使用/定义的任何氨基酸也可以代表其修饰形式。例如,本文所用的丙氨酸残基可以包含经修饰的丙氨酸残基。此类修饰,除其它以外,可以是甲基化或酰化等,由此这种修饰或经修饰的氨基酸是优选的,只要这样修饰的氨基酸,更具体地说,含有所述这样修饰的氨基酸的大环寡肽仍然具有如本文所定义的功能活性。用于确定这种大环寡肽(即包含一个或几个经修饰的氨基酸的大环寡肽)是否满足这一要求的各个测定是本领域技术人员已知的,并且除其它以外,在本文中,尤其是在实施例部分中也有描述。
[0167]
本发明还提供了所公开的大环寡肽衍生物诸如与生理有机酸和无机酸(如hcl、h2so4、h3po4、苹果酸、富马酸、香茅酸、酒石酸、乙酸)的盐的用途。
[0168]
特别地设想了本文中定义的大环寡肽,以及本文中定义的突变型大环寡肽和变异的大环寡肽(参见,例如,上文第(iv)项或第(i)至(iii)项)具有至少一种根据本发明的所需功能,特别是一种(或多种)如下文第(i)至(v)项所述的功能。根据本发明,这种/这些功能使得大环寡肽和大环寡肽突变体/变体非常适合于治疗ms和相关疾病、缺陷和/或症状。
[0169]
根据本发明使用/施用的(即与kor的配体组合的)以及如本文中定义的大环寡肽或大环寡肽突变体/变体被设想为
[0170]
(i)能够增加(体外和/或体内)本文定义的kor的配体的偏向性因子(例如≥5%、≥10%、≥15%、≥20%、≥30%、≥50%、≥75%、≥100%、≥1.5倍、≥2倍、≥3倍或≥5倍);
[0171]
(ii)能够(在体外和/或在体内)结合和/或(在体外和/或在体内)激活本文定义的kor(例如,“激活”意指减少细胞内camp减少,或本文定义的β-抑制蛋白的募集);
[0172]
(iii)能够(在体外和/或在体内)充当本文所定义的kor的正构激动剂,例如充当具有低μm亲和力和/或低μm效力(例如在约0.5μm
–
20μm的范围内)的本文所定义的kor的正构激动剂;
[0173]
(iv)能够(在体外和/或体内)充当本文中定义的kor配体的变构调节剂(负性或优选正性变构调节剂),特别是kor的内源性配体(例如,如本文中定义的kor的内源性配体);和/或
[0174]
(v)不能诱导β-抑制蛋白2募集和/或(能够充当)本文定义的kor的偏向性配体(例如,无/减少的抑制蛋白募集,例如β-抑制蛋白2募集;kor内化较少和/或较慢或无内化;耐受性机会减少(参考阿片样物质危象);和/或无/减少的副作用(诸如阿片样物质危象/耐受性和/或烦躁不安、镇静、多尿和/或幻觉))。
[0175]
特别地,根据本发明使用/施用的(即与kor的配体组合)以及如本文所定义的大环
寡肽或大环寡肽突变体/变体被设想表现出上述(i)或(v)的功能,优选上述(i)和(v)的功能。
[0176]
现有技术中已知有可通过血脑屏障进入脑的打结蛋白的实例(例如蝎子来源的蝎氯毒素(chlorotoxin))。另外,在某些情况(例如,当存在脆弱的血脑屏障时,其可能例如与疾病(例如,某些炎症或自身免疫性疾病,如本文所定义的疾病)相关联),大环寡肽可通过血脑屏障进入脑。
[0177]
因此,根据本发明使用/施用的(即与kor的配体组合)以及如本文所定义的大环寡肽或大环寡肽突变体/变体可能能够穿透cns(例如脑或脊髓);例如除了一个或多个上述功能之外。
[0178]
另外,根据本发明使用/施用的(即与kor的配体组合)以及如本文所定义的大环寡肽或大环寡肽突变体/变体可能能够通过血脑屏障;例如除了一个或多个上述功能之外。
[0179]
然而,在本领域中认为大环寡肽通常不能(或仅在低或边缘程度上)穿过血脑屏障。
[0180]
因此,根据本发明(即与kor的配体组合)以及如本文所定义,优先使用/施用不能穿透cns(例如脑或脊髓)或通过血脑屏障的大环寡肽或大环寡肽突变体/变体。此类大环寡肽或大环寡肽突变体/变体可以根据本发明在外周发挥作用。换句话说,此类大环寡肽或大环寡肽突变体/变体可以通过外周作用发挥功能。外周作用可以是减少或抑制外周免疫细胞侵入和/或一种或多种外周免疫反应(例如,通过cd4+和/或cd8+ t细胞的cns(例如脑或脊髓)浸润)。
[0181]
本领域技术人员能够容易地测试给定的大环寡肽,如本文定义(例如,通过结构)的大环寡肽,是否表现出根据本发明的一个或多个相关特征,特别是上文第(i)、(ii)、(iii)、(iv)和/或(v)项中定义的一个或多个特征。各自的工具和方法在本领域中是已知的,并且在本文中,例如在所附的实施例中也有描述。在本说明书中,技术人员可以选择和/或优化相关条件,例如(大环寡肽和/或kor配体和/或kor)的浓度。例如,在这方面,低微摩尔范围(例如0.5至20μm)的大环寡肽浓度可能是合适的。
[0182]
能够充当kor配体的变构调节剂(负性或优选正性)的大环寡肽(参见上文第(iv)项)可以调节(降低或优选增加)(i)kor配体的效力(约)≥1.1倍、1.2倍、1.3倍、1.5倍、1.8倍、2倍、3倍、5倍、10倍、20倍或30倍;和/或(ii)kor配体的效率(约)≥5%、10%、15%、20%、25%、30%、50%、75%、100%、150%或200%。
[0183]
特别设想的是,大环寡肽充当kor配体的变构调节剂的能力并不伴随着(可测量的)抑制蛋白募集(另参见上文第(v)项)。
[0184]
能够结合和/或激活(在体外和/或在体内)本文所定义的kor的大环寡肽(见上文第(ii)项)可结合kor,其中ki在例如(约)0.5-10、1-5、2-4、2.4-3或2.7
±
0.01-0.25μm的范围内;和/或可以激活kor(例如,减少细胞内camp减少),其中ec
50
在例如(约)1-50、5-30、10-25、14-20或17
±
0.11-2.2μm的范围内。
[0185]
如果本文别处没有不同的说明,本发明的说明书中的“抑制”、“减少”、“阻断”、“压抑”或“降低”等被设想为意指初始状态(例如脱髓鞘状态,特别是少突神经胶质细胞的脱髓鞘状态,现存cns损伤(例如脑损伤),kor配体的效力和/或效率,大环寡肽的活性,kor的活性等)降低(在体外和/或在体内)例如至少10%、至少20%、至少30%、至少50%、至少80%、
至少90%、至少95%、至少99%或甚至100%(原则上,更高的百分比值是优选的)。本领域技术人员能够容易地测试“抑制”、“减少”、“阻断”、“压抑”或“降低”的各自程度(例如通过确定脱髓鞘状态,特别是少突神经胶质细胞的脱髓鞘状态、现存cns损伤(例如脑损伤)、kor配体的效力和/或功效、大环寡肽的活性等)。此外,技术人员能够容易地确定给定药物(例如本文公开的大环寡肽或kor配体)各自“抑制”、“减少”、“阻断”、“压抑”或“降低”作用/活性的ic
50
。
[0186]
同样,如果在本文另处没有不同的说明,在本发明的说明书中,“增加”、“诱导”或“改善”等特别地意指(在体外和/或在体内)初始状态(例如髓鞘(再)形成的状态,特别是少突神经胶质细胞的髓鞘(再)形成,kor配体的效力和/或功效,大环寡肽的活性,kor的活性等)增加例如至少10%、至少20%、至少30%、至少50%、至少80%、至少90%、至少95%、至少99%或至少100%(原则上较高的百分比值是优选的)。特别地,“增加”意指已经有了进一步“增加”的初始程度的活性/状态(例如髓鞘(再)形成、kor配体的效力和/或功效、大环寡肽的活性等)。特别地,“诱导”意指(基本上)没有随后被“诱导”的初始程度的活性/状态。技术人员能够容易地测试“增加”、“诱导”或“改善”的各自应程度(例如通过确定髓鞘(再)形成的状态,特别是少突神经胶质细胞的髓鞘(再)形成的状态、kor配体的效力和/或功效、大环寡肽的活性等)。此外,技术人员能够容易地确定给定药物(例如本文公开的大环寡肽或kor配体)各自“增加”、“诱导”或“改善”作用/活性的ic
50
。
[0187]
如果没有不同的说明,本发明的说明书中的“诱导”、“诱发”或“诱发的”意指从实际上为零的基线开始。“增加”/“增加的”或“增强”/“增强的”不一定是指从实际上为零的基线开始,但也可以是指从已经高于零的水平开始。例如,诱导的髓鞘再生是指当开始时根本没有髓鞘再生活性或表达时;增强/增加的髓鞘再生是指当最开始时已经有一定的髓鞘再生活性,然后该活性得到进一步增强/增加。
[0188]
技术人员能够容易地测试给定的大环寡肽或大环寡肽突变体/变体或kor配体是否能够根据本发明发挥功能,例如具有一种或多种本文所述的功能,例如上文第(i)至(iv)节中定义的一种或多种功能。为此目的,技术人员可以例如依赖于本文别处和所附实施例中描述的测定法,以及本领域中描述的(例如du同前)以及在本文别处和所附实施例中提及的相应的测定法。例如,在du(同前)中公开了测试kor的激活的测定法。特别地,在du(同前;参考其图3、图4和图5)中描述了用于测试kor激活对髓鞘再生(髓鞘再生的促进)和少突神经胶质细胞分化和髓鞘形成的刺激的作用的测定法。相应的动物模型,如小鼠模型,也是本领域已知的。这些是例如eae小鼠模型和铜宗诱导的脱髓鞘小鼠模型(另参见du,同前)。
[0189]
依靠本文所述的工具和方法以及技术人员的常识,技术人员能够例如在/从(植物)提取物中鉴定和分离合适的大环寡肽或大环寡肽突变体/变体。因此,技术人员也能够鉴定和分离可以根据本发明使用的尚未已知的大环寡肽/大环寡肽突变体/变体。还设想了根据本发明此类新鉴定/分离的大环寡肽的用途。
[0190]
这种新分离/鉴定的大环寡肽的实例是已在本发明的说明书中鉴定的“vitri”大环寡肽(分离自三色堇,参考实施例2和图2)。“vitri”大环寡肽已经通过分析性rp-hplc色谱和maldi质谱进行了表征。其肽质量约为3431.87[m/z](在图2e中标记为单同位素质量([m+h]
+
))。特别地,使用例如半制备型(关于细节,参见例如下文)和分析型(例如,250mm
×
4.6mm)kromasil c
18
柱(例如5μm,柱(例如5μm,)(其中线性梯度为例如0.1-1%min-1
的溶剂b[例如
90%(体积/体积)乙腈,0.1%(体积/体积)的于水中的tfa],流速分别为例如3ml
·
min-1
和1ml
·
min-1
),例如在dionex ultimate 3000hplc单元(thermo-fisher dionex)上通过rp-hplc纯化“vitri”大环寡肽。
[0191]
依靠相同或相似的分离/鉴定工具和方法,技术人员能够容易地鉴定和分离可根据本发明使用的(即与本文所定义的kor的配体组合)其它尚未已知的大环寡肽/大环寡肽突变体/变体。
[0192]
本发明还涉及可以通过与本文所述相同或相似的分离/鉴定工具和方法来分离/鉴定并且可以根据本发明使用的大环寡肽。这种分离/鉴定的大环寡肽的实例是本文公开的“vitri”大环寡肽。本发明还涉及这种特定的“vitri”大环寡肽及其突变体/变体。本文另处关于大环寡肽突变体/变体的描述在加以必要的修正后适用于此处。
[0193]
本发明还涉及核酸分子,其包含编码本发明的说明书中公开和/或分离/鉴定的大环寡肽的氨基酸主链/一级氨基酸序列的核苷酸序列;以及这种核酸分子的各自用途。例如,这种核酸分子可以包含如seq id no.11、12、15和16中的任一个所示的核苷酸序列,或包含在seq id no.11、12、15和16中的任一个中并且对应于成熟大环寡肽的核苷酸序列,或由于遗传密码的简并性而与其不同的核苷酸序列。
[0194]
术语“一种或多种核酸分子”、“一种或多种核酸序列”和“一种或多种核苷酸序列”的含义在本领域是公知的,且相应地用于本发明的说明书中。
[0195]
例如,当贯穿本发明使用时,这些术语是指所有形式的天然存在或重组产生的类型的核苷酸序列和/或核酸序列/分子,以及化学合成的核苷酸序列和/或核酸序列/分子。这些术语还涵盖核酸类似物和核酸衍生物,诸如锁定的dna、pna、寡核苷酸硫代磷酸酯和经取代的核糖寡核苷酸。此外,这些术语还指包含核苷酸或核苷酸类似物的任何分子。
[0196]
优选地,术语“一种或多种核酸分子”、“一种或多种核酸序列”和“一种或多种核苷酸序列”等是指脱氧核糖核酸(dna)或核糖核酸(rna)。“一种或多种核酸分子”、“一种或多种核酸序列”和“一种或多种核苷酸序列”可以通过本领域普通技术人员已知的合成化学方法,或者通过使用重组技术来制备,或者可以从天然来源分离,或者通过它们的组合来制备。dna和rna可以任选地包含非天然核苷酸,并且可以是单链或双链的。“一种或多种核酸分子”、“一种或多种核酸序列”和“一种或多种核苷酸序列”也指有义和反义dna和rna,即与dna和/或rna中特定核苷酸序列互补的核苷酸序列。
[0197]
此外,术语“一种或多种核酸分子”、“一种或多种核酸序列”和“一种或多种核苷酸序列”等可以指dna或rna或其杂交体或现有的技术中已知的其任何修饰(关于修饰的实例,参见,例如,us 5525711、us 4711955、us 5792608或ep 302175)。本发明的这些分子可以是单链或双链的、线性或环状的、天然的或合成的,并且没有任何大小限制。例如,“一种或多种核酸分子”、“一种或多种核酸序列”和/或“一种或多种核苷酸序列”可以是基因组dna、cdna、mrna、反义rna、核酶(ribozymal)或编码此类rna或嵌合体的dna(cole-strauss science 1996 273(5280)1386-9)。它们可呈现质粒或病毒dna或rna的形式。“一种或多种核酸分子”、“一种或多种核酸序列”和“一种或多种核苷酸序列”等也可以指一种或多种寡核苷酸,其中包括任何现有的技术的修饰,诸如硫代磷酸酯或肽核酸(pna)。
[0198]
本文提供的核酸分子特别适用于例如通过本文公开的相应方法产生本发明的环肽。
[0199]
本文公开和描述的核酸分子可以包含在载体中。
[0200]
所述载体可以是克隆性载体或表达载体,例如噬菌体、质粒、病毒或逆转录病毒载体。逆转录病毒载体可具有复制能力或具有复制缺陷。在后一种情况下,病毒繁殖通常只在互补的宿主/细胞中发生。本文公开的核酸分子可以连接到包含用于在宿主中繁殖的可选择标记的特定载体。通常,将质粒载体引入沉淀物,诸如磷酸钙沉淀物或氯化铷沉淀物,或与带电荷的脂质的复合物中,或碳基簇诸如富勒烯中。如果载体是病毒,在应用于宿主细胞之前,可以使用合适的包装细胞系对其进行体外包装。
[0201]
优选地,公开的核酸分子与表达控制序列(例如,在本文公开的载体内)可操作地连接,允许在原核或真核细胞或其分离的级分中表达。所述多核苷酸的表达包括核酸分子的转录,优选转录成可翻译的mrna。确保在真核细胞,优选哺乳动物细胞中表达的调控元件是本领域技术人员熟知的。它们通常包含确保转录起始的调控序列和任选地包含确保转录终止和转录物稳定的多聚腺苷酸信号。额外的调控元件可包括转录增强子以及翻译增强子。允许在原核宿主细胞中表达的可能的调控元件包括例如大肠杆菌(e.coli)中的lac、trp或tac启动子,允许在真核宿主细胞中表达的调控元件的实例是酵母中的aox1或gal1启动子或哺乳动物和其它动物细胞中的cmv-启动子、sv40-启动子、rsv-启动子(劳斯肉瘤病毒)、cmv-增强子、sv40-增强子或珠蛋白内含子。除了负责转录起始的元件之外,此类调控元件还可以包含转录终止信号,诸如多核苷酸下游的sv40-多聚腺苷酸位点或tk-多聚腺苷酸位点。在这种情况下,合适的表达载体是本领域已知的,诸如okayama-berg cdna表达载体pcdv1(pharmacia)、pcdm8、prc/cmv、pcdna1、pcdna3(invitrogen)、psport1(gibco brl)。优选地,所述载体是表达载体和/或基因转移载体。源自诸如逆转录病毒、腺病毒、痘苗病毒、腺相关病毒、疱疹病毒或牛乳头状瘤病毒等病毒的表达载体可用于将本发明的多核苷酸或载体递送到靶细胞群中。本领域技术人员熟知的方法可用于构建本发明的载体;参见,例如,sambrook,molecular cloning a laboratory manual,cold spring harbor laboratory(1989)n.y.和ausubel,current protocols in molecular biology,green publishing associates and wiley interscience,n.y.(1994)中描述的技术。或者,所公开的多核苷酸和载体可以重建成用于递送至靶细胞的脂质体。
[0202]
术语“其分离的级分”指真核或原核细胞或组织的级分,所述级分能够从载体转录rna或者转录并翻译rna。所述级分包含rna转录或者rna转录和所述rna翻译成多肽所需的蛋白质。所述分离的级分可以是例如真核细胞诸如网织红细胞的细胞核级分和细胞质级分。包含所述细胞或组织的分离级分的用于转录和翻译rna的试剂盒是商购可得的,例如作为tnt网状溶酶体(reticulolysate)(promega)购得。
[0203]
同样,与所公开的核酸分子一样,所公开的载体也特别适用于例如通过本文公开的相应方法生产本发明的环肽。
[0204]
在又一方面,本文公开了包含本文公开的核酸分子和/或载体和/或编码的大环寡肽的重组宿主细胞。在这方面的上下文中,核酸分子和/或载体除其它以外,可用于遗传工程宿主细胞,例如,以便表达和分离本文公开的大环寡肽的氨基酸主链/一级氨基酸序列。
[0205]
所述宿主细胞可以是原核或真核细胞。存在于宿主细胞中的核酸分子或载体既可以被整合到宿主细胞的基因组中,也可以保持在染色体外。
[0206]
宿主细胞可以是任何原核或真核细胞,诸如细菌细胞、昆虫细胞、真菌细胞、植物
peptide synthesis.crc-press,2005)。基于本文提供的教导,本领域技术人员能够容易地将现有技术知识应用于所公开的生产环肽的方法的特定要求。
[0217]
本发明还涉及通过根据本文提供的公开内容的一种或多种上述途径或方法可获得的或获得的大环寡肽的使用/施用。
[0218]
本发明还涉及以下的组合(产品):
[0219]
(a)如本文所定义的大环寡肽;和
[0220]
(b)如文定义的kor的配体。
[0221]
本文其它地方关于所述大环寡肽和配体的描述在加以必要的修正后适用于此处。
[0222]
根据本发明的大环寡肽和kor的配体的组合(产品)的具体但非限制性的实例选自由以下组成的组:
[0223]
(a)t20k(seq id no.7)和选自由以下组成的组的配体
[0224]
(i)纳呋拉啡、collybolide、降伊波加因碱(noribogaine)、salvinorin a衍生物b-64、三唑1.1、6-gnti、hs666、hs665和甲磺酰基salvinorin b;或
[0225]
(ii)u50,488、强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林(difelikefalin)、强啡肽、纳布啡、pentasozin、哌替啶和舒芬太尼;
[0226]
(b)n29k(seq id no.5),并且配体选自由以下组成的组
[0227]
(i)纳呋拉啡、collybolide、降伊波加因碱、salvinorin a衍生物b-64(22-硫氰酸根salvinorin a(rb-64))、三唑1.1和6-gnti、hs666、hs665和甲磺酰基salvinorin b;或
[0228]
(ii)u50,488、强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林、强啡肽、纳布啡、pentasozin、哌替啶和舒芬太尼;
[0229]
(c)g18k(seq id no.4),并且配体选自由以下组成的组
[0230]
(i)纳呋拉啡、collybolide、降伊波加因碱、salvinorin a衍生物b-64、三唑1.1、6-gnti、hs666、hs665和甲磺酰基salvinorin b;或
[0231]
(ii)u50,488、强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林、强啡肽、纳布啡、pentasozin、哌替啶和舒芬太尼;
[0232]
(d)t20k/g1k(seq id no.6),并且配体选自由以下组成的组
[0233]
(i)纳呋拉啡、collybolide、降伊波加因碱、salvinorin a衍生物b-64、三唑1.1、6-gnti、hs666、hs665和甲磺酰基salvinorin b;或
[0234]
(ii)u50,488、强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林、强啡肽、纳布啡、pentasozin、哌替啶和舒芬太尼;或
[0235]
(e)vitri大环寡肽(seq id no.155),并且配体选自由以下组成的组
[0236]
(i)纳呋拉啡、collybolide、降伊波加因碱、salvinorin a衍生物b-64、三唑1.1、6-gnti、hs666、hs665和甲磺酰基salvinorin b;
[0237]
(ii)u50,488、强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林、强啡肽、纳布啡、pentasozin、哌替
啶和舒芬太尼;或
[0238]
(f)caripe 10(seq id no.86),并且配体选自由以下组成的组
[0239]
(i)纳呋拉啡、collybolide、降伊波加因碱、salvinorin a衍生物b-64、三唑1.1、6-gnti、hs666、hs665和甲磺酰基salvinorin b;或
[0240]
(ii)u50,488、强啡肽a-(1-13)、强啡肽-(1-11)、强啡肽a、强啡肽a-(1-8)、u69593、gr 89696、螺朵林、brl-52537、jt09、地非法林、强啡肽、纳布啡、pentasozin、哌替啶和舒芬太尼。
[0241]
更具体地,然而非限制性地,根据本发明的大环寡肽和kor的配体的组合(产品)的实例选自由以下组成的组:
[0242]
(a)t20k(seq id no.7)和纳呋拉啡;
[0243]
(b)n29k(seq id no.5)和纳呋拉啡;
[0244]
(c)g18k(seq id no.4)和纳呋拉啡;
[0245]
(d)t20k/g1k(seq id no.6)和纳呋拉啡;
[0246]
(e)vitri(seq id no.155)和纳呋拉啡;
[0247]
(f)caripe 10(seq id no.86)和纳呋拉啡;
[0248]
(g)t20k(seq id no.7)和u50,488;
[0249]
(h)n29k(seq id no.5)和u50,488;
[0250]
(i)g18k(seq id no.4)和u50,488;
[0251]
(j)t20k/g1k(seq id no.6)和u50,488;
[0252]
(k)vitri(seq id no.155)和u50,488;
[0253]
(l)caripe 10(seq id no.86)和u50,488;
[0254]
(m)t20k(seq id no.7)和强啡肽a 1-13;
[0255]
(n)n29k(seq id no.5)和强啡肽a1-13;
[0256]
(o)g18k(seq id no.4)和强啡肽a1-13;
[0257]
(p)t20k/g1k(seq id no.6)和强啡肽a1-13;
[0258]
(q)vitri(seq id no.155)和强啡肽a1-13;
[0259]
(r)caripe 10(seq id no.86)和强啡肽a 1-13;(s)t20k(seq id no.7)和地非法林
[0260]
(t)n29k(seq id no.5)和地非法林
[0261]
(u)g18k(seq id no.4)和地非法林
[0262]
(v)t20k/g1k(seq id no.6)和地非法林
[0263]
(w)vitri(seq id no.155)和地非法林
[0264]
(x)caripe 10(seq id no.86)和地非法林
[0265]
(y)t20k(seq id no.7)和纳布啡;
[0266]
(z)n29k(seq id no.5)和纳布啡;
[0267]
(aa)g18k(seq id no.4)和纳布啡;
[0268]
(ab)t20k/g1k(seq id no.6)和纳布啡;
[0269]
(ac)vitri(seq id no.155)和纳布啡;
[0270]
(ad)caripe 10(seq id no.86)和纳布啡;
[0271]
(ae)t20k(seq id no.7)和pentasozin;
[0272]
(af)n29k(seq id no.5)和pentasozin;
[0273]
(ag)g18k(seq id no.4)和pentasozin;
[0274]
(ah)t20k/g1k(seq id no.6)和pentasozin;
[0275]
(ai)vitri(seq id no.155)和pentasozin;
[0276]
(aj)caripe 10(seq id no.86)和pentasozin;
[0277]
(ak)t20k(seq id no.7)和哌替啶;
[0278]
(al)n29k(seq id no.5)和哌替啶;
[0279]
(am)g18k(seq id no.4)和哌替啶;
[0280]
(an)t20k/g1k(seq id no.6)和哌替啶;
[0281]
(ao)vitri(seq id no.155)和哌替啶;
[0282]
(ap)caripe 10(seq id no.86)和哌替啶;
[0283]
(aq)t20k(seq id no.7)和舒芬太尼;
[0284]
(ar)n29k(seq id no.5)和舒芬太尼;
[0285]
(as)g18k(seq id no.4)和舒芬太尼;
[0286]
(at)t20k/g1k(seq id no.6)和舒芬太尼;
[0287]
(au)vitri(seq id no.155)和舒芬太尼;和
[0288]
(av)caripe 10(seq id no.86)和舒芬太尼。
[0289]
本发明还涉及药物组合物,其包含本发明的组合(产品)或本文所述的大环寡肽和kor配体,以及任选地包含药学上可接受的运载体(carrier)。
[0290]
本发明还涉及本文定义的大环寡肽用于以下方面的用途:
[0291]
(i)减少本文定义的kor的配体(特别是本文定义的完全(“无偏”)kor激动剂)的副作用;和/或
[0292]
(ii)增加本文定义的kor的配体(特别是本文定义的完全(“无偏”)kor激动剂)的功效和/或效力。
[0293]
本发明还涉及试剂盒/内容物试剂盒/部件试剂盒,所述试剂盒包含(以下的组合(产品))
[0294]
(a)如本文定义的大环寡肽;和
[0295]
(b)如文定义的kor的配体。
[0296]
另外,在本发明的试剂盒/内容物试剂盒/部件试剂盒的说明书中,所述
[0297]
(a)大环寡肽;和
[0298]
(b)kor的配体
[0299]
(的组合)可以(与所述试剂盒分开且独立地)用于以下中的用途:
[0300]
(i)治疗ms(例如通过疗法或预防性/防治性治疗进行治疗);
[0301]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生(即其诱导或增加),和/或改善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0302]
(iii)预防或减少脱髓鞘(特别是少突神经胶质细胞的脱髓鞘)和/或预防cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0303]
(iv)治疗(例如通过疗法治疗或预防性/防治治疗)疼痛,特别是神经性疼痛(例如
中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0304]
本发明还涉及作为本发明的试剂盒/内容物试剂盒/部分试剂盒的部分的药物组合物,
[0305]
其中
[0306]
(a)如本文所定义的大环寡肽;和
[0307]
(b)如本文所定义的kor的配体
[0308]
(的组合)或所述药物组合物,
[0309]
可以(与所述试剂盒分开且独立地)用于以下中的用途:
[0310]
(i)治疗ms(例如通过疗法或预防性/防治性治疗进行治疗);
[0311]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生(即其诱导或增加),和/或改善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0312]
(iii)预防或减少脱髓鞘(特别是少突神经胶质细胞的脱髓鞘)和/或预防cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0313]
(iv)治疗(例如通过疗法治疗或预防性/防治性治疗)疼痛,特别是神经性疼痛(例如中枢神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0314]
本发明还涉及包含药物组合物的试剂盒/内容物试剂盒/部件试剂盒,所述药物组合物包含(以下的组合(产品))
[0315]
(a)如本文所定义的大环寡肽;和
[0316]
(b)本文定义的kor的配体,
[0317]
其中所述药物组合物和/或所述
[0318]
(a)大环寡肽;和
[0319]
(b)kor的配体(的组合)
[0320]
可以(与所述试剂盒分开且独立地)用于以下的用途:
[0321]
(i)治疗ms(例如通过疗法或预防性/防治性治疗进行治疗);
[0322]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生(即其诱导或增加),和/或改善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0323]
(iii)预防或减少脱髓鞘(特别是少突神经胶质细胞的脱髓鞘)和/或预防cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0324]
(iv)治疗(例如通过疗法治疗或预防性/防治治疗)疼痛,特别是神经性疼痛(例如中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0325]
根据本发明的试剂盒/内容物试剂盒/部件试剂盒或药物组合物可用于以下的用途:
[0326]
(i)治疗ms(例如通过疗法或预防性/防治性治疗进行治疗);
[0327]
(ii)髓鞘再生(即其诱导或增加),特别是少突神经胶质细胞的髓鞘再生(即其诱导或增加),和/或改善(例如减少或治愈/愈合)cns损伤(例如脑损伤);
[0328]
(iii)预防或减少脱髓鞘,特别是少突神经胶质细胞的脱髓鞘,和/或预防cns损伤(例如脑损伤)的形成和/或减少现存cns损伤(例如脑损伤);和/或
[0329]
(iv)治疗(例如通过疗法治疗或预防性/防治治疗)疼痛,特别是神经性疼痛(例如中枢或外周神经性疼痛)和/或由ms引起/伴随ms的疼痛。
[0330]
在本发明的试剂盒/内容物试剂盒/部件试剂盒和各自的药物组合物的上下文中,以及在本文所述的一般药物组合物的上下文中,大环寡肽和kor配体或其组合可以包含在单一容器或小瓶中,或者优选包含在两个不同的容器或小瓶中。
[0331]
根据本发明,所公开的药物组合物或大环寡肽和kor配体或其组合可以以/将会以药学/治疗有效剂量施用。这意味着达到了待施用的每种化合物(活性成分)的药学/治疗有效量。优选地,药物/治疗有效剂量是指例如使受试者的疾病(的症状)产生缓解、状况产生改善和/或存活期得以延长的所施用的化合物的量。这可由本领域技术人员进行常规测试来确定。
[0332]
根据本发明施用的化合物的剂量方案将由主治医生和临床因素决定。如医学领域所公知的,任何一个患者的剂量取决于许多因素,包括患者的体型、体表面积、年龄、待施用的特定化合物、性别、施用时间和途径、总体健康状况和/或同时施用的其它药物。本领域技术人员知道并能够测试根据本发明医学应用的化合物的相关剂量。
[0333]
根据本发明,大环寡肽和/或kor配体可以例如以在10μg/kg bw至100mg/kg bw的范围内,优选在200μg/kg bw至60mg/kg bw的范围内,更优选在400μg/kg bw至40mg/kg bw的范围内,更优选在600μg/kg bw至20mg/kg bw的范围内,甚至更优选在800μg/kg bw至10mg/kg bw的范围内的剂量施用。其它优选剂量范围为最高20mg/kg bw。
[0334]
当然,剂量可以根据施用方案和/或施用途径而变化。例如,如果静脉内(i.v.)施用,剂量通常低于口服(p.o.)施用。在p.o.施用的情况,可能的剂量的非限制性实例是在10μg/kg bw至100mg/kg bw的范围内,优选在200μg/kg bw至60mg/kg bw的范围内,更优选在400μg/kg bw to 40mg/kg bw范围内的剂量。在i.v.施用的情况,可能的剂量的非限制性实例是在600μg/kg bw至20mg/kg bw的范围内,优选在800μg/kg bw至10mg/kg bw的范围内的剂量。例如,在所有三种(p.o.、i.p.和i.v.)施用的情况,高达20mg/kg bw的范围内的剂量可以是合适和安全的。
[0335]
可以每天一次、每周一次或每月一次施用根据本发明的一个剂量/多个剂量。大环寡肽和/或kor配体可以以1次或多次单剂量的形式施用;特别是以1次、2次、3次、4次或5次单剂量(例如每天、每周、每月)的形式施用。具体的但非限制性的实例是一周(最多)3次单剂量的施用。在本发明的说明书中也设想了连续施用。大环寡肽和/或kor配体可以例如腹膜内或口服施用。因此,在优选但非限制性的实施方案的情况中,大环寡肽和/或kor配体或包含它们的药物组合物通过i.v.、i.p.或口服施用,被配制用于i.p.或口服施用和/或包含用于i.p.或口服施用的药学上可接受的运载体。特定施用方案的非限制性实例是以每周一次的间隔进行3次(最多10mg/kg bw,例如在pbs中)单次腹膜内注射。具体施用方案的另一个非限制性实例是以每周一次的间隔进行3次(最多50mg/kg bw,例如在pbs中)单次口服施用。其它可能的施用方案在本文别处进行了描述。
[0336]
根据本发明使用的大环寡肽和kor配体的剂量/剂量方案可以相同或相似或不同。特别地,大环寡肽的剂量可以与kor配体的剂量相同。大环寡肽的剂量(例如如上所述的剂量)也可以高于或低于kor配体的剂量(例如如上所述的剂量)。例如,大环寡肽的剂量(例如上述剂量)可以比kor配体的剂量(例如上述剂量)高或低1.1倍、1.2倍、1.5倍、2倍或3倍。类似的剂量可以是最多相差50%、40%、30%、20%、10%、5%或3%的剂量。
[0337]
本文所述的药物组合物或组合还可包含一种或多种大环寡肽和/或一种或多种
kor配体。因此,在另外的具体实施方案中,本文所述的药物组合物或组合可以包含至少两种、三种、四种或五种大环寡肽和/或至少两种、三种、四种或五种kor配体。
[0338]
本文所述的大环寡肽和kor配体可以一起施用,即同时,但是在相同或不同的施用部位或通过相同或不同的施用途径施用,或者它们可以先后在相同或不同的施用部位或通过相同或不同的施用途径施用。在后一种情况下,可以首先施用大环寡肽,随后施用kor配体,或者可以首先施用kor配体,随后施用大环寡肽。
[0339]
在一个具体实施方案中,本文所述的药物组合物还可包含(除了一种或多种大环寡肽和一种或多种kor配体之外的)一种或多种附加活性剂。同样,本文所述的(包含以下的药物组合物/组合)一种或多种大环寡肽和一种或多种kor配体可以与一种或多种附加活性剂共同施用。本文所述的一种或多种大环寡肽和一种或多种kor配体也可以在联合治疗或联用治疗的情况例如与或不与一种或多种附加活性剂一起使用/施用。优选地,这种(这些)附加活性剂不是一种或多种“接枝物”,即不是大环寡肽的接枝形式的部分,而是独立地包含在药物组合物中。在另一个具体的实施方案中,一种或多种附加活性剂是临时和/或空间分开施用的。本文所述的(包含下述的药物组合物/组合)一种或多种大环寡肽和一种或多种kor配体可以与一种或多种附加活性剂一起施用,即在施用一种或多种附加活性剂之前、与之同时或之后施用。一种或多种附加活性剂的非限制性实例可以选自由以下组成的组:kor配体(例如https://www.guidetopharmacology.org/grac/objectdisplayforward?obj ectid=318&familyid=50&familytype=gpcr)或ms治疗剂(例如https://pubmed.ncbi.nlm.nih.gov/30315270-treatment-of-multiple-sclerosi s-success-from-bench-to-bedside/?from_term=tintore+2019&from_pos=1;tintore,nat rev neurol,15(1),2019,53-8)。
[0340]
在一个实施方案中,本发明的药物组合物可以包含(天然)提取物,特别是含有大环寡肽的(天然)植物提取物,或者呈其形式。可从中获得这种提取物的植物的非限制性实例是:白花蛇舌草、吐根苦荽(特别是radix ipecacuanhae)、来自堇菜科的植物(例如堇菜属的某一种,优选香堇菜和三色堇)、南瓜物种(葫芦科,例如西葫芦)、喷瓜属物种(ecballium species)、豆科物种(legume species)(豆科)、九节属物种(psychotria species)(茜草科(rubiaceae family;例如多脉九节(psychotria polyphlebia)、热唇草(p.poeppigiana)、恰帕斯九节(p.chiapensis)、p.borucana、p.buchtienii、p.pillosa、p.mortomiana、穗花九节(p.deflexa)、p.makrophylla、天麻九节(p.elata)、(p.solitudinum)、头序九节(p.capitata))、白泻根(bryonia alba)、苦瓜(momordica charantia)、毒毛旋花子(strophantus kombe)、向日葵(helianthus annuus)、西洋接骨木(sambuca nigra)、苋属物种(amaranthus sp.)如尾穗苋(amaranthus caudatus)、甜菜(beta vulgaris)、萝芙藤(rauwolfia serpentina)、海巴戟天(morinda citrifolia)、辣木(moringa oleifera)、白柳(salix alba)、红皮柳(salix purpurea)和木豆(cajanus cajan)。kor配体可以加入到(这种)含大环寡肽的提取物中,或者可以与(这种)含大环寡肽的提取物共同给药。
[0341]
除了它们的氨基酸主链之外,根据本发明使用的大环寡肽还可以包含或偶联(例如共价结合)一种或多种其它取代基(如标记物)、其它活性剂、锚(如蛋白质性质的膜锚)、标签(如his标签)。一种或多种取代基可以与所述大环寡肽直接或通过接头共价或非共价
地结合。一种或多种另外的取代基可以与大环寡肽偶联的一个特定位点是k残基,例如对应于(例如同源于)特定大环寡肽t20k的20k残基的k残基。技术人员能够很容易找到在这种情况下使用的合适的接头。此外,合适的取代基和将它们添加到大环寡肽的合适的方法是本领域普通技术人员已知的或可由他们建立。
[0342]
标记物的实例除其它以外,包括荧光染剂(如氟-18、荧光素、罗丹明、texas red等)、酶(如辣根过氧化物酶、β-半乳糖苷酶、碱性磷酸酶)、放射粒子/放射性同位素(如32p、33p、35s、125i或123i、135i、124i、11c、15o)、生物素、地高辛、胶体金属、化学或生物发光化合物(如二氧杂环丁烷、鲁米诺或吖啶鎓(acridiniums))。可以与大环寡肽结合的标记物的一个非限制性实例是荧光染剂,如fret荧光染剂,例如gfp、yfp或cfp变体(例如gfp、yfp、cfp、egfp、eyfp或ecfp)。多种技术可用于标记生物分子,除其它以外,包括酶或生物素基团的共价偶联、磷酸化、生物素化、随机引发、切口翻译、拖尾(使用末端转移酶)。这些技术例如描述于tijssen,"practice and theory of enzyme immunoassays",burden和von knippenburg(编辑),volume 15(1985);"basic methods in molecular biology",davis lg,dibmer md,battey elsevier(1990);mayer,(编辑)"immunochemical methods in cell and molecular biology"academic press,london(1987)中;或系列"methods in enzymology",academic press,inc.中。相应的检测方法包括但不限于放射自显影术、荧光显微镜检查、直接和间接酶促反应等。
[0343]
本文所述和定义的大环寡肽,特别是上述标记的大环寡肽,可以用于生物分布研究,即例如在动物或优选人受试者/患者中产生大环寡肽分布模式的研究。例如,此类生物分布研究可以包括通过单光子或pet成像设备进行成像。各自的工具和方法是本领域已知的(例如perkinelmer的光谱体内成像系统)。
[0344]
可与待使用/施用的大环寡肽偶联的其它(活性)剂的实例除其它以外,包括作为特异性细胞穿透肽的抗体(例如用于定向靶向细胞、组织等(例如脑)的穿梭肽)。
[0345]
在本发明的说明书中,“进行治疗”/“治疗”通常被设想为涵盖疗法和预防性/防治性治疗。疗法可能导致改善,或甚至治愈/愈合。
[0346]
根据本发明使用/施用的大环寡肽和kor配体可以包含在一种或多种药物组合物中。它们可以包含在一种且同一药物组合物中(即组合中)。它们的每一种也可以单独和独立地包含在不同的药物组合物中。另外,大环寡肽和kor配体中的每一种或两者可以作为单独的一种或多种活性成分包含在一种或多种相应的药物组合物中或与一种或多种其它活性成分一起包含在一种或多种相应的药物组合物中。
[0347]
本发明的药物组合物可以包含药学上可接受的运载体、赋形剂或稀释剂。
[0348]
运载体可以特别地是药学上可接受的运载体、赋形剂或稀释剂,所述运载体任选地包含在本发明的药物组合物中或与药物组合物或与本发明的大环寡肽和kor配体一起施用。
[0349]
此类运载体在本领域是公知的。技术人员能够容易地找到适合根据本发明使用的此类运载体。
[0350]
可用于包含本文定义的活性化合物(或其盐)的药物组合物制剂的药学上可接受的运载体/赋形剂/稀释剂通常可包含运载体、媒介物(vehicles)、稀释剂、溶剂诸如一元醇(诸如乙醇、异丙醇)和多元醇(诸如乙二醇)以及可食用油诸如大豆油、椰子油、橄榄油、红
花油、棉籽油、油性酯诸如油酸乙酯、肉豆蔻酸异丙酯;粘合剂、佐剂、增溶剂、增稠剂、稳定剂、崩解剂、助流剂、润滑剂、缓冲剂、乳化剂、湿润剂、助悬剂、甜味剂、着色剂、调味剂、包衣剂、防腐剂、抗氧化剂、加工助剂、药物递送改性剂和增强剂,诸如磷酸钙、镁状态(magnesium state)、滑石、单糖、二糖、淀粉、明胶、纤维素、甲基纤维素、羧甲基纤维素钠、葡萄糖、羟丙基-β-环糊精、聚乙烯吡咯烷酮、低熔点蜡、离子交换树脂。这些和其它合适的药学上可接受的运载体/赋形剂描述于remington's pharmaceutical sciences,第15版,mack publishing co.,new jersey(1991)中。
[0351]
根据本发明的药物组合物或一种或多种大环寡肽的施用可以通过不同的方式实现。这可以是例如经口、静脉内、动脉内、腹膜内、膀胱内、结内或皮下施用,或者通过吸入施用以及经皮肤施用。其它实例是肠胃外施用,诸如皮下施用、静脉内施用、肌内施用、腹膜内施用、结内施用、硬膜内施用、经皮肤施用、经粘膜施用、经肺施用、硬膜下施用、局域或局部施用以及通过离子电渗法施用、舌下施用、通过吸入喷雾施用或气雾剂施用或直肠施用等。
[0352]
特别地,对于患者和/或对于特定的医疗用途,可以指示特定的施用途径,如血液输注(例如静脉内输注)、直肠施用(例如以灌肠剂或栓剂的形式)或局部施用途径。
[0353]
在下文中,描述了几种非限制性施用方案和相应合适的药学上可接受的运载体的使用。
[0354]
对于通过皮下(s.c.)注射或静脉内(i.v.)注射/动脉内(i.a.)注射施用根据本发明的药物组合物或一种或多种大环寡肽和一种或多种kor配体,可在水性溶液中,优选在生理学相容的缓冲剂(诸如hank's溶液、林格氏溶液或生理盐水缓冲剂中配制一种或多种大环寡肽(或编码序列)。对于经粘膜施用和经肺施用,在制剂中使用适于透过屏障的渗透剂。此类渗透剂在本领域通常是已知的。
[0355]
使用药学上可接受的运载体将一种或多种大环寡肽和一种或多种kor配体配制成适于全身性(即静脉内/动脉内、结内或皮下)施用的剂量或药物组合物在本发明的范围内。通过适当选择运载体和适当的生产实践,本发明的组合物,特别是配制成溶液的那些,可以肠胃外施用,诸如通过静脉注射来施用。所述化合物可以使用本领域公知的药学上可接受的运载体容易地配制成适于皮下或口服施用的剂量。此类运载体使得根据本发明的化合物能够被配制成片剂、丸剂、胶囊、糖衣丸、液体、凝胶、糖浆、浆液、混悬液等,特别地用于待治疗的受试者的口服摄入。
[0356]
旨在体内/细胞内施用的根据本发明的化合物或包含它们的药物或药物组合物,可以使用本领域普通技术人员公知的技术施用。例如,可将此类药物包封到脂质体中,然后如上所述施用。脂质体是具水性内部的球形脂质双层。脂质体形成时水性溶液中存在的所有分子都被掺入到水性内部。脂质体内容物既受到保护而免受外部微环境的影响,又因为脂质体与细胞膜融合,所以被高效地递送到细胞表面附近。属于janoff等人的美国专利第4,880,635号中公开了涉及脂质体的递送系统。出版物和专利提供了脂质体药物递送技术的有用描述。
[0357]
用于肠胃外和/或皮下施用的包含本发明的化合物的药物组合物包括呈水溶性形式的一种或多种活性化合物的水性溶液。另外,可将活性化合物的混悬剂制成合适的油性注射混悬剂。合适的亲脂性溶剂或媒介物包括脂肪油(诸如芝麻油或蓖麻油)或合成脂肪酸酯(诸如油酸乙酯或甘油三酯)或脂质体。水性注射剂混悬剂可含有增强混悬剂粘度的化合
物,诸如羧甲基纤维素钠、山梨醇、葡聚糖等。任选地,所述混悬剂还可含有合适的稳定剂或增加化合物溶解度的试剂,以允许制备高浓度的溶液,并允许该物质在生物体内持续缓慢释放。
[0358]
用于本发明目的的“患者”/“受试者”,即将向其施用根据本发明的一种或多种药物组合物或一种或多种大环寡肽和一种或多种kor配体的患者/受试者和/或患有本文定义和描述的疾病或病症和/或症状的患者/受试者,包括人和动物,以及其它生物体。因此,本发明的组合物和方法适用于以下方面或与以下方面结合:人治疗和兽医应用(包括治疗和预防程序和方法)。在优选实施方案中,患者/受试者是哺乳动物,在最优选实施方案中,患者/受试者是人。
[0359]
本发明的药物组合物、活性成分、组合、试剂盒/内容物试剂盒/部件试剂盒等可以包含在医疗装置、医药产品包装或药物组合物包装中,可以是医疗装置、医药产品包装或药物组合物包装的部分,或者可以是医疗装置、医药产品包装或药物组合物包装。这种装置或包装可以例如包括或者是一个或多个小瓶/一个或多个容器、一个或多个注射器或泡罩包装。活性成分和一种或多种药物组合物可以分别独立地包含在装置或包装中(例如,在不同的小瓶/容器或注射器或泡罩中),或者可以以组合的方式(例如,在相同的小瓶/容器或注射器或泡罩中)包含它们。
[0360]
本发明还涉及生产药物组合物的方法,例如用于治疗ms和/或相关疾病和/或症状,所述方法包括将
[0361]
(i)如本文所定义的大环寡肽和/或kor配体;或
[0362]
(ii)如本文所述筛选、选择、生产、分离或鉴定的大环寡肽和/或kor配体
[0363]
与药学上可接受的运载体,例如本文别处定义的药学上可接受的运载体、赋形剂或稀释剂混合的步骤。
[0364]
用于生产药物组合物的方法可以包括将以下物质混合的步骤:
[0365]
(i)如本文所定义的大环寡肽;
[0366]
(ii)如本文所定义的kor配体;和
[0367]
(iii)药学上可接受的运载体,例如本文别处定义的药学上可接受的运载体/赋形剂/稀释剂。
[0368]
可将本发明的任何药物组合物、活性成分、组合、试剂盒等与说明书手册或说明书散页一起提供。说明书手册/说明书散页可包括指导技术人员/主治医师如何根据本发明治疗或预防本文所述的疾病、病症或症状,特别是ms和相关疾病、缺陷和/或症状的指南。特别地,说明书手册/说明书散页可包括关于本文所述的施用方式/施用方案(例如施用途径、剂量方案、施用时间、施用频率)模式的指南。原则上,本文别处关于施用方式/施用方案的描述可以包含在说明书手册/说明书散页中。
[0369]
参考以下非限制性附图和实施例进一步描述本发明。
[0370]
这些图显示:
[0371]
图1.富含半胱氨酸的植物提取物对kor的结合作用。数据显示测试浓度为300μg/ml时的结合分数。提供的数据来自两个独立的实验,每个实验以一式两份进行。通过从总结合中减去非特异性结合并以1.0(1nm[3h]-二丙诺啡)作归一化来计算特异性结合。强啡肽a1-13(10nm)用作阳性对照。红色的植物提取物显示出最明显的结合作用。
[0372]
图2.kor上的吐根苦荽和三色堇的植物提取物的受体药理学。a)通过测量吐根苦荽(300μg/ml)和对照强啡肽a 1-13(10nm)的肽富集级分对放射性[3h]-二丙诺啡(1nm)的置换来获得结合数据(n=2)。b)分离的caripe肽(10μm)和强啡肽a 1-13(10nm)(n=2)的置换结合,以及c)稳定表达kor的hek293细胞膜中caripe 10的浓度-反应曲线(n=3)。caripe 10和强啡肽a 1-13的ki值分别计算为1μm和280μm。d)三色堇的肽富集级分(300μg/ml)和阳性对照强啡肽a 1-13(10nm)对放射性标记的[3h]-二丙诺啡的置换结合(n=2)。e)分离自三色堇的vitri肽的分析rp-hplc色谱图和maldi质谱图。肽质量(3431.87)被标记为单同位素质量([m+h]
+
)。f)测试分离的vitri肽(100μg/ml)的竞争性1nm放射性配体。强啡肽a 1-13(10nm)用作阳性对照(n=2)。通过从总结合中减去非特异性结合并以1.0(分数)或100%(百分比)作归一化来计算特异性结合。1.0或100%是指每毫克膜结合约5-7皮摩尔的配体。数据显示为平均值
±
sd,浓度-反应曲线通过非线性回归来进行拟合(s形曲线,三参数,hill斜率为1)。
[0373]
图3.kor上的[t20k]-kalata b1的受体药理学。在稳定表达kor的hek293细胞膜中[t20k]-kalata b1对放射性二丙诺啡(1nm)的置换放射性配体结合(n=2)。通过从总结合中减去非特异性结合并以100%(5-7pmol/mg蛋白质)作归一化来计算特异性结合。b)稳定表达kor的hek293细胞中[t20k]-kalata b1的功能性camp分析(n=4)。在37℃用指定浓度的[t20k]-kalata b1处理细胞30分钟。将数据以在最高内源配体浓度检测到的最大激活百分比作归一化。c)在nano-荧光素酶(nluc)和于kor的c-末端引入的egfp(kor-egfp)以及β-抑制蛋白2(β-抑制蛋白2-nluc)之间监测bret。在加入荧光素酶底物(furimazine(呋喃西林))后5分钟,用强啡肽a 1-13(10μm)和t20k(10和100μm)刺激共表达kor-egfp和β-抑制蛋白2-nluc的hek293细胞。结果显示为在激动剂存在和不存在的情况下bret信号的差异,并以平均值
±
sd表示(n=3)。d)强啡肽a1-13和t20k的浓度反应应曲线(n=3)。将配体孵育5分钟,然后进行生物发光的终点测量。如下计算配体促进的bret:(排放egfp配体/排放nluc配体)-(排放egfp hbss/排放nluc hbss)。将数据以强啡肽1-13的最大激活作归一化。数据显示为平均值
±
sd,并通过非线性回归拟合(s形曲线,三个参数,hill斜率为1)。
[0374]
图4.[t20k]-kalata b1充当为kor的变构调节剂。a)通过共孵育不同浓度的[t20k]-kalata b1和强啡肽a1-13置换放射性二丙诺啡(1nm)的放射性配体结合或b)稳定表达kor的hek293细胞膜中的u50,488(n=2)。通过从总结合中减去非特异性结合并以100%(5-7pmol/mg蛋白质)作归一化来计算特异性结合。c)[t20k]-kalata b1与强啡肽a 1-13的组合的功能性camp测定或d)稳定表达kor的hek293细胞中的u50,488(n=5)。将细胞与[t20k]-kalata b1在37℃孵育30分钟,然后将强啡肽a 1-13或u50,488在37℃再孵育30分钟。将数据以在最高内源配体浓度检测到的最大激活百分比作归一化。e)在nano-荧光素酶(nluc)和在kor的c-末端引入的egfp(kor-egfp)以及β-抑制蛋白2(β-抑制蛋白2-nluc)之间监测bret。在加入荧光素酶底物(呋喃西林)后5分钟,用u50,488(10μm)和t20k(10μm)刺激共表达kor-egfp和β-抑制蛋白2-nluc的hek293细胞。结果显示为在激动剂存在和不存在的情况下bret信号的差异,并以平均值
±
sd表示(n=3)。f)u50,488和t20k的浓度反应曲线(n=4)。将配体孵育5分钟,然后进行生物发光的终点测量。如下计算配体促进的bret:(排放egfp配体/排放nluc配体)-(排放egfp hbss/排放nluc hbss)。将数据以u50,488的最大激活作归一化。数据显示为平均值
±
sd,并通过非线性回归拟合(s形曲线,三个参数,
hill斜率为1)。
[0375]
图5.vivotag标记的[t20k]-kalata b1的生物分布。将[t20k-vivotag]-kb1(5mg/kg)i.p.注射到eae小鼠中。通过使用ivis,以指定的疾病评分(0.5和1.75)监测标记肽的生物分布。注射后4h扫描器官的荧光强度a)[t20k-vivotag]-kb1和b)伊文思蓝染料在脑中以及c)、d)在脊柱中累积。e)[t20k-vivotag]-kb1和f)伊文思蓝染料的定量使用ivis活体成像软件进行。
[0376]
图6.大环寡肽的序列多样性。在a)白花蛇舌草,b)吐根苦荽和c)三色堇中鉴定的大环寡肽构成了发现新型kor配体作为ms的潜在治疗的不断增长的利基。使用可在http://www.cybase.org.au/上获得的工具生成了序列比对和序列多样性轮。
[0377]
图7.大环寡肽的合成。使用fmoc化学将大环寡肽组装为线性前体,并使用天然化学连接进行环化。(1)以含有二-fmoc-3,4-二氨基苯甲酸(dbz)作为接头的dawson树脂为起点。(2)使用微波辅助的fmoc合成进行偶联(星号标记第一个氨基酸;最后一个氨基酸是boc保护的半胱氨酸)。(3)酰化和活化树脂结合的dbz-前体,以产生n-酰基脲肽(nbz-肽)。(4)在一个步骤中对nbz-肽进行完全去保护和树脂开裂(ar,芳基)。肽环化(5a)通过硫酯化,(5b)s,n-分子内酰基位移和天然化学连接,以及(5c)氧化折叠以产生具有天然折叠的大环寡肽。显示了大环寡肽(kalata b1,pdb id代码1nb1)的条带表示和[t20k]kalata b1的序列。显示了半胱氨酸、二硫键(黄色)和半胱氨酸间环。
[0378]
在本说明书中,引用了包括专利申请在内的许多文献。尽管这些文件的公开内容被认为与本发明的专利性无关,但据此将其以其整体并入。更具体地说,所有参考文献均通过引用并入,其程度就如同每个单独的文献都被具体地和单独地指明以引用的方式并入一样。
[0379]
现在将参考下面的实施例来描述本发明,所述实施例仅仅是说明性的,并且不被解释为对本发明范围的限制。
[0380]
实施例1:材料和方法
[0381]
植物提取
[0382]
植物材料购自alfred galke gmbh(bad grund,germany),在25℃于永久搅拌的条件用甲醇和二氯甲烷的1:1(体积/体积)混合物提取过夜。在滤纸上过滤后,加入0.5体积的水,并蒸发水性相,直至甲醇浓度低于10%。将提取物进一步施加到c
18
硅胶柱(40-63μm,zeoprep60;zeochem)上。用100%溶剂b[90%(体积/体积)乙腈,0.1%(体积/体积)的tfa水溶液]洗涤并用100%溶剂a[100%(体积/体积)的水,0.1%(体积/体积)的tfa]平衡后,收集20%与80%溶剂b之间的级分。然后将提取物冷冻干燥并于-20℃储存,以备进一步使用。
[0383]
rp-hplc分级分离和肽分离
[0384]
将粗提取物或级分溶解在5%溶剂b中,并装载到用5%溶剂平衡的制备型(10μm,250mm
×
21.2mm;phenomenex jupiter)或半准备型(5μm,250mm
×
10mm;kromasil)rp c
18
硅胶柱上。b.使用5-80%的溶剂b梯度,以8ml min-1
(制备规模)或3ml min-1
(半制备规模)的流速在perkin elmer series 200系统上进行制备型分级分离。分别记录214nm和280nm处的紫外吸光度,用于分析和制备目的。使用半制备型(见上文)和分析型(250mm
×
4.6mm)kromasil c
18
柱(5μm,),利用0.1-1%min-1
溶剂b[90%(体积/体积)乙腈,0.1%(vol/vol)tfa水溶液]线性梯度,分别以3ml
·
min-1
和1ml
·
min-1
的流速在
dionex ultimate 3000hplc单元(thermo-fisher dionex)上通过rp-hplc纯化caripe和vitri肽。
[0385]
maldi ms和串联ms分析以及肽鉴定
[0386]
在maldi-tof/tof 4800分析仪(ab sciex)上进行粗提物和所有级分的分析,该分析仪以反射器正模式操作,并在激光强度设定为3,500-4,000(任意单位)的情况下每光谱获得2,000-5,000次总发射。ms和串联ms实验使用在50%(体积/体积)乙腈中的10mg-ml-1
α-氰基羟基肉桂酸作为基质来进行。将每个样品的等分试样(0.5μl)与3μl基质混合,然后点在板上。使用4800分析仪软件(ab sciex)获得并处理光谱。然后通过数据库搜索或通过借助dataexplorer软件(ab sciex)的手工测序来鉴定大环寡肽。
[0387]
酶促消化和肽测序
[0388]
为了减少粗提取物中的所有半胱氨酸残基,将新鲜制备的0.2m dtt(2μl;sigma aldrich)添加到样品等分试样(20μl)中,并在60℃于黑暗中孵育30分钟。为了烷基化每个还原的样品,加入新鲜制备的0.5m碘乙酰胺(4μl;sigma aldrich)并在25℃孵育10分钟。如果进行消化,然后在无进一步纯化步骤的情况下,通过加入2μl的0.5μg.μl-1
内切蛋白酶glu-c(sigma aldrich)或0.1μg.μl-1
胰蛋白酶(sigma aldrich)并在37℃孵育3小时来将还原和烷基化的样品进行酶促消化。通过加入稀释的tfa(1μl)终止反应。在ms分析之前,使用c
18 ziptips(millipore)对样品进行脱盐处理,并于4℃储存。
[0389]
克隆、细胞培养、转染和膜制备
[0390]
使用bamhi和hindlll限制性位点将kor序列插入到pegfp-n1质粒(clontech)中(以产生c末端gfp融合蛋白)。用于hek293细胞的增殖和稳定转染细胞系的产生的条件与先前描述的(hicks,j neuroendocrinol 24(7),2012,1012-29)相似。收获细胞,如前所述(hicks,同前)制备膜。
[0391]
放射性配体结合测定
[0392]
将来自稳定表达小鼠kor的hek293细胞的膜(每次测定5-10μg)在终体积为300μl的含有50mm tris hcl、5mm mgcl2、0.1%(重量/体积)bsa(ph 7.4)、竞争性配体和[3h]-二丙诺啡(对于竞争性结合为1nm)的溶液中孵育。[3h]-二丙诺啡购自perkinelmer life sciences。在37℃进行60分钟后,通过在玻璃纤维过滤垫[skatron filtermat 11731(molecular devices,sunnyvale,ca)])上快速过滤来终止反应。在10μm纳洛酮(sigma aldrich)存在下测定非特异性结合。特异性结合代表总结合与非特异性结合之间的差异,并以经归一化的数据表示。通过使用levenberg-marquardt算法将数据拟合到三参数逻辑方程(hill方程),获得ic
50
值和hill系数。
[0393]
功能性camp测定
[0394]
使用cisbio camp gi试剂盒(62am9pec)在稳定表达kor的hek293细胞中测量细胞camp水平。以800rpm离心细胞,吸出上清液,并将细胞沉淀重悬于含有0.5mm ibmx的1x刺激缓冲液中。将2000个细胞/孔接种到白色384孔板中,然后按照指示用稀释在1x刺激缓冲液中的配体处理,随后在37℃孵育30分钟。通过依次加入5μl/孔穴状化合物标记的camp和5μl/孔抗camp d2缀合物终止刺激,每种都在裂解检测缓冲液中稀释(1:20)。在室温下孵育1小时后,使用flexstation 3(molecular devices,san jose,usa)以100μs的滞后时间和300μs的积分时间测量时间分辨荧光能量转移(tr-fret)。在graphpad prism 5.0
(graphpad software,la jolla,ca)中绘制所得的620/665nm荧光比值。
[0395]
β抑制蛋白募集测定
[0396]
通过实时测量β-抑制蛋白-荧光素酶与egfp标记的kor之间的生物发光共振能量转移(bret)来测量受体刺激时β-抑制蛋白2的募集。以1:10的比率用β-抑制蛋白2-nluc(由kevin pfleger在有限使用标签许可(nanoluc,promega,madison,usa)下作为礼物获得的)和kor-egfp编码质粒共转染细胞。转染后6小时,将细胞在含有10%胎牛血清的不含酚红的dmem中以50,000个细胞/孔转移到白色、透明底部的96孔板中。第二天,将细胞在无酚dmem中血清饥饿1小时。在监测前5分钟,将在hank’s平衡盐溶液中以1:50稀释的呋喃西林(promega,madison,usa)以1:1的比例加入到细胞中。在flexstation 3(molecular devices,san jose,usa)上在460nm(nluc)和510nm(egfp)处测量光发射。建立基线5分钟后,加入稀释在hbss中的配体,测量反应35分钟。如下计算配体诱导的bret信号:(发射egf
配体
/发射nluc
配体
)-(发射egfp
hbss
/发射nluc
hbss
)。在加入不同浓度的配体后5分钟,由bret信号生成kor上的浓度-反应曲线。[t20k]-kalata b1和u50,488在kor上的变构调节通过在37℃共孵育5分钟来测量。
[0397]
肽缀合
[0398]
类似于先前所述(thell,同前)进行肽缀合。将[t20k]-kalata b1溶解在0.1m nahco3缓冲液(ph 8.5)中。在无水dmso中制备20倍摩尔过量的vivotag 680xl(perkinelmer),使反应在25℃进行4小时。用0.1%tfa终止反应。使用dichrom kromasil c
18
柱(250
×
10mm,5μm)和线性梯度5-80%溶剂b[双蒸h2o/ch3cn/tfa,10/90/0.1%(体积/体积/体积),溶剂a为0.1%tfa水性溶液],通过半制备型hplc从过量试剂中纯化标记的肽,通过maldi-tof质谱在负反射器模式下分析hplc级分。基于分析型hplc和a
280 uv迹线中vivotag标记的检测,肽样品的纯度被确定为≥5%。
[0399]
eae和体内成像
[0400]
在第0天用75μl等量的mog(mog
35-55
,1mg/ml;charite berlin)和补充有10mg/ml结核分枝杆菌(mycobacterium tuberculosis)h37ra(difco)的不完全弗氏佐剂(sigma-aldrich)s.c.注射到左右胁腹来免疫c57bl/6小鼠。另外,小鼠接受i.p.注射在第0天和第2天,将200ng百日咳毒素(millipore)溶解在100μl pbs中。在第0天按照最近在(thell,同前)描述的方案免疫c57bl/6小鼠。eae的进展分为五个临床阶段:0分,无体征;1分,完全尾部麻痹;2分,部分下肢瘫痪;3分,重度下肢瘫痪;4分,四肢轻瘫;5分,濒死状态。当小鼠符合排除标准(得分》4,体重减轻》20%,不摄入水和食物,不梳理毛发)时,则认为其濒临死亡。根据伦理准则,通过用氯胺酮深度麻醉小鼠达到3-4分来对其实施安乐死。在疾病阶段0.5和1.75,i.p.注射缀合的[t20k]-kalata b1(5mg
·
kg-1
)。注射后4小时收获器官,通过ivis监测信号反应。
[0401]
实施例2:从吐根苦荽和三色堇中分离的大环寡肽是kor的配体。
[0402]
kor最近成为开发多发性硬化的髓鞘再生疗法的有吸引力的靶标以及开发更安全和更有效的镇痛药的替代方案(du,同前;mei,2014,同前;che,cell 172(1-2),2018,55-67e15)。用植物文库进行的结合筛选努力鉴定了几种含有与kor结合的富含半胱氨酸的肽的植物提取物(图1)。在这些植物中,来自psychotria solitudinum、三色堇、吐根苦荽、香堇菜、苦瓜和甜菜的植物提取物显示出最显著的结合作用。考虑到它们对kor的亲和力,试
图鉴定这些提取物中存在的富含半胱氨酸的肽。它是从吐根苦荽(吐根)开始的,因为以前已经从这种植物中分离出了几种富含半胱氨酸的肽,即所谓的大环寡肽。首先将吐根提取物进行基于hplc的纯化,以从肽中分离生物碱(例如吐根碱、吐根酚碱)。然后在放射性配体结合测定中分析富含肽的级分,事实上,它们显示出与kor结合的能力(图2a)。随后,在放射性配体结合中测定先前从吐根根提取物中分离的六种大环寡肽(fahradpour,同前)。有趣的是,所有六种大环寡肽都能够与kor结合(图2b)。然后用caripe 10生成浓度-反应曲线。当与强啡肽a1-13—内源性kor肽配体相比时,caripe 10以浓度依赖性方式置换了氚化的二丙诺啡,其中ki为1μm(图2c)。由于来自吐根提取物的大环寡肽作为kor的配体,将来自三色堇的富含大环寡肽的植物提取物进一步进行生物活性导向的分级分离。富含肽的级分表现出对kor的亲和力,其中级分9是最有活性的级分(图2d)。该富含肽的级分被进一步纯化以分离负责结合亲和力的大环寡肽。有趣的是,从最有活性的级分中分离新型大环寡肽并对其进行测序(图2e),随后证明了这种新型vitri大环寡肽能够与kor结合(图2f)。总的来说,这些数据提供了从吐根苦荽和三色堇中分离的大环寡肽以低μm范围的亲和力与kor结合的证据。
[0403]
实施例3:[t20k]-kalata b1结合并激活kor
[0404]
从吐根苦荽和三色堇中分离的大环寡肽结合kor的能力,促使我们在放射性配体结合和功能研究中对[t20k]-kalata b1进行药理学表征。结合和功能数据揭示[t20k]-kalata b1结合并激活kor,其中分别地以ki为2.7μm,ec
50
为17μm(图3a和图3b)。强啡肽a1-13用作阳性对照,显著ki值为280pm,ec
50
为14nm。kor在整个中枢神经系统(cns)中广泛表达。kor的选择性激活在动物模型中产生抗伤害感受,而无身体依赖性或呼吸衰竭的风险。然而,值得注意的是,除了止痛效果之外,kor激活还已被证明具有不期望的副作用,包括烦躁不安和镇静(darcq,nat rev neurosci 19(8),2018,499-514)。这些副作用可能会抑制kor激动剂在治疗脱髓鞘疾病中的治疗潜力。有趣的是,β抑制蛋白(调节gpcr信号传导的细胞溶胶蛋白)与阿片样物质受体激活相关联的副作用的发生相关(darcq,同前)。因此,开始在基于bret的测定中检测[t20k]-kalata b1诱导β抑制蛋白募集的能力。因此,当[t20k]-kalata b1与瞬时共表达nanoluc-β-抑制蛋白2和egfp-kor的hek293细胞一起孵育时,未检测到β抑制蛋白的募集(图3c和图3d)。相比之下,强啡肽a1-13能够以183nm的ec
50
募集β抑制蛋白。这些数据表明[t20k]-kalata b1是kor的完全激动剂,并且不太可能产生中枢介导的kor副作用。
[0405]
实施例4:[t20k]-kalata b1是kor的变构调节剂
[0406]
在过去的几年中,变构调节的概念在gpcr领域获得了科学动力(conn,nat rev drug discov 8(1),2009,41-54]。几种与不同于正构位点的受体位点结合的变构调节剂已被鉴定为治疗cns病症的新方法(conn,同前)。作为潜在的治疗剂,具有变构作用模式的化合物可以显示出多种优于正构配体的理论优势。例如,不显示任何激动作用的变构调节剂在缺乏内源性正构活性(orthosteric activity)时是静止的,并且仅在释放的正构激动剂存在时发挥它们的作用(conn,同前)。因此,此类变构调节剂具有维持活性依赖性以及内源性生理信号传导的时间和空间方面的潜力。变构配体的第二个潜在优势是更大的受体选择性,这归因于相对于保守的正构结构域,受体亚型之间变构位点的序列差异更大,或者归因于在给定亚型上排斥其它亚型的选择性协同效应(conn,同前)。或者,可以通过在同一分子
内结合正构和变构药效团来产生选择性,从而产生一类新型“双位”gpcr配体(conn,同前;valant,annu rev pharmacol toxicol 52,2012,153-78)。因此,使用放射性配体和功能测定,试图研究[t20k]-kalata b1在kor上的变构效应。放射性配体结合研究在稳定表达kor的hek293细胞中进行,并将不同浓度的[t20k]-kalata b1与强啡肽a 1-13或u50,488(一种选择性kor激动剂)共孵育。在本文中,揭示了[t20k]-kalata b1负调节氚化二丙诺啡,并且仅轻微影响内源性强啡肽a 1-13的亲和力(图4a,表1)。当将[t20k]-kalata b1与u50,488共孵育时,激发了类似的作用(图3b,表2)。令人惊讶的是,当通过测量细胞camp水平进行功能研究时,观察到[t20k]-kalata b1不影响强啡肽a 1-13的功效,而是导致其功效增强(图4c,表1)。然而,与u50,488的共孵育导致了反向变构效应,即[t20k]-kalata b1诱导了9倍的功效左移,并且其仅轻微影响了正构配体的功效(图4d,表2)。这一观察结果与kor上的变构相互作用的探针依赖性的经典例子相一致。显然,变构调节的方向和/或幅度的变化很大程度上取决于正构探针配体的性质。鉴于u50,488能够诱导β抑制蛋白募集,将[t20k]-kalata b1进一步与u50,488共孵育,以检查[t20k]-kalata b1是否对u50,488募集β抑制蛋白的能力有影响。事实上,kor与[t20k]-kalata b1的共刺激导致u50,488的功效显著减弱,从而不影响其效力(图4e和图4f,表2)。
[0407]
这些数据表明[t20k]-kalata b1不仅是kor上的正构配体,而且还充当能够以变构方式与kor结合的双位配体。因此,[t20k]-kalata b1在kor上的变构调节现象可能在ms的治疗中发挥额外的有益作用。
[0408]
实施例5:在ms的eae模型中,[t20k]-kalata b1在脑中累积
[0409]
为了考虑将[t20k]-kalata b1和kor作为治疗ms的候选物,必须探究[t20k]-kalata b1穿过血脑屏障(bbb)的能力。为此,使用了最先进的ms体内模型-鼠eae测定。注射前,[t20k]-kalata b1与vivotag 680xl荧光染料缀合,然后如前所述(thell,同前)进行基于hplc的纯化。一旦小鼠出现疾病,在不同的疾病阶段(0.5和1.75)腹膜内注射缀合的[t20k]-kalata b1,并在注射后4小时收获器官,使用ivis监测生物分布。标记的大环寡肽在脑中积累,并且也在脊柱中积累,但程度要小得多(图5a、图5c和图5d)。伊文思蓝(evans blue)染料用作阳性对照,其在脑和脊柱中显示强信号(图5b,图5e,图5f)。
[0410]
最后,这些数据证实了[t20k]-kalata b1在eae模型中穿透cns的能力,从而使得[t20k]-kalata b1明显适合于对与u50,488组合的ms治疗的进一步研究。
[0411]
实施例6:[t20k]-kalata b1联合u50,488/强啡肽a 1-13对eae小鼠的离体/体内治疗导致髓鞘再生增加/脱髓鞘减少以及eae临床评分增加
[0412]
kor被鉴定为促进少突神经胶质细胞分化和髓鞘形成的有希望的靶标。少突神经胶质细胞是形成髓鞘的cns的支持神经胶质细胞之一。髓磷脂是cns的必要组分,并且支持电传导和对潜在轴突(underlying axon)的代谢支持。在神经变性疾患诸如多发性硬化(ms)中,髓鞘被破坏。成人脑包含一群干细胞样少突神经胶质祖细胞(opc),它们可以分化成新的少突神经胶质细胞,然后使暴露的轴突重新髓鞘化,从而显示内源性修复过程。
[0413]
kor激动剂纳呋拉啡和u50,488在体外和体内都显示出活性(denny,同前;du同前)。因此,设计了一项研究,该研究使得能够比较例如t20k与这些配体对opc分化和髓鞘再生的促进作用以及它们组合的改进效果。
[0414]
1.离体研究方案:
[0415]
解剖大鼠新生脑,并取出小脑和脑膜。通过酶消化解离脑1小时,之后通过向细胞中加入培养基(dulbecco改良eagle培养基,dmem)、10%胎牛血清(fbs)、1%青霉素-链霉素(pen/strep)来停止消化。离心解离的细胞,并去除上清液。通过用18规针和23规针研磨,将细胞悬浮在培养基中,并以每烧瓶大约1.5个皮层加入到t75烧瓶中。将细胞培养10天,每2-3天更换一次培养基。在第10天,通过以250rpm摇动烧瓶1小时除去松散粘附的小神经胶质细胞。然后向烧瓶中补充培养基,并以230rpm摇动过夜18.20小时。
[0416]
第二天,从每个烧瓶中取出含有opc的培养基。将收集的细胞铺在未经处理的tc皮氏培养皿上20分钟,以通过它们的差异粘附去除任何污染的星形胶质细胞。将剩余的纯化opc离心,计数,并将其在sato培养基(dmem、5ml 100x sato、5ml pen/strep、5ml胰岛素、转铁蛋白、亚硒酸盐(its)补充剂)中以每孔7,000个细胞铺在多聚-d-赖氨酸包被的96孔板中,所述培养基含有10ng/ml生长因子pdgfaa和fgf(第0天)。在开始测定之前,将opc在培养物中保持48小时。
[0417]
第2天,除去培养基并加入新鲜培养基(含有测试物质(t20k和/或u50,488和/或纳呋拉啡)或合适的参考物质(例如t3,3,3
′
,5
‑‑
三碘-l-甲状腺素)。优化这些物质的孵育时间段。最初的方案建议孵育72小时,但由于细胞毒性,这可能导致不确定的结果(因为这些原代神经元细胞对异生素(xenobiotika)诸如t20k非常敏感)。因此,针对更短的时间段(例如30分钟、1小时、4小时、8小时或24小时)对孵育方案进行了优化。随后,用pfa(4%,10分钟)固定细胞,并施用针对olig2(诸如merck;mabn50)、ng2(merck;ab5320)和mbp(biorad;mca409s)的抗体。使用合适的高内涵成像系统对平板进行成像,并进行细胞计数,定量对每种标志物呈阳性的细胞数。定期拍摄低功率相位对比图像,以突出培养过程中观察到的形态学变化。免疫染色后,将孔在10x放大倍数成像。使用自动图像分析处理图像,以计算细胞计数。对每个孔的五个视野进行成像,并对对每种标志物呈阳性的细胞进行计数。评估不同浓度的测试和参考化合物;用3次技术重复培养处理,并且对从多只大鼠幼鼠汇集的细胞独立进行实验至少3次(n=3)。
[0418]
该研究被设计来定量t20k单独使用以及与已知kor激动剂组合使用的髓鞘再生作用。为此,计算每种条件下呈mbp阳性的少突神经胶质细胞的百分比,以揭示对分化的任何影响。mbp阳性少突神经胶质细胞的增加表明了这种作用。olig2是未分化opc的标志物,ng2是在许多不同细胞类型的质膜中发现的整合膜蛋白聚糖,其提供了细胞的整体细胞活力状态。
[0419]
2.体内研究方案:
[0420]
在多发性硬化的eae小鼠模型中测定了t20k与kor激动剂的组合的体内髓鞘再生活性。诱导eae,并按照先前建立的方法(thell等人)治疗小鼠。与对照处理相比,髓鞘形成的程度通过组织学来进行。分离小鼠的脊髓,于4%缓冲福尔马林中固定,并进行组织学评价。使用标准方案用h&e和lfb对切片进行染色。此外,使用利用大鼠抗cd3(例如abd serotech)和山羊抗大鼠(例如vector laboratories)抗体的免疫组织化学分析切片的cd3表面表达。对每只动物的至少三个横截面进行组织学评估。如下计算炎症指数:将脊髓横截面中血管周围浸润的数量除以每只动物使用的横截面数量。因此,炎症指数越高,表明炎症浸润越多。为了评估脱髓鞘面积的程度,在klb染色中测量每个横截面的总面积和脱髓鞘面积。然后计算脱髓鞘面积,并以占总横截面的百分比作图。例如,图像j用于所有的组织学评
估。
[0421]
另外,还确定了t细胞从外周渗入cns的程度,因为外周t细胞上的kor活化被认为对其cns髓鞘再生活性很重要(参考新西兰论文)。通过用5ml胶原酶d(0.233u/mg;roche)和dna酶i(roche)(每个器官0.17u/ml胶原酶d和0.01mg/ml dna酶i)的混合物消化适当动物的脑来从cns分离免疫细胞。将脑在37℃的摇动培养箱中孵育30分钟。为了进一步破碎组织,加入edta(ph 8.0,于pbs中)使终浓度为2mm,在通过70μm细胞过滤器过滤之前,在23℃用移液管上下吸取悬浮液5分钟。在重悬于rpmi培养基之前,在4℃以400
×
g用pbs洗涤细胞8分钟。将细胞用于facs分析,或以3
×
106/ml的浓度接种,并用30μg/ml的mog离体刺激。使用elisa将受刺激的细胞的上清液用于检测细胞因子分泌(关于详细内容,请参考thell等人)。
[0422]
与eae诱导的对照治疗的小鼠相比,用t20k结合kor激动剂治疗eae患病小鼠预期导致较低的炎症指数和减少的轴突脱髓鞘面积。另外,来自受治疗小鼠脑的cd3-阳性细胞、cd4-阳性细胞或cd8-阳性细胞的定量预期会导致cns中cd3+细胞、cd4+细胞的数量减少,并且预期在脊髓细胞中cd3减少。
[0423]
本发明涉及下列表格:
[0424]
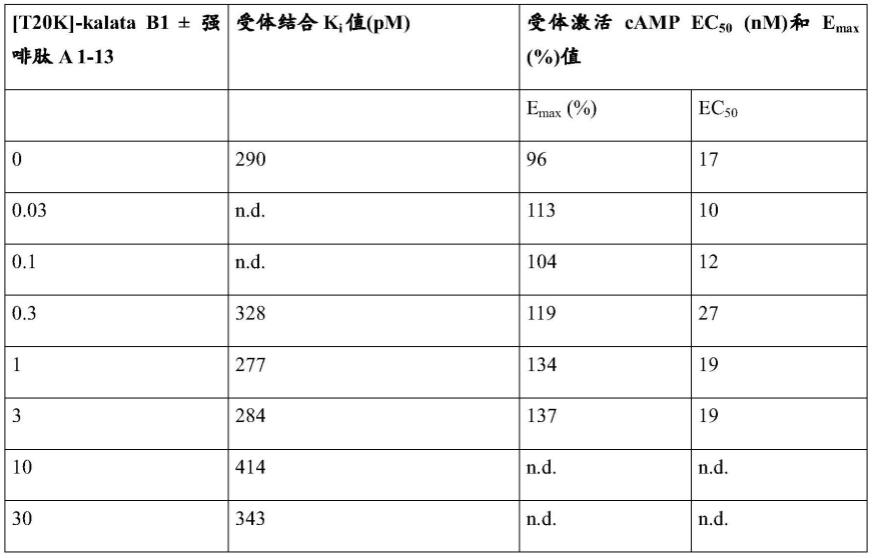
表1:在强啡肽a 1-13存在或不存在的情况[t20k]的结合和功能数据
[0425][0426]
表2:在u50,488存在或不存在的情况[t20k]的结合和功能数据
[0427][0428]
表3:kalata型大环寡肽
[0429]
[0430]
[0431][0432]
表4:caripe型大环寡肽
[0433][0434]
表5:堇菜型大环寡肽
[0435]
[0436]
[0437]
[0438]
[0439]
[0440][0441]
表6:kor的配体/激动剂
[0442]
[0443]
[0444]
[0445][0446]
本发明涉及下列核苷酸和氨基酸序列:
[0447]
本发明涉及下列核苷酸和氨基酸序列:
[0448]
seq id no.1:
[0449]
kalata b1的氨基酸序列:
[0450]
glpvcgetcvggtcntpgctcswpvctrn
[0451]
seq id no.2:
[0452]
kalata b2的氨基酸序列:
[0453]
glpvcgetcfggtcntpgcsctwpictrd
[0454]
seq id no.3:
[0455]
d-kalata b2的参考氨基酸序列:
[0456]
all-dglpvcgetcfggtcntpgcsctwpictrd
[0457]
seq id no.4:
[0458]
kalata g18k的氨基酸序列:
[0459]
glpvcgetcvggtcntpkctcswpvctrn
[0460]
seq id no.5:
[0461]
kalata n29k的氨基酸序列:
[0462]
glpvcgetcvggtcntpgctcswpvctrk
[0463]
seq id no.6:
[0464]
kalata t20k,g1k的氨基酸序列:
[0465]
klpvcgetcvggtcntpgckcswpvctrn
[0466]
seq id no.7:
[0467]
kalata t20k的氨基酸序列:
[0468]
glpvcgetcvggtcntpgckcswpvctrn
[0469]
seq id no.8:
[0470]
t8k的氨基酸序列:
[0471]
glpvcgekcvggtcntpgctcswpvctrn
[0472]
seq id no.9:
[0473]
v10a的氨基酸序列:
[0474]
glpvcgetcaggtcntpgctcswpvctrn
[0475]
seq id no.10:
[0476]
kalata v10k的氨基酸序列:
[0477]
glpvcgetckggtcntpgctcswpvctrn
[0478]
seq id no.11:
[0479]
编码kalata b1的核苷酸序列:
[0480]
ggacttccagtatgcggtgagacttgtgttgggggaacttgcaacactccaggctgcacttgctcctggcctgtttgcacacgcaat
[0481]
seq id no.12:
[0482]
编码kalata b2的核苷酸序列:
[0483]
ggtcttccagtatgcggcgagacttgctttgggggaacttgcaacactccaggctgctcttgcacctggcctatctgcacacgcgatseq id no.13:
[0484]
kalata b1前体蛋白的氨基酸序列。成熟kalata b1结构域用下划线标出。
[0485]
p56254,kalata-b1,白花蛇舌草
[0486][0487]
seq id no.14:
[0488]
kalata b2前体蛋白的氨基酸序列。三个成熟kalata b2结构域用下划线标出。
[0489]
p58454,kalata-b2,白花蛇舌草
[0490][0491]
seq id no.15:
[0492]
编码kalata b1前体蛋白的核苷酸序列。对应于成熟kalata b1结构域的核苷酸序列用下划线标出。
[0493]
》gi|15667740|gb|af393825.1|白花蛇舌草kalata b1前体,mrna,完整cds
[0494]
xxx
10-xxx
11-ala-xxx
12-xxx
13-xxx
14-cys-xxx
15-cys-xxx
16-xxx
17-xxx
18-xxx
19-cys-tyr-xxx
20-xxx
21
[0505]
seq id no.19:
[0506]
活性大环寡肽,特别是堇菜型大环寡肽的共有氨基酸序列(xxx1至xxx
20
中的任一个或全部可以是任意氨基酸、非天然氨基酸或肽模拟物;优选地,xxx1至xxx
20
中的任一个或全部可以是seq id no.155中所示的“vitri”大环寡肽的一个或多个对应氨基酸残基的一个或多个保守氨基酸交换。):
[0507]
gly-xxx
1-xxx
2-xxx
3-cys-gly-glu-xxx
4-cys-xxx
5-xxx
6-xxx
7-xxx
8-cys-xxx
9-xxx
10-xxx
11-xxx
12-cys-xxx
13-cys-xxx
14-xxx
15-xxx
16-xxx
17-cys-xxx
18-xxx
19-xxx
20
(seq id no.19)
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1