用于癌症治疗的抗CD137抗原结合分子的制作方法
用于癌症治疗的抗cd137抗原结合分子
技术领域
1.本公开涉及包含抗cd137抗原结合分子的抗癌剂,以及组合使用这种试剂和另一种抗癌剂的治疗方法。
背景技术:
2.癌症是一种致命疾病,除某些情况外,很难完全治愈。作为主要治疗方法的化疗试剂的治疗结果不是很好。已经提出,不仅癌细胞本身的异质性起着重要作用,而且肿瘤微环境作为使癌症治疗困难的因素也起着重要作用(非专利文献1)。近来,已示出不可切除的恶性黑色素瘤等可能用抗ctla-4抗体治愈,该抗体抑制ctla-4的免疫抑制功能,从而促进t细胞的激活(非专利文献2)。2011年,抗人ctla-4单克隆抗体(伊匹单抗(ipilimumab))被美国食品药品监督管理局(fda)批准为世界上第一个免疫激活抗体药物。此外,据报道,针对pd-1和pd-l1(除ctla-4以外的其他免疫检查点分子)的抑制性抗体具有治疗作用(非专利文献3),并已获得fda批准。
3.可以理解,在肿瘤免疫中具有重要作用的t细胞被两个信号激活:1)t细胞受体(tcr)与主要组织相容性复合物(mhc)i类分子呈递的抗原肽结合,和tcr的激活;2)t细胞表面上的共刺激分子与其在抗原呈递细胞上的配体的结合以及该共刺激分子的激活。另外,已经描述了在t细胞表面上属于包括cd137(4-1bb)的肿瘤坏死因子受体超家族(tnfrsf)的共刺激分子的激活,对t细胞激活很重要(非专利文献4)。
4.肿瘤坏死因子受体超家族包括cd137、cd40、ox40、rank、gitr等分子。据报道,cd137不仅在t细胞表面表达,而且在其他免疫细胞如树突细胞(dc)、b细胞、nk细胞、巨噬细胞和嗜中性粒细胞(npl 5)的表面表达。
5.已经证明cd137激动剂抗体在小鼠模型中示出抗肿瘤作用,并且这主要是由小鼠模型实验激活cd8阳性t细胞和nk细胞引起的(npl 6)。然而,由于cd137激动剂抗体的非特异性肝毒性而引起的副作用已成为临床和非临床问题,阻碍了药物开发的预期进展(非专利文献7,非专利文献8)。提示副作用主要是由非肿瘤、非免疫组织(例如肝脏)中免疫细胞的激活引起的,这涉及抗体通过抗体恒定区与fcγ受体的结合(非专利文献9)。另一方面,据报道,为了使激动性抗tnf受体超家族成员抗体在体内表现出激动活性,需要将该抗体与表达fcγ受体的细胞(表达fcγrii的细胞)交联(非专利文献10)。即,cd137激动剂抗体与fcγ受体的结合既参与抗体的抗肿瘤作用的药效,也参与其副作用如肝毒性。因此,增加抗体与fcγ受体之间的结合有望增强药效,但也可能增加肝毒性副作用,而降低抗体与fcγ受体之间的结合可能减少副作用但也降低药效。迄今为止,尚无关于cd137激动剂抗体的药效和副作用分开的报告。而且,cd137激动剂抗体本身的抗肿瘤作用在临床上不是都有效,希望进一步提高药效而避免毒性。因此,期望开发一种能够诱导抗肿瘤免疫应答同时减少那些副作用的新药物。
6.当将治疗性抗体施用于活体时,期望其靶抗原仅在病变部位特异性表达。但是,在许多情况下,相同的抗原也在非病变部位即正常组织中表达,这可能是从治疗的观点来看
不希望的副作用的产生原因。例如,虽然抗肿瘤抗原的抗体可以通过adcc等对肿瘤细胞表现出细胞毒性活性,但是如果相同的抗原在正常细胞中表达,它们也可能损害正常细胞。为了解决上述问题,着眼于在靶组织(例如肿瘤组织)中大量存在某些化合物的现象,开发了查找依赖于这种化合物的浓度而改变抗原结合活性的抗原结合分子的技术(例如,专利文献1)。
7.近年来,以靶向免疫检查点分子诸如ctla-4、pd-1、pd-l1的抑制剂为代表的免疫治疗剂的疗效已得到临床证实。但这些药物并非对所有患者都有效,需要进一步提高药效。关于免疫疗法的联合使用,已确认与单独使用伊匹单抗(ipilimumab)相比,纳武利尤单抗(nivolumab)和伊匹单抗的联合使用提高了在黑色素瘤中的药效(非专利文献11)。
8.引用列表
9.专利文献
10.[ptl 1]wo2013/180200
[0011]
非专利文献
[0012]
[npl 1]hanahan,cell,2011,144,646-74
[0013]
[npl 2]prieto,clin cancer res.2012,18,2039-47
[0014]
[npl 3]hamid,expert opin.biol.ther.,2013,6,847-61
[0015]
[npl 4]summers,nat rev immunol,2012,12,339-51
[0016]
[npl 5]vinay,cellular&molecular immunology,2011,8,281-284
[0017]
[npl 6]houot,blood,2009,114,3431-8
[0018]
[npl 7]ascierto,semin oncol,2010,37,508-16
[0019]
[npl 8]dubrot,cancer immunol immunother,2010,59,1223-33
[0020]
[npl 9]schabowsky,vaccine,2009,28,512-22
[0021]
[npl 10]li,proc natl acad sci u s a.2013,110(48),19501-6
[0022]
[npl 11]n eng j med(2015)vol.373,p.23-34
技术实现要素:
[0023]
技术问题
[0024]
本公开涉及包含抗cd137抗原结合分子的抗癌剂,以及与另一种抗癌剂的联合疗法。
[0025]
解决问题的方案
[0026]
为了提供具有免疫细胞激活作用、细胞毒活性或抗肿瘤活性,同时对非肿瘤组织诸如正常组织的作用降低且副作用较小的抗cd137抗原结合分子,并提供使用该抗cd137抗原结合分子的方法,本发明提供包含抗cd137抗原结合分子作为活性成分的抗癌剂,其特征在于其与cd137的结合活性根据靶组织(例如肿瘤组织)中的各种化合物(例如小分子化合物)而变化。本公开还提供了使用这种包含抗cd137抗原结合分子的抗癌剂和另一种试剂的联合疗法。
[0027]
具体地,本公开提供包含抗cd137抗原结合分子的抗癌剂、其使用方法、使用这种抗癌剂和另一种抗癌剂的联合疗法、试剂盒等,如下文示例性所描述的。
[0028]
[1]
[0029]
抗癌剂,其包含抗cd137抗原结合分子作为活性成分,所述抗cd137抗原结合分子包含选自以下(a)至(m)的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的任意组合:
[0030]
(a)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:8的氨基酸序列;hvr-h3,其包含seq id no:17的氨基酸序列;hvr-l1,其包含seq id no:21的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0031]
(b)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:9的氨基酸序列;hvr-h3,其包含seq id no:17的氨基酸序列;hvr-l1,其包含seq id no:22的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0032]
(c)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:10的氨基酸序列;hvr-h3,其包含seq id no:17的氨基酸序列;hvr-l1,其包含seq id no:22的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0033]
(d)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:11的氨基酸序列;hvr-h3,其包含seq id no:18的氨基酸序列;hvr-l1,其包含seq id no:21的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0034]
(e)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:8的氨基酸序列;hvr-h3,其包含seq id no:18的氨基酸序列;hvr-l1,其包含seq id no:21的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0035]
(f)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:12的氨基酸序列;hvr-h3,其包含seq id no:18的氨基酸序列;hvr-l1,其包含seq id no:21的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:28的氨基酸序列;
[0036]
(g)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:13的氨基酸序列;hvr-h3,其包含seq id no:18的氨基酸序列;hvr-l1,其包含seq id no:21的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:29的氨基酸序列;
[0037]
(h)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:14的氨基酸序列;hvr-h3,其包含seq id no:19的氨基酸序列;hvr-l1,其包含seq id no:23的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0038]
(i)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:15的氨基酸序列;hvr-h3,其包含seq id no:20的氨基酸序列;hvr-l1,其包含seq id no:24的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0039]
(j)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:15的氨
基酸序列;hvr-h3,其包含seq id no:20的氨基酸序列;hvr-l1,其包含seq id no:25的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0040]
(k)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:16的氨基酸序列;hvr-h3,其包含seq id no:20的氨基酸序列;hvr-l1,其包含seq id no:25的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;
[0041]
(l)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:14的氨基酸序列;hvr-h3,其包含seq id no:19的氨基酸序列;hvr-l1,其包含seq id no:24的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列;和
[0042]
(m)hvr-h1,其包含seq id no:7的氨基酸序列;hvr-h2,其包含seq id no:14的氨基酸序列;hvr-h3,其包含seq id no:17的氨基酸序列;hvr-l1,其包含seq id no:21的氨基酸序列;hvr-l2,其包含seq id no:26的氨基酸序列;和hvr-l3,其包含seq id no:27的氨基酸序列。
[0043]
[1.1]
[0044]
抗癌剂,其包含抗cd137抗原结合分子作为活性成分,所述抗cd137抗原结合分子包含:
[0045]
(a)vh,其与seq id no:43至53的任一氨基酸序列具有至少95%序列同一性;或者
[0046]
(b)vl,其与seq id no:54至60的任一氨基酸序列具有至少95%序列同一性。
[0047]
[1.2]
[0048]
抗癌剂,其包含抗cd137抗原结合分子,所述抗cd137抗原结合分子包含选自以下(a)至(m)的vh和vl的任意组合:
[0049]
(a)vh,其与seq id no:43的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:54的氨基酸序列具有至少95%的序列同一性;
[0050]
(b)vh,其与seq id no:44的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:55的氨基酸序列具有至少95%的序列同一性;
[0051]
(c)vh,其与seq id no:45的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:55的氨基酸序列具有至少95%的序列同一性;
[0052]
(d)vh,其与seq id no:46的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:54的氨基酸序列具有至少95%的序列同一性;
[0053]
(e)vh,其与seq id no:47的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:54的氨基酸序列具有至少95%的序列同一性;
[0054]
(f)vh,其与seq id no:48的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:56的氨基酸序列具有至少95%的序列同一性;
[0055]
(g)vh,其与seq id no:49的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:57的氨基酸序列具有至少95%的序列同一性;
[0056]
(h)vh,其与seq id no:50的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:58的氨基酸序列具有至少95%的序列同一性;
[0057]
(i)vh,其与seq id no:51的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:59的氨基酸序列具有至少95%的序列同一性;
[0058]
(j)vh,其与seq id no:51的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:60的氨基酸序列具有至少95%的序列同一性;
[0059]
(k)vh,其与seq id no:52的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:60的氨基酸序列具有至少95%的序列同一性;
[0060]
(l)vh,其与seq id no:50的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:59的氨基酸序列具有至少95%的序列同一性;和
[0061]
(m)vh,其与seq id no:53的氨基酸序列具有至少95%的序列同一性;和vl,其与seq id no:54的氨基酸序列具有至少95%的序列同一性。
[0062]
[2]
[0063]
抗癌剂,其包含抗cd137抗原结合分子,所述抗cd137抗原结合分子包含选自以下(a)至(m)的vh和vl的任意组合:
[0064]
(a)vh,其包含seq id no:43的氨基酸序列;和vl,其包含seq id no:54的氨基酸序列;
[0065]
(b)vh,其包含seq id no:44的氨基酸序列;和vl,其包含seq id no:55的氨基酸序列;
[0066]
(c)vh,其包含seq id no:45的氨基酸序列;和vl,其包含seq id no:55的氨基酸序列;
[0067]
(d)vh,其包含seq id no:46的氨基酸序列;和vl,其包含seq id no:54的氨基酸序列;
[0068]
(e)vh,其包含seq id no:47的氨基酸序列;和vl,其包含seq id no:54的氨基酸序列;
[0069]
(f)vh,其包含seq id no:48的氨基酸序列;和vl,其包含seq id no:56的氨基酸序列;
[0070]
(g)vh,其包含seq id no:49的氨基酸序列;和vl,其包含seq id no:57的氨基酸序列;
[0071]
(h)vh,其包含seq id no:50的氨基酸序列;和vl,其包含seq id no:58的氨基酸序列;
[0072]
(i)vh,其包含seq id no:51的氨基酸序列;和vl,其包含seq id no:59的氨基酸序列;
[0073]
(j)vh,其包含seq id no:51的氨基酸序列;和vl,其包含seq id no:60的氨基酸序列;
[0074]
(k)vh,其包含seq id no:52的氨基酸序列;和vl,其包含seq id no:60的氨基酸序列;
[0075]
(l)vh,其包含seq id no:50的氨基酸序列;和vl,其包含seq id no:59的氨基酸序列;和
[0076]
(m)vh,其包含seq id no:53的氨基酸序列;和vl,其包含seq id no:54的氨基酸序列。
[0077]
[2.1]
[0078]
[1]至[2]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子具有依赖于小分子化合物的cd137结合活性。
[0079]
[2.2]
[0080]
抗癌剂,其含有抗cd137抗原结合分子,所述抗cd137抗原结合分子具有依赖于小分子化合物的cd137结合活性,其中所述抗cd137抗原结合分子与根据[1]至[2.1]中任一项所述的抗原结合分子在10μm或更多、50μm或更多、100μm或更多、150μm或更多、200μm或更多、或250μm或更多的小分子化合物存在下竞争结合至cd137。
[0081]
[2.3]
[0082]
抗癌剂,其含有抗cd137抗原结合分子,所述抗cd137抗原结合分子具有依赖于小分子化合物的cd137结合活性,其中在存在10μm或更多、50μm或更多、100μm或更多、150μm或更多、200μm或更多、或250μm或更多的小分子化合物时,所述抗cd137抗原结合分子结合至与[1]至[2.1]中任一项所述的抗原结合分子所结合的相同的cd137的表位。
[0083]
[2.4]
[0084]
[2.1]至[2.3]中任一项所述的抗癌剂,其中,所述小分子化合物为含腺苷化合物。
[0085]
[2.5]
[0086]
[2.1]至[2.4]中任一项所述的抗癌剂,其中,所述小分子化合物是atp。
[0087]
[2.6]
[0088]
[1]至[3.4]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子是单克隆抗体或其抗原结合片段。
[0089]
[3]
[0090]
[1]至[2.6]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子是人抗体、人源化抗体或嵌合抗体,或它们中任一种的抗原结合片段。
[0091]
[3.1]
[0092]
[1]至[3]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子为全长igg1抗体。
[0093]
[3.2]
[0094]
[1]至[3.1]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子包含其中至少一个氨基酸被改变的改变的fc区,其中与不包含氨基酸改变的亲本fc区相比,所述改变的fc区与fcγriib的结合活性增加。
[0095]
[3.3]
[0096]
[3.2]所述的抗癌剂,其中所述至少一个氨基酸改变是选自由根据eu编号的g236n、h268d和a330k组成的组的至少一个氨基酸置换。
[0097]
[3.4]
[0098]
[3.2]或[3.3]所述的抗癌剂,其中所述至少一个氨基酸改变是根据eu编号的氨基酸置换g236n/h268d/a330k的组合。
[0099]
[3.5]
[0100]
[1]至[3.4]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子包含其中至少一个氨基酸被改变的改变的fc区,其中与包含不包含氨基酸改变的亲本fc区的亲本抗
cd137抗原结合分子相比,所述抗cd137抗原结合分子具有增加的等电点(pi)。
[0101]
[3.6]
[0102]
[3.5]所述的抗癌剂,其中所述至少一个氨基酸改变是选自由根据eu编号的q311r、p343r和d413k组成的组的至少一个氨基酸置换。
[0103]
[3.7]
[0104]
[3.5]或[3.6]所述的抗癌剂,其中所述至少一个氨基酸改变是根据eu编号的(i)氨基酸置换p343r,(ii)氨基酸置换q311r/p343r的组合,或(iii)氨基酸置换q311r/d413k的组合。
[0105]
[4]
[0106]
[1]至[3.7]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子包含改变的fc区,并且所述改变的fc区包含选自以下的根据eu编号的氨基酸改变的任意一种组合:
[0107]
l235w/g236n/h268d/q295l/k326t/a330k/p343r/d413k;
[0108]
k214r/l235w/g236n/h268d/q295l/k326t/a330k/p343r/d413k;
[0109]
l234y/p238d/t250v/v264i/t307p/a330k/p343r/d413k;
[0110]
l234y/p238d/v264i/a330k/p343r/d413k;
[0111]
l234y/g237d/p238d/t250v/t307p/a330k/p343r/d413k;
[0112]
l234y/g237d/p238d/a330k/p343r/d413k;
[0113]
l235w/g236n/h268d/q295l/k326t/a330k/q311r/p343r;
[0114]
l234y/p238d/t250v/v264i/t307p/a330k/q311r/p343r;
[0115]
l234y/p238d/v264i/a330k/q311r/p343r;
[0116]
l234y/g237d/p238d/t250v/t307p/a330k/q311r/p343r;
[0117]
l234y/g237d/p238d/a330k/q311r/p343r;
[0118]
l235w/g236n/h268d/q295l/k326t/a330k/p343r;
[0119]
k214r/l235w/g236n/h268d/q295l/k326t/a330k/p343r;
[0120]
l235w/g236n/h268d/q295l/k326t/a330k/d413k;
[0121]
k214r/g236n/h268d/a330k/p343r;
[0122]
k214r/l235w/g236n/h268d/a330k/p343r;
[0123]
k214r/g236n/h268d/a330k/d413k;
[0124]
k214r/g236n/h268d/a330k/p343r/d413k;
[0125]
k214r/l235w/g236n/h268d/a330k/p343r/d413k;
[0126]
k214r/g236n/h268d/a330k/q311r;
[0127]
k214r/l235w/g236n/h268d/a330k/q311r;
[0128]
k214r/g236n/h268d/a330k/q311r/p343r;
[0129]
k214r/l235w/g236n/h268d/a330k/q311r/p343r;
[0130]
k214r/g236n/h268d/a330k/q311r/d413k;
[0131]
k214r/l235w/g236n/h268d/a330k/q311r/d413k;和
[0132]
k214r/l235w/g236n/h268d/q295l/k326t/a330k/q311r。
[0133]
[4.1]
[0134]
[3.2]至[4]中任一项所述的抗癌剂,其中,所述改变的fc区衍生自人igg1fc区。
[0135]
[4.2]
[0136]
[3.2]至[4.1]中任一项所述的抗癌剂,其中,所述改变的fc区进一步包含根据eu编号的在位置446和447处的缺失。
[0137]
[4.3]
[0138]
[1]至[4.2]中任一项所述的抗癌剂,其中,所述抗cd137抗原结合分子包含重链恒定区,所述重链恒定区包含seq id no:64至85中的任一项氨基酸序列。
[0139]
[5]
[0140]
抗癌剂,其包含抗cd137抗原结合分子,所述抗cd137抗原结合分子包含选自以下(i)至(xxxviii)的vh、vl、ch和cl的任意组合:
[0141]
(i)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:64的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0142]
(ii)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:66的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0143]
(iii)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:67的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0144]
(iv)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:68的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0145]
(v)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:69的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0146]
(vi)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:70的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0147]
(vii)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:71的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0148]
(viii)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:73的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0149]
(ix)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:75的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0150]
(x)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:78的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0151]
(xi)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:80的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0152]
(xii)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:82的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0153]
(xiii)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:84的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0154]
(xiv)vh,其包含seq id no:43的氨基酸序列;ch,其包含seq id no:85的氨基酸序列;vl,其包含seq id no:54的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0155]
(xv)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:65的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0156]
(xvi)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:72的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0157]
(xvii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:74的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0158]
(xviii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:75的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0159]
(xix)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:77的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0160]
(xx)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:78的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0161]
(xxi)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:79的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0162]
(xxii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:80的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0163]
(xxiii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:81的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0164]
(xxiv)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:82的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0165]
(xxv)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:83的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0166]
(xxvi)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:84的氨基酸序列;vl,其包含seq id no:59的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0167]
(xxvii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:72的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0168]
(xxviii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:74的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0169]
(xxix)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:75的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0170]
(xxx)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:77的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0171]
(xxxi)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:78的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0172]
(xxxii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:79的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0173]
(xxxiii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:80的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0174]
(xxxiv)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:81的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0175]
(xxxv)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:82的氨基酸
序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0176]
(xxxvi)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:83的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;
[0177]
(xxxvii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:84的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列;和
[0178]
(xxxviii)vh,其包含seq id no:51的氨基酸序列;ch,其包含seq id no:85的氨基酸序列;vl,其包含seq id no:60的氨基酸序列;和cl,其包含seq id no:63的氨基酸序列。
[0179]
[6]
[0180]
[1]至[5]中任一项所述的抗癌剂,其被施用至具有以下疾病的癌症患者:(i)选自b细胞、树突细胞、自然杀伤细胞、巨噬细胞和cd8
+
t细胞中的一种或多种细胞浸润的实体癌,和/或(ii)调节性t(treg)细胞或cd4
+
t细胞浸润的实体癌。
[0181]
[6.1]
[0182]
[1]至[6]中任一项所述的抗癌剂,其被施用至患有cd8
+
t细胞浸润的实体癌的癌症患者。
[0183]
[7]
[0184]
[1]至[6.1]中任一项所述的抗癌剂,其被施用至患有免疫检查点抑制剂治疗难治的癌症的患者。
[0185]
[8]
[0186]
[1]至[7]中任一项所述的抗癌剂,其被施用至患有选自由以下各项组成的组的一种或多种癌症的癌症患者:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0187]
[8.1]
[0188]
[1]至[8]中任一项所述的抗癌剂,其被施用至患有选自由以下各项组成的组的一种或多种癌症的癌症患者:胃癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0189]
[9]
[0190]
[1]至[5]中任一项所述的抗癌剂,其与至少一种其他抗癌剂组合使用。
[0191]
[9.1]
[0192]
[9]所述的抗癌剂,其中所述抗癌剂的特征在于与其他抗癌剂同时施用。
[0193]
[9.2]
[0194]
[9]所述的抗癌剂,其中所述抗癌剂的特征在于在施用其他抗癌剂之前或之后施用。
[0195]
[10]
[0196]
[9]至[9.2]中任一项所述的抗癌剂,其中,所述其他抗癌剂是选自以下各项的至
少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0197]
[10.1]
[0198]
[10]所述的抗癌剂,其中所述其他抗癌剂是化疗剂。
[0199]
[10.2]
[0200]
[10]或[10.1]所述的抗癌剂,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0201]
[10.3]
[0202]
[10]所述的抗癌剂,其中所述其他抗癌剂是t细胞活化激动剂。
[0203]
[10.4]
[0204]
[10]或[10.3]所述的抗癌剂,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0205]
[11]
[0206]
[10]所述的抗癌剂,其中所述其他抗癌剂是免疫检查点抑制剂。
[0207]
[12]
[0208]
[10]或[11]所述的抗癌剂,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0209]
[12.1]
[0210]
[10]、[11]和[12]中任一项所述的抗癌剂,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0211]
[12.2]
[0212]
[9]至[12.1]中任一项所述的抗癌剂,其被施用至患有免疫检查点抑制剂治疗难治的癌症的患者。
[0213]
[12.3]
[0214]
[12.2]所述的抗癌剂,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0215]
[13]
[0216]
[10]所述的抗癌剂,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0217]
[13.1]
[0218]
[10]或[13]所述的抗癌剂,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0219]
[13.2]
[0220]
[13.1]所述的抗癌剂,其中所述多特异性抗体是双特异性抗体。
[0221]
[14]
[0222]
[9]至[9.2]中任一项所述的抗癌剂,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞的一种或多种细胞的试剂。
[0223]
[15]
[0224]
[9]至[14]中任一项所述的抗癌剂,其被施用至患有选自由以下各项组成的组的一种或多种癌症的癌症患者:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅
克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0225]
[15.1]
[0226]
[9]至[15]中任一项所述的抗癌剂,其被施用至患有选自由以下各项组成的组的一种或多种癌症的癌症患者:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0227]
[16]
[0228]
[1]至[5]中任一项所述的抗癌剂,其用于与至少一种其他抗癌剂联合治疗以增强个体肿瘤组织中t细胞的活化。
[0229]
[16.1]
[0230]
[16]所述的抗癌剂,其中当肿瘤组织中选自cd8b1、gzmb、prf1和ifng的至少一种基因的表达水平升高时,判断肿瘤组织中t细胞的活化已经增强。
[0231]
[17]
[0232]
[1]至[5]中任一项所述的抗癌剂,其用于与至少一种其他抗癌剂联合治疗以促进个体肿瘤组织中cd8
+ t细胞的增殖。
[0233]
[17.1]
[0234]
[16]至[17]中任一项所述的抗癌剂,其特征在于,与其他抗癌剂同时施用。
[0235]
[17.2]
[0236]
[16]至[17]中任一项所述的抗癌剂,其特征在于,在施用其他抗癌剂之前或之后施用。
[0237]
[17.3]
[0238]
[16]至[17.2]中任一项所述的抗癌剂,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0239]
[17.4]
[0240]
[16]至[17.2]中任一项所述的抗癌剂,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞的一种或多种细胞的试剂。
[0241]
[18]
[0242]
用于治疗癌症的药物组合物,其包含[1]至[5]中任一项所述的抗cd137抗原结合分子与至少一种其他抗癌剂的组合。
[0243]
[18.1]
[0244]
[18]所述的药物组合物,其中使用所述抗cd137抗原结合分子以便与其他抗癌剂同时施用至患者。
[0245]
[18.2]
[0246]
[18]所述的药物组合物,其中使用所述抗cd137抗原结合分子以便在施用其他抗癌剂之前或之后施用至患者。
[0247]
[19]
[0248]
[18]至[18.2]中任一项所述的药物组合物,其中,所述其他抗癌剂是选自以下各
项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0249]
[19.1]
[0250]
[19]所述的药物组合物,其中所述其他抗癌剂是化疗剂。
[0251]
[19.2]
[0252]
[19]或[19.1]所述的药物组合物,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0253]
[19.3]
[0254]
[19]所述的药物组合物,其中所述其他抗癌剂是t细胞活化激动剂。
[0255]
[19.4]
[0256]
[19]或[19.3]所述的药物组合物,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0257]
[20]
[0258]
[19]所述的药物组合物,其中所述其他抗癌剂是免疫检查点抑制剂。
[0259]
[21]
[0260]
[19]或[20]所述的药物组合物,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0261]
[21.1]
[0262]
[19]、[20]和[21]中任一项所述的药物组合物,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0263]
[21.2]
[0264]
[18]至[21.1]中任一项所述的药物组合物,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0265]
[21.3]
[0266]
[21.2]所述的药物组合物,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0267]
[22]
[0268]
[19]所述的药物组合物,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0269]
[22.1]
[0270]
[19]或[22]所述的药物组合物,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0271]
[22.2]
[0272]
[22.1]所述的药物组合物,其中所述多特异性抗体是双特异性抗体。
[0273]
[23]
[0274]
[18]至[18.2]中任一项所述的药物组合物,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0275]
[24]
[0276]
[18]至[23]中任一项所述的药物组合物,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细
胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0277]
[24.1]
[0278]
[18]至[24]中任一项所述的药物组合物,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0279]
[25]
[0280]
[1]至[5]中任一项所述的抗cd137抗原结合分子与至少一种其他抗癌剂的组合,其用于治疗癌症。
[0281]
[25.1]
[0282]
[25]所述的组合,其中使用所述抗cd137抗原结合分子以便与其他抗癌剂同时施用至患者。
[0283]
[25.2]
[0284]
[25]所述的组合,其中使用所述抗cd137抗原结合分子以便在施用其他抗癌剂之前或之后施用至患者。
[0285]
[26]
[0286]
[25]至[25.2]中任一项所述的组合,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0287]
[26.1]
[0288]
[26]所述的组合,其中所述其他抗癌剂是化疗剂。
[0289]
[26.2]
[0290]
[26]或[26.1]所述的组合,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0291]
[26.3]
[0292]
[26]所述的组合,其中所述其他抗癌剂是t细胞活化激动剂。
[0293]
[26.4]
[0294]
[26]或[26.3]所述的组合,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0295]
[27]
[0296]
[26]所述的组合,其中所述其他抗癌剂是免疫检查点抑制剂。
[0297]
[28]
[0298]
[26]或[27]所述的组合,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0299]
[28.1]
[0300]
[26]、[27]和[28]中任一项所述的组合,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0301]
[28.2]
[0302]
[25]至[28.1]中任一项所述的组合,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0303]
[28.3]
[0304]
[28.2]所述的组合,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0305]
[29]
[0306]
[26]所述的组合,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0307]
[29.1]
[0308]
[26]或[29]所述的组合,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0309]
[29.2]
[0310]
[29.1]所述的组合,其中所述多特异性抗体是双特异性抗体。
[0311]
[30]
[0312]
[25]至[25.2]中任一项所述的组合,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0313]
[31]
[0314]
[25]至[30]中任一项所述的组合,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0315]
[31.1]
[0316]
[25]至[31]中任一项所述的组合,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0317]
[32]
[0318]
[1]至[5]中任一项所述的抗cd137抗原结合分子与至少一种其他抗癌剂的组合作为抗癌剂的用途。
[0319]
[32.1]
[0320]
[32]所述的用途,其中使用所述抗cd137抗原结合分子以便与其他抗癌剂同时施用至患者。
[0321]
[32.2]
[0322]
[32]所述的用途,其中使用所述抗cd137抗原结合分子以便在施用其他抗癌剂之前或之后施用至患者。
[0323]
[33]
[0324]
[32]至[32.2]中任一项所述的用途,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0325]
[33.1]
[0326]
[33]所述的用途,其中所述其他抗癌剂是化疗剂。
[0327]
[33.2]
[0328]
[33]或[33.1]所述的用途,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0329]
[33.3]
[0330]
[33]所述的用途,其中所述其他抗癌剂是t细胞活化激动剂。
[0331]
[33.4]
[0332]
[33]或[33.3]所述的用途,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0333]
[34]
[0334]
[33]所述的用途,其中所述其他抗癌剂是免疫检查点抑制剂。
[0335]
[35]
[0336]
[33]或[34]所述的用途,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0337]
[35.1]
[0338]
[33]、[34]和[35]中任一项所述的组合,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0339]
[35.2]
[0340]
[32]至[35.1]中任一项所述的用途,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0341]
[35.3]
[0342]
[35.2]所述的用途,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0343]
[36]
[0344]
[33]所述的用途,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0345]
[36.1]
[0346]
[33]或[36]所述的用途,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0347]
[36.2]
[0348]
[36.1]所述的用途,其中所述多特异性抗体是双特异性抗体。
[0349]
[37]
[0350]
[32]至[32.2]中任一项所述的用途,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0351]
[38]
[0352]
[32]至[37]中任一项所述的用途,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0353]
[38.1]
[0354]
[32]至[38]中任一项所述的用途,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白
血病。
[0355]
[39]
[0356]
用于治疗癌症的试剂盒,其包括:
[0357]
(1)包含[1]至[5]中任一项所述的抗cd137抗原结合分子作为活性成分的药物组合物;和
[0358]
(2)包装说明书或标签,其指示在所述药物组合物施用之前、同时或之后施用至少一种其他抗癌剂。
[0359]
[39.1]
[0360]
[39]所述的试剂盒,其中所述药物组合物填充在容器中。
[0361]
[39.2]
[0362]
[39]至[39.2]中任一项所述的试剂盒,其中,使用包含抗cd137抗原结合分子作为活性成分的药物组合物,以便与其他抗癌剂同时施用至患者。
[0363]
[39.3]
[0364]
[39]或[39.1]中任一项所述的试剂盒,其中,使用包含抗cd137抗原结合分子作为活性成分的药物组合物,以便在施用其他抗癌剂之前或之后施用至患者。
[0365]
[40]
[0366]
[39]至[39.2]中任一项所述的试剂盒,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0367]
[40.1]
[0368]
[40]所述的试剂盒,其中所述其他抗癌剂是化疗剂。
[0369]
[40.2]
[0370]
[40]或[40.1]所述的试剂盒,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0371]
[40.3]
[0372]
[40]所述的试剂盒,其中所述其他抗癌剂是t细胞活化激动剂。
[0373]
[40.4]
[0374]
[40]或[40.3]所述的试剂盒,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0375]
[41]
[0376]
[40]所述的试剂盒,其中所述抗癌剂是免疫检查点抑制剂。
[0377]
[42]
[0378]
[40]或[41]所述的试剂盒,其中所述抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0379]
[42.1]
[0380]
[40]、[41]和[42]中任一项所述的试剂盒,其中,所述抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0381]
[42.2]
[0382]
[39]至[42.1]中任一项所述的试剂盒,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0383]
[42.3]
[0384]
[42.2]所述的试剂盒,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0385]
[43]
[0386]
[40]所述的试剂盒,其中所述抗癌剂是t细胞重定向抗原结合分子。
[0387]
[43.1]
[0388]
[40]或[43]所述的试剂盒,其中,所述抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0389]
[43.2]
[0390]
[43.1]所述的试剂盒,其中所述多特异性抗体是双特异性抗体。
[0391]
[44]
[0392]
[39]至[39.2]中任一项所述的试剂盒,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0393]
[45]
[0394]
[39]至[44]中任一项所述的试剂盒,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0395]
[45.1]
[0396]
[39]至[44]中任一项所述的试剂盒,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0397]
[46]
[0398]
用于治疗癌症的方法,其包括将[1]至[5]中任一项所述的抗cd137抗原结合分子施用至具有以下疾病的患者:(i)选自b细胞、树突细胞、自然杀伤细胞、巨噬细胞和cd8
+
t细胞中的一种或多种细胞浸润的实体癌,和/或(ii)调节性t(treg)细胞或cd4
+
t细胞浸润的实体癌。
[0399]
[46.1]
[0400]
[46]所述的方法,其中所述患者是患有cd8
+
t细胞浸润的实体癌的患者。
[0401]
[47]
[0402]
[46]或[46.1]所述的方法,其中所述患者患有免疫检查点抑制剂治疗难治的癌症。
[0403]
[48]
[0404]
[46]至[47]中任一项所述的方法,其中所述患者患有选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0405]
[48.1]
[0406]
[46]至[48]中任一项所述的方法,其中所述患者是患有选自由以下各项组成的组的一种或多种癌症的患者:胃癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0407]
[49]
[0408]
用于治疗癌症的方法,其包括将[1]至[5]中任一项所述的抗cd137抗原结合分子与至少一种其他抗癌剂组合施用至患者。
[0409]
[49.1]
[0410]
[49]所述的方法,其中将所述抗cd137抗原结合分子与其他抗癌剂同时施用至患者。
[0411]
[49.2]
[0412]
[49]所述的方法,其中,将所述抗cd137抗原结合分子在施用其他抗癌剂之前或之后施用至患者。
[0413]
[50]
[0414]
[49]至[49.2]中任一项所述的方法,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0415]
[50.1]
[0416]
[50]所述的方法,其中所述其他抗癌剂是化疗剂。
[0417]
[50.2]
[0418]
[50]或[50.1]所述的方法,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0419]
[50.3]
[0420]
[50]所述的方法,其中所述其他抗癌剂是t细胞活化激动剂。
[0421]
[50.4]
[0422]
[50]或[50.3]所述的方法,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0423]
[51]
[0424]
[50]所述的方法,其中所述其他抗癌剂是免疫检查点抑制剂。
[0425]
[52]
[0426]
[50]或[51]所述的方法,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0427]
[52.1]
[0428]
[50]、[51]和[52]中任一项所述的方法,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0429]
[52.2]
[0430]
[49]至[52.1]中任一项所述的方法,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0431]
[52.3]
[0432]
[52.2]所述的方法,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2
和/或b2m中具有基因突变的癌症。
[0433]
[53]
[0434]
[50]所述的方法,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0435]
[53.1]
[0436]
[50]或[53]所述的方法,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0437]
[53.2]
[0438]
[53.1]所述的方法,其中所述多特异性抗体是双特异性抗体。
[0439]
[54]
[0440]
[49]至[49.2]中任一项所述的方法,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0441]
[55]
[0442]
[49]至[54]中任一项所述的方法,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0443]
[55.1]
[0444]
[49]至[55]中任一项所述的方法,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0445]
[56]
[0446]
[1]至[5]中任一项所述的抗cd137抗原结合分子,其用于治疗:
[0447]
(i)选自b细胞、树突细胞、自然杀伤细胞、巨噬细胞和cd8
+
t细胞中的一种或多种细胞浸润的实体癌,和/或
[0448]
(ii)调节性t(treg)细胞或cd4
+
t细胞浸润的实体癌。
[0449]
[56.1]
[0450]
[56]所述的抗cd137抗原结合分子,其中所述癌症是cd8
+
t细胞浸润的实体癌。
[0451]
[57]
[0452]
[56]或[56.1]所述的抗cd137抗原结合分子,其中所述癌症是免疫检查点抑制剂治疗难治的癌症。
[0453]
[58]
[0454]
[56]至[57]中任一项所述的抗cd137抗原结合分子,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0455]
[58.1]
[0456]
[56]至[58]中任一项所述的抗cd137抗原结合分子,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0457]
[59]
[0458]
[1]至[5]中任一项所述的抗cd137抗原结合分子,其用于与至少一种其他抗癌剂组合用于治疗癌症。
[0459]
[59.1]
[0460]
[59]所述的抗cd137抗原结合分子,其中所述治疗的特征在于,与其他抗癌剂同时施用所述抗cd137抗原结合分子。
[0461]
[59.2]
[0462]
[59]所述的抗cd137抗原结合分子,其中所述治疗的特征在于,在施用其他抗癌剂之前或之后施用所述抗cd137抗原结合分子。
[0463]
[60]
[0464]
[59]至[59.2]中任一项所述的抗cd137抗原结合分子,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0465]
[60.1]
[0466]
[60]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是化疗剂。
[0467]
[60.2]
[0468]
[60]或[60.1]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0469]
[60.3]
[0470]
[60]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是t细胞活化激动剂。
[0471]
[60.4]
[0472]
[60]或[60.3]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0473]
[61]
[0474]
[60]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是免疫检查点抑制剂。
[0475]
[62]
[0476]
[60]或[61]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0477]
[62.1]
[0478]
[60]、[61]和[62]中任一项所述的抗cd137抗原结合分子,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0479]
[62.2]
[0480]
[59]至[62.1]中任一项所述的抗cd137抗原结合分子,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0481]
[62.3]
[0482]
[62.2]所述的抗cd137抗原结合分子,其中所述免疫检查点抑制剂治疗难治的癌
症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0483]
[63]
[0484]
[60]所述的抗cd137抗原结合分子,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0485]
[63.1]
[0486]
[60]或[63]所述的抗cd137抗原结合分子,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0487]
[63.2]
[0488]
[63.1]所述的抗cd137抗原结合分子,其中所述多特异性抗体是双特异性抗体。
[0489]
[64]
[0490]
[59]至[59.2]中任一项所述的抗cd137抗原结合分子,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0491]
[65]
[0492]
[59]至[64]中任一项所述的抗cd137抗原结合分子,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0493]
[65.1]
[0494]
[59]至[65]中任一项所述的抗cd137抗原结合分子,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0495]
[66]
[0496]
[1]至[5]中任一项所述的抗cd137抗原结合分子在制备用于治疗癌症的药物中的用途,其中所述癌症是
[0497]
(i)选自b细胞、树突细胞、自然杀伤细胞、巨噬细胞和cd8
+
t细胞中的一种或多种细胞浸润的实体癌,和/或
[0498]
(ii)调节性t(treg)细胞或cd4
+
t细胞浸润的实体癌。
[0499]
[66.1]
[0500]
[66]所述的用途,其中所述癌症是cd8
+
t细胞浸润的实体癌。
[0501]
[67]
[0502]
[66]或[66.1]所述的用途,其中所述癌症是免疫检查点抑制剂治疗难治的癌症。
[0503]
[68]
[0504]
[66]至[67]中任一项所述的用途,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,
阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0505]
[68.1]
[0506]
[66]至[68]中任一项所述的用途,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[0507]
[69]
[0508]
[1]至[5]中任一项所述的抗cd137抗原结合分子在制备用于治疗癌症的药物中的用途,其中所述药物的特征在于与至少一种其他抗癌剂组合使用。
[0509]
[69.1]
[0510]
[69]所述的用途,其中所述药物的特征在于与其他抗癌剂同时施用。
[0511]
[69.2]
[0512]
[69]所述的用途,其中所述药物的特征在于在施用其他抗癌剂之前或之后施用。
[0513]
[70]
[0514]
[69]至[69.2]中任一项所述的用途,其中,所述其他抗癌剂是选自以下各项的至少一种抗癌剂:化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂和血管生成抑制剂。
[0515]
[70.1]
[0516]
[70]所述的用途,其中所述其他抗癌剂是化疗剂。
[0517]
[70.2]
[0518]
[70]或[70.1]所述的用途,其中所述其他抗癌剂是选自抗代谢物、植物生物碱和铂化合物中的至少一种化疗剂。
[0519]
[70.3]
[0520]
[70]所述的用途,其中所述其他抗癌剂是t细胞活化激动剂。
[0521]
[70.4]
[0522]
[70]或[70.3]所述的用途,其中所述其他抗癌剂是tnfrsf的激动性抗体。
[0523]
[71]
[0524]
[70]所述的用途,其中所述其他抗癌剂是免疫检查点抑制剂。
[0525]
[72]
[0526]
[70]或[71]所述的用途,其中所述其他抗癌剂是选自抗pd1抗体,抗pdl1抗体,抗tigit抗体,抗tim3抗体,和抗lag3抗体的至少一种免疫检查点抑制剂。
[0527]
[72.1]
[0528]
[70]、[71]和[72]中任一项所述的用途,其中,所述其他抗癌剂为抗pdl1抗体和/或抗tigit抗体。
[0529]
[72.2]
[0530]
[69]至[72.1]中任一项所述的用途,其用于治疗免疫检查点抑制剂治疗难治的癌症。
[0531]
[72.3]
[0532]
[72.2]所述的用途,其中所述免疫检查点抑制剂治疗难治的癌症是在jak1、jak2和/或b2m中具有基因突变的癌症。
[0533]
[73]
[0534]
[70]所述的用途,其中所述其他抗癌剂是t细胞重定向抗原结合分子。
[0535]
[73.1]
[0536]
[70]或[73]所述的用途,其中,所述其他抗癌剂是对cd3和癌抗原具有结合活性的多特异性抗体。
[0537]
[73.2]
[0538]
[73.1]所述的用途,其中所述多特异性抗体是双特异性抗体。
[0539]
[74]
[0540]
[69]至[69.2]中任一项所述的用途,其中,所述其他抗癌剂是消耗和/或灭活选自调节性t细胞、cd4
+
t细胞、b细胞、nk细胞和巨噬细胞中的一种或多种细胞的试剂。
[0541]
[75]
[0542]
[69]至[74]中任一项所述的用途,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病和小儿癌症。
[0543]
[75.1]
[0544]
[69]至[75]中任一项所述的用途,其中所述癌症是选自由以下各项组成的组的一种或多种癌症:胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
附图说明
[0545]
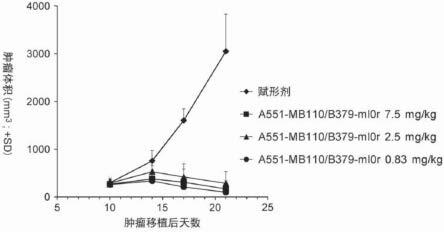
图1显示了a551-mb110/b379-ml0r在移植llc1/ova/gpc3克隆c5细胞的小鼠模型中的抗肿瘤效果。
[0546]
每个点显示一组(n=7)肿瘤体积的平均值。
[0547]
图2显示在移植有llc1/ova/gpc3克隆c5细胞的小鼠模型中,通过施用a551-mb110/b379-ml0r的肿瘤样品中的基因表达水平。
[0548]
子图(a)显示cd8b1的表达水平,子图(b)显示gzmb的表达水平,子图(c)显示prf1的表达水平,并且子图(d)显示ifng的表达水平。
[0549]
图3显示了在移植有llc1/ova/gpc3克隆c5细胞的小鼠模型中,通过施用a551-mb110/b379-ml0r的肿瘤组织中的cd8
+
t细胞的活化程度。
[0550]
子图(a)显示了ova四聚体
+
t细胞在cd8
+
t细胞中的比例。子图(b)显示了颗粒酶b
+
t细胞在cd8
+
t细胞中的比例。子图(c)显示了pd-1
+ t细胞在cd8
+ t细胞中的比例。子图(d)显示了klrg-1
+ t细胞在cd8
+ t细胞中的比例。子图(e)显示了icos
+ t细胞在cd8
+ t细胞中的比例。
[0551]
图4显示了a551-mb110/b379-ml0r在移植e.g7-ova细胞的小鼠模型中的抗肿瘤效果。
[0552]
子图(a)显示了赋形剂施用组中每只小鼠的肿瘤体积变化。子图(b)显示了在a551-mb110/b379-ml0r(2.5mg/kg)施用组中每只小鼠的肿瘤体积变化。
[0553]
图5显示了a375-migg1/b167-ml0r在移植e.g7-ova细胞的小鼠模型中的抗肿瘤效
l1抗体施用组的肿瘤组织中pd-l1的表达程度,子图(d)显示了a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合施用组的肿瘤组织中pd-l1的表达程度。
[0571]
图15显示了由于向移植有mc38细胞的小鼠模型施用a551-mb110/b379-ml0r、抗小鼠pd-l1抗体或其组合而通过血液检查检测到的肝功能标志物的程度。
[0572]
顶部子图显示alt(u/l),底部子图显示ast(u/l)。
[0573]
图16显示了由于向移植有mc38细胞的小鼠模型施用a551-mb110/b379-ml0r、抗小鼠pd-l1抗体或其组合的肿瘤组织中cd8
+
t细胞数量的增加程度。
[0574]
图17显示了a551-mb110/b379-ml0r、抗小鼠pd-l1抗体或其组合在移植有llc1/ova/gpc3克隆c5细胞的小鼠模型中的抗肿瘤效果。
[0575]
每个点显示一组(n=5)肿瘤体积的平均值。
[0576]
图18显示了a375-migg1/b167-ml0r、抗小鼠pd-l1抗体或其组合在移植了c1498细胞的小鼠模型中的抗肿瘤效果。
[0577]
每个点显示一组(n=5)肿瘤体积的平均值。
[0578]
图19显示了a375-migg1/b167-ml0r、抗小鼠pd-l1抗体或其组合在移植了ae17细胞的小鼠模型中的抗肿瘤效果。
[0579]
每个点显示一组(n=5)肿瘤体积的平均值。
[0580]
图20显示了a551-mb110/b379-ml0r、抗hgpc3-mcd3抗体或其组合在移植有llc1/hgpc3的小鼠模型中的抗肿瘤效果。
[0581]
每个点显示一组(n=5)肿瘤体积的平均值。
[0582]
图21显示了在移植有llc1/hgpc3的小鼠模型中,由于施用a551-mb110/b379-ml0r、抗-hgpc3-mcd3抗体或其组合而导致的肿瘤样品中的基因表达水平。
[0583]
分别地,子图(a)显示了cd3e的表达水平,子图(b)显示了cd8b1的表达水平,子图(c)显示了gzmb的表达水平,子图(d)显示了prf1的表达水平,子图(e)显示了ifng的表达水平。
[0584]
图22是示出在存在或不存在atp的情况下使用jurkat细胞测试的各种抗cd137抗体的激动剂活性的图。
[0585]
x轴示出抗体浓度(μg/ml),y轴示出相对光单位。
[0586]
图23是示出在存在或不存在adp的情况下使用jurkat细胞测试的各种抗cd137抗体的激动剂活性的图。
[0587]
x轴示出抗体浓度(μg/ml),y轴示出相对光单位。
[0588]
图24是示出在存在或不存在adpβs的情况下使用人t细胞测试的各种抗cd137抗体的激动剂活性的图。
[0589]
图25是示出在存在或不存在adpβs的情况下使用人t细胞测试的dbbat119-p253/dbbat119l-lamlib(小分子转换抗cd137抗体)或ns1-p253(非转换抗cd137抗体)的激动剂活性的图。
[0590]
x轴示出抗体浓度(μg/ml),y轴示出ifn-γ产生量(ng/ml)。
[0591]
图26是示出通过噬菌体elisa测试的各种抗cd137抗体(具有增强的结合活性的转换抗cd137抗体)的atp依赖性抗原结合活性的图。
[0592]
y轴示出在存在/不存在atp的情况下吸光度的s/n比,x轴示出在存在/不存在抗原
的情况下吸光度的s/n比。
[0593]
图27是示出在存在或不存在atp的情况下抗cd137抗体的各种变体(dbbat119h-p253/dbbat119l-lamlib)与人cd137的结合活性的图。
[0594]
上排示出在不存在atp的情况下与人cd137的结合活性,下排示出在存在atp的情况下与人cd137的结合活性。
[0595]
图28是示出在存在或不存在adpβs的情况下使用人t细胞测试的dbbat119h-p253/dbbat119l-lamlib、dbbatk119h024-p253/dbbatk119l020-lamlib、ic17hdk-higg1/ic17l-k0(对照)或ns1-p253(非转换抗cd137抗体)的激动剂活性的图。
[0596]
子图(a)示出了在不存在adpβs的情况下的测试结果,子图(b)示出了在存在adpβs的情况下的测试结果。
[0597]
x轴示出抗体浓度(μg/ml),y轴示出ifn-γ产生量(ng/ml)。
[0598]
图29是示出在存在或不存在atp的情况下使用4-1bb jurkat报告基因测定法测试的各种转换抗cd137抗体的激动剂活性的图。
[0599]
子图(a)示出了不存在atp的测试结果,子图(b)示出了存在atp的测试结果。
[0600]
图30是示出使用人外周血单核细胞测试的,在存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0601]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0602]
图31是示出使用人外周血单核细胞进行测试的,在存在atp时,由于重链恒定区与fcγ受体的结合活性增加或重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0603]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0604]
图32是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0605]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0606]
图33是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0607]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0608]
图34是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0609]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0610]
图35是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0611]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0612]
图36是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0613]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0614]
图37是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0615]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0616]
图38是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0617]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0618]
图39是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0619]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0620]
图40是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0621]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0622]
图41是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0623]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0624]
图42是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0625]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0626]
图43是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区的pi增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0627]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0628]
图44是示出使用人外周血单核细胞测试的,在存在或不存在atp时,由于重链恒定区与fcγ受体的结合活性增加,各种转换抗cd137抗体的激动剂活性增强的图。
[0629]
子图(a)示出使用il-2产生量为指标测定的激动剂活性,子图(b)示出使用ifn-γ产生量为指标测定的激动剂活性。
[0630]
图45是示出使用人cd137敲入小鼠测试的各种转换和非转换抗cd137抗体的血浆浓度的图。
[0631]
fc都是migg1。
[0632]
图46是示出使用人cd137敲入小鼠测试的各种转换和非转换抗cd137抗体的血浆浓度的图。
[0633]
fc都是mb110。
[0634]
图47是示出使用人cd137敲入小鼠测试的各种转换和非转换抗cd137抗体的血浆浓度的图。
[0635]
fc都是mb492。
[0636]
图48是示出在移植了mc38细胞的小鼠模型中a375-migg1/b167-ml0r的抗肿瘤作用的图。
[0637]
每个点示出一组(n=5)肿瘤体积的平均值。
[0638]
图49是示出在施用抗体(no1-migg1或a375-migg1/b167-ml0r)后移植了mc38细胞的小鼠模型中器官的重量的图。
[0639]
子图(a)示出淋巴结重量,子图(b)示出脾脏重量。
[0640]
图50是示出在施用no1-migg1或a375-migg1/b167-ml0r后,移植了mc38细胞的小鼠模型中淋巴结中t细胞活化程度的图。
[0641]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中icos阳性t细胞的百分比,子图(c)示出cd8阳性t细胞中颗粒酶b阳性t细胞的百分比。
[0642]
图51是示出在施用no1-migg1或a375-migg1/b167-ml0r后,移植了mc38细胞系的小鼠模型中的脾脏中t细胞活化程度的图。
[0643]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中icos阳性t细胞的百分比,子图(c)示出cd8阳性t细胞中颗粒酶b阳性t细胞的百分比。
[0644]
图52是示出在施用no1-migg1或a375-migg1/b167-ml0r后移植了mc38细胞系的小鼠模型中肝脏中t细胞活化程度的图。
[0645]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中颗粒酶b阳性t细胞的百分比。
[0646]
图53是示出在移植了mc38细胞系的小鼠模型中a356-mb110/b040-ml0r的抗肿瘤作用的图。
[0647]
每个点示出一组(n=5)肿瘤体积的平均值。
[0648]
图54是示出在施用ns2-mb110或a356-mb110/b040-ml0r后,移植了mc38细胞系的小鼠模型中器官的重量的图。
[0649]
子图(a)示出淋巴结重量,子图(b)示出脾脏重量。
[0650]
图55是示出在施用ns2-mb110或a356-mb110/b040-ml0r后移植了mc38细胞系的小鼠模型的肝脏中t细胞激活程度的图。
[0651]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中icos阳性t细胞的百分比。
[0652]
图56是示出了在移植了mc38细胞系的小鼠模型中,a372-migg1/b040-ml0r的抗肿瘤作用的图。
[0653]
每个点示出一组(n=5)肿瘤体积的平均值。
[0654]
图57示出了在施用a372-migg1/b040-ml0r后,移植了mc38细胞系的小鼠模型中的淋巴结细胞数量(子图(a))和脾脏重量(子图(b))。
migg1/b256-ml0r的抗肿瘤作用。
[0678]
图72是示出了在施用ns1-migg1、a548-migg1/b256-ml0r或a551-migg1/b256-ml0r后,移植了mc38细胞系的小鼠模型中器官的重量的图。
[0679]
子图(a)示出淋巴结重量,子图(b)示出脾脏重量。
[0680]
图73是示出了在施用ns1-migg1、a548-migg1/b256-ml0r或a551-migg1/b256-ml0r后,移植了mc38细胞系的小鼠模型的肝脏中,t细胞活化程度的图。
[0681]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中颗粒酶b阳性t细胞的百分比。
[0682]
图74是示出了在移植了mc38细胞系的小鼠模型中,a551-mb110/b379-ml0r的抗肿瘤作用的图。
[0683]
图75是示出了在施用ns1-migg1或a551-mb110/b379-ml0r后,移植了mc38细胞系的小鼠模型中器官的重量的图。
[0684]
子图(a)示出淋巴结重量,子图(b)示出脾脏重量。
[0685]
图76是示出了在施用ns1-migg1或a551-mb110/b379-ml0r后,移植了mc38细胞系的小鼠模型的脾脏中,t细胞活化程度的图。
[0686]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中icos阳性t细胞的百分比,子图(c)示出cd8阳性t细胞中颗粒酶b阳性t细胞的百分比。
[0687]
图77是示出了在施用ns1-migg1或a551-mb110/b379-ml0r后,移植了mc38细胞系的小鼠模型的肝脏中,t细胞活化程度的图。
[0688]
子图(a)示出cd8阳性t细胞中pd-1阳性t细胞的百分比,子图(c)示出cd8阳性t细胞中icos阳性t细胞的百分比,子图(b)示出cd8阳性t细胞中颗粒酶b阳性t细胞的百分比。
[0689]
x轴示出抗体浓度(μg/ml),y轴示出相对光单位。
[0690]
图78是示出在存在或不存在小分子化合物(atp或adp)时使用4-1bb jurkat细胞测试的各种抗cd137抗体的激动剂活性的图。
[0691]
x轴示出抗体浓度(μg/ml),y轴示出相对光单位。
[0692]
图79是示出在存在atp的情况下使用4-1bb jurkat报告基因测定法测试的各种转换抗cd137抗体的激动剂活性的图。
[0693]
图80是示出每种抗cd137转换抗体a375-scf041aph/b167-lamlib和a375-my201aph/b167-lamlib的血浆动力学比较的图。图的纵轴示出每种抗体的血浆浓度。
[0694]
图81是示出在通过将llc1/ova/gpc3细胞系移植到hcd137ki/mfcγr2bko/hfcγr2btg#90小鼠中制备的小鼠模型中,a375/b167-scf041aph和a375/b167-my201aph各自的抗肿瘤作用的图。
[0695]
每个点示出一组(n=5)肿瘤体积的平均值。
[0696]
图82显示了向移植有mc38细胞的小鼠模型施用a551-mb110/b379-ml0r、抗小鼠pd-l1抗体或其组合后肿瘤组织中cd8
+
细胞的数量。
[0697]
图83显示了向移植有mc38细胞的小鼠模型施用a551-mb110/b379-ml0r、抗小鼠pd-l1抗体或其组合后肿瘤组织中pd-l1
+
细胞的数量。
[0698]
图84显示了向移植有mc38细胞的小鼠模型施用a551-mb110/b379-ml0r、抗小鼠pd-l1抗体或其组合后肿瘤组织中pd-l1中或高表达的细胞的数量。
[0699]
图85显示了通过单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),在移植了mc38细胞的小鼠模型中的肿瘤生长抑制效果。
[0700]
图86显示了由于单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),在移植了mc38细胞的小鼠模型中的血液参数(白细胞浓度、血小板浓度和淋巴细胞浓度)的波动程度。
[0701]
图87显示了在单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,在移植了mc38细胞的小鼠模型中的脾脏和肿瘤引流淋巴结(dln)的器官重量。
[0702]
图88显示了在单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,在移植了mc38细胞的小鼠模型的脾脏中,klrg-1、icos、pd-1、lag-3在cd8
+ t细胞中的表达比率和foxp3
+
调节性t细胞在cd4
+ t细胞中的比率。
[0703]
图89显示了在单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,移植了mc38细胞的小鼠模型的脾脏中的cd45
+
白细胞中的各活化标志物阳性cd8+ t细胞的比率和cd45
+
白细胞中foxp3
+
调节性t细胞的比率。
[0704]
图90显示了在单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,在移植了mc38细胞的小鼠模型的肿瘤引流淋巴结(dln)中,klrg-1、icos、pd-1和lag-3在cd8
+ t细胞中的表达比率和foxp3
+
调节性t细胞在cd4
+ t细胞中的比率。
[0705]
图91显示了在单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,在移植了mc38细胞的小鼠模型的肿瘤引流淋巴结(dln)中,各活化标志物阳性cd8
+ t细胞的绝对数量和cd4
+ t细胞中foxp3
+
调节性t细胞的绝对数量。
mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,在移植了llc1/ova细胞的小鼠模型的肿瘤引流淋巴结(dln)中的cd8
+ t细胞中klrg-1、icos和pd-1的表达率。
[0719]
图103显示了在单独施用a551-mb110/b379-ml0r(“sta-mb”),ureh-mb110/urel-mk1(“ure-mb”)或抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用a551-mb110/b379-ml0r(“sta-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”),或组合施用ureh-mb110/urel-mk1(“ure-mb”)和抗小鼠pd-l1抗体(“pd-l1-ab”)之后,在移植了llc1/ova细胞的小鼠模型的肿瘤引流淋巴结(dln)中的各活化标志物阳性cd8
+ t细胞的绝对数量。
[0720]
图104显示了通过单独施用a551-mb110/b379-ml0r(“sta-mb”),在移植有llc1/ova细胞的小鼠模型中的肿瘤生长抑制效果。
[0721]
图105显示通过单独施用转换抗cd137抗体a551-mb110/b379-ml0r或抗tigit抗体,或转换抗cd137抗体a551-mb110/b379-ml0r和抗tigit抗体的组合,在移植了小鼠aml c1498细胞系的小鼠模型中的肿瘤生长抑制效果。
[0722]
图106显示了转换抗cd137抗体a551-mb110/b379-ml0r在移植了mc38-hgpc3#g64b2m ko克隆5细胞系的小鼠模型中的抗肿瘤作用。
[具体实施方式]
[0723]
i.定义
[0724]
术语“结合活性”是指分子(例如,抗体)的一个或多个结合位点与其结合伴侣(例如,抗原)之间的非共价相互作用的总和的强度。在本文中,“结合活性”不严格限于结合对的成员(例如抗体和抗原)之间的1:1相互作用。例如,当结合对的成员反映单价1:1相互作用时,结合活性特别称为内在结合亲和力(亲和力)。当结合对的成员既能单价结合又能多价结合时,结合活性是每种结合强度的总和。分子x对其伴侣y的结合活性通常可以用解离常数(kd)或“每单位配体量的分析物的结合量”(以下称为“结合量”)表示。本领域技术人员将理解,通常,解离常数(kd)越低意味着结合活性越高,“每单位配体量的分析物结合量”或“结合量”的值越高意味着结合活性越高。结合活性可以通过本领域已知的常规方法,包括本文所述的那些方法来测量。下面描述了用于测量结合活性的具体说明性和示例性实施方案。
[0725]“结合活性成熟的”抗原结合分子或抗体,或“结合活性增加(增强)的”抗原结合分子或抗体是指与不带有改变的亲本抗原结合分子或亲本抗体相比,一个或多个高变区(hvr)具有一个或多个改变的抗体,这种改变导致抗原结合分子或抗体对抗原的结合活性的提高。
[0726]
术语“抗cd137抗原结合分子”或“抗cd137抗体”和“与cd137结合的抗原结合分子”或“与cd137结合的抗体”是指能够以足够的结合活性结合cd137的抗原结合分子或抗体,使得抗原结合分子或抗体可用作靶向cd137的诊断剂和/或治疗剂。在某些实施方案中,抗cd137抗体结合在不同物种的cd137之间保守的cd137表位。
[0727]
术语“具有依赖于小分子化合物的cd137结合活性”的抗cd137抗原结合分子或抗cd137抗体是指与在不存在小分子化合物时对cd137的结合活性相比,在小分子化合物存在
下对cd137具有更高结合活性的抗原结合分子或抗体。在一个实施方案中,“小分子化合物的存在”是指其中小分子化合物以10微摩尔或更高、50微摩尔或更高、100微摩尔或更高、150微摩尔或更高、200微摩尔或更高、或250微摩尔或更高的浓度存在的条件。在一个实施方案中,在小分子化合物存在下,抗cd137抗原结合分子或抗体对不相关的非cd137蛋白的结合活性的程度小于抗原结合分子或抗体对cd137的结合的约10%,例如如通过放射免疫分析(ria)或表面等离振子共振(spr)所测量的。在某些实施方案中,在低分子量化合物存在下,抗cd137抗原结合分子或抗体的解离常数(kd)为1μm以下、100nm以下、10nm以下、1nm以下、0.1nm以下、0.01nm以下或0.001nm以下(例如10-6
m以下、10-7
m以下、10-8
m以下、10-9
m以下、10-10
m以下,例如10-6
m至10-10
m、10-7
m至10-9
m,例如10-7
m至10-8
m)。
[0728]
在本文中,术语“抗原结合分子”以其最广义使用,指的是与抗原决定簇特异性结合的分子。在一个实施方案中,抗原结合分子是抗体,抗体片段或抗体衍生物。
[0729]
如本文所使用的,“激动性抗原结合分子”或“激动性抗体”是显著诱导或增强其所结合的抗原(例如,cd137和cd3)的生物学活性的抗原结合分子或抗体。
[0730]
因此,如果抗原是例如cd137,则将具有激动作用的这种抗原结合分子或抗体分别称为“cd137激动性抗原结合分子”或“cd137激动性抗体”。以相同的方式,如果抗原是例如cd3,则将具有激动作用的这种抗原结合分子或抗体分别称为“cd3激动性抗原结合分子”或“cd3激动性抗体”。
[0731]
本文中的术语“抗体”以最广义使用,并且涵盖各种抗体结构,包括但不限于单克隆抗体、多克隆抗体、多特异性抗体(例如,双特异性抗体)和抗体片段,只要它们表现出所需的抗原-结合活性即可。
[0732]“抗体片段”是指除完整抗体以外的分子,其包含完整抗体的部分,所述部分结合完整抗体所结合的抗原。抗体片段的实例包括但不限于fv、fab、fab’、fab
’‑
sh、f(ab’)2;双抗体、线性抗体、单链抗体分子(例如scfv)、由抗体片段形成的多特异性抗体。
[0733]
与参照抗原结合分子或参照抗体的“相同表位结合的抗原结合分子”或“相同表位结合的抗体”是指这样的抗体或抗原结合分子:在竞争测定法中,阻断参照抗体或参照抗原结合分子与其抗原的结合50%或更高,并且相反,在竞争测定法中,参照抗体将抗体与其抗原的结合阻断50%或更高。本文提供了示例性竞争测定法。在一个实施方案中,在参照抗原结合分子或参照抗体示出以依赖于低分子量化合物的方式的抗原结合活性的情况下,在低分子量化合物的存在下进行竞争测定。
[0734]
术语“嵌合”抗体是指这样的抗体,其中重链和/或轻链的一部分衍生自特定来源或物种,而重链和/或轻链的其余部分衍生自不同来源或物种。
[0735]
抗体的“类别”是指其重链所具有的恒定结构域或恒定区的类型。抗体主要分为五类:iga、igd、ige、igg和igm,其中一些可以进一步分为亚类(亚型),例如igg1、igg2、igg3、igg4、iga1和iga2。对应于不同类别的免疫球蛋白的重链恒定结构域分别称为α、δ、ε、γ和μ。
[0736]“效应子功能”是指归因于抗体的fc区的那些生物学活性,其随抗体同种型而变化。抗体效应子功能的例子包括:c1q结合和补体依赖性细胞毒性(cdc);fc受体结合;抗体依赖性细胞介导的细胞毒性(adcc);吞噬作用;细胞表面受体(例如b细胞受体)的下调;和b细胞活化。
[0737]“细胞毒性”是指抑制或阻止细胞功能和/或引起细胞死亡或破坏的活性。细胞毒
性可以是例如抗体依赖性细胞介导的细胞毒性(adcc)活性、补体依赖性细胞毒性(cdc)活性和t细胞的细胞毒性;可能是由细胞毒性剂(例如,放射性同位素和化学治疗剂)(例如免疫缀合物)引起的细胞毒性。
[0738]
本文中的术语“fc区”用于定义包含至少一部分恒定区的免疫球蛋白重链的c末端区域。该术语包括天然序列fc区和变体fc区。在一个实施方案中,人igg重链fc区从cys226或从pro230延伸至重链的羧基末端。然而,fc区的c-末端赖氨酸(lys447)或甘氨酸-赖氨酸(残基446-447)可以存在或不存在。除非本文另有说明,否则fc区或恒定区中氨基酸残基的编号是根据eu编号系统(也称为eu索引)进行的,如在kabat等,sequences of proteins of immunological interest,第5版.public health service,national institutes of health,bethesda,md,1991中所述。
[0739]
本文中的术语“变体fc区”包含由于至少一个氨基酸修饰,优选一个或多个氨基酸置换而不同于天然序列fc区的氨基酸序列。优选地,与天然序列fc区或亲本多肽的fc区相比,变体fc区具有至少一个氨基酸置换,例如,天然序列fc区或亲本多肽的fc区中约1个至约10个氨基酸置换,优选约1个至约5个氨基酸置换。本文的变体fc区优选与天然序列fc区和/或与亲本多肽的fc区具有至少约80%的同源性,最优选与其具有至少约90%的同源性,更优选至少约95%的同源性。
[0740]
在本文中,可以通过eu编号系统和氨基酸的组合来表示fc区域或恒定区域内的氨基酸改变或置换。例如,s424n代表eu编号中424位从丝氨酸(ser)到天冬酰胺(asn)的置换。eu424n代表eu编号中424位从氨基酸(任何类型)到天冬酰胺(asn)的置换。
[0741]
本文中的术语“包含fc区的抗体”是指抗体,其包含fc区。fc区的c末端赖氨酸(根据eu编号系统的残基447)或c末端甘氨酸赖氨酸(446-447的残基)可以例如在抗体的纯化过程中或通过将编码抗体的核酸进行重组工程化改造来除去。因此,包含具有根据本公开的fc区的抗体的组合物可以包含具有g446-k447的抗体、具有g446和不具有k447的抗体、去除了所有g446-k447的抗体,或上述三种类型的抗体的混合物。
[0742]
术语“全长抗体”,“完整抗体”和“整个抗体”在本文中可互换使用,是指具有与天然抗体结构基本相似的结构或具有包含如本文所定义的fc区或变体fc区的重链的抗体。
[0743]“人抗体”指具有这样的氨基酸序列的抗体,所述氨基酸序列对应于由人或人细胞生成或来源于利用人抗体库或其它人抗体编码序列的非人来源的抗体的氨基酸序列。人抗体的这种定义特别排除了包含非人抗原结合残基的人源化抗体。
[0744]“框架”或“fr”是指除高变区(hvr)残基之外的可变结构域残基。可变结构域的fr通常由四个fr结构域组成:fr1、fr2、fr3和fr4。因此,hvr和fr序列通常以以下顺序出现在vh(或vl)中:fr1-h1(l1)-fr2-h2(l2)-fr3-h3(l3)-fr4,
[0745]
出于本文目的,“受体人框架”是如下定义的包含衍生自人免疫球蛋白框架或人共有框架的轻链可变结构域(vl)框架或重链可变结构域(vh)框架的氨基酸序列的框架。“源自”人免疫球蛋白框架或人共有框架的受体人框架可包含其相同的氨基酸序列,或可包含氨基酸序列变化。在一些实施方案中,氨基酸变化的数目为10或更少,9或更少,8或更少,7或更少,6或更少,5或更少,4或更少,3或更少,或2或更少。在一些实施方案中,vl受体人框架序列与vl人免疫球蛋白框架序列或人共有框架序列序列相同。
[0746]“人共有框架”是代表在人免疫球蛋白vl框架序列或vh框架序列选择中最常见的
氨基酸残基的框架。通常,人免疫球蛋白vl序列或vh序列的选择来自可变结构域序列的亚组。通常,序列亚组是如kabat等人,sequences of proteins of immunological interest,第五版,nih出版物91-3242,bethesda md(1991),卷1-3中的亚组。在一个实施方案中,对于vl,亚组是如上文kabat等中的κi亚组。在一个实施方案中,对于vh,亚组是如上文kabat等所述的亚组iii。
[0747]“人源化”抗体是指包含来自非人hvr的氨基酸残基和来自人fr的氨基酸残基的嵌合抗体。在某些实施方案中,人源化抗体将包含至少一个且通常是两个可变结构域的基本上所有,其中所有或基本上所有的hvr(例如cdr)对应于非人抗体的那些,并且所有或基本上所有的fr都对应于人抗体的那些。人源化抗体可任选地包含源自人抗体的抗体恒定区的至少一部分。抗体例如非人抗体的“人源化形式”是指已经历人源化的抗体。
[0748]
术语“可变区”或“可变结构域”是指参与抗体与抗原结合的抗体重链或轻链的结构域。天然抗体的重链和轻链的可变结构域(分别为vh和vl)通常具有相似的结构,其中每个结构域包含四个保守构架区(fr)和三个高变区(hvr)。(参见,例如,kindt等,kuby immunology,第6版,w.h.freeman和co.,第91页(2007))。单个vh或vl结构域可足以赋予抗原结合特异性。此外,结合特定抗原的抗体可以使用vh或vl结构域从结合抗原的抗体分离,以分别筛选互补的vl或vh结构域的文库。参见例如portolano等,j.immunol.(免疫学杂志).150:880-887(1993);clarkson等,nature 352:624-628(1991)。
[0749]
如本文所使用的,术语“高变区”或“hvr”是指抗体可变结构域中序列上高变(“互补决定区”或“cdr”)和/或形成结构上限定的环(“高变环”)和/或包含抗原接触残基(“抗原接触”)的每个区域。通常,抗体包含六个hvr:vh中三个(h1、h2、h3)和vl中三个(l1、l2、l3)。本文中的示例性hvr包括:
[0750]
(a)氨基酸残基26-32(l1)、50-52(l2)、91-96(l3)、26-32(h1)、53-55(h2)和96-101(h3)处的高变环(chothia和lesk,j.mol.biol.(分子生物学杂志)196:901-917(1987));
[0751]
(b)氨基酸残基24-34(l1)、50-56(l2)、89-97(l3)、31-35b(h1)、50-65(h2)和95-102(h3)处的cdr(kabat等,《免疫学意义的蛋白质序列》,第五版,国家卫生研究院公共卫生服务,马萨诸塞州贝塞斯达市,(1991));
[0752]
(c)氨基酸残基27c-36(l1)、46-55(l2)、89-96(l3)、30-35b(h1)、47-58(h2)和93-101(h3)处的抗原接触(maccallum等,j.mol.biol.(分子生物学杂志)262:732-745(1996));和
[0753]
(d)(a),(b)和/或(c)的组合,包括hvr氨基酸残基46-56(l2)、47-56(l2)、48-56(l2)、49-56(l2)、26-35(h1)、26-35b(h1)、49-65(h2)、93-102(h3)和94-102(h3)。
[0754]
除非另有说明,否则可变结构域中的hvr残基和其他残基(例如fr残基)在本文中根据如上kabat等进行编号。本文中,可变结构域内的hvr残基或其他残基(例如fr残基)以及在这些残基处的氨基酸改变或置换可以通过kabat编号系统和氨基酸的组合来表示。例如,n99代表在kabat编号中第99位的天冬酰胺(asn),而n99a代表在kabat编号中99位从天冬酰胺(asn)到丙氨酸(ala)的置换。
[0755]“免疫缀合物”是缀合至一个或多个异源分子的抗体,包括但不限于细胞毒性剂。
[0756]
如本文所使用的,术语“细胞毒性剂”是指抑制或阻止细胞功能和/或引起细胞死
亡或破坏的物质。细胞毒性剂包括但不限于放射性同位素(例如
211
at,
131
i,
125
i,
90
y,
186
re,
188
re,
153
sm,
212
bi,
32
p,
212
pb和lu的放射性同位素);化学治疗剂或药物(例如甲氨蝶呤,阿霉素(adriamycin),长春花生物碱(长春新碱,长春碱,依托泊苷),阿霉素(doxorubicin),美法仑,丝裂霉素c,苯丁酸氮芥,道诺霉素或其他嵌入剂);生长抑制剂;酶及其片段,例如溶核酶;抗生素;毒素,例如细菌、真菌、植物或动物来源的小分子毒素或酶活性毒素,包括其片段和/或变体;以及以下公开的各种抗肿瘤剂或抗癌剂。
[0757]“分离的”抗体是已经从其自然环境的组分中分离出来的抗体。在一些实施方案中,将抗体纯化至大于95%或99%的纯度,所述纯度例如通过电泳(例如,sds-page,等电聚焦(ief),毛细管电泳)或色谱法(例如,离子交换或反相hplc)所确定的。对于评估抗体纯度的方法的综述,参见例如flatman等,j.chromatogr.b 848:79-87(2007)。
[0758]“分离的”核酸是指已经与其天然环境的组分分离的核酸分子。分离的核酸包括在通常包含所述核酸分子的细胞中所含的核酸分子,但是该核酸分子存在于染色体外或在不同于其天然染色体位置的染色体位置。
[0759]
如本文所使用的,术语“载体”是指能够繁殖与其连接的另一核酸的核酸分子。该术语包括作为自我复制核酸结构的载体,以及整合入已引入其的宿主细胞基因组中的载体。某些载体能够指导与其可操作地连接的核酸的表达。此类载体在本文中称为“表达载体”。
[0760]“编码抗cd137抗原结合分子的编码核酸”是指编码构成抗原结合分子的多肽的一个或多个核酸分子。“编码抗cd137抗体的分离的核酸”是指编码抗体重链和轻链(或其片段)的一个或多个核酸分子,包括在单个载体或单独载体中的此类核酸分子,以及存在于宿主细胞中一个或多个位置的此类核酸分子。
[0761]
术语“宿主细胞”、“宿主细胞系”和“宿主细胞培养物”可互换使用,是指已引入外源核酸的细胞,包括此类细胞的后代。宿主细胞包括“转化体”和“转化细胞”,其包括原代转化细胞和从其衍生的后代,而与传代次数无关。后代的核酸含量可能与亲代细胞不完全相同,但可能含有突变。与在原始转化细胞中筛选或选择的具有相同功能或生物学活性的突变后代包括在本文中。
[0762]
如本文所使用的,术语“单克隆抗体”是指从基本上均质的抗体群体中获得的抗体,即,组成该群体的各个抗体是相同的和/或结合相同的表位,除了可能的变体抗体,例如含有天然发生的突变的变体抗体或在单克隆抗体制剂的生产过程中出现的变体抗体,这种变体通常以少量存在。与通常包括针对不同决定簇(表位)的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂的每种单克隆抗体都针对抗原上的单个决定簇。因此,修饰语“单克隆”表示抗体的特征是从基本上同质的抗体群体中获得的,并且不应解释为要求通过任何特定方法来生产抗体。例如,可以通过多种技术制备根据本公开使用的单克隆抗体,所述技术包括但不限于杂交瘤方法、重组dna方法、噬菌体展示方法以及利用包含全部或部分人免疫球蛋白基因座的转基因动物的方法,本文描述了制备单克隆抗体的此类方法和其他示例性方法。
[0763]“裸抗体”是指未与异源部分(例如,细胞毒性部分)或放射性标记缀合的抗体。裸抗体可以存在于药物制剂中。
[0764]“天然抗体”指具有不同结构的天然存在的免疫球蛋白分子。例如,天然igg抗体是
约150,000道尔顿的异四聚体糖蛋白,由二硫键结合的两条相同的轻链和两条相同的重链组成。从n末端到c末端,每条重链都有可变区(vh),也称为可变重链结构域或重链可变结构域,随后是三个恒定结构域(ch1、ch2和ch3)。同样,从n末端到c末端,每个轻链都有可变区(vl),也称为可变轻链结构域或轻链可变结构域,随后是恒定轻链结构(cl)结构域。抗体的轻链可根据其恒定结构域的氨基酸序列分配给两种类型之一,称为kappa(κ)和lambda(λ)。
[0765]
相对于参考多肽序列的“氨基酸序列同一性百分比(%)”定义为在将序列进行比对并引入空位(如果需要的话)以实现最大百分比序列同一性并且不将任何保守置换视为序列同一性的一部分之后,候选序列中与参考多肽序列中的氨基酸残基相同的氨基酸残基的百分比。可以通过本领域技术范围内的各种方式实现比对,以确定氨基酸序列同一性的百分比,例如,使用诸如blast、blast-2、align、megalign(dnastar)软件或genetyx(注册商标)(genetyx有限公司)之类的公共计算机软件。本领域技术人员可以确定适当的参数用于比对序列,包括在所比较序列的全长上实现最大比对所需的任何算法。
[0766]
align-2序列比较计算机程序由基因泰克公司(genentech,inc.)编写,源代码已与用户文档一起递交至20559华盛顿特区的美国版权局中,并在美国版权注册号txu510087中进行了注册。align-2程序可从加利福尼亚南旧金山的基因泰克公司公开获得,也可以从源代码中进行编译。align-2程序应编译为在unix操作系统(包括digital unix v4.0d)上使用。所有序列比较参数均由align-2程序设置,并且没有变化。在使用align-2进行氨基酸序列比较的情况下,给定氨基酸序列a与、和或针对给定氨基酸序列b的氨基酸序列同一性%(可以用短语表示为给定氨基酸序列a与、和或针对给定氨基酸序列b具有或包含一定的氨基酸序列同一性%)计算如下:
[0767]
100乘以分数x/y
[0768]
其中,x是序列比对程序align-2在该程序对a和b的比对中被评为相同匹配的氨基酸残基数,其中y是b中氨基酸残基的总数。应当理解,如果氨基酸序列a的长度与氨基酸序列b的长度不同,则a与b的氨基酸序列同一性%将不等于b与a的氨基酸序列同一性%。除非另有特别说明,否则如本文所使用的所有氨基酸序列同一性%值如前一段落所述,使用align-2计算机程序获得。
[0769]
术语“药物制剂”是指这样的制剂,其形式为允许其中所含活性成分的生物学活性有效,并且不包含对于该制剂所施用的受试者具有不可接受的毒性的其他组分。
[0770]“药学上可接受的载体”是指药物制剂中除活性成分之外对受试者无毒的成分。药学上可接受的载体包括但不限于缓冲剂、辅料、稳定剂或防腐剂。
[0771]
试剂例如药物制剂的“有效量”是指在所需剂量和时间段内有效实现所需治疗或预防结果的量。
[0772]“个体”或“受试者”是哺乳动物。哺乳动物包括但不限于家养动物(例如牛,绵羊,猫,狗和马),灵长类动物(例如人和非人类灵长类动物,例如猴子),兔子和啮齿动物(例如小鼠和大鼠)。在某些实施方案中,个体或受试者是人。
[0773]
除非另有说明,否则本文所使用的术语“cd137”是指来自任何脊椎动物来源(包括哺乳动物,例如灵长类动物(例如人)和啮齿动物(例如小鼠和大鼠))的任何天然cd137。该术语涵盖“全长”未处理的cd137以及由于在细胞中加工而产生的任何形式的cd137。该术语还涵盖cd137的天然存在的变体,例如剪接变体或等位基因变体。
[0774]
示例性的人全长cd137的氨基酸序列示于seq id no:1(ncbi参考序列:np_001552.2),示例性的人cd137胞外区的氨基酸序列示于seq id no:2。示例性的小鼠全长cd137的氨基酸序列示于seq id no:3(ncbi参考序列:np_035742.1),示例性的小鼠cd137胞外区的氨基酸序列示于seq id no:4。示例性猴子全长cd137的氨基酸序列示于seq id no:5(ncbi参考序列:aby47575.1),示例性猴子cd137胞外区的氨基酸序列示于seq id no:6。
[0775]
cd137是肿瘤坏死因子(tnf)受体家族的成员。它的替代名称是肿瘤坏死因子受体超家族成员9(tnfrsf9)、4-1bb和ila。除了在激活的cd4
+
t细胞和cd8
+ t细胞上表达外,cd137还可以在b细胞、树突细胞、天然杀伤(nk)和nk-t细胞、巨噬细胞、单核细胞、嗜中性粒细胞、cd4
+
cd25
+
调节性t细胞和血管内皮细胞中表达。还报道了在癌细胞中的表达(labiano等,肿瘤免疫学(oncoimmunology),第24卷:e1062967(2015))。天然cd137配体cd137l由抗原呈递细胞(例如b细胞、单核细胞/巨噬细胞和树突细胞)呈递(watts等,免疫学年度综述(annu.rev.immunol.),第23卷:23-68页(2005))。通过与配体的相互作用,cd137导致tcr诱导的t细胞增殖的增加、细胞因子生成、功能成熟、细胞凋亡抑制以及cd8
+ t细胞的长期存活(nam等,癌症药靶研究最新进展(curr.cancer drug targets),第5卷:第357-363页(2005);watts等,免疫学年度综述(annu.rev.immunol.),第23卷:第23-68页(2005))。
[0776]
术语“调节性t细胞”或“treg细胞”是负责免疫反应的抑制性调节(免疫耐受)的t细胞。在一个实施方案中,调节性t细胞是cd4
+
和/或cd25
+ t细胞。
[0777]
术语“癌”、“癌症”和“癌性”是指或描述哺乳动物中通常以细胞生长/增殖失控为特征的生理状况。
[0778]
术语“肿瘤”是指所有赘生性细胞生长和增殖,无论是恶性还是良性,以及所有癌前和癌性细胞和组织。术语“癌”、“癌症”、“癌性”、“细胞增殖性疾病”、“增殖性疾病”和“肿瘤”在本文中并不互相排斥。
[0779]
术语“细胞增殖性疾病”和“增殖性疾病”是指与某种程度的异常细胞增殖相关的疾病。在一个实施方案中,细胞增殖性疾病是癌症。
[0780]
如本文使用的,“治疗(treatment)”(及其语法变化,例如“治疗(treat)”或“治疗(treating)”)是指试图改变被治疗个体的自然病程的临床干预,并且可以用于预防或在临床病理过程期间进行。理想的治疗效果包括但不限于预防疾病的发生或复发、减轻症状、减少疾病的任何直接或间接病理后果、预防转移、降低疾病进展的速度、缓解或减轻疾病的状态、缓解或改善预后。在一些实施方案中,本公开的抗体用于延迟疾病的发作或减慢疾病的进展。
[0781]
ii.组合物和方法(抗cd137激动性抗原结合分子)
[0782]
一方面,本发明部分基于抗cd137激动性抗原结合分子及其用途。在某些实施方案中,提供了结合cd137的抗体。本公开中的抗体可表现出对免疫细胞的激活作用、细胞毒性或抗肿瘤活性,因此可用于例如诊断或治疗癌症。
[0783]
a.示例性的抗cd137抗原结合分子或抗体
[0784]
一方面,本公开提供了分离的结合cd137的抗原结合分子或抗体。在某些实施方案中,抗cd137抗原结合分子或抗体
[0785]-具有依赖于小分子化合物的cd137结合活性;
[0786]-结合至cd137的胞外区;
[0787]-与低分子量化合物和cd137形成三元复合物;
[0788]-结合人源性cd137和猴源性cd137;
[0789]-对cd137活性有激动作用;
[0790]-在低分子量化合物存在下对cd137示出激动活性;
[0791]-在不存在低分子量化合物时对cd137具有低激动活性;和/或
[0792]-在不存在低分子量化合物时,基本上不表现出对cd137的激动活性。
[0793]
[抗原结合分子或抗体的结合活性]
[0794]
在某些实施方案中,在低分子量化合物存在下,本文提供的抗原结合分子或抗体的结合活性的解离常数(kd)为1μm以下,100nm以下,10nm以下,1nm以下,0.1nm以下,0.01nm以下或0.001nm以下(例如10-6
m以下,10-7
m以下,10-8
m以下,10-9
m以下,10-10
m以下,例如10-6
m至10-10
m,10-7
m至10-9
m,例如10-7
m至10-8
m)。
[0795]
在一个实施方案中,抗原结合分子或抗体的结合活性通过放射性标记的抗原结合测定法(ria)来测量并且由kd表示。在一个实施方案中,用感兴趣的抗体及其抗原的fab形式进行放射性标记的抗原结合测定法。例如,通过在一系列未标记的抗原滴定液存在下用最小浓度的(
125
i)标记抗原平衡fab,然后用抗fab抗体包被的板捕获结合的抗原,来测量fab对抗原的溶液结合亲和力(参见,例如,chen等,分子生物学杂志(j.mol.biol.),293:865-881(1999))。为了建立测定条件,将microtiter(注册商标)多孔板(thermo scientific)用在50mm碳酸钠(ph 9.6)中的5μg/ml捕获抗fab抗体(cappel labs)包被过夜。随后在室温下(约23摄氏度)用pbs中的2%(w/v)牛血清白蛋白封闭2至5小时。在非吸附板(nunc#269620)中,将100pm或26pm[
125
i]抗原与感兴趣的fab的系列稀释液混合(例如,与抗vegf抗体fab-12的评估相一致,presta等,癌症研究(cancer res.),57:4593-4599(1997)。然后将感兴趣的fab孵育过夜。然而,孵育可以持续更长的时间(例如约65小时)以确保达到平衡。此后,将混合物转移至捕获板,以在室温下孵育(例如,一小时)。然后除去溶液,并用pbs中的0.1%聚山梨醇酯20(吐温20(注册商标))洗涤板八次。当板干燥后,加入150微升/孔的闪烁剂(microscint-20
tm
;packard),并将板在topcount
tm
伽玛计数器(packard)上计数十分钟。选择产生小于或等于最大结合的20%的每个fab的浓度用于竞争性结合测定。
[0796]
在一个实施方案中,为了测量抗体的结合活性,使用配体捕获方法,例如,使用biacore(注册商标)t200或biacore(注册商标)4000(ge医疗(ge healthcare),瑞典乌普萨拉),其依赖于表面等离振子共振分析方法作为测量原理。biacore(注册商标)控制软件用于设备的操作。在一个实施方案中,根据制造商的说明书使用胺偶联试剂盒(ge医疗),瑞典乌普萨拉)来使用于配体捕获的分子例如抗标签抗体、抗igg抗体、蛋白a等固定在涂有羧甲基葡聚糖的传感器芯片(ge医疗),瑞典乌普萨拉)上。捕获配体的分子在适当的ph值用10mm乙酸钠溶液稀释,并以适当的流速和适当的注入时间注入。使用含0.05%聚山梨醇酯20(即吐温(注册商标)-20)的缓冲液作为测量缓冲液,以10-30微升/分钟的流速,并在优选的25℃或37℃测量温度下测量结合活性。对于用被配体捕获分子捕获的抗体作为配体进行的测量,注入抗体以使目标量的抗体被捕获,然后注入用测量缓冲液制备的抗原和/或fc受体(分析物)的系列稀释液。对于用被配体捕获分子捕获的抗原和/或fc受体作为配体进行的
测量,注入抗原和/或fc受体以使其目标量被捕获,然后注入用测量缓冲液制备的抗体(分析物)的系列稀释液。
[0797]
在一个实施方案中,使用biacore(注册商标)评估软件来分析测量结果。通过使用1:1结合模型同时拟合缔合和解离的传感图,进行动力学参数计算,计算缔合速率(kon或ka)、解离速率(koff或kd)和平衡解离常数(kd)。对于弱结合活性的情况,特别是对于解离快且动力学参数难以计算的情况,可以使用稳态模型来计算平衡解离常数(kd)。作为关于结合活性的附加参数,可以通过将特定浓度下的分析物的结合量(共振单位:ru)除以捕获的配体的量来计算“每单位配体量的分析物的结合量”。
[0798]
[小分子化合物依赖性结合活性]
[0799]
一方面,抗cd137抗原结合分子或抗体具有小分子化合物依赖性cd137结合活性。在一个非限制性实施方案中,与在不存在小分子化合物的情况下对cd137的结合活性相比,在存在小分子化合物的情况下,抗cd137抗原结合分子或抗体对cd137具有更高的结合活性。在不同的实施方案中,与在低浓度的小分子化合物存在下的cd137结合活性相比,在高浓度的小分子化合物存在下,抗cd137抗原结合分子或抗体对cd137具有更高的结合活性。在一个优选的实施方案中,在小分子化合物存在下,抗cd137抗原结合分子或抗体对cd137的结合活性是不存在小分子化合物的情况下的结合活性的2倍以上,3倍以上,5倍以上,10倍以上,15倍以上,20倍以上,25倍以上,30倍以上,50倍以上,100倍以上,200倍以上,300倍以上,500倍以上,1x103倍以上,2x103倍以上,3x103倍以上,5x103倍以上,1x104倍以上,2x104倍以上,3x104倍以上,5x104倍以上或1x105倍以上。在不同的优选实施方案中,在小分子化合物存在下,抗cd137抗原结合分子或抗体对cd137的结合活性是在不存在小分子化合物的情况下的结合活性的2倍高,3倍高,5倍高,10倍高,15倍高,20倍高,25倍高,30倍高,50倍高,100倍高,200倍高,300倍高,500倍高,1x103倍高,2x103倍高,3x103倍高,5x103倍高,1x104倍高,2
×
104倍高,3
×
104倍高,5
×
104倍高或1
×
105倍高。
[0800]
小分子化合物的浓度可以是任意浓度,只要检测到抗cd137抗原结合分子或抗体的结合活性的差异即可。在一个实施方案中,“在存在小分子化合物的情况下”和/或“在存在高浓度的小分子化合物的情况下”小分子化合物的浓度是例如100nm以上,500nm以上,1μm以上,3μm以上,5μm以上,10μm以上,50μm以上,100μm以上,150μm以上,200μm以上,250μm以上,300μm以上,400μm以上,500μm以上或1mm以上。或者,可以将浓度定义为足以使抗cd137抗原结合分子或抗体示出最大结合活性的量。此外,在一个实施方案中,“在低浓度的小分子化合物的存在下”小分子化合物的浓度可以例如是500μm以下,250μm以下,200μm以下,150μm以下,100μm以下,50μm以下,10μm以下,1μm以下,500nm以下,100nm以下,50nm以下或10nm或1nm以下。小分子化合物的浓度为零或基本浓度为零的情况也可以选择为低浓度的实施方案。
[0801]
在此,术语“基本浓度为零”是指,例如,即使存在小分子化合物,其浓度如此之小至于不能被当前技术检测到的浓度。
[0802]
在一个实施方案中,在浓度为10μm、50μm、100μm、150μm、200μm或250μm的小分子化合物存在下,对cd137的结合活性是不存在小分子化合物的情况下对cd137的结合活性的2倍以上,5倍以上,10倍以上,15倍以上,16倍以上,17倍以上,18倍以上,19倍以上,或20倍以上。在一个实施方案中,在小分子化合物以10μm以上存在的情况下,抗cd137抗原结合分子
或抗体对cd137的结合活性是不存在小分子化合物的情况下对cd137的结合活性的2倍以上,5倍以上,10倍以上,15倍以上,16倍以上,17倍以上,18倍以上,19倍以上,或20倍以上。在一个实施方案中,在小分子化合物以100μm以上存在的情况下,抗cd137抗原结合分子或抗体对cd137的结合活性是不存在小分子化合物的情况下对cd137的结合活性的2倍以上,5倍以上,10倍以上,15倍以上,16倍以上,17倍以上,18倍以上,19倍以上,或20倍以上。
[0803]
在一个实施方案中,在小分子化合物以10μm以上存在的情况下,抗cd137抗原结合分子或抗体对cd137的结合活性(kd)是9x10-7
m以下,8x10-7
m以下,7x10-7
m以下,6x10-7
m以下,5x10-7
m以下,或4x10-7
m以下的解离常数(kd),或优选地,5x10-7
m以下的解离常数(kd)。在另一个实施方案中,在不存在小分子化合物的情况下,抗cd137抗原结合分子或抗体对cd137的结合活性(kd)太大而无法由biacore计算(弱结合活性),或者是解离常数(kd)为1x10-7
m以上,5x10-7
m以上,7x10-7
m以上,8x10-7
m以上,9x10-7
m以上,1
×
10-6
m以上,2
×
10-6
m以上,3
×
10-6
m以上,或4
×
10-6
m以上,或优选地,解离常数(kd)为1x10-6
m以上。在另一个实施方案中,在小分子化合物以100μm以上存在时,抗cd137抗原结合分子或抗体对cd137的结合活性(kd)是9x10-7
m以下,8x10-7
m以下,7x10-7
m以下,6x10-7
m以下,5x10-7
m以下,4x10-7
m以下,3x10-7
m以下,2
×
10-7
m以下,或1
×
10-7
m以下,或优选地,解离常数(kd)为2
×
10-7
m以下。在另一个实施方案中,在不存在小分子化合物的情况下,抗cd137抗原结合分子或抗体对cd137的结合活性(kd)太大而无法由biacore计算(弱结合活性),或者解离常数(kd)为1x10-7
m以上,5x10-7
m以上,7x10-7
m以上,8x10-7
m以上,9x10-7
m以上,1x10-6
m以上,2x10-6
m以上,3x10-6
m以上,或4x10-6
m以上,或者优选地,解离常数(kd)为1x10-6
m以上。
[0804]
在一个实施方案中,在小分子化合物以10μm以上存在的情况下,抗cd137抗原结合分子或抗体对cd137的结合活性(kd)是8x10-8
m以下的解离常数(kd),并且在不存在化合物的情况下对cd137的结合活性(kd)太大,无法通过biacore进行计算(弱结合活性)。在另一个实施方案中,在小分子化合物以100μm存在的情况下,抗cd137抗原结合分子或抗体对cd137的结合活性(kd)是2x10-8
m以下的解离常数(kd),并且在不存在小分子化合物的情况下对cd137的结合活性太大,无法通过biacore进行计算(弱结合活性)。
[0805]
一方面,本公开提供了抗cd137抗原结合分子或抗体,其中[在低分子化合物以10μm以上存在的情况下对cd137的结合活性(结合量)]/[在不存在小分子化合物的情况下对cd137的结合活性(结合量)]的值等于或大于参考抗cd137抗原结合分子的值。在不同的方面,本公开提供了抗cd137抗原结合分子或抗体,其中[在低分子化合物以100μm以上存在的情况下对cd137的结合活性(结合量)]/[在不存在小分子化合物的情况下对cd137的结合活性(结合量)]的值等于或大于参考抗cd137抗原结合分子的值。在以上任何方面中,参考抗cd137抗原结合分子可以选自含有hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。
[0806]
在一个实施方案中,参考抗cd137抗原结合分子是包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167的氨基酸序列作为重链可变区/轻链
可变区组合的抗体。在不同的优选实施方案中,参考抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与a375/b167中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在另一个实施方案中,参考抗cd137抗原结合分子是包含a375/b167作为重链可变区/轻链可变区组合的抗cd137抗体。在不同的优选实施方案中,参考抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与a551/b379中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在另一个实施方案中,参考抗cd137抗原结合分子是包含a551/b379作为重链可变区/轻链可变区组合的抗cd137抗体。在优选的实施方案中,参考抗原结合分子包含人源的重链和轻链恒定区(例如,g1t3(seq id no:138)作为重链恒定区,人λ链lamlib(seq id no:63)作为轻链恒定区)。
[0807]
一方面,本公开提供了抗cd137抗原结合分子或抗体,其中在不存在小分子化合物的情况下,其对cd137的结合活性(结合量)与参考抗cd137抗原结合分子对cd137的结合活性(结合量)相同或更低,以及在10μm以上的小分子化合物存在下对cd137的结合活性(结合量)等于或高于在相同的条件下参考抗cd137抗原结合分子对cd137的结合活性(结合量)。在不同的方面,本公开提供了抗cd137抗原结合分子或抗体,其中在不存在小分子化合物的情况下对cd137的结合活性与参考抗cd137抗原结合分子对cd137的结合活性(结合量)相同或更低。并且,在10μm以上的小分子化合物存在下对cd137的结合活性(结合量)等于或高于在相同条件下参考抗cd137抗原结合分子对cd137的结合活性(结合量)。在以上任何方面中,参考抗cd137抗原结合分子可以选自包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167中所包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。
[0808]
在一个实施方案中,参考抗cd137抗原结合分子是抗cd137抗体,其包含在表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167的氨基酸序列作为重链可变区/轻链可变区组合。在优选实施方案中,参考抗cd137抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与a375/b167中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在另一个实施方案中,参考抗cd137抗原结合分子是包含a375/b167作为重链可变区/轻链可变区组合的抗cd137抗体。在不同的优选实施方案中,参考抗cd137抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与a551/b379中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在另一个实施方案中,参考抗cd137抗原结合分子是包含a551/b379作为重链可变区/轻链可变区组合的抗cd137抗体。在优选的实施方案中,参考抗原结合分子包含人源的重链恒定区和轻链恒定区(例如,g1t3(seq id no:138)作为重链恒定区,人λ链lamlib(seq id no:63)作为轻链恒定区)。
[0809]
在一个方面,本公开提供了抗cd137抗原结合分子或抗体,其中[在1μm低分子化合物存在下对cd137的结合活性(kd)]/[在10μm以上的低分子化合物存在下对cd137的结合活性(kd)]的值等于或大于参考抗原结合分子的值。在不同的方面,本公开提供了抗cd137抗原结合分子或抗体,其中[在1μm低分子化合物的存在下对cd137的结合活性(kd)]/[在100μm以上的低分子化合物存在下对cd137的结合活性(kd)]的值等于或大于参考抗原结合分子的值。在以上任何方面中,参考抗原结合分子可选自包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与表37中列出的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167中所包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。
[0810]
在一个实施方案中,参考抗原结合分子是包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167的氨基酸序列作为重链可变区/轻链可变区组合的抗体。在优选的实施方案中,参考抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的氨基酸序列与a375/b167中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的氨基酸序列相同。在另一个实施方案中,参考抗原结合分子是包含a375/b167作为重链可变区/轻链可变区组合的抗体。在不同的实施方案中,参考抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗体,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的氨基酸序列与a551/b379中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的氨基酸序列相同。在另一个实施方案中,参考抗原结合分子是包含a551/b379作为重链可变区/轻链可变区组合的抗体。在优选的实施方案中,参考抗原结合分子包含人源的重链恒定区和轻链恒定区(例如,g1t3(seq id no:138)作为重链恒定区,人λ链lamlib(seq id no:63)作为轻链恒定区)。
[0811]
在一个实施方案中,在存在小分子化合物、不存在小分子化合物、高浓度和/或低浓度小分子化合物的情况下抗cd137抗体对cd137的结合活性是例如通过配体捕获方法使用biacore(注册商标)t200以表面等离振子共振光谱为测量原理来测量的。
[0812]
下文描述了用于测量抗cd137抗体对cd137的结合活性的示例性方法的详情。在一个实施方案中,通过biacore(注册商标)t200评估抗cd137抗体对cd137的结合活性。在优选的实施方案中,该测定法使用20mm aces(ph 7.4)、150mm nacl、2mm mgcl2和0.05%吐温20作为运行缓冲液,并在37℃下进行。在一个实施方案中,在将抗体作为配体捕获在配体捕获分子上之后进行测量。具体地,通过使使用运行缓冲液而制备的抗体溶液与首先通过将sure proteina(ge医疗)固定在s系列传感器芯片cm3(ge医疗)上而制备的芯片相互作用,来捕获合适量(例如,约100ru,200ru,300ru,400ru或500ru)的抗体。
[0813]
在优选的实施方案中,捕获了约100ru至500ru,优选约250ru至400ru的抗体。接下来,通过使使用添加了小分子化合物至目标浓度(例如1μm,10μm,50μm或100μm)的运行缓冲液制备的cd137溶液相互作用,或使使用不含小分子化合物的运行缓冲液制备的cd137溶液相互作用,评估在存在和不存在小分子化合物的情况下对cd137的结合活性。尽管可以适当地确定cd137溶液中cd137的浓度,例如,当使用hcd137-hisbap(参见参考实施例1-1)作为
抗原时,分别使用抗原浓度0nm、15.625nm、62.5nm、250nm和1000nm进行测量。在一个实施方案中,使用biacore t200评估软件2.0计算抗cd137抗体与人cd137的解离常数(kd)。具体地,缔合速率常数ka(l/mol/s)和解离速率常数kd(1/s)通过使用1:1langmuir结合模型对通过测量获得的传感图进行整体拟合来计算。由这些值计算解离常数kd(mol/l)。
[0814]
下面将详细描述用于测量抗cd137抗体与cd137的结合活性的其他示例性测定方法。用biacore t200评估抗cd137抗体与人cd137的结合。使用20mm aces(ph 7.4)、150mm nacl、2mm mgcl2和0.05%吐温20作为运行缓冲液,测定对人cd137的结合,并在37℃下进行。首先,通过将使用运行缓冲液而制备的抗体溶液与其中将sure protein a(ge医疗)固定在s系列传感器芯片cm3(ge医疗)上的芯片相互作用来捕获约250ru至400ru的抗体。接下来,将使用添加了目标浓度(例如1μm,10μm,50μm或100μm)的atp的运行缓冲液而制备的人cd137溶液,或使用不含atp的运行缓冲液而制备的人cd137溶液进行相互作用,以评估存在和不存在atp的情况下对cd137的结合活性。将通过参考实施例(1-1)的方法制备的hcd137-hisbap用作作为抗原的人cd137,并在抗原浓度0nm、15.625nm、62.5nm、250nm和1000nm下分别进行测量。使用25mm naoh和10mm甘氨酸-hcl(ph 1.5)再生芯片,并通过重复捕获抗体进行测量。使用biacore t200评估软件2.0计算每种抗体对人cd137的解离常数。具体而言,缔合速率常数ka(l/mol/s)和解离速率常数kd(1/s)通过使用1:1langmuir结合模型对通过测量获得的传感图进行整体拟合来计算。由这些值计算解离常数kd(mol/l)。
[0815]
在一个实施方案中,抗cd137抗体对cd137(优选人cd137)的结合活性也可以改写为“每单位量抗体的cd137结合量”。具体地,通过使用通过上述使用biacore(注册商标)t200的测定方法所获得的传感图,将cd137与抗体的结合量(ru)除以捕获的抗体量,从而计算“每单位量抗体的cd137结合量”。在一个实施方案中,抗cd137抗体对cd137(优选人cd137)的结合活性也可以通过参考实施例5-3或6-2中所述的方法测量。
[0816]
术语“小分子”和“小分子化合物”是指存在于活体内的除“生物聚合物”以外的天然存在的化学物质,或非天然存在的化学物质。优选地,其是靶组织特异性化合物或非天然存在的化合物,但不限于此。在一个实施方案中,本公开中的“小分子化合物”是“癌组织特异性化合物”或“癌组织特异性代谢产物”。本公开中的术语“对癌组织特异性的化合物(癌组织特异性化合物)”是指与非肿瘤组织相比在肿瘤组织中差异性存在的化合物。如本文所使用的,术语“癌症”通常用于描述恶性肿瘤,并且可以是转移性的或非转移性的。术语“代谢”是指在生物体组织内发生的化学变化,包括“同化”和“分解代谢”。同化是指分子的生物合成或积累,分解代谢是指分子的降解。“代谢产物”是物质代谢产生的中间体或产物。
[0817]
术语“靶组织”是指活体内的要向其递送本公开的抗原结合分子的任何组织。靶组织可以是组织学上可区分的组织,例如各种器官,或是病理学上可区分的组织,例如正常组织和患病组织。在某些实施方案中,靶组织是肿瘤组织。相反,“非靶组织”是指除了靶组织以外的活体内的组织。
[0818]
术语“肿瘤组织”是指包含至少一个肿瘤细胞的组织。通常,肿瘤组织由构成肿瘤主体的肿瘤细胞群(实质)和存在于肿瘤细胞之间并支持肿瘤的结缔组织和血管(间质)组成。在某些情况下,这些显然是可区分的,但是在某些情况下,它们是混在一起的。在某些情况下,存在着这样的细胞,例如已经渗透到肿瘤组织中的免疫细胞。相反,“非肿瘤组织”是指除肿瘤组织以外的活体内的组织。未患病的健康组织/正常组织是此类非肿瘤组织的代
表。
[0819]
作为本公开中使用的癌组织特异性化合物或癌组织特异性代谢产物的非限制性实施方案,可以适当地举例选自以下详述的化合物中的至少一种化合物。“至少一种化合物”的含义包括:除了下述相同抗原结合结构域对抗原的结合活性依赖于一种类型的癌组织特异性化合物或癌组织特异性代谢产物的情况以外,还包括结合活性依赖于几种类型的癌组织特异性化合物或癌组织特异性代谢产物的情况。
[0820]
如本文所使用的,术语“靶组织特异性化合物”是指与非靶组织相比差异性地存在于靶组织中的化合物。在几个实施方案中,靶组织特异性化合物可以是由定性靶组织特异性定义的化合物,例如存在于靶组织中但不存在于非靶组织中,或存在于非靶组织中但不存在于靶组织中。在不同的实施方案中,靶组织特异性化合物可以是由定量靶组织特异性定义的化合物,例如以与非靶组织不同的浓度(例如,更高的浓度或更低的浓度)存在于靶组织中。在具体的实施方案中,靶组织特异性化合物在靶组织中的浓度比非靶组织高例如1.05倍以上,1.1倍以上,1.15倍以上,1.2倍以上,1.25倍以上,1.3倍以上,1.35倍以上,1.4倍以上,1.45倍以上,1.5倍以上,1.55倍以上,1.6倍以上,1.65倍以上,1.7倍以上,1.75倍以上,1.8倍以上,1.85倍以上,1.9倍以上,1.95倍以上,2倍以上,2.1倍以上,2.2倍以上,2.3倍以上,2.4倍以上,2.5倍以上,3倍以上,5倍以上,10倍以上,50倍以上,100倍以上,103倍以上,104倍以上,105倍以上,106倍以上或更高。在另一个实施方案中,靶组织特异性化合物在靶组织中的浓度比非靶组织高例如1.05倍以上,1.1倍以上,1.15倍以上,1.2倍以上,1.25倍以上,1.3倍以上,1.35倍以上,1.4倍以上,1.45倍以上,1.5倍以上,1.55倍以上,1.6倍以上,1.65倍以上,1.7倍以上,1.75倍以上,1.8倍以上,1.85倍以上,1.9倍以上,1.95倍以上,2倍以上,2.1倍以上,2.2倍以上,2.3倍以上,2.4倍以上,2.5倍以上,3倍以上,5倍以上,10倍以上,50倍以上,100倍以上,103倍以上,104倍以上,105倍以上,106倍以上或更高。在具体的实施方案中,与非靶组织相比,靶组织特异性化合物在靶组织中的存在浓度在统计学上显著更高或更低(即,如使用welch氏t-检验或wilcoxon的秩和检验所确定的,p值小于0.05和/或q值小于0.10)。在具体的实施方案中,靶组织特异性化合物是肿瘤组织特异性化合物。
[0821]
在具体的实施方案中,肿瘤组织特异性化合物是由肿瘤细胞特异性代谢产生的代谢产物。代谢产物可以是生命活动所必需的新陈代谢所产生的产物(主要代谢产物),也可以是生命活动不必需的新陈代谢所产生的产物(次生代谢产物)。主要代谢产物的实例可以包括糖、蛋白质、脂质、核酸等。次生代谢产物的例子包括抗生素和染料。代谢产物可以是生物聚合物或小分子。在具体的实施方案中,生物聚合物是分子量为约5000或更高的分子,其由一种或多种类型的重复单元组成,包括例如多糖、多肽和多核苷酸。在具体的实施方案中,小分子是分子量为约500以下的分子,并且是存在于活体内的化学物质。在进一步的实施方案中,肿瘤组织特异性化合物是在肿瘤细胞中特异性产生的小分子代谢产物(eva gottfried,katrin peter和marina p.kreutz,分子与模块化肿瘤治疗(2010)3(2),111-132)。在进一步的实施方案中,肿瘤组织特异性化合物是代谢产物,其是通过浸润于肿瘤组织中的细胞(例如免疫细胞)或存在于肿瘤组织中的基质细胞(例如癌相关成纤维细胞(caf))而特异性产生的。浸润到肿瘤组织中的免疫细胞的实例是树突细胞、抑制性树突细胞、调节性t细胞、耗尽的t细胞、骨髓瘤来源的抑制细胞(mdsc)等。在进一步的实施方案中,
由肿瘤组织中存在的细胞(例如,肿瘤细胞、免疫细胞、基质细胞等)产生的并且当细胞因凋亡或坏死等而死亡时被释放到细胞外的代谢产物,也可以包括在本公开的肿瘤组织特异性化合物中。
[0822]
为了鉴定肿瘤组织特异性化合物,可以适当使用在转录组水平上进行的分析(例如,dhanasekaran等(自然(2001)41 2,822-826),lapointe等(proc.natl.acad.sci.美国(2004)101,811-816)或perou等(自然,(2000)406,747-752)),在蛋白质组水平上进行的分析(例如ahram等(mol.carcinog.(2002)33,9-15)和hood等(分子细胞蛋白质组学(mol.cell.proteomics)(2005)4,1741-1753)),以代谢组学分析(代谢组学)为中心的代谢学分析。即,为了鉴定测试样品中的代谢产物,可以适当地单独使用和/或组合使用高效液相色谱(hplc)、核磁共振(nmr)(brindle等(j.mol.recognit.(1997)10,182-187)、质谱(gc/ms和lc/ms)(gates和sweeley(clin.chem.(1978)24,1663-1673))和使用elisa的代谢谱分析等。
[0823]
在具体的实施方案中,肿瘤组织特异性化合物是选自由以下组成的组的至少一种化合物:具有嘌呤环结构的核苷,氨基酸和其代谢产物,脂质和其代谢产物,碳水化合物代谢的主要代谢产物以及烟酰胺及其代谢产物。在进一步的实施方案中,肿瘤组织特异性化合物是选自以下(1)至(6)的至少一种化合物:
[0824]
(1)具有嘌呤结构的核苷,例如腺苷(ado)、三磷酸腺苷(atp)、二磷酸腺苷(adp)、单磷酸腺苷(amp)和肌苷;
[0825]
(2)氨基酸,例如丙氨酸、谷氨酸和天冬氨酸;
[0826]
(3)氨基酸的代谢产物,例如犬尿氨酸(kynurenine)、邻氨基苯甲酸、3-羟基犬尿氨酸和犬尿酸(kynurenic acid);
[0827]
(4)花生四烯酸的代谢产物,例如前列腺素e2;
[0828]
(5)糖酵解途径或克雷布斯循环(krebs cycle)的主要代谢产物,例如乳酸、琥珀酸和柠檬酸;和,
[0829]
(6)烟酰胺的代谢产物,例如1-甲基烟酰胺。
[0830]
(1)具有嘌呤结构的核苷,例如腺苷(ado)、三磷酸腺苷(atp)、二磷酸腺苷(adp)、单磷酸腺苷(amp)和肌苷
[0831]
众所周知,当肿瘤细胞死亡时,大量的细胞内atp会泄漏出去。因此,肿瘤组织中的atp浓度显著高于正常组织中的atp浓度(plos one.(2008)3,e2599)。amp被细胞表面上的酶代谢,例如细胞外5'-核苷酸酶(eco-5'-核苷酸酶)(cd73)(resta和thompson(免疫学综述(immunol.rev.),(1998)161,95-109)和sadej等(黑素瘤研究(melanoma res.),2006)16,21 3-222)。腺苷是嘌呤核苷,以低浓度组成性地存在于细胞外环境中,但据报道在实体瘤中发现的低氧组织中细胞外腺苷浓度显著增加(blay和hoskin(癌症研究(cancer res.),(1997)57,260 2-2605))。cd73在肿瘤和免疫细胞表面表达(kobie等(免疫学杂志(j.immunol.),(2006)177,6780-6786)),并且发现在乳腺癌(canbolat等(breast cancer res.treat.(1996)37,189-193))、胃癌(durak等(癌症通讯(cancer lett.),1994)84,199-202))、胰腺癌(flocke和mannherz(biochim.biophys.acta(1991).1076,273-281)和胶质母细胞瘤(bardot等(br.j.cancer(1994)70,212-218))中活性升高。已经提出腺苷在肿瘤组织中的积累是细胞质5'-核苷酸酶对amp的去磷酸化增加的结果(headrick和willis(生
物化学杂志(biochem.j.),(1989)261,541-550))。此外,浸润到肿瘤组织中的调节性t细胞也表达atp酶并产生腺苷(proc.natl.acad.sci.美国(2006)103(35),13132-13137;curr.med.chem.(2011)18:5217-5223)。据认为,产生的腺苷通过腺苷受体例如a2a受体将肿瘤组织保持在免疫抑制环境中(curr.med.chem.(2011)18,5217-5223)。因此,被认为通过嘌呤核苷酸的代谢以高浓度累积在肿瘤组织中的atp、adp、amp、腺苷等是本公开中使用的肿瘤组织特异性化合物的实例。另外,随着腺苷被腺苷脱氨酶降解为肌苷,肌苷以高浓度积累。
[0832]
在具体的实施方案中,具有嘌呤环结构的核苷包括含腺苷的化合物。在特定的实施方案中,含腺苷的化合物包括例如腺苷(ado)、三磷酸腺苷(atp)、二磷酸腺苷(adp)、单磷酸腺苷(amp)、环状单磷酸腺苷(camp)、脱氧腺苷(dado)、脱氧腺苷三磷酸(datp)、二磷酸脱氧腺苷(dadp)、单磷酸脱氧腺苷(damp),[γ-硫代]三磷酸腺苷(atpγs)等。在另一个实施方案中,具有嘌呤环结构的核苷包括肌苷,肌苷是腺苷的代谢产物。
[0833]
此外,在具体的实施方案中,具有嘌呤环结构的核苷包括可商购的具有嘌呤环结构的核苷,例如adpbetas(sigma公司)等。
[0834]
(2)氨基酸,例如丙氨酸、谷氨酸、天冬氨酸等
[0835]
在肿瘤细胞中,作为活体中的氮载体的谷氨酰胺的摄取速率增加,并且认为谷氨酰胺的掺入以及由此转化为谷氨酸和乳酸(谷氨酰胺降解(谷氨酰胺分解))是肿瘤细胞的特征(mazurek和eigenbrodt(抗癌研究(anticancer res.),(2003)23,1149-1154,和mazurek等(细胞生理学杂志(j.cell.physiol.),(1999)181,136-146))。癌症患者血浆中的谷氨酰胺水平降低,而谷氨酸浓度升高(droge等(免疫学(immunobiology)(1987)174,473-479)),肺癌组织中
13
c标记的葡萄糖代谢的研究表明
13
c标记的琥珀酸、
13
c标记的丙氨酸、
13
c标记的谷氨酸和
13
c标记的柠檬酸盐浓度之间存在相关性。由于这些原因,被认为例如由于谷氨酰胺降解而在肿瘤组织中高浓度积累的丙氨酸、谷氨酸、天冬氨酸等是在本公开中使用的肿瘤组织特异性化合物的实例。
[0836]
(3)氨基酸的代谢产物,例如犬尿氨酸、邻氨基苯甲酸、3-羟基犬尿氨酸和犬尿酸
[0837]
吲哚胺2,3-二加氧酶(ido)是一种色氨酸代谢酶,在许多癌症例如黑素瘤、结肠癌、肾癌等中高度表达(uyttenhove等(nat.med.(2003)9,1269-1274)。ido催化色氨酸向犬尿氨酸的转化。在不表达ido的神经胶质瘤中,通过肝脏的色氨酸2,3-二加氧酶(tdo)从色氨酸产生犬尿氨酸(opitz等(自然(2011)478(7368),197-203))。ido也在浸润到肿瘤组织中的树突细胞上表达,并且树突细胞也产生犬尿氨酸(免疫学研究(j.immunol.),(2008)181,5396-5404)。此外,ido也在肿瘤组织的髓源抑制性细胞(mdsc)中表达,并且mdsc还产生犬尿氨酸(yu等(免疫学研究(j.immunol.),(2013)190,3783-3797))。犬尿氨酸酶将犬尿氨酸转化为邻氨基苯甲酸,犬尿氨酸3-羟化酶将犬尿氨酸转化为3-羟基犬尿氨酸。邻氨基苯甲酸和3-羟基犬尿氨酸都转化为3-羟基邻氨基苯甲酸,即nad的前体。犬尿氨酸转氨酶将犬尿氨酸转化为犬尿酸。由于这些原因,犬尿氨酸及其代谢产物,即邻氨基苯甲酸、3-羟基犬尿氨酸、犬尿酸等是本公开中使用的肿瘤组织特异性化合物,特别是肿瘤细胞特异性代谢产物的实例。
[0838]
(4)花生四烯酸的代谢产物,例如前列腺素e2
[0839]
前列腺素e2(pge2)促进结肠癌细胞的生长并抑制其凋亡(sheng等(癌症研究
(cancer res.),(1998)58,362-366)。在pge2合成酶中,主要发现cox-1在几乎所有组织中组成性表达,而cox-2由肿瘤中的某些炎性细胞因子和致癌基因诱导(warner和mitchell(faseb j.(2004)18,790-804))。据报道,cox-2的过表达与乳腺癌的不良预后(denkert等(临床乳腺癌研究(clin.breast cancer),(2004)4,428-433))和卵巢癌中疾病的快速进展(denker等(mod.pathol.(2006)19,1261-1269)有关。另外,浸润到肿瘤组织中的调节性t细胞也产生pge 2(curr.med.chem.(2011)18,5217-5223)。由于这些原因,花生四烯酸的代谢产物例如pge2是肿瘤组织特异性化合物,特别是肿瘤细胞特异性代谢产物或浸润肿瘤组织的免疫细胞的特异性代谢产物的实例。除了pge2之外,在肿瘤组织例如结肠癌中,血栓烷a2(txa 2)的产生得以增强(j.lab.clin.med.(1993)122,518-523)。
[0840]
(5)糖酵解途径或克雷布斯循环的主要代谢产物,例如乳酸、琥珀酸和柠檬酸
[0841]
以糖酵解(embden-meyerhof途径)酶例如丙酮酸激酶、己糖激酶和乳酸脱氢酶(ldh)的上调为特征的糖酵解表型通常被称为warburg效应,这是实体瘤的特征。已知糖酵解的终产物乳酸,以及由克雷布斯循环产生的琥珀酸和柠檬酸在肿瘤组织中积累(teresa等(分子癌症(2009)8,41-59))。由于这些原因,通过糖酵解产生的主要代谢产物乳酸、琥珀酸、柠檬酸等是在本公开中使用的肿瘤组织特异性化合物,特别是肿瘤细胞特异性代谢产物的实例。另外,已知由于细胞死亡,以高浓度存在于细胞中的琥珀酸酯泄漏出细胞(自然免疫学(nature immunology),(2008)9,1261-1269)。认为这是在频繁发生细胞死亡的肿瘤组织中琥珀酸浓度增加的原因。
[0842]
(6)烟酰胺的代谢产物,例如1-甲基烟酰胺
[0843]
已知烟酰胺n-甲基转移酶在许多人肿瘤组织中高表达。还已知1-甲基烟酰胺(其是由该酶产生的烟酰胺的稳定代谢产物)被分泌到肿瘤细胞的外部(yamada等(j.nutr.sci.vitaminol.(2010)56,83-86))。由于这个原因,被认为由于烟酰胺的代谢而高浓度地累积在肿瘤组织中的1-甲基烟酰胺等是本公开中使用的肿瘤组织特异性化合物的实例。
[0844]
本公开的“抗原结合分子”包含“抗原结合结构域”。作为“抗原结合结构域”,可以使用任何结构的结构域,只要其结合靶抗原即可。在一个实施方案中,本公开的抗原结合结构域包括,例如,抗体重链和/或轻链的可变区,包含在生物体各种细胞膜蛋白中所包含的约35个氨基酸的模块(a结构域)的avimer(国际公开wo2004/044011和wo2005/040229),包含在细胞膜上表达的糖蛋白的纤连蛋白的10fn3结构域的adnectin(国际公开wo2002/032925),使用蛋白质a的58个氨基酸的igg结合结构域作为支架的affibodies(wo1995/001937),darpins(设计的锚蛋白重复蛋白),其使用33个氨基酸的重复序列的锚蛋白重复序列(ar)作为基础(国际公开wo2002/020565),含有脂质运载蛋白(例如嗜中性粒细胞明胶酶相关脂质运载蛋白(ngal))为基础的anticalin(国际公开wo2003/029462),可变淋巴细胞受体(vlr),它们是在无颌脊椎动物例如日本七鳃鳗和粘盲鳗属的适应性免疫系统中起作用的蛋白,并且含有富含亮氨酸重复序列的模块(lrr)(国际公开wo2008/016854)等。在具体的实施方案中,本公开的抗原结合结构域包含抗体的重链和轻链可变区。在进一步的实施方案中,本公开的抗原结合结构域包括例如scfv(单链fv)、单链抗体、fv、scfv2(单链fv2)、fab或f(ab')2。
[0845]
[hvr和可变区]
[0846]
一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含选自以下的至少一个,至少两个或全部三个vh hvr序列:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含选自seq id no:8、9、10、11、12、13、14、15和16中的任一个氨基酸序列;和(c)hvr-h3,其包含选自seq id no:17、18、19或20中的任一个的氨基酸序列。在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含选自seq id no:8、9、10、11、12、13、14、15和16中的任一个的氨基酸序列;和(c)hvr-h3,其包含选自seq id no:17、18、19或20中的任一个氨基酸序列。
[0847]
在一个实施方案中,抗cd137抗原结合分子是包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256或a549/b167的氨基酸序列作为重链可变区/轻链可变区组合的抗体。在优选的实施方案中,抗原结合分子是抗cd137抗体,其包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与a375/b167中所包括的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在进一步的实施方案中,抗cd137抗原结合分子是包含a375/b167作为重链可变区/轻链可变区组合的抗cd137抗体。在不同的优选实施方案中,抗cd137抗原结合分子是这样的抗cd137抗体,其包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3,其中所述hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3具有与a551/b379中所包括的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在进一步的实施方案中,抗cd137抗原结合分子是包含a551/b379作为重链可变区/轻链可变区组合的抗cd137抗体。
[0848]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:8的氨基酸序列;和(c)hvr-h3,其包含seq id no:17的氨基酸序列。
[0849]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:9的氨基酸序列;和(c)hvr-h3,其包含seq id no:17的氨基酸序列。
[0850]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:10的氨基酸序列;和(c)hvr-h3,其包含seq id no:17的氨基酸序列。
[0851]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:11的氨基酸序列;和(c)hvr-h3,其包含seq id no:18的氨基酸序列。
[0852]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:8的氨基酸序列;和(c)hvr-h3,其包含seq id no:18的氨基酸序列。
[0853]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:12的氨基酸序列;和(c)hvr-h3,其包含seq id no:18的氨基酸序列。
[0854]
在一个实施方案中,抗cd137抗原结合分子或抗体包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:13的氨基酸序列;和(c)hvr-h3,其包含
no:25的氨基酸序列;(b)hvr-l2,其包含seq id no:26的氨基酸序列;和(c)hvr-l3,其包含seq id no:27的氨基酸序列。
[0867]
在另一方面,本公开的抗cd137抗原结合分子或抗体包含(a)vh结构域,其包含选自以下(i)、(ii)和(iii)的至少一个、至少两个或所有三个vh hvr序列:(i)hvr-h1,其包含seq id no:7的氨基酸序列;(ii)hvr-h2,其包含选自seq id no:8、9、10、11、12、13、14、15和16中的任何一个的氨基酸序列;和(iii)hvr-h3,其包含选自seq id no:17、18、19或20中的任何一个的氨基酸序列;和(b)vl结构域,其包含选自以下(i)、(ii)和(iii)的至少一个、至少两个或全部三个vl hvr序列:(i)hvr-l1,其包含选自seq id no:21、22、23、24和25中的任何一个的氨基酸序列;(ii)hvr-l2,其包含seq id no:26的氨基酸序列;和(iii)hvr-l3,其包含选自seq id no:27、28和29中的任何一个的氨基酸序列。
[0868]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:8的氨基酸序列;(c)hvr-h3,其包含seq id no:17的氨基酸序列;(d)hvr-l1,其包含seq id no:21的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0869]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:9的氨基酸序列;(c)hvr-h3,其包含seq id no:17的氨基酸序列;(d)hvr-l1,其包含seq id no:22的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0870]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:10的氨基酸序列;(c)hvr-h3,其包含seq id no:17的氨基酸序列;(d)hvr-l1,其包含seq id no:22的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0871]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:11的氨基酸序列;(c)hvr-h3,其包含seq id no:18的氨基酸序列;(d)hvr-l1,其包含seq id no:21的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0872]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:8的氨基酸序列;(c)hvr-h3,其包含seq id no:18的氨基酸序列;(d)hvr-l1,其包含seq id no:21的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0873]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:12的氨基酸序列;(c)hvr-h3,其包含seq id no:18的氨基酸序列;(d)hvr-l1,其包含seq id no:21的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:28的氨基
酸序列。
[0874]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:13的氨基酸序列;(c)hvr-h3,其包含seq id no:18的氨基酸序列;(d)hvr-l1,其包含seq id no:21的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:29的氨基酸序列。
[0875]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:14的氨基酸序列;(c)hvr-h3,其包含seq id no:19的氨基酸序列;(d)hvr-l1,其包含seq id no:23的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0876]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:15的氨基酸序列;(c)hvr-h3,其包含seq id no:20的氨基酸序列;(d)hvr-l1,其包含seq id no:24的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0877]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:15的氨基酸序列;(c)hvr-h3,其包含seq id no:20的氨基酸序列;(d)hvr-l1,其包含seq id no:25的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0878]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:16的氨基酸序列;(c)hvr-h3,其包含seq id no:20的氨基酸序列;(d)hvr-l1,其包含seq id no:25的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0879]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:14的氨基酸序列;(c)hvr-h3,其包含seq id no:19的氨基酸序列;(d)hvr-l1,其包含seq id no:24的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0880]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含seq id no:14的氨基酸序列;(c)hvr-h3,其包含seq id no:17的氨基酸序列;(d)hvr-l1,其包含seq id no:21的氨基酸序列;(e)hvr-l2,其包含seq id no:26的氨基酸序列;和(f)hvr-l3,其包含seq id no:27的氨基酸序列。
[0881]
在具体的实施方案中,上述抗cd137抗体的任何一个或多个氨基酸在以下hvr位置被置换:
[0882]
在hvr-h2(seq id no:30)中:位置5、6、7、10、13、14和/或17;
[0883]
在hvr-h3(seq id no:31)中:位置3和/或6;
[0884]
在hvr-l1(seq id no:32)中:位置4、5、9和/或11;
[0885]
在hvr-l3(seq id no:33)中:位置6、7和/或8。
[0886]
在具体的实施方案中,本说明书提供的置换是保守置换。在具体的实施方案中,以下的任意一个或多个置换可以任意组合进行:
[0887]
在hvr-h2(seq id no:8)中:k5h或s;s6g;t7s;e10y;d13e;s14q;v17g或l;
[0888]
在hvr-h3(seq id no:17)中:a3p、k或i;f6e;
[0889]
在hvr-l1(seq id no:21)中:r4s;y5t;y9f;e11n;
[0890]
在hvr-l3(seq id no:27)中:e6p;h7a;q8i
[0891]
对于hvr-h2、hvr-h3、hvr-l1和hvr-l3,上述置换的所有可能组合分别包含在seq id no:30、31、32和33的共有序列中。
[0892]
在以上任何实施方案中,抗cd137抗原结合分子或抗体是人源化的。在一个实施方案中,抗cd137抗原结合分子或抗体包含如上述实施方案中的任意hvr,并且还包含受体人框架,例如人免疫球蛋白框架或人共有框架。在另一个实施方案中,抗cd137抗原结合分子或抗体包含如上述实施方案中的任意hvr,并且还包含包含框架(fr)序列的重链可变区(vh)或轻链可变区(vl)。在一个实施方案中,重链可变区中的fr1包含seq id no:35的氨基酸序列,重链可变区中的fr2包含seq id no:36的氨基酸序列,重链可变区中的fr3包含seq id no:37的氨基酸序列,和重链可变区的fr4包含seq id no:38的氨基酸序列。在一个实施方案中,轻链可变区的fr1包含seq id no:39的氨基酸序列,轻链可变区中的fr2包含seq id no:40的氨基酸序列,轻链可变区中的fr3包含seq id no:41的氨基酸序列,和轻链可变区中的fr4包含seq id no:42的氨基酸序列。
[0893]
在另一方面,抗cd137抗原结合分子或抗体包含重链可变结构域(vh)序列,所述重链可变结构域(vh)序列与seq id no:43、44、45、46、47、48、49、50、51、52或53的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性。在某些实施方案中,具有至少90%、91%、92%、93%、94%、95%、96%,97%、98%或99%同一性的vh序列包含相对于参考序列的置换(例如保守置换)、插入或缺失,但是,包含该序列的抗cd137抗原结合分子或抗体保留了与cd137的结合能力。在某些实施方案中,在seq id no:43、44、45、46、47、48、49、50、51、52或53中,总共有1至10个氨基酸被置换、插入和/或缺失。在某些实施方案中,置换、插入或缺失发生在hvr之外的区域(即,在fr中)。任选地,抗cd137抗体包含seq id no:43、44、45、46、47、48、49、50、51、52或53中的vh序列,包括该序列的翻译后修饰。在特定的实施方案中,vh包含一个、两个或三个选自以下的hvr:(a)hvr-h1,其包含seq id no:7的氨基酸序列;(b)hvr-h2,其包含选自seq id no:8、9、10、11、12、13、14、15和16中的任何一个的氨基酸序列;和(c)hvr-h3,其包含选自seq id no:17、18、19或20中的任何一个的氨基酸序列。翻译后修饰包括但不限于通过焦谷氨酰化将重链或轻链n末端的谷氨酰胺或谷氨酸修饰为焦谷氨酸。
[0894]
在另一方面,提供了抗cd137抗原结合分子或抗体,其中所述抗体包含轻链可变结构域(vl),所述轻链可变结构域与seq id no:54、55、56、57、58、59或60的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性。在某些实施方案中,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性
的vl序列包含相对于参考序列的置换(例如,保守置换)、插入或缺失,但包含该序列的抗cd137抗原结合分子或抗体保留了与cd137的结合能力。在某些实施方案中,在seq id no:54、55、56、57、58、59或60中,总共有1至10个氨基酸被置换、插入和/或缺失。在某些实施方案中,置换、插入或缺失发生在hvr之外的区域(即fr中)。任选地,抗cd137抗原结合分子或抗体包含seq id no:54、55、56、57、58、59或60中的vl序列,包括该序列的翻译后修饰。在特定的实施方案中,vl包含选自以下的一个、两个或三个hvr:(a)hvr-l1,其包含选自seq id no:21、22、23、24和25中的任何一个氨基酸序列;(b)hvr-l2,其包含seq id no:26的氨基酸序列;和(c)hvr-l3,其包含选自seq id no:27、28和29中的任何一个氨基酸序列。翻译后修饰包括但不限于通过焦谷氨酰化将重链或轻链n末端的谷氨酰胺或谷氨酸修饰为焦谷氨酸。
[0895]
在另一方面,提供了抗cd137抗原结合分子或抗体,其中所述抗原结合分子或抗体包含如上文提供的任何实施方案中的vh和如上文提供的任何实施方案中的vl。
[0896]-在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:43和seq id no:54中的vh和vl序列,包括那些序列的翻译后修饰。
[0897]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:44和seq id no:55中的vh和vl序列,包括那些序列的翻译后修饰。
[0898]-在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:45和seq id no:55中的vh和vl序列,包括那些序列的翻译后修饰。
[0899]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:46和seq id no:54中的vh和vl序列,包括那些序列的翻译后修饰。
[0900]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:47和seq id no:54中的vh和vl序列,包括那些序列的翻译后修饰。
[0901]-在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:48和seq id no:56中的vh和vl序列,包括那些序列的翻译后修饰。
[0902]-在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:49和seq id no:57中的vh和vl序列,包括那些序列的翻译后修饰。
[0903]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:50和seq id no:58中的vh和vl序列,包括这些序列的翻译后修饰。
[0904]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:51和seq id no:59中的vh和vl序列,包括那些序列的翻译后修饰。
[0905]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:51和seq id no:60中的vh和vl序列,包括那些序列的翻译后修饰。
[0906]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:52和seq id no:60中的vh和vl序列,包括那些序列的翻译后修饰。
[0907]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:50和seq id no:59中的vh和vl序列,包括那些序列的翻译后修饰。
[0908]
在一个实施方案中,抗cd137抗原结合分子或抗体分别包含seq id no:53和seq id no:54中的vh和vl序列,包括那些序列的翻译后修饰。
[0909]
上述翻译后修饰包括但不限于通过焦谷氨酰化将重链或轻链的n末端的谷氨酰胺
或谷氨酸修饰为焦谷氨酸。
[0910]
对于本公开的每个抗cd137抗原结合分子或抗体,对应于优选重链可变区和轻链可变区的氨基酸序列及其hvr1、hvr2和hvr3的seq id no在下表中示出。
[0911]
[表1]
[0912][0913]
当本文提供的抗cd137抗原结合分子或抗体具有谷氨酰胺作为重链或轻链n末端氨基酸时,该氨基酸可以被谷氨酸置换。当本文提供的抗cd137抗体具有谷氨酸作为重链或轻链n末端氨基酸时,该氨基酸可以被谷氨酰胺置换。
[0914]
在优选的实施方案中,包含上述hvr、重链可变区和/或轻链可变区的抗cd137抗原结合分子或抗体都具有如上所述的对cd137的低分子量化合物依赖性结合活性。
[0915]
[恒定区]
[0916]
在另一方面,抗cd137抗原结合分子或抗体包含恒定区。恒定区可以是重链恒定区(包括fc区)、轻链恒定区或两者。在另一方面,抗cd137抗原结合分子或抗体包含fc区。在一些实施方案中,恒定区是具有天然序列的恒定区。衍生自天然抗体的重链恒定区的实例包括,例如,人igg1(seq id no:61、62)、人igg2、人igg3、人igg4等的重链恒定区。衍生自天然抗体的轻链恒定区的实例包括例如人κ链、人λ链(例如,seq id no:63)等。
[0917]
本文所使用的“亲本恒定区”或“亲本fc区”是指在引入本文所述的氨基酸改变之前的恒定区或fc区。“亲本抗原结合分子”是指包含亲本恒定区或亲本fc区的抗原结合分子。在一些实施方案中,亲本fc区是具有天然序列的fc区(或天然抗体的fc区)。抗体包括,例如,iga(iga1,iga2)、igd、ige、igg(igg1、igg2,igg3、igg4)、igm等。抗体可以源自人或猴(例如食蟹猴、恒河猴、狨猴、黑猩猩或狒狒)。天然抗体也可以包括天然产生的突变。nih出版物号91-3242“具有免疫学意义的蛋白质序列”中描述了由于遗传多态性而产生的多个igg同种异型序列,并且它们中的任何一个都可以用于本公开中。在一个实施方案中,亲本fc区是源自人igg1的重链恒定区的fc区,如seq id no:61、62或182所示。
[0918]
一方面,与包含天然序列fc区或亲本fc区的抗cd137抗原结合分子或抗体相比,抗cd137抗原结合分子或抗体具有增加的等电点(pi)。在一些实施方案中,变体fc区包含至少
一个氨基酸改变。在进一步的实施方案中,与亲本fc区相比,氨基酸改变导致变体fc区的等电点(pi)升高。不受特定理论的束缚,据信生物流体(例如血浆)的ph在中性ph范围内。在生物流体中,pi增加的抗原结合分子或抗体的净正电荷由于pi的增加而增加,结果,物理化学库仑相互作用更牢固地将抗原结合分子或抗体吸引至内皮细胞表面,其中与不具有增加pi的抗原结合分子或抗体相比,所述内皮细胞表面具有净负电荷。这样,激动性抗原结合分子(或抗体)或结合抗原的激动性抗原结合分子(或抗体)可更靠近表达fc-γ受体的细胞表面,导致抗原结合分子或抗体与fc-γ受体表达细胞的的结合增加。对于那些基于对fc-γ受体的结合活性的贡献而表现出cd137激动活性的抗cd137激动性抗原结合分子或抗体,与不具有增加pi的氨基酸改变的抗cd137激动性抗原结合分子或抗体相比,由于增加pi的氨基酸改变而增加对fc-γ受体表达细胞的结合的抗cd137激动性抗原结合分子或抗体可表现出更强的cd137激动活性。
[0919]
在本公开中,pi可以是理论上或实验上确定的pi。pi的值可以例如通过本领域技术人员已知的等电聚焦来确定。可以使用例如基因和氨基酸序列分析软件(genetyx等)来计算理论pi的值。在计算中,抗体的性质可以反映在计算公式中。例如,(i)通常,抗体中保守的cys形成二硫键并且不携带侧链的电荷;因此,此类cys可以从计算中排除,并且仅不形成二硫键的游离形式cys可以包括在计算中。或者,(ii)由于翻译后修饰,抗体的电荷状态或等电点可能改变;因此,考虑到这种翻译后修饰,可以对计算公式进行如下修改:(a)当重链的n端为q(谷氨酰胺)时,假设发生焦谷氨酰化,n端氨基不计入计算;(b)当重链的c末端为k(赖氨酸)时,假设发生截短,则将k(仅一个残基)排除在计算之外;和(c)假设所有这些c在分子内形成二硫键,则将存在于通常保守位置的所有c(半胱氨酸)的侧链从计算中排除。在一个优选实施方案中,上述(i)和(ii)都可以反映在计算公式中。
[0920]
在一个实施方案中,与修饰前相比,pi值可以增加例如至少0.01、0.03、0.05、0.1、0.2、0.3、0.4、0.5以上,至少0.6、0.7、0.8、0.9以上,至少1.0、1.1、1.2、1.3、1.4、1.5以上,或者至少1.6、1.7、1.8、1.9、2.0、2.1、2.2、2.3、2.4、2.5、3.0以上。
[0921]
在一个实施方案中,与pi增加有关的氨基酸改变和增加抗原结合分子或抗体的pi的方法在本文“iii.组合物和方法(包含具有增加的等电点(pi)的变体fc区的激动性抗原结合分子)”进行了详细描述。本领域技术人员将理解,在“iii.组合物和方法(包含具有增加的等电点(pi)的变体fc区的激动性抗原结合分子)”中描述的用于增加pi的任何氨基酸改变和方法可以应用于抗cd137抗原结合分子或抗体。
[0922]
在一个实施方案中,抗cd137抗原结合分子或抗体具有增加的pi的变体fc区,并且变体fc区包含选自由以下组成的组中的至少一个位置的至少一个氨基酸改变:根据eu编号的位置285、311、312、315、318、333、335、337、341、342、343、384、385、388、390、399、400、401、402、413、420、422和431。在进一步的实施方案中,具有增加的pi的变体fc区在每个选择的位置处包含arg或lys。
[0923]
在进一步的实施方案中,抗cd137抗原结合分子或抗体具有pi增加的变体fc区,并且该变体fc区包含选自由以下组成的组中的至少一个位置的至少一个氨基酸改变:根据eu编号的位置311、343和413。在进一步的实施方案中,具有pi增加的变体fc区包括根据eu编号在位置311、343或413处的氨基酸改变。在进一步的实施方案中,具有增加的pi的变体fc区在每个选择的位置处包含arg或lys。
3252(2003);kono等,hum.mol.genet.14:2881-2892(2005);和kyogoju等,关节炎与风湿病(arthritis rheum.),46:1242-1254(2002)),以及将来将报道的每种遗传多态性。
[0932]
在fcγriia中,有两种同种异型,一种在fcγriia的131位氨基酸为组氨酸(h型),另一种在131位的氨基酸被精氨酸置换(r型)(warrmerdam,j.exp.med.172:19-25(1990))。
[0933]
fcγr包括人、小鼠、大鼠、兔和猴来源的fcγr,但不限于此,并且可以源自任何生物。小鼠fcγr包括fcγri(cd64)、fcγrii(cd32)、fcγriii(cd16)和fcγriii-2(cd16-2),以及任何小鼠fcγr或fcγr同种型,但不限于此。
[0934]
在另一方面,本公开提供了抗cd137抗原结合分子或抗体,其包含对fc-γriib具有增加的结合活性的变体fc区,所述变体fc区包含以下(1)至(8)中任一项的氨基酸改变:根据eu编号,(1)在位置234、238、264和330处;(2)在位置234、238和330处;(3)在位置234、237、238和330处;(4)在位置236、268和330处;(5)在位置235、236、268、295、326和330处。
[0935]
在一个实施方案中,本发明的抗cd137抗原结合分子或抗体包含变体fc区,所述变体fc区包含下表3中鉴定的氨基酸改变。在另一个实施方案中,本公开的抗cd137抗原结合分子或抗体包含变体fc区,所述变体fc区除了表2中描述的氨基酸改变(参与增加fc区的pi的氨基酸改变)外,还包含在下表3中鉴定出的氨基酸改变的任何一种组合。
[0936]
用于增加fc区fc-γriib结合活性的氨基酸改变
[0937]
[表3]
[0938]
编号氨基酸置换(eu编号)1l234y/p238d/v264i/a330k2l234y/p238d/a330k3l234y/g237d/p238d/a330k4g236n/h268d/a330k5l235w/g236n/h268d/q295l/k326t/a330k
[0939]
在一个实施方案中,本公开提供了变体fc区,所述变体fc区包括具有至少一个氨基酸改变并且对fc-γriib具有等于或高于参考fc区的结合活性的那些变体fc区。在一个实施方案中,参考fc区是包含以上表3中鉴定的氨基酸改变的任何一种组合的fc区。在一个优选的实施方案中,参考fc区是重链恒定区tt14(seq id no:149)、tt16(seq id no:150)、my201(seq id no:153)或my518(seq id no:154)中包含的fc区。在一个优选的实施方案中,参考fc区是重链恒定区my201(seq id no:153)或my518(seq id no:154)中包含的fc区。
[0940]
在另一方面,本公开提供了分离的激动性抗原结合分子或抗体,其包含变体fc区,所述变体fc区具有对fc-γ受体(优选地,fc-γriib)的增加的结合活性和增加的pi。在某实施方案中,本文所述的变体fc区包含在亲本fc区中的至少两个氨基酸改变。如上所述,与不具有增加的pi的抗原结合分子或抗体相比,具有增加的pi的抗原结合分子或抗体被物理化学库仑相互作用更强烈地吸引到具有净负电荷的内皮细胞表面。因此,对于那些基于对fc-γ受体(优选fc-γriib)的结合活性的贡献而表现出激动活性的激动性抗原结合分子或抗体,可以通过组合增加fc-γ受体(优选fc-γriib)的氨基酸改变或增加pi的氨基酸改变来提高抗原结合分子或抗体的激动活性。
[0941]
在一个实施方案中,抗cd137抗原结合分子或抗体包含变体fc区,所述变体fc区包
含如上所述的增加对fc-γ受体(例如,fc-γriib)的结合活性的氨基酸改变和增加等电点(pi)的氨基酸改变二者。如上所述,与不具有增加的pi的抗原结合分子或抗体相比,具有增加的pi的抗原结合分子或抗体通过物理化学库仑相互作用被更强烈地吸引至具有净负电荷的内皮细胞表面。因此,对于那些基于对fc-γ受体(优选fc-γriib)的结合活性的贡献而示出cd137激动活性的抗cd137激动抗原结合分子或抗体,抗cd137抗原结合分子或抗体的激动活性可以通过组合增加fc-γ受体(优选fc-γriib)的氨基酸改变和增加pi的氨基酸改变来增加。
[0942]
一方面,本公开提供了包含对fc-γriib具有增加的结合活性并且具有增加的pi的变体fc区的多肽,所述变体fc区包含至少三个氨基酸改变,所述氨基酸改变包括(a)选自由根据eu编号的位置234、235、236、237、238、264、268、295、326和330组成的组中的至少一个位置处的至少一个氨基酸改变,和(b)选自由根据eu编号的位置311、343和413组成的组中的至少两个位置处的至少两个氨基酸改变。
[0943]
在另一个方面,本公开提供了包含具有对fc-γriib的增加的结合活性和增加的pi的变体fc区的多肽,其包含以下(1)至(26)中任一项的氨基酸改变:根据eu编号
[0944]
(1)位置235、236、268、295、326、330、343和413;
[0945]
(2)位置214、235、236、268、295、326、330、343和413;
[0946]
(3)位置234、238、250、264、307、330、343和413;
[0947]
(4)位置234、238、264、330、343和413;
[0948]
(5)位置234、237、238、250、307、330、343和413;
[0949]
(6)位置234、237、238、330、343和413;
[0950]
(7)位置235、236、268、295、326、330、311和343;
[0951]
(8)位置234、238、250、264、307、330、311和343;
[0952]
(9)位置234、238、264、330、311和343;
[0953]
(10)位置234、237、238、250、307、330、311和343;
[0954]
(11)位置234、237、238、330、311和343;
[0955]
(12)位置235、236、268、295、326、330和343;
[0956]
(13)位置214、235、236、268、295、326、330和343;
[0957]
(14)位置235、236、268、295、326、330和413;
[0958]
(15)位置214、236、268、330和343;
[0959]
(16)位置214、235、236、268、330和343;
[0960]
(17)位置214、236、268、330和413;
[0961]
(18)位置214、236、268、330、343和413;
[0962]
(19)位置214、235、236、268、330、343和413;
[0963]
(20)位置214、236、268、330和311;
[0964]
(21)位置214、235、236、268、330和311;
[0965]
(22)位置214、236、268、330、311和343;
[0966]
(23)位置214、235、236、268、330、311和343;
[0967]
(24)位置214、236、268、330、311和413;
[0968]
(25)位置214、235、236、268、330、311和413;
[0969]
(26)位置214、235、236、268、295、326、330和311。
[0970]
在一个实施方案中,本公开的变体fc区包含下表4中鉴定的氨基酸改变的任一组合。
[0971]
[表4]
[0972]
编号氨基酸置换(eu编号)1l235w/g236n/h268d/q295l/k326t/a330k/p343r/d413k2k214r/l235w/g236n/h268d/q295l/k326t/a330k/p343r/d413k3l234y/p238d/t250v/v264i/t307p/a330k/p343r/d413k4l234y/p238d/v264i/a330k/p343r/d413k5l234y/g237d/p238d/t250v/t307p/a330k/p343r/d413k6l234y/g237d/p238d/a330k/p343r/d413k7l235w/g236n/h268d/q295l/k326t/a330k/q311r/p343r8l234y/p238d/t250v/v264i/t307p/a330k/q311r/p343r9l234y/p238d/v264i/a330k/q311r/p343r10l234y/g237d/p238d/t250v/t307p/a330k/q311r/p343r11l234y/g237d/p238d/a330k/q311r/p343r12l235w/g236n/h268d/q295l/k326t/a330k/p343r13k214r/l235w/g236n/h268d/q295l/k326t/a330k/p343r14l235w/g236n/h268d/q295l/k326t/a330k/d413k15k214r/g236n/h268d/a330k/p343r16k214r/l235w/g236n/h268d/a330k/p343r17k214r/g236n/h268d/a330k/d413k18k214r/g236n/h268d/a330k/p343r/d413k19k214r/l235w/g236n/h268d/a330k/p343r/d413k20k214r/g236n/h268d/a330k/q311r21k214r/l235w/g236n/h268d/a330k/q311r22k214r/g236n/h268d/a330k/q311r/p343r23k214r/l235w/g236n/h268d/a330k/q311r/p343r24k214r/g236n/h268d/a330k/q311r/d413k25k214r/l235w/g236n/h268d/a330k/q311r/d413k26k214r/l235w/g236n/h268d/q295l/k326t/a330k/q311r
[0973]
在一个实施方案中,包含以上表4中描述的氨基酸改变的任一组合的变体fc区缺少根据eu编号在位置447处的氨基酸。在优选的实施方案中,包含以上表4中描述的氨基酸改变的任一组合的变体fc区缺少根据eu编号在位置446和447处的氨基酸。
[0974]
本领域技术人员将理解,除了上面举例说明的改变之外,可以使用如例如在wo2013/047752、wo2013/125667、wo2014/030728、wo2014/163101或wo2017104783中所描述或暗示的与亲本fc区相比增加对fc-γr(包括fc-γriib)的结合活性的至少一个氨基酸改变,以及如例如在wo2017/104783、wo2017/046994中所描述或暗示的与亲本fc区相比增加pi的至少一个氨基酸改变,和这些氨基酸改变的任何组合。
[0975]
另外,为其他目的而进行的氨基酸改变可以结合在本文所述的变体fc区中。例如,可以添加以下氨基酸置换:增加fcrn结合活性的氨基酸置换(hinton等,j.immunol.176(1):346-356(2006);dall'acqua等,j.biol.chem.281(33):23514-23524(2006);petkova等,intl.immunol.18(12):1759-1769(2006);zalevsky等,nat.biotechnol.28(2):157-159(2010);wo 2006/019447;wo 2006/053301;和wo 2009/086320),和用于改善抗体异质性或稳定性的氨基酸置换(wo 2009/041613)。或者,在wo 2011/122011、wo 2012/132067、wo 2013/046704或wo 2013/180201中描述的具有促进抗原清除的性质的多肽,在wo 2013/180200中描述的具有与靶组织特异性结合的性质的多肽,在wo 2009/125825、wo 2012/073992或wo 2013/047752中描述的具有重复结合多个抗原分子的性质的多肽可以与本文描述的变体fc区组合。或者,为了赋予与其他抗原的结合活性,可以将ep1752471和ep1772465中公开的氨基酸改变组合在本文描述的变体fc区的ch3中。
[0976]
在一个实施方案中,本公开的抗cd137抗原结合分子或抗体包含重链恒定区,所述重链恒定区包含选自seq id no:64-85的任一氨基酸序列。优选地,本公开的抗cd137抗原结合分子或抗体包含重链恒定区,所述重链恒定区包含seq id no:75或82的氨基酸序列。
[0977]
在一个优选的实施方案中,包含上述变体fc区的抗cd137抗原结合分子或抗体具有上述依赖于小分子化合物的cd137结合活性。
[0978]
在一个实施方案中,本公开的抗cd137抗原结合分子或抗体包含以下可变区和恒定区:包含上述hvr,重链可变区和/或轻链可变区的可变区;和上述变体fc区。在一个优选的实施方案中,本公开的抗cd137抗原结合分子或抗体可以是选自表72中描述的抗体的任一抗cd137抗体。
[0979]
在另一方面,本公开提供了在低分子量化合物存在下(例如,在10μm以上、50μm以上、100μm以上、150μm以上、200μm以上、或250μm以上的所述低分子量化合物存在下),结合至与本文提供的抗cd137抗原结合分子或抗体的cd137上相同表位的抗原结合分子或抗体。例如,在某实施方案中,提供了抗原结合分子或抗体,所述抗原结合分子或抗体结合至与包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256和/或a549/b167作为重链可变区/轻链可变区的组合的抗cd137抗原结合分子或抗体相同的抗原表位。在一个实施方案中,本公开的具有依赖于小分子化合物的抗原结合活性的cd137结合活性的抗cd137抗原结合分子或抗体识别由抗原(例如,cd137)和低分子量化合物(例如atp)形成的复合物形成的表位。
[0980]
在另一方面,本公开提供了在低分子量化合物(例如,在10μm以上、50μm以上、100μm以上、150μm以上、200μm以上、或250μm以上的所述低分子量化合物存在下)与本文提供的抗cd137抗原结合分子或抗体竞争结合cd137的抗原结合分子或抗体。例如,在某实施方案中,这些抗cd137抗原结合分子或抗体与包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256和/或a549/b167作为重链可变区/轻链可变体组合的抗cd137抗原结合分子或抗体竞争与cd137结合的位点。
[0981]
在本公开的另一方面,根据以上任何实施方案的抗cd137抗原结合分子或抗体是单克隆抗体,包括嵌合抗体、人源化抗体或人抗体。在一个实施方案中,抗cd137抗体是抗体
片段,例如fv、fab、fab’、scfv、双体抗体或f(ab’)2片段。在另一个实施方案中,抗体是全长抗体,例如完整的igg1抗体或本文定义的其他抗体类型或同种型。
[0982]
在另一方面,根据任何以上实施方案的抗cd137抗原结合分子或抗体可以单独或组合地包含任何特征,如以下章节1-7中所述:
[0983]
1.抗cd137抗原结合分子或抗体的激动活性
[0984]
在具体的实施方案中,本公开中的抗cd137抗原结合分子或抗体具有cd137激动活性。cd137信号传导不仅刺激nk细胞的ifn-γ分泌和增殖(buechele等,2012;lin等,2008;melero等,1998),而且增强它们的存活率和由上调共刺激分子和细胞因子分泌表示的dc激活(choi等,2009;futagawa等,2002;wilcox等,2002)。但是,cd137最佳表征为在t细胞的cd4
+
和cd8
+
子集中调节tcr诱导的激活的共刺激分子。与tcr激活相组合,抗cd137激动剂抗体增强t细胞增殖、刺激淋巴因子分泌并降低t淋巴细胞对激活诱导的细胞死亡的敏感性(snelet等,2011年综述)。在这些现象中,cd137信号传导之后在t细胞上观察到的生理现象是由cd137信号传导激活的下游信号介导的,例如traf2、traf1,特别是nf-κb、jnk、erk、akt、存活蛋白(survivin)、bcl-xl和/或bcl-2(ward-kavanagh等,免疫(immunity),44:1005(2016))。
[0985]
在一个实施方案中,“抗cd137激动性抗原结合分子”或“抗cd137激动性抗体”是这样的抗原结合分子或抗体:其通过结合cd137而转导cd137信号并显著诱导或增强nk细胞的ifn-γ分泌、增殖和增加的存活率;由细胞因子分泌和共刺激分子的上调指示的dc激活;tcr诱导;t细胞增殖;和/或淋巴因子分泌。在不同的实施方案中,“抗cd137激动性抗原结合分子”或“抗cd137激动性抗体”是其通过与t细胞上的cd137结合来转导cd137信号,并显著诱导激活t细胞的nf-κb的抗原结合分子或抗体。此外,抗原结合分子或抗体“示出cd137激动活性”是指当抗原结合分子或抗体结合cd137时观察到任何上述生理现象。测量cd137激动活性的方法在下文的“c.测定”中详细描述。
[0986]
在具体的实施方案中,本公开中的抗cd137抗原结合分子或抗体具有小分子化合物依赖性cd137激动活性。在一个非限制性实施方案中,在存在小分子化合物的情况下,抗cd137抗原结合分子或抗体对cd137的cd137激动活性高于在不存在小分子化合物的情况下的cd137激动活性。在不同的实施方案中,与在低浓度小分子化合物存在下的cd137激动活性相比,在高浓度小分子化合物存在下抗cd137抗原结合分子或抗体的cd137激动活性更高。在进一步的实施方案中,在小分子化合物存在下,抗cd137抗原结合分子或抗体的cd137激动活性是不存在小分子化合物的情况下的cd137激动活性的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,100倍以上,200倍以上,300倍以上,500倍以上,1x103倍以上,2x103倍以上,3x103倍以上,5x103倍以上,1x104倍以上,2x104倍以上,3x104倍以上,5x104倍以上,或者1x105倍以上。
[0987]
可以选择任何合适的浓度作为小分子化合物的浓度,只要检测到抗cd137抗原结合分子或抗体的结合活性的差异即可。在一个实施方案中,抗cd137抗原结合分子或抗体通过与细胞表面上的cd137结合来转导cd137信号。因此,本领域技术人员将理解具有小分子化合物依赖性cd137结合活性的抗cd137抗原结合分子或抗体具有依赖于小分子化合物的cd137激动活性。然而,另一方面,由于测量结合活性和激动活性的方法不同,因此本领域技术人员将理解,检测到结合活性差异的小分子化合物的浓度可以不同于检测到激动活性差
异的小分子化合物的浓度(例如,对于在存在10μm小分子化合物时cd137结合活性是不存在小分子化合物的情况下的cd137结合活性的2倍以上的抗cd137抗原结合分子或抗体,在存在10μm小分子化合物的情况下的cd137激动活性(测定值)可以是在不存在小分子化合物的情况下cd137激动活性(测定值)的少于2倍)。此外,本领域技术人员将理解,激动活性的确定可以根据cd137激动活性的测定(参见“c.测定”)而变化。
[0988]
在一个实施方案中,抗cd137抗原结合分子或抗体(i)在存在10μm、50μm、100μm、150μm、200μm或250μm的小分子化合物的情况下,示出对cd137的激动活性,和(ii)在不存在小分子化合物的情况下对cd137基本上没有激动活性,或者在不存在小分子化合物的情况下对cd137具有低激动活性(与存在小分子化合物相比)。
[0989]
在一个实施方案中,当通过在“c.测定”中详细描述的“a)激动活性测定(pbmc)”评估抗cd137抗原结合分子或抗体的激动活性时,抗cd137抗原结合分子或抗体(i)在存在250μm小分子化合物的情况下对cd137表现出激动活性,和(ii)在不存在小分子化合物的情况下对cd137具有低激动作用(与存在小分子化合物时相比)。在进一步的实施方案中,抗cd137抗原结合分子或抗体(i)在存在250μm的小分子化合物的情况下对cd137表现出激动活性,并且(ii)在不存在小分子化合物的情况下对cd137表现出基本上无激动活性。
[0990]
在一个实施方案中,当通过在“c.测定”中详细描述的“b)激动活性测定(报告基因测定)”评价抗cd137抗原结合分子或抗体的激动活性时,抗cd137抗原结合分子或抗体(i)在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物时对cd137表现出激动活性,并且(ii)在不存在小分子化合物的情况下对cd137基本上没有激动活性或具有较低的激动活性(与在存在小分子化合物的情况下相比)。报告基因测定中的抗体浓度可以任意选择,例如抗体的终浓度为0、0.001、0.01、0.1、1或10μg/ml。在优选的实施方案中,抗体的终浓度为0.1μg/ml或1μg/ml。
[0991]
在一个实施方案中,当抗体的终浓度为0.1μg/ml时,在“c.测定”中详细描述的“b.激动活性测定(报告基因测定)”中,(i)在存在10μm小分子化合物的情况下,抗cd137抗原结合分子或抗体的cd137激动活性(相对光单位)是ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,60倍以上,70倍以上,80倍以上,或90倍以上高。在一个实施方案中,当在“c.测定”中详细描述的“b.激动活性测定(报告基因测定)”中,抗体的终浓度为0.1μg/ml时,(i)在存在100μm小分子化合物的情况下,抗cd137抗原结合分子或抗体的cd137激动活性(相对光单位)是ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,60倍以上,70倍以上,80倍以上,或90倍以上高。在一个实施方案中,当在“c.测定”中详细描述的“b.激动活性测法(报告基因测定)”中,抗体的终浓度为0.1μg/ml时,(i)在存在250μm小分子化合物的情况下,抗cd137抗原结合分子或抗体的cd137激动活性(相对光单位)是ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,60倍以上,70倍以上,80倍以上,或90倍以上高。在以上任何实施方案中,此外,在不存在小分子化合物的情况下,0.1μg/ml的抗cd137抗原结合分子或抗体基本上不示出cd137激动活性。
[0992]
在一个实施方案中,当抗体的最终浓度为“1μg/ml”时,在“c.测定”中详细描述的“b.激动活性测定(报告基因测定)”中,(i)在存在10μm小分子化合物的情况下,抗cd137抗原结合分子或抗体的cd137激动活性(相对光单位)是ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,60倍以上,70倍以上,80倍以上,或90倍以上高。在一个实施方案中,当抗体的终浓度为0.1μg/ml时,在“c.测定”中详细描述的“b.激动活性测定(报告基因测定)”中,(i)在存在100μm小分子化合物的情况下,抗cd137抗原结合分子或抗体的cd137激动活性(相对光单位)是ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,60倍以上,70倍以上,80倍以上,或90倍以上高。在一个实施方案中,当抗体的终浓度为0.1μg/ml时,在“c.测定”中详细描述的“b.激动活性测定(报告基因测定)”中(i)在存在250μm小分子化合物的情况下,抗cd137抗原结合分子或抗体的cd137激动活性(相对光单位)是ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的2倍以上,3倍以上,5倍以上,10倍以上,20倍以上,30倍以上,50倍以上,60倍以上,70倍以上,80倍以上,或90倍以上高。在以上任何一个实施方案中,此外,在不存在小分子化合物的情况下,1μg/ml的抗cd137抗原结合分子或抗体基本上不示出cd137激动活性。
[0993]
2.抗体片段
[0994]
在某些实施方案中,本文提供的抗体是抗体片段。抗体片段包括但不限于fab、fab’、fab
’‑
sh、f(ab’)2、fv和scfv片段,以及以下描述的其他片段。有关某些抗体片段的综述,请参见hudson等,nat.med.,9:129-134(2003)。对于scfv片段的综述,请参见例如pluckthun,单克隆抗体的药理学,卷113,rosenburg和moore eds.,(springer-verlag,纽约),第269-315页(1994);还参见wo 93/16185;美国专利号5,571,894和5,587,458。关于包含拯救受体结合表位残基并具有增加的体内半衰期的fab和f(ab')2片段的讨论,参见美国专利号5,869,046。
[0995]
双体抗体是具有两个抗原结合位点的抗体片段,可以是二价或双特异性的。参见例如ep 404,097;wo 1993/01161;hudson等,nat.med.,9:129-134(2003);和hollinger等,proc.natl.acad.sci.usa,90:6444-6448(1993)。三体抗体和四体抗体也描述于hudson等,nat.med.9:129-134(2003)中。
[0996]
单域抗体是包含抗体的全部或部分重链可变结构域或全部或部分轻链可变结构域的抗体片段。在某些实施方案中,单域抗体是人单域抗体(domantis,inc.,waltham,ma;参见,例如,美国专利号6,248,516b1)。
[0997]
抗体片段可通过多种技术制备,包括但不限于完整抗体的蛋白水解消化以及由重组宿主细胞(例如大肠杆菌或噬菌体)产生,如本文所述。
[0998]
3.嵌合抗体和人源化抗体
[0999]
在某些实施方案中,本文提供的抗体是嵌合抗体。某些嵌合抗体描述于例如美国专利号4,816,56;和morrison等,proc.natl.acad.sci.usa,81:6851-6855(1984))。在一个实例中,嵌合抗体包含非人可变区(例如,衍生自小鼠,大鼠,仓鼠,兔或非人灵长类动物,例如猴子的可变区)和人恒定区。在另一个实例中,嵌合抗体是其中类别或亚类已经从亲本抗体的类别或亚类发生改变的“类别转换”抗体。嵌合抗体包括其抗原结合片段。
[1000]
在某些实施方案中,嵌合抗体是人源化抗体。通常,非人抗体被人源化以降低对人
的免疫原性,同时保留亲本非人抗体的特异性和亲和力。通常,人源化抗体包含一个或多个可变结构域,其中hvr例如cdr(或其部分)衍生自非人抗体,并且fr(或其部分)衍生自人抗体序列。人源化抗体任选地还将包含人恒定区的至少一部分。在一些实施方案中,人源化抗体中的一些fr残基被来自非人抗体(例如,hvr残基所源自的抗体)的相应残基置换,例如以恢复或改善抗体特异性或亲和力。
[1001]
人源化抗体及其制备方法例如在almagro和fransson,front.biosci.13:1619-1633(2008)中进行了综述,并进一步描述于例如riechmann等,自然(nature)332:323-329(1988);queen等,proc.nat’l acad.sci.usa86:10029-10033(1989);us专利号5,821,337、7,527,791、6,982,321和7,087,409;kashmiri等,方法(methods)36:25-34(2005)(描述了特异性决定区(sdr)移植);padlan,mol.immunol.28:489-498(1991)(描述“重铺”);dall’acqua等,方法(methods)36:43-60(2005)(描述“fr改组”);和osbourn等,方法(methods)36:61-68(2005)和klimka等,br.j.cancer,83:252-260(2000)(描述了fr改组的“指导选择”方法)中。
[1002]
可以用于人源化的人框架区包括但不限于:使用“最佳拟合”方法选择的框架区(参见,例如,sims等,j.immunol.151:2296(1993));和从轻链可变区或重链可变区的特定亚组的人抗体的共有序列衍生的框架区(参见,例如,carter等,proc.natl.acad.sci.usa,89:4285(1992);和presta等,j.immunol.,151:2623(1993));人成熟的(体细胞突变的)框架区或人种系框架区(参见,例如,almagro和fransson,front.biosci.13:1619-1633(2008));源自筛选fr文库的框架区(参见,例如,baca等,j.biol.chem.272:10678-10684(1997)和rosok等,j.biol.chem.271:22611-22618(1996))。
[1003]
4.人抗体
[1004]
在某些实施方案中,本文提供的抗体是人抗体。可以使用本领域已知的多种技术来产生人抗体。人抗体通常在van dijk和van de winkel,curr.opin.pharmacol.5:368-74(2001)和lonberg,curr..opin.immunol.20:450-459(2008)中描述。
[1005]
人抗体可以通过将免疫原施用于转基因动物来制备,该转基因动物已经被修饰以响应抗原攻击而产生完整的人抗体或具有人可变区的完整抗体。此类动物通常包含全部或部分人类免疫球蛋白基因座,它们取代了内源性免疫球蛋白基因座,或者存在于染色体外或随机整合到动物的染色体中。在这种转基因小鼠中,内源性免疫球蛋白基因座通常已被失活。对于从转基因动物中获得人抗体的方法的综述,请参见lonberg,nat.biotech.23:1117-1125(2005)。还参见例如描述xenomouse
tm
技术的美国专利号6,075,181和6,150,584;描述humab(注册商标)技术的美国专利5,770,429;描述了k-m mouse(注册商标)技术的美国专利号7,041,870,以及描述了velocimouse(注册商标)技术的美国专利申请公开号us 2007/0061900)。来自这类动物产生的完整抗体的人可变区可以被进一步修饰,例如通过与不同的人恒定区结合。
[1006]
人抗体也可以通过基于杂交瘤的方法制备。已经描述了用于产生人单克隆抗体的人骨髓瘤和小鼠-人异源骨髓瘤细胞系。(参见,例如,kozbor j.immunol.,133:3001(1984);brodeur等,单克隆抗体生产技术和应用,第51-63页(marcel dekker,inc.,纽约,1987);和boerner li等,j.immunol.,147:86(1991))。通过人b细胞杂交瘤技术产生的人抗体描述在li等,proc.natl.acad.sci.usa,103:3557-3562(2006)中。另外的方法包括例如
在美国专利号7,189,826(描述从杂交瘤细胞系生产单克隆人igm抗体)和ni,xiandai mianyixue,26(4):265-268(2006)(描述人-人杂交瘤)中描述的那些方法。人杂交瘤技术(trioma技术)也描述于vollmers和brandlein,组织学和组织病理学,20(3):927-937(2005)和vollmers和brandlein,实验和临床药理学的方法和发现,27(3):185-91(2005)中。
[1007]
人抗体还可以通过分离选自人源噬菌体展示文库的fv克隆可变结构域序列来产生。然后可以将此类可变结构域序列与所需的人恒定结构域结合。从抗体库中选择人抗体的技术描述如下。
[1008]
5.源自文库的抗体
[1009]
可通过筛选组合文库中具有所需活性或多种活性的抗体来分离本公开的抗体。例如,本领域已知多种方法用于产生噬菌体展示文库并筛选此类文库中具有所需结合特性的抗体。此类方法在例如hoogenboom等,分子生物学方法,178:1-37(o’brien等编辑,人类出版社(human press),新泽西州托托瓦市,2001)中进行了综述,并在如下中进一步描述:例如,mccafferty等,自然(nature),348:552-554;clackson等,自然(nature),352:624-628(1991);marks等,j.mol.biol.222:581-597(1992);marks和bradbury,methods in molecular biology,248:161-175(lo,ed.,人类出版社(human press),新泽西州托托瓦市,2003);sidhu等,j.mol.biol.,338(2):299-310(2004);lee等,j.mol.biol.340(5):1073-1093(2004);fellouse,proc.natl.acad.sci.usa 101(34):12467-12472(2004)和lee等,j.immunol.methods,284(1-2):119-132(2004)。
[1010]
在某些噬菌体展示方法中,通过聚合酶链式反应(pcr)分别克隆vh和vl基因库,并在噬菌体文库中随机重组,然后可以按照winter等,ann.rev.immunol.,12:433-455(1994)中所描述的筛选抗原结合噬菌体。噬菌体通常展示抗体片段,呈单链fv(scfv)片段或fab片段。来自免疫源的文库无需构建杂交瘤即可提供针对免疫原的高亲和力抗体。备选地,可以如griffiths等,embo j.,12:725-734(1993)所描述的那样,克隆幼稚库(例如,从人)以提供针对广泛的非自身以及自身抗原的抗体的单一来源,而无需任何免疫。最后,如hoogenboom和winter,j.mol.biol.,227:381-388(1992)中所描述的,还可以通过从干细胞克隆未重排的v基因片段,并使用包含随机序列的pcr引物来编码高度可变的cdr3区并在体外完成重排,来合成幼稚文库。描述人抗体噬菌体文库的专利出版物包括,例如:美国专利号5,750,373和美国专利公开号2005/0079574、2005/0119455、2005/0266000、2007/0117126、2007/0160598、2007/0237764、2007/0292936和2009/0002360。
[1011]
从人抗体文库分离的抗体或抗体片段在本文中被认为是人抗体或人抗体片段。
[1012]
可以通过在抗原结合分子的文库上进行筛选来选择本公开的具有依赖于低分子量化合物的抗原结合活性的抗原结合分子或抗体。作为这样的文库,可以使用上述组合文库。抗原结合分子的文库可以是具有无偏差的抗原结合分子的文库(幼稚文库),或者可以是具有偏差的抗原结合分子的文库。后一种类型的文库的实例包括预先赋予针对特定化合物的结合活性的抗原结合分子文库。在某个实施方案中,抗原结合分子文库是预先向其引入赋予特定化合物结合活性的氨基酸改变的抗原结合分子的文库。这种类型的文库的实例包括例如在国际公开wo 2015/083764中描述的文库。
[1013]
6.多特异性抗体
1,dna酶,dpp,dppiv/cd26,dtk,ecad,eda,eda-a1,eda-a2,edar,egf,egfr(erbb-1),ema,emmprin,ena,内皮素受体,脑啡肽酶,enos,eot,嗜酸细胞活化趋化因子1,epcam,肝配蛋白b2/ephb4,epo,ercc,e-选择蛋白,et-1,因子iia,因子vii,因子viiic,因子ix,纤维细胞活化蛋白(fap),fas,fcr1,fen-1,铁蛋白,fgf,fgf-19,fgf-2,fgf-3,fgf-8,fgfr,fgfr-3,纤维蛋白,fl,flip,flt-3,flt-4,促卵胞激素,cxxxc趋化分子(fractalkine),fzd1,fzd2,fzd3,fzd4,fzd5,fzd6,fzd7,fzd8,fzd9,fzd10,g250,gas6,gcp-2,gcsf,gd2,gd3,gdf,gdf-1,gdf-3(vgr-2),gdf-5(bmp-14,cdmp-1),gdf-6(bmp-13,cdmp-2),gdf-7(bmp-12,cdmp-3),gdf-8(肌骨素),gdf-9,gdf-15(mic-1),gdnf,gdnf,gfap,gfra-1,gfr-α1,gfr-α2,gfr-α3,gitr,胰高血糖素,glut4,糖蛋白iib/iiia(gpiib/iiia),gm-csf,gp130,gp72,gro,生长激素释放激素,半抗原(np-cap或nip-cap),hb-egf,hcc,hcmv gb包膜糖蛋白,hcmv gh包膜糖蛋白,hcmv ul,造血生长因子(hgf),hep b gp120,类肝素酶,her2,her2/neu(erbb-2),her3(erbb-3),her4(erbb-4),单纯疱疹病毒(hsv)gb糖蛋白,hsv gd糖蛋白,hgfa,高分子量黑色素瘤相关抗原(hmw-maa),hiv gp120,hiv iiib gp 120v3环,hla,hla-dr,hm1.24,hmfg pem,hrg,hrk,人心脏肌球蛋白,人巨细胞病毒(hcmv),人类生长激素(hgh),hvem,i-309,iap,icam,icam-1,icam-3,ice,icos,ifng,ig,iga受体,ige,igf,igf结合蛋白,igf-1r,igfbp,igf-i,igf-ii,il,il-1,il-1r,il-2,il-2r,il-4,il-4r,il-5,il-5r,il-6,il-6r,il-8,il-9,il-10,il-12,il-13,il-15,il-18,il-18r,il-21,il-23,il-27,干扰素(inf)-α,inf-β,inf-γ,抑制素,inos,胰岛素a链,胰岛素b链,胰岛素样生长因子1,整联蛋白α2,整联蛋白α3,整联蛋白α4,整联蛋白α4/β1,整联蛋白α4/β7,整联蛋白α5(αv),整联蛋白α5/β1,整联蛋白α5/β3,整联蛋白α6,整联蛋白β1,整联蛋白β2,干扰素γ,ip-10,i-tac,je,激肽释放酶2,激肽释放酶5,激肽释放酶6,激肽释放酶11,激肽释放酶12,激肽释放酶14,激肽释放酶15,激肽释放酶l1,激肽释放酶l2,激肽释放酶l3,激肽释放酶l4,kc,kdr,角质化细胞生长因子(kgf),层粘连蛋白5,lamp,lap,lap(tgf-1),潜伏性tgf-1,潜伏性tgf-1bp1,lbp,ldgf,lect2,lefty,lewis-y抗原,lewis-y相关抗原,lfa-1,lfa-3,lfo,lif,light,脂蛋白,lix,lkn,lptn,l-选择蛋白,lt-a,lt-b,ltb4,ltbp-1,肺表面,黄体生成素,淋巴毒素β受体,mac-1,madcam,mag,map2,marc,mcam,mcam,mck-2,mcp,m-csf,mdc,mer,metalloproteases,mgdf受体,mgmt,mhc(hla-dr),mif,mig,mip,mip-1-α,mk,mmac1,mmp,mmp-1,mmp-10,mmp-11,mmp-12,mmp-13,mmp-14,mmp-15,mmp-2,mmp-24,mmp-3,mmp-7,mmp-8,mmp-9,mpif,mpo,msk,msp,粘蛋白(muc1),muc18,米勒氏管抑制物质,mug,musk,naip,nap,ncad,n-c粘附素(adherin),nca90,ncam,ncam,脑啡肽酶(neprilysin),神经营养因子-3,-4,或-6,神经秩蛋白(neurturin),神经生长因子(ngf),ngfr,ngf-β,nnos,no,nos,npn,nrg-3,nt,ntn,ob,ogg1,opg,opn,osm,ox40l,ox40r,p150,p95,padpr,甲状旁腺素,parc,parp,pbr,pbsf,pcad,p-钙粘蛋白,pcna,pdgf,pdgf,pdk-1,pecam,pem,pf4,pge,pgf,pgi2,pgj2,pin,pla2,胎盘碱性磷酸酶(plap),plgf,plp,pp14,胰岛素原,prorelaxin,蛋白c,ps,psa,psca,前列腺特异性膜抗原(psma),pten,pthrp,ptk,ptn,r51,rank,rankl,rantes,rantes,松弛素a链,松弛素b链,肾素,呼吸道合胞病毒(rsv)f,rsv fgp,ret,类风湿因子,rlip76,rpa2,rsk,s100,scf/kl,sdf-1,serine,血清白蛋白,sfrp-3,shh,sigirr,sk-1,slam,slpi,smac,smdf,smoh,sod,sparc,stat,steap,steap-ii,tace,taci,tag-72(肿瘤相关糖蛋白-72),tarc,tca-3,t细胞受体(例如,t细胞
受体α/β),tdt,teck,tem1,tem5,tem7,tem8,tert,睾丸plap样碱性磷酸酶,tfr,tgf,tgf-α,tgf-β,tgf-β泛特异性,tgf-βri(alk-5),tgf-βrii,tgf-βriib,tgf-βriii,tgf-β1,tgf-β2,tgf-β3,tgf-β4,tgf-β5,凝血酶,胸腺ck-1,促甲状腺激素,tie,timp,tiq,组织因子,tmeff2,tmpo,tmprss2,tnf,tnf-α,tnf-αβ,tnf-β2,tnfc,tnf-ri,tnf-rii,tnfrsf10a(trail r1 apo-2,dr4),tnfrsf10b(trail r2 dr5,killer,trick-2a,trick-b),tnfrsf10c(trail r3 dcr1,lit,trid),tnfrsf10d(trail r4 dcr2,trundd),tnfrsf11a(rank odf r,trance r),tnfrsf11b(opg ocif,tr1),tnfrsf12(tweak r fn14),tnfrsf13b(taci),tnfrsf13c(baff r),tnfrsf14(hvem atar,hvea,light r,tr2),tnfrsf16(ngfr p75ntr),tnfrsf17(bcma),tnfrsf18(gitr aitr),tnfrsf19(troy taj,trade),tnfrsf19l(relt),tnfrsf1a(tnf ri cd120a,p55-60),tnfrsf1b(tnf rii cd120b,p75-80),tnfrsf26(tnfrh3),tnfrsf3(ltbr tnf riii,tnfc r),tnfrsf4(ox40act35,txgp1r),tnfrsf5(cd40p50),tnfrsf6(fas apo-1,apt1,cd95),tnfrsf6b(dcr3m68,tr6),tnfrsf7(cd27),tnfrsf8(cd30),tnfrsf9(4-1bb cd137,ila),tnfrsf21(dr6),tnfrsf22(dctrail r2tnfrh2),tnfrst23(dctrail r1tnfrh1),tnfrsf25(dr3apo-3,lard,tr-3,tramp,wsl-1),tnfsf10(trail apo-2配体,tl2),tnfsf11(trance/rank配体odf,opg配体),tnfsf12(tweak apo-3配体,dr3配体),tnfsf13(april tall2),tnfsf13b(baff blys,tall1,thank,tnfsf20),tnfsf14(light hvem配体,ltg),tnfsf15(tl1a/vegi),tnfsf18(gitr配体aitr配体,tl6),tnfsf1a(tnf-a conectin,dif,tnfsf2),tnfsf1b(tnf-b lta,tnfsf1),tnfsf3(ltb tnfc,p33),tnfsf4(ox40配体gp34,txgp1),tnfsf5(cd40配体cd154,gp39,higm1,imd3,trap),tnfsf6(fas配体apo-1配体,apt1配体),tnfsf7(cd27配体cd70),tnfsf8(cd30配体cd153),tnfsf9(4-1bb配体cd137配体),tp-1,t-pa,tpo,trail,trail r,trail-r1,trail-r2,trance,转铁蛋白受体,trf,trk,trop-2,tlr1(toll样受体1),tlr2,tlr3,tlr4,tlr5,tlr6,tlr7,tlr8,tlr9,tlr10,tsg,tslp,肿瘤相关抗原ca125,肿瘤相关抗原表达lewis-y相关碳水化合物,tweak,txb2,ung,upar,upar-1,尿激酶,vcam,vcam-1,vecad,ve-钙粘蛋白,ve-钙粘蛋白-2,vefgr-1(flt-1),vegf,vegfr,vegfr-3(flt-4),vegi,vim,病毒抗原,vla,vla-1,vla-4,vnr整联蛋白,血管假性血友病因子,wif-1,wnt1,wnt2,wnt2b/13,wnt3,wnt3a,wnt4,wnt5a,wnt5b,wnt6,wnt7a,wnt7b,wnt8a,wnt8b,wnt9a,wnt9b,wnt10a,wnt10b,wnt11,wnt16,xcl1,xcl2,xcr1,xedar,xiap,xpd,hmgb1,iga,aβ,cd81,cd97,cd98,ddr1,dkk1,ereg,hsp90,il-17/il-17r,il-20/il-20r,氧化的ldl,pcsk9,前激肽释放酶,ron,tmem16f,sod1,嗜铬粒蛋白a,嗜铬粒蛋白b,tau,vap1,高分子量激肽原,il-31,il-31r,nav1.1,nav1.2,nav1.3,nav1.4,nav1.5,nav1.6,nav1.7,nav1.8,nav1.9,epcr,c1,c1q,c1r,c1s,c2,c2a,c2b,c3,c3a,c3b,c4,c4a,c4b,c5,c5a,c5b,c6,c7,c8,c9,因子b,因子d,因子h,备解素,骨硬化蛋白(sclerostin),纤维蛋白原,纤维蛋白,凝血酶原,凝血酶,组织因子,因子v,因子va,因子vii,因子viia,因子viii,因子viiia,因子ix,因子ixa,因子x,因子xa,因子xi,因子xia,因子xii,因子xiia,因子xiii,因子xiiia,tfpi,抗凝血酶iii,epcr,血栓调节蛋白,tapi,tpa,纤溶酶原,纤维蛋白溶酶,pai-1,pai-2,gpc3,多配体聚糖-1,多配体聚糖-2,多配体聚糖-3,多配体聚糖-4,lpa,和s1p。在一些实施方案中,抗原的实例包括激素受体和生长因子。在某些实施方案中,抗原是在存在于肿瘤组织中的细胞(例如,肿瘤细胞、免疫细胞、基质细胞等)中表达或分泌
的那些。
[1017]
制备多特异性抗体的技术包括但不限于具有不同特异性的两个免疫球蛋白重链-轻链对的重组共表达(参见milstein和cuello,自然(nature),305:537(1983)、wo 93/08829和traunecker等,embo j.10:3655(1991)),和“杵臼”(knob-in-hole)工程改造(参见,例如,美国专利号5,731,168)。多特异性抗体也可以通过以下方法来制备:工程化静电转向效应用于制备抗体fc-异二聚体分子(wo 2009/089004a1);交联两种或更多种抗体或片段(参见,例如,美国专利号4,676,980和brennan等,科学(science),229:81(1985));使用亮氨酸拉链产生双特异性抗体(参见例如kostelny等,j.immunol.148(5):1547-1553(1992));使用“双体抗体”技术制备双特异性抗体片段(参见,例如,hollinger等,美国国家科学院院刊(proc.natl.acad.sci.usa),90:6444-6448(1993));和使用单链fv(scfv)二聚体(参见,例如,gruber等,j.immunol.,152:5368(1994));和如例如tutt等,免疫学杂志(j.immunol.),147:60(1991)中所述制备三特异性抗体。
[1018]
本文还包括具有三个或多个功能性抗原结合位点的工程抗体,包括“章鱼抗体”(参见例如us 2006/0025576a1)。
[1019]
本文的抗体或片段还包括“双重作用fab”或“daf”,其包含与cd137以及另一种不同抗原结合的抗原结合位点(例如,参见us 2008/0069820)。
[1020]
7.抗体变体
[1021]
在某些实施方案中,考虑了本文提供的抗体的氨基酸序列变体。例如,可能需要改善抗体的结合亲和力和/或其他生物学特性。可以通过将适当的修饰引入编码抗体的核苷酸序列中,或通过肽合成来制备抗体的氨基酸序列变体。此类修饰包括,例如,抗体氨基酸序列内残基的缺失和/或插入和/或置换。可以进行缺失、插入和置换的任何组合以获得最终的构建体,条件是最终的构建体具有所需的特性,例如抗原结合。
[1022]
a)置换、插入和缺失变体
[1023]
在某些实施方案中,提供了具有一个或多个氨基酸置换的抗体变体。用于置换性诱变的感兴趣位点包括hvr和fr。保守置换显示于表5的“优选置换”标题下。表5在“示例性置换”的标题下提供了更实质性的变化,并且如以下参考氨基酸侧链类别进所一步描述的。可以将氨基酸置换引入感兴趣的抗体中,并筛选所需活性的产物,例如,保留/改善的抗原结合,降低的免疫原性或改善的adcc或cdc。
[1024]
[表5]
[1025]
原始残基示例性置换优选置换ala(a)val;leu;ilevalarg(r)lys;gln;asnlysasn(n)gln;his;asp;lys;argglnasp(d)glu;asnglucys(c)ser;alasergln(q)asn;gluasnglu(e)asp;glnaspgly(g)alaalahis(h)asn;gln;lys;argarg
ile(i)leu;val;met;ala;phe;正亮氨酸leuleu(l)正亮氨酸;ile;val;met;ala;pheilelys(k)arg;gln;asnargmet(m)leu;phe;ileleuphe(f)trp;leu;val;ile;ala;tyrtyrpro(p)alaalaser(s)thrthrthr(t)val;sersertrp(w)tyr;phetyrtyr(y)trp;phe;thr;serpheval(v)ile;leu;met;phe;ala;正亮氨酸leu
[1026]
氨基酸可以根据常见的侧链特性进行分组:
[1027]
(1)疏水性的:正亮氨酸、met、ala、val、leu、ile;
[1028]
(2)中性亲水性:cys、ser、thr、asn、gln;
[1029]
(3)酸性的:asp、glu;
[1030]
(4)碱性的:his、lys、arg;
[1031]
(5)影响链取向的残基:gly、pro;
[1032]
(6)芳香族:trp、tyr、phe。
[1033]
非保守置换将使得将这些类别中的一个类别的成员交换为另一个类别。
[1034]
一种类型的置换变体涉及置换亲本抗体(例如人源化或人抗体)的一个或多个高变区残基。通常,选择用于进一步研究的所得变体将相对于亲本抗体在某些生物学特性(例如,增加的亲和力,降低的免疫原性)上具有修饰(例如,改进),和/或将基本上保留了亲本抗体的某些生物学特性。示例性的置换变体是亲和力成熟的抗体,其可以方便地产生,例如,使用基于噬菌体展示的亲和力成熟技术,例如本文所描述的那些。简而言之,将一个或多个hvr残基突变,并将变体抗体展示在噬菌体上并筛选特定的生物学活性(例如结合亲和力)。
[1035]
可以在hvr中进行改变(例如置换),例如以改善抗体亲和力。这样的改变可以在hvr“热点”中进行,即由在体细胞成熟过程中以高频发生突变的密码子编码的残基中(参见,例如,chowdhury,分子生物学方法(methods mol.biol.),207:179-196(2008)),和/或与抗原接触的残基,测试所得的变体vh或vl的结合亲和力。通过构建二级文库并从二级文库中重选择来进行的亲和力成熟描述于例如hoogenboom等,分子生物学方法(methods in molecular biology),178:1-37(o'brien等,人类出版社(human press),新泽西州托托瓦市,(2001))中。在亲和力成熟的一些实施方案中,通过多种方法中的任何一种(例如,易错pcr,链改组或寡核苷酸定向突变)将多样性引入被选择用于成熟的可变基因中。然后创建二级文库。然后筛选该文库以鉴定具有所需亲和力的任何抗体变体。引入多样性的另一种方法涉及hvr定向方法,其中几个hvr残基(例如一次4-6个残基)被随机化。可以例如使用丙氨酸扫描诱变或建模来特异性地鉴定涉及抗原结合的hvr残基。特别是cdr-h3和cdr-l3通常是靶向的。
[1036]
在某些实施方案中,置换、插入或缺失可在一个或多个hvr内发生,只要这种改变
基本上不降低抗体结合抗原的能力。例如,可以在hvr中进行基本上不降低结合亲和力的保守改变(例如,本文提供的保守置换)。这样的改变可以例如在hvr中的抗原接触残基之外。在上文提供的变体vh和vl序列的某些实施方案中,每个hvr要么保持不变,要么包含不超过一个、两个或三个氨基酸置换。
[1037]
如cunningham和wells(1989),科学(science),244:1081-1085所描述的,用于鉴定可被靶向诱变的抗体的残基或区域的有用方法称为“丙氨酸扫描诱变”。在该方法中,鉴定靶残基的残基或基团(例如带电荷的残基,例如arg,asp,his,lys和glu),并用中性或带负电荷的氨基酸(例如丙氨酸或聚丙氨酸)取代,以确定抗体与抗原的相互作用是否受到影响。可以在对初始置换显示功能敏感性的氨基酸位置处引入进一步的置换。替代地或另外地,可以分析抗原-抗体复合物的晶体结构以鉴定抗体和抗原之间的接触点。这样的接触残基和邻近残基可以被靶向或消除作为置换的候选物。可以筛选变体以确定它们是否包含所需的特性。
[1038]
氨基酸序列插入包括长度为一个残基至包含百个或更多个残基的多肽的范围内的氨基和/或羧基末端融合,以及单个或多个氨基酸残基的序列内插入。末端插入的实例包括具有n末端甲硫氨酰基残基的抗体。抗体分子的其他插入变体包括酶(例如,对于adept)或增加抗体的血浆半衰期的多肽与抗体的n-末端或c-末端的融合。
[1039]
b)糖基化变体
[1040]
在某些实施方案中,本文提供的抗体被改变以增加或减少抗体被糖基化的程度。可以通过改变氨基酸序列以产生或去除一个或多个糖基化位点来方便地实现抗体中糖基化位点的添加或缺失。
[1041]
当抗体包含fc区时,与其相连的碳水化合物可以被改变。由哺乳动物细胞产生的天然抗体通常包含分支的双触角寡糖,其通常通过n-键连接至fc区ch2结构域的asn297。参见,例如,wright等,tibtech,15:26-32(1997)。寡糖可包括各种碳水化合物,例如,甘露糖、n-乙酰基葡糖胺(glcnac)、半乳糖和唾液酸,以及附着于双触角寡糖结构的“茎”中的glcnac的岩藻糖。在一些实施方案中,可以对本公开的抗体中的寡糖进行修饰,以产生具有某些改善的特性的抗体变体。
[1042]
在一个实施方案中,提供了具有碳水化合物结构的抗体变体,该碳水化合物结构缺少(直接或间接)连接至fc区的岩藻糖。例如,此类抗体中的岩藻糖含量可以为1%至80%,1%至65%,5%至65%或20%至40%。岩藻糖的量是通过计算糖链中asn297处岩藻糖的平均量相对于与asn 297附接的所有糖结构(例如,复合、杂合和高甘露糖结构)的总和来确定的,如通过maldi-tof质谱所测量的,例如,如wo 2008/077546中所述。asn297是指位于fc区中约297位的天冬酰胺残基(fc区残基的eu编号)。然而,由于抗体的微小序列变化,asn297也可以位于位置297上游或下游大约+/-3个氨基酸,即在位置294和300之间。这样的岩藻糖基化变体可以具有改善的adcc功能。参见,例如,美国专利公开号us 2003/0157108(presta,l.);us 2004/0093621(kyowa hakko kogyo公司)。与“去岩藻糖基化的”或“岩藻糖缺陷的”抗体变体有关的出版物的实例包括:us 2003/0157108;wo 2000/61739;wo 2001/29246;us 2003/0115614;us 2002/0164328;us 2004/0093621;us 2004/0132140;us2004/0110704;us 2004/0110282;us 2004/0109865;wo 2003/085119;wo 2003/084570;wo 2005/035586;wo 2005/035778;wo2005/053742;wo2002/031140;okazaki等,
j.mol.biol.336:1239-1249(2004);yamane-ohnuki等,生物技术生物工程(biotech.bioeng.),87:614(2004)。能够产生去岩藻糖基化抗体的细胞系的实例包括蛋白质岩藻糖基化缺陷的lec13cho细胞(ripka等,arch.biochem.biophys.249:533-545(1986);美国专利申请号us 2003/0157108 a1,presta,l.;和wo 2004/056312 a1,adams等,尤其是实施例11),以及敲除细胞系,例如α-1,6-岩藻糖基转移酶基因fut8,敲除cho细胞(参见,例如yamane-ohnuki等,生物技术生物工程(biotech.bioeng.),87:614(2004);kanda,y.等,生物技术生物工程(biotech.bioeng.),94(4):680-688(2006);和wo2003/085107)。
[1043]
抗体变体进一步提供有分叉的寡糖,例如,其中附接于抗体fc区的双触角寡糖被glcnac分叉。这样的抗体变体可以具有减少的岩藻糖基化和/或改善的adcc功能。此类抗体变体的实例描述于例如wo2003/011878(jean-mairet等);美国专利号6,602,684(umana等);和us2005/0123546(umana等)。还提供了在附接至fc区的寡糖中具有至少一个半乳糖残基的抗体变体。这样的抗体变体可以具有改善的cdc功能。此类抗体变体描述于例如wo 1997/30087(patel等);wo 1998/58964(raju,s.);和wo 1999/22764(raju,s.)。
[1044]
c)fc区变体
[1045]
在某些实施方案中,可以将一种或多种氨基酸修饰引入本文提供的抗体的fc区中,从而产生fc区变体(也可以称为“改变的fc区”)。fc区变体可包含在一个或多个氨基酸位置包含氨基酸改变(例如置换)的人fc区序列(例如人igg1、igg2、igg3或igg4fc区)。
[1046]
在某些实施方案中,本公开内容考虑了具有一些但不是全部效应子功能的抗体变体,这使其成为其中抗体的体内半衰期很重要而某些效应子功能(例如补体和adcc)是不必要或有害的应用的所需候选者。可以进行体外和/或体内细胞毒性测定,以确认cdc和/或adcc活性的降低/消耗。例如,可以进行fc受体(fcr)结合测定以确保抗体缺乏fcγr结合(因此可能缺乏adcc活性),但是保留fcrn结合活性。介导adcc的主要细胞nk细胞仅表达fcγriii,而单核细胞表达fcγri、fcγrii和fcγriii。ravetch和kinet,annu.rev.immunol.9:457-492(1991)第464页表3总结了造血细胞上的fcr表达。评估目的分子的adcc活性的体外测定法的非限制性实例描述于美国专利号5,500,362中(参见,例如,hellstrom,i.等,proc.nat'l acad.sci.usa 83:7059-7063(1986))和hellstrom,i等,proc.nat'l acad.sci.usa 82:1499-1502(1985);5,821,337(参见bruggemann,m.等,j.exp.med.166:1351-1361(1987))。可替代地,可以采用非放射性测定方法(例如,参见用于流式细胞术的act1
tm
非放射性细胞毒性测定法(加利福尼亚州山景城的celltechnology公司;和cytotox 96(注册商标)非放射性细胞毒性测定法(promega,密歇根麦迪逊)。用于这种测定的有用的效应细胞包括外周血单核细胞(pbmc)和自然杀伤(nk)细胞。或者,此外,可以在体内,例如在clynes等人的美国国家科学院院刊(proc.nat'l acad.sci.usa)95:652-656(1998)中公开的动物模型中评估目标分子的adcc活性。也可以进行c1q结合测定以证实抗体不能结合c1q,因此缺乏cdc活性。参见,例如,wo 2006/029879和wo 2005/100402中的c1q和c3c结合elisa。为了评估补体激活,可以进行cdc测定(参见,例如,gazzano-santoro等,免疫方法杂志(j.immunol.methods),202:163(1996);cragg,m.s.等,血液(blood),101:1045-1052(2003);和cragg,m.s.和m.j.glennie,血液(blood),103:2738-2743(2004))。还可使用本领域已知的方法进行fcrn结合和体内清除/半衰期的确定(参见,
例如,petkova,s.b.等,国际免疫学(int'l.immunol.),18(12):1759-1769(2006))。
[1047]
具有降低的效应子功能的抗体包括那些具有fc区残基238、265、269、270、297、327和329中的一个或多个置换的抗体(美国专利号6,737,056)。这样的fc突变体包括在两个或更多个氨基酸位置265、269、270、297和327处具有置换的fc突变体,包括所谓的“dana”fc突变体,其残基265和297被置换为丙氨酸(美国专利号7,332,581)。
[1048]
描述了与fcr的结合增加或减少的某些抗体变体(参见,例如,美国专利号6,737,056;wo 2004/056312,以及shields等,j.biol.chem.9(2):6591-6604(2001)。)
[1049]
在某些实施方案中,抗体变体包含具有改善adcc的一个或多个氨基酸置换的fc区,例如,在fc区的298、333和/或334位的置换(残基的eu编号)。
[1050]
在一些实施方案中,例如,如美国专利号6,194,551、wo 99/51642以及idusogie等,免疫学杂志(j.immunol.),164:4178-4184(2000)中所述,在fc区中进行改变,导致改变的(即,增加或减少的)c1q结合和/或补体依赖性细胞毒性(cdc)。
[1051]
具有延长的半衰期和增加的与新生儿fc受体(fcrn)的结合的抗体,负责将母体igg转移至胎儿(guyer等,免疫学杂志(j.immunol.),117:587(1976)和kim等,免疫学杂志(j.immunol.),24:249(1994))描述于us2005/0014934a1(hinton等)中。那些抗体包含其中具有一个或多个置换的fc区,所述置换增加fc区与fcrn的结合。此类fc变体包括以下一个或多个fc区残基被置换的fc变体:238、256、265、272、286、303、305、307、311、312、317、340、356、360、362、376、378、380、382、413、424或434,例如fc区残基434的置换(美国专利号7,371,826)。
[1052]
还参见duncan&winter,自然(nature),322:738-40(1988);美国专利号5,648,260;美国专利号5,624,821;和关于fc区变体的其他实例的wo 94/29351。
[1053]
在一个实施方案中,抗体fc区(包括变体fc区(以下同样适用))对每个人fc-γ受体(fc-γr)的结合活性可以通过例如使用biacore(注册商标)t200的配体捕获方法来测量,它依靠表面等离振子共振分析方法作为测量原理。
[1054]
下面描述测量抗体fc区对各种人fc-γ受体(fc-γrs)的结合活性的示例性方法的详情。在一个实施方案中,使用biacore(注册商标)t200评估抗体fc区对fc-γr的结合活性。在优选的实施方案中,该测量在25℃下使用测量缓冲液50mm磷酸盐、150mm nacl、0.05w/v%-p20,ph 7.4进行。具体地,首先将约1000ru的包含变体fc区的抗体捕获到传感器芯片上,并将captureselect(商标)人fab-λ动力学生物素缀合物(赛默飞世尔科技(thermofisher science))固定为捕获配体的分子。用测量缓冲液将人fc-γr稀释至fc-γria浓度为8nm,其他fc-γr浓度为1000nm,并使其与捕获的抗体结合。通过使用biacore t200评估软件2.0计算每单位量抗体(ru)的结合fc-γr的量来评估每种抗体对每种fc-γr的结合活性。在一个实施方案中,可以通过参考实施例7-4中描述的方法测量抗体fc区对各种人fc-γ受体(fc-γr)的结合活性。
[1055]
在一个优选的实施方案中,用于上述测量方法的fc-γr可以是通过下述方法制备的fc-γr的胞外域。首先,通过本领域技术人员已知的方法合成fc-γr的胞外域的基因。对于该合成,基于在ncbi登记的信息来制备每个fc-γr的序列。更具体地,基于ncbi登录号#nm_000566.3的序列制备fc-γri的序列,基于ncbi登录号#nm_001136219.1的序列制备fc-γriia的序列,基于ncbi登录号nm_004001.3的序列制备fc-γriib的序列,并根据ncbi登
录号nm_001127593.1的序列制备fc-γriiia的序列,并将his标签添加到c末端。fc-γriia的多态性位点参考j.exp.med.,1990,172,19-25来制备,fc-γriiia的多态性位点参考j.clin.invest.,1997,100,1059-1070来制备。将获得的基因片段插入动物细胞的表达载体中以制备表达载体。将制备的表达载体瞬时导入衍生自人胚胎肾癌细胞的freestyle293细胞(invitrogen)中,并表达感兴趣的蛋白质。收集培养物上清液,并通过0.22微米的过滤器过滤,然后基本上通过以下所述的四个步骤纯化。第一步,进行阳离子交换柱层析(sp sepharose ff);第二步,对his标签进行亲和柱层析(histrap hp);第三步,凝胶过滤柱色谱法(superdex200);第四步,无菌过滤。注意,对于fc-γri,第一步是使用q sepharose ff进行阴离子交换柱层析。基于吸收系数来计算纯化蛋白的浓度,该吸收系数是通过使用分光光度计并使用pace或用于测量值的此类方法测量280nm处的吸光度来计算的(蛋白质科学(protein science),1995,4,2411-2423)。
[1056]
在一个实施方案中,抗体fc区对人fcrn的结合活性可以通过使用例如依赖于表面等离振子共振分析方法作为测量原理的biacore(注册商标)t200的配体捕获方法来测量。
[1057]
测量抗体fc区对人fcrn的结合活性的示例性方法的细节如下所述。在一个实施方案中,使用biacore(注册商标)t200评估抗体fc区对人fcrn的结合活性。在优选的实施方案中,使用测量缓冲液50mm磷酸盐、150mm nacl,0.05w/v%-p20,ph 6.0在25℃下进行该测量。具体而言,首先将约400ru的包含fc区的抗体捕获到传感器芯片上,其中在所述传感器芯片上固定有captureselect(商标)人fab-λ动力学生物素缀合物(赛默飞世尔科技)作为捕获配体的分子,然后将用测量缓冲液稀释的人fcrn与其结合。通过使用biacore t200评估软件2.0中的稳态模型计算kd(m)来评估每种抗体对fcrn的结合活性。在一个优选的实施方案中,根据wo2010107110的参考实施例2中描述的方法制备用于该测量的人fcrn蛋白。在一个实施方案中,可以通过参考实施例7-5中所述的方法测量抗体fc区对各种人fcrn的结合活性。
[1058]
d)半胱氨酸工程化的抗体变体
[1059]
在某些实施方案中,可能需要产生半胱氨酸工程化的抗体,例如“thiomab”,其中抗体的一个或多个残基被半胱氨酸残基置换。在特定的实施方案中,置换的残基出现在抗体的可及位置。通过用半胱氨酸置换那些残基,反应性硫醇基团由此位于抗体的可及位点,并可用于将抗体与其他部分例如药物部分或接头-药物部分缀合,以产生免疫缀合物,如本文进一步所述。在某些实施方案中,以下任何一个或多个残基可以被半胱氨酸置换:轻链的v 205(kabat编号);重链的a118(eu编号);和重链fc区的s400(eu编号)。半胱氨酸工程化的抗体可以如例如美国专利号7,521,541中所描述的产生。
[1060]
e)抗体衍生物
[1061]
在某些实施方案中,本文提供的抗体可以被进一步修饰以包含本领域已知且容易获得的其他非蛋白质部分。适用于抗体衍生的部分包括但不限于水溶性聚合物。水溶性聚合物的非限制性实例包括但不限于聚乙二醇(peg),乙二醇/丙二醇共聚物,羧甲基纤维素,葡聚糖,聚乙烯醇,聚乙烯吡咯烷酮,聚-1、3-二氧戊环,聚1,3,6-三恶烷,乙烯/马来酸酐共聚物,聚氨基酸(均聚物或无规共聚物)和右旋糖酐或聚(正乙烯基吡咯烷酮)聚乙二醇,聚丙二醇均聚物,聚环氧丙烷/环氧乙烷共聚物,聚氧乙烯多元醇(例如甘油),聚乙烯醇及其混合物。聚乙二醇丙醛由于在水中的稳定性而在制造中可能具有优势。该聚合物可以具有
任何分子量,并且可以是支链或无支链的。连接至抗体的聚合物的数量可以变化,并且如果附接多于一个的聚合物,则它们可以是相同的分子或不同的分子。通常,用于衍生化的聚合物的数量和/或类型可以基于以下考虑因素来确定,这些考虑因素包括但不限于待改进抗体的特定特性或功能,是否将抗体衍生物用于限定条件的治疗中等。
[1062]
在另一个实施方案中,提供了抗体和可以通过暴露于辐射而被选择性加热的非蛋白质部分的缀合物。在一个实施方案中,非蛋白质部分是碳纳米管(kam等,proc.natl.acad.sci.usa,102:11600-11605(2005))。辐射可以是任何波长,并且包括但不限于不损害普通细胞但将非蛋白质部分加热至杀死邻近抗体-非蛋白质部分的细胞的温度的波长。
[1063]
b.重组方法和组合物
[1064]
可以使用重组方法和组合物来生产抗体,例如,如美国专利号4,816,567中所述。在一个实施方案中,提供了编码本文描述的抗cd137抗原结合分子或抗体的分离的核酸。这样的核酸可以编码包含抗体的vl的氨基酸序列和/或包含抗体的vh的氨基酸序列(例如,抗体的轻链和/或重链)。在进一步的实施方案中,提供了包含此类核酸的一种或多种载体(例如,表达载体)。在进一步的实施方案中,提供了包含此类核酸的宿主细胞。在一个这样的实施方案中,宿主细胞包含以下各项(例如,已经用以下各项转化):(1)载体,其包含核酸,所述核酸编码包含抗体的vl的氨基酸序列和包含抗体的vh的氨基酸序列,或(2)第一载体,其包含编码包含抗体的vl的氨基酸序列的核酸,以及第二载体,其包含编码包含抗体的vh的氨基酸序列的核酸。在一个实施方案中,宿主细胞是真核的,例如中国仓鼠卵巢(cho)细胞或淋巴样细胞(例如,y0,ns0,sp2/0细胞)。在一个实施方案中,提供了一种制备抗cd137抗原结合分子或抗体的方法,其中所述方法包括在适合于表达抗cd137抗原结合分子或抗体的条件下培养宿主细胞,所述宿主细胞包含如上所提供的编码抗体的核酸,并任选地从宿主细胞(或宿主细胞培养基)中回收抗体。
[1065]
为了重组产生抗cd137抗原结合分子或抗体,例如,如上所述,分离编码抗体的核酸,并将其插入一种或多种载体中,以在宿主细胞中进一步克隆和/或表达。可以使用常规程序(例如,通过使用能够与编码抗体的重链和轻链的基因特异性结合的寡核苷酸探针)容易地分离和测序此类核酸。
[1066]
用于克隆或表达编码抗体的载体的合适的宿主细胞包括本文所述的原核细胞或真核细胞。例如,可以在细菌中产生抗体,特别是在不需要糖基化和fc效应子功能时。关于抗体片段和多肽在细菌中的表达,参见,例如,美国专利号5,648,237、5,789,199和5,840,523。(还参见charlton,分子生物学方法(methods in molecular biology),第248卷(b.k.c.lo,编辑,人类出版社(humana press),新泽西州托托瓦市,2003),第245-254页,其描述了抗体片段在大肠杆菌中的表达)。表达后,抗体可以以可溶级分从细菌细胞糊中分离出来,并可以进一步纯化。
[1067]
除原核生物外,真核微生物(例如丝状真菌或酵母菌)也是适合编码抗体的载体的克隆或表达宿主,包括其糖基化途径已被“人源化”的真菌和酵母菌株,导致产生具有部分或全部人糖基化模式的抗体。参见gerngross,自然生物技术(nat.biotech.),22:1409-1414(2004),以及li等,自然生物技术(nat.biotech.),24:210-215(2006)。
[1068]
用于表达糖基化抗体的合适宿主细胞也衍生自多细胞生物(无脊椎动物和脊椎动
物)。无脊椎动物细胞的实例包括植物细胞和昆虫细胞。已经鉴定出许多杆状病毒株,它们可以与昆虫细胞结合使用,特别是用于草地贪夜蛾(spodoptera frugiperda)细胞的转染。
[1069]
植物细胞培养物也可以用作宿主。参见,例如,美国专利号5,959,177、6,040,498、6,420,548、7,125,978和6,417,429(描述了在转基因植物中产生抗体的plantibodies
tm
技术)。
[1070]
脊椎动物细胞也可以用作宿主。例如,适于在悬浮液中生长的哺乳动物细胞系可能是有用的。有用的哺乳动物宿主细胞系的其他实例是由sv40(cos-7)转化的猴肾cv1系;和人胚胎肾系(293或293细胞,如graham等,j.gen virol.36:59(1977)中所述);幼仓鼠肾细胞(bhk);小鼠滋养细胞(tm4细胞,例如,在mather,biol.reprod.23:243-251(1980)中描述的);猴肾细胞(cv1);非洲绿猴肾细胞(vero-76);人宫颈癌细胞(hela);犬肾细胞(mdck);水牛大鼠肝细胞(brl 3a);人肺细胞(w138);人肝细胞(hep g2);小鼠乳腺肿瘤(mmt 060562);例如在mather等,annals n.y.acad.sci.,383:44-68(1982)中描述的tri细胞;mrc 5细胞;和fs4细胞。其他有用的哺乳动物宿主细胞系包括中国仓鼠卵巢(cho)细胞,包括dhfr-cho细胞(urlaub等,proc.natl.acad.sci.usa 77:4216(1980));和骨髓瘤细胞系,例如y0、ns0和sp2/0。对于某些适于产生抗体的哺乳动物宿主细胞系的综述,参见,例如,yazaki和wu,分子生物学方法(methods in molecular biology),第248卷(b.k.c.lo编辑,人类出版社(humana press),新泽西州托托瓦市),第255-268页(2003)。
[1071]
c.测定
[1072]
本文提供的抗cd137抗原结合分子或抗体可以通过本领域已知的各种测定法对其物理/化学性质和/或生物学活性进行鉴定、筛选或表征。
[1073]
1.结合测定和其他测定
[1074]
一方面,例如通过已知方法如elisa、western杂交等测试本公开的抗原结合分子或抗体的抗原结合活性。
[1075]
在另一方面,可以利用在小分子化合物存在下的竞争测定法,以鉴定这样的抗原结合分子或抗体:其在低分子量化合物存在下(例如,在存在10μm以上,50μm以上,100μm以上,150μm以上,200μm以上,或250μm以上低分子量化合物的情况下),与包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256和/或a549/b167作为重链可变区/轻链可变区的组合的抗cd137抗原结合分子或抗体竞争结合cd137。在某些实施方案中,此类竞争性抗原结合分子或抗体结合至包含表17中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256和/或a549/b167作为重链可变区/轻链可变区的组合的抗cd137抗原结合分子或抗体所结合的相同表位(例如,线性表位或构象性表位)。morris(1996)“表位映射方案(epitope mapping protocols)”,“分子生物学方法”(methods in molecular biology),第66卷,(人类出版社(humana press),新泽西州托托瓦市),提供了映射抗原结合分子或抗体所结合的表位的详细示例性方法。在一个实施方案中,本公开的具有依赖于小分子化合物的抗原结合活性的cd137结合活性的抗cd137抗原结合分子或抗体,识别由抗原(例如,cd137)和低分子量化合物(例如atp)形成的复合物形成的表位。
[1076]
在使用抗体的示例性竞争测定中,将固定的cd137在低分子量化合物的存在下(例
如,在存在10μm以上,50μm以上,100μm以上,150μm以上,200μm以上,或250μm以上的低分子量化合物的情况下),在含有与cd137结合的第一标记抗体(例如,包含表37中描述的a375/b167、a372/b040、a356/b040、a486/b167、a487/b167、a488/b226、a489/b223、a548/b376、a551/b256、a551/b379、a555/b379、a548/b256和/或a549/b167作为重链可变区/轻链可变区的组合的抗cd137抗体)和第二未标记抗体(测试其与第一抗体竞争结合cd137的能力)的溶液中孵育。第二抗体可以存在于杂交瘤上清液中。作为对照,将固定化的cd137在包含第一标记抗体但不包含第二未标记抗体的溶液中孵育。在允许第一抗体结合cd137的条件下孵育后,除去过量的未结合抗体,并测量与固定的cd137缔合的标记物的量。如果相对于对照样品,测试样品中与固定的cd137缔合的标记物的量实质性减少,则表明第二抗体与第一抗体竞争结合cd137。参见harlow和lane(1988)抗体:实验室手册第14章(antibodies:a laboratory manual ch.14)(冷泉港实验室,纽约冷泉港)。本领域技术人员将理解,可以与除抗体以外的抗原结合分子类似地进行测定。
[1077]
2.活性测定
[1078]
一方面,提供了用于鉴定具有生物学活性的抗cd137抗原结合分子或抗体的生物学活性的测定法。生物学活性可包括例如cd137激动剂活性;血浆半衰期;抗肿瘤活性;以及肿瘤以外组织中的全身反应低或受抑制。还提供了在体内和/或体外具有这种生物学活性的抗原结合分子或抗体。
[1079]
在某些实施方案中,测试本公开的抗原结合分子(例如,抗cd137抗原结合分子)或抗体的这种生物学活性。
[1080]
a)激动活性测定(pbmc)
[1081]
在一个实施方案中,通过使表达cd137的细胞与抗cd137抗原结合分子或抗体在添加或不添加小分子化合物的溶液中接触来测量对cd137的激动活性。在一个实施方案中,分别通过细胞因子的产生量(例如il-2、ifn-γ和/或il-6的产生量)来评估在添加了小分子化合物的溶液中对cd137的激动活性和在未添加小分子化合物的溶液中对cd137的激动活性,所述细胞因子的产生量是在表达cd137的细胞和cd137抗原结合分子或抗体在溶液中接触之后的18小时、24小时、36小时、48小时或72小时内测量的。在一个实施方案中,调节其中添加了小分子化合物的溶液,使得调节后的小分子化合物的浓度为10μm、50μm、100μm、150μm、200μm或250μm。在进一步的实施方案中,待使用的表达cd137的细胞是分离的人外周血单核细胞(pbmc)或从分离的人pbmc扩增的t细胞。
[1082]
在一个实施方案中,使用通过在室温下以400
×
g离心30分钟从健康个体收集的血液中分离的人pbmc。优选地,使用在以下两个步骤中分离的人pbmc。第一步,在室温下将补充有ficoll-paque plus(ge医疗)的leucosep(greiner bio-one)以1000xg下离心1分钟,然后加入用pbs稀释的血液,并以400xg在室温下离心30分钟。在第二步中,离心后从管中收集血沉棕黄层,然后将其用60ml pbs(wako)洗涤。
[1083]
下面描述使用人pbmc测量cd137激动活性的示例性方法的详情。注意,即使以下实施例说明性地使用atp作为小分子化合物,但这也不排除其他小分子化合物。在一个实施方案中,用培养基(5%人血清(sigma),95%aim-v(赛默飞世尔科技))将分离的人pbmc稀释至细胞密度5
×
106/ml。然后,使分离的人pbmc与抗人cd3ε抗体和/或抗人cd28抗体接触,从而在人pbmc中诱导cd137表达。优选地,将50μl用培养基稀释的0.04μg/ml抗人cd3ε抗体(bd公
1和5-5-2中所述的方法测量cd137激动活性。
[1089]
在一个实施方案中,当通过人pbmc测定中细胞因子产生的量(例如,il-2、ifn-γ和/或il-6产生的量)评估对cd137的激动活性时,在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物的情况下,如果添加抗cd137抗原结合分子或抗体时细胞因子的产生量是添加阴性对照抗体时的细胞因子产生量的1.01倍以上、1.02倍以上、1.03倍以上、1.05倍以上、1.06倍以上、1.07以上、1.08倍以上、1.09倍以上、1.1倍以上、1.11倍以上、1.12倍以上、1.13倍以上、1.14倍以上、或1.15倍以上、1.5倍以上、2倍以上、或3倍以上高,则可以判断为在存在小分子化合物的情况下,抗cd137抗原结合分子或抗体显示出对cd137的激动活性。
[1090]
在一个实施方案中,当通过人pbmc测定中il-2产生的量评估对cd137的激动活性时,在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物的情况下,如果添加抗cd137抗原结合分子或抗体时il-2的产生量是添加阴性对照抗体时il-2的产生量的1.01倍以上、1.02倍以上、1.03倍以上、或1.05倍以上高,在优选实施方案中为1.05倍以上高,则可以判断为在存在小分子化合物的情况下,抗cd137抗原结合分子或抗体显示出对cd137的激动活性。
[1091]
在一个实施方案中,当通过人pbmc测定中il-γ产生的量评估对cd137的激动活性时,如果在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物的情况下,添加抗cd137抗原结合分子或抗体时il-γ的产生量是添加阴性对照抗体时il-γ产生量的1.01倍以上、1.11倍以上、1.12倍以上、1.13倍以上、1.14倍以上、或1.15倍以上高,在优选实施方案中为1.15倍以上高,则可以判断为在存在小分子化合物的情况下,抗cd137抗原结合分子或抗体显示出对cd137的激动活性。
[1092]
在进一步的实施方案中,在上述与阴性对照的比较中被判断为在小分子化合物存在下对cd137表现出激动活性的抗cd137抗原结合分子或抗体中,进一步确定被判断为在不存在小分子化合物的情况下(与存在小分子化合物的情况相比)不显示cd137激动活性或具有较低的cd137激动活性的抗体。具体地,当以下(ii)大于(i)时,判断抗cd137抗原结合分子或抗体在不存在小分子化合物的情况下不显示cd137激动剂活性或具有较低的cd137激动剂活性:
[1093]
(i)[当添加抗cd137抗原结合分子或抗体时,在不存在小分子化合物的情况下细胞因子的产生量]/[当添加阴性对照抗体时,在不存在小分子化合物的情况下细胞因子的产生量]
[1094]
(ii)[当添加抗cd137抗原结合分子或抗体时,在存在小分子化合物的情况下细胞因子的产生量]/[当添加阴性对照抗体时,在存在小分子化合物的情况下细胞因子的产生量]
[1095]
在不同的实施方案中,当使用人pbmc测定中细胞因子的产生量(例如,il-2、ifn-γ和/或il-6的产生量)比较第一抗cd137抗原结合分子或抗体和第二抗cd137抗原结合分子或抗体的cd137激动活性时,如果(i)在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物的情况下,当添加第一抗cd137抗原结合分子或抗体时,细胞因子的产生量是(ii)在相同条件下,当添加第二抗cd137抗原结合分子或抗体时细胞因子的产生量的1.01倍以上、1.02倍以上、1.03倍以上、1.04以上、1.05倍以上、1.06倍以上、1.07倍以上、1.08倍以
上、1.09倍以上、1.1倍以上、1.11倍以上、1.12倍以上、1.13倍以上、1.14倍以上、或1.15倍以上、1.5倍以上、2倍以上或3倍以上高,则可以判断为第一抗cd137抗原结合分子或抗体的激活活性比第二cd137抗原结合分子或抗体的激活活性高。
[1096]
在一个实施方案中,当通过人pbmc测定中il-2的产生量评估对cd137的激动活性时,如果(i)在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物的情况下,当添加第一抗cd137抗原结合分子或抗体时,细胞因子的产生量是(ii)在相同条件下当添加第二抗cd137抗原结合分子或抗体时il-2的产生量的1.01倍以上、1.02倍以上、1.03倍以上、或1.04倍以上高,或在优选实施方案中为1.04倍以上高,则可以判断为第一抗cd137抗原结合分子或抗体的激活活性比第二cd137抗原结合分子或抗体的激活活性高。
[1097]
在一个实施方案中,当通过人pbmc测定中il-γ的产生量评估对cd137的激动活性时,如果(i)在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物的情况下,当添加第一抗cd137抗原结合分子或抗体时,细胞因子的产生量是(ii)在相同条件下当添加第二抗cd137抗原结合分子或抗体时il-γ的产生量的1.05倍以上、1.06倍以上、1.07倍以上、1.08倍以上、1.09倍以上、或1.1倍以上高,或在优选实施方案中为1.1倍以上高,则可以判断为第一抗cd137抗原结合分子或抗体的激活活性比第二cd137抗原结合分子或抗体的激活活性高。在一个实施方案中,第一抗cd137抗原结合分子或抗体是包含亲本fc区的抗原结合分子或抗体,第二抗cd137抗原结合分子或抗体是包含变体fc区的抗原结合分子或抗体。
[1098]
在一个实施方案中,参考实施例5-5-1和5-5-2中描述的方法可用于使用人pbmc测量cd137激动活性,并且参考实施例2-6中描述的方法可用于使用从分离的人pbmc中扩增的t细胞测量cd137激动活性。
[1099]
在一个实施方案中,可以通过使从人pbmc分离的cd8阳性t细胞或cd4阳性t细胞与抗cd137抗原结合分子或抗体在添加了小分子化合物或未添加小分子化合物的溶液中接触来测量对cd137的激动活性。此时,可以将表达fcγriib的细胞进一步添加到溶液中。或者,可以通过使b细胞(其可以从人pbmc分离,或者可以使用已知的b细胞系)与抗cd137抗原结合分子或抗体接触来测量对cd137的激动活性。在一个实施方案中,对cd137的激动活性可以通过在cd8阳性t细胞、cd4阳性t细胞或b细胞与抗cd137抗原结合分子或抗体在溶液中接触后,测量的细胞因子产生量(例如,il-2,ifn-γ和/或il-6产生量)来评估。
[1100]
在一个实施方案中,激动活性测定使用的人外周血单核细胞(pbmc)是从健康个体收集的血液中分离的。因此,在任何上述实施方案中,本领域技术人员将理解,使用测定的测定结果可能因每个血液样本的供体而不同。考虑到这一点,对于部分或大部分从多个供体分离的人pbmc不显示激动活性的抗体不被判断为显示cd137激动活性,即使人pbmc的另一部分满足激动活性的标准。此外,当对从多个供体分离的人pbmc进行根据上述方法的测定,并且在大多数供体中满足cd137激动活性的标准时,则可以判断为表现出cd137激动活性。替代地,当对从多个供体分离的人pbmc进行根据上述方法的测定时,测定值的平均值或中值(例如,il-2、ifn-γ和/或il-6的产生量)可用于确定cd137激动活性的存在或不存在。在一个实施方案中,当根据上述方法对从多个供体分离的人pbmc进行测定时,供体的数目为例如2以上、3以上、4以上、5以上、10以上、15以上或20以上。
[1101]
b)激动活性测定(报告基因测定)
[1102]
在一个实施方案中,在添加或不添加小分子化合物的溶液中,通过报告基因测定
法评估对cd137的激动活性。在一个实施方案中,在使表达nf-κb荧光素酶报告基因构建体和cd137的t细胞与抗cd137抗原结合分子接触并在相应溶液中静置一定时间后,分别通过测量的荧光素酶发光信号评估在添加了小分子化合物的溶液中对cd137的激动活性和在未添加小分子化合物的溶液中对cd137的激动活性。在一个实施方案中,调节其中添加了小分子化合物的溶液,使得调节后的小分子化合物浓度为10μm、50μm、100μm、150μm、200μm或250μm。表达nf-κb-荧光素酶报告基因构建体和cd137的t细胞优选是gloresponse
tm nf-κb-luc2/4-1bb jurkat细胞系(promega,cs196004)。
[1103]
下面描述使用报告基因测定法测量cd137激动活性的示例性方法的详情。在以下实施例中,将atp用作小分子化合物的实例,但是不排除其他小分子化合物。在一个实施方案中,首先,用培养基(cho培养基(90%ham's f12,10%fbs))将表达fcγriib的细胞的浓度调节至5x104/ml,并在37℃下于5%co2培养箱放置过夜。在一个实施方案中,作为表达fcgriib的细胞,不仅可以使用强制表达fcgriib的细胞,而且可以使用内源性表达fcgriib的细胞系,例如b细胞系,从活体分离的b细胞等。在优选的实施方案中,表达fcγriib的细胞是fcγriib cho-k1细胞(promega)。接下来,在通过抽吸去除培养基后,用不同的培养基(99%rpmi,1%fbs)将gloresponse
tm nf-κb-luc2/4-1bb jurkat细胞系(以下称为“4-1bb jurkat”)调整为2x106/ml。在优选的实施方案中,每200μl用培养基调节的表达fcγriib的细胞,添加25μl用培养基调节的gloresponse
tm nf-κb-luc2/4-1bb jurkat细胞系细胞。随后,加入25μl每个用上述培养基(99%rpmi,1%fbs)稀释至所需浓度(例如,终浓度为0、0.001、0.01、0.1、1、10μg/ml)的抗cd137抗原结合分子,此外,加入25μl用上述培养基(99%rpmi,1%fbs)稀释至所需浓度(例如,最终浓度为0、10、50、100、150、200、250μm)的atp溶液。在一个实施方案中,在向4-1bb jurkat添加抗cd137抗原结合分子后静置2小时或更短、4小时或更短、6小时或更短、24小时或更短之后,测量荧光素酶发光信号。在优选的实施方案中,将4-1bb jurkat在5%co2培养箱中在37℃下静置6小时。静置后,添加75μl的bio-glo试剂,并用酶标仪测量发光。在一个优选的实施方案中,bio-glo试剂是bio-glo荧光素酶测定系统(缓冲液和底物)。在一个实施方案中,为了保持反应过程中的温度恒定,将4-1bb jurkat从培养箱中取出后可以使其在室温下静置5分钟、10分钟、15分钟或20分钟。在优选的实施方案中,将4-1bb jurkat从培养箱中取出后使其在室温下放置15分钟。在一个实施方案中,将添加有抗cd137抗原结合分子的4-1bb jurkat的发光值除以未添加抗cd137抗原结合分子的4-1bb jurkat的发光值,取该值作为倍数诱导(相对光单位),并用作评估每个抗原结合分子的cd137激动活性的指标。
[1104]
下文描述了使用报告基因测定法测量cd137激动活性的另一示例性方法。将每个200μl的fcγriib cho-k1细胞(promega)用培养基调节至5x104/ml的浓度,然后添加到96孔板的每个孔中,并在5%co2培养箱中于37℃放置过夜。作为培养基,使用cho培养基(90%的ham’f12、10%的fbs)。然后,在通过抽吸将培养基完全去除后,将25μl gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系用测定培养基(99%rpmi,1%fbs)调整至2x106/ml,然后添加到每个孔中。随后,加入25μl用测定培养基稀释至终浓度为0、0.001、0.01、0.1、1或10μg/ml的每种抗原溶液,最后加入25μl用测定培养基稀释至0或250μm的atp溶液。将板在5%co2培养箱中于37℃静置6小时后,在室温放置15分钟,然后将75μl bio-glo试剂添加到每个孔中。作为bio-glo试剂,例如,可以使用bio-glo荧光素酶测定系统(缓冲液和底物)。此后,用
酶标仪测量每个孔的发光。通过将每个孔的发光值除以未添加任何抗体的孔的发光值而获得的值定义为倍数诱导。在报告基因测定中,可以通过添加了每种抗体的孔的发光相对于未添加任何抗体的孔的发光量的倍数变化(相对光单位)来评估cd137激动活性。
[1105]
下文描述了使用报告基因测定法测量cd137激动活性的另一示例性方法。向384孔板的每个孔中,添加10μl用测定培养基(99%rpmi,1%fbs)将其浓度调整为2x106/ml的fcγriib cho-k1细胞(promega)。随后,向每个孔中添加10μl含adp的抗体溶液或含atp的抗体溶液,或不含atp或adp的抗体溶液。然后,向每个孔中加入10μl用测定培养基(99%rpmi,1%fbs)将其调节至2
×
106/ml的gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系。adp的终浓度为50μm,atp的终浓度为50μm。将板在5%co2培养箱中于37℃放置6小时后,在室温放置15分钟,然后向每个孔中添加30μl bio-glo试剂。作为bio-glo试剂,使用了bio-glo荧光素酶测定系统(缓冲液和底物)。此后,用酶标仪测量每个孔的发光。cd137激动活性可以通过添加了每种抗体的孔的发光相对于未添加任何抗体的孔的发光的相对光单位(也称为发光倍数或倍数变化)来评价。
[1106]
下文描述了使用报告基因测定法测量cd137激动活性的另一示例性方法。向384孔板的每个孔中,添加10μl用测定培养基(99%rpmi,1%fbs)将其浓度调整为4x105/ml的fcγriib cho-k1细胞(promega)。随后,向每个孔中添加10μl含adp的抗体溶液或含atp的抗体溶液,或不含atp或adp的抗体溶液。然后,向每个孔中加入10μl用测定培养基(99%rpmi,1%fbs)将其调节至2
×
106/ml的gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系。adp的终浓度为10μm,atp的终浓度为10μm。将板在5%co2培养箱中于37℃放置6小时后,在室温放置15分钟,然后向每个孔中添加30μl的bio-glo试剂。作为bio-glo试剂,使用了bio-glo荧光素酶测定系统(缓冲液和底物)。此后,用酶标仪测量每个孔的发光。cd137激动活性可以通过添加了每种抗体的孔的发光相对于未添加任何抗体的孔的发光的相对光单位(也称为发光倍数或倍数变化)来评价。
[1107]
在一个实施方案中,当使用报告基因测定法测量对cd137的激动活性时,如果(i),在存在10μm、50μm、100μm、150μm、200μm或250μm小分子化合物情况下,对cd137的激动活性(相对光单位)是(ii)在不存在小分子化合物的情况下的cd137激动活性(相对光单位)的1.1倍以上、1.2倍以上、1.3倍以上、1.5倍以上、2倍以上、3倍以上、5倍以上、10倍以上、20倍以上、30倍以上、50倍以上、60倍以上、70倍以上、80倍以上、或90倍以上高,则可以判断为在存在小分子化合物的情况下,抗cd137抗原结合分子或抗体对cd137表现出激动活性。在一个实施方案中,上述(i)和(ii)中的抗体的终浓度为0、0.001、0.01、0.1、1或10μg/ml,并且在优选的实施方案中,为0.1μg/ml或1μg/ml。
[1108]
在进一步的实施方案中,当抗cd137抗原结合分子或抗体以特定浓度(例如0.001、0.01、0.1、1或10μg/ml的终浓度,或在优选实施方案中为0.1μg/ml或1μg/ml)添加时,如果在不存在小分子化合物的情况下倍数诱导(相对光单位)为10以下、9以下、8以下、或在优选实施方案中为5以下,在更优选的实施方案中基本上为1,则判断为在不存在小分子化合物的情况下,抗cd137抗原结合分子或抗体基本上不表现出cd137激动活性。在一个实施方案中,“在不存在小分子化合物的情况下倍数诱导(相对光单位)基本上为1”是指在不存在小分子化合物的情况下的倍数诱导(相对光单位)小于2倍、小于1.9倍、小于1.8倍、小于1.7倍、小于1.6倍、小于1.5倍、小于1.4倍、小于1.3倍、小于1.2倍或小于1.1倍。
[1109]
c)血浆浓度
[1110]
在一个实施方案中,使用人cd137敲入小鼠测量和/或比较本公开的抗cd137抗原结合分子或抗体的血液动力学。例如,通过将人cd137基因替代载体导入小鼠胚胎干细胞(es细胞)中,用人cd137基因替代小鼠cd137基因,从而制备人cd137敲入小鼠。在一个实施方案中,通过单次静脉内施用向人cd137敲入小鼠中施用本公开的cd137抗原结合分子或抗体,并且从施用后立即到施用后大约5天、10天、15天、20天、25天或30天多次收集血液。在优选的实施方案中,本公开的cd137抗原结合分子或抗体通过单次静脉内施用而被施用到人cd137敲入小鼠中,并且在施用后5分钟至28天的时间中多次收集血液。从收集的血液中迅速分离血浆,并通过电化学发光(ecl)测量血浆中的抗体浓度。在一个实施方案中,血浆中的抗体浓度可以通过参考实施例6-3-2中描述的方法测量。
[1111]
在使用人cd137敲入小鼠的血浆半衰期的测量中,如果抗cd137抗原结合分子或抗体从血浆中消失的速度比参考分子慢,则判定该抗cd137抗原结合分子或抗体具有与参考分子相比改善的血液动力学。另外,如果具有依赖于小分子化合物的结合活性的抗cd137抗原结合分子或抗体(转换分子或转换抗体)从血浆中消失的速度比不具有依赖于小分子化合物的结合活性的抗cd137抗原结合分子或抗体(非转换分子或非转换抗体)慢,可以判断为与非转换分子(或非转换抗体)相比,转换分子(或转换抗体)不与非肿瘤组织中表达的cd137结合。
[1112]
d)抗肿瘤活性
[1113]
一方面,测试了抗cd137抗原结合分子或其抗体在体内抑制细胞生长或增殖的能力。在某些实施方案中,测试抗cd137抗原结合分子或其抗体在体内抑制肿瘤生长的能力。体内模型系统,例如同种异体移植模型或异种移植模型,可以用于这种测试。在示例性异种移植系统中,将人肿瘤细胞引入适当免疫受损的非人动物,例如无胸腺“裸”小鼠中。向动物施用本公开的抗体。测量了抗体抑制或减少肿瘤生长的能力。在上述异种移植系统的某些实施方案中,人肿瘤细胞是来自人患者的肿瘤细胞。此类异种移植模型可从oncotest公司(frieberg,德国)商购获得。在某些实施方案中,通过皮下注射或通过移植到合适的部位例如乳脂垫中,将人肿瘤细胞引入合适的免疫受损的非人动物中。
[1114]
在一个实施方案中,可以使用基于上述人cd137敲入小鼠的同系肿瘤细胞移植模型来测量和/或比较本公开的抗cd137抗原结合分子或抗体的抗肿瘤活性。可以适当地选择在测试中使用的癌细胞系,但是优选小鼠结肠癌细胞系mc38细胞系。在一个实施方案中,将mc38细胞系移植到小鼠腹部区域的皮肤下,并且当肿瘤体积达到约50-300mm3时,认为建立了模型。建立模型后,将mc38细胞移植的小鼠分组,然后接受每种抗cd137抗原结合分子或抗体的施用。在一个实施方案中,以每周一次至两次的频率进行肿瘤体积测量,以评估抗肿瘤活性。使用以下方程式计算肿瘤体积:肿瘤体积=(长轴
×
短轴
×
短轴)/2。在一个实施方案中,可以按照参考实施例6-4中描述的方法测试和评估抗cd137抗原结合分子或抗体的抗肿瘤活性。
[1115]
在一个实施方案中,当抗cd137抗原结合分子或抗体施用组中的肿瘤体积小于赋形剂组中的肿瘤体积,或抗cd137抗原结合分子或抗体施用组的肿瘤体积增加小于赋形剂组时,则认为抗cd137抗原结合分子或抗体显示抗肿瘤活性。
[1116]
e)全身反应
[1117]
在一个实施方案中,使用基于上述人cd137敲入小鼠的同系肿瘤细胞移植模型来测量和/或比较对本公开的抗cd137抗原结合分子或抗体的全身反应。可以适当地选择用于测量全身反应的器官,但是优选肝脏、脾脏和/或淋巴结。在一个实施方案中,通过在施用抗cd137抗原结合分子或抗体后的合适时间从人cd137敲入的小鼠中摘除肝脏、脾脏和/或淋巴结来评估全身反应。当要摘除的器官是脾脏和/或淋巴结时,称量器官和/或计数淋巴细胞级分中的细胞。在计数中,优选将溶血后的淋巴细胞级分用于脾脏,将通过均质化得到的淋巴细胞级分用于淋巴结。当要摘除的器官是肝脏时,对用肝脏解离试剂盒小鼠(milteny biotec)获得的淋巴细胞级分中的细胞进行计数。此外,可以对来自每个器官(肝脏、脾脏和/或淋巴结)的淋巴细胞级分进行使用流式细胞术(fcm)的t细胞分析。在fcm分析中,例如使用cd8-α阳性t细胞中的颗粒酶b表达或pd-1表达或icos表达或cd8-α阳性t细胞与cd45阳性细胞之比。在一个实施方案中,可以按照参考实施例6-4中描述的方法测试和评估对抗cd137抗原结合分子或抗体的全身反应。
[1118]
在一个实施方案中,在上述各种指标的评价中,当抗cd137抗原结合分子或抗体施用组的值低于接受相同量参考分子的施用的组的值时,则认为抗cd137抗原结合分子或抗体相比于参考分子抑制全身反应和/或抑制非肿瘤组织(例如,肝脏、脾脏和/或淋巴结)中免疫细胞的激活。此外,在上述各种指标的评价中,当接受具有依赖于小分子化合物的结合活性的抗cd137抗原结合分子或抗体(转换分子或转换抗体)的施用组的值低于接受相同量的不具有依赖于小分子化合物的结合活性的抗cd137抗原结合分子或抗体(非转换分子或非转换抗体)的施用组时,则认为与非转换分子(或非转换抗体)相比,转换分子(转换抗体)抑制全身反应和/或抑制非肿瘤组织(例如,肝脏、脾脏和/或淋巴结)中免疫细胞的激活。
[1119]
应当理解,可以使用本公开的免疫缀合物代替抗cd137抗原结合分子或抗体,或除抗cd137抗原结合分子或抗体之外,使用本公开的免疫缀合物,执行任何上述测量方法。
[1120]
d.免疫缀合物
[1121]
本公开内容还提供了免疫缀合物,其包含与一种或多种细胞毒性剂例如化学治疗剂或药物、生长抑制剂、毒素(例如蛋白质毒素,细菌、真菌、植物或动物起源的酶活性毒素,或其片段)、或放射性同位素缀合的本公开的抗cd137抗原结合分子或抗体。
[1122]
在一个实施方案中,免疫缀合物是抗体-药物缀合物(adc),其中抗体缀合至一种或多种药物,所述药物包括但不限于美登木素生物碱(参见美国专利号5,208,020、5,416,064和欧洲专利ep 0 425 235b1);澳瑞他汀(auristatin),例如单甲基澳瑞他汀药物部分de和df(mmae和mmaf)(参见美国专利5,635,483和5,780,588,以及7,498,298);尾海兔素(dolastatin);加利车霉素(calicheamicin)或其衍生物(参见美国专利号5,712,374、5,714,586、5,739,116、5,767,285、5,770,701、5,770,710、5,773,001和5,877,296;hinman等,癌症研究(cancer res.),53:3336-3342(1993);和lode等,癌症研究(cancer res.)58:2925-2928(1998));蒽环类药物如道诺霉素或阿霉素(参见kratz等,现行的药物化学(current med.chem.),13:477-523(2006);jeffrey等,生物有机物&医药化学通讯(bioorganic&med.chem.letters),16:358-362(2006);torgov等,bioconj.chem.16:717-721(2005);nagy等,proc.natl.acad.sci.usa 97:829-834(2000);dubowchik等,生物有机物&医药化学通讯(bioorg.&med.chem.letters),12:1529-1532(2002);king等,医药化学杂志(j.med.chem.),45:4336-4343(2002);和美国专利号6,630,579);甲氨蝶呤;长春地
辛;紫杉烷,例如多西他赛、紫杉醇、拉洛他赛、替塞他赛(tesetaxel)和奥他他赛(ortataxel);单端孢菌毒素;和cc1065。
[1123]
在另一个实施方案中,免疫缀合物包含与酶活性毒素或其片段缀合的本文所述的抗体,所述酶活性毒素或其片段包括但不限于白喉a链、白喉毒素的非结合活性片段、外毒素a链(来自铜绿假单胞菌(pseudomonas aeruginosa)),蓖麻毒蛋白a链、相思豆毒素a链、塑莲根毒蛋白ii a链、α-帚曲霉素、油桐(aleurites fordii)蛋白、石竹素蛋白、美洲商陆(phytolacca americana)蛋白(papi、papii和pap-s)、苦瓜抑制因子、泻果素、巴豆素、石碱花抑制剂、多花白树毒蛋白、分裂素、局限曲霉素、酚霉素、依诺霉素和单端孢菌毒素。
[1124]
在另一个实施方案中,免疫缀合物包含与放射性原子缀合以形成放射性缀合物的本文所述的抗体。多种放射性同位素可用于生产放射性缀合物。实例包括
211
at、
131
i、
125
i、
90
y、
186
re、
188
re、
153
sm、
212
bi、
32
p、
212
pb和lu的放射性同位素。当放射性缀合物用于检测时,它可以包含用于闪烁显像研究的放射性原子,例如tc-99m或
123
i,或用于核磁共振(nmr)成像(也称为磁共振成像,mri)的自旋标记,例如碘123、碘131、铟111、氟19、碳13、氮15、氧17、钆、锰或铁。
[1125]
可以使用多种双功能蛋白偶联剂来制备抗体和细胞毒剂的缀合物,所述双功能蛋白偶联剂例如n-琥珀酰亚胺基-3-(2-吡啶基二硫代)丙酸酯(spdp),琥珀酰亚胺基-4-(n-马来酰亚胺基甲基)环己烷-1-甲酸酯(smcc),亚氨基噻吩(it),亚氨基酯的双官能衍生物(例如二甲基己二亚酰胺化物),活性酯(例如辛二酸二琥珀酰亚胺基酯),醛(例如戊二醛),双叠氮基化合物(例如双(对叠氮基苯甲酰基)己二胺),双重氮衍生物(例如双-(对重氮苯甲酰基)-乙二胺),二异氰酸酯(例如甲苯2,6-二异氰酸酯)和双活性氟化合物(例如1,5-二氟-2,4-二硝基苯)。例如,可以如vitetta等,科学(science),238:1098(1987)中描述的制备蓖麻毒素免疫毒素。碳-14标记的1-异硫氰酸基合苄基-3-甲基二亚乙基三胺五乙酸(mx-dtpa)是用于放射性核素与抗体缀合的示例性螯合剂。参见wo94/11026。接头可以是“可切割的接头”,其促进细胞毒性药物在细胞中的释放。可以使用例如,酸不稳定的接头、肽酶敏感的接头、光不稳定的接头、二甲基接头或含二硫键的接头(chari等,癌症研究(cancer res.),52:127-131(1992);美国专利号5,208,020)。
[1126]
本文的免疫缀合物或adc明确考虑但不限于用交联剂制备的此类缀合物,所述交联剂包括但不限于可商购的(例如,从美国伊利诺伊州罗克福德的皮尔斯生物技术有限公司)bmps、emcs、gmbs、hbvs、lc-smcc、mbs、mpbh、sbap、sia、siab、smcc、smpb、smph、磺基-emcs、磺基-gmbs、磺基-kmus、磺基-mbs、磺基-siab、磺基-smcc和磺基-smpb和svsb(琥珀酰亚胺基-(4-乙烯基砜)苯甲酸酯)。
[1127]
e.用于诊断和检测的方法和组合物
[1128]
在某些实施方案中,本文提供的任何抗cd137抗原结合分子或抗体可用于检测生物样品中cd137抗原结合分子的存在。如本文所使用的,术语“检测”涵盖定量检测或定性检测。在某些实施方案中,生物样品包含细胞或组织。
[1129]
在一个实施方案中,提供了用于诊断或检测方法中的抗cd137抗原结合分子或抗体。在另一方面,提供了检测生物样品中cd137的存在的方法。在某些实施方案中,所述方法包括在允许抗cd137抗原结合分子或抗体与cd137结合的条件下,使生物样品与本文所述的抗cd137抗原结合分子或抗体接触,并检测是否在抗cd137抗原结合分子或抗体和cd137之
间形成复合物。这样的方法可以是体外方法或体内方法。在一个实施方案中,使用抗cd137抗原结合分子或抗体来选择适合于用抗cd137抗原结合分子或抗体治疗的受试者,例如其中cd137是用于选择患者的生物标志物。
[1130]
可以使用本公开的抗体诊断的示例性疾病包括癌症。
[1131]
在某些实施方案中,提供了标记的抗cd137抗原结合分子或抗体。标记包括但不限于直接检测的标记或部分(例如荧光、发色、电子致密、化学发光和放射性标记),以及例如通过酶促反应或分子相互作用间接检测的部分(例如酶或配体)。示例性标记包括但不限于放射性同位素
32
p,
14
c,
125
i,3h和
131
i,荧光团,例如稀土螯合物或荧光素及其衍生物,若丹明及其衍生物,丹酰,伞形酮,荧光素酶,例如萤火虫荧光素酶和细菌荧光素酶(美国专利号4,737,456),荧光素,2,3-二氢酞嗪二酮,辣根过氧化物酶(hrp),碱性磷酸酶,β-半乳糖苷酶,葡糖淀粉酶,溶菌酶,糖类氧化酶,例如葡萄糖氧化酶,半乳糖氧化酶和葡萄糖6-磷酸脱氢酶,杂环氧化酶(例如尿酸酶和黄嘌呤氧化酶),那些与使用过氧化氢氧化染料前体(例如hrp)的酶偶联的酶,乳过氧化物酶或微过氧化物酶,生物素/亲和素,自旋标记,噬菌体标记,稳定的自由基等等。
[1132]
f.药物制剂
[1133]
通过将具有所需纯度的抗体与一种或多种任选的药学上可接受的载体混合以冻干制剂或水溶液的形式来制备本文所述的抗cd137抗原结合分子或抗体的药物制剂(雷明顿药物科学(remington's pharmaceuticalsciences),第16版,osol,a.(1980))。药学上可接受的载体在所采用的剂量和浓度下通常对受体无毒,包括但不限于:缓冲剂,例如磷酸盐,柠檬酸盐和其他有机酸;抗氧化剂,包括抗坏血酸和蛋氨酸;防腐剂(例如十八烷基二甲基苄基氯化铵;六甲基氯化铵;苯扎氯铵;苄索氯铵;苯酚,丁醇或苄醇;对羟基苯甲酸烷基酯,例如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯;邻苯二酚;间苯二酚;环己醇;3-戊醇和间甲酚);小分子(少于约10个残基)多肽;蛋白质,例如血清白蛋白,明胶或免疫球蛋白;亲水性聚合物,例如聚乙烯吡咯烷酮;氨基酸,例如甘氨酸,谷氨酰胺,天冬酰胺,组氨酸,精氨酸或赖氨酸;单糖,二糖和其他碳水化合物,包括葡萄糖,甘露糖或糊精;螯合剂,例如edta;糖,例如蔗糖,甘露醇,海藻糖或山梨糖醇;成盐的反离子,例如钠;金属配合物(例如锌蛋白配合物);和/或非离子表面活性剂,例如聚乙二醇(peg)。本文中的示例性药学上可接受的载体还包括间质药物分散剂,例如可溶性中性活性透明质酸酶糖蛋白(shasegp),例如人可溶性ph-20透明质酸酶糖蛋白,例如rhuph20(hylenex(注册商标),baxter国际公司)。在美国专利公开号2005/0260186和2006/0104968中描述了某些示例性的shasegp及使用方法,包括rhuph20。一方面,将shasegp与一种或多种另外的糖胺聚糖酶如软骨素酶组合。
[1134]
示例性的冻干抗体制剂在美国专利号6,267,958中描述。水性抗体制剂包括在美国专利号6,171,586和wo2006/044908中描述的那些,后者的制剂包括组氨酸-乙酸盐缓冲液。
[1135]
活性成分可以被包埋在胶体药物递送系统(例如,脂质体,白蛋白微球、微乳液、纳米颗粒和纳米胶囊)的微胶囊中或粗乳液中,微胶囊例如分别通过凝聚技术或通过界面聚合而制备,例如羟甲基纤维素微胶囊或明胶-微胶囊和聚(甲基丙烯酸甲酯)微胶囊。这样的技术公开在雷明顿药物科学(remington's pharmaceutical sciences)第16版,osol,a.编(1980)中。
[1136]
可以制备缓释制剂。缓释制剂的合适实例包括含有抗体的固体疏水性聚合物的半透性基质,该基质为定型制品的形式,例如,薄膜或微胶囊。
[1137]
用于体内施用的制剂通常是无菌的。无菌可以容易地实现,例如通过无菌滤膜过滤。
[1138]
g.治疗方法和治疗组合物
[1139]
本文提供的任何抗cd137抗原结合分子或抗体均可用于治疗方法。
[1140]
一方面,在本公开中,提供了用作药物的抗cd137抗原结合分子或抗体。在本公开中,药物的实例具体包括用于诱导抗肿瘤作用的药物,例如,通过抗cd137抗原结合分子或抗体与免疫细胞如t细胞上表达的cd137的结合产生的细胞激活,抑制肿瘤中的新血管形成,抑制肿瘤细胞增殖,耗竭促进肿瘤的b细胞等。在其他方面,在本公开中,提供了用于治疗肿瘤的抗cd137抗原结合分子或抗体。在某些实施方案中,提供了用于治疗方法的抗cd137抗原结合分子或抗体。在某些实施方案中,本公开提供了用于治疗患有肿瘤的个体的方法中的抗cd137抗原结合分子或抗体,所述方法包括向所述个体施用有效量的抗cd137抗原结合分子或抗体。在进一步的实施方案中,在本公开中,肿瘤的实例包括其中浸润了b细胞、树突细胞、天然杀伤细胞、巨噬细胞、cd8阳性t细胞和/或调节性t细胞(treg细胞)的实体瘤。
[1141]
在其他方面,本公开提供了用于在个体中激活免疫细胞的方法中使用的抗cd137抗原结合分子或抗体,所述方法包括向个体施用有效量的抗cd137抗原结合分子或抗体,以激活免疫细胞,例如b细胞、树突细胞、天然杀伤细胞、巨噬细胞和/或cd8阳性t细胞(更具体地讲,这些免疫细胞已渗透到肿瘤组织中)。
[1142]
在进一步的方面,本公开提供了抗cd137抗原结合分子或抗体,所述抗cd137抗原结合分子或抗体用于破坏个体中的细胞(例如肿瘤细胞)的方法中,所述方法包括向个体施用有效量的抗cd137抗原结合分子或抗体。在某些实施方案中,肿瘤的实例包括其中浸润了b细胞、树突细胞、天然杀伤细胞、巨噬细胞、cd8阳性t细胞和/或调节性t细胞(treg细胞)的实体瘤。根据以上任何实施方案中的“个体”优选是人。
[1143]
在进一步的方面,本公开提供了抗cd137抗原结合分子或抗体在药物的生产或制备中的用途。在一个实施方案中,所述药物用于治疗肿瘤(根据于上下文,将其称为“癌症”可能更合适(此后同样适用))。在进一步的实施方案中,所述药物用于治疗肿瘤(或根据上下文为癌症)的方法中,所述方法包括向患有肿瘤(或根据上下文为癌症)的个体施用有效量的药物。在进一步的实施方案中,所述药物用于诱导抗肿瘤作用,例如,通过抗cd137抗原结合分子或抗体与在免疫细胞(例如t细胞)上表达的cd137结合导致的细胞激活,抑制肿瘤中的新血管形成,抑制肿瘤细胞增殖,耗竭促进肿瘤的b细胞等。在进一步的实施方案中,所述药物用于(例如通过抗cd137抗原结合分子或抗体与在个体中免疫细胞(例如t细胞)上表达的cd137结合导致的细胞激活)抑制肿瘤中的新血管形成,抑制肿瘤细胞增殖,消耗促进肿瘤的b细胞等的方法中,所述方法包括向个体施用有效量的用于其的药物。根据以上实施方案中的任何一个的“个体”可以是人。
[1144]
在进一步的方面,本公开提供了用于治疗肿瘤的方法。在一个实施方案中,所述方法包括向患有这种肿瘤的个体施用有效量的抗cd137抗原结合分子或抗体。在进一步的实施方案中,在本公开中,肿瘤的实例包括其中浸润了b细胞、树突细胞、天然杀伤细胞、巨噬
细胞、cd8阳性t细胞和/或调节性t细胞(treg细胞)的实体瘤。
[1145]
在进一步的方面,本公开提供了用于激活个体中的免疫细胞的方法。在一个实施方案中,所述方法包括向个体施用有效量的抗cd137抗原结合分子或抗体。在进一步的实施方案中,在本公开中,免疫细胞包括免疫细胞例如b细胞、树突细胞、天然杀伤细胞、巨噬细胞和/或cd8阳性t细胞(更具体地,这些免疫细胞已浸润到肿瘤组织中)。在该方法中,当肿瘤组织中选自cd8b1、gzmb、prf1和ifng中的至少一种基因的表达水平升高时,可以判断肿瘤组织中t细胞的活化增强。
[1146]
在进一步的方面,本公开提供了用于活化或促进个体肿瘤组织中的免疫细胞特别是cd8
+ t细胞增殖的方法。在一个实施方案中,此类方法包括一种方法,该方法包括向个体施用有效量的抗cd137抗原结合分子或抗体。在活化cd8
+
t细胞的方法中,当至少一种选自ova四聚体、颗粒酶b、pd-1、dlrg-1和icos的cd8
+ t细胞活化标志物的阳性率增加时(阳性率(%)=肿瘤组织中活化标志物阳性的cd8
+ t细胞数/肿瘤组织中cd8
+ t细胞数
×
100),可以判断肿瘤组织中的cd8
+ t细胞被活化。
[1147]
在进一步的方面,本公开提供了用于破坏个体中的细胞(特别是肿瘤细胞)的方法。在一个实施方案中,所述方法包括包含对个体施用有效量的抗cd137抗原结合分子或抗体的那些方法。在某些实施方案中,肿瘤的实例包括其中浸润了b细胞、树突细胞、天然杀伤细胞、巨噬细胞、cd8阳性t细胞和/或调节性t细胞(treg细胞)的实体瘤。根据以上任何实施方案的“个体”可以是人。
[1148]
在一些实施方案中,个体是具有癌细胞或含有癌细胞的肿瘤组织的患者。本公开中优选的癌症类型包括例如胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,骨髓性白血病,小儿癌症(肾母细胞瘤,成神经细胞瘤,肉瘤,肝母细胞瘤,和生殖细胞肿瘤),但不限于此。更优选的癌症类型包括胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病,但不限于此(tumori.(2012)98,478-484;tumor biol.(2015)36,4671-4679;am j clin pathol(2008)130,224-230;adv anat pathol(2014)21,450-460;med oncol(2012)29,663-669;clinical cancer research(2004)10,6612-6621;appl immunohistochem mol morphol(2009)17,40-46;eur j pediatr surg(2015)25,138-144;j clin pathol(2011)64,587-591;am j surg pathol(2006)30,1570-1575;oncology(2007)73,389-394;diagnostic pathology(2010)64,1-6;diagnostic pathology(2015)34,1-6;am j clin pathol(2008)129,899-906;virchows arch(2015)466,67-76)。更优选的癌症类型包括胃癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和骨髓性白血病。
[1149]
本公开的包含抗cd137抗原结合分子的抗癌剂可用于治疗患有免疫检查点抑制剂治疗难治的癌症的患者。例如,可以用本公开的抗癌剂治疗对其施用免疫检查点抑制剂未产生期望功效的患者。“免疫检查点抑制剂治疗难治的癌症”也可以表示为“已经用免疫检查点抑制剂治疗的癌症”,“在用免疫检查点抑制剂治疗期间或之后恶化的癌症”,“免疫检查点抑制剂对其无效的癌症”,“免疫检查点抑制剂治疗后复发的癌症”,“对免疫检查点抑制剂治疗有抗性的癌症”,“免疫检查点抑制剂治疗效果不佳的癌症”,或“用免疫检查点抑
制剂治疗不成功的癌症”。
[1150]
上述免疫检查点抑制剂治疗难治的癌症包括在jak1、jak2/或b2m基因中具有突变的癌症(参见例如shin,daniel sanghoon等人“primary resistance to pd-1 blockade mediated by jak1/2 mutations.”cancer discovery vol.7,2(2017):188-201;或sade-feldman,moshe等人“resistance to checkpoint blockade therapy through inactivation of antigen presentation.”nature communications vol.8(1):1136.2017年10月26日),但不限于此。
[1151]
在进一步的方面,在本公开中,用于上述治疗方法、治疗用途和药物的包含抗cd137抗原结合分子或抗体的药物制剂可以包含有效量与不具有依赖于小分子化合物的cd137结合活性的抗cd137抗原结合分子相比,在非肿瘤组织中具有较低免疫激活水平的抗cd137抗原结合分子或抗体。
[1152]
在一个实施方案中,非肿瘤组织包括淋巴结、脾脏和/或肝脏。
[1153]
在进一步的实施方案中,用于上述治疗方法、治疗用途和药物的包含抗cd137抗原结合分子或抗体的药物制剂可以包含有效量的基本上不结合在非肿瘤组织中表达的cd137的抗cd137抗原结合分子或抗体。
[1154]
在进一步的实施方案中,用于上述治疗方法、治疗用途和药物的包含抗cd137抗原结合分子或抗体的药物制剂可以包含有效量的与不具有依赖于小分子化合物的cd137结合活性的抗cd137抗原结合分子相比,具有延长的血液半衰期的抗cd137抗原结合分子或抗体。
[1155]
在进一步的实施方案中,用于上述治疗方法、治疗用途和药物的包含抗cd137抗原结合分子或抗体的药物制剂可以包含有效量的与不具有依赖于小分子化合物的cd137结合活性的抗cd137抗原结合分子相比,具有低水平副作用的抗cd137抗原结合分子或抗体。
[1156]
在进一步的实施方案中,副作用包括ast升高、alt升高、发烧、恶心、急性肝炎、肝损伤、脾肿大、肠炎、皮肤化脓性炎症、中性粒细胞减少、淋巴细胞减少、血小板减少、转氨酶表达和/或高胆红素血症。
[1157]
在一个实施方案中,本公开的抗cd137抗原结合分子具有低副作用,因此可以增加剂量而无需担心副作用,结果,它们可以表现出更强的药物功效(细胞毒性活性或抗肿瘤活性)。
[1158]
在另一方面,本公开提供了包含本文提供的任何抗cd137抗原结合分子或抗体的药物制剂,例如,用于以上任何治疗方法中。在一个实施方案中,药物制剂包含本文提供的任何抗cd137抗原结合分子或抗体和药学上可接受的载体。
[1159]
本公开的抗原结合分子或抗体可以通过任何合适的方式施用,包括肠胃外、肺内和鼻内,并且如果需要局部治疗,则可以病灶内施用。肠胃外输注包括肌内、静脉内、动脉内、腹膜内或皮下施用。给药可以通过任何合适的途径进行,例如通过注射,例如静脉内或皮下注射,部分取决于是短期还是长期施用。本文考虑了各种给药方案,包括但不限于在各个时间点上的单次或多次施用、推注施用和脉冲输注。
[1160]
本公开的抗体将根据临床医学指南的方式配制、给药和施用。在此情况下考虑的因素包括正在治疗的特定病症、正在治疗的特定哺乳动物、个体患者的临床状况、病症的起因、药物的递送部位、施用方法,施用时间表以及其他从业人员已知的因素。该抗体不必但
是是任选地与目前用于预防或治疗所述病症的一种或多种试剂一起配制。这些其他试剂的有效量取决于制剂中存在的抗体的量、病症或治疗的类型以及上面讨论的其他因素。这些通常以与本文所述相同的剂量和施用途径使用,或以本文所述的剂量的约1-99%,或以经验/临床确定为合适的任何剂量和任何途径使用。
[1161]
为了预防或治疗疾病,本公开的抗体的合适剂量将取决于待治疗的疾病的类型,抗体的类型,疾病的严重程度和病程(无论该抗体是用于预防还是治疗目的),先前的治疗方法,患者的临床病史和对抗体的反应以及主治医师的判断力。将抗体在一次或一系列治疗中适当地施用于患者。根据疾病的类型和严重程度,大约1微克/千克至15毫克/千克(例如0.1毫克/千克-10毫克/千克)的抗体可以作为向患者施用的初始候选剂量,例如通过一次或多次单独施用,或通过连续输注。根据上述因素,一种典型的每日剂量范围可能从约1微克/千克到100毫克/千克或更高。对于几天或更长的重复给药,取决于病况,通常将持续治疗直至出现所需的疾病症状抑制。抗体的一种示例性剂量将在约0.05mg/kg至约10mg/kg的范围内。因此,可以向患者施用约0.5mg/kg、2.0mg/kg、4.0mg/kg或10mg/kg的一个或多个剂量(或其任何组合)。这样的剂量可以间歇地施用,例如每周或每三周(例如使患者接受约两至约二十剂,或例如约六剂抗体)。可以施用初始较高的负荷剂量,然后施用一个或多个较低的剂量。通过常规技术和测定很容易监测该疗法的进展。
[1162]
应该理解,可以使用本公开的免疫缀合物代替本公开的抗cd137抗原结合分子或抗体,或除本公开的抗cd137抗原结合分子或抗体之外使用本公开的免疫缀合物来进行任何上述制剂或治疗方法。使用的抗cd137抗原结合分子是包含表37所示的作为重链可变区/轻链可变区组合的a375/b167,a372/b040,a356/b040,a486/b167,a487/b167,a488/b226,a489/b223,a548/b376,a551/b256,a551/b379,a555/b379,a548/b256,或a549/b167的氨基酸序列的抗体。在优选的实施方案中,抗cd137抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其具有与a375/b167中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在进一步的实施方案中,抗cd137抗原结合分子可以是包含a375/b167作为重链可变区/轻链可变区的组合的抗cd137抗体。在不同的优选实施方案中,抗cd137抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其具有与a551/b379中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在进一步的实施方案中,抗cd137抗原结合分子可以是包含a551/b379作为重链可变区/轻链可变区的组合的抗cd137抗体。此外,所使用的抗cd137抗体可以是选自表72中所列抗体的任何一种抗cd137抗体。
[1163]
h.制品
[1164]
在本公开的另一方面,提供了制品,其包含用于治疗、预防和/或诊断上述病症的材料。所述制品包括容器和与所述容器相关联的标签或包装插页。合适的容器包括例如瓶、小瓶、注射器、iv溶液袋等。容器可以由多种材料形成,例如玻璃或塑料。所述容器本身容纳有组合物,并且可以具有无菌进入口(例如,所述容器可以是静脉内溶液袋或具有可被皮下注射针刺穿的塞子的小瓶)。组合物中的至少一种活性成分是本公开的抗体。标签或包装插页表明所述组合物用于治疗所选病况。在本公开的该实施方案中的制品可以进一步包括包装插页,其指示所述组合物可以用于治疗特定病况。替代地或另外地,制品可以进一步包括第二(或第三)容器,所述第二(或第三)容器包含药学上可接受的缓冲液,例如可抑菌注射
用水(bwfi)、磷酸盐缓冲盐水、林格氏溶液和葡萄糖溶液。从商业和用户的角度来看,它还可以包括其他材料,包括其他缓冲液、稀释剂、过滤器、针头和注射器。
[1165]
术语“包装插页”用于指通常包含在治疗产品的商业包装中的说明,该说明包含有关使用此类治疗产品的适应症、用法、剂量、施用、联合治疗、禁忌症和/或警告的信息。
[1166]
应当理解,以上任何制品均可包括本公开的免疫缀合物来代替抗cd137抗原结合分子或抗体,或在抗cd137抗原结合分子或抗体之外包括本公开的免疫缀合物。
[1167]
iii.组合疗法
[1168]
a.组合疗法和用于组合疗法的治疗组合物
[1169]
本公开涉及治疗和/或预防癌症的方法,其包括使用上述抗cd137抗原结合分子和另一种抗癌剂的组合。在一个实施方案中,本公开涉及包含抗cd137抗原结合分子的药物组合物,其与另一种抗癌剂用于组合疗法中。在进一步的实施方案中,本公开涉及与本公开的抗cd137抗原结合分子用于组合疗法中的药物组合物,其包含另一种抗癌剂。本公开涉及治疗或预防个体中的癌症和/或激活肿瘤组织内的免疫的方法,其包括施用抗cd137抗原结合分子和另一种抗癌剂。抗cd137抗原结合分子和/或其他抗癌剂通过组合使用来治疗癌症和/或发挥治疗癌症的协同或相加作用。
[1170]
在一些实施方案中,本公开的组合疗法提供了一种通过将另一种抗癌剂与上述抗cd137抗原结合分子一起使用来增强另一种抗癌剂在治疗或预防癌症中的治疗或预防效果的方法。此外,本公开的组合疗法提供了通过将抗cd137抗原结合分子与另一种抗癌剂一起使用来增强上述抗cd137抗原结合分子在治疗癌症时的治疗或预防效果的方法。在此,治疗或预防效果的增强是指,例如,治疗反应率的提高,用于治疗而施用的抗癌剂的量的减少,和/或抗癌剂的治疗期的缩短等,但不限于此。此外,本公开的组合疗法提供了一种增加个体无进展生存期的方法,包括施用有效量的上述抗cd137抗原结合分子和另一种抗癌剂。
[1171]
在一些实施方案中,本公开的组合疗法包括施用上述抗cd137抗原结合分子和另一种抗癌剂。抗cd137抗原结合分子和其他抗癌剂可以通过本领域已知的任何合适方法施用。例如,抗cd137抗原结合分子和其他抗癌剂可以并行(即同时)或顺序(即在不同时间)施用。当顺序施用抗cd137抗原结合分子和其他抗癌剂(即,在不同时间)时,抗cd137抗原结合分子和其他抗癌剂之间的施用间隔没有特别限定,并且可以考虑施用途径、剂型等因素进行设定。例如0至168小时,优选0至72小时,优选0至24小时,更优选0至12小时,但不限于此。
[1172]
上述抗cd137抗原结合分子和其他抗癌剂可以共同施用。抗cd137抗原结合分子也可以间断地(即,以不规则的间隔)施用。抗cd137抗原结合分子可以在施用其他抗癌剂之前施用。或者,抗cd137抗原结合分子可以在施用其他抗癌剂后施用。
[1173]
此外,其他抗癌剂可以间断地施用(即,以不规则的间隔)。其他抗癌剂也可以在施用抗cd137抗原结合分子之前施用。或者,其他抗癌剂可以在施用抗cd137抗原结合分子之后施用。
[1174]
在一些实施方案中,本文所述的抗cd137抗原结合分子和其他已知的或本文所述的抗癌剂可用于上述抗cd137抗原结合分子和另一种抗癌剂的组合疗法中。
[1175]
除了上述抗cd137抗原结合分子与其他抗癌剂的组合疗法之外,还可以进行另外的疗法。添加到本公开的组合疗法的疗法可以包括额外施用抗cd137抗原结合分子和/或其他抗癌剂。
[1176]
作为非限制性方面,本发明提供了针对癌细胞或含有癌细胞的肿瘤组织的免疫应答活化剂、癌症治疗剂或癌症预防剂(下文称为药物组合物等),其包含上述抗cd137抗原结合分子,另一种抗癌剂或抗cd137抗原结合分子与另一种抗癌剂的组合。本公开的药物组合物等可用于本公开的组合疗法。在一些实施方案中,通过将上述抗cd137抗原结合分子与另一种抗癌剂联合使用,与单独使用这些的治疗相比,本公开的药物组合物等在抑制细胞增殖、激活针对癌细胞或含有癌细胞的肿瘤组织的免疫,或治疗或预防癌症方面具有更强的作用。此外,通过将上述抗cd137抗原结合分子与另一种抗癌剂联合使用,本发明的药物组合物在抑制细胞生长,激活针对癌细胞或含癌细胞的肿瘤组织的免疫,或治疗或预防癌症方面具有协同或相加作用。
[1177]
在一些实施方案中,本公开的“包含抗cd137抗原结合分子和另一种抗癌剂的组合”的药物组合物等是指其中上述抗cd137抗原结合分子和另一种抗癌剂组合用于在治疗或预防疾病中同时、单独或顺序施用的药物组合物等。例如,本公开的药物组合物等可以以包含抗cd137抗原结合分子和另一种抗癌剂两者的组合药物的形式提供。此外,例如,在本公开的药物组合物等中,可以分别提供包含抗cd137抗原结合分子的药物和包含另一种抗癌剂的药物,并且这些药物可以同时或顺序使用。疾病没有特别限制,但优选为癌症。
[1178]
本公开提供与其他抗癌剂组合使用的药物组合物等,其包含上述抗cd137抗原结合分子作为活性成分。本公开还提供与上述抗cd137抗原结合分子组合使用的药物组合物等,其包含另一种抗癌剂作为活性成分。
[1179]
本发明提供通过将上述抗cd137抗原结合分子与其他抗癌剂组合来提高在用其他抗癌剂治疗癌症中的另一种抗癌剂的治疗效果的药物组合物等。此外,本公开提供通过将另一种抗癌剂与上述抗cd137抗原结合分子组合来提高在用抗cd137抗原结合分子治疗癌症中抗cd137抗原结合分子的治疗效果的药物组合物等。
[1180]
在一些实施方案中,本公开提供了抗cd137抗原结合分子和/或另一种抗癌剂在制备包含抗cd137抗原结合分子和/或其他抗癌剂作为活性成分的上述药物组合物等中的用途。
[1181]
在本发明中,含有上述抗cd137抗原结合分子和/或另一种抗癌剂作为活性成分是指含有抗cd137抗原结合分子和/或其他抗癌剂作为主要活性成分。因此,抗cd137抗原结合分子和/或其他抗癌剂的含量比例没有限制。
[1182]
在一些实施方案中,本文所述的抗cd137抗原结合分子和其他已知的或本文所述的抗癌剂可用于上述药物组合物等中。
[1183]
在一个非限制性实施方案中,与抗cd137抗原结合分子组合使用的其他抗癌剂包括氮芥类似物,烷基磺酸盐,乙烯亚胺,亚硝基脲,环氧化物,其他烷化剂,叶酸类似物,嘌呤类似物,嘧啶类似物,其他代谢拮抗剂,长春花生物碱或类似物,鬼臼毒素衍生物,喜树碱类似物,秋水仙碱衍生物,紫杉烷,其他植物生物碱或天然物质,放线菌素,蒽环类或相关物质,其他细胞毒性抗生素,铂化合物,甲基肼(methylhydrazine),激酶抑制剂,血管生成抑制剂,激素,dna修饰酶抑制剂,免疫刺激剂,蛋白酶体抑制剂,酶,组蛋白去乙酰化酶抑制剂,dna修饰酶抑制剂,细胞因子制剂,类视黄醇(retinoid),t细胞活化激动剂,免疫检查点抑制剂,吲哚胺2,3-双加氧酶(ido)抑制剂,共刺激性分子激活剂,天然杀伤细胞激活剂,t细胞重定向抗原结合分子,抗纤维化剂,调节性t细胞消耗剂,cd4
+ t细胞消耗剂,b细胞消
耗剂,天然杀伤细胞消耗剂,巨噬细胞消耗剂,单克隆抗体,其他分子靶向药物或其他抗癌剂,但不限于此。
[1184]
本公开中的“免疫检查点”是指在免疫活性细胞(包括t细胞)上表达并通过与配体结合向免疫活性细胞传递抑制免疫应答的信号的分子。免疫检查点及其配体包括,例如,pd-1,ctla-4,tim3,lag3,pd-l1,pd-l2,btnl2,b7-h3,b7-h4,cd48,cd80,2b4,btla,cd160,cd60,cd86,vista或tigit分子,但不限于这些。在一些实施方案中,本公开中的“免疫检查点抑制剂”是指通过抑制免疫检查点与其配体的结合来抑制免疫检查点的信号转导的试剂。优选地,免疫检查点抑制剂是与免疫检查点或其配体结合并抑制免疫检查点的信号转导的抗原结合分子,优选抗体或抗体片段。
[1185]
在一个非限制性实施方案中,提供了一种药物组合物,其中上述其他抗癌剂为化疗剂、t细胞活化激动剂、免疫检查点抑制剂、t细胞重定向抗原结合分子、抗纤维化剂、血管生成剂抑制剂、调节性t细胞消耗剂、cd4
+
t细胞消耗剂、b细胞消耗剂、天然杀伤细胞消耗剂或巨噬细胞消耗剂。
[1186]
在一个非限制性实施方案中,化疗剂包括但不限于抗代谢物、植物生物碱或铂化合物。抗代谢物的优选实例包括但不限于依诺他滨、卡培他滨、卡莫氟、吉西他滨、阿糖胞苷、替加氟、替加氟尿嘧啶、奈拉滨、氟尿嘧啶、氟达拉滨、培美曲塞、喷司他丁和甲氨蝶呤。抗代谢物的特别优选的实例是卡培他滨。植物生物碱的优选实例包括但不限于伊立替康、依托泊苷、索布佐生多西他赛、诺替康(nogitecan)、紫杉醇、长春瑞滨、长春新碱、长春地辛和长春碱。特别优选的植物生物碱的实例包括紫杉醇。铂化合物的优选实例包括但不限于奥沙利铂、卡铂、顺铂和奈达铂。特别优选的铂化合物的实例包括顺铂、卡铂或它们的组合。
[1187]
在一个非限制性实施方案中,t细胞活化激动剂包括但不限于tnf受体超家族(tnfrsf)的激动性抗体或共刺激分子的激动性抗体。
[1188]“共刺激分子的激动性抗体”靶向的分子包括tmigd2、hhla2、icos、icos配体、cd28、cd80、cd86等。优选的共刺激分子激动性抗体的实例是抗cd28抗体。
[1189]“tnf受体超家族的激动性抗体”所靶向的分子没有特别限定,只要是活化表达tnf受体超家族的细胞(例如t细胞、nk细胞)的因子即可,但优选是属于“tnf超家族”或“tnf受体超家族”的因子。作为属于“tnf超家族”或“tnf受体超家族”的因子,已知具有三聚体结构的配体和与该配体结合的具有三聚体结构的受体(其有助于各种免疫细胞的活化)(nat.rev.immunol.,2012,12,339-51)。属于tnf超家族或tnf受体超家族的因子包括,例如,cd137,cd137l,cd40,cd40l,ox40,ox40l,cd27,cd70,hvem,light,rank,rankl,cd30,cd153,gitr,gitrl,tnfrsf25和tl1a。ox40激动剂抗体的实例包括moxr0916,medi6469,medi0562,medi6383,pf-04518600,gsk-3174998和各种已知的ox40激动剂抗体。cd40激动剂抗体的实例包括rg-7876,adc-1013,sea-cd40,apx005m,达西组单抗(dacetuzumab)和各种已知的cd40激动剂抗体。gitr激动性抗体的实例包括amg228,amk-1248,mk-4166,bms-986156,trx518和各种已知的gitr激动剂抗体。cd27激动剂抗体的实例包括伐立鲁单抗(varlilumab)(cas登记号:1393344-72-3)和各种已知的cd27激动剂抗体。cd137激动剂抗体的实例包括乌瑞鲁单抗(urelumab)(cas登记号:934823-49-1),pf-05082566和各种已知的cd137激动剂抗体。cd137激动性抗体可以是与cd137结合的双特异性抗原结合分子(例如,与cd137和癌抗原结合的双特异性抗体,或与cd137配体(4-1bbl)和癌抗原结合的融合
蛋白等)。
[1190]
在一个非限制性实施方案中,免疫检查点抑制剂的实例包括抗pd-1抗体、抗pd-l1抗体、抗ctla-4抗体、抗tim3抗体、抗lag3抗体或抗tigit抗体,但不限于此。例如,抗pd-1抗体的实例包括派姆单抗(cas注册号:1374853-91-4)、纳武单抗(cas注册号:946414-94-4)、medi0680、pdr001、bgb-a317、regn2810、shr-1210、pf-06801591和各种已知的抗pd1抗体。抗pd-l1抗体的实例包括阿特珠单抗(cas注册号:1380723-44-3)、阿维单抗(avelumab)(cas注册号:1537032-82-8)、度伐鲁单抗(cas注册号:1428935-60-7)、mdx-1105和各种已知的抗pd-l1抗体。抗ctla-4抗体的实例包括伊匹单抗(ipilimumab)(cas注册号:477022-00-9)、替西木单抗(tremelimumab)(cas注册号:745013-59-6)和各种已知的抗ctla-4抗体。抗tim3抗体的实例包括mbg452和各种已知的抗tim3抗体。抗lag3抗体的实例包括bms-986016、lag525和各种已知的抗lag3抗体。抗tigit抗体的实例包括替瑞利尤单抗(tiragolumab)(rg6058)和各种已知的抗tigit抗体。免疫检查点抑制剂还可以是与(1)免疫检查点分子和(2)tnf受体超家族(tnfrsf)成员或共刺激分子结合的双特异性抗原结合分子。在一个实施方案中,本公开的组合疗法可以是使用cd137抗原结合分子、抗pd-1抗体和抗tigit抗体的三剂组合,或使用cd137抗原结合分子、抗pd-l1抗体和抗tigit抗体的三剂组合。
[1191]
在一个实施方案中,本公开的抗cd137抗原结合分子和免疫检查点抑制剂(优选抗pd-l1抗体)在联合使用时治疗癌症和/或在治疗癌症中发挥协同或相加作用,并有暂时或轻微的副作用。尽管这不旨在受特定理论的约束,但将抗cd137抗原结合分子施用于个体会活化个体肿瘤组织内的免疫细胞。pd-l1的表达是由免疫细胞的这种活化诱导的,pd-l1
+
细胞具有抑制活化的免疫应答的作用。因此,在抗cd137抗原结合分子与抗pd-l1抗体的组合疗法中,pd-l1
+
细胞的作用被抗pd-l1抗体抑制,并且可以发挥更强的抗肿瘤作用。副作用的实例包括但不限于体重减轻和肝功能障碍(asl和/或alt水平升高)。
[1192]
在一个非限制性实施方案中,“t细胞重定向抗原结合分子”是包含“含有具有t细胞受体复合物结合活性的抗体可变区的结构域”和“含有具有癌抗原结合活性的抗体可变区的结构域”的多特异性抗原结合分子。优选多特异性抗体,更优选双特异性抗体。多特异性(或双特异性)抗体可以具有单链抗体结构,例如抗体可变区通过接头所结合的结构。t细胞重定向抗原结合分子还可以含有与fcγ受体的结合活性降低的fc区。
[1193]“包含具有癌抗原结合活性的抗体可变区的结构域”是指抗体的一部分,其包含与癌抗原的一部分或整个癌抗原特异性结合并且与其互补的区域。如本文所用,术语“癌症特异性抗原”是指由癌细胞表达的能够区分癌细胞和健康细胞的抗原,例如,包括随着细胞变为恶性而表达的抗原,或当细胞癌变时出现在细胞表面和蛋白质分子上的异常糖链。实例是本文公开的各种抗原(例如,在“ii.组合物和方法(抗cd137激动性抗原结合分子),a.示例性抗cd137抗原结合分子或抗体,6.多特异性抗体”中),但不仅限于此。本公开的癌症特异性抗原结合结构域所靶向的癌症特异性抗原特别优选为在细胞表面表达的抗原,这种抗原例如包括gpc3,cd19,cd20,egfr,her2,epcam,ereg,fap,cea,dll3,密蛋白(claudin)-6和fgfr3。
[1194]
在一个实施方案中,抗t细胞抗原结合分子是多特异性抗体,优选双特异性抗体,其包含(1)含有具有磷脂酰肌醇聚糖3结合活性的抗体可变区的结构域,(2)含有具有t细胞
受体复合物结合活性的抗体可变区的结构域,和(3)含有对fcγ受体的结合活性降低的fc区的结构域。在一个实施方案中,关于具有磷脂酰肌醇聚糖3结合活性的抗体可变区和具有t细胞受体复合物结合活性的抗体可变区中所含的抗体l链可变区,优选获得能够对具有磷脂酰肌醇聚糖3结合活性的h链和具有t细胞受体复合物结合活性的h链两者都赋予结合能力的共同l链,并将其用作上述双特异性抗体的共同l链可变区。
[1195]
在一个实施方案中,抗t细胞抗原结合分子是ery974。ery974是一种双特异性抗体,其包含(1)含有具有磷脂酰肌醇聚糖3结合活性的抗体可变区的结构域,(2)含有具有t细胞受体复合物结合活性的抗体可变区的结构域,和(3)含有对fcγ受体的结合活性降低的fc区的结构域,并且包含:
[1196]-tr01h113,公开于wo2016/047722作为cd3侧的重链可变区,
[1197]-e2702sksc,公开于wo 2016/047722作为cd3侧的重链恒定区,
[1198]-gch065,公开于wo2016/047722作为gpc3侧的重链可变区,
[1199]-e2704sepsc,公开于wo2016/047722作为gpc3侧的重链恒定区,
[1200]-l0011,公开于wo2016/047722作为共同轻链可变区,和
[1201]-k0,公开于wo 2016/047722作为共同轻链恒定区。
[1202]“含有具有t细胞受体复合物结合活性的抗体可变区的结构域”优选为包含具有t细胞受体结合活性的抗体可变区的结构域,更优选为包含具有cd3结合活性的抗体可变区的结构域。此外,上述“含有抗体可变区的结构域”由一个或多个抗体的可变结构域提供,优选地,含有抗体可变区的结构域含有抗体轻链可变区(vl)和抗体重链可变区(vh)。含有这种抗体可变区的结构域的实例包括各种抗体片段,例如“scfv(单链fv)”、“单链抗体”、“fv”和“scfv2(单链fv2)”、“fab”或“f(ab’)2”等。
[1203]
在一个非限制性实施方案中,“抗纤维化药物”是抑制或压制纤维化的药物,实例包括但不限于吡非尼酮和尼达尼布(nintedanib)。此外,抗纤维化药物可以是透明质酸酶药物,例如pegph20。
[1204]
在一个非限制性实施方案中,血管生成抑制剂的实例包括但不限于抗-vegf抗体和抗-vegfr2抗体。血管生成抑制剂的实例包括贝伐单抗、雷莫芦单抗(ramucirumab)、索拉非尼、依维莫司、西罗莫司(temsirolimus)、乐伐替尼(lenvatinib)、阿柏西普(aflibercept)和各种已知的血管生成抑制剂。
[1205]
在一个非限制性实施方案中,“调节性t细胞消耗剂”是消耗调节性t细胞的试剂,包括抗cd4抗体、抗cd25抗体、抗ccr4抗体和抗ctla4抗体,但不限于此。
[1206]
在一个非限制性实施方案中,“cd4
+
细胞消耗剂”是消耗cd4
+
细胞的药剂,其实例包括但不限于抗cd4抗体。
[1207]
在一个非限制性实施方案中,“b细胞消耗剂”、“天然杀伤细胞消耗剂”和“巨噬细胞消耗剂”是分别消耗b细胞、天然杀伤细胞和巨噬细胞的试剂。例如,b细胞消耗剂包括但不限于利妥昔单抗和奥比妥珠单抗(obinutuzumab),而巨噬细胞消耗剂包括但不限于抗csflr抗体。
[1208]
在一个非限制性实施方案中,“单克隆抗体”包括例如抗tgfβ抗体、抗潜在tgfβ抗体、抗il-8抗体等,但不限于此。
[1209]
在一些实施方案中,本发明的其他抗癌剂可以是任何抗癌剂,没有特别限制,只要
与本发明的抗cd137抗原结合分子联合使用时,其治疗或预防作用增强或它增强了抗cd137抗原结合分子的治疗或预防作用即可。
[1210]
在一个非限制性实施方案中,本公开的组合疗法可以包括上述抗cd137抗原结合分子和至少一种其他治疗剂、免疫调节剂、癌症治疗疫苗、过继(adopted)t细胞疗法等,但不限于这些。合适的癌症治疗疫苗包括但不限于全肿瘤细胞疫苗、肿瘤抗原疫苗、基于载体的疫苗、溶瘤病毒疫苗和树突细胞疫苗。除上述疗法外,还可以进行多学科治疗联合手术、放射疗法等。
[1211]
在一个非限制性实施方案中,本公开的组合疗法可以通过将上述抗cd137抗原结合分子与使用细胞因子作为抗肿瘤免疫应答增强剂的细胞因子疗法组合来进行。此类细胞因子的实例包括il-2,il-7,il-12,il-15,il-17,il-18,il-21,il-23,il-27,gm-csf,ifnα(干扰素-α),ifnα-2b,ifnβ和ifnγ,但不限于此。
[1212]
在一个非限制性方面,本发明提供一种细胞生长压制剂、细胞生长抑制剂、免疫应答激活剂、癌症治疗剂或癌症预防剂,其包含上述药物组合物。
[1213]
施用上述抗cd137抗原结合分子和/或另一种抗癌剂的“个体”可以是人。在一些实施方案中,个体是具有癌细胞或包含癌细胞的肿瘤组织的患者。本公开中优选的癌症类型包括例如胃癌,头颈癌,食道癌,结肠直肠癌,肺癌,间皮瘤,肝癌,卵巢癌,乳腺癌,结肠癌,肾癌,皮肤癌,肌肉肿瘤,胰腺癌,前列腺癌,睾丸癌,子宫癌,胆管癌,梅克尔细胞癌,膀胱癌,甲状腺癌,神经鞘瘤,肾上腺癌,肛门癌,中枢神经系统肿瘤,神经内分泌组织肿瘤,阴茎癌,胸膜肿瘤,唾液腺肿瘤,外阴癌,胸腺瘤,淋巴瘤,髓细胞性白血病,小儿癌症(肾母细胞瘤,成神经细胞瘤,肉瘤,肝母细胞瘤和生殖细胞瘤),但不限于此。更优选的癌症类型包括胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和髓细胞性白血病,但不限于此(tumori.(2012)98,478-484;tumor biol.(2015)36,4671-4679;am j clin pathol(2008)130,224-230;adv anat pathol(2014)21,450-460;med oncol(2012)29,663-669;clinical cancer research(2004)10,6612-6621;appl immunohistochem mol morphol(2009)17,40-46;eur j pediatr surg(2015)25,138-144;j clin pathol(2011)64,587-591;am j surg pathol(2006)30,1570-1575;oncology(2007)73,389-394;diagnostic pathology(2010)64,1-6;diagnostic pathology(2015)34,1-6;am j clin pathol(2008)129,899-906;virchows arch(2015)466,67-76)。更优选的癌症类型包括胃癌、结肠直肠癌、肺癌、间皮瘤、肝癌、乳腺癌、皮肤癌、淋巴瘤和髓细胞性白血病。
[1214]
在本公开中,个体可以是在抗cd137抗原结合分子和另一种抗癌剂的组合疗法之前已接受上述抗cd137抗原结合分子和/或任何抗癌剂治疗的患者。或者,个体可以是不能接受标准疗法或标准疗法对其无效的个体。在一些实施方案中,个体所具有的癌症处于早期或晚期。
[1215]
包含本公开的抗cd137抗原结合分子和另一种抗癌剂的组合疗法或用于组合疗法的药物组合物可用于治疗患有免疫检查点抑制剂治疗难治的癌症的患者。例如,本公开的组合疗法(药物组合物)可用于治疗通过施用免疫检查点抑制剂未观察到所需功效的患者。“免疫检查点抑制剂难治的癌症”也可以表示为“已经用免疫检查点抑制剂治疗的癌症”,“在用免疫检查点抑制剂治疗期间或之后恶化的癌症”,“免疫检查点抑制剂对其无效的癌症”,“免疫检查点抑制剂治疗后复发的癌症”,“对免疫检查点抑制剂治疗有抗性的癌症”,“免疫检查点抑制剂治疗效果不佳的癌症”,或“用免疫检查点抑制剂治疗不成功的癌症”。包含在组合疗法(药物组合物)中的其他抗癌剂的优选实例包括但不限于免疫检查点抑制剂或t细胞重定向抗原结合分子。
[1216]
上述免疫检查点抑制剂治疗难治的癌症包括在jak1、jak2/或b2m中具有基因突变的癌症(shin,daniel sanghoon等人“primary resistance to pd-1 blockade mediated by”jak1/2 mutations”.cancer discovery vol.7,2(2017):188-201;或sade-feldman,moshe等人“resistance to checkpoint blockade therapy through inactivation of antigen presentation.”nature communications vol.8,1 1136.26 oct.2017,等),但不限于此。
[1217]
或者,本公开的组合疗法(药物组合物)可用于治疗患有本公开的抗癌剂治疗难治的癌症的个体。例如,本公开的组合疗法(药物组合物)用于治疗在施用抗癌剂后对本公开的抗癌剂变得具有抗性的个体,或通过施用本公开的抗癌剂未观察到所需功效的个体。换言之,已经用本公开的抗癌剂疗法治疗过的癌症可以用本公开的组合疗法(药物组合物)来治疗。包含在药物组合物中的另一种抗癌剂的优选实例包括但不限于免疫检查点抑制剂或t细胞重定向抗原结合分子。
[1218]
在另一方面,本公开提供了一种通过上述组合疗法激活个体肿瘤组织中的免疫细胞的方法。在一个实施方案中,该方法包括向个体施用有效量的抗癌剂,其中该抗癌剂包含抗cd137抗原结合分子和另一种抗癌剂。在进一步的实施方案中,在本公开中,此类免疫细胞包括b细胞、树突状细胞、天然杀伤细胞、巨噬细胞和/或cd8
+ t细胞(更具体地,这些免疫细胞侵入肿瘤组织)。在该方法中,当肿瘤组织中选自cd3e、cd8b1、gzmb、prf1和ifng中的至少一种基因的表达水平升高时,可以判断肿瘤组织中t细胞的活化增强。
[1219]
在另一方面,本公开提供了一种通过上述组合疗法激活个体肿瘤组织中的免疫细胞特别是cd8
+
t细胞或促进其增殖的方法。在一个实施方案中,该方法包括向个体施用有效量的抗癌剂,其中该抗癌剂包含抗cd137抗原结合分子和另一种抗癌剂。在激活cd8
+
t细胞的方法中,当至少一种选自ova四聚体、颗粒酶b、pd-1、klrg-1和icos的cd8
+ t细胞活化标志物的阳性率增加时(阳性率(%)=肿瘤组织中活化标志物阳性的cd8
+ t细胞数/肿瘤组织中cd8
+ t细胞数
×
100),可以判断肿瘤组织中的cd8
+ t细胞被激活。
[1220]
应当理解,可以使用本公开的免疫缀合物代替本公开的抗cd137抗原结合分子或抗体,或除本公开的抗cd137抗原结合分子或抗体之外使用本公开的免疫缀合物来进行任何上述组合疗法或用于组合疗法的治疗组合物。使用的抗cd137抗原结合分子是包含表37所示的作为重链可变区/轻链可变区组合的a375/b167,a372/b040,a356/b040,a486/b167,a487/b167,a488/b226,a489/b223,a548/b376,a551/b256,a551/b379,a555/b379,a548/b256,或a549/b167的氨基酸序列的抗体。在优选的实施方案中,抗cd137抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其具有与a375/b167中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在进一步的实施方案中,抗cd137抗原结合分子可以是包含a375/b167作为重链可变区/轻链可变区的组合的抗cd137抗体。在不同的优选实施方案中,抗cd137抗原结合分子是包含hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3的抗cd137抗体,其具有与a551/b379中包含的hvr-h1、hvr-h2、hvr-h3、hvr-l1、hvr-l2和hvr-l3相同的氨基酸序列。在进一步的实施方案中,抗
cd137抗原结合分子可以是包含a551/b379作为重链可变区/轻链可变区的组合的抗cd137抗体。此外,所使用的抗cd137抗体可以是选自表72中所列抗体的任何一种抗cd137抗体。
[1221]
b.试剂盒
[1222]
在另一个方面,本公开提供了用于治疗或预防在以上“g.治疗方法或预防组合物”中详细描述的肿瘤或癌症所示例的多种疾病或病症的试剂盒,在该治疗或预防中,本公开的抗cd137抗原结合分子(或其免疫缀合物)或包含它们的药物组合物与在以上“a.组合疗法和用于组合疗法的治疗组合物”中详细描述的至少一种其他抗癌剂组合。本公开中的这种试剂盒可以例如作为用于治疗或预防癌症(或肿瘤)的试剂盒提供。
[1223]
本公开中的试剂盒包含本公开的抗cd137抗原结合分子(或其免疫偶联物)或包含它们的药物组合物(或药物制剂)作为活性成分,以及(2)说明书或标签,指示在向患者施用药物组合物之前、同时或之后施用至少一种其他抗癌剂。
[1224]
在本公开的试剂盒中,活性成分可以填充在容器中。
[1225]
本公开的试剂盒可包括容器上的标签或附接到容器的包装插页。
[1226]
本公开的试剂盒被提供作为商业包装,例如作为治疗产品。
[1227]
本公开中的容器优选包括例如瓶子、小瓶、注射器、iv溶液袋等。容器可以由各种材料制成,例如玻璃和塑料。容器可以单独容纳活性成分或可以具有无菌入口(例如,容器可以是袋子或小瓶,其中含有用于静脉内施用的溶液,带有可以被皮下注射针刺穿的塞子)。
[1228]
本公开中的标签或包装插页通常包含在上述治疗产品的商业包装中,其是本公开试剂盒的一个实例,用于指此类治疗产品的使用说明书,其包含有关适应症、使用方法、剂量、施用方法、组合疗法、禁忌症和/或警告的信息。对于组合疗法,例如,它可以包含说明书,该说明书用于组合使用本公开中的抗cd137抗原结合分子(或其免疫缀合物)或包含它们的药物组合物(或药物制剂)以及如上文“a.组合疗法和用于组合疗法的治疗组合物”中详细描述的至少一种其他抗癌剂。
[1229]
本公开的试剂盒还可包括第二(或第三)容器,该容器包括药学上可接受的缓冲液,例如抑菌注射用水(bwfi)、磷酸盐缓冲盐水、林格溶液和葡萄糖溶液。本公开的试剂盒还可包括从商业角度或从用户角度所需的其他设备,例如其他缓冲剂、稀释剂、过滤器、针头和注射器。
[1230]
[实施例]
[1231]
以下是本公开的方法和组合物的实施例。可以理解,可以根据以上的一般描述来实施各种其他方面。
[1232]
实施例1:通过使用hcd137ki小鼠(llc1/ova/gpc3克隆c5细胞)的同系(syngeneic)肿瘤细胞移植模型的抗cd137抗体的抗肿瘤活性评估
[1233]
(1-1)细胞系和同系肿瘤移植小鼠模型的制备及抗肿瘤活性评价
[1234]
在该研究中,使用了内部建立的小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞(如参考实施例9-4-1所述)和hcd137 ki小鼠(如参考实施例6-3中所述)。将llc1/ova/gpc3克隆c5细胞系皮下移植到小鼠腹部,当肿瘤体积达到164-465mm3时将小鼠分组。移植后10天进行分组。如下表6所示,在移植后11天和14天将a551-mb110/b379-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。
[1235]
[表6]
[1236][1237][1238]
在移植后10天、14天、17天和21天测量肿瘤体积。
[1239]
通过以下公式计算肿瘤体积(tv)。
[1240]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1241]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1242]
tv变化(mm3)=测量时的肿瘤体积-分组时的肿瘤体积
[1243]
tgi(%)=(1-(每组tv变化的平均值/赋形剂对照组tv变化的平均值))
×
100
[1244]
结果,a551-mb110/b379-ml0r抗体在7.5、2.5和0.83mg/kg针对llc1/ova/gpc3克隆c5细胞显示103、101和106%的肿瘤生长抑制率(图1,表7)。即,a551-mb110/b379-ml0r抗体在本实施例的所有剂量下都显示出可比的高抗肿瘤活性。2.5mg/kg施用组中的一名个体必须实施安乐死,因为在肿瘤移植后15天,由于肿瘤细胞在腹膜内扩散,总体状况恶化。
[1245]
[表7]
[1246][1247]
(1-2)细胞系和同系肿瘤移植小鼠模型的制备,和肿瘤内反应(基因表达水平)的评价
[1248]
在该研究中,使用了内部建立的llc1/ova/gpc3克隆c5细胞(如参考实施例9-4-1所述)和hcd137 ki小鼠(如参考实施例6-3中所述)。将llc1/ova/gpc3克隆c5细胞系皮下移植到小鼠腹部,当肿瘤体积达到100-180mm3时将小鼠分组。移植后10天进行分组。如下表8所示,在移植后11天和14天将赋形剂对照和a551-mb110/b379-ml0r抗体抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂。
[1249]
[表8]
[1250][1251][1252]
移植后15天收集肿瘤。将收集的肿瘤浸入rna-later(qiagen)中并储存。从肿瘤样品中提取总rna。使用ncounter pancancer mouse immune profiling panel(nanostring technologies)和ncounter digital analyzer(nanostring technologies)测量总rna的基因表达水平。
ova细胞)的抗cd137抗体的抗肿瘤活性评估
[1269]
(2-1)细胞系和同系肿瘤移植小鼠模型的制备,以及a551-mb110/b379-ml0r抗体的抗肿瘤活性的评估
[1270]
在本研究中,使用了小鼠淋巴瘤细胞系e.g7-ova细胞(atcc,crl-2113)和hcd137 ki小鼠(参考实施例6-3中所述)。将e.g7-ova细胞系皮下移植到小鼠腹部,当肿瘤体积达到约200mm3时将小鼠分组。移植后7天进行分组。如下表10所示,在移植后7天和10天将a551-mb110/b379-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。
[1271]
[表10]
[1272][1273]
在移植后7天、10天、14天、17天、21天、24天和28天测量肿瘤体积。
[1274]
通过以下公式计算肿瘤体积(tv)。
[1275]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1276]
结果,在e.g7-ova细胞移植模型中,在移植后21天,赋形剂对照组的平均肿瘤体积为2611.8mm3。a551-mb110/b379-ml0r 0.83和2.5mg/kg组的平均肿瘤体积分别为1755.7mm3和1322.1mm3。与赋形剂对照组相比,a551-mb110/b379-ml0r 0.83和2.5mg/kg组在移植后28天显示出显著较低的值(williams检验)。赋形剂对照组和a551-mb110/b379-ml0r2.5mg/kg组的肿瘤体积变化见图4。
[1277]
(2-2)细胞系和同系肿瘤移植小鼠模型的制备,以及评估a375-migg1/b167-ml0r抗体抗肿瘤活性的方法
[1278]
在本研究中,使用了来自atcc的小鼠淋巴瘤细胞系e.g7-ova细胞(crl-2113)和hcd137 ki小鼠(参考实施例6-3中所述)。将e.g7-ova细胞皮下移植到小鼠腹部,当肿瘤体积达到约200-400mm3时将小鼠分组。移植后7天进行分组。如下表11所示,在移植后7天和10天将a375-migg1/b167-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。
[1279]
[表11]
[1280][1281]
在移植后7天、10天、15天、18天、21天、25天、29天和36天测量肿瘤体积。
[1282]
通过以下公式计算肿瘤体积(tv)。
[1283]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1284]
结果,a375-migg1/b167-ml0r抗体对e.g7-ova细胞显示出强的抗肿瘤作用,并且在5只小鼠中有4只观察到完全肿瘤消退(图5)。
[1285]
实施例3:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(c1498细胞)的抗cd137抗体的抗肿瘤活性评估
[1286]
在本研究中,使用了来自atcc的小鼠aml(急性髓细胞性白血病)细胞系c1498细胞(atcc,item号:tib-49)和hcd137 ki小鼠(参考实施例6-3中所述)。将c1498细胞系皮下移植到小鼠腹部,当肿瘤体积达到约270mm3时将小鼠分组。移植后7天进行分组。如下表12所示,在移植后7天和10天将a551-mb110/b379-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。
[1287]
[表12]
[1288][1289]
在移植后7天、10天、14天、17天、21天、24天和28天测量肿瘤体积。
[1290]
通过以下公式计算肿瘤体积(tv)。
[1291]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1292]
结果,在c1498细胞移植模型中,在移植后17天,赋形剂对照组的平均肿瘤体积为3405.3mm3。a551-mb110/b379-ml0r 2.5mg/kg组的平均肿瘤体积为2181.3mm3。与赋形剂对照组相比,a551-mb110/b379-ml0r2.5mg/kg组在移植后17天显示出较低的值。赋形剂对照组和a551-mb110/b379-ml0r 2.5mg/kg组的肿瘤体积变化见图6。
[1293]
实施例4:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(hepa1-6/hgpc3细胞)的抗cd137抗体的抗肿瘤活性评估
[1294]
(4-1)细胞系和同系肿瘤移植小鼠模型的制备,以及a551-mb110/b379-ml0r抗体的抗肿瘤活性的评估
[1295]
在本研究中,使用小鼠肝癌细胞系hepa1-6/hgpc3细胞(science translational medicine 04oct 2017,vol.9,issue 410,eaal4291)和hcd137ki小鼠(参考实施例6-3中所述),其中所述hepa1-6/hgpc3细胞是通过将人磷脂酰肌醇聚糖-3(gpc3)的表达质粒引入来自atcc的hepa1-6细胞(crl-1830)而制备的。将hepa1-6/hgpc3细胞系皮下移植到小鼠腹部,当肿瘤体积达到约200mm3时将小鼠分组。移植后10天进行分组。如下表13所示,在移植后10天和13天将a551-mb110/b379-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。
[1296]
[表13]
[1297][1298]
在移植后10天、13天、17天、20天、24天、27天和31天测量肿瘤体积。
[1299]
通过以下公式计算肿瘤体积(tv)。
[1300]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1301]
结果,在hepa1-6/hgpc3细胞移植模型中,在移植后31天,赋形剂对照组的平均肿瘤体积为1525.3mm3。a551-mb110/b379-ml0r 2.5mg/kg组的平均肿瘤体积为471.6mm3。与赋形剂对照组相比,a551-mb110/b379-ml0r 2.5mg/kg组在移植后31天显示出较低的值。赋形
剂对照组和a551-mb110/b379-ml0r 2.5mg/kg组的肿瘤体积变化见图7。
[1302]
(4-2)细胞系和同系肿瘤移植小鼠模型的制备,以及a375-migg1/b167-ml0r抗体的抗肿瘤活性的评估
[1303]
在本研究中,使用小鼠肝癌细胞系hepa1-6/gpc3细胞(science translational medicine 2017年10月4日,vol.9,issue 410,eaal4291)和hcd137ki小鼠(参考实施例6-3中所述),其中所述hepa1-6/gpc3细胞是通过将人磷脂酰肌醇聚糖-3(gpc3)的表达质粒引入来自atcc的hepa1-6细胞(crl-1830)而制备的。将hepa1-6/gpc3细胞皮下移植到小鼠腹部,当肿瘤体积达到约200-300mm3时将小鼠分组。移植后7天进行分组。如下表14所示,在移植后7天和10天将a375-migg1/b167-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。
[1304]
[表14]
[1305][1306][1307]
在移植后7天、10天、13天、18天和20天测量肿瘤体积。
[1308]
通过以下公式计算肿瘤体积(tv)。
[1309]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1310]
结果,a375-migg1/b167-ml0r抗体对hepa1-6/gpc3细胞显示出抗肿瘤作用(图8)。
[1311]
实施例5:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(llc1/ova/gpc3克隆c5)评估各种免疫细胞对抗cd137抗体的抗肿瘤活性的作用
[1312]
在该研究中,使用了内部建立的小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞(如参考实施例9-4-1所述)和hcd137 ki小鼠(如参考实施例6-3中所述)。将llc1/ova/gpc3克隆c5细胞系皮下移植到小鼠腹部,当肿瘤体积达到约200-300mm3时将小鼠分组。移植后9天进行分组。如下表15所示,在移植后10天和14天将a551-mb110/b379-ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。此外,如下表16所示,施用用于消耗各种免疫细胞的试剂。
[1313]
[表15]
[1314][1315]
[表16]
[1316][1317]
在移植后9天、14天、17天和20天测量肿瘤体积。
[1318]
通过以下公式计算肿瘤体积(tv)。
[1319]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1320]
结果,a551-mb110/b379-ml0r抗体针对llc1/ova/gpc3克隆c5细胞的功效通过cd8t细胞的消耗而显著受损(图9)。由此推断,该模型中的药效主要由cd8t细胞发挥。另一方面,cd4t细胞、b细胞、nk细胞和巨噬细胞的消耗倾向于增强药效(图9)。由此表明,a551-mb110/b379-ml0r抗体与消耗这些免疫细胞的试剂的联合使用可有效提高药效。
[1321]
实施例6:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(mc38细胞)评估抗cd137抗体单剂或与抗pd-l1抗体的组合疗法
[1322]
(6-1)细胞系和同系肿瘤移植小鼠模型的制备,以及a551-mb110/b379-ml0r(单剂或组合)的抗肿瘤活性及体重变化率的评估
[1323]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到约100-240mm3时认为模型建立。模型建立后,对移植mc38细胞系的小鼠进行分组,然后以表17所示的剂量,施用a551-mb110/b379-ml0r和/或抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)。a551-mb110/b379-ml0r在移植后15天和18天通过尾静脉途径施用两次。抗小鼠pd-l1抗体在移植后15天和18天通过腹膜内途径施用两次。含有0.05%吐温20的pbs用于赋形剂对照。
[1324]
[表17]
[1325][1326]
在移植后14天、18天、21天和25天测量肿瘤体积和体重。
[1327]
通过以下公式计算肿瘤体积(tv)。
[1328]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1329]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1330]
tv变化(mm3)=移植后25天的肿瘤体积-分组时的肿瘤体积
[1331]
tgi(%)=(1-(每组tv变化的平均值/赋形剂对照组tv变化的平均值))
×
100
[1332]
根据下式计算重量变化率。
[1333]
重量变化率(%)=100
×
测量日重量/移植后14天重量
[1334]
结果,对于mc38细胞,与a551-mb110/b379-ml0r单剂组或抗小鼠pd-l1抗体单剂组相比,a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组观察到肿瘤生长抑制作用增强。具体来说,a551-mb110/b379-ml0r单剂组的肿瘤生长抑制率为82%,而与抗小鼠pd-l1抗体的a551-mb110/b379-ml0r组合组的肿瘤生长抑制率为117%(图10,表18)。在所有施用组中,与施用开始相比,观察到在6.5%内的短暂体重减轻,但此后有恢复的趋势(图11)。
[1335]
[表18]
[1336]
移植后25天肿瘤生长抑制
[1337][1338]
(6-2)基于同系小鼠模型的rna-seq数据绘制显示药物施用前后免疫相关基因表达变化的热图(尤其是抗pd-l1抗体组合组)
[1339]
表达值fpkm通过rsem方法(版本1.2.31)通过使用hcd137ki小鼠(参考实施例6-3中描述)从同系肿瘤移植小鼠模型的rna-seq数据来计算。参考mrna列表(基因列表)是grcm38。mc38用作细胞系。有4组:赋形剂对照、a551-mb110/b379-ml0r施用组、抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)施用组、a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组。
[1340]
通过将每单位fpkm的表达水平加1,将单位从[fpkm]转换为[fpkm+1]。这是因为当表达值存在0时无法进行log转换,因此添加了微小(minute)的数值。之后,执行log2转换。
[1341]
接下来,将人类直系同源物(ortholog)分配给小鼠基因。原则上,它们是根据ncbi homologene数据集分配的。然而,尽管ncbi homologene尚未进行直系同源分配,但截至2019年9月已在ncbi基因网页上进行直系同源分配的人cxcl9和小鼠cxcl9以及人gzmb和小鼠gzmb被分别视为直系同源物。接下来,从肿瘤免疫相关文献中收集了一组肿瘤免疫相关基因(包括cd3d、cd8a等在内的所有54个基因)。然后,从54个基因中选出51个基因(其不包括无小鼠直系同源物的基因)进行检查。
[1342]
接下来,从获自rna-seq的grcm38基因列表(mrna列表)中,只选择了上述肿瘤免疫相关基因组中的基因。由于rna-seq是小鼠数据,并且肿瘤免疫相关基因组是人类基因组,所以通过直系同源物转换获得小鼠基因组。接下来,使用编程语言r程序绘制热图。在这里,热图是标准化的,因此所有样本的平均值为0,每个基因的方差为1。每个基因的平均表达水平的变化通过渐变显示(图12)。
[1343]
(6-3)抗cd137抗体作为单药或与抗pd-l1抗体组合的肿瘤内作用评估(在肿瘤组
织中cd8表达和pd-l1表达)
[1344]
(6-3-1)细胞系和同系肿瘤移植小鼠模型的制备,以及评价肿瘤内作用的方法
[1345]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到约100mm3时认为模型建立。模型建立后,对移植mc38细胞系的小鼠进行分组,然后以表19所示的剂量,施用a551-mb110/b379-ml0r和抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)。a551-mb110/b379-ml0r在移植后14天通过尾静脉途径施用一次。通过腹膜内途径在移植后14天进行一次抗小鼠pd-l1抗体施用。含有0.05%吐温20的pbs用于赋形剂对照。
[1346]
以肿瘤组织中cd8表达和pd-l1表达的增加为指标分析肿瘤内作用的评估。通过免疫组织化学染色评估cd8表达和pd-l1表达。在这些评估中,当肿瘤组织的cd8表达水平或pd-l1表达水平在a551-mb110/b379-ml0r单药组、抗小鼠pd-l1抗体单药组或a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中高于赋形剂对照组,或在组合组中高于各单药施用组时,则判断cd8
+
细胞数或pd-l1表达细胞数增加。
[1347]
[表19]
[1348][1349]
(6-3-2)从mc38细胞系移植的小鼠中切除肿瘤组织并制备肿瘤组织样品
[1350]
将切除的肿瘤组织浸入10%中性缓冲福尔马林溶液中1天。然后将经过石蜡包埋的肿瘤组织切片,然后进行免疫组织化学染色。
[1351]
(6-3-3)来自mc38细胞系移植小鼠的肿瘤组织样品的免疫组织化学染色和cd8
+
细胞和pd-l1
+
细胞浸润到肿瘤组织的评估
[1352]
抗cd8α抗体(cell signaling technology,克隆d4w2z)和optiview dab试剂盒(ventana medical systems)用于cd8的免疫组织化学染色。抗兔hq抗体和hrp标记的抗hq抗体用作检测二抗和检测三抗。多克隆抗pd-l1抗体(r&d)和ultraview dab试剂盒(ventana medical systems)用于pd-l1的免疫组织化学染色。hrp标记的抗山羊抗体用作检测二抗。benchmark xt自动染色仪(ventana medical systems)用于染色。
[1353]
cd8的免疫组织化学染色结果见图13,pd-l1的免疫组织化学染色结果见图14。在a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中,与赋形剂对照组和各单药施用组相比,观察到肿瘤组织中增加的cd8表达和pd-l1表达。此外,在a551-mb110/b379-ml0r单药施用组和抗小鼠pd-l1抗体单药施用组中,与赋形剂对照施用组相比,肿瘤组织中cd8表达和pd-l1表达增加。
[1354]
此外,使用用于明场显微镜的病理学扫描仪系统(aperio scanscope cs2玻片扫
描仪,leica biosystems)和20倍物镜捕获免疫组织化学染色标本的所有组织的高分辨率数字图像。对于肿瘤中cd8或pd-l1的免疫组织化学染色阳性细胞的测量,分别使用halo图像分析软件(indica labs,v2.3)中的分析算法“immune cell v1.3”或“membrane v1.7”。每个组织中的肿瘤区域由病理学家手动注释并评估。每个阳性细胞的数量由每个肿瘤面积的数量(mm2)表示。目视检查数字图像分析的阳性阈值质量(图82、83和84)。
[1355]
以上结果显示,a551-mb110/b379-ml0r和抗小鼠pd-l1抗体的单药施用增加了肿瘤组织中的cd8
+
细胞和pd-l1
+
细胞。此外,显示了相比于各单药的施用,a551-mb110/b379-ml0r和抗小鼠pd-l1抗体的组合施用进一步增加了肿瘤组织中cd8
+
细胞和pd-l1
+
细胞的数量。由于cd8
+
细胞针对癌细胞具有细胞毒活性,因此认为当肿瘤组织中的cd8
+
细胞数量增加时,会表现出更强的抗肿瘤作用。在这里,pd-l1表达是由肿瘤免疫相关基因例如ifn-γ诱导的(见图12),并且pd-l1
+
细胞具有抑制异常激活的免疫反应的作用。如上所述,肿瘤免疫相关基因显示在a551-mb110/b379-ml0r施用组中升高(实施例6-2,图12)。因此,认为在a551-mb110/b379-ml0r与抗小鼠pd-l1抗体的组合组中,由于抗小鼠pd-l1抗体抑制了pd-l1的作用,从而获得了更强的抗肿瘤作用。认为这些事件有助于实施例6-1所示的组合施用的强功效。
[1356]
(6-4)抗cd137抗体作为单药或与抗pd-l1抗体组合的肝脏和肿瘤内作用的评估
[1357]
(6-4-1)细胞系和同系肿瘤移植小鼠模型的制备,以及评价肝脏作用和肿瘤内作用的方法
[1358]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到约111-200mm3时认为模型建立。模型建立后,对移植mc38细胞系的小鼠进行分组,然后以表20所示的剂量,施用a551-mb110/b379-ml0r和抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)。a551-mb110/b379-ml0r在移植后11天和14天通过尾静脉途径施用两次。抗小鼠pd-l1抗体在移植后11天和14天通过腹膜内途径施用两次。含有0.05%吐温20的pbs用于赋形剂对照。
[1359]
使用第一次施用后4天收集的血液评估肝脏作用。将所得血液离心并分离血浆。通过以下详述的方法评估血浆中各种标志物的测量值。在这些各项指标的评估中,当显示肝功能障碍的指标在a551-mb110/b379-ml0r单药组、抗小鼠pd-l1抗体单药组或a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中高于赋形剂对照组时,则评估肝功能受损。
[1360]
为了评价肿瘤内反应,在初次施用4天后,通过以下详述的方法取出肿瘤组织,并测定淋巴细胞级分中的细胞数。在本次评估中,当肿瘤组织中cd8
+
细胞数在a551-mb110/b379-ml0r单药组、抗小鼠pd-l1抗体单药组或a551-mb110/b379-ml0r和抗-小鼠pd-l1抗体组合组中高于赋形剂对照组时,则评价促进了肿瘤组织中cd8
+ t细胞的增殖。
[1361]
[表20]
[1362][1363]
(6-4-2)通过测试mc38细胞系移植小鼠的血液评估肝功能标志物值
[1364]
通过样品测试系统tba-120fr(佳能医疗系统)测量采血中的肝功能标志物。
[1365]
作为通过血液测试的肝功能标志物测量的结果,相比于赋形剂施用组,在a551-mb110/b379-ml0r单药组和抗小鼠pd-l1抗体单药施用组和a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中均未观察到ast和alt值的变化(图15)。
[1366]
综上所述,a551-mb110/b379-ml0r和抗小鼠pd-l1抗体均未损伤肝功能。
[1367]
(6-4-3)从mc38细胞系移植小鼠中切除肿瘤组织并制备淋巴细胞级分
[1368]
对于切除的肿瘤组织,测量淋巴细胞级分中的细胞数。通过使用小鼠肿瘤解离试剂盒(miltenyi biotec)获得的淋巴细胞级分用于测量淋巴细胞级分中的细胞数。
[1369]
(6-4-4)源自mc38细胞系移植小鼠的淋巴细胞级分的评价
[1370]
作为使用fcm测量淋巴细胞级分中细胞数的结果,相比于赋形剂施用组,a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组观察到肿瘤组织中cd8
+ t细胞的数量增加(图16)。
[1371]
综上所述,a551-mb110/b379-ml0r与抗小鼠pd-l1抗体的联用促进了肿瘤内cd8
+ t细胞的增殖。
[1372]
实施例7:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(llc1/ova/gpc3克隆c5细胞)的抗cd137抗体作为单药或与抗pd-l1抗体组合的抗肿瘤活性评估
[1373]
在该研究中,使用了内部建立的小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞(如参考实施例9-4-1所述)和hcd137 ki小鼠(如参考实施例6-3中所述)。将llc1/ova/gpc3克隆c5细胞系皮下移植到小鼠,当肿瘤体积达到148-495mm3时将小鼠分组。移植后11天进行分组。如下表21所示,在移植后11天和14天将赋形剂对照和a551-mb110/b379-ml0r施用于小鼠的尾静脉。此外,如下表21所示,在移植后11天和14天向小鼠腹膜内施用赋形剂对照和抗小鼠pd-l1抗体(bioxcell,克隆:10f.9g2)。含有0.05%吐温20的pbs用作赋形剂对照。
[1374]
[表21]
[1375][1376]
在移植后11天、14天、17天、20天、25天、28天、31天和35天测量肿瘤体积。通过以下公式计算肿瘤体积(tv)。
[1377]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1378]
结果,移植后35天a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组的平均肿瘤体积为782mm3,但a551-mb110/b379-ml0r单药组的平均肿瘤体积为1812mm3(表22)。因此,a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组显示出比a551-mb110/b379-ml0r单药组或抗小鼠pd-l1抗体单药组更强的肿瘤生长抑制作用。特别是,尽管抗小鼠pd-l1抗体单药组与赋形剂对照相比几乎没有肿瘤生长抑制作用,但a551-mb110/b379-ml0r和抗-小鼠pd-l1抗体组合组中有高肿瘤生长抑制作用(图17)。因此,这表明a551-mb110/b379-ml0r和免疫检查点抑制剂的联合使用对于使用免疫检查点抑制剂(如pd1和/或pd-l1抑制剂)治疗效果不佳的癌症类型是有效的。
[1379]
[表22]
[1380][1381]
实施例8-1:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(c1498细胞)的抗cd137抗体作为单药或与抗pd-l1抗体组合的抗肿瘤活性评估
[1382]
在本研究中,使用了小鼠aml(急性髓细胞性白血病)细胞系c1498细胞(atcc,item号:tib-49)和hcd137 ki小鼠(参考实施例6-3中所述)。将c1498细胞系皮下移植到小鼠,当肿瘤体积达到173-381mm3时将小鼠分组。移植后8天进行分组。如下表23所示,在移植后8天和12天将赋形剂对照、a375-migg1/b167-ml0r抗体和抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)施用到小鼠的尾静脉中。含有0.05%吐温20的pbs用作赋形剂对照。
[1383]
[表23]
[1384][1385]
在移植后8天、10天、12天和15天测量肿瘤体积(tv)。
[1386]
通过以下公式计算肿瘤体积。
[1387]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1388]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1389]
tv变化(mm3)=测量时的肿瘤体积-分组时的肿瘤体积
[1390]
tgi(%)=(1-(每组tv变化的平均值/赋形剂对照组tv变化的平均值))
×
100
[1391]
结果,针对c1498细胞,与a375-migg1/b167-ml0r单药组或抗小鼠pd-l1抗体单药组相比,a375-migg1/b167-ml0r和抗小鼠pd-l1抗体组合组观察到肿瘤生长抑制作用增强。具体来说,a375-migg1/b167-ml0r单药组的肿瘤生长抑制率为62%,而a375-migg1/b167-ml0r与抗小鼠pd-l1抗体组合组的肿瘤生长抑制率为82%(图18,表24)。
[1392]
[表24]
[1393][1394]
实施例8-2:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(c1498细胞)评价单药转换抗cd137抗体或转换抗cd137抗体和抗tigit抗体的组合的抗肿瘤活性
[1395]
在本研究中,使用了小鼠aml(急性髓细胞性白血病)细胞系c1498细胞(atcc item号:tib-49)和hcd137 ki小鼠(参考实施例6-3中所述)。将c1498细胞系皮下移植到小鼠右腹部,移植后7天进行分组。肿瘤体积约为270至546mm3的个体用于分组。移植后7天,将赋形剂和a551-mb110/b379-ml0r抗体施用于小鼠的尾静脉。赋形剂和抗tigit抗体(克隆:1g9;目录号:be0274;bioxcell)在移植后7天、9天、11天、13天、15天和18天腹膜内施用于小鼠,如下表所示。含有0.05%吐温-20的pbs用作赋形剂。
[1396]
[表86]
[1397][1398]
在移植后7天、9天、11天、13天、15天、17天、19天、22天、25天、27天、29天和32天测量肿瘤体积。当肿瘤体积超过体重的10%时,根据内部安乐死标准对个体实施安乐死,将1000mm3的肿瘤体积转换为1g。对于每组,在所有个体都活着时计算平均肿瘤体积。
[1399]
通过以下公式计算肿瘤体积。
[1400]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1401]
结果,对于单药转换抗cd137抗体a551-mb110/b379-ml0r以及转换抗cd137抗体a551-mb110/b379-ml0r和抗tigit抗体的组合均观察到肿瘤生长抑制作用。
[1402]
移植22天后,转换抗cd137抗体a551-mb110/b379-ml0r单药施用组的平均肿瘤体
积为1588mm3,并且转换抗cd137抗体a551-mb110/b379-ml0r和抗tigit抗体联合施用组的平均肿瘤体积为734mm3。与转换抗cd137抗体单药施用组相比,在用转换抗cd137抗体和抗tigit抗体的组合施用的组中肿瘤生长抑制效果趋于更强(图105)。
[1403]
实施例9:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(ae17细胞)的抗cd137抗体作为单药或与抗pd-l1抗体组合的抗肿瘤活性评估
[1404]
在本研究中,使用了小鼠恶性间皮瘤ae17细胞(ds pharma biomedical)和hcd137 ki小鼠(参考实施例6-3中所述)。将体内传代的ae17肿瘤皮下移植到小鼠体内,当肿瘤体积达到70-306mm3时进行分组。移植后9天进行分组。如下表25所示,在移植后9天和12天将赋形剂对照、a375-migg1/b167-ml0r和抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)施用到小鼠的尾静脉中。含有0.05%吐温20的pbs用作赋形剂对照。
[1405]
[表25]
[1406][1407]
在移植后9天、12天、15天和19天测量肿瘤体积。
[1408]
通过以下公式计算肿瘤体积(tv)。
[1409]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1410]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1411]
tv变化(mm3)=测量时的肿瘤体积-分组时的肿瘤体积
[1412]
tgi(%)=(1-(每组tv变化的平均值/赋形剂对照组tv变化的平均值))
×
100
[1413]
结果,针对ae17细胞,与a375-migg1/b167-ml0r单药组或抗小鼠pd-l1抗体单药组相比,a375-migg1/b167-ml0r和抗小鼠pd-l1抗体组合组观察到肿瘤生长抑制作用增强。具体来说,a375-migg1/b167-ml0r单药组的肿瘤生长抑制率为39%,而a375-migg1/b167-ml0r与抗小鼠pd-l1抗体组合组的肿瘤生长抑制率为60%(图19,表26)。
[1414]
[表26]
[1415][1416]
实施例10:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(llc1/hgpc3细胞)评估抗cd137抗体作为单药或与抗hgpc3-mcd抗体的组合
[1417]
(10-1)细胞系和同系肿瘤移植小鼠模型的制备,以及a551-mb110/b379-ml0r(单药或组合)的抗肿瘤活性的评估
[1418]
在本研究中,使用了内部建立的小鼠肺癌细胞系llc1/hgpc3细胞(science translational medicine 2017年10月4日,第9卷,第410期,eaal4291)和hcd137ki小鼠(参考实施例6-3中所述)。将llc1/hgpc3细胞系皮下移植到小鼠腹部,当肿瘤体积达到约287mm3时将小鼠分组。移植后11天进行分组。如下表27所示,移植后11天,将赋形剂对照、
a551-mb110/b379-ml0r抗体和抗hgpc3-mcd3抗体(与人gpc3和小鼠cd3结合的双特异性抗体)施用至小鼠尾静脉中。含有0.05%吐温20的pbs用作赋形剂对照。
[1419]
[表27]
[1420][1421]
在移植后11天、14天、17天和21天测量肿瘤体积(tv)。
[1422]
通过以下公式计算肿瘤体积。
[1423]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1424]
结果如图20所示。在移植后21天,赋形剂对照组的平均肿瘤体积为2393mm3。抗hgpc3-mcd3抗体单药组、a551-mb110/b379-ml0r单药组、和抗hgpc3-mcd3抗体和a551-mb110/b379-ml0r组合组的平均肿瘤体积分别为1592mm3,1340mm3和35mm3。与赋形剂对照组相比,a551-mb110/b379-ml0r单药组和抗hgpc3-mcd3抗体单药组均显示出较低的平均肿瘤体积。此外,与a551-mb110/b379-ml0r单药组和抗hgpc3-mcd3抗体单药组相比,抗hgpc3-mcd3抗体和a551-mb110/b379-ml0r组合组的平均肿瘤体积显著减少。
[1425]
由以上可知,抗hgpc3-mcd3抗体和a551-mb110/b379-ml0r的联用协同增强了对llc1/hgpc3荷癌人cd137敲入小鼠的抗肿瘤作用。
[1426]
(10-2)细胞系和同系肿瘤移植小鼠模型的制备,以及评价瘤内反应的方法
[1427]
在本研究中,使用了内部建立的小鼠肺癌细胞系llc1/hgpc3细胞(science translational medicine 2017年10月4日,第9卷,第410期,eaal4291)和hcd137ki小鼠(参考实施例6-3中所述)。将llc1/hgpc3细胞系皮下移植到小鼠腹部,当肿瘤体积达到约230mm3时将小鼠分组。移植后10天进行分组。如下表28所示,移植后10天,将赋形剂对照、a551-mb110/b379-ml0r抗体和抗hgpc3-mcd3抗体(与人gpc3和小鼠cd3结合的双特异性抗体)施用至小鼠尾静脉中。含有0.05%吐温20的pbs用作赋形剂对照。
[1428]
[表28]
[1429][1430]
用于上述分组的肿瘤体积通过下式计算。
[1431]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1432]
移植后13天收集肿瘤。将收集的肿瘤浸入rna-later(qiagen)中并储存。使用rneasy mini试剂盒(qiagen)从肿瘤样品中提取总rna。使用ncounter pancancer mouse immune profiling panel(nanostring technologies)和ncounter digital analyzer(nanostring technologies)测量总rna的基因表达水平。
[1433]
使用nsolver(nanostring technologies)和microsoft excel 2013(微软公司)分析所测量的基因表达水平。在测量其表达水平的基因中,绘制了与t细胞的细胞毒活性相关的cd3e,cd8b1,gzmb,prf1,ifng的表达水平(图21)。与赋形剂对照组相比,a551-mb110/b379-ml0r和抗hgpc3-mcd3抗体组合组显示出cd3e、cd8b1、gzmb和prf1基因的升高的表达水平(dunnett检验,*p《0.05,**p《0.01,***p《0.001))。与赋形剂组相比,a551-mb110/b379-ml0r和抗hgpc3-mcd3抗体组合组的表达水平即使对于ifng也有增加的趋势。与a551-mb110/b379-ml0r单药组和抗hgpc3-mcd3抗体单药组相比,a551-mb110/b379-ml0r和抗hgpc3-mcd3抗体组合组的表达水平对于所有基因有升高趋势。此外,与赋形剂相比,每个单药组中细胞毒活性相关基因的表达水平趋于增加。
[1434]
由上可知,在本研究的条件下,a551-mb110/b379-ml0r和抗hgpc3-mcd3抗体的联合使用对llc1/hgpc3荷癌人cd137敲入小鼠诱导了强烈的瘤内反应。
[1435]
实施例11:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(乳腺癌细胞系)的抗cd137抗体的抗肿瘤活性评估
[1436]
在这项研究中,使用了普遍可得或可建立的乳腺癌细胞系和hcd137ki(敲入)小鼠。将乳腺癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。然后将抗cd137抗体和赋形剂施用于小鼠。
[1437]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对乳腺癌细胞系具有抗肿瘤活性。
[1438]
实施例12:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(乳腺癌细胞系)评估抗cd137抗体单药或与抗pd-l1抗体的组合疗法
[1439]
在这项研究中,使用了普遍可得或可建立的乳腺癌细胞系和hcd137ki小鼠。将乳腺癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。然后,将抗cd137抗体单药、抗pd-l1抗体单药、抗cd137抗体和抗pd-l1抗体组合或赋形剂施用至小鼠。
[1440]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对乳腺癌细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗pd-l1抗体联合施用组显示出比任何单药施用组更高的肿瘤生长抑制率时,可以评价通过联合使用存在肿瘤生长抑制作用的协同或相加增强。
[1441]
实施例13:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(乳腺癌细胞系)评估抗cd137抗体单药或与抗pd-l1抗体和/或抗tigit抗体的组合疗法
[1442]
在这项研究中,使用了普遍可得或可建立的乳腺癌细胞系和hcd137ki小鼠。将乳腺癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。之后,将(1)抗cd137抗体单药,(2)抗pd-l1抗体单药,(3)抗cd137抗体和抗pd-l1抗体二药组合,(4)抗cd137抗体和抗tigit抗体二药组合,(5)抗cd137抗体、抗pd-l1抗体和抗tigit抗体三药组合,或(6)赋形剂施用至小鼠。
[1443]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对乳腺癌细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗pd-l1抗体二药组合施用组,或抗cd137抗体和抗tigit抗体二药组合施用组与它们的单药施用组相比肿瘤生长抑制率更高时,则可以评价通过联合使用存在肿瘤生长抑制效果的协同或相加增强。此外,如果抗cd137抗体、抗pd-l1抗体和抗tigit抗体的三
药组合组显示出比上述单药组或二药组合组更高的肿瘤生长抑制率,则可以评价通过三药组合存在肿瘤生长抑制作用的协同或相加的增强。
[1444]
实施例14:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(肺癌细胞系)评估抗cd137抗体单药或与抗pd-l1抗体和/或抗tigit抗体的组合疗法
[1445]
在这项研究中,使用了普遍可得或可建立的肺癌细胞系和hcd137 ki小鼠。将肺癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。之后,将(1)抗cd137抗体单药,(2)抗pd-l1抗体单药,(3)抗cd137抗体和抗pd-l1抗体二药组合,(4)抗cd137抗体和抗tigit抗体二药组合,(5)抗cd137抗体、抗pd-l1抗体和抗tigit抗体三药组合,或(6)赋形剂施用至小鼠。
[1446]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对肺癌细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗pd-l1抗体二药组合施用组,或抗cd137抗体和抗tigit抗体二药组合施用组与这些单药施用组相比肿瘤生长抑制率更高时,则可以评价通过联合使用存在肿瘤生长抑制效果的协同或相加增强。此外,如果抗cd137抗体、抗pd-l1抗体和抗tigit抗体的三药组合组显示出比上述单药组或二药组合组更高的肿瘤生长抑制率,则可以评价通过三药组合存在肿瘤生长抑制作用的协同或相加的增强。
[1447]
实施例15:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(黑色素瘤细胞系)评估抗cd137抗体单药或与抗pd-l1抗体和/或抗tigit抗体的组合疗法
[1448]
在这项研究中,使用了普遍可得或可建立的黑色素瘤细胞系和hcd137 ki小鼠。将黑色素瘤细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。之后,将(1)抗cd137抗体单药,(2)抗pd-l1抗体单药,(3)抗cd137抗体和抗pd-l1抗体二药组合,(4)抗cd137抗体和抗tigit抗体二药组合,(5)抗cd137抗体、抗pd-l1抗体和抗tigit抗体三药组合,或(6)赋形剂施用至小鼠。
[1449]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对黑色素瘤细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗pd-l1抗体二药组合施用组,或抗cd137抗体和抗tigit抗体二药组合施用组与这些单药施用组相比肿瘤生长抑制率更高时,则可以评价通过联合使用存在肿瘤生长抑制效果的协同或相加增强。此外,如果抗cd137抗体、抗pd-l1抗体和抗tigit抗体的三药组合组显示出比上述单药组或二药组合组更高的肿瘤生长抑制率,则可以评价通过三药组合存在肿瘤生长抑制作用的协同或相加的增强。
[1450]
实施例16:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(结肠直肠癌细胞系)评估抗cd137抗体单药或与抗tigit抗体的组合疗法
[1451]
在这项研究中,使用了普遍可得或可建立的结肠直肠癌细胞系和hcd137 ki小鼠。将结肠直肠癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。然后,将抗cd137抗体单药,抗tigit抗体单药,抗cd137抗体和抗tigit抗体组合中的任一种以及赋形剂施用于小鼠。
[1452]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对结肠直肠癌细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗tigit抗体联合施用组相比于任何单药施用组显示出更高的肿瘤生
长抑制率时,则可以评价通过联合使用存在肿瘤生长抑制作用的协同或相加增强。
[1453]
实施例17:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(jak1敲除癌细胞系)评估抗cd137抗体单药或与抗pd-l1抗体和/或抗tigit抗体的组合疗法
[1454]
在这项研究中,使用了普遍可得或可建立的jak1敲除癌细胞系和hcd137 ki小鼠。将jak1敲除癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。之后,将(1)抗cd137抗体单药,(2)抗pd-l1抗体单药,(3)抗cd137抗体和抗pd-l1抗体二药组合,(4)抗cd137抗体和抗tigit抗体二药组合,(5)抗cd137抗体、抗pd-l1抗体和抗tigit抗体三药组合,或(6)赋形剂施用至小鼠。
[1455]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对jak1敲除癌细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗pd-l1抗体二药组合施用组,或抗cd137抗体和抗tigit抗体二药组合施用组与这些单药施用组相比显示出更高的肿瘤生长抑制率时,则可以评价通过联合使用存在肿瘤生长抑制效果的协同或相加增强。此外,如果抗cd137抗体、抗pd-l1抗体和抗tigit抗体的三药组合组显示出比上述单药组合组或二药组合组更高的肿瘤生长抑制率,则可以评价通过三药组合存在肿瘤生长抑制作用的协同或相加的增强。
[1456]
实施例18-1:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(b2m敲除癌细胞系)评估抗cd137抗体单药或与抗pd-l1抗体和/或抗tigit抗体的组合疗法
[1457]
在这项研究中,使用了普遍可得或可建立的b2m敲除癌细胞系和hcd137 ki小鼠。将b2m敲除癌细胞系移植到小鼠体内,当肿瘤体积达到一定水平时进行分组。之后,将(1)抗cd137抗体单药,(2)抗pd-l1抗体单药,(3)抗cd137抗体和抗pd-l1抗体二药组合,(4)抗cd137抗体和抗tigit抗体二药组合,(5)抗cd137抗体、抗pd-l1抗体和抗tigit抗体三药组合,或(6)赋形剂施用至小鼠。
[1458]
移植后多次测量肿瘤体积。当抗cd137抗体施用组与赋形剂施用组相比显示出更高的肿瘤生长抑制率时,可以评价抗cd137抗体对b2m敲除癌细胞系具有抗肿瘤活性。此外,当抗cd137抗体和抗pd-l1抗体二药组合施用组,或抗cd137抗体和抗tigit抗体二药组合施用组与这些单药施用组相比显示出更高的肿瘤生长抑制率时,则可以评价通过联合使用存在肿瘤生长抑制作用的协同或相加增强。此外,如果抗cd137抗体、抗pd-l1抗体和抗tigit抗体的三药组合组显示出比上述单药组合组或二药组合组更高的肿瘤生长抑制率,则可以评价通过三药组合存在肿瘤生长抑制作用的协同或相加的增强。
[1459]
实施例18-2:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型的转换抗cd137抗体的抗肿瘤活性评估
[1460]
(18-2-1)肿瘤细胞系和同系肿瘤移植小鼠模型的制备,以及评价抗肿瘤活性的方法
[1461]
已知具有β2微球蛋白(b2m)基因突变(b2m突变)的肿瘤对抗pd-1抗体、抗pd-l1抗体等的治疗具有抗性。(sharma p.,等,cell.168,(9),707-232017;和zaretsky jm.等人,n engl j med.375(9):819-29.2016)。
[1462]
在该研究中,使用了内部建立的具有β2微球蛋白(b2m)基因敲除的小鼠结肠癌细胞系mc38-hgpc3#g64b2m ko克隆5细胞和hcd137 ki小鼠(参考实施例6-3中所述)。将mc38-hgpc3#g64b2m ko克隆5细胞系皮下移植到小鼠右腹部,移植后14天进行分组。具有111至
228mm3肿瘤体积的个体用于分组。在移植后14天和21天,将转换抗cd137抗体a551-mb110/b379-ml0r施用到小鼠的尾静脉中。含有0.05%吐温-20的pbs用作赋形剂。
[1463]
[表87]
[1464][1465]
在移植后14天、17天、21天、24天、27天和31天测量肿瘤体积。
[1466]
通过以下公式计算肿瘤体积。
[1467]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1468]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1469]
tv变化(mm3)=测量时的肿瘤体积-分组时的肿瘤体积
[1470]
tgi(%)=(1-(每组tv变化的平均值/赋形剂组tv变化的平均值))
×
100
[1471]
结果,与对照相比,转换抗cd137抗体a551-mb110/b379-ml0r在肿瘤移植后的整个期间对mc38-hgpc3#g64b2m ko克隆5细胞显示出肿瘤生长抑制作用,并显示出在肿瘤移植后31天,肿瘤生长抑制率为29%(图106)。
[1472]
本发明的cd137转换抗体显示出对已知对抗pd-1抗体、抗pd-l1抗体等的治疗具有抗性的具有b2m突变的肿瘤具有极其显著的抗肿瘤活性。
[1473]
实施例19:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(mc38细胞)的抗cd137抗体作为单药或与抗pd-l1抗体组合的抗肿瘤活性评估
[1474]
(19-1)肿瘤细胞系和同系肿瘤移植小鼠模型的制备,以及a551-mb110/b379-ml0r和ureh-mb110/urel-mk1(单药或与抗小鼠pd-l1抗体的组合)的抗肿瘤活性的评估
[1475]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到106-200mm3时认为模型建立。模型建立后,对mc38细胞系移植的小鼠进行分组,然后以表77所示的剂量,施用转换抗体a551-mb110/b379-ml0r或非转换抗体ureh-mb110/urel-mk1(阳性对照),和/或抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)。在移植后11天和14天,通过尾静脉途径施用转换抗体a551-mb110/b379-ml0r或非转换抗体ureh-mb110/urel-mk1两次。抗小鼠pd-l1抗体在移植后11天和14天通过腹膜内途径施用两次。含有0.05%吐温20的pbs用于赋形剂对照。
[1476]
用作阳性对照的非转换抗体ureh-mb110/urel-mk1是具有已知抗cd137抗体urelumab(cas注册号:934823-49-1)的可变区作为可变区和在wo2014030750中描述的mb110(seq id no:145)作为重链恒定区以及小鼠κ链mk1(与小鼠κ链mk0(seq id no:147)相同的氨基酸序列)作为轻链恒定区的非转换cd137抗体。
[1477]
[表77]
[1478][1479]
在移植后10天、14天、18天、22天、25天、29天和32天测量肿瘤体积和体重。
[1480]
通过以下公式计算肿瘤体积(tv)。
[1481]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1482]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1483]
tv变化(mm3)=移植后32天的肿瘤体积-分组时的肿瘤体积
[1484]
tgi(%)=(1-(每组tv变化的平均值/赋形剂对照组tv变化的平均值))
×
100
[1485]
结果,针对mc38细胞,转换抗体a551-mb110/b379-ml0r单药施用组,转换抗体a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组,以及非转换抗体ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组较赋形剂组表现出显著的肿瘤生长抑制作用,并且肿瘤生长抑制率分别为78%、109%和81%(图85,表78)。因此,显示了转换抗体a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组具有与非转换抗体ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组相同或更高的抗肿瘤作用。
[1486]
[表78]
[1487]
移植后32天的肿瘤生长抑制
[1488][1489]
实施例20:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型的抗cd137抗体作为单药或与抗pd-l1抗体组合的全身作用评估
[1490]
(20-1)肿瘤细胞系和同系肿瘤移植小鼠模型的制备,以及评价瘤内作用的方法
[1491]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到约200mm3时认为模型建立。模型建立后,对mc38细胞系移植的小鼠进行分组,然后以表79所示的剂量,施用转换抗体a551-mb110/b379-ml0r和抗小鼠pd-l1抗体(bioxcell,克隆10f.9g2)。作为阳性对照物质,施用非转换抗cd137抗体ureh-mb110/urel-mk1(上)和抗小鼠pd-l1抗体。
[1492]
在移植后15天和18天,从尾静脉途径施用转换抗体a551-mb110/b379-ml0r或非转换抗体ureh-mb110/urel-mk1两次。抗小鼠pd-l1抗体在移植后15天和18天通过腹膜内途径施用两次。含有0.05%吐温20的pbs用于赋形剂对照。
[1493]
(20-2)从mc38细胞系移植小鼠切除脾脏,肿瘤区域淋巴结(dln)和肝脏,淋巴细胞级分制备和外周血取样
[1494]
从下腔静脉采集外周血用于采血。使用切除的脾脏、肿瘤区域淋巴结和肝脏进行淋巴细胞级分分离。对于切除的脾脏和肿瘤区域淋巴结,在进行淋巴细胞级分分离之前测量器官重量。对于脾脏和肿瘤区域淋巴结,使用在组织破坏后通过使用细胞过滤器获得的淋巴细胞级分。对于肝脏,使用通过使用肝脏解离试剂盒,小鼠(miltenyi biotec)然后使用细胞过滤器进行组织破坏而获得的淋巴细胞级分。通过血细胞分析仪分析获得的外周血,通过流式细胞仪(fcm)分析获得的脾脏、肿瘤区域淋巴结和肝脏来源的淋巴细胞级分。
[1495]
[表79]
[1496][1497]
(20-3)通过mc38细胞系移植小鼠的血液测试评估血液参数值
[1498]
对于样品血液,使用样品测试系统xt-2000iv(sysmex corp.)测量血液参数。
[1499]
血液测试的血液参数测量显示a551-mb110/b379-ml0r单药组的白细胞浓度、血小板浓度和淋巴细胞浓度没有变化。在抗小鼠pd-l1抗体单药组中,观察到白细胞浓度和淋巴细胞浓度有轻微波动,而在a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中,观察到与抗小鼠pd-l1抗体单剂组相似的白细胞浓度和淋巴细胞浓度的轻微波动(图86)。
[1500]
另一方面,在ureh-mb110/urel-mk1单药组中,观察到白细胞浓度和淋巴细胞浓度显著降低(图86)。此外,在ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组中,除了白细胞浓度和淋巴细胞浓度显著降低外,还观察到血小板浓度降低(图86)。
[1501]
综上所述,与ureh-mb110/urel-mk1相比,a551-mb110/b379-ml0r即使与抗小鼠pd-l1抗体联合使用也不会引起血液参数的波动,并且其对外周血的作用极其有限。
[1502]
(20-4)使用mc38细胞系移植小鼠通过器官重量测量和流式细胞术(fcm)分析评估免疫细胞活化
[1503]
脾脏和肿瘤区域淋巴结(dln)的器官重量评估显示在a551-mb110/b379-ml0r单药组、抗小鼠pd-l1抗体单药组和a551-mb110/b379-ml0r和抗小鼠pd-l1组合组中各器官重量没有增加(图87)。
[1504]
另一方面,在ureh-mb110/urel-mk1单药组中,观察到各器官的器官重量增加。此外,在ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组中,与ureh-mb110/urel-mk1单药组相比,观察到每个器官的器官重量更为显著的增加(图87)。
[1505]
接下来,使用fcm分析源自脾脏、肿瘤区域淋巴结和肝脏的t细胞的活化。在fcm评估免疫细胞活化时,使用cd8
+ t细胞中活化标志物的表达率、cd4
+ t细胞中foxp3
+
调节性t细胞的增加率和cd45
+
细胞中foxp3
+
调节性t细胞的增加率。klrg-1、icos、pd-1和lag-3被用作cd8
+ t细胞中的活化标志物。fcm分析中,使用抗cd45抗体(bd biosciences)、抗cd3抗体(biolegend)、抗cd8抗体(biolegend)、抗cd4抗体(biolegend)、抗klrg-1抗体(bd biosciences)、抗-icos抗体(biolegend)、抗pd-1抗体(biolegend)、抗lag-3抗体(bd biosciences)和抗foxp3抗体(bd biosciences)。bd lsr fortessa x-20(bd biosciences)用于测量。
[1506]
脾脏评估结果显示,与ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组相比,在a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中,cd8
+ t细胞中klrg-1、icos、pd-1、lag-3的表达率,cd45
+
细胞中各活化标志物阳性cd8
+ t细胞的比率,以及cd4
+ t细胞中foxp3
+
调节性t细胞的比率和cd45
+
细胞中foxp3
+
调节性t细胞的比率没有显著增加(图88和89)。
[1507]
肿瘤区域淋巴结评估结果显示,与ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组相比,在a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中,cd8
+ t细胞中klrg-1、icos、pd-1、lag-3的表达率和绝对数量,以及cd4
+ t细胞中foxp3
+
调节性t细胞的比率和绝对数量没有显著增加(图90和91)。
[1508]
肝脏评估结果显示,与ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组相比,在a551-mb110/b379-ml0r和抗小鼠pd-l1抗体组合组中,cd8
+ t细胞中klrg-1、icos、pd-1、lag-3的表达率,cd45
+
细胞中各活化标志物阳性cd8
+ t细胞的比率,以及cd4
+ t细胞中foxp3
+
调节性t细胞的比率和cd45
+
细胞中foxp3
+
调节性t细胞的比率没有显著增加(图92和93)。
[1509]
基于上述,即使转换抗体a551-mb110/b379-ml0r显示出与非转换抗体ureh-mb110/urel-mk1相当的肿瘤生长抑制效果,即使当与抗小鼠pd-l1抗体组合使用时,其对正常器官诸如外周血、脾脏、肿瘤区域淋巴结、和肝脏中免疫细胞的作用极为有限。
[1510]
实施例21:抗cd137抗体的组织分布评估
[1511]
(21-1)肿瘤细胞系和同系肿瘤移植小鼠模型的制备,以及评价抗体组织分布的方法
[1512]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到约200mm3时认为模型建立。模型建立后,对mc38细胞系移植小鼠进行分组,然后以表80所示的剂量施用alexa488标记的a551-mb110/b379-ml0r。作为阴性对照物质,施用alexa488标记的ic17hdk-mb110/ic17l-mk。作为阳性对照物质,施用非转换抗cd137抗体alexa488标记的ureh-mb110/urel-mk1。对于每种抗体的alexa488标记,使用alexa fluor 488抗体标记试剂盒(thermo fisher scientific)。在移植后14天,通过尾静脉途径施用alexa488标记的ic17hdk-mb110/ic17l-mk或alexa488标记的a551-mb110/b379-ml0r或alexa488标记的ureh-mb110/urel-mk1一次。
[1513]
(21-2)从mc38细胞系移植小鼠中切除肿瘤、脾脏和肝脏并制备淋巴细胞级分
[1514]
对切除的肿瘤、脾脏和肝脏进行淋巴细胞级分分离。对于脾脏,使用在组织破坏后
通过细胞过滤器获得的淋巴细胞级分。对于肿瘤或肝脏,使用通过使用肿瘤解离试剂盒,小鼠(miltenyi biotec)或肝脏解离试剂盒,小鼠(miltenyi biotec)然后使用细胞过滤器进行组织破坏而获得的淋巴细胞级分。对获得的肿瘤、肝脏和脾脏来源的淋巴细胞级分进行流式细胞术(fcm)分析。
[1515]
[表80]
[1516][1517]
(21-3)通过mc38细胞系移植小鼠的流式细胞术(fcm)分析来评价抗体组织分布
[1518]
使用fcm对与肿瘤、脾脏和肝脏来源的淋巴细胞级分结合的每种alexa488标记的抗体进行分析。alexa488在cd8
+ t细胞中的表达率用于通过fcm评估。抗cd45抗体(bd biosciences)、抗cd3抗体(biolegend)、抗cd8抗体(biolegend)、抗cd19抗体(biolegend)和抗cd11b抗体(biolegend)用于fcm分析。bd lsr fortessa x-20(bd biosciences)用于测量。
[1519]
作为评估与浸润肿瘤的cd8
+ t细胞结合的每种alexa488标记抗体的结果,相比于alexa488标记的ic17hdk-mb110/ic17l-mk施用组,在alexa488标记的a551-mb110/b379-ml0r施用组或alexa488标记的ureh-mb110/urel-mk1施用组中观察到高结合率(图94)。在脾脏和肝脏中,转换抗体alexa488标记的a551-mb110/b379-ml0r施用组的cd8
+ t细胞结合率几乎与阴性对照物质alexa488标记的ic17hdk-mb110/ic17l-mk施用组相当(图94)。
[1520]
另一方面,在alexa488标记的ureh-mb110/urel-mk1施用组中(它是一种非转换抗体),与alexa488标记的ic17hdk-mb110/ic17l-mk施用组和alexa488标记的a551-mb110/b379-ml0r施用组相比,cd8
+ t细胞结合率非常高(图94)。
[1521]
由以上可知,转换抗体a551-mb110/b379-ml0r仅与存在于肿瘤组织中的淋巴细胞结合,并且与存在于正常器官、脾脏和肝脏中的淋巴细胞的结合是有限的。
[1522]
实施例22:验证一组显示与肿瘤组织中细胞外atp相关的表达变化的基因
[1523]
(22-1)基于同系肿瘤移植小鼠模型的rna-seq数据,绘制显示与细胞外atp相关的表达变化的基因热图
[1524]
从通过将mc38细胞系、llc/ova/hgpc3细胞系、llc/ova细胞系或hepa1-6/hgpc3细胞系移植到c57bl/6小鼠中制备的每个同系肿瘤移植小鼠模型获得的rna-seq数据,通过rsem方法(版本1.2.31)计算表达值(单位:fpkm)。参考mrna列表(基因列表)为grcm38。此外,表达值通过rsem方法由从c57bl/6小鼠的每个正常组织获得的rna-seq数据类似地计算。对于12种正常器官的rna-seq原始数据(.fastq文件),使用了发表在文献中的数据(sollner,sci data,2017,4:170185)。
[1525]
通过将fpkm单位中的基因表达水平加1,将单位从[fpkm]转换为[fpkm+1]。这是因为当表达值存在0时无法进行log转换,因此添加了微小(minute)的数值。之后,执行log2转换。
[1526]
接下来,将人类直系同源物(ortholog)分配给小鼠基因。原则上,它们是根据ncbi homologene数据集分配的。
[1527]
接下来,从文献中收集与细胞外atp相关的基因(hu,clin cancer res,2019,25(4),1318-1330;li,cancer discov,2019,9(12),1754-1773;yang.,cancer sci,2019,110(8),2456-2470;gombault,front immunol,2013,3:414)。
[1528]
此外,从文献(yang,cancer sci,2019,110(8),2456-2470)(emt:上皮间质转化)中收集通过添加atp其表达增加的emt相关基因组。
[1529]
接下来,从获自rna-seq的grcm38基因列表(mrna列表)中,只选择了上述atp相关基因组和emt相关基因组中的基因。由于rna-seq是小鼠数据,并且atp相关基因组和emt相关基因组是人类基因组,所以将其通过直系同源物转换获得小鼠基因组。接下来,通过t检验选择在每个癌细胞系中表达显著高于正常组织组(p《0.05)的基因。
[1530]
接下来,使用编程语言r程序绘制热图。在这里,热图是标准化的,因此所有样本的平均值为0,每个基因的方差为1。每个基因的平均表达水平的变化通过渐变显示(图95)。
[1531]
结果表明,与12种正常器官相比,在肿瘤组织中,atp相关基因组和emt相关基因组中存在多个显著高表达的基因。为此,认为a551-mb110/b379-ml0r仅与肿瘤组织中的免疫细胞结合,而不与肝和脾等正常组织中的免疫细胞结合(实施例21)。此外,认为在atp的存在下与抗原结合的转换抗体仅在肿瘤组织中诱导强烈的免疫反应(实施例20),而在正常器官如肝、脾、肿瘤区域淋巴结和外周血中不引发免疫反应(实施例20)。
[1532]
实施例23:通过流式细胞术(fcm)分析来评估cd73和cd39在各种癌细胞中的表达
[1533]
(23-1)各种癌细胞系中cd73表达的评价
[1534]
本研究中,使用了购自atcc的小鼠急性髓细胞性白血病细胞系c1498细胞(实施例3所述)和小鼠白血病细胞系e.g7-ova细胞(实施例2所述);美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞(在实施例6中描述);和小鼠肝癌细胞系hepa1-6/hgpc3细胞(如实施例4所述),小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞(如参考例9-4-1所述),和内部建立的小鼠肺癌细胞系llc1/ova克隆17细胞。
[1535]
小鼠肺癌细胞系llc1/ova克隆17细胞通过将鸡卵清蛋白(ova)表达质粒引入小鼠肺癌来源的细胞系llc1(ll/2(也称为llc1),经销商:atcc,目录号:crl-1642)而制备。抗cd73抗体(bio legend)在每个细胞系中用于fcm分析。facs lyric(bd biosciences)用于测量。
[1536]
作为评价各细胞系中cd73的膜表面表达的结果,在c1498细胞和e.g7-ova细胞的细胞膜上几乎没有观察到cd73的表达,而在mc38细胞,hepa1-6/hgpc3细胞、llc1/ova/gpc3克隆c5细胞和llc1/ova克隆17细胞的细胞膜上观察到了cd73的表达(图96)。已知cd73是一种膜型酶,可将amp分解为腺苷。因此,即使mc38细胞、hepa1-6/hgpc3细胞、llc1/ova/gpc3克隆c5细胞和llc1/ova克隆17细胞具有将amp(其是转换抗体与抗原结合所需的)分解为腺苷的特性,但转换抗体能够展示出抗肿瘤作用(实施例1至10),这表明转换抗体对肿瘤组织发挥作用而不受cd73表达的影响。
[1537]
(23-2)来自llc1/ova/gpc3克隆c5细胞系移植小鼠的肿瘤组织中cd39和cd73表达的评价
[1538]
(23-2-1)细胞系和同系肿瘤移植小鼠模型的制备,以及评估肿瘤内浸润免疫细胞
和肿瘤细胞cd39和cd73表达的方法
[1539]
在该研究中,使用了内部建立的小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞和hcd137 ki小鼠(如参考实施例6-3中所述)。将llc1/ova/gpc3克隆c5细胞系皮下移植到小鼠腹部,当肿瘤体积达到约500mm3或更大时取样。移植后14天进行取样。取样后,取出肿瘤组织,并通过下文详述的方法制备肿瘤细胞级分或淋巴细胞级分,进一步,cd39或cd73在肿瘤细胞,cd4
+ t细胞,cd8
+ t细胞,和非t细胞级分上的表达使用流式细胞术(fcm)评估。
[1540]
(23-2-2)从llc1/ova/gpc3克隆c5细胞系移植小鼠中切除肿瘤组织并制备肿瘤细胞级分或淋巴细胞级分
[1541]
对于切除的肿瘤组织,进行肿瘤细胞级分或淋巴细胞级分的细胞制备。将肿瘤解离试剂盒,小鼠(miltenyi biotec)用于细胞制备,并将获得的肿瘤细胞级分或淋巴细胞级分用于fcm分析。
[1542]
(23-2-3)通过fcm评估来自llc1/ova/gpc3克隆c5细胞系移植小鼠的肿瘤细胞级分或淋巴细胞级分中的cd39和cd73表达
[1543]
为了通过fcm进行评估,使用了cd39和cd73在肿瘤细胞、cd4
+ t细胞、cd8
+ t细胞和非t细胞级分上的阳性率。为此,在fcm分析中,使用了抗cd45抗体(bd biosciences)、抗cd3抗体(biolegend)、抗cd8抗体(biolegend)、抗cd4抗体(biolegend)、抗cd39抗体(biolegend)和抗cd73抗体(biolegend)。bd lsr fortessa x-20(bd biosciences)用于测量。
[1544]
作为分析每个级分中cd39表达的结果,肿瘤细胞、cd4
+ t细胞、cd8
+ t细胞和非t细胞上的cd39表达是这样的,在一些肿瘤细胞中并且在几乎所有的cd4
+ t细胞、cd8
+ t细胞和非t细胞中均观察到表达(图97)。接下来,作为分析每个级分中cd73表达的结果,在一些肿瘤细胞、一些cd8
+ t细胞和一些非t细胞中观察到了表达,而在几乎所有的cd4
+
t细胞中都观察到了表达(图97)。每个数据的代表性示例如图98所示。
[1545]
(23-3)来自mc38细胞系移植小鼠的肿瘤组织中cd39和cd73表达的评价
[1546]
(23-3-1)细胞系和同系肿瘤移植小鼠模型的制备,以及评估肿瘤内浸润免疫细胞和肿瘤细胞cd39和cd73表达的方法
[1547]
在本研究中,使用了美国国家癌症研究所许可的小鼠结肠癌细胞系mc38细胞和hcd137ki小鼠(参考实施例6-3中所述)。将mc38细胞系皮下移植到小鼠腹部,当肿瘤体积达到163-204mm3时将小鼠分组。移植后14天进行分组,并且移植后16天进行取样。通过以下详细描述的方法去除肿瘤组织以制备肿瘤细胞级分或淋巴细胞级分,并且进一步使用流式细胞术(fcm),评估cd39或cd73在肿瘤细胞、cd4
+ t细胞、cd8
+ t细胞上和非t细胞级分上的表达。
[1548]
(23-3-2)从mc38细胞系移植小鼠中切除肿瘤组织并制备肿瘤细胞级分或淋巴细胞级分
[1549]
对于切除的肿瘤组织,进行肿瘤细胞级分或淋巴细胞级分的细胞制备。将肿瘤解离试剂盒,小鼠(miltenyi biotec)用于细胞制备,并将获得的肿瘤细胞级分或淋巴细胞级分用于fcm分析。
[1550]
(23-3-3)通过fcm评估来自mc38细胞系移植小鼠的肿瘤细胞级分或淋巴细胞级分的cd39和cd73表达
[1551]
为了通过fcm进行评估,使用了cd39和cd73在肿瘤细胞、cd4
+ t细胞、cd8
+ t细胞和非t细胞级分上的阳性率。为此,在fcm分析中,使用了抗cd45抗体(bd biosciences)、抗cd3抗体(biolegend)、抗cd8抗体(biolegend)、抗cd4抗体(biolegend)、抗cd39抗体(biolegend)和抗cd73抗体(biolegend)。bd lsr fortessa x-20(bd biosciences)用于测量。
[1552]
作为分析每个级分中cd39表达的结果,肿瘤细胞、cd4
+ t细胞、cd8
+ t细胞和非t细胞上的cd39表达是这样的,在一些cd4
+ t细胞和一些cd8
+ t细胞以及在大多数非t细胞中均观察到表达(图99)。随后,作为分析每个级分中cd73表达的结果,在一些肿瘤细胞中并且在几乎所有cd4
+ t细胞和cd8
+ t细胞中都观察到了表达(图99)。在非t细胞中几乎没有观察到表达。每个数据的代表性示例如图100所示。
[1553]
基于上述结果,表明在来自用小鼠结肠癌细胞系mc38细胞和小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞移植的小鼠的肿瘤组织中,除了肿瘤细胞之外,cd39和cd73在肿瘤内浸润免疫细胞中广泛表达。已知膜型酶cd39和cd73是将atp分解为腺苷的酶。转换抗体在atp、adp和amp存在下显示抗原结合能力,但在腺苷存在下不显示(参见wo2020/032230)。然而,正如已证明,即使在cd39和cd73广泛表达的肿瘤组织中,例如来自用小鼠结肠癌细胞系mc38细胞和小鼠肺癌细胞系llc1/ova/gpc3克隆c5细胞移植的小鼠的肿瘤组织中,转换抗体与免疫细胞结合(实施例21)并表现出抗肿瘤作用(实施例1-10),显示了转换抗体可作用于肿瘤组织,而不受cd39和cd73表达的影响。
[1554]
实施例24:通过使用hcd137ki小鼠的同系肿瘤移植模型(llc1/ova克隆17细胞的皮下移植),评估抗cd137抗体作为单药或与抗pd-l1抗体组合的抗肿瘤活性
[1555]
(24-1)肿瘤细胞系和同系肿瘤移植小鼠模型的制备,以及a551-mb110/b379-ml0r(单药或与抗小鼠pd-l1抗体的组合)的抗肿瘤活性的评估
[1556]
在本研究中,使用了内部建立的小鼠肺癌细胞系llc1/ova克隆17细胞(如实施例23所述,本实施例中以下简称llc1/ova细胞系)和hcd137 ki小鼠(如参考实施例6-3所述)。将llc1/ova细胞系皮下移植到小鼠腹部,当肿瘤体积达到79-199mm3时认为模型建立。模型建立后,对llc1/ova细胞系移植的小鼠进行分组,然后以表81所示的剂量,施用转换抗体a551-mb110/b379-ml0r和抗小鼠pd-l1抗体(bioxcell,inc.,克隆10f.9g2)。作为阳性对照物质,施用非转换抗体ureh-mb110/urel-mk1和抗小鼠pd-l1抗体。在移植后10天和13天,通过尾静脉途径施用转换抗体a551-mb110/b379-ml0r或非转换抗体ureh-mb110/urel-mk1两次。抗小鼠pd-l1抗体的施用在移植后10天和13天通过腹膜内途径进行两次。含有0.05%吐温20的pbs用于赋形剂对照。
[1557]
[表81]
[1558][1559]
在移植后10天、13天、17天和20天测量肿瘤体积。
[1560]
通过以下公式计算肿瘤体积(tv)。
[1561]
肿瘤体积(mm3)=长(mm)x宽(mm)x宽(mm)/2
[1562]
根据以下公式计算肿瘤生长抑制(tgi(%))。
[1563]
tv变化(mm3)=移植后20天的肿瘤体积-分组时的肿瘤体积
[1564]
tgi(%)=(1-(每组tv变化的平均值/赋形剂对照组tv变化的平均值))
×
100
[1565]
结果,针对llc1/ova肿瘤,转换抗体a551-mb110/b379-ml0和抗小鼠pd-l1抗体组合组,非转换抗体ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组,以及转换抗体a551-mb110/b379-ml0r单药组表现出几乎相同的肿瘤生长抑制作用。
[1566]
具体而言,转换抗体a551-mb110/b379-ml0和抗小鼠pd-l1抗体组合组的肿瘤生长抑制率为95%,而非转换抗体ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组表现出93%的肿瘤生长抑制率,并且转换抗体a551-mb110/b379-ml0r单药组表现出101%的肿瘤生长抑制率(图101,表82)。
[1567]
由以上结果显示,转换抗体a551-mb110/b379-ml0和抗小鼠pd-l1抗体组合组具有与非转换抗体ureh-mb110/urel-mk1和抗小鼠pd-l1抗体组合组相似的肿瘤生长抑制作用(图101,表82)。
[1568]
[表82]
[1569]
移植后20天的肿瘤生长抑制(%)
[1570][1571]
实施例25:通过使用hcd137ki小鼠的同系肿瘤细胞移植模型(llc1/ova细胞)的抗cd137抗体作为单药或与抗pd-l1抗体组合的全身作用评估
[1572]
(25-1)肿瘤细胞系和同系肿瘤移植小鼠模型的制备,以及评价瘤内作用的方法
[1573]
在该研究中,使用了内部建立的小鼠肺癌细胞系llc1/ova细胞(如实施例23所述)和hcd137 ki小鼠(如参考实施例6-3中所述)。将llc1/ova细胞系皮下移植到小鼠腹部,当肿瘤体积达到91-205mm3时认为模型建立。模型建立后,对llc1/ova细胞系移植的小鼠进行分组,然后以表83所示的剂量,施用转换抗体a551-mb110/b379-ml0r和抗小鼠pd-l1抗体(bioxcell,inc.,克隆10f.9g2)。
ml0r抗体施用于小鼠的尾静脉。含有0.05%吐温20的pbs用作赋形剂对照。肿瘤移植后18天测量体重,在放血和麻醉下安乐死之后测量肺重量。在同一天通过同样方法对10只未进行细胞移植的正常小鼠进行取样。肺重量计算为每100克体重的肺重量值。
[1586]
[表84]
[1587][1588]
结果,与赋形剂施用组相比,转换抗体a551-mb110/b379-ml0r施用组具有显著抑制的肺重量(图104,表85)。因此,显示转换抗体a551-mb110/b379-ml0r不仅对皮下移植的肿瘤(如实施例24所述)具有药效,而且对肺的微转移也具有药效。赋形剂施用组中的一只小鼠在肿瘤移植后11天死亡。在死亡小鼠的肺部发现了表明肿瘤的小痕迹和肿块。
[1589]
[表85]
[1590]
移植后18天的肺重量
[1591][1592]
参考实施例1:抗原制备
[1593]
(1-1)人cd137细胞外区域的制备
[1594]
用本领域技术人员已知的方法制备人cd137胞外域(也称为hcd137)。具体地,在编码人cd137的细胞外区域的基因片段的下游,连接编码组氨酸标签的基因片段和编码添加有生物素的特定序列(avitag序列,seq id no:86)的基因片段。将编码其中连接人cd137的细胞外区域、组氨酸标签和avitag的蛋白质(人cd137或hcd137-hisbap,seq id no:87)的基因片段掺入动物细胞表达载体中。使用293-fectin(invitrogen)将构建的质粒载体转染到freestyle293细胞(invitrogen)中。此时,同时转染包含表达ebna1(seq id no:88)的基因的质粒载体。将按照上述步骤转染了基因的细胞在37℃,8%co2下培养;然后将感兴趣的蛋白质(人cd137细胞外区域)分泌到培养物上清液中。通过0.22μm的过滤器过滤该细胞培养基以获得培养物上清液。
[1595]
将培养物上清液施加到histrap-hp(ge医疗)上,并将人cd137细胞外区域与柱结合。使用20mm磷酸钠、500mm氯化钠和500mm咪唑(ph 7.5)的溶液洗脱人cd137细胞外区域。然后通过使用superdex 200 26/600(ge医疗)的凝胶过滤色谱法除去聚集体,以产生纯化的人cd137细胞外区域。
[1596]
人cd137的浓度使用pace等的方法,基于排除从seq id no:87推断的信号序列的氨基酸序列(seq id no:183)计算(pace,c.n.等,蛋白质科学(protein science),1995;4;2411-2423)。
[1597]
(1-2)人cd137胞外域的制备(hcd137(fxa消化的))
[1598]
人cd137胞外域(也称为hcd137(fxa消化的))以本领域技术人员已知的方法制备。具体地,将编码因子xa可切割序列的基因片段和编码抗体的恒定区的基因片段连接在编码
人cd137的细胞外区域的基因片段的下游。将编码其中连接人cd137的细胞外区域、因子xa可切割序列和抗体恒定区的蛋白质(hcd137-f-fc,seq id no:89)的基因片段掺入动物细胞表达载体中。使用293-fectin(invitrogen)将构建的质粒载体转染到freestyle293细胞(invitrogen)中。此时,同时转染含有ebna1(seq id no:88)编码基因的质粒载体。将根据上述步骤转染有基因的细胞在37℃,8%co2下培养;hcd137-f-fc被分泌到培养物上清液中。通过0.22μm的过滤器过滤细胞培养基,并收集培养物上清液。
[1599]
将培养物上清液施加到装有蛋白质a的柱子上(mabselect sure,ge医疗)。将hcd137-f-fc结合到柱上,并用50mm乙酸溶液洗脱。用1m tris-hcl,ph 8.0中和洗脱液后,将hcd137-f-fc的溶剂用20mm tris、100mm氯化钠、2mm氯化钙(ph 8.0)替代。接下来,添加因子xa蛋白酶(new england biolabs,目录号p8010l),并消化hcd137-f-fc。然后加入蛋白酶抑制剂(dns-ggack,calbiochem,目录号251700)以终止反应。将5m氯化钠添加至蛋白酶反应溶液中,并将所制备的溶液的总体积施加至hitrap苄脒(ge医疗,目录号17-5143-01)。将该柱过滤后的溶液进一步应用于蛋白质a柱(mabselect sure,ge医疗),并收集通过级分。通过凝胶过滤色谱法使用superdex 200increase,10/30(ge医疗,目录号28990944)除去通过级分的聚集物,得到纯化的人cd137细胞外区域。
[1600]
(1-3)生物素化的fc融合人cd137的制备
[1601]
通过本领域技术人员已知的方法,制备生物素化的fc融合人cd137(也称为“生物素化的hcd137-fc”或“bio-hcd137-fc”或hcd137-fc-bio)。具体地,将编码抗体恒定区的基因片段和编码添加有生物素的特定序列(avitag序列,seq id no:86)的基因片段连接到编码人cd137的细胞外区域的基因片段的下游。将其中已连接有编码人cd137胞外区域、抗体恒定区和avitag的蛋白质(fc融合的人cd137,seq id no:90)的基因片段掺入到动物表达载体中。使用293-fectin(invitrogen)将构建的质粒载体转染到freestyle293细胞(invitrogen)中。此时,同时转染表达ebna1(seq id no:88)的基因和表达生物素连接酶(bira,seq id no:91)的基因,并添加生物素以使fc融合的人cd137生物素化。将按照上述步骤转染了基因的细胞在37℃,8%co2下培养;然后将目标蛋白质(生物素化的fc融合人cd137)分泌到培养物上清液中。通过0.22μm的过滤器过滤细胞培养物以获得培养物上清液。
[1602]
将培养物上清液施加到装有蛋白质a的柱子(mabselect sure,ge医疗)上,并将生物素化的fc融合人cd137结合到该柱子上。使用50mm乙酸溶液洗脱生物素化的fc融合人cd137。然后通过用superdex 200,26/600(ge医疗)进行凝胶过滤色谱除去聚集体,并获得纯化的生物素化的fc融合人cd137。
[1603]
(1-4)fc融合人cd137的制备
[1604]
通过本领域技术人员已知的方法制备fc融合的人cd137(也称为hcd137-fc)。具体地,将编码抗体恒定区的基因片段和编码添加有生物素的特定序列(avitag序列,seq id no:86)的基因片段连接到编码人cd137的细胞外区域的基因片段的下游。将编码其中已连接有人cd137的细胞外区域、抗体恒定区和avitag的蛋白质(fc融合的人cd137,seq id no:90)的基因片段掺入到动物表达载体中。使用293-fectin(invitrogen)将构建的质粒载体转染到freestyle293f细胞(invitrogen)中。此时,同时转染表达ebna1(seq id no:88)的基因。将按照上述步骤转染了基因的细胞在37℃,8%的co2中培养,并将目标蛋白(fc融合
的人cd137)分泌到培养物上清液中。通过0.22μm的过滤器过滤细胞培养物以获得培养物上清液。
[1605]
将培养物上清液施加到装有蛋白质a的柱子(mabselect sure,ge医疗)上,并将fc融合的人cd137结合到柱子上。使用50mm乙酸溶液洗脱fc融合的人cd137。接下来,通过用superdex 200、26/600(ge医疗)进行凝胶过滤色谱除去聚集体,从而获得纯化的fc融合人cd137。
[1606]
(1-5)生物素化的fc融合猴cd137的制备
[1607]
通过本领域技术人员已知的方法制备生物素化的fc融合猴cd137(也称为“cycd137-fc-bap”)。具体地,将编码抗体恒定区的基因片段和编码添加了生物素的特定序列(avitag序列,seq id no:86)的基因片段连接到编码猴cd137的细胞外区域的基因片段的下游。将编码其中已连接有猴cd137细胞外区域、抗体恒定区和avitag的蛋白质(fc融合猴cd137,seq id no:92)的基因片段掺入到动物表达载体中。
[1608]
使用293-fectin(invitrogen)将构建的质粒载体转染到freestyle293细胞(invitrogen)中。此时,同时转染表达ebna1(seq id no:88)的基因和表达生物素连接酶(bira,seq id no:91)的基因;并且添加生物素以用生物素标记fc融合的猴cd137。将按照上述步骤转染了基因的细胞在37℃,8%co2下培养;然后将目标蛋白质(生物素化的fc融合猴cd137)分泌到培养物上清液中。通过0.22μm的过滤器过滤细胞培养物以获得培养物上清液。
[1609]
将培养物上清液施加到装有蛋白质a的柱子(mabselect sure,ge医疗)上,并将生物素化的fc融合猴cd137结合到柱子上。使用50mm乙酸溶液洗脱生物素化的fc融合猴cd137。然后通过凝胶过滤色谱使用superdex 200递增10/300(ge医疗)除去聚集体,并获得纯化的生物素化的fc融合猴cd137。
[1610]
参考实施例2:获得atp依赖性cd137抗体
[1611]
(2-1)利用atp通过合理设计的文库获得具有小分子依赖性抗原结合活性的抗体(小分子转换抗体)(1)
[1612]
(2-1-1)淘选
[1613]
从先前专利wo2015/083764中构建的合理设计的抗体噬菌体展示文库中获得在三磷酸腺苷(腺苷5
’‑
三磷酸;atp)存在下表现出对抗原的结合活性的抗体。注意,具有小分子依赖性抗原(例如,cd137)结合活性的抗体可以被称为“转换抗体”或“小分子转换抗体”,具有atp依赖性抗原(例如,cd137)结合活性的抗体被称为“转换抗体”或“atp转换抗体”。为了获得,收获了呈递抗体的噬菌体,所述抗体在atp存在下对捕获在珠子上的抗原表现出结合活性。随后,在不存在atp的情况下,从珠子洗脱的洗脱液中收集噬菌体。
[1614]
以常规方法从携带构建的噬菌体展示噬菌粒的大肠杆菌中产生噬菌体。具体地,用m13ko7δpiii(称为“超级噬菌体”)(progen biotechnik)感染携带构建的噬菌粒载体的大肠杆菌,并从在30℃下培养过夜的上清液中收集噬菌体。通过用tris-缓冲盐溶液(tbs)稀释噬菌体群体来获得噬菌体文库溶液,其中所述噬菌体群体是通过向其中进行噬菌体生产的大肠杆菌培养物中加入2.5m nacl/10%peg而沉淀的。然后将bsa以4%的终浓度加入到噬菌体文库溶液中。使用固定在磁珠上的抗原进行淘选。对于磁珠,使用了sera-mag neutravidin珠(赛默飞世尔科技)或dynabeads m-280 streptavidin(美国生命技术公
司)。作为抗原,使用购自jena生物科学的生物素化的三磷酸腺苷(5
’‑
三磷酸腺苷;atp)或hcd137-fc-bio(seq id no:90)或bio-hcd137(seq id no:89),其中所述hcd137-fc-bio(seq id no:90)或bio-hcd137(seq id no:89)是参考实施例1-2和1-3中制备的使用预先测定的无重量的nhs-peo4-生物素(pierce)从hcd137(fxa消化的)进行生物素化的。
[1615]
进行淘选以有效地获得可在癌症组织中发挥转换作用的小分子的依赖性转换抗体。具体地,参照先前专利wo2015/083764中所示的方法,淘选以富集在存在小分子atp的情况下与抗原结合且在不存在atp的情况下不与抗原结合的抗体。在第1轮中,对于所有生物素化的hcd137(bio-hcd137),hcd137-fc-bio和生物素化的atp(bio-atp),使用这样的方法进行淘选:将生物素化的抗原固相固定在磁珠上(称为“珠固相法”),然后加入准备好的噬菌体文库溶液。对于bio-atp,参照上述在先专利wo2015/083764中描述的方法进行淘选以富集可在不存在作为小分子化合物的atp的情况下结合抗原(bio-atp)的抗体。对于hcd137-fc-bio,添加4nmol的未生物素化的人igg1fc区,以去除与fc区结合的抗体。将收获的噬菌体添加到大肠杆菌菌株er2738中,以使大肠杆菌感染噬菌体,然后用超级噬菌体感染收获的大肠杆菌,并从在30℃下培养过夜的上清液中收获噬菌体。
[1616]
从第2轮开始,仅对生物素化的hcd137(bio-hcd137)和hcd137-fc-bio进行淘选,以富集在珠固相方法中在atp存在下与抗原结合且在不存在atp时不与抗原结合的抗体,参考在先专利wo2015/083764中所示的方法。对于两种情况中的hcd137-fc-bio,都添加4nmol的未生物素化的人igg1fc区,以去除与fc区结合的抗体。重复相似的淘选直到第5轮以富集目的抗体序列。
[1617]
(2-1-2)通过噬菌体elisa评估存在和不存在atp时的结合活性
[1618]
使用常规方法(分子生物学方法(methods mol.biol.),(2002)178,133-145)从通过上述方法获得的大肠杆菌的单个菌落中收获含噬菌体的培养物上清液。nucleofast 96(macherey-nagel)用于超滤收获的培养物上清液。通过离心(4,500g,45分钟)nucleofast 96(每孔中已加入100μl培养物上清液)来去除流通物。通过向每个孔中添加100μl h2o并通过离心(4,500g,30分钟)再次洗涤nucleofast 96。最后,添加100μl的tbs,并回收已在室温下静置5分钟的nucleofast 96的孔中的上清液中所包含的噬菌体溶液。
[1619]
通过以下步骤对添加了tbs或atp/tbs的纯化噬菌体进行elisa。将384孔链霉亲和素包被的微孔板(greiner)用10μl tbs包被过夜,该tbs包含参考实施例1中产生的生物素化抗原(bio-hcd137、hcd137-fc-bio和bio-fc)。通过用带有吐温20的tris缓冲盐水溶液(tbst)洗涤板的每个孔来去除未结合至板的生物素化的抗原后,将孔用80μl 2%脱脂牛奶tbs封闭1小时或更长时间。通过tbst洗涤除去2%的脱脂牛奶-tbs,然后通过使每孔加入制备的纯化的噬菌体的板在室温放置1小时,使呈递抗体的噬菌体在不存在和存在atp的情况下与存在于每个孔中的生物素化抗原结合。向用tbst或atp/tbst洗涤的每个孔中,加入用tbs或atp/tbs稀释的hrp缀合的抗m13抗体(ge医疗27-9421-01),并将板孵育1小时。用tbst或atp/tbst洗涤后,通过添加硫酸使添加了tmb单一溶液(zymed)的各孔中的溶液的显色停止,然后通过在450nm下的吸光度来测量显色。
[1620]
结果,鉴定了在存在和不存在atp的情况下对bio-hcd137或hcd137-fc-bio的结合活性改变的几种抗体。
[1621]
使用在第4轮和第5轮淘选后的克隆的噬菌体elisa结果如表29所示。
[1622]
在此,将在atp存在下吸光度为0.2以上并且在抗原存在/不存在下吸光度的s/n比大于2的克隆确定为阳性克隆。此外,在阳性克隆中,在存在/不存在atp的情况下,吸光度s/n高于2的克隆被判断为具有atp依赖性抗原结合活性的克隆(转换克隆)。
[1623]
[表29]
[1624][1625]
(2-1-3)存在/不存在atp时抗原结合活性改变的转换抗体的序列分析
[1626]
根据噬菌体elisa结果,分析了使用特异引物pbad-f,g1seq-r从具有atp依赖性抗原结合活性的克隆(转换克隆)中扩增的基因的核苷酸序列。作为分析的结果,获得了被判断为在atp存在下与人cd137结合而在不存在atp下与人cd137不结合的克隆的核苷酸序列。
[1627]
(2-2)利用atp从合理设计的文库中获得在小分子存在下与抗原结合的抗体(2)
[1628]
(2-2-1)淘选
[1629]
从在现有专利wo2015/083764中构建的合理设计的抗体噬菌体展示文库获得在atp存在下表现出对抗原的结合活性的抗体。为了获得,回收了呈递抗体的噬菌体,所述抗体在atp存在下示出与抗原的结合活性,然后在不存在atp的情况下从珠子洗脱的洗脱液中回收噬菌体。
[1630]
以常规方法从携带构建的噬菌体展示噬菌粒的大肠杆菌中产生噬菌体。具体地,用m13ko7tc(wo2015046554a1)或m13ko7δpiii(超级噬菌体)(progen biotechnik)感染携带构建的噬菌粒载体的大肠杆菌,并从在30℃下培养过夜的上清液中回收噬菌体。通过用tbs稀释噬菌体群体来获得噬菌体文库溶液,其中所述噬菌体群体是通过向其中进行噬菌体生产的大肠杆菌培养物中加入2.5m nacl/10%peg而沉淀的。然后将bsa以4%的终浓度加入到噬菌体文库溶液中。使用固定在磁珠上的抗原进行淘选。将中性抗生物素蛋白包被的珠子(sera-mag速珠(speedbead)中性抗生物素蛋白包被的)、中性抗生物素蛋白珠子(tamagawa seiki)或dynabeads myone streptavidin t1(赛默飞世尔科技)用作磁珠。作为抗原,使用参考实施例1中生产的hcd137-fc-bio或bio-hcd137。
[1631]
进行淘洗以有效获得依赖于可在癌症组织中发挥转换作用的小分子的小分子转换抗体。具体地,参照在先前的专利wo2015/083764中所描述的方法进行淘选以富集在小分子腺苷三磷酸(腺苷5'-三磷酸;atp)存在下结合抗原并且在不存在atp时不与抗原结合的抗体。对于bio-hcd137,进行如下方法:预先将生物素化抗原固相固定在磁珠上后添加制备的噬菌体文库溶液的方法(称为“珠固相法”),以及在预先混合制备的噬菌体文库溶液和生物素化的抗原后添加磁珠的方法(称为“液相法”)。对于hcd137-fc-bio,添加4nmol的未生物素化的人igg1fc区,以除去与fc区结合的抗体,仅在液相法中进行淘选。将收集的噬菌体添加到大肠杆菌菌株er2738中并使其感染大肠杆菌,然后用m13ko7tc(wo2015046554a1)或
m13ko7δpiii(超级噬菌体)(progen biotechnik)感染收集的大肠杆菌,并在30℃培养过夜后从上清液中收集噬菌体。重复类似的淘选,直到第5轮。
[1632]
(2-2-2)通过噬菌体elisa评估存在和不存在atp时的结合活性
[1633]
使用常规方法(分子生物学方法(methods mol.biol.),(2002)178,133-145)从在每一轮后通过上述方法获得的大肠杆菌的单个菌落中收获含噬菌体的培养物上清液。nucleofast 96(macherey-nagel)用于超滤收获的培养物上清液。通过离心(4,500g,45分钟)nucleofast 96(每孔中已加入100μl培养物上清液)去除流通物。通过离心(4,500g,30分钟)再次洗涤其中向每个孔中添加100μl h2o的nucleofast 96。最后,添加100μl的tbs,并回收已在室温下静置5分钟的nucleofast 96孔的上清液中包含的噬菌体溶液。
[1634]
通过以下步骤对添加了tbs或atp/tbs的纯化噬菌体进行elisa。将streptawell 96微量滴定板(roche)与100μl包含参考实施例1中产生的生物素化抗原(hcd137-fc-bio或bio-hcd137)的tbs固定过夜。在通过用tbst洗涤板的每个孔,除去不结合于板的生物素化抗原之后,用250μl的2%脱脂牛奶-tbs封闭孔1小时或更长时间。除去2%的脱脂牛奶-tbs,然后通过使每个孔中添加了制备的纯化的噬菌体的板在37℃下静置1小时,在存在和不存在atp的情况下,使呈递抗体的噬菌体结合至存在于每个孔中的生物素化抗原上。向用tbst或atp/tbst洗涤的每个孔中,加入在tbs或atp/tbs中稀释的hrp缀合的抗m13抗体(ge医疗27-9421-01),并将板孵育1小时。tbst或atp/tbst洗涤后,通过添加硫酸使添加了tmb单一溶液(zymed)的每个孔中的溶液显色停止,然后通过在450nm处的吸光度测量显色。
[1635]
结果,鉴定了在存在和不存在atp的情况下对bio-hcd137或hcd137-fc-bio的结合活性改变的几种抗体。
[1636]
例如,使用第5轮淘选后的克隆的噬菌体elisa结果如表30所示。
[1637]
在此,将在atp存在下吸光度为0.2以上并且在抗原存在/不存在下吸光度的s/n比大于2的克隆确定为阳性克隆。另外,在阳性克隆中,将存在/不存在atp的情况下吸光度的s/n比大于2的那些确定为具有atp依赖性抗原结合活性的克隆(转换克隆)。
[1638]
[表30]
[1639][1640]
(2-2-3)存在/不存在atp时抗原结合活性改变的转换抗体的序列分析
[1641]
使用特异性引物pbad-f、g1seq-r分析了基于噬菌体elisa结果从具有atp依赖性
抗原结合活性的克隆(转换克隆)中扩增的基因的核苷酸序列。作为分析的结果,获得了被判断为在atp存在下与人cd137结合而在不存在atp下与人cd137不结合的克隆的核苷酸序列。
[1642]
(2-3)转换抗体的选择
[1643]
从参考实施例2-1-3和2-2-3的分析结果中,从判断具有atp依赖性抗原结合活性的克隆中选择17个样品,并如表31中所述重新分配克隆名称。
[1644]
[表31]
[1645][1646][1647]
(2-4)存在/不存在atp时抗原结合活性改变的转换抗体的表达和纯化
[1648]
从合理设计的噬菌体文库中获得的编码表31中所述抗体可变区的基因被插入人igg1/λ质粒中,以在动物中表达。使用以下方法表达抗体。通过脂质转染法将制备的质粒导入人胎儿肾细胞衍生的freestyle 293-f(invitrogen)中,该细胞以1.33x106细胞/ml的细胞密度悬浮在freestyle293表达培养基(invitrogen)中,其中3ml接种在6孔板的每个孔中。以本领域技术人员已知的方法,使用rprotein a sepharose
tm fast flow(amersham生物科学)从培养物上清液中纯化抗体,该培养物上清液在co2培养箱(37℃,8%co2,90rpm)中培养四天。使用分光光度计测量纯化的抗体溶液在280nm处的吸光度。从获得的测量值,使用通过pace法(蛋白质科学(protein science)(1995)4,2411-2423)计算的消光系数计算纯化的抗体的浓度。
[1649]
(2-5)通过噬菌体展示法鉴定的抗cd137抗体的评价
[1650]
(2-5-1)依赖于atp及其代谢产物的存在或不存在结合抗原的转换抗体的表达和纯化
[1651]
将编码从人合理设计的噬菌体文库获得的抗体的可变区的基因插入具有重链恒定区(seq id no:93)和轻链恒定区λ链lamlib(seq id no:63)的动物表达质粒中,该重链恒定区与编码修饰的人igg1(p253)下游的gly和lys的基因融合。克隆名称和序列号在表32中列出。
[1652]
评估的克隆
[1653]
[表32]
[1654] 克隆名称重链(全长)seq id no轻链(全长)seq id no1dbbat007-p253941132dbbat013-p253951143dbbat015-p253961154dbbat017-p253971165dbbat019-p253981176dbbat025-p253991187dbbat029-p2531001198dbbat031-p2531001199dbbat037-p25310112010dbbat042-p25310212111dbbat053-p25310312212dbbat056-p25310412313dbbat021-p25310512414dbbat091-p25310612515dbbat112-p25310712616dbbat118-p25310812717dbbat119-p25310912818dbbat121-p25311012919dbbat122-p25311113020dbbat134-p253112131
[1655]
使用本领域技术人员已知的方法表达和纯化抗体。使用分光光度计测量纯化的抗体溶液在280nm处的吸光度。从获得的测量值,使用通过pace法(蛋白质科学(protein science),1995)4,2411-2423)计算的消光系数计算纯化的抗体的浓度。
[1656]
(2-5-2)通过表面等离振子共振评估atp、adp和amp对人cd137结合的影响
[1657]
使用biacore t200(ge医疗)来分析抗cd137抗体与hcd137(fxa消化)之间的抗原抗体反应的相互作用。将抗cd137抗体捕获在传感器芯片cm3(ge医疗)上,其中所述传感器芯片cm3上通过胺偶联方法固定了适量的蛋白质g(calbiochem),并使参考实施例1-2中制备的hcd137(fxa消化)相互作用。对于运行缓冲液,使用20mm aces、150mm nacl、2mm mgcl2、0.05%吐温20(ph 7.4),并使用10mm甘氨酸-hcl(ph 1.5)作为再生溶液。
[1658]
捕获悬浮在tbs中的抗cd137抗体后,以10μl/min的流速将500nm hcd137(fxa消化)注入每个流通池中3分钟。该三分钟的时间段用作hcd137(fxa消化)的结合阶段,在结合阶段结束后,切换到运行缓冲液的两分钟时间段用作hcd137(fxa消化)的解离阶段。解离阶段完成后,将再生溶液以30μl/min的流速注入30秒钟。以上是用于测量抗cd137抗体的结合活性的循环。在结合阶段与抗cd137抗体相互作用的hcd137(fxa消化)的结合量通过捕获的抗体量来调节。使用biacore t200评估软件2.0版本示出每个捕获配体1ru的结合量(ru),并获得抗体捕获量(捕获的抗体量)和抗原结合量的值。抗原的结合量示于表33。因为抗原的结合量反映了结合活性,所以可以说,当存在小分子(atp、adp或amp)时的值高于不存在小分子的值时,识别出对小分子的依赖性。尤其是,差异越大,对小分子的依赖性越高。
[1659]
[表33]
[1660][1661]
(2-5-3)评估对猴cd137抗原的结合活性
[1662]
通过elisa评估获得的抗体与猴cd137的结合。将参考实施例1中制备的cycd137-fc-bap固定在streptawell微量滴定板上。通过用洗涤缓冲液洗涤板的每个孔从板上除去
未结合的抗原后,将孔用150μl封闭缓冲液(含2%bsa的tbs)封闭1小时或更长时间。从每个孔中去除封闭缓冲液,并向每个孔中添加100μl在终浓度为1mm adp的tbs中稀释的纯化抗体或在终浓度为1mm adp的tbs中稀释的纯化抗体。将添加了抗体的板在600rpm下摇动1小时。在用含有终浓度1mm adp的洗涤缓冲液(含0.1%吐温20的tbs)洗涤后,将在终浓度为1mm adp的tbs中稀释的ap缀合的抗人λ抗体(bethyl)添加到每个孔中。孵育一小时并用含终浓度1mm atp的洗涤缓冲液洗涤后,添加bluephos磷酸底物(kpl)。通过600nm处的吸光度测量显色。抗体浓度为0μg/ml时的吸光度增加率示于表34。可以认为吸光度比值具有浓度依赖性增加的样品与猴cd137结合。
[1663]
吸光度比值
[1664]
[表34]
[1665][1666]
(2-5-4)使用jurkat细胞评估cd137激动剂活性
[1667]
gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系(promega)用于测量体外抗体活性。向384孔板的每个孔中,加入10μl以2x106/ml的浓度用测定培养基(99%rpmi,1%fbs)制备的fcγriib cho-k1细胞(promega)。随后,将10μl含有adp的抗体溶液、含有atp的抗体溶液或不含atp或adp的抗体溶液添加至每个孔。然后,将10μl以2x106/ml用测定培养基(99%rpmi,1%fbs)制备的gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系添加至每个孔。adp的终浓度为50μm;并且atp的终浓度为50μm。将板在5%co2培养箱中于37℃放置6小时,然后在室温下放置15分钟,然后将30μl bio-glo试剂添加到每个孔中。bio-glo荧光素酶测定系统(缓冲液和底物)用于bio-glo试剂。随后,用酶标仪测量每个孔的发光。将各孔的发光值除以不添加抗体的孔的发光值,为发光倍数,作为评价各抗体的活性的指标。
[1668]
所得结果示于图22和23中。从图22和23中,证实除ns1-p253(非转换抗体)以外的所有抗体均示出atp和adp依赖性方式的人cd137激动剂活性。
[1669]
(2-6)使用人t细胞淘选获得的转换抗体的体外cd137激动剂活性评估
[1670]
(2-6-1)人t细胞培养物的扩增
[1671]
使用从健康志愿者的血液样本中分离出的人外周血单核细胞。将50ml血液与0.5ml肝素混合,并进一步用50ml pbs稀释。通过以下两个步骤分离出人外周血单核细胞。第一步,将添加有ficoll-paque plus(ge医疗)的leucosep(greiner bio-one)在室温下以
1000x g离心一分钟,然后添加pbs稀释的血液,并在室温下以400x g离心30分钟。第二步,离心后从试管中收集血沉棕黄层,然后用60ml pbs(wako)洗涤。然后,使用t细胞激活/扩增试剂盒/人(macs miltenyi biotec)来扩增t细胞的培养物。
[1672]
(2-6-2)使用人t细胞体外评估cd137激动剂活性
[1673]
将2x104人外周血单核细胞衍生的t细胞和2x104rec-1细胞悬浮在100μl的rpmi1640培养基中,该培养基包含30u/ml人il-2(sigma)、10ng/ml pma(sigma)、0.5μg/ml离子霉素、500μm adpbetas(sigma)和10%fbs(sigma),并接种在具有对照抗体ic17hdk-higg1/ic17l-k0、ns1-p253,或表32中所述的任何克隆的96孔多孔平底板(corning)中,其中对照抗体是具有不依赖于atp的人cd137结合活性的抗体(在整个实施例和参考实施例中称为“非转换抗体”或“非转换cd137抗体”)。将ns1-p253、ic17hdk-higg1/ic17l-k0和表32中描述的克隆在10μg/ml评估。还评估了adpbetas最小培养基中的ifn-γ产生。摇动板,然后在5%co2培养箱中于37℃放置72小时。随后,收获培养物上清液,并使用人ifn-γelisa开发试剂盒(peprotech)定量培养物上清液中所含的ifn-γ的量。根据试剂盒制造商(peprotech)的说明进行elisa。用envision(perkinelmer)进行吸光度测量。
[1674]
结果如图24所示。
[1675]
已确认dbbat007-p253、dbbat013-p253、dbbat015-p253、dbbat019-p253、dbbat021-p253、dbbat025-p253、dbbat031-p253、dbbat042-p253、dbbat056-p253、dbbat118-p253、dbbat121-p253、dbbat122-p253和dbbat119-p253示出了adpbetas依赖性方式的人cd137激动剂活性。adpbetas是adp的类似物,与adp相比,它不易水解。这表明这些人cd137转换抗体可能以依赖于小分子(例如atp、adp或amp)的方式表现出人cd137激动剂活性。
[1676]
(2-6-3)使用人t细胞体外评估cd137激动剂活性(2)
[1677]
将2x104人外周血单核细胞衍生的t细胞和2x104rec-1细胞悬浮在100μl rpmi1640培养基中,该培养基包含30u/ml人il-2(sigma)、10ng/ml pma(sigma)、0.5μg/ml离子霉素、500μm adpbetas(sigma)和10%fbs(sigma),并接种到带有ns1-p253(非转换抗体)或dbbat119-p253的96孔多孔平底板(corning)中。ns1-p253和dbbat119-p253是以10、2、0.4、0.08、0.016、0.0032和0.00064μg/ml进行评估的。摇动板,然后在5%co2培养箱中于37℃放置72小时。随后,收获培养物上清液,并使用人ifn-γelisa开发试剂盒(peprotech)定量培养物上清液中所含的ifn-γ的量。根据试剂盒制造商(peprotech)的说明进行elisa。用envision(perkinelmer)进行吸光度测量。
[1678]
结果示于图25。
[1679]
证实了在adpβs存在下,dbbat119-p253表现出人cd137激动剂活性。这表明dbbat119-p253可能以依赖于小分子(例如atp、adp或amp)的方式表现出人cd137激动剂活性。
[1680]
参考实施例3:使用合理设计的轻链和重链文库,在小分子存在下增强结合抗原的抗体的结合活性
[1681]
(3-1)使用合理设计的轻链文库构建用于增强结合活性的文库
[1682]
对于包含大量在参考实施例2-2-1中收获的具有atp依赖性抗原结合活性的抗体的抗体文库,通过重建抗体轻链文库来增强结合活性。
[1683]
现有专利wo2015/083764中构建的合理设计的抗体噬菌体展示文库的轻链和重链区用于构建抗体轻链文库和抗体重链文库以增强结合活性。将它们引入上述轻链文库或参考实施例2-2-1中收获的噬菌粒载体文库的轻链或重链区,并通过电穿孔引入大肠杆菌菌株er2738。
[1684]
(3-2)使用合理设计的文库增强具有atp依赖性抗原结合活性的抗体的结合活性
[1685]
以常规方法从携带构建的噬菌体展示噬菌粒的大肠杆菌中产生噬菌体。具体地,用m13ko7tc(wo2015/046554)或m13ko7δpiii(超级噬菌体)(progen biotechnik)感染携带构建的噬菌粒载体的大肠杆菌,并从在30℃下培养过夜的上清液中收集噬菌体。通过用tbs稀释噬菌体群体来获得噬菌体文库溶液,其中所述噬菌体群体是通过向其中进行噬菌体生产的大肠杆菌培养物中添加2.5m nacl/10%peg而沉淀的。然后将bsa以4%的终浓度加入到噬菌体文库溶液中。使用固定在磁珠上的抗原进行淘选。将中性抗生物素蛋白包被的珠子(中性抗生物素蛋白包被的sera-mag speedbeads)、中性抗生物素蛋白珠子(tamagawa seiki)或dynabeads myone streptavidin t1(赛默飞世尔科技)用作磁珠。作为抗原,使用生物素化的hcd137-fc。
[1686]
进行淘洗以有效获得依赖于可在癌症组织中发挥转换作用的小分子的小分子转换抗体。具体地,参照在先前的专利wo2015/083764中所描述的方法进行淘选以富集在小分子腺苷三磷酸(腺苷5'-三磷酸;atp)存在下结合抗原并且在不存在atp下不结合抗原的与抗原结合的抗体。
[1687]
(3-3)通过噬菌体elisa评估在存在和不存在atp时的结合活性
[1688]
使用常规方法(分子生物学方法(methods mol.biol.),(2002)178,133-145)从每轮通过上述方法获得的大肠杆菌的单个菌落中收获包含噬菌体的培养物上清液。然后用参考实施例2-2-2中所述的方法通过噬菌体elisa确认在atp存在和不存在下与人cd137的结合活性。
[1689]
结果如图5所示。
[1690]
获得了许多被判断为具有atp依赖性抗原结合活性的克隆,其在存在/不存在抗原的情况下的吸光度s/n比大于2,并且在atp存在/不存在下其吸光度s/n比大于2(转换克隆)。
[1691]
参考实施例4:产生修饰的cd137抗体并评估其活性
[1692]
(4-1)由于dbbat119h-p253/dbbat119l-lamlib的改变而引起的结合活性的增加
[1693]
参考实施例2-4中获得的抗cd137抗体(克隆名称:dbbat119h-p253/dbbat119l-lamlib)的重链可变区dbbat119h和轻链可变区dbbat119l的变体是通过本领域技术人员已知的方法(例如pcr)制备的。对于重链可变区,制备了变体,其中dbdb119h的d10(指第10位的天冬氨酸(asp)(kabat编号))和g17(指第17位的甘氨酸(gly)(kabat编号))分别用甘氨酸(gly)和丝氨酸(ser)代替以产生dbbat119h010;并且dbbat119h010的n99(指第99位(kabat编号)的天冬酰胺(asn))、m100a(第100a位(kabat编号)的蛋氨酸(met))和n100b(第100b位(kabat编号)的天冬酰胺(asn)用其他氨基酸代替。对于轻链可变区,产生变体,其中用酪氨酸(tyr)代替dbbat119l的f87(指在第87位(kabat编号)的苯丙氨酸(phe))以产生dbbat119l010;并且用其他氨基酸替代dbbat119l010的d27b(第27b位(kabat编号)的天冬氨酸(asp))、n31(第31位(kabat编号)的天冬酰胺(asn))和d94(第94位(kabat编号)的天冬
氨酸(asp))。
[1694]
对于重链可变区的变体,通过表面等离振子共振分析仪biacoret200(ge医疗)测量对人cd137的结合活性。通过使纯化的变体与蛋白质g(calbiochem)固定的s系列传感器芯片cm3(ge医疗)相互作用来捕获抗体。然后,在存在atp和不存在atp的情况下,将补充有atp的人cd137(fxa消化的)溶液或不具有atp的人cd137(fxa消化的)溶液进行相互作用,以评估变体对人cd137(fxa消化的)的结合活性。使用20mm aces、150mm nacl、0.05%吐温20和2mm mgcl2(ph 7.4)作为运行缓冲液,在25℃下进行测量。测量结果表明,仅在存在atp的情况下,l100a变体(其中第100a位的蛋氨酸(met)(kabat编号)被亮氨酸(leu)替代的变体)与人cd137的结合活性增强(图27)。l100a变体的重链可变区是dbbatk119h024(seq id no:132)。人cd137的结合量通过每种变体的捕获量(1000ru)来调节。
[1695]
对于轻链可变区的变体,通过biacoret200在与上述相似的条件下测定与人cd137(fxa消化的)的结合活性。测量结果表明,仅在存在atp的情况下,e94变体(其中第94位(kabat编号)的天冬氨酸(asp)被谷氨酸(glu)替代的变体)与人cd137的结合活性增强(图27)。e94变体的轻链可变区是dbbatk119l020(seq id no:133)。
[1696]
将这些重链和轻链变体组合在一起的此类变体缩写为dbbatk119h024-p253/dbbatk119l020-lamlib(重链可变区seq id no:132;轻链可变区seq id no:133;重链恒定区seq id no:93;和轻链恒定区seq id no:63)。
[1697]
根据以下规则指定本说明书中的抗体:(重链可变区)-(重链恒定区)/(轻链可变区)-(轻链恒定区)。
[1698]
例如,抗体名称为dbbat119h-p253/dbbat119l-lamlib,表示抗体的重链可变区为dbbat119h,重链恒定区为p253,轻链可变区为dbbat119l,和轻链恒定区是lamlib。
[1699]
(4-2)使用人t细胞评估修饰的抗人cd137抗体的体外cd137激动剂活性
[1700]
(4-2-1)人t细胞培养物的扩增
[1701]
如参考实施例2-6-1中所述扩增人t细胞并培养。
[1702]
(4-2-2)使用人t细胞评估体外cd137激动剂活性
[1703]
参考实施例2-6-2中所述的方法评估了分别在存在10、2、0.4、0.08和0.016μg/ml的ns1-p253(非转换抗体)、dbbat119h-p253/dbbat119l-lamlib、dbbatk119h024-p253/dbbatk119l020-lamlib或对照抗体ic17hdk-higg1/ic17l-k0的情况下的ifn-γ的产生。还评估了adpbetas最小培养基中的ifn-γ产生。
[1704]
这两个结果如图28所示。
[1705]
修饰的dbbatk119h024-p253/dbbatk119l020-lamlib表现出比dbbat119h-p253/dbbat119l-lamlib更强的adpbetas依赖性激动剂活性。这表明,dbbatk119h024-p253/dbbatk119l020-lamlib可能比dbbat119h-p253/dbbat119l-lamlib表现出更强的atp、adp和amp依赖性人cd137激动剂活性。
[1706]
参考实施例5:cd137抗体的进一步修饰
[1707]
(5-1)通过引入全面的修饰来寻找增加结合活性的修饰
[1708]
为了产生优异的抗cd137抗体,将氨基酸修饰全面引入参考实施例4-1中产生的抗cd137抗体的重链可变区dbbatk119h024和轻链可变区dbbatk119l020。通过本领域技术人员已知的方法,例如pcr,各自制备变体,其中用半胱氨酸以外的全部18个氨基酸代替构成
dbbatk119h024和dbbatk119l020的cdr的所有氨基酸残基中的每一个。使用biacore4000对产生的结合人cd137的大约1200个变体进行了测量。通过使变体的培养物上清液与固定有蛋白g(calbiochem)的s系列传感器芯片cm3(ge医疗)相互作用来捕获抗体。然后,在存在小分子或不存在小分子的情况下,使补充有小分子(atp)的人cd137溶液或不添加小分子的人cd137溶液相互作用,以评估抗体对人cd137的结合活性。使用补充了cacl2的20mm aces、150mm nacl、0.02%吐温20和2mm mgcl2(ph 7.4)的运行缓冲液在25℃下进行测量。
[1709]
(5-2)atp结合增加
[1710]
抗体重链基因a002-p253(seq id no:134)是在具有dbbatk119h024(seq id no:132)作为重链可变区和p253(seq id no:93)作为重链恒定区的dbbatk119h024-p253基因中通过组合参考实施例5-1中发现的修饰(该修饰在小分子存在下增加对人cd137的结合活性)而创建的,所述重链恒定区是通过将s267e/l328f修饰引入到人igg1中,并从人igg1缺失c末端gly和lys而产生的。抗体轻链基因b040-lamlib(seq id no:135)也是在具有dbbatk119l020(seq id no:133)作为轻链可变区和人λ链lamlib(seq id no:63)作为轻链恒定区的抗体轻链dbbatk119l020-lamlib中通过组合参考实施例5-1中发现的修饰(所述修饰在小分子存在下增加对人cd137的结合活性)而创建的。通过本领域技术人员已知的方法将这些基因组合以表达和纯化抗体,以产生目的抗cd137抗体a002-p253/b040-lamlib。a002-p253/b040-lamlib的重链可变区是a002(seq id no:136),轻链可变区是b040(seq id no:137),重链恒定区是p253(seq id no:93),并且轻链恒定区是人λ链lamlib(seq id no:63)。
[1711]
对于本节中生产的a002-p253/b040-lamlib的重链可变区,进行了各种变异,其中kabat编号的第53、54或55位氨基酸被其他氨基酸置换,目的是提高atp结合活性。表35显示了在生成的抗体的重链可变区中a002的氨基酸修饰(kabat编号)。
[1712]
[表35]
[1713]
重链可变区a002的氨基酸改变(kabat编号)a002―a146s54a/n55sa159r53s/n55sa160r53t/n55sa161r53q/n55sa162r53k/n55sa163r53h/n55sa164r53s/n55ta165r53t/n55ta166r53q/n55ta167r53k/n55ta168r53h/n55ta169r53s/n55ha170r53t/n55ha171r53q/n55h
lamlib、a163-p253/b040-lamlib、a164-p253/b040-lamlib、a167-p253/b040-lamlib和a168-p253/b040-lamlib对人cd137的缔合速率常数增加。
[1721]
(5-3)通过引入全面的修饰来增加结合活性
[1722]
为了产生更好的抗cd137抗体,将参考实施例5-1中发现的在存在小分子的情况下增加人cd137结合活性并在不存在小分子的条件下降低与人cd137的结合的修饰,和在参考实施例5-2中发现的增加atp结合活性并增加对于人cd137的缔合速率常数的修饰进行组合,以产生表现出更好特征的抗人cd137抗体。生成了抗体重链基因,其在具有重链可变区a002(seq id no:136)和重链恒定区g1t3(seq id no:138)的抗体重链基因a002-g1t3中组合了参考实施例5-1和5-2中发现的修饰,其中所述重链恒定区是通过将k214r/q419e修饰引入人igg1,并从人igg1缺失c端的gly和lys而产生的。抗体轻链基因是通过将参考实施例5-1中发现的修饰组合在具有轻链可变区b040(seq id no:137)和轻链恒定区人λ链lamlib的抗体轻链b040-lamlib中而产生的。
[1723]
作为比较的对象,生成了以下基因:抗体重链基因20h4.9-p253,其具有us8137667中描述的现有抗cd137抗体的重链可变区20h4.9(seq id no:139)和重链恒定区p253(seq id no:93);和抗体轻链基因,其组合轻链可变区20h4.9lc(seq id no:140)与轻链恒定区人κ链k0(seq id no:141)。作为另一比较对象,产生了具有重链可变区mor-7480.1h(seq id no:142)和重链恒定区p253(seq id no:93)的抗体重链基因mor-7480.1h-p253,其中所述重链可变区mor-7480.1h构成了us8337850中描述的现有抗cd137抗体mor-7480.1;和包含轻链可变区mor-7480.1l(seq id no:143)和轻链恒定区人λ链lam(seq id no:63)的抗体轻链mor-7480.1l-lam(注意:人λ链lamlib和lam都具有相同的氨基酸序列(seq id no:63))。
[1724]
使用本领域技术人员已知的方法,将这些基因组合以表达和纯化抗体,以产生目的抗cd137抗体。表37是产生的抗体的重链可变区、轻链可变区、重链恒定区、轻链恒定区和高变区(超可变区;也称为hvr或cdr)的序列号列表。
[1725]
重链和轻链的氨基酸序列及其高变区(由序列id号指示)
[1726]
[表37]
[1727][1728]
在biacore t200中评估了产生的变体与atp以及与人cd137的结合。使用20mm aces(ph 7.4)、150mm nacl、2mm mgcl2和0.05%吐温20作为运行缓冲液,在37℃下进行人cd137结合的测量。首先,通过将在运行缓冲液中制备的抗体溶液与sure protein a(ge医疗)固定的s系列传感器芯片cm3(ge医疗)相互作用,捕获250-400ru的抗体。然后通过与在补充有所需浓度的atp的运行缓冲液中制备的人cd137溶液或在不带atp的运行缓冲液中制备的人cd137溶液相互作用,评估在存在atp或不存在atp的情况下的人cd137结合活性。对于人cd137抗原,使用参考实施例(1-1)中制备的hcd137-hisbap,并且在0、15.625、62.5、250和1000nm的抗原浓度下进行kd值测量。为了评估结合量,在0和1000nm的抗原浓度下进行测量。使用25mm naoh和10mm甘氨酸-hcl(ph 1.5)再生芯片,并通过重复捕获抗体进行测量。使用biacore t200评估软件2.0计算各种抗体对于人cd137的解离常数。具体地,通过用1:1langmuir结合模型将测量获得的传感图进行整体拟合来计算缔合速率常数ka(l/mol/s)和解离速率常数kd(1/s),以及由这些值算出解离常数kd(mol/l)。
[1729]
表38示出了这些测量的结果。
[1730]
修饰抗体与人cd137的结合分析
[1731]
[表38]
[1732][1733]
上面表38中的“与人cd137的结合”的值表示当在上述每个atp浓度条件下使人cd137以1000nm相互作用时每单位抗体的人cd137的结合量,而“人cd137的kd(m)”表示在每个atp浓度条件下人cd137的解离常数。表中标有*的kd值是通过稳态模型计算得出的。在存在10μm atp的情况下,所有生成的变体的结合量均大于在存在1μm atp的条件下的结合量,
甚至在存在100μm的条件下的结合量更高,这表明它们与人cd137以atp浓度依赖性的方式结合。另一方面,比较对象20h4.9-p253/20h4.9lc-k0和mor-7480.1h-p253/mor-7480.1l-lam没有示出以atp浓度依赖性的方式与人cd137结合。
[1734]
(5-4)使用4-1bb jurkat报告基因测定法评估修饰的抗人cd137抗体的体外atp依赖性cd137激动剂活性
[1735]
gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系(promega,cs196004)用于测量所产生变体的体外活性。向96孔板的每个孔中,加入200μl浓度为5x104/ml的用培养基制备的fcγriib cho-k1细胞(promega),并在5%co2培养箱中于37℃放置过夜。将cho培养基(90%ham氏f12,10%fbs)用作培养基。然后,在吸除所有培养基后,将25μl用测定培养基(99%rpmi,1%fbs)制备的2x106/ml的gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系添加到每个孔中。随后,加入25μl用测定培养基稀释的每种抗体溶液,以使最终浓度为0、0.001、0.01、0.1、1和10μg/ml;最后加入25μl用测定培养基稀释的atp溶液,使最终浓度变为0和250μm。将板在5%co2培养箱中在37℃下静置6小时,在室温下静置15分钟。向每个孔中添加75μl bio-glo试剂。bio-glo荧光素酶测定系统(缓冲液和底物)用于bio-glo试剂。随后,用酶标仪测量每个孔的发光。每个孔的发光值除以不添加抗体的孔的发光值即为相对光单位(倍数诱导),并且用作评估每种抗体的cd137激动剂活性的指标。
[1736]
结果如图29所示。
[1737]
(5-5)使用人外周血单核细胞评估修饰的抗人cd137抗体的体外atp依赖性cd137激动剂活性
[1738]
(5-5-1)人外周血单核细胞的分离
[1739]
如参考实施例2-6-1所述,从申请人公司的健康志愿者的血样中分离出人外周血单核细胞(pbmc)。随后,将细胞在培养基(5%人血清(sigma)、95%aim-v(赛默飞世尔科技))中稀释,细胞密度为5x106/ml。
[1740]
(5-5-2)使用人外周血单核细胞评估cd137激动剂活性
[1741]
将人外周血单核细胞的细胞密度调整为5x106/ml,并以100μl接种到96孔多孔平底板(corning)的每个孔中。随后,添加在培养基中稀释的50μl 0.04μg/ml抗人cd3ε抗体(bd,克隆sp34)和20μg/ml抗人cd28抗体(bd,克隆:cd28.2)。摇动板,然后在37℃的5%co2培养箱中放置6小时。然后,向每个孔中补充25μl 2mm atp(sigma)培养基或无atp的培养基,以及25μl 40μg/ml的每种抗体,振摇培养板,然后将其置于5%co2培养箱中,37℃放置18小时。随后,收获部分培养物上清液,并使用人il-2 duoset elisa试剂盒(r&d系统)或人il-2elisa set(bd生物科学)将培养物上清液用于定量培养物上清液中的il-2含量。收获培养物上清液后,将板再次置于5%co2培养箱中于37℃培养24小时。随后,收获部分培养物上清液,并使用人ifn-γduoset elisa试剂盒(r&d系统)或人ifn-γelisa开发试剂盒(peprotech)对培养物上清液中所含的ifn-γ进行定量。基本上按照试剂盒所附的方案进行elisa。对于人il-2 duoset elisa试剂盒(r&d系统)和人ifn-γduoset elisa试剂盒(r&d系统),根据方案,使用含有h2o2和四甲基联苯胺、1n h2so4(wako)的底物溶液(r&d系统)进行显色和终止显色。对于人il-2elisa试剂盒(bd生物科学),使用1n h2so4(wako)终止显色。对于ifn-γelisa开发试剂盒(peprotech),tmb色原溶液(赛默飞世尔科技)和1n h2so4(wako)用于显色和终止显色。然后用envision(perkinelmer)进行吸光度测量。
[1742]
结果在参考实施例5-5-3及之后详细介绍。
[1743]
(5-5-3)通过增加fcγ受体的结合活性,评估重链恒定区的激动剂活性的增强
[1744]
通过如参考实施例5-5-1和5-5-2中所述使用人外周血单核细胞进行体外评估,评估了使用p587、my518、tt14和tt16对cd137激动剂活性的作用,其中所述p587、my518、tt14和tt16不同地增加了重链恒定区的fcγriib结合活性。
[1745]
评估的抗体如表39所示。
[1746]
表39中列举的抗体的产生描述于参考实施例7-1中。与在250μm atp存在下添加阴性对照抗体(ic17hdk-my518/ic17l-k0、ic17hdk-g4d/ic17l-k0)时培养物上清液中il-2和ifn-γ的量相比,当抗体的添加使培养物上清液中的il-2量增加1.05倍以上且ifn-γ的量增加1.15倍以上时,则可以判断该抗体表现出cd137激动剂活性。使用人外周血单核细胞(pbmc)测量激动剂活性可能因血液样本的供体而异。考虑到这一点,可以确定,对于从多个供体分离的部分或多于一半的人pbmc中不示出cd137激动剂活性的抗体,即使其对于另一部分的人pbmc符合激动剂活性的标准,也可以判断为不示出cd137激动剂活性。
[1747]
表39示出了在250μmatp存在下被判断具有cd137激动剂活性的抗体。这表明通过将tt16与增加重链恒定区的fcγriib结合活性的p587进行组合增强了cd137激动剂活性(图30和31)。认为通过增加对表达fcγriib的细胞的结合活性来增强激动活性,其中所述表达fcγriib的细胞是抗体对表达cd137的细胞表现出激动活性所需的交联支架(参见protein eng des sel.2013.10;26(10):589-598。在线发表于2013年6月5日。doi:10.1093/蛋白质)。
[1748]
[表39]
[1749]
评估的抗体名称判断为在存在atp时具有活性的抗体名称a375-my518/b167-lamliba375-p587/b167-lamliba356-my518/b040-lamliba356-p587/b040-lamliba375-p587/b167-lamliba375-tt16/b167-lamliba356-p587/b040-lamliba356-tt16/b040-lamliba375-tt16/b167-lamlib a356-tt16/b040-lamlib a375-tt14/b167-lamlib [1750]
(5-5-4)可变区的atp依赖性cd137激动剂活性的评估
[1751]
如参考实施例5-5-1和5-5-2中所述,通过使用人外周血单核细胞体外评估来评估通过将重链恒定区p587和p253与各种可变区组合的每个可变区的atp依赖性cd137激动剂活性。
[1752]
评价的抗体如表40所示。表40中列举的抗体的产生描述于参考实施例7-1中。与在250μm atp存在下添加阴性对照抗体(ic17hdk-p253/ic17l-k0,ic17hdk-p587/ic17l-k0)时培养物上清液中il-2和ifn-γ的量相比,当抗体的添加使培养物上清液中的il-2量增加了1.05倍以上且ifn-γ的量增加了1.15倍以上时,则可以判断该抗体具有cd137激动剂活性。使用人外周血单核细胞(pbmc)测量激动剂活性可能因血液样本的供体而不同。考虑到这一点,可以确定,对于从多个供体分离的部分或多于一半的人pbmc中不示出cd137激动剂活性的抗体,即使其对于人pbmc其它部分符合激动剂活性标准,也可以判断为不示出cd137
激动剂活性。表40(图32、图33、图34、图35和图36)示出了在250μm atp存在下被判断为表现出cd137激动剂活性的抗体。
[1753]
此外,在被判断为在250μm atp存在下示出cd137激动剂活性的抗体中,以下抗体被判断为在无atp条件下具有较低的cd137激动剂:就培养物上清液中il-2和ifn-γ的量而言,在无atp条件下其相对于添加了阴性对照抗体(ic17hdk-p253/ic17l-k0、ic17hdk-p587/ic17l-k0)的组的倍数变化小于在存在250μm atp的条件下相对于阴性对照的倍数变化。表40(图32、图33、图34、图35和图36)示出了在存在250μm atp的情况下示出cd137激动剂活性且被判断为在不存在atp的情况下具有较低cd137激动剂活性的抗体。这些抗体被判断为表现出atp依赖性cd137激动剂活性。
[1754]
由上可确认,对于可变区,(a375/b167)、(a356/b040)、(a372/b040)、(a486/b167)、(a488/b226)、(a489/b223)、(a551/b256)、(a548/b256)和(a551/b379)的重链可变区/轻链可变区的组合示出atp依赖性方式的cd137激动剂活性。
[1755]
[表40]
[1756]
评估的抗体名称判断为在atp存在下具有活性的抗体名称判断为在atp不存在下具有较低活性的抗体名称a372-p253/b040-lamliba372-p253/b040-lamliba372-p253/b040-lamliba486-p253/b167-lamliba486-p253/b167-lamliba486-p253/b167-lamliba488-p253/b226-lamliba488-p253/b226-lamliba488-p253/b226-lamliba489-p253/b223-lamliba489-p253/b223-lamliba489-p253/b223-lamliba551-p587/b256-lamliba551-p587/b256-lamliba551-p587/b256-lamliba375-p587/b167-lamliba375-p587/b167-lamliba375-p587/b167-lamliba548-p587/b256-lamliba548-p587/b256-lamliba548-p587/b256-lamliba356-p587/b040-lamliba356-p587/b040-lamliba356-p587/b040-lamliba551-p587/b379-lamliba551-p587/b379-lamliba551-p587/b379-lamlib
[1757]
(5-5-5)评估将增加重链恒定区的pi的改变和具有增加的fcγ受体结合活性的重链恒定区进行组合对cd137激动剂活性的增强作用
[1758]
通过使用在参考实施例5-5-1和5-5-2中描述的人外周血单核细胞进行体外评估,评估了将增加重链恒定区pi的各种氨基酸修饰引入具有各种增加的fcγriib结合活性的重链恒定区中对cd137激动剂活性的作用。将增加pi的氨基酸改变引入重链恒定区tt16、my518和tt14中,从而生成了重链恒定区tt16+p343r/d413k(scf028)、tt16+q311r/p343r(scf033)、my518+p343r/d413k(scf025)、my518+q311r/p343r(scf030)、tt14+p343r/d413k(scf027)和tt14+q311r/p343r(scf032)。表41中示出了已引入了增加pi的氨基酸改变的评估抗体的名称,以及引入增加pi的氨基酸改变之前的相应抗体的名称。表41中引用的抗体的产生在参考实施例7-2中进行了描述。
[1759]
关于通过引入增加pi的氨基酸修饰来增强激动剂活性的评估,相对于添加了含有不包含这些氨基酸修饰的重链恒定区的抗体的组a375-tt16/b167-lamlib、a375-my518/b167-lamlib和a375-tt14/b167-lamlib,当抗体的添加使得培养物上清液中il-2的量增加1.04倍以上且ifn-γ的量增加1.1倍以上时,则判断为cd137激动剂活性增强。与包含没有增加pi的氨基酸修饰的重链恒定区的抗体相比,包含在其中引入了在存在250μm atp时示出增强的cd137激动剂活性的氨基酸修饰的重链恒定区的抗体示出在表42(图31)中。
[1760]
这表明与重链恒定区的fcγriib结合活性的增加程度无关,引入增加重链恒定区pi的修饰增强抗人cd137抗体的cd137激动剂活性。这显示了,将增加重链恒定区pi的修饰
与增加重链恒定区的fcγriib结合的修饰组合至重链恒定区中,增强了与带负电荷的表达fcγriib的细胞表面的相互作用;抗体或抗原结合抗体的免疫复合物更接近表达fcγriib的细胞表面;并且这进一步增加了与表达fcγriib的细胞的结合,所述表达fcγriib的细胞是抗体对表达cd137的细胞展示激动活性所需的交联支架;因此,激动活性被进一步增强。
[1761]
[表41]
[1762][1763]
[表42]
[1764]
判断为展示增加的激动活性的抗体名称a375-scf028/b167-lamliba375-scf033/b167-lamliba375-scf025/b167-lamliba375-scf030/b167-lamliba375-scf027/b167-lamliba375-scf032/b167-lamlib
[1765]
(5-5-6)评估引入增加重链恒定区的pi的修饰对激动剂活性的影响
[1766]
通过使用参考实施例5-5-1和5-5-2中描述的人外周血单核细胞体外评估来评估引入增加重链恒定区my201aph和my518的pi的各种氨基酸修饰对cd137激动剂活性的影响。将具有增加pi的氨基酸修饰引入至重链恒定区my518、my518a和my201aph;从而生成my518+p343r/d413k(scf025)、my518+q311r/p343r(scf030)、my518+p343r(scf039)、my518+d413k(scf040)、my518a+q311r(scf060a)、my201aph+p343r(scf041aph)、my201aph+p343r/d413k(scf043aph)、my201aph+q311r(scf056aph)、my201aph+q311r/p343rb(scf057aph)和my201aph+q311r/d413k(scf059aph)。表43中示出了其中已引入了增加pi的氨基酸改变的评估的抗体名称,以及引入增加相应pi的氨基酸改变之前的抗体名称。表43中引用的抗体的产生在参考实施例7-2进行描述。
[1767]
关于通过引入增加pi的氨基酸修饰来增强激动剂活性的评估,相对于添加了包含不含有这些氨基酸修饰的重链恒定区的抗体的组,即a375-my518a/b167-lamlib和a375-my201aph/b167-lamlib,当抗体的添加使培养物上清液中il-2的量增加1.04倍以上且ifn-γ的量增加1.1倍以上时,则判断cd137激动剂活性增强。与包含不具有增加pi的氨基酸修饰的重链恒定区的抗体相比,包含其中已引入在250μm atp存在下示出具有增强的cd137激动剂活性的氨基酸改变的重链恒定区的抗体示于表44(图37和38)。
[1768]
[表43]
atp的条件下相对于阴性对照的倍数变化。表45中示出了在不存在atp的情况下被判断为具有较低cd137激动剂活性的抗体(图37、图38、图39、图40、图41、图42、图43和图44)。这些抗体示出atp依赖性cd137激动剂活性。
[1776]
[表45]
[1777][1778]
参考实施例6:抗人cd137转换抗体的人cd137敲入小鼠施用试验
[1779]
(6-1)用于人cd137敲入小鼠施用研究的抗体的产生
[1780]
产生具有小鼠恒定区的抗人cd137转换抗体和非转换抗体用于人cd137敲入小鼠施用研究。具体而言,产生了抗人cd137非转换抗体(20h4.9-migg1/20h4.9lc-mk0,缩写:
ns1-migg1,20h4.9-mb110/20h4.9lc-mk0,缩写:ns1-mb110,20h4.9-mb492/20h4.9lc-mk0,缩写:ns1-mb492,mor-7480.1h-mb110/mor-7480.1l-ml0r,缩写:ns2-mb110,mor-7480.1h-mb492/mor-7480.1l-ml0r,缩写:ns2-mb492),以及抗人cd137转换抗体(a375-migg1/b167-ml0r,a372-migg1/b040-ml0r,a372-mb110/b040-ml0r,a372-mb492/b040-ml0r,a356-mb110/b040-ml0r,a486-mb492/b167-ml0r,a488-mb492/b226-ml0r,a489-mb492/b223-ml0r,a551-migg1/b256-ml0r,a551-mb110/b379-ml0r和a548-migg1/b256-ml0r)。
[1781]
对于ns1-migg1、ns1-mb110和ns1-mb492抗体的重链,抗体重链的基因是通过将重链可变区20h4.9(seq id no:139)与以下任何一种作为重链恒定区组合而产生的:(i)migg1,鼠igg1的重链恒定区(seq id no:144),
[1782]
(ii)如wo2014030750中描述的mb110(seq id no:145),和
[1783]
(iii)如wo2014030750中描述的mb492(seq id no:146),即,产生了20h4.9-migg1、20h4.9-mb110和20h4.9-mb492的基因。
[1784]
对于ns1-migg1、ns1-mb110和ns1-mb492抗体的轻链,通过将轻链可变区20h4.9lc(seq id no:140)与轻链恒定区鼠κ链mk0(seq id no:147)进行组合生成抗体轻链基因20h4.9lc-mk0。通过组合这些重链和轻链基因,通过本领域技术人员已知的方法表达和纯化每种抗体。
[1785]
对于ns2-mb110和ns2-mb492抗体的重链,抗体重链的基因是通过将重链可变区mor-7480.1h(seq id no:142)与以下任一种作为重链恒定区组合而产生的:
[1786]
(i)mb110(seq id no:145),或
[1787]
(ii)mb492(seq id no:146),
[1788]
即,产生了mor-7480.1h-mb110和mor-7480.1h-mb492基因。
[1789]
对于ns2-mb110和ns2-mb492抗体的轻链,通过将轻链可变区mor-7480.1l(seq id no:143)与鼠λ链ml0r(seq id no:148)作为轻链恒定区进行组合,产生抗体轻链基因mor-7480.1l-ml0r。通过组合这些重链和轻链基因,通过本领域技术人员已知的方法表达和纯化每种抗体。
[1790]
对于抗cd137转换抗体,产生了下表46和47中的抗体重链和抗体轻链的基因;并且通过本领域技术人员已知的方法通过组合这些基因来表达和纯化每种抗体。
[1791]
具有鼠恒定区的抗cd137转换抗体的抗体重链
[1792]
[表46]
[1793][1794]
具有鼠恒定区的抗cd137转换抗体的抗体轻链
[1795]
[表47]
[1796]
全长轻链b040-ml0r可变区b040(seq id no:55)
ꢀꢀ
恒定区ml0r(seq id no:148)全长轻链b167-ml0r可变区b167(seq id no:54)
ꢀꢀ
恒定区ml0r(seq id no:148)全长轻链b226-ml0r可变区b226(seq id no:56)
ꢀꢀ
恒定区ml0r(seq id no:148)全长轻链b223-ml0r可变区b223(seq id no:57)
ꢀꢀ
恒定区ml0r(seq id no:148)全长轻链b256-ml0r可变区b256(seq id no:59)
ꢀꢀ
恒定区ml0r(seq id no:148)全长轻链b379-ml0r可变区b379(seq id no:60)
ꢀꢀ
恒定区ml0r(seq id no:148)
[1797]
(6-2)评估用于人cd137敲入小鼠施用研究的抗体的人cd137结合活性
[1798]
评价了参考实施例6-1中产生的抗人cd137非转换抗体和抗cd137转换抗体对人cd137的结合活性。使用20mm aces(ph 7.4),150mm nacl,2mm mgcl2和0.05%吐温20作为运行缓冲液,在37℃下测量人cd137的结合力。首先,通过将运行缓冲液中制备的抗体溶液
与兔抗鼠igg(赛默科技)固定的s系列传感器芯片cm5(ge医疗)相互作用来捕获抗体。然后通过与在补充有所需浓度的atp的运行缓冲液中制备的人cd137溶液或与在不带atp的运行缓冲液中制备的人cd137溶液相互作用,评估在存在atp和不存在atp的情况下的人cd137结合活性。对于人cd137抗原,使用在参考实施例(1-2)中制备的hcd137(fxa消化的),并且在0、15.625、62.5、250和1000nm的抗原浓度下进行测量。使用25mm naoh和10mm甘氨酸-hcl(ph 1.5)再生芯片,并通过重复捕获抗体进行测量。使用biacore t200评估软件2.0计算各种抗体对人cd137的解离常数(kd)。具体地,通过用1:1朗缪尔(langmuir)结合模型对通过测量获得的传感图进行整体拟合来计算缔合速率常数ka(l/mol/s)和解离速率常数kd(1/s),以及由这些值算出解离常数kd(mol/l)。
[1799]
表48示出了这些测量的结果。
[1800]
具有鼠恒定区的抗cd137抗体的人cd137结合分析
[1801]
[表48]
[1802][1803]
n.a.:太弱无法确定kd值。
[1804]
n.d.:未确定。
[1805]
证实了上述产生的包含鼠恒定区的抗人cd137非转换抗体和抗人cd137转换抗体均与人cd137结合。还示出所有抗人cd137转换抗体均以atp浓度依赖性方式结合人cd137。另一方面,对于非转换抗体,未观察到与人cd137的这种atp浓度依赖性结合,并且在任一atp浓度下结合几乎相同。
[1806]
(6-3)人cd137敲入小鼠中修饰抗体的血浆动力学评估
[1807]
(6-3-1)人cd137敲入小鼠的产生
[1808]
通过将人cd137基因置换载体导入小鼠胚胎干细胞(es细胞)中,产生了人cd137敲入小鼠,其中小鼠cd137基因被人cd137基因替代。将该小鼠描述为hcd137 ki小鼠。
[1809]
(6-3-2)hcd137ki小鼠模型中血浆抗人cd137抗体浓度的测量
[1810]
在参考实施例6-3-1中产生hcd137ki小鼠后,将各自的抗体以单剂量静脉内施用给hcd137ki小鼠,如表49所示。在表49中,ns1-migg1、ns1-mb110和ns1-mb492都是非转换抗体,其它是转换抗体。从施用后5分钟到28天,随着时间的推移多次采血。将获得的血液离心分离血浆。将血浆保存在低于-20℃的冰箱中直至测量。
[1811]
血浆动力学评估研究的组别详细信息
[1812]
[表49]
[1813]
组动物数药剂剂量[mg/kg]13ns1-migg17.5单次施用23ns1-mb1107.5单次施用33ns1-mb4927.5单次施用43a375-migg1/b167-ml0r7.5单次施用53a356-mb110/b040-ml0r7.5单次施用63a372-migg1/b040-ml0r7.5单次施用73a372-mb110/b040-ml0r7.5单次施用83a372-mb492/b040-ml0r7.5单次施用93a486-mb492/b167-ml0r7.5单次施用103a488-mb492/b226-ml0r7.5单次施用113a489-mb492/b223-ml0r7.5单次施用123a548-migg1/b256-ml0r7.5单次施用133a551-migg1/b256-ml0r7.5单次施用143a551-mb110/b379-ml0r7.5单次施用
[1814]
通过电化学发光(ecl)方法测量血浆中每种转换抗体的浓度。具体而言,将hcd137(sino biological inc.)在pbs(-)中稀释,然后添加到multi-array 96孔板(meso scale diagnostics,llc)中。将hcd137添加到板上并在室温下振荡1小时,并将hcd137固定在板上。接下来,为了封闭,加入包含1%bsa和0.05%吐温20的pbs溶液,并在室温下振荡1小时。在血浆浓度为64、32、16、8、4、2和1ng/ml,制备单个转换抗体的校准曲线。向hcd137固定的板中加入含3mm adp、1%bsa和0.05%吐温20的pbs溶液后,添加在含1%bsa和0.05%吐温20的pbs溶液中稀释两倍的血浆样品及校准曲线样品。在室温下将板振荡一小时后,添加生物素化的抗小鼠igg抗体(jackson immunoresearch laboratories,inc.)。另外,将板在室
温下振荡一小时后,添加sulfo-tag标记的链霉亲和素(meso scale diagnostics,llcs)。另外,将板在室温下振荡一小时后,加入用含有2mm adp、1%bsa和0.05%吐温20的pbs溶液稀释两倍的读取缓冲液t(read buffer t)(meso scale diagnostics,llcs)。通过使用sector成像仪(meso scale diagnostics,llc)上的sulfo-tag检测进行hcd137ki小鼠血浆中抗体浓度的测量。使用softmax pro(molecular devices)进行小鼠血浆中各个抗体浓度的计算。
[1815]
通过电化学发光(ecl)方法测量血浆中非转换抗体的浓度。具体而言,将hcd137(sino biological inc.)在pbs(-)中稀释,然后添加到multi-array 96孔板(meso scale diagnostics,llc)中。将hcd137添加到板上并在室温下振荡1小时,并将hcd137固定在板上。接下来,为了封闭,加入包含1%bsa和0.05%吐温20的pbs溶液,并在室温下振荡1小时。在血浆浓度为32、16、8、4、2、1和0.5ng/ml,制备各个非转换抗体的校准曲线。将在含1%bsa、0.05%吐温20的pbs溶液中稀释的血浆样品以及校准曲线样品添加到hcd137固定的板上。在室温下将板振荡一小时后,添加生物素化的抗小鼠igg抗体(jackson immunoresearch laboratories,inc.)。另外,将板在室温下振荡一小时后,添加sulfo-tag标记的链霉亲和素(meso scale diagnostics,llcs)。另外,将板在室温下振荡一小时后,添加稀释两倍的读取缓冲液t(meso scale diagnostics,llcs)。hcd137ki小鼠血浆中抗体浓度的测量与上述转换抗体相似。
[1816]
结果示出在图45、46和47中。
[1817]
图45示出了在hcd137 ki小鼠中,表49中所示的抗体中具有migg1为fc的抗体的平均血浆浓度随时间变化的过程(ns1-migg1为非转换抗体,a375-migg1/b167-ml0r、a372-migg1/b040-ml0r、a548-migg1/b256-ml0r或a551-migg1/b256-ml0r为转换抗体)。图46示出了在hcd137 ki小鼠中,具有mb110为fc的抗体的平均血浆浓度随时间变化的过程(ns1-mb110为非转换抗体,a356-mb110/b040-ml0r,a372-mb110/b040-ml0r和a551-mb110/b379-ml0r为转换抗体)。图47示出了在cd137 ki小鼠中,具有mb492作为fc的抗体的平均血浆浓度随时间变化的过程(ns1-mb492为非转换抗体,以及a372-mb492/b040-ml0r、a486-mb492/b167-ml0r、a488-mb492/b226-ml0r或a489-mb492/b223-ml0r为转换抗体)。在图47中,对于a488-mb492/b226-ml0r,在一个受试者中证实了怀疑是由ada引起的血浆浓度时间进程的急剧下降,并且平均值取自两个受试者。
[1818]
在具有任一fc的hcd137 ki小鼠中,转换抗体示出从血浆中清除的速度比非转换抗体慢。认为这是因为与转换抗体相比,非转换抗体与在体内表达的cd137结合并从血浆中更快地消除。此外,这提示正常组织中细胞外atp浓度足够低,以至于本研究中使用的转换抗体不与人cd137结合。这些结果表明,通过使用转换抗体可以减少与全身表达的抗原的结合,因此可以制备具有增强的血液动力学的抗体。
[1819]
(6-4)通过使用hcd137ki小鼠的同系肿瘤细胞移植模型的抗cd137抗体的药效和全身反应标志物的运动(movement)
[1820]
(6-4-1)细胞系和同系肿瘤移植小鼠模型的生成以及抗肿瘤作用和全身反应的评价方法
[1821]
由国家癌症研究所许可的鼠结肠直肠癌细胞系mc38的细胞和参考实施例6-3-1中描述的hcd137 ki小鼠用于各种研究。通过将mc38细胞系皮下植入小鼠腹部,当肿瘤体积达
到约50-300mm3时,形成模型。建立模型后,将移植有mc38细胞系的小鼠分组,然后施用各种抗cd137抗体。
[1822]
为了评估抗肿瘤作用,以每周1-2次的频率进行肿瘤体积的测量。根据以下公式计算肿瘤体积:
[1823]
肿瘤体积(mm3)=长度(mm)x宽度(mm)x宽度(mm)/2
[1824]
通过在施用抗体后的适当时间去除肝脏和脾脏或淋巴结,可以通过器官重量、淋巴细胞级分的细胞计数或使用流式细胞仪(fcm)进行的t细胞分析来评估全身反应。在这些指标的评估中,当与相同量的非转化抗体量(无atp依赖性人cd137结合活性的对照抗人cd137抗体)相比全身反应指标低时,受试者转换抗体被评估为具有抑制的全身反应和/或在非肿瘤组织(例如淋巴结、脾脏和肝脏)中的t细胞激活。
[1825]
参考实施例6-1中产生的抗体(用于人cd137敲入小鼠施用测试的抗体的产生)用于各种测试中。
[1826]
(6-4-2)从mc38细胞系移植小鼠收集各种器官并制备淋巴细胞级分
[1827]
进行收集的脾脏和淋巴结的重量测量,以及淋巴细胞级分的细胞计数。将使用肝脏解离试剂盒,小鼠(milteny biotec)获得的淋巴细胞级分也用于评估肝激活。将红细胞裂解后的淋巴细胞级分用于评估脾脏中的激活,并且将通过研磨获得的淋巴细胞级分用于评估淋巴结中的激活。
[1828]
(6-4-3)使用来自各种器官的淋巴细胞级分进行fcm分析
[1829]
为了通过fcm评估激活标志物,使用了cd8α阳性t细胞上的颗粒酶b或pd-1表达或icos表达,或cd45阳性细胞中cd8α阳性t细胞的百分比。因此,在fcm分析中使用了荧光标记的抗颗粒酶b抗体、抗pd-1抗体、抗icos抗体、抗cd8α抗体和抗cd45抗体。用bd lsrfortessa tm x-20(bd biosciences)进行测量。
[1830]
(6-4-4)a375-migg1/b167-ml0r抗体的药效(抗肿瘤作用)研究
[1831]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表50所示的剂量施用赋形剂和a375-migg1/b167-ml0r。在分组当天和分组后四天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1832]
a375-migg1/b167-ml0r药效研究的组别详细信息
[1833]
[表50]
[1834]
[1835]
通过如参考实施例6-4-1中描述的计算的肿瘤体积评估每组中的抗肿瘤作用。结果,证实了a375-migg1/b167-ml0r抗体的剂量依赖性抗肿瘤作用(图48)。
[1836]
(6-4-5)用于评估a375-migg1/b167-ml0r的全身作用的抗体施用和取样以及fcm分析
[1837]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表51所示,施用赋形剂、ns1-migg1(非转换抗体)和a375-migg1/b167-ml0r。分组当天和分组后三天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1838]
初次施用后五天,如参考实施例6-4-2所示收集肝脏、淋巴结和脾脏(从移植了mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。此外,对于脾脏和淋巴结,合并来自三只小鼠的器官,并且如参考实施例6-4-3中所示进行fcm分析(使用来自各种器官的淋巴细胞级分进行fcm分析)。
[1839]
评估a375-migg1/b167-ml0r抗体的全身反应的组别详细信息
[1840]
[表51]
[1841][1842]
评价了所施用抗体的全身作用。评价淋巴结和脾脏的器官重量的结果是,当以0.3mg/kg施用ns1-migg1时,观察到器官重量增加,并且在1.5mg/kg和7.5mg/kg下观察到更强烈的器官过度增大。另一方面,当施用a375-migg1/b167-ml0r时,在1.5mg/kg、7.5mg/kg或37.5mg/kg的任一剂量下均未观察到器官增大(图49)。
[1843]
另外,作为通过fcm评估来评估t细胞激活的结果,在施用ns1-migg1后,在0.3mg/kg观察到所有标志物pd-1、icos和颗粒酶b的表达增加。另一方面,当施用a375-migg1/b167-ml0r时,在1.5mg/kg、7.5mg/kg和37.5mg/kg的剂量下,所有标志物pd-1、icos和颗粒酶b的表达均受到显著抑制(图50和图51)。由于a375-migg1/b167-ml0r结果表明器官重量与淋巴结和脾脏中的t细胞激活标志物相关,因此器官重量主要用作随后抗体评估中源自淋巴结和脾脏的免疫细胞激活的指标。
[1844]
评价肝脏中t细胞激活的结果是,当以0.3mg/kg施用ns1-migg1时,观察到pd-1和颗粒酶b的表达增加。另一方面,当施用a375-migg1/b167-ml0r时,在1.5mg/kg、7.5mg/kg和37.5mg/kg的所有剂量下表达均被抑制(图52)。
[1845]
因此,与相同量的非转换抗体相比,转换抗体抑制淋巴结、脾脏和肝脏中t细胞的激活。
[1846]
(6-4-6)a356-mb110/b040-ml0r抗体的药效(抗肿瘤作用)研究
[1847]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表52所示的剂量施用赋形剂和a356-mb110/b040-ml0r。在分组当天和分组后三天通过尾静脉途径进行了两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1848]
a356-mb110/b040-ml0r药效研究的组别详细信息
[1849]
[表52]
[1850][1851]
通过如参考实施例6-4-1中所描述的计算的肿瘤体积评估每组的抗肿瘤作用。结果证实了a356-mb110/b040-ml0r的剂量依赖性抗肿瘤作用(图53)。
[1852]
(6-4-7)用于评估a356-mb110/b040-ml0r的全身作用的抗体施用和取样以及fcm分析
[1853]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表53所示施用赋形剂、ns2-mb110(非转换抗体)和a356-mb110/b040-ml0r。在分组当天和分组后三天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1854]
第一次施用7天后,以参考实施例6-4-2所示的方式收集肝脏、淋巴结和脾脏(从移植有mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏和淋巴结,仅进行器官重量测量。
[1855]
评估a356-mb110/b040-ml0r抗体的全身反应的组别详细信息
[1856]
[表53]
[1857][1858]
评估了所施用抗体的全身作用。施用ns2-mb110和a356-mb110/b040-ml0r时评估淋巴结和脾脏器官重量的结果表明,当以2.5mg/kg施用ns2-mb110时也观察到过度增大。另一方面,在施用a356-mb110/b040-ml0r时,即使在7.5mg/kg下也可抑制淋巴结病,在2.5mg/kg下可抑制脾肿大(图54)。
[1859]
另外,评价肝脏中t细胞激活的结果表明,当以0.3mg/kg施用ns2-mb110时,还观察到了cd8α阳性细胞中pd-1表达的增加。同时,当施用a356-mb110/b040-ml0r时,pd-1表达在7.5mg/kg被抑制,并且在2.5mg/kg被显著抑制。以0.3mg/kg施用ns2-mb110抗体后,还观察到cd8α阳性细胞中icos表达略有增加。另一方面,当施用a356-mb110/b040-ml0r时,观察到赋形剂的表达在2.5mg/kg被抑制(图55)。
[1860]
因此,与非转换抗体相比,转换抗体抑制淋巴结、脾脏和肝脏中t细胞的激活。
[1861]
(6-4-8)a372-migg1/b040-ml0r抗体的药效(抗肿瘤作用)研究
[1862]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表54所示的剂量施用赋形剂和a372-migg1/b040-ml0r。在分组当天和分组后4天、7天和10天通过尾静脉途径进行了四次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1863]
a372-migg1/b040-ml0r药效研究的组别详细信息
[1864]
[表54]
[1865][1866]
通过如参考实施例6-4-1中所描述的计算的肿瘤体积评估每组的抗肿瘤作用。结果,在施用7.5mg/kg时观察到了a372-migg1/b040-ml0r抗体的抗肿瘤作用(图56)。
[1867]
(6-4-9)用于评估a372-migg1/b040-ml0r的全身作用的抗体施用和取样以及fcm分析
[1868]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表55所示施用赋形剂和a372-migg1/b040-ml0r。在分组当天和分组后的3天和6天通过尾静脉途径进行了3次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1869]
初次给药7天后,以参考实施例6-4-2所示的方式收集肝脏、淋巴结和脾脏(从移植有mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏,仅测量器官重量。对于淋巴结,仅对从三只小鼠汇集的淋巴细胞中获得的淋巴细胞级分进行细胞计数。
[1870]
用于评估a372-migg1/b040-ml0r抗体的全身反应的组别详细信息
[1871]
[表55]
[1872][1873]
评估了所施用抗体的全身作用。作为测量淋巴结中的细胞数量并评估脾脏的器官重量的结果,可以确定施用a372-migg1/b040-ml0r时,淋巴结中的细胞数量没有增加,并且脾脏的重量没有增加,并且器官重量与赋形剂组相同(图57)。
[1874]
作为评估肝脏中t细胞激活的结果,当施用a372-migg1/b040-ml0r时,颗粒酶b的表达水平与赋形剂组相似(图58)。
[1875]
因此,证实了转换抗体抑制淋巴结、脾脏和肝脏中t细胞的激活。
[1876]
(6-4-10)a372-mb110/b040-ml0r抗体的药效(抗肿瘤作用)研究
[1877]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表56中所示的剂量施用赋形剂和a372-mb110/b040-ml0r。在分组当天和分组后四天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1878]
a372-mb110/b040-ml0r药效研究的组别详细信息
[1879]
[表56]
[1880][1881]
通过如参考实施例6-4-1中所述计算的肿瘤体积评估每组的抗肿瘤作用。结果,证实了a372-mb110/b040-ml0r的抗肿瘤作用(图59)。
[1882]
(6-4-11)用于评估a372-mb110/b040-ml0r的全身作用的抗体施用和取样以及fcm分析
[1883]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表57所示,施用赋形剂、ns2-mb110(非转换抗体)和a372-mb110/b040-ml0r。分组当天和分组后3天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1884]
初次施用后7天,如参考实施例6-4-2所示收集肝脏、淋巴结和脾脏(从移植了mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏和淋巴结,仅进行器官重量测量。
[1885]
评估a372-mb110/b040-ml0r抗体的全身反应的组别详细信息
[1886]
[表57]
[1887][1888][1889]
评估了所施用抗体的全身作用。评价淋巴结和脾脏的器官重量的结果是,当以2.5mg/kg和7.5mg/kg施用ns2-mb110时,观察到器官重量增加。另一方面,当施用a372-mb110/b040-ml0r时,在2.5mg/kg和7.5mg/kg的两个剂量下均观察到了器官肿大的抑制(图60)。
[1890]
评价肝脏中t细胞激活的结果是,当施用ns2-mb110时观察到pd-1表达的增加。当施用a372-mb110/b040-ml0r时也可见到pd-1表达的增加(图61)。
[1891]
总之,与非转换抗体相比,转换抗体抑制淋巴结和脾脏中t细胞的激活。
[1892]
(6-4-12)a372-mb492/b040-ml0r抗体的药效(抗肿瘤作用)研究
[1893]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表58中所示的剂量施用赋形剂和a372-mb492/b040-ml0r。在分组当天和分组后三天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1894]
a372-mb492/b040-ml0r药效研究的组别详细信息
[1895]
[表58]
[1896][1897]
通过如参考实施例6-4-1中所描述的计算的肿瘤体积评估每组的抗肿瘤作用。结果,在所有剂量下都观察到了a372-mb492/b040-ml0r抗体的抗肿瘤作用(图62)。
[1898]
(6-4-13)用于评估a372-mb492/b040-ml0r抗体的全身作用的抗体施用和采样以及fcm分析
[1899]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表59所示,施用赋形剂、ns1-mb492(非转换抗体)和a372-mb492/b040-ml0r。分组当天和分组后3天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1900]
初次施用后八天,以参考实施例6-4-2中所示的方式收集肝脏、淋巴结和脾脏(从移植了mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏,仅测量器官重量。对于淋巴结,仅对制备的淋巴细胞级分进行细胞计数。
[1901]
评估a372-mb492/b040-ml0r抗体全身反应的组别详细信息
[1902]
[表59]
[1903][1904]
评价了所施用抗体的全身作用。当施用ns1-mb492时,观察到了脾脏器官重量增加,当施用ns1-mb492时,观察到了淋巴细胞级分细胞计数测量增加。另一方面,当以1.5mg/kg、3.0mg/kg和7.5mg/kg的剂量施用a372-mb492/b040-ml0r时,与ns1-mb492相比,观察到了对器官肿大的抑制(图63)。
[1905]
作为评估肝脏中t细胞激活的结果,与赋形剂相比,当施用ns1-mb492和a372-mb492/b040-ml0r时,观察到颗粒酶b的表达增加(图64)。
[1906]
总之,与非转换抗体相比,转换抗体抑制淋巴结和脾脏中t细胞的激活。
[1907]
(6-4-14)a486-mb492/b167-ml0r和a488-mb492/b226-ml0r抗体的药效(抗肿瘤作用)研究
[1908]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表60所示的剂量施用赋形剂、a486-mb492/b167-ml0r和a488-mb492/b226-ml0r。在细胞移植后后10天进行分组,在细胞移植后第11、15、18和22天通过尾静脉途径进行共四次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1909]
a486-mb492/b167-ml0r和a488-mb492/b226-ml0r抗体的药效研究的组别详细信息
[1910]
[表60]
[1911][1912]
通过如参考实施例6-4-1中所描述的计算的肿瘤体积评估每组的抗肿瘤作用。结果证实了a486-mb492/b167-ml0r和a488-mb492/b226-ml0r的抗肿瘤作用(图65)。
[1913]
(6-4-15)用于评估a486-mb492/b167-ml0r和a488-mb492/b226-ml0r的全身作用的抗体施用和取样以及fcm分析
[1914]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表61所示施用赋形剂、ns1-mb492(非转换抗体)、a486-mb492/b167-ml0r和a488-mb492/b226-ml0r。在细胞移植后10天进行分组,并且在细胞移植后第11、15、18和22天通过尾静脉途径进行总共四次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1915]
初次施用后13天,以参考实施例6-4-2所示的方式收集肝脏、淋巴结和脾脏(从移植了mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏,仅进行测量器官重量。对于淋巴结,仅对淋巴细胞级分进行细胞计数。
[1916]
评估a486-mb492/b167-ml0r和a488-mb492/b226-ml0r抗体的全身反应的组别详细信息
[1917]
[表61]
[1918][1919]
作为对淋巴结的淋巴细胞级分的细胞计数测量和脾脏重量测量的结果,当施用ns1-mb492时,观察到淋巴细胞的细胞计数和脾脏重量增加。另一方面,观察到与施用ns1-mb492时相比,施用a486-mb492/b167-ml0r和a488-mb492/b226-ml0r时淋巴细胞计数和脾脏重量的增加受到抑制(图66)。
[1920]
作为评估肝脏中t细胞激活的结果,与赋形剂相比,当施用ns1-mb492、a486-mb492/b167-ml0r和a488-mb492/b226-ml0r时,观察到cd8α阳性细胞百分比的增加(图67)。
[1921]
由上可知,与非转换抗体相比,转换抗体抑制了淋巴结和脾脏中的t细胞激活。
[1922]
(6-4-16)a489-mb492/b223-ml0r抗体的药效(抗肿瘤作用)研究
[1923]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表62中所示的剂量施用赋形剂和a489-mb492/b223-ml0r。分组后第二天和分组后4、7和10天通过尾静脉途径进行抗体施用四次。对于赋形剂,使用含有0.05%吐温20的pbs。
[1924]
a489-mb492/b223-ml0r药效研究的组别详细信息
[1925]
[表62]
[1926][1927]
通过如参考实施例6-4-1中所述计算的肿瘤体积评估每组的抗肿瘤作用。结果,在7.5mg/kg施用证实了抗肿瘤作用(图68)。
[1928]
(6-4-17)用于评估a489-mb492/b223-ml0r抗体的全身作用的抗体施用和取样以及fcm分析
[1929]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表63所示施用赋形剂、ns1-mb492(非转换抗体)和a489-mb492/b223-ml0r。在分组当天、分组后3天和6天通过尾部静脉途径进行抗体施用,共3次。对于赋形剂,使用含有0.05%吐温20的pbs。
[1930]
初次施用7天后,以参考实施例6-4-2所示的方式收集肝脏、淋巴结和脾脏(从移植有mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏和淋巴结,仅对制备的淋巴细胞级分进行细胞计数测量。
[1931]
评估a489-mb492/b223-ml0r抗体全身反应的组别详细信息
[1932]
[表63]
[1933][1934]
作为对淋巴结和脾脏的淋巴细胞级分进行细胞计数测量的结果,当施用ns1-mb492时观察到细胞计数增加。另一方面,与施用ns1-mb492时相比,当施用a489-mb492/b223-ml0r时,观察到淋巴细胞计数增加的抑制(图69)。
[1935]
作为评价肝脏中t细胞激活的结果,与赋形剂相比,当施用ns1-mb492和a489-mb492/b223-ml0r时,观察到cd8α阳性细胞百分比的增加(图70)。
[1936]
由上可确认,与非转换抗体相比,转换抗体抑制了淋巴结和脾脏中的t细胞的激活。
[1937]
(6-4-18)a548-migg1/b256-ml0r和a551-migg1/b256-ml0r抗体的药效研究(抗肿瘤作用)
[1938]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表64中所示的剂量施用赋形剂、a548-migg1/b256-ml0r和a551-migg1/b256-ml0r。在分组当天和分组后3天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1939]
a548-migg1/b256-ml0r和a551-migg1/b256-ml0r抗体的药效研究的组别详细信
息
[1940]
[表64]
[1941][1942][1943]
通过如参考实施例6-4-1中所描述的计算的肿瘤体积评估每组的抗肿瘤作用。结果示出以37.5mg/kg和100mg/kg施用a548-migg1/b256-ml0r具有抗肿瘤作用。a551-migg1/b256-ml0r在100mg/kg时也示出显著的抗肿瘤作用(图71)。
[1944]
(6-4-19)用于评估a548-migg1/b256-ml0r和a551-migg1/b256-ml0r抗体的全身作用的抗体施用和采样以及fcm分析
[1945]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表65所示施用赋形剂、ns1-migg1(非转换抗体)、a548-migg1/b256-ml0r和a551-migg1/b256-ml0r。在分组当天和分组后3天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1946]
初次施用后五天,以参考实施例6-4-2所示的方式收集肝脏、淋巴结和脾脏(从移植了mc38细胞系的小鼠中收集各种器官并制备淋巴细胞级分)。对于脾脏和淋巴结,仅进行器官重量测量。
[1947]
评估a548-migg1/b256-ml0r抗体和a551-migg1/b256-ml0r抗体的全身反应的组别详细信息
[1948]
[表65]
[1949][1950][1951]
作为评价淋巴结和脾脏的器官重量的结果,当以0.3mg/kg、1.5mg/kg和7.5mg/kg施用ns1-migg1时,观察到器官重量增加。另一方面,当以1.5mg/kg、7.5mg/kg、37.5mg/kg和
100mg/kg的任一剂量施用a548-migg1/b256-ml0r或a551-migg1/b256-ml0r时,未观察到器官过度增大(图72)。
[1952]
作为评估肝脏中t细胞激活的结果,当以0.3mg/kg的剂量施用ns1-migg1时,观察到颗粒酶b和pd-1的表达均增加。另一方面,当以1.5mg/kg、7.5mg/kg、37.5mg/kg和100mg/kg的任一剂量施用a548-migg1/b256-ml0r和a551-migg1/b256-ml0r时,表达被抑制(图73)。
[1953]
因此,与非转换抗体相比,转换抗体抑制淋巴结、脾脏和肝脏中t细胞的活化。
[1954]
(6-4-20)a551-mb110/b379-ml0r抗体的药效(抗肿瘤作用)研究
[1955]
在参考实施例6-4-1中建立mc38移植小鼠模型后,以表66中所示的剂量施用赋形剂和a551-mb110/b379-ml0r。在分组当天和分组后3天通过尾静脉途径进行了两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1956]
a551-mb110/b379-ml0r抗体药效研究的组别详细信息
[1957]
[表66]
[1958][1959]
通过如参考实施例6-4-1中所描述的计算的肿瘤体积评估每组的抗肿瘤作用。结果,在任一剂量下都证实了抗肿瘤作用(图74)。
[1960]
(6-4-21)用于评估全身作用的抗体施用和采样以及fcm分析
[1961]
在参考实施例6-4-1中建立mc38移植小鼠模型后,如表67所示施用赋形剂、ns1-migg1(非转换抗体)和a551-mb110/b379-ml0r。分组当天和分组后3天通过尾静脉途径进行两次抗体施用。对于赋形剂,使用含有0.05%吐温20的pbs。
[1962]
初次施用后第5天,以参考实施例6-4-2所示的方式收集肝脏、淋巴结和脾脏(从mc38细胞系移植小鼠收集各种器官并制备淋巴细胞级分),并以参考实施例6-4-3中所示的方式进行fcm分析(使用各种器官的淋巴细胞级分进行fcm分析)。
[1963]
评估a551-mb110/b379-ml0r抗体全身反应的组别详细信息
[1964]
[表67]
[1965][1966]
评价淋巴结和脾脏的器官重量的结果是,当以7.5mg/kg施用ns1-migg1时,观察到器官重量的增加。另一方面,当以0.83mg/kg、2.5mg/kg、7.5mg/kg和22.5mg/kg的任一剂量
施用a551-mb110/b379-ml0r时,未观察到器官增大(图75)。此外,在通过fcm评估的脾脏中t细胞激活的评估中,当a551-mb110/b379-ml0r以任何剂量施用时,未确认ns1-migg1施用后观察到的激活标志物(pd-1、icos、颗粒酶b)的增加(图76)。
[1967]
在评估肝脏中的t细胞激活时,当以7.5mg/kg的剂量施用ns1-migg1时,观察到pd-1和icos的表达均增加。另一方面,当以0.83mg/kg和2.5mg/kg施用a551-mb110/b379-ml0r时,表达被抑制至赋形剂水平,并且当以7.5mg/kg施用a551-mb110/b379-ml0r时,其表达的抑制甚至超过ns1-migg1(图77)。
[1968]
因此,与非转换抗体相比,转换抗体抑制淋巴结、脾脏和肝脏中t细胞的激活。
[1969]
参考实施例7:产生能够增强激动剂活性的修饰的fc
[1970]
(7-1)产生具有增加的fcγr结合活性的变体
[1971]
将以下序列与转换抗体的重链可变区(a375;a372;a356;a486;a488;a489;a548;和a551)或阴性对照抗体的重链可变区(ic17hdk(seq id no:152))进行组合:如wo2017104783中所述增加fcγriib结合活性的重链恒定区tt14(seq id no:149)(重链恒定区,其在包含seq id no:182的fc区中包含t250v/t307p作为氨基酸修饰和l234y/p238d/v264i/a330k作为氨基酸修饰以增加fcγriib结合活性(修饰的位置均在eu编号中)),如wo2017104783中所述的包含引入重链恒定区tt11的g237d氨基酸突变的tt16(seq id no:150),该突变增加fcγriib的结合活性(重链恒定区,在包含seq id no:182的fc区中含有t250v/t307p和l234y/p238d/a330k的氨基酸修饰,作为增加fcγriib结合活性的修饰(修饰的位置均在eu编号中);如wo2014163101中所述的重链恒定区p587(seq id no:151),其增加fcγriib结合活性;p253(seq id no:93),其是预先存在的fcγriib结合增加的重链恒定区与。这产生了具有如下每个恒定区和重链可变区的组合的基因。
[1972]
[表68]
[1973]
全长重链重链可变区(seq id no)重链恒定区(seq id no)a375-tt14a375(seq id no:43)tt14(seq id no:149)a375-tt16a375(seq id no:43)tt16(seq id no:150)a375-p587a375(seq id no:43)p587(seq id no:151)a372-p253a372(seq id no:44)p253(seq id no:93)a356-tt16a356(seq id no:45)tt16(seq id no:150)a356-p587a356(seq id no:45)p587(seq id no:151)a486-p253a486(seq id no:46)p253(seq id no:93)a488-p253a488(seq id no:48)p253(seq id no:93)a489-p253a489(seq id no:49)p253(seq id no:93)a548-p587a548(seq id no:50)p587(seq id no:151)a551-tt16a551(seq id no:51)tt16(seq id no:150)a551-p587a551(seq id no:51)p587(seq id no:151)ic17hdk-tt16ic17hdk(seq id no:152)tt16(seq id no:150)ic17hdk-p587ic17hdk(seq id no:152)p587(seq id no:151)ic17hdk-p253ic17hdk(seq id no:152)p253(seq id no:93)
[1974]
将转换抗体的重链可变区(a375、a356和a551)或阴性对照抗体的重链可变区
(ic17hdk(seq id no:152))与以下序列进行组合:重链恒定区my201(seq id no:153)(重链恒定区,其在包含seq id no:182氨基酸序列的fc区中含有g236n/h268d/a330k作为增加结合fcγriib的活性的氨基酸修饰(修饰位置均在eu编号中)),或my518(seq id no:154)(重链恒定区,其在包含seq id no:182的氨基酸序列的fc区中含有l235w/g236n/h268d/q295l/k326t/a330k作为增强结合fcγriib的活性的氨基酸修饰(修饰位置全部在eu编号中),其在wo 2017104783中进行了描述,并与fcγr具有增加的结合活性;其中k214r修饰已经被引入my201或my518中的重链恒定区my201a(seq id no:155)或my518a(seq id no:156),或其中l235w修饰已被引入my201a中的重链恒定区my201aph(seq id no:157)。这产生了具有如下每个恒定区和重链可变区的组合的基因。
[1975]
[表69]
[1976]
全长重链重链可变区(seq id no)重链恒定区(seq id no)a375-my201apha375(seq id no:43)my201aph(seq id no:157)a375-my518a375(seq id no:43)my518(seq id no:154)a375-my518aa375(seq id no:43)my518a(seq id no:156)a356-my518a356(seq id no:45)my518(seq id no:154)a551-my201aa551(seq id no:51)my201a seq id no:155)a551-my201apha551(seq id no:51)my201aph(seq id no:157)a551-my518a551(seq id no:51)my518(seq id no:154)a551-my518aa551(seq id no:51)my518a(seq id no:156)ic17hdk-my201ic17hdk(seq id no:152)my201(seq id no:153)ic17hdk-my201aphic17hdk(seq id no:152)my201aph(seq id no:157)ic17hdk-my518ic17hdk(seq id no:152)my518(seq id no:154)ic17hdk-my518aic17hdk(seq id no:152)my518a(seq id no:156)
[1977]
如表70所示,通过将上述抗体重链基因与转换抗体的抗体轻链基因(参考实施例5-2和5-3中制备的b040-lamlib、b167-lamlib、b226-lamlib、b223-lamlib、b256-lamlib和b379-lamlib)组合,或与阴性对照抗体的抗体轻链基因(ic17l-k0,通过将轻链可变区ic17l(seq id no:158)与人κ链k0(seq id no:141)作为轻链恒定区组合产生)组合,使用本领域技术人员已知的方法表达和纯化目的抗体。
[1978]
具有增加的fcγr结合活性的变体
[1979]
[表70]
[1980]
[1981][1982]
(7-2)通过恒定区的氨基酸修饰产生具有增加的pi的变体
[1983]
通过将参考实施例7-1中制备的具有增加的fcγr结合活性的重链恒定区与q311r、p343r和d413k组合,产生重链恒定区,其中所述q311r、p343r和d413k是如wo2017046994中描述的增加pi而不大大改变fcγr结合活性的氨基酸突变。
[1984]
具体而言,如下所示,生成了具有导入各抗体重链恒定区中的氨基酸突变的重链恒定区的基因。
[1985]-将p343r/d413k引入my518(seq id no:154):scf025(seq id no:64)
[1986]-将p343r/d413k引入my518a(seq id no:156):scf025a(seq id no:65)
[1987]-将p343r/d413k引入tt14(seq id no:149):scf027(seq id no:66)
[1988]-将p343r/d413k引入tt16(seq id no:150):scf028(seq id no:67)
[1989]-将q311r/p343r引入my518(seq id no:154):scf030(seq id no:68)
[1990]-将q311r/p343r引入tt14(seq id no:149):scf032(seq id no:69)
[1991]-将q311r/p343r引入tt16(seq id no:150):scf033(seq id no:70)
[1992]-将p343r引入my518(seq id no:154):scf039(seq id no:71)
[1993]-将p343r引入my518a(seq id no:156):scf039a(seq id no:72)
[1994]-将d413k引入my518(seq id no:154):scf040(seq id no:73)
[1995]-将p343r引入my201a(seq id no:155):scf041a(seq id no:74)
[1996]-将p343r引入my201aph(seq id no:157):scf041aph(seq id no:75)
[1997]-将d413k引入my201a(seq id no:155):scf042a(seq id no:76)
[1998]-将p343r/d413k引入my201a(seq id no:155):scf043a(seq id no:77)
[1999]-将p343r/d413k引入my201aph(seq id no:157):scf043aph(seq id no:78)
[2000]-将q311r引入my201a(seq id no:155):scf056a(seq id no:79)
[2001]-将q311r引入my201aph(seq id no:157):scf056aph(seq id no:80)
[2002]-将q311r/p343r引入my201a(seq id no:155):scf057a(seq id no:81)
[2003]-将q311r/p343r引入my201aph(seq id no:157):scf057aph(seq id no:82)
[2004]-将q311r/d413k引入my201a(seq id no:155):scf059a(seq idno:83)
[2005]-将q311r/d413k引入my201aph(seq id no:157):scf059aph(seq id no:84)
[2006]-将q311r引入my518a(seq id no:156):scf060a(seq id no:85)
[2007]
通过将此处产生的重链恒定区基因与重链可变区a375(seq id no:43)或a551(seq id no:51)的基因组合,产生如下表71所示抗体重链基因。
[2008]
[表71]
[2009]
全长重链重链可变区(seq id no)重链恒定区(seq id no)a375-scf025a375(seq id no:43)scf025(seq id no:64)a375-scf027a375(seq id no:43)scf027(seq id no:66)a375-scf028a375(seq id no:43)scf028(seq id no:67)a375-scf030a375(seq id no:43)scf030(seq id no:68)a375-scf032a375(seq id no:43)scf032(seq id no:69)a375-scf033a375(seq id no:43)scf033(seq id no:70)a375-scf039a375(seq id no:43)scf039(seq id no:71)a375-scf040a375(seq id no:43)scf040(seq id no:73)a375-scf041apha375(seq id no:43)scf041aph(seq id no:75)a375-scf043apha375(seq id no:43)scf043aph(seq id no:78)a375-scf056apha375(seq id no:43)scf056aph(seq id no:80)a375-scf057apha375(seq id no:43)scf057aph(seq id no:82)a375-scf059apha375(seq id no:43)scf059aph(seq id no:84)a375-scf060aa375(seq id no:43)scf060a(seq id no:85)a551-scf025aa551(seq id no:51)scf025a(seq id no:65)a551-scf039aa551(seq id no:51)scf039a(seq id no:72)a551-scf041aa551(seq id no:51)scf041a(seq id no:74)a551-scf041apha551(seq id no:51)scf041aph(seq id no:75)a551-scf043aa551(seq id no:51)scf043a(seq id no:77)a551-scf043apha551(seq id no:51)scf043aph(seq id no:78)a551-scf056aa551(seq id no:51)scf056a(seq id no:79)
a551-scf056apha551(seq id no:51)scf056aph(seq id no:80)a551-scf057aa551(seq id no:51)scf057a(seq id no:81)a551-scf057apha551(seq id no:51)scf057aph(seq id no:82)a551-scf059aa551(seq id no:51)scf059a(seq id no:83)a551-scf059apha551(seq id no:51)scf059aph(seq id no:84)a551-scf060aa551(seq id no:51)scf060a(seq id no:85)
[2010]
另外,通过将这些抗体重链基因与参考实施例5-3中产生的b167-lamlib、b256-lamlib和b379-lamlib基因作为抗体轻链基因组合,通过本领域技术人员已知的方法如表72所示表达和纯化期望的抗体。
[2011]
[表72]
[2012][2013]
(7-3)产生用于比较激动剂活性的对照抗体
[2014]
产生了抗体(ic17hdk-my201/ic17l-k0;ic17hdk-my201aph/ic17l-k0;ic17hdk-my518/ic17l-k0;ic17hdk-my518a/ic17l-k0;ic17hdk-p253/ic17l-k0;ic17hdk-p587/ic;
ic17hdk-tt16/ic17l-k0)作为比较激动剂活性的对照抗体,其具有参考实施例7-1中产生的重链可变区ic17hdk(seq id no:152)。另外,通过组合抗体轻链ic17l-k0(seq id no:158,可变区;seq id no:141,恒定区)基因与抗体重链基因ic17hdk-g4d的基因,通过本领域已知的方法表达和纯化目的抗体(ic17hdk-g4d/ic17l-k0),其中所述抗体重链基因ic17hdk-g4d的基因是通过将重链可变区ic17hdk(seq id no:152)的基因与g4d基因(seq id no:159)结合而产生的,其中在g4d基因中已去除了人igg4重链恒定区c末端的gly和lys。这些对照抗体用于参考实施例5。
[2015]
(7-4)变体的人fcγ受体结合的评估,其中所述变体通过恒定区的氨基酸修饰而具有增加的pi
[2016]
使用biacore t200(ge医疗)来评估与各自的人fcγ受体(以下称为fcγr)的结合活性。使用50mm磷酸盐、150mm nacl、0.05w/v%-p20,ph 7.4作为缓冲液在25℃进行测量。使用固定有captureselect
tm
人fabλ动力学生物素缀合物(赛默飞世尔科技)的传感器芯片作为配体捕获分子,捕获约1000ru抗体。在测量缓冲液中,将人fcγr的fcγria稀释至8nm,将其他fcγr稀释至1000nm,然后将其与捕获的抗体相互作用。通过使用biacore t200评估软件2.0计算每单位量抗体的fcγr的结合量(ru)来评估每种抗体与fcγr的结合活性。
[2017]
fcγr的胞外域通过以下方法制备。首先,通过本领域技术人员已知的方法进行fcγr的胞外域的基因合成。那时,根据ncbi注册数据制备fcγr序列。具体而言,基于ncbi登录号nm_000566.3生成fcγri的序列,基于ncbi登录号nm_001136219.1生成fcγriia序列,基于ncbi登录号nm_004001.3生成fcγriib序列和基于ncbi登录号nm_001127593.1生成fcγriiia的序列;然后将his标签添加到他们的c末端。fcγriia的多态性位点是通过参考j.exp.med.,1990,172,19-25产生的;fcγriiia的多态性位点是通过参照j.clin.invest.,1997,100,1059-1070而产生的。将得到的基因片段插入动物细胞表达载体中以产生表达载体。将产生的表达载体瞬时导入人胚胎肾细胞来源的freestyle293细胞(invitrogen)中,并表达目的蛋白。收集培养物上清液,然后使其通过0.22μm过滤器,原则上通过以下四个步骤将其纯化。第一步通过阳离子交换柱色谱(sp琼脂糖ff)进行,第二步通过his标签的亲和柱色谱(histrap hp)进行,第三步通过凝胶过滤柱色谱(superdex200)进行,第四步通过无菌过滤进行。但是,对于fcγri,在第一步中使用q琼脂糖ff进行阴离子交换柱色谱。通过使用分光光度计测量在280nm处的吸光度和通过pace等人(蛋白质科学,1995,4,2411-2423)的方法从获得的值中计算的吸光系数来计算纯化蛋白的浓度。
[2018]
表73示出了每单位抗体量的结合量,以及相对于a375-g1t3/b167-lamlib的结合量的量。表73中的所有抗体均示出每单位量的抗体对人fcγriib的结合量大于a375-g1t3/b167-lamlib的结合量,当a375-g1t3/b167-lamlib对人fcγriib的结合量设置为1.0时,结合量相对值是2.85-14.26。在存在或不存在恒定区的用于增加pi的氨基酸修饰的情况下,每单位抗体量的人fcγriib结合量和结合量的相对值相似。而且,与a375-tt14/b167-lamlib相比,包含l235w修饰的抗体对hfcgria的结合量减少。
[2019]
每种人fcγr的结合活性
[2020]
[表73]
[2021][2022]
(7-5)变体的人fcrn结合的评估,其中所述变体通过恒定区的氨基酸修饰而具有增加的pi
[2023]
使用biacore t200(ge医疗)评估对人fcrn的结合活性。使用50mm磷酸盐、150mm nacl、0.05w/v%-p20,ph 6.0作为缓冲液在25℃进行测量。通过wo2010107110中描述的程序制备用于该测定的人fcrn蛋白。使用固定有captureselect
tm
人fabλ动力学生物素缀合物(赛默飞世尔科技)的传感器芯片作为配体捕获分子,捕获了约400ru的抗体,然后结合在测量缓冲液中稀释的人fcrn。通过使用biacore t200评估软件2.0通过稳态模型计算kd(mol/l)来评估各个抗体结合fcrn的活性。在存在或不存在恒定区的用于增加pi的氨基酸修饰的情况下,kd值相似。表74示出了各个抗体对于人fcrn的kd(mol/l)。
[2024]
[表74]
[2025]
缩写名称kd(mol/l)a375-g1t3/b167-lamlib1.27e-06a375-my201a/b167-lamlib1.19e-06a375-my201aph/b167-lamlib1.18e-06a375-my518/b167-lamlib1.27e-06a375-my518a/b167-lamlib1.32e-06a375-tt11/b167-lamlib1.56e-06a375-tt14/b167-lamlib1.77e-06a375-tt16/b167-lamlib1.51e-06a375-p587/b167-lamlib1.70e-06a375-p253/b167-lamlib1.42e-06a375-scf025/b167-lamlib1.10e-06a375-scf025a/b167-lamlib1.13e-06a375-scf027/b167-lamlib1.33e-06a375-scf028/b167-lamlib1.27e-06a375-scf030/b167-lamlib8.63e-07a375-scf032/b167-lamlib9.66e-07a375-scf033/b167-lamlib8.74e-07a375-scf039/b167-lamlib1.09e-06a375-scf039a/b167-lamlib1.11e-06a375-scf040/b167-lamlib1.46e-06a375-scf041a/b167-lamlib1.10e-06a375-scf042a/b167-lamlib1.49e-06a375-scf043a/b167-lamlib1.18e-06a375-scf056a/b167-lamlib9.56e-07a375-scf057a/b167-lamlib9.28e-07a375-scf059a/b167-lamlib1.03e-06a375-scf060a/b167-lamlib1.01e-06a375-scf041aph/b167-lamlib1.13e-06a375-scf043aph/b167-lamlib1.21e-06a375-scf056aph/b167-lamlib1.00e-06
a375-scf057aph/b167-lamlib9.09e-07a375-scf059aph/b167-lamlib1.05e-06
[2026]
参考实施例8:使用4-1bb jurkat报告基因测定,评估经修饰的抗人cd137抗体的体外atp依赖性和adp依赖性cd137激动剂活性
[2027]
gloresponse
tm
nf-κb luc2/4-1bb jurkat细胞系(promega,cs196004)用于测量参考实施例7-2中产生的变体的体外活性(表72)。向384孔板的每个孔中,加入10μl用测定培养基(99%rpmi,1%fbs)制备的浓度为4
×
105/ml的fcγriib cho-k1细胞(promega)。随后,每个孔中加入10μl含adp的抗体溶液或含atp的抗体溶液,或不含atp或adp的抗体溶液。然后,将10μl用测定培养基(99%rpmi,1%fbs)制备为2
×
106/ml的gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系添加到每个孔中。adp的终浓度为10μm,atp的终浓度为10μm。将板在5%co2培养箱中在37℃下静置6小时,在室温下静置15分钟;将30μl bio-glo试剂添加到每个孔中。bio-glo荧光素酶测定系统(缓冲液和底物)用于bio-glo试剂。随后,用酶标仪测量每个孔的发光量。将每个孔的发光值除以不添加抗体的孔的发光值定义为“相对光单位”(倍数诱导),其用作评估每种抗体的cd137激动剂活性的指标。
[2028]
结果在图78中示出。从图78中可以确认,a375-p587/b167-lamlib、a551-p587/b256-lamlib、a551-p587/b379-lamlib、a375-scf041aph/b167-lamlib、a551-scf041aph/b256-lamlib、a551-scf041aph/b379-lamlib、a375-scf043aph/b167-lamlib、a551-scf043aph/b256-lamlib、a551-scf043aph/b379-lamlib、a375-scf057aph/b167-lamlib、a551-scf057aph/b256-lamlib和a551-scf057aph/b379-lamlib以atp和adp依赖性方式示出人cd137激动剂活性。
[2029]
参考实施例9:通过修饰的抗cd137抗体增强激动剂活性
[2030]
(9-1)用于评估的抗体的制备
[2031]
关于将增加pi的各种氨基酸修饰引入到具有增加对fcγriib的结合活性的重链恒定区的情况下,评价这种氨基酸修饰对hcd137ki/mfcγr2bko/hfcγr2btg#90小鼠中cd137激动剂活性以及血浆动力学和药效的影响。首先,如参考实施例7-1、参考实施例7-2和参考实施例7-3中所述,制备a375-my201aph/b167-lamlib、a375-scf041aph/b167-lamlib、a375-scf057aph/b167-lamlib和ic17hdk-my201aph/ic17l-k0。
[2032]
(9-2)使用4-1bb jurkat报告基因测定评估修饰的抗人cd137抗体的体外atp依赖性cd137激动剂活性
[2033]
关于将增加pi的各种氨基酸修饰引入到对fcγriib的结合活性增强的重链恒定区中的情况,为了评估此类氨基酸修饰对cd137激动剂活性的影响,评估了a375-my201aph/b167-lamlib、a375-scf041aph/b167-lamlib、a375-scf057aph/b167-lamlib和ic17hdk-my201aph/ic17l-k0的cd137激动剂活性。
[2034]
使用gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系(promega,cs196004)测量所产生抗体的体外活性。向96孔板的每个孔中,添加用培养基制备的浓度为5x104/ml的200μl fcγriib cho-k1细胞(promega),并将该板在5%co2培养箱中37℃放置过夜。使用cho培养基(90%的ham's f12,10%的fbs)作为培养基。接下来,通过抽吸去除所有培养基,然后将用测定培养基(99%rpmi,1%fbs)以2x106/ml制备的25μl gloresponse
tm
nf-κb-luc2/4-1bb jurkat细胞系添加到每个孔中。接下来,以终浓度为0、0.001、0.01、0.1、1和10μg/ml的
adp的读取缓冲液t(meso scale diagnostics,llc)。通过用sector成像仪(meso scale diagnostics,llc)检测sulfo-tag来测量小鼠血浆中每种抗体的浓度。使用softmax pro(molecular devices)计算小鼠血浆中每种抗体的浓度。
[2045]
结果在图80中示出。a375-scf041aph/b167-lamlib示出比a375-my201aph/b167-lamlib更快的消除。认为这是因为a375-scf041aph/b167-lamlib的重链恒定区引入了增加pi的氨基酸修饰。
[2046]
(9-4)修饰的抗人cd137抗体在小鼠中的药效评估
[2047]
(9-4-1)细胞系和同系肿瘤系移植的小鼠模型的制备
[2048]
作为细胞,使用通过将鸡卵清蛋白(ova)和人磷脂酰肌醇聚糖-3(gpc3)的表达质粒导入小鼠肺癌细胞来源的细胞系llc1[ll/2(别名:llc1),经销商:atcc,目录号:crl-1642]而产生的llc1/ova/gpc3克隆c5(llc1/ova/gpc3)细胞系。将上述(19-3-1)中所述的hcd137ki/mfcγr2bko/hfcγr2btg#90小鼠(11周大,雌性)用作小鼠。将llc1/ova/gpc3细胞系在含有9.8%胎牛血清(sigma-aldrich,co.llc)、0.44mg/ml g418(nacalai tesque,inc.)和0.88mg/ml zeocin(赛默飞世尔科技有限公司)的rpmi1640培养基(sigma-aldrich,co.llc.)中维持和传代。将llc1/ova/gpc3细胞系皮下移植到小鼠的腹部,当肿瘤体积达到约250-500mm3时,认为该模型已形成。模型形成后,将llc1/ova/gpc3细胞系移植小鼠分组,然后分别施用赋形剂和相应的抗人cd137抗体。
[2049]
(9-4-2)待施用药剂的制备和施用以及肿瘤测量
[2050]
在肿瘤移植后第11天和第14天,将用含0.05%吐温20的pbs制备至表76所示剂量的a375-my201aph/b167-lamlib或a375-scf041aph/b167-lamlib施用至llc1/ova/gpc3细胞系移植模型。将含有0.05%吐温20的pbs施用于赋形剂组。将制备的施用液以10ml/kg的剂量通过尾静脉施用。
[2051]
在llc1/ova/gpc3细胞系移植模型中抗肿瘤作用的测量
[2052]
[表76]
[2053][2054][2055]
为了评估抗肿瘤效果,每周测量1至2次肿瘤体积。通过以下方程式计算肿瘤体积。肿瘤体积(mm3)=长度(mm)x宽度(mm)x宽度(mm)/2
[2056]
结果,参考实施例(9-3-2)的结果表明,与a375-my201aph/b167-lamlib相比,施用a375-scf041aph/b167-lamlib的小鼠的血液浓度变化较小。然而,a375-scf041aph/b167-lamlib表现出比a375-my201aph/b167-lamlib更强的抗肿瘤作用(图81)。
[2057]
基于本小鼠模型中的上述结果,通过将增加pi的氨基酸修饰引入重链恒定区增加抗人cd137抗体的抗肿瘤作用。
[2058]
为了帮助清楚理解的目的,已经通过实施例和说明详细地描述了上述发明,并且
这里的描述和说明不应解释为限制本发明的范围。本文通篇引用的专利和科学文献的所有公开内容均明确地通过引用并入本文。
[2059]
[工业适用性]
[2060]
包含本公开的抗cd137抗原结合分子作为活性成分的抗癌剂,组合使用这种包含抗cd137抗原结合结构域作为活性成分的抗癌剂和另一种抗癌剂的组合疗法,用于该组合疗法的药物组合物等,适用于具有免疫细胞激活作用、细胞毒性作用或抗肿瘤作用但对非肿瘤组织(例如正常组织)具有较低的作用或较少的副作用的药物的开发、制造、提供和使用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1