使用鲑鱼油组合物的呼吸治疗的制作方法
使用鲑鱼油组合物的呼吸治疗
1.相关申请的交叉引用
2.本技术要求2020年4月7日提交的美国临时申请号63/006,327和2020年11月17日提交的63/114,960的优先权和权益,其全部公开内容通过全文引用并入本文。
技术领域
3.本公开通常地涉及呼吸治疗,并且更具体地涉及鲑鱼油产品在治疗对类固醇疗法表现出抗性的患者亚组的呼吸病症、疾病或障碍(如哮喘)的用途。
背景技术:
4.炎性是免疫难题。一方面,伴随炎性的生理变化使我们对外部威胁做出急性反应,否则这些威胁将会消灭人。另一方面,慢性炎性,即年龄或外部压力因素使我们的免疫系统处于过度驱动,可导致许多使人衰弱的疾病,从阿尔茨海默氏症到糖尿病和支气管哮喘。
5.嗜酸性粒细胞是一种储存在全身组织中并不断从骨髓中补充的白细胞。嗜酸性粒细胞通常在血液中通常有两天的寿命,但是炎性病症如感染和过敏性疾病将通过嗜酸性粒细胞活化的细胞因子将寿命延长至两周。参见parkym&bochner bs,allergy asthma immunol res.2010,2:87-101。嗜酸性粒细胞计数是测量人体内嗜酸性粒细胞数量的血液测试(test)。通常在常规全血细胞计数测试期间测量的水平升高,表明感染或过敏。
6.在炎性条件下由嗜酸性粒细胞活化细胞因子促进的活化嗜酸性粒细胞是活性氧,细胞毒性蛋白和促炎性细胞因子的主要来源。它们发信号活化常驻组织细胞如上皮细胞,内皮细胞和成纤维细胞,导致炎性和粘液分泌的发展。因此,嗜酸性粒细胞是如支气管哮喘,特应性皮炎和溃疡性结肠炎等疾病的有效活化剂和调节剂。见hogan sp,int arch allergy immunol.2007,143(suppl 1):3-14;simon d等人,allergy.2004,59:561-570;wedemeyer j&vosskuhle k.,best pract res clin gastroenterol.2008,22:537-549。此外,在哮喘患者中,嗜酸性粒细胞颗粒蛋白如嗜酸性粒细胞阳离子蛋白(ecp)和嗜酸性粒细胞过氧化物酶(epo)的水平与哮喘的严重程度密切相关。参见parra a,等人,j investig allergol clin immunol.1999;9:27-34。如在慢性鼻窦炎(crs)受试者中观察到的,上呼吸道的嗜酸性粒细胞炎性也可独立于过敏而发生。参见hutcheson ps,等人,j rhinol allergy.2010,24:405-408。此类个体代表了一个独特的亚组,其对药物和手术干预具有广泛抗性,并且可通过靶向嗜酸性粒细胞扩增和效应器功能的治疗显示出直接的益处。
技术实现要素:
7.在一些方面,本文提供了使用鲑鱼油的呼吸治疗,如哮喘治疗。在一些实施方式中,所述哮喘是支气管哮喘。在某些实施方式中,所提供的治疗靶向对药物和手术干预(包含类固醇疗法)具有广泛抗性的患者亚组。
8.在某些方面,提供了用于治疗有需要的人的炎性病症,障碍或疾病的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组
合物以治疗炎性病症,障碍或疾病。
9.在某些方面,提供了用于治疗有需要的人的呼吸病症,障碍或疾病的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以治疗炎性病症,障碍或疾病。
10.在本文提供的方法的一些变型中,所治疗的病状,病症或疾病是嗜酸性粒细胞病症,障碍或疾病。在一些实施方式中,炎性病症,障碍或疾病是嗜酸性粒细胞炎性病症,障碍或疾病。在一些实施方式中,呼吸病症,障碍或疾病是嗜酸性粒细胞呼吸病症,障碍或疾病。
11.在某些方面,提供了用于在有需要的人中降低嗜酸性粒细胞效应器功能的方法,其包括向所述人施用包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以降低嗜酸性粒细胞效应器功能。
12.在前述方面的一些实施方式中,所述鲑鱼油是酶提取的鲑鱼油。在某些变型中,鲑鱼油是从鲑鱼的下脚料的温和酶水解获得的。
13.在本文提供的方法的一些实施方式中,组合物是口服施用的。一些变型中,组合物是吸入的。一些变型中,组合物是经鼻施用的。一些变型中,组合物是注射的。一些变型中,组合物是局部施用的。
14.在某些方面,还提供了包含至少一种本文所述的生物活性物质的鲑鱼油组合物。在某些方面,提供了包含至少一种从鲑鱼油中分离出来的生物活性物质的组合物。在另一方面,提供了这样的组合物用于治疗本文所述的各种病症,障碍或疾病的用途。
15.在其他方面,提供了一种制品,其包含:包含组合物的容器,所述组合物包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质;以及标签,其包含该组合物的使用说明。
16.在其它方面,提供了试剂盒,其包含:鲑鱼油组合物或包含至少一种从鲑鱼油中分离组合物的生物活性物质的组合物的剂型;以及包装插页(package insert),其包含使用该组合物的使用说明。
17.在前述方面的一些变型中,剂型是糖浆剂,咀嚼剂,胶囊剂或软凝胶剂。
附图说明
18.通过结合附图参考以下描述可以理解本技术。
19.图1和3描述了在不同预处理条件下pmnl的形状变化(100%作为基线)作为ccl11浓度的函数。
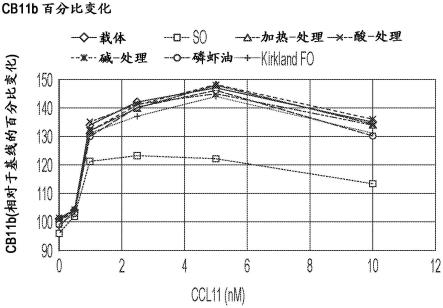
20.图2和4描绘了在不同预处理条件下pmnl表面上cb11b变化(100%作为基线)作为ccl11浓度的函数。
具体实施方式
21.以下描述阐述了示例性方法,参数等。然而,应当认识到,这种描述并不旨在限制本公开的范围,而是作为示例性实施例的描述而提供。
22.在一些方面,本文提供了通过口服施用鲑鱼油组合物来治疗有需要的人的炎性病症,障碍或疾病的方法。
23.鲑鱼油组合物及其生产方法
24.在一些实施方式中,在本文提供的方法中施用的组合物是鲑鱼油组合物。鲑科属
于鲑目中的鱼科,并且包含例如鲑鱼、鳟鱼、鲫鱼、淡水白鱼和茴鱼。
25.在一些方面,鲑鱼油组合物包含酶提取的鲑鱼油。一些变型中,酶提取的鲑鱼油是从鲑鱼的下脚料的温和酶水解获得的。在一些变型中,鲑鱼油组合物是天然的,未精炼的并且从鲑鱼中温和释放。一些变型中,生产鲑鱼油组合物的方法不使用或不需要使用化学品,溶剂,高压或加热。
26.本文所述方法中使用的鲑鱼油组合物通过温和酶水解制备,其不需要苛刻的化学品、分馏、再酯化、冬化、高压和/或加热。例如,在一些变型中,用于本文所述方法中的鲑鱼油组合物通过酶水解制备,不需要使用强酸或强碱(例如,包括3n或更高的酸或碱)、分馏、再酯化、冬化、至少30psi的压力或在至少130℃的温度下加热来制备。使用本文所述温和酶水解条件通常比本领域常用生产鲑鱼油的技术更温和,例如分馏或“冷压”加工,其包含使用强酸或强碱、分馏、再酯化、冬化、高压和/或加热。当使用如本文所述的温和酶水解时,所得组合物具有出人意料地有益于治疗与嗜酸性粒细胞或嗜酸性粒细胞功能障碍相关的病症的生物活性组分。
27.在一些实施方式中,产生鲑鱼油组合物的酶水解方法使用少于3n,少于2.5n,少于2n,少于1.5n,少于1n,少于0.5n,少于0.1n,少于0.01n或少于0.001n的酸。在一些实施方式中,酶水解方法不使用或不需要使用任何额外的酸。在前述的一些变型中,酸是强酸。在前述的一些变型中,酸是hcl或hno3,或其任何组合。
28.在一些实施方式中,生产鲑鱼油组合物的方法使用少于3n,少于2.5n,少于2n,少于1.5n,少于1n,少于0.5n,少于0.1n,少于0.01n或少于0.001n的碱。在一些实施方式中,所述方法不使用或不需要使用任何额外的碱。在前述的一些变型中,碱是强碱(例如naoh和/或kcl)。
29.在一些实施方式中,从温和酶水解获得的鲑鱼油不与或不要求与3n或更高浓度,2.5n或更高浓度,2n或更高浓度,1.5n或更高浓度,1n或更高浓度,0.5n或更高浓度,0.1n或更高浓度,0.01n或更高浓度,或0.001n或更高浓度的酸混合。在前述的一些变型中,酸是强酸(例如hcl和/或hno3)。
30.在一些实施方式中,从温和酶水解获得的鲑鱼油不与或不要求与3n或更高,2.5n或更高,2n或更高,1.5n或更高,1n或更高,0.5n或更高,0.1n或更高,0.01n或更高,或0.001n或更高浓度的碱混合。在前述的一些变型中,碱是强碱(例如naoh和/或koh)。
31.在一些实施方式中,每克酶提取的鲑鱼油加入少于3mmol,少于2.5mmol,少于2mmol,少于1.5mmol,少于1mmol,少于0.5mmol,少于0.1mmol,少于0.01mmol或少于0.01mmol的酸或h
+
。在一些实施方式中,不向酶提取的鲑鱼油中加入或不要求加入酸或h
+
。
32.在一些实施方式中,每克酶提取的鲑鱼油加入少于3mmol,少于2.5mmol,少于2mmol,少于1.5mmol,少于1mmol,少于0.5mmol,少于0.1mmol,少于0.01mmol或少于0.01mmol碱或oh
-
,小于6mmol。在一些实施方式中,不向酶提取的鲑鱼油中加入或不要求加入碱或oh
-
。
33.在一些实施方式中,在酶水解以产生本文方法中使用的鲑鱼油期间或之后不加入或不要求加入酸。在一些实施方式中,在酶水解期间或之后加入少于3n,少于2.5n,少于2n,少于1.5n,少于1n,少于0.5n,少于0.1n,少于0.01n或少于0.001n的酸。在前述的一些变型中,酸是强酸(例如hcl和/或hno3)。
34.在一些实施方式中,在酶水解以产生本文方法中使用的鲑鱼油的过程中或之后不加入或不要求加入任何碱。在一些实施方式中,在酶水解期间或之后加入少于3n,少于2.5n,少于2n,少于1.5n,少于1n,少于0.5n,少于0.1n,少于0.01n或少于0.001n的碱。在一些实施方式中,碱是强碱(例如naoh和/或koh)。
35.在一些实施方式中,生产鲑鱼油组合物的方法在低于130℃,低于120℃,低于110℃,低于100℃,低于90℃,低于80℃,低于70℃,低于60℃,低于55℃,低于50℃,低于45℃,低于40℃,低于35℃,低于30℃或低于25℃的温度下进行。在一些实施方式中,将酶水解期间或之后的温度维持在低于130℃,低于120℃,低于110℃,低于100℃,低于90℃,低于80℃,低于70℃,低于60℃,低于55℃,低于50℃,低于45℃,低于40℃,低于35℃,低于30℃或低于25℃。
36.在一些实施方式中,由温和酶水解获得的鲑鱼油不暴露于或不要求暴露于150℃或更高,140℃或更高,130℃或更高,120℃或更高,110℃或更高,100℃或更高,90℃或更高,80℃或更高,70℃或更高,60℃或更高,55℃或更高,50℃或更高,45℃或更高,40℃或更高,35℃或更高,30℃或更高,或25℃或更高的温度。
37.在一些实施方式中,生产鲑鱼油组合物的方法在低于2atm,低于1.5atm,低于1.4atm,低于1.3atm,低于1.2atm,低于1.1atm,或处于或约1.0atm的压力下进行。在一些实施方式中,生产鲑鱼油组合物的方法在低于30psi,低于25psi,低于20psi,低于15psi,或处于或约14.7psi的压力下进行。
38.在一些实施方式中,酶水解期间或之后的压力维持在2atm以下,1.5atm以下,1.4atm以下,1.3atm以下,1.2atm以下,1.1atm以下,或1.0atm或约1.0atm。在一些实施方式中,在酶水解期间或之后的压力维持在30psi以下,25psi以下,20psi以下,15psi以下,或14.7psi或约14.7psi。
39.在一些实施方式中,酶提取的鲑鱼油不暴露于或不要求暴露于大于2atm,大于1.5atm,大于1.4atm,大于1.3atm,大于1.2atm,大于1.1atm或大于1.0atm。在一些实施方式中,酶提取的鲑鱼油不暴露于或不要求暴露于大于30psi,大于25psi,大于20psi,大于15psi或大于14.7psi。
40.在一些实施方式中,本文提供的鲑鱼油是在不使用以下方法(processes)或条件(conditions)中的一种或多种的情况下生产的:(i)与3n或更高浓度的酸混合;(ii)与3n或更高浓度的碱混合;(iii)分馏;(iv)再酯化;(v)冬化;(vi)130℃或更高的温度;或(vi)2atm或更高的压力。在一些变型中,本文提供的鲑鱼油是在不使用任何上述方法或条件的情况下生产的。
41.在某些变型中,获得鲑鱼油组合物的方法包括使用含有相对脂肪酶活性低于一定百分比(例如,小于1%或小于0.5%)的蛋白酶,从屠宰起小于一定时长(例如,从屠宰起小于24小时长)的下脚料原料,和/或在酶水解期间涡轮混合(turbine mixing)。这允许定量提取在整条鱼中发现的所有脂质成分,而最小化至没有损失次要的、非脂肪酸的生物活性成分。
42.此外,使用具有低脂肪酶活性的酶使混合物中游离脂肪酸分子的量最小化,其中这些游离脂肪酸分子可以降解生物活性成分和/或以其促氧化特性缩短鲑鱼油的保质期。因此,使用具有低脂肪酶活性的酶,相对新鲜的下脚料原料,和涡轮混合以缩短酶水解的时
间,所有这些都有助于产生对嗜酸性粒细胞功能具有最大影响的鲑鱼油。
43.在一些实施方式中,生产鲑鱼油组合物的方法包含使用含有小于3%、小于2%、小于1%、小于0.9%、小于0.8%、小于0.7%、小于0.6%、小于0.5%、小于0.4%、小于0.3%、小于0.2%、小于0.15%、小于0.1%、小于0.05%或小于0.01%脂肪酶活性的酶。在一些实施方式中,鲑鱼的下脚料的温和酶水解包含使用具有小于3%、小于2%、小于1%、小于0.9%、小于0.8%、小于0.7%、小于0.6%、小于0.5%、小于0.4%、小于0.3%、小于0.2%、小于0.15%、小于0.1%、小于0.05%或小于0.01%脂肪酶活性的酶。
44.在一些实施方式中,酶提取的鲑鱼油包含小于3%、小于2.5%、小于2%、小于1.5%、小于1%、小于0.9%、小于0.8%、小于0.7%、小于0.6%、小于0.5%、小于0.4%、小于0.3%、小于0.2%、小于0.1%、小于0.05%或小于0.01%的游离脂肪酸。在一些实施方式中,酶提取的鲑鱼油包含小于3%、小于2.5%、小于2%、小于1.5%、小于1%、小于0.9%、小于0.8%、小于0.7%、小于0.6%、小于0.5%、小于0.4%、小于0.3%、小于0.2%、小于0.1%、小于0.05%或小于0.01%的游离脂肪酸,而不经历冬化或再酯化。在一些实施方式中,酶提取的鲑鱼油包含少于0.5%的游离脂肪酸,而不经历冬化或再酯化。
45.在一些实施方式中,本文所述的酶提取的鲑鱼油是从在鲑鱼屠宰后少于1小时、少于2小时、少于3小时、少于4小时、少于5小时、少于6小时、少于7小时、少于8小时、少于9小时、少于10小时、少于11小时、少于12小时、少于24小时、少于36小时、少于48小时、2-6小时、4-8小时、6-10小时或2-10小时的鲑鱼制备。
46.在一个实施方式中,鲑鱼油组合物是鲑鱼油,鲑鱼油或鲑鱼油,它们中的每一种都是可从hofseth biocare asa商购的酶提取的鲑鱼油的变体。
47.出乎意料地观察到在鱼油中发现的甘油三酯或磷脂形式的常见脂肪酸不负责降低嗜酸性粒细胞效应器功能。相反,正是本文所述鲑鱼油组合物中存在的某些次要的、具有生物活性的成分才有这种作用。
48.在某些实施方式中,鲑鱼油组合物中的生物活性成分包含少量脂肪酸甘油三酯组分。一些变型中,生物活性组分包含饱和酸。在某些变型中,生物活性组分包含己酸、辛酸、癸酸、月桂酸、山嵛酸或二十四烷酸或其任何组合。
49.在一些变型中,鲑鱼油组合物中的生物活性成分包含单不饱和酸。在某些变型中,生物活性组分包含肉豆蔻烯酸(myristoleic acid),十七碳烯酸、反油酸、鳕油酸、芥酸、巴西烯酸(brassidic acid)和/或神经酸。
50.一些变型中,鲑鱼油组合物中的生物活性成分包含多不饱和酸。在某些变型中,生物活性组分包含γ亚麻酸、哥伦比亚酸(columbinic acid)、十八碳四烯酸、二十碳三烯酸和/或二高γ亚麻酸。
51.在其它变型中,鲑鱼油组合物中的生物活性成分包含小有机分子。在一些变型中,生物活性组分包含萜烯(例如,藁本内酯)、倍半萜烯(例如,大根香叶烯)、酚类(例如、百里酚、丁子香酚、香芹酚)、醇类(例如,芳樟醇、香茅醇、萜品醇)、倍半萜醇(例如,红没药醇(bisabolol)、檀香醇)、酮(例如,侧柏酮、松莰酮(pinacamphone)、斜立酮(italidone))、酯(例如,乙酸芳樟酯、乙酸香叶酯、甲酸香茅酯)、内酯和香豆素(例如,心菊内酯(helenalin)、土木香、呋喃香豆素)、醚(例如,萎叶酚)、类固醇衍生物(例如,谷甾醇、豆甾
醇)、和/或苯酞衍生物(例如,3-亚丁基-4,5-二氢苯酞)。
52.在一些变型中,鲑鱼油组合物中的生物活性成分包含脂肽。在一些变型中,生物活性组分包含直链和/或环状脂肽。在某些变型中,生物活性成分包含伊枯草菌素a、全息酰胺(hoiamides)、海洛内酰胺(heronamides)、拉沙霉素(laxaphycin)、安帕酰胺(apramides)、龙酰胺(dragonamides)、盖格四烯菌素(gageotetrins)、鞘丝藻贝林(lyngbyabellins)、环丁西丁素(cyclodycidin)、帕尔格琳(parguerine)、普米酸丁(pumilacidin)、磺基脂肽(sulforeido脂肽)、丰原素、甲巴酰胺、微球菌素(microcolin)、青霉酰胺、磺基糖脂、卤代尔(halovir)、卡海拉利和/或促吞噬素。
53.在一些变型中,鲑鱼油组合物中的生物活性成分包含线性脂肽。在某些变型中,鲑鱼油组合物中的生物活性成分包含微球菌素a。在一个变型中,鲑鱼油组合物包含浓度为至少5μg/ml,至少10μg/ml,至少20μg/ml,或至少25μg/ml,或在5μg/ml至100μg/ml之间,在10μg/ml至100μg/ml之间,或在20μg/ml至75μg/ml之间的微球菌素a。
54.在其它变型中,鲑鱼油组合物中的生物活性成分包含一种或多种保护素。
55.在其它变型中,鲑鱼油组合物中的生物活性成分包含一种或多种脂氧素。
56.在上述生物活性组分的一些变型中,化合物可以以盐形式存在。在某些变型中,化合物可以以其任何组合存在。
57.病症、疾病或障碍
58.在一些方面,本文提供的鲑鱼油组合物可用于治疗包含呼吸病症,障碍或疾病的炎性病症,障碍或疾病。在一些实施方式中,所述病症,障碍或疾病是呼吸道炎性。在一些方面,提供了用于治疗有需要的人的炎性病症,障碍或疾病的方法,其包含向人施用本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物。
59.在一些变型中,“治疗/处理(treatment)”或“治疗/处理(treating)”是用于获得有益的或期望的结果(包含临床结果)的方法。有益或期望的临床结果可包含以下一项或多项:
60.(i)减少由病症、疾病或障碍引起的一种或多种症状;
61.(ii)减少疾病的程度和/或稳定病症、疾病或障碍(例如,延迟
62.病症、疾病或障碍的恶化);
63.(iii)延迟所述病症、疾病或障碍的传播;
64.(iv)延迟或减缓所述病症、疾病或障碍的复发和/或所述病症、疾病或障碍的进展;
65.(v)改善疾病状态和/或提供病症、疾病或障碍的缓解(无论是部分或全部)和/或降低治疗病症、疾病或障碍所需的一种或多种其它药物的剂量;
66.(vi)提高生活质量;和/或
67.(vii)延长生存期。
68.在一些实施方式中,本文提供的鲑鱼油组合物可用于治疗哮喘,肺炎,支气管扩张,肺气肿,肺结核,肺萎陷,肺纤维化,纤维化肺泡炎,慢性阻塞性肺病(copd),过敏性鼻炎,慢性鼻窦炎(crs)和/或急性呼吸系统疾病综合征。
69.在一些实施方式中,所述病症、疾病或障碍是慢性炎性障碍。在某些实施方式中,慢性炎性障碍是气道的慢性炎性病症。在某些变形中,所述病症、疾病或障碍是炎性肺病。
在一些变型中,病症、疾病或障碍涉及气道变窄和/或肿胀,从而使呼吸困难并引发咳嗽,喘鸣和/或呼吸短促。在某些变型中,所述病症、疾病或障碍是哮喘。在某些变型中,哮喘是支气管哮喘。在一个变形中,所述病症、疾病或障碍涉及类固醇治疗抗性哮喘和气道狭窄。
70.在其它实施方式中,所述病症、疾病或障碍是过敏或过敏性炎性。
71.在其它实施方式中,所述病症、疾病或障碍是病毒性呼吸道疾病。在一些变型中,病症、疾病或障碍是严重急性呼吸综合征。在某些变型中,严重急性呼吸综合征由冠状病毒引起。
72.在一些变型中,有需要的人是肺功能不全个体。在某些变型中,肺功能不全的个体在肺部的肺泡中积聚液体。由于肺泡中的保护膜的破坏,该液体可以从肺中的最小血管泄漏到肺泡中。由于严重的疾病或损伤引起的免疫应答的中断,通常在血管中保持这种液体的膜可能被破坏。液体进入肺泡并防止肺充满足够的空气,这意味着较少的氧气到达血流。这剥夺了器官的功能所需的氧,其可造成导致死亡的多器官衰竭。
73.在一个实施方式中,提供了用于治疗有需要的住院肺功能不全的人的方法,其包含向人施用本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物分离的生物活性物质的组合物以减少或延迟向人提供辅助呼吸的需要。
74.一些变型中,“延迟”病症、疾病或障碍的发展意指推迟、阻碍、减缓、延迟、稳定和/或推迟病症、疾病或障碍的发展。这种延迟可以具有不同的时间长度,这取决于病症、疾病或障碍和/或被治疗的个体的病史。
75.在前述的一些变型中,所治疗的病症,障碍或疾病是嗜酸性粒细胞病症,障碍或疾病。
76.在其它方面,本文提供的鲑鱼油组合物通过降低嗜酸性粒细胞效应器功能改善抗炎功效。因此,在某些实施方式中,提供了用于在有需要的人中降低嗜酸性粒细胞效应器功能的方法,其包含向人施用本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物以降低嗜酸性粒细胞效应器功能。
77.亚患者人群
78.在一些实施方式中,本文提供的方法涉及治疗有需要的人。在某些实施方式中,人对用于治疗本文所述的炎性病症,障碍或疾病的药物和手术干预具有广泛抗性。在一个实施方式中,人表现出或具有对类固醇疗法的抗性。例如,在一个变体中,人患有类固醇治疗抗性哮喘。
79.在前述的一些变型中,人是儿童。在某些变型中,人小于18岁,小于12岁,小于10岁,小于5岁,小于2岁,或小于1岁;或在2岁和12岁之间。
80.制剂
81.在一些实施方式中,本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物是为口服施用制剂。适于口服施用的形式可包含例如片剂、丸剂、胶囊剂、扁囊剂、糖衣丸、锭剂、液体剂、凝胶剂、糖浆剂、浆液、酏剂、混悬剂、气雾剂或散剂。
82.在某些实施方式中,本文所述的药物组合物为糖浆剂,胶囊剂和软凝胶剂(包含例如咀嚼胶)的形式。
83.配制和施用组合物的技术可参见remington
′
s pharmaceutical sciences,
18thed.,mack publishing co,easton,pa.,1990。本文所述的药物组合物可以使用任何常规方法制备,例如混合,溶解,制粒,制糖衣丸,研磨,乳化,封装,包埋,熔纺,喷雾干燥或冻干方法。最佳药物制剂可由本领域技术人员根据给药途径和所需剂量来确定。此类制剂可影响所施用药剂的物理状态,稳定性,体内释放速率和体内清除速率。
84.在一些变型中,本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物作为单位剂量施用于人,例如以本文所述的糖浆,胶囊和软凝胶(包含例如咀嚼胶)的形式。在一个变型中,“单位剂型”是指物理上离散的单位,适合作为单位剂量,每个单位含有预定量的本文提供的鲑鱼油组合物,或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物的组合物,其可以在药学上可接受的载体中。
85.如本文所用,“药学上可接受的”是指在生物学或其它方面不是不合需要的材料,例如,可将所述材料掺入施用于个体的药物组合物中,而不引起明显的不合需要的生物效应或以有害方式与包含材料的组合物的任何其它组分相互作用。因此,在一些实施方式中,药学上可接受的载体或赋形剂优选满足毒理学和制造测试和/或包含在由美国食品和药品管理局编制的非活性成分指南上的所需标准。
86.在一些实施方式中,配制本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物的组合物用于吸入。适于吸入的形式可包含例如干粉,非水性液体制剂或液体制剂(例如用于喷雾)。
87.在一些实施方式中,配制本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物分离的生物活性物质的组合物用于注射。在一些实施方式中,适于注射的制剂可包含一种或多种水性或非水性载体,一种或多种抗微生物剂,一种或多种抗氧化剂,一种或多种缓冲剂,一种或多种填充剂(bulking agent),一种或多种螯合剂,一种或多种增溶剂,一种或多种表面活性剂和/或一种或多种张度剂(tonicity agent)。
88.在一些实施方式中,本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物被配制用于局部施用。适于局部施用的形式可包含例如溶液,洗剂,乳膏,软膏,凝胶,糊剂,气溶胶泡沫或喷雾剂,粉末,固体或透皮贴剂。在一些实施方式中,适于局部施用的制剂可包含水,油,醇,丙二醇,一种或多种防腐剂,一种或多种乳化剂,一种或多种吸收促进剂和/或一种或多种香料。
89.在一些实施方式中,本文提供的鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物经口服、吸入、注射施用或局部施用。
90.剂量
91.在一些实施方式中,提供的方法包含向有需要的人施用有效量的鲑鱼油组合物,或包含从本文提供的鲑鱼油组合物中分离的生物活性物质的组合物。在一些变型中,“有效量”是指在给定治疗形式中应有效的本发明组合物或生物活性物质的量。在某些变型中,本文提供的鲑鱼油组合物或包含从鲑鱼油中分离组合物的生物活性物质的组合物的有效量是足以降低人中嗜酸性粒细胞效应器功能的量,从而治疗患有本文所述的病症、疾病或障碍的人,或减轻此类病症、疾病或障碍的现有症状。
92.在一些变型中,本文提供的鲑鱼油组合物对于人的示例性剂量水平可以为每天4g至10g,或每天4g至6g。
93.在一些变型中,本文提供的用于人的从鲑鱼油中分离组合物的生物活性物质的示
例性剂量水平可为10mg至1000mg。
94.最终的剂量方案由主治医师根据良好的医疗实践,考虑改变本文提供的鲑鱼油组合物或包含从鲑鱼油中分离组合物的生物活性物质的组合物的作用,疾病状态的特性和严重程度,受试者的反应性,受试者的年龄,状况,体重,性别和饮食以及任何感染的严重程度的各种因素来确定。可考虑的其它因素包含给药时间和频率,药物组合,反应敏感性和对治疗的耐受性/反应。适于涉及本文提及的任何制剂的治疗的剂量的进一步改进由熟练的从业者常规地进行而不伴随过度的实验,尤其是根据公开的剂量信息和测定,以及在人体临床试验中观察到的药代动力学数据。
95.有效量可以是一个或多个剂量,即,可能需要单剂量或多剂量以达到期望的治疗终点。在某些实施方式中,鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物每天施用一次,两次或三次。在某些实施方式中,所述鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物每天施用一次或两次。在某些实施方式中,鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物质的组合物每天施用一次。
96.制品和试剂盒
97.可制备可以在一种或多种药学上可接受的载体,赋形剂或其它成分中配制的鲑鱼油组合物,或包含从本文提供的鲑鱼油组合物中分离出来的生物活性物的组合物,置于合适的容器中,并标记用于治疗指定的病症、疾病或障碍。因此,在某些方面,还提供了制品,例如包含鲑鱼油组合物或包含从本文提供的鲑鱼油组合物中分离的生物活性物质的组合物的剂型的容器,以及包含此类组合物或活性物质的使用说明的标签。
98.在一些实施方式中,制品是包含鲑鱼油组合物或包含分离自本文提供的鲑鱼油组合物的生物活性物质的组合物和一种或多种药学上可接受的载体,赋形剂或其它成分的剂型的容器。在本文所述制品的一个实施方式中,剂型是糖浆剂,胶囊剂和软凝胶剂(包含例如可咀嚼的口香糖)。
99.在某些方面,还提供了试剂盒。例如,在一些实施方式中,试剂盒可包含鲑鱼油组合物从本文提供的鲑鱼油组合物分离的生物活性物质的组合物的剂型,使用组合物/活性物质治疗病症、疾病或障碍的说明书的包装插页。试剂盒中的使用说明书可以是用于治疗呼吸炎性(respiratory inflammation)或呼吸道炎性(inflammation of the respiratory tract),包含例如哮喘。在一个变型中,试剂盒中的使用说明书可以是用于治疗支气管哮喘。在另一个变体中,试剂盒中的使用说明书可以是用于治疗严重急性呼吸综合征。
100.制品和试剂盒的标签和包装插页分别包含用于治疗本文所述的任何病症、疾病或障碍的说明书。在一些实施方式中,标签包含用于治疗炎性病症,障碍或疾病的说明书,包含呼吸病症,障碍或疾病。在一些变型中,标签包含用于治疗气道的慢性炎性障碍的说明书。在一个变型中,标签包含用于治疗哮喘(例如支气管哮喘和/或类固醇治疗抗性哮喘)的说明书,。在其它实施方式中,标签包含治疗病毒性呼吸疾病的说明书,例如严重急性呼吸综合征(包含例如由冠状病毒引起的严重急性呼吸综合征)。
101.应当理解,本文所述的任何鲑鱼油组合物或包含从鲑鱼油中分离组合物的生物活性物质的组合物,以及本文所述的任何病症、疾病或障碍,可以与本文所述的制品和试剂盒
的各种实施方式一起使用。
102.列举的实施方式
103.以下列举的实施方式代表本发明的一些方面。
104.1.一种治疗有需要的人的炎性病症,障碍或疾病的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以治疗炎性病症,障碍或疾病。
105.2.一种治疗有需要的人的嗜酸性粒细胞炎性病症,障碍或疾病的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以治疗所述嗜酸性粒细胞炎性病症,障碍或疾病,
106.其中所述鲑鱼油是从鲑鱼类的下脚料的温和酶水解获得的,和/或
107.其中所述鲑鱼油是在不使用以下方法(processes)或条件中的一种或多种的情况下生产的:
108.(i)与3n或更高浓度的酸混合;
109.(ii)与3n或更高浓度的碱混合;
110.(iii)分馏;
111.(iv)再酯化;
112.(v)冬化;
113.(vi)130℃或更高的温度;或
114.(vi)2atm或更高的压力。
115.3.根据实施方式1或2所述的方法,其中所述炎性病症,障碍或疾病是气道的慢性炎性病症。
116.4.根据实施方式1或2所述的方法,其中所述炎性病症,障碍或疾病是哮喘。
117.5.根据实施方式1或2所述的方法,其中所述炎性病症,障碍或疾病是支气管哮喘。
118.6.根据实施方式1至5中任一项所述的方法,其中所述炎性病症,障碍或疾病是嗜酸性粒细胞炎性病症,障碍或疾病。
119.7.一种用于治疗有需要的人的呼吸病症,障碍或疾病的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以治疗炎性病症,障碍或疾病。
120.8.一种治疗有需要的人的嗜酸性粒细胞呼吸病症,障碍或疾病的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以治疗嗜酸性粒细胞呼吸病症,障碍或疾病,
121.其中所述鲑鱼油是从鲑鱼类的下脚料的温和酶水解获得的,和/或
122.其中所述鲑鱼油是在不使用以下方法或条件中的一种或多种的情况下生产的:
123.(i)与3n或更高浓度的酸混合;
124.(ii)与3n或更高浓度的碱混合;
125.(iii)分馏;
126.(iv)再酯化;
127.(v)冬化;
128.(vi)130℃或更高的温度;或
129.(vi)2atm或更高的压力。
130.9.根据实施方式7或8所述的方法,其中所述呼吸病症,障碍或疾病是病毒性呼吸疾病。
131.10.根据实施方式7或8所述的方法,其中所述呼吸病症,障碍或疾病是严重急性呼吸综合征。
132.11.根据实施方式10所述的方法,其中所述严重急性呼吸综合征由冠状病毒引起。
133.12.根据实施方式7至11中任一项所述的方法,其中所述呼吸病症,障碍或疾病是嗜酸性粒细胞呼吸病症,障碍或疾病。
134.13.一种用于在有需要的人中降低嗜酸性粒细胞效应器功能的方法,其包含:向所述人施用包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以降低嗜酸性粒细胞效应器功能。
135.14.一种在有需要的人中降低嗜酸性粒细胞效应器功能的方法,其包括:向所述人施用有效剂量的包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物以治疗嗜酸性粒细胞呼吸病症,障碍或疾病,
136.其中所述鲑鱼油从鲑鱼类的下脚料的温和酶水解获得的,和/或
137.其中所述鲑鱼油是在不使用以下方法或条件中的一种或多种的情况下生产的:
138.(i)与3n或更高浓度的酸混合;
139.(ii)与3n或更高浓度的碱混合;
140.(iii)分馏;
141.(iv)再酯化;
142.(v)冬化;
143.(vi)130℃或更高的温度;或
144.(vi)2atm或更高的压力。
145.15.根据前述实施方式中任一项所述的方法,其中所述组合物是口服施用的。
146.16.根据前述实施方式中任一项所述的方法,其中所述组合物是吸入的。
147.17.根据前述实施方式中任一项所述的方法,其中所述组合物是经鼻施用的。
148.18.根据前述实施例中任一项所述的方法,其中所述组合物是注射的。
149.19.根据前述实施方式中任一项所述的方法,其中所述组合物是局部施用的。
150.20.根据前述实施例中任一项所述的方法,其中所述人对用于治疗所述病症、障碍或疾病的药物和手术干预具有广泛抗性。
151.21.根据前述实施方式中任一项所述的方法,其中所述人表现出或具有对类固醇治疗的抗性。
152.22.根据前述实施方式中任一项所述的方法,其中所述人患有类固醇治疗抗性哮喘。
153.23.根据前述实施方式中任一项所述的方法,其中包含鲑鱼油的所述组合物的有效剂量为每天4g至6g。
154.24.根据前述实施方式中任一项所述的方法,其中所述包含至少一种从鲑鱼油中分离的生物活性物质的组合物的有效剂量为每天10mg至1000mg。
155.25.根据前述实施方式中任一项所述的方法,其中向人施用所述组合物减少或延
迟向人提供辅助呼吸的需要。
156.26.根据前述实施方式中任一项所述的方法,其中所述鲑鱼油是酶提取的鲑鱼油。
157.27.前述实施方式中任一项的方法,其中所述鲑鱼油从鲑鱼类的下脚料的温和酶水解获得的。
158.28.根据实施方式27所述的方法,其中所述温和酶水解使用具有小于1%脂肪酶活性的酶。
159.29.根据前述实施方式中任一项所述的方法,其中所述鲑鱼油包含少于0.5%的游离脂肪酸。
160.30.根据前述实施方式中任一项所述的方法,其中所述鲑鱼油包含微球菌素。
161.31.根据前述实施方式中任一项所述的方法,其中所述鲑鱼油包含微球菌素a。
162.32.根据前述实施方式中任一项所述的方法,其中所述鲑鱼油还包含:
163.(i)己酸、辛酸、癸酸、月桂酸、山嵛酸、二十四烷酸、肉豆蔻烯酸、十七碳烯酸、反油酸、鳕油酸、芥酸、巴西烯酸、神经酸、γ亚麻酸、哥伦比亚酸、十八碳四烯酸、二十碳三烯酸或二高γ亚麻酸、或其任何组合;
164.(ii)藁本内酯、大根香叶烯、百里酚、丁子香酚、香芹酚、芳樟醇、香茅醇、萜品醇、红没药醇(bisbalol)、檀香醇、侧柏酮(thujone)、松莰酮(pinacamphone)、斜立酮(italidone)、乙酸芳樟酯、乙酸香叶酯、甲酸香茅酯、心菊内酯(helenalin)、土木香、呋喃香豆素、萎叶酚、谷甾醇、豆甾醇或3-亚丁基-4,5-二氢苯酞、或其任何组合;
165.(iii)伊枯草菌素a、全息酰胺(hoiamides)、海洛内酰胺、拉沙霉素、安帕酰胺(apramides)、龙酰胺、盖格四烯菌素(gageotetrins)、鞘丝藻贝林(lyngbyabellins)、环丁西丁素、帕尔格琳、普米酸丁、磺基脂肽、丰原素、甲巴酰胺、微球菌素、青霉酰胺、磺基糖脂、卤代尔、卡海拉利或促吞噬素、或前述的任何组合;
166.(iv)保护素;或
167.(v)脂氧素,
168.或(i)-(v)的任何组合。
169.33.根据前述实施方式中任一项所述的方法,其中所述组合物作为糖浆剂,咀嚼剂,胶囊剂或软凝胶剂施用。
170.34.一种制品,其包含:
171.包含组合物的容器,所述组合物包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质;以及
172.标签,所述标签包含该组合物的使用说明。
173.35.根据实施方式34所述的制品,其中所述鲑鱼油是酶提取的鲑鱼油。
174.36.根据实施方式34所述的制品,其中所述鲑鱼油是从鲑鱼的下脚料下脚料的温和酶水解获得的。
175.37.一种制品,包含:
176.包含组合物的容器,所述组合物包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质;以及
177.标签,所述标签包含此类组合物使用说明,
178.其中所述鲑鱼油是从鲑鱼的下脚料的温和酶水解获得的,和/或
179.其中所述鲑鱼油是在不使用以下方法或条件中的一种或多种的情况下生产的:
180.(i)与3n或更高浓度的酸混合;
181.(ii)与3n或更高浓度的碱混合;
182.(iii)分馏;
183.(iv)再酯化;
184.(v)冬化;
185.(vi)130℃或更高的温度;或
186.(vi)2atm或更高的压力。
187.38.根据实施方式34至37中任一项所述的制品,其中所述标签含有针对在有需要的人中降低嗜酸性粒细胞效应器功能的使用说明。
188.39.根据实施方式34至37中任一项所述的制品,其中所述标签含有针对在有需要的人中治疗嗜酸性粒细胞炎性病症,障碍或疾病的使用说明。
189.40.根据实施方式39所述的制品,其中所述嗜酸性粒细胞炎性病症,障碍或疾病是气道的慢性炎性病症。
190.41.根据实施方式39所述的制品,其中所述嗜酸性粒细胞炎性病症,障碍或疾病是哮喘。
191.42.根据实施方式39所述的制品,其中所述嗜酸性粒细胞炎性病症,障碍或疾病是支气管哮喘。
192.43.根据实施方式34至37中任一项所述的制品,其中所述标签含有针对在有需要的人中治疗嗜酸性粒细胞呼吸病症,障碍或疾病的使用说明。
193.44.根据实施方式43所述的制品,其中所述嗜酸性粒细胞呼吸病症,障碍或疾病为病毒性呼吸疾病。
194.45.根据实施方式43所述的制品,其中所述嗜酸性粒细胞呼吸病症,障碍或疾病为严重急性呼吸综合征。
195.46.根据实施方式45所述的制品,其中所述严重急性呼吸综合征由冠状病毒引起。
196.47.根据实施方式38至46中任一项所述的制品,其中所述人对用于治疗所述病状,病症或疾病的药物和手术干预具有广泛抗性。
197.48.根据实施方式38至46中任一项所述的制品,其中所述人表现出或具有对类固醇治疗的抗性。
198.49.根据实施方式38至46中任一项所述的制品,其中所述人患有类固醇治疗抗性哮喘。
199.50.根据实施方式34至49中任一项所述的制品,其中所述标签含有使用说明,所述使用说明指示包含鲑鱼油的所述组合物的有效剂量为每天4g至6g。
200.51.所述实施方式34至49中任一项所述的制品,其中所述标签含有指示包含至少一种从鲑鱼油中分离的生物活性物质的组合物的有效剂量为每天10mg至1000mg的使用说明。
201.52.根据实施方式34至51中任一项所述的制品,其中向人施用所述组合物减少或延迟向人提供辅助呼吸的需要。
202.53.根据实施方式34至51中任一项所述的制品,其中所述温和酶水解使用具有小
于1%脂肪酶活性的酶。
203.54.实施方式34至53中任一项的制品,其中所述鲑鱼油包含少于0.5%的游离脂肪酸。
204.55.根据实施方式34至54中任一项所述的制品,其中所述鲑鱼油包含微球菌素。
205.56.根据实施方式34至55中任一项所述的制品,其中所述鲑鱼油包含微球菌素a。
206.57.根据实施方式34至56中任一项所述的制品,其中所述鲑鱼油包含:
207.(i)己酸、辛酸、癸酸、月桂酸、山嵛酸、二十四烷酸、肉豆蔻烯酸、十七碳烯酸、反油酸、鳕油酸、芥酸、巴西烯酸、神经酸、γ亚麻酸、哥伦比亚酸、十八碳四烯酸、二十碳三烯酸或二高γ亚麻酸、或其任何组合;
208.(ii)藁本内酯、大根香叶烯、百里酚、丁子香酚、香芹酚、芳樟醇、香茅醇、萜品醇、红没药醇(bisbalol)、檀香醇、侧柏酮(thujone)、松莰酮(pinacamphone)、斜立酮(italidone)、乙酸芳樟酯、乙酸香叶酯、甲酸香茅酯、心菊内酯(helenalin)、土木香、呋喃香豆素、萎叶酚、谷甾醇、豆甾醇或3-亚丁基-4,5-二氢苯酞、或其任何组合;
209.(iii)伊枯草菌素a、全息酰胺(hoiamides)、海洛内酰胺、拉沙霉素、安帕酰胺(apramides)、龙酰胺、盖格四烯菌素(gageotetrins)、鞘丝藻贝林(lyngbyabellins)、环丁西丁素、帕尔格琳、普米酸丁、磺基脂肽、丰原素、甲巴酰胺、微球菌素、青霉酰胺、磺基糖脂、卤代尔、卡海拉利或促吞噬素、或前述的任何组合;
210.(iv)保护素;或
211.(v)脂氧素,
212.或(i)-(v)的任何组合。
213.58.根据实施方式34至57中任一项所述的制品,其中所述组合物经口服、吸入、注射施用或局部施用。
214.59.根据实施方式34至58中任一项所述的制品,其中所述组合物以剂型提供。
215.60.根据实施方式34至59中任一项所述的制品,其中所述剂型为糖浆剂,咀嚼剂,胶囊剂或软凝胶剂。
216.61.一种试剂盒,包含:
217.包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物的剂型;以及
218.包含使用此类组合物的说明的包装插页。
219.62.根据实施方式61所述的试剂盒,其中所述鲑鱼油是酶提取的鲑鱼油。
220.63.根据实施方式61所述的试剂盒,其中所述鲑鱼油是从鲑鱼的下脚料的温和酶水解获得的。
221.64.一种试剂盒,包含:
222.包含鲑鱼油或至少一种从鲑鱼油中分离的生物活性物质的组合物的剂型;以及
223.含有该组合物的使用说明的包装插页,
224.其中所述鲑鱼油是从鲑鱼的下脚料的温和酶水解获得的,和/或
225.其中所述鲑鱼油在不使用以下方法或条件中的一种或多种的情
226.况下生产:
227.(i)与3n或更高浓度的酸混合;
228.(ii)与3n或更高浓度的碱混合;
229.(iii)分馏;
230.(iv)再酯化;
231.(v)冬化;
232.(vi)130℃或更高的温度;或
233.(vi)2atm或更高的压力。
234.65.根据实施方式61至64中任一项所述的试剂盒,其中所述标签含有针对在有需要的人中降低嗜酸性粒细胞效应器功能的使用说明。
235.66.根据实施方式61至64中任一项所述的试剂盒,其中所述标签含有针对在有需要的人中治疗嗜酸性粒细胞炎性病症,障碍或疾病的使用说明。
236.67.根据实施方式66所述的试剂盒,其中所述嗜酸性粒细胞炎性病症,障碍或疾病是气道的慢性炎性病症。
237.68.根据实施方式66所述的试剂盒,其中所述嗜酸性发炎性病症、障碍或疾病是哮喘。
238.69.根据实施方式66所述的试剂盒,其中所述嗜酸性发炎性病症、障碍或疾病是支气管哮喘。
239.70.根据实施方式61至64中任一项所述的试剂盒,其中所述标签含有针对在有需要的人中治疗嗜酸性粒细胞呼吸病症、障碍或疾病的使用说明。
240.71.根据实施方式70所述的试剂盒,其中所述嗜酸性粒细胞呼吸道病状,病症或疾病是病毒性呼吸道疾病。
241.72.根据实施方式70所述的试剂盒,其中所述嗜酸性粒细胞呼吸病症,障碍或疾病是严重急性呼吸综合征。
242.72.根据实施方式72的试剂盒,其中所述严重急性呼吸综合征由冠状病毒引起。
243.74.根据实施方式65至73中任一项所述的试剂盒,其中所述人对用于治疗所述病症、障碍或疾病的药物和手术干预具有广泛抗性。
244.75.根据实施方式65至73中任一项所述的试剂盒,其中所述人表现出或具有对类固醇治疗的抗性。
245.76.根据实施方式65至73中任一项所述的试剂盒,其中所述人具有类固醇治疗抗性哮喘。
246.77.根据实施方式61至76中任一项所述的试剂盒,其中所述包装插页含有指示包含鲑鱼油的所述组合物的有效剂量为每天4g至6g的使用说明。
247.78.根据实施方式61至77中任一项所述的试剂盒,其中所述包装插页含有指示包含至少一种从鲑鱼油中分离的生物活性物质的组合物的有效剂量为每天10mg至1000mg的使用说明。
248.79.根据实施方式61至78中任一项所述的试剂盒,其中向所述人施用所述组合物减少或延迟向所述人提供辅助呼吸的需要。
249.80.根据实施方式61至79中任一项所述的试剂盒,其中所述温和酶水解使用具有小于1%脂肪酶活性的酶。
250.81.根据实施方式61至80中任一项所述的试剂盒,其中所述鲑鱼油包含少于0.5%的游离脂肪酸。
251.82.根据实施方式61至81中任一项所述的试剂盒,其中所述鲑鱼油包含微球菌素。
252.83.根据实施方式61至82中任一项所述的试剂盒,其中所述鲑鱼油包含微球菌素a。
253.84.根据实施方式61至83中任一项所述的试剂盒,其中所述鲑鱼油包含:
254.(i)己酸、辛酸、癸酸、月桂酸、山嵛酸、二十四烷酸、肉豆蔻烯酸、十七碳烯酸、反油酸、鳕油酸、芥酸、巴西烯酸、神经酸、γ亚麻酸、哥伦比亚酸、十八碳四烯酸、二十碳三烯酸或二高γ亚麻酸、或其任何组合;
255.(ii)藁本内酯、大根香叶烯、百里酚、丁子香酚、香芹酚、芳樟醇、香茅醇、萜品醇、红没药醇(bisbalol)、檀香醇、侧柏酮(thujone)、松莰酮(pinacamphone)、斜立酮(italidone)、乙酸芳樟酯、乙酸香叶酯、甲酸香茅酯、心菊内酯(helenalin)、土木香、呋喃香豆素、萎叶酚、谷甾醇、豆甾醇或3-亚丁基-4,5-二氢苯酞、或其任何组合;
256.(iii)伊枯草菌素a、全息酰胺(hoiamides)、海洛内酰胺、拉沙霉素、安帕酰胺(apramides)、龙酰胺、盖格四烯菌素(gageotetrins)、鞘丝藻贝林(lyngbyabellins)、环丁西丁素、帕尔格琳、普米酸丁、磺基脂肽、丰原素、甲巴酰胺、微球菌素、青霉酰胺、磺基糖脂、卤代尔、卡海拉利或促吞噬素、或前述的任何组合;
257.(iv)保护素;或
258.(v)脂氧素,
259.或(i)-(v)的任何组合。
260.85.根据实施方式61至84中任一项所述的试剂盒,其中所述组合物经口服、吸入、注射施用或局部施用。
261.86.根据实施方式61至85中任一项所述的试剂盒,其中所述组合物以剂型提供。
262.87.根据实施方式61至86中任一项所述的试剂盒,其中所述剂型是糖浆剂,咀嚼剂,胶囊剂或软凝胶剂。
263.实施例
264.通过参考以下实施例将更好地理解当前公开的主题,所述实施例作为本发明的示例性内容提供的,而不是以限制的方式提供。
265.实施例1
266.酶提取鲑鱼油的抗炎作用
267.本实施例通过降低酶提取的鲑鱼油中的嗜酸性粒细胞效应器功能来探索抗炎作用。本实施例中使用的酶提取的鲑鱼油是brilliant鲑鱼油(购自hofseth biocare asa),在本文中也称为“so”。为了探索这一假设,我们使用三种体外试验,分别测量(i)正常多形核白细胞(pmnl)中的嗜酸性粒细胞形状变化,(ii)正常pmnl中的整合素上调,和(iii)过敏性人纯化外周血嗜酸性粒细胞中的细胞凋亡试验。
268.形变测定
269.pmnl样品用3μg/m apoa-iv(阳性对照),100μg/ml的so和制剂载体(阴性对照)预处理30分钟,并在37℃用ccl11的梯度稀释刺激20分钟。通过流式细胞仪监测形状变化作为前向散射(fsc)的增加,并表示为载体响应的百分比。注意,嗜酸性粒细胞可通过其ssc特性和自身荧光与中性粒细胞区分。
270.趋化因子ccl11用于引发嗜酸性粒细胞以通过重新排列它们的细胞骨架来立即准
备通过内皮进行血球渗出。随着这些细胞前向散射特性的增加,通过流式细胞仪检测到这种形态学变化。研究100μg/ml的so的影响,并与3μg/mlapoa-iv对健康供体pmnl样品中嗜酸性粒细胞形状变化的已知影响进行比较。用梯度稀释的ccl11刺激预处理的样品,并通过流式细胞仪监测形状变化。如下表1和图1所示,与载体相比,100μg/ml的so导致嗜酸性粒细胞形状改变明显减少。
271.表1.在不同预处理条件下,不同浓度的ccl11刺激的pmnl的形状变化(100%作为基线)。
[0272][0273]
cd11b(整合素)上调测定
[0274]
用3μg/m apoa-iv(阳性对照),100μg/mlso和制剂载体(阴性对照)预处理pmnl样品30分钟,并在37℃下用ccl11的梯度稀释孵育30分钟。用抗-cd16-pe-cy5和抗cd11b-pe(icrf44)抗体染色样品。嗜酸性粒细胞被鉴定为cd16阴性细胞。通过流式细胞仪分析cd11b的上调。
[0275]
嗜酸性粒细胞迁移的前提条件是粘附分子如αmβ2整合素(cd11b/cd18)的上调。与上述观察到的对形状改变的作用相似,so和apoa-iv明显地将细胞表面的cd11b分子的存在减少了20-30%(在最佳约2-4nm ccl11浓度下),如下表2和图2所示。
[0276]
表2.在不同预处理条件下,不同浓度的ccl11刺激pmnl表面的cb11b变化(100%作为基线)。
[0277][0278]
细胞凋亡试验
[0279]
在3μg/ml apoa-iv(阳性对照),100μg/ml so和制剂载体(阴性对照)存在下,将过敏性人嗜酸性粒细胞置于补充有il-5(50pm),1%fbs和penstrep的rpmi 1640培养基中。孵育18小时后取出等分试样,在pbs中洗涤两次,并重悬于结合缓冲液中。使用annexin v-fitc apoptosis detection kit i(sigma aldrich)对嗜酸细胞进行染色,并立即用流式细胞仪进行分析。采集每个样品1分钟,记录前向散射/侧向散射图上门控的嗜酸性粒细胞总数和活细胞(膜联蛋白vneg)和凋亡细胞(膜联蛋白vpos)的百分比。
[0280]
apoa-iv和so均加速这些过敏性供体细胞中的嗜酸性粒细胞凋亡。活细胞(膜联蛋白vneg)的百分比从载体处理的57.6%
±
4.5降低至3μg/ml apoa-iv-处理的嗜酸性粒细胞(阳性对照)中的31.5
±
2.3%和100μg/ml so-处理的嗜酸性粒细胞中的41.6
±
3.0%。apoa-iv和so还将凋亡细胞(膜联蛋白vpos)的百分比从44.1
±
2.9%(载体处理)增加至使用3μg/mlapoa-iv的60
±
3.8%和使用100μg/mlso的54.4
±
2.5%。
[0281]
结论
[0282]
本实施例的结果证明,so对于治疗过敏性和炎性病症,特别是涉及嗜酸性粒细胞效应物功能的那些病症具有潜在的治疗前景。具体地,在形变测定中观察到100μg/ml的so抑制嗜酸性粒细胞对趋化因子ccl11的应答。此外,在整合素(cd11b)表面上调测定中,观察到100μg/ml的so抑制嗜酸性粒细胞对趋化因子ccl11的应答。最后,观察到so增强源自过敏个体的嗜酸性粒细胞的凋亡。
[0283]
实施例2
[0284]
各种加工条件对酶提取的鲑鱼油的抗炎功效的影响
[0285]
本实施例比较了各种加工条件(例如加热,酸和碱处理)对酶提取的鲑鱼油通过降低嗜酸性粒细胞效应器功能的抗炎功效的影响。本实施例中使用的酶提取的鲑鱼油是brilliant鲑鱼油(购自hofseth biocare asa),在本文中也称为“so”。使用上述实施例1中描述的相同的三种体外测定来研究加工处理对so的影响,以及比较磷虾油和标准18/12鱼油(指鱼油中18%dha和12%epa含量)的影响。磷虾油和标准18/12鱼油是kirkland signature krill oil和kirkland signature wild alaskan fish oil,两者都来自costco,usa。
[0286]
形变测定
[0287]
将pmnl样品用100μg/ml so,加热,酸和碱处理的so,磷虾油,标准18/12鱼油和制
剂载体(阴性对照)预处理30分钟,并在37℃用梯度稀释的ccl11刺激20分钟。通过流式细胞仪监测形状变化作为前向散射(fsc)的增加,并表示为载体响应的百分比。嗜酸性粒细胞可通过其ssc特性和自发荧光与中性粒细胞区分。
[0288]
趋化因子ccl11用于引发嗜酸性粒细胞以通过重新排列它们的细胞骨架立即准备通过内皮进行血球渗出。随着这些细胞前向散射特性的增加,通过流式细胞仪检测到这种形态学变化。研究了100μg/mlso的影响,并与so、磷虾油和标准18/12鱼油的各种加工处理对健康供体pmnl样品中嗜酸性粒细胞的形状变化进行比较。用梯度稀释的ccl11刺激预处理的样品,并通过流式细胞仪监测形状变化。如下表3和图3所示,在该测定中,用加热,酸或碱的各种处理明显降低了so在该测定中的功效。此外,磷虾油与载体相比没有变化。在该测定中,与制剂载体相比,标准18/12鱼油样品显示出一些功效(~33%的so反应)。
[0289]
表3.在不同预处理条件下,不同浓度的ccl11刺激的pmnl的形状变化(100%作为基线)。
[0290][0291]
cd11b(整合素)上调测定
[0292]
pmnl样品用100μg/ml so,加热,酸和碱处理的so,磷虾油,标准18/12鱼油和制剂载体(阴性对照)预处理30分钟,并在37℃下与梯度稀释的ccl11孵育30分钟。用抗cd16-pe-cy5和抗cd11b-pe(icrf44)抗体染色样品。嗜酸性粒细胞被鉴定为cd16阴性细胞。通过流式细胞仪分析cd11b上调。
[0293]
嗜酸性粒细胞迁移的前提条件是粘附分子如αmβ2整合素(cd11b/cd18)的上调。与上述实施例1中看到的效果相似,so明显地将细胞表面的cd11b分子减少了约30%(在最佳约2-4nm ccl11浓度下),而其它样品均未显示出与制剂载体的任何差异,如下表4和图4所示。
[0294]
表4.在不同预处理条件下,不同浓度的ccl11刺激pmnl表面的cb11b变化(100%作为基线)。
[0295][0296]
细胞凋亡试验
[0297]
在100μg/ml so,加热,酸和碱处理的so,磷虾油,标准18/12鱼油和制剂载体(阴性对照)存在下,将过敏性人嗜酸性粒细胞置于补充有il-5(50pm),1%fbs和青霉素的rpmi1640培养基中。孵育18小时后取出等分试样,在pbs中洗涤两次,并重悬于结合缓冲液中。使用annexin v-fitc apoptosis detection kit i(sigma aldrich)对嗜酸性粒细胞进行染色,并立即通过流式细胞仪进行分析。采集每个样品1分钟,记录前向散射/侧向散射图上门控的嗜酸性粒细胞总数,以及活细胞(膜联蛋白vneg)和凋亡细胞(膜联蛋白vpos)的百分比。
[0298]
如以上实施例1所示,so再次加速这些过敏性供体细胞中的嗜酸性粒细胞凋亡。在100μg/ml so处理的嗜酸性粒细胞中,活细胞(膜联蛋白vneg)的百分比从载体处理的59.3%
±
4.1降低至100μg/ml so处理的嗜酸性粒细胞的40.2%
±
3.8。so还将凋亡细胞(膜联蛋白vpos)的百分比从46.5%
±
2.7(载体处理)增加至52.6%
±
3.8。其它处理与自载体处理相比,均未显示出活细胞(膜联蛋白vneg)百分比有任何明显变化。(加热-57.0%
±
3.8;酸-60.9%
±
3.3;碱-59.5%
±
2.7;磷虾油-53.2%
±
3.6;鱼油-52.1%
±
4.3)
[0299]
结论
[0300]
本实施例的结果证明,加热so或使其与弱酸或碱接触减少/消除了其用于治疗过敏性和炎性病症的潜在治疗应用,特别是如这些嗜酸性粒细胞效应器功能体外结果所示。这些结果表明,加热或酸或碱处理明显降解/消除了存在于so中的活性组分,这解释了观察到的阳性嗜酸性粒细胞效应器功能结果。此外,磷虾油似乎不含有这些组分,而标准18/12鱼油可能含有非常少量的这些组分,如单形态改变试验中的轻微阳性结果所示,但在cd11b上调或细胞凋亡中没有响应。最后,不希望受任何理论的束缚,存在于油中的脂肪酸可能不在该功效中起作用,因为(a)在加热或酸/碱处理后在so中没有注意到脂肪酸组成的变化,和(b)鱼油和so显示出非常相似的脂肪酸分布,并且都是天然甘油三酯形式。
[0301]
实施例3
[0302]
评价酶提取的鲑鱼油的抗炎作用的比较体内研究
[0303]
本实施例比较了鲑鱼油(从hofseth biocare asa商购的酶提取的鲑鱼油)与鱼肝油、fevipiprant(作为阳性对照)和linoleic acid(作为阴性对照)对白三烯
b4的趋化性和化学动力学以及豚鼠腹腔嗜酸性粒细胞细胞活力的影响。
[0304]
本实施例中的试验品目包含:
[0305]
-鲑鱼油(可从hofseth biocare asa商购的酶法提取的鲑鱼油,本文中也称为“omego”)
[0306]
-seacod鱼肝油(本文中也称为“seacod”)
[0307]
-fevipiprant;以及
[0308]
-亚油酸
[0309]
本实施例中使用的动物来自cavia porcellus(豚鼠)物种。共选择21只体重在200-250g之间的雄性豚鼠。将这些动物人工随机分成7组,即g1和g2(omego鲑鱼油30和300mg/kg),g3和g4(seacod 30和300mg/kg),g5和g6是阳性对照(fevipiprant 5和20mg/kg),g7是阴性对照(亚油酸300mg/kg),其中每组由3只动物组成。
[0310]
测试项目制剂的制备
[0311]
将omego和seacod封装在胶囊中。使用注射器收集胶囊内的油。称量适量试验品并悬浮于生理盐水中。在给药时,将试品制剂放在磁力搅拌器上以保持均匀性。
[0312]
一般方法
[0313]
通过每周一次腹腔内注射多粘菌素b(1mg/动物)持续6周,使豚鼠致敏以产生轻度嗜酸性粒细胞增多症。通过将多粘菌素b溶解在0.9%盐水溶液中来给予。每只动物注射0.5ml含有1mg多粘菌素b的0.9%生理盐水。在第6周,除多粘菌素b外,给动物注射属于其特定组的试验品,如下表5所示。
[0314]
表5.组和组大小
[0315]
[01]组号动物处理剂量动物编号g1omego鲑鱼油(cardio软凝胶)30mg/kg03g2omego鲑鱼油(cardio软凝胶)300mg/kg03g3seacod(鱼肝油胶囊)30mg/kg03g4seacod(鱼肝油胶囊)300mg/kg03g5fevipiprant
–
pc5mg/kg03g6fevipiprant
–
pc20mg/kg03g7亚油酸-nc300mg/kg03
[0316]
关键词:no.=数量、nc=阴性对照、pc-阳性对照。
[0317]
腹腔内液体的给药和收集方法
[0318]
通过腹腔内注射用多粘菌素b处理动物。与多粘菌素b一起,通过腹腔内途径给予试验品。在第6周,使用异氟烷麻醉动物,并通过在腹腔腔内注射50ml生理盐水来收集腹腔内液体。按摩腹部15秒后,将液体排出并收集在离心管中。从每只动物收集约30-35ml液体。将该液体离心10分钟(400x g 4℃)并重悬于fbs(胎牛血清)培养基中。在此步骤之后,将液体再离心10分钟(400
×
g4℃)且使用96孔微趋化性测试小室分析细胞沉淀的嗜酸性粒细胞对白三烯b4的趋化性和化学动力学反应及细胞计数。
[0319]
使用fukusa等人报告的改进方法以大于90%的纯度回收嗜酸性粒细胞。(increased numbers of hypodense eosinophils in the blood of patients with bronchial asthma.am.rev.respir.dis.1985;132:981-985)。
[0320]
给药频率
[0321]
每周用多粘菌素b生理盐水溶液处理动物一次,持续5周,并且在第6周,按照组给予多粘菌素b试验品。每只动物接受1mg多粘菌素b。
[0322]
血液采集
[0323]
在首次给药的前一天和研究的最后一天采集血液。通过眼眶后丛(retro-orbital plexus)收集每只动物的约1.5ml血液,并从中分离出血浆并储存在-20℃用于进一步的抗炎生物标志物测定。
[0324]
观察结果
[0325]
对白三烯b4的趋化和化学动力学活性:使用96孔微小室通过boyden小室方法测量趋化性和化学动力学活性,并以
×
400放大倍数下在膜滤器上计数的嗜酸性粒细胞数(细胞/5个视野)表示。通过将相同浓度的白三烯b4(0.1μm)置于小室的两个隔室中来检查对白三烯b4的化学动力学活性。孵育90分钟后通过台盼蓝排斥试验测定嗜酸性粒细胞的活力。所有样品一式两份测定。在同一天也采集血液,分离血浆并储存在-20℃用于后续抗炎生物标志物测定。
[0326]
死亡率/发病率:在整个适应期和研究期,每天至少两次(早和晚)观察所有动物的发病率和死亡率。
[0327]
中毒的临床症状:在整个研究期间,所有动物在试验品施用后和所有其他天观察的临床症状。笼侧观察包含(但不限于)皮肤和皮毛,眼睛,以及粘膜以及呼吸,循环,自主和中枢神经系统,躯体运动活动和行为模式的变化。
[0328]
体重:在随机化过程中,在治疗开始时和此后每周对动物称重,直到实验期结束。
[0329]
结果评价/统计分析:使用统计软件sigma plot 14处理原始数据。使用软件计算平均值和标准差,并以表格形式总结所有数据。检查所有连续数据如体重的正态性和均质性数据,使用anova。
[0330]
结果和讨论
[0331]
对白三烯b4的趋化和化学动力学活性:各组中个体动物的数据见表6。
[0332]
表6.用试验品预处理对从豚鼠腹腔获得的嗜酸性粒细胞中白三烯b4(0.1μm)的趋化性(a)和化学动力学(b)活性的总结。
[0333][0334]
死亡率/发病率:在整个研究期间,在所有7组的任何动物中未观察到与治疗相关
的死亡率/发病率。
[0335]
毒性临床症状:在任何组中均未观察到与治疗相关的临床症状。
[0336]
体重和体重增长:在整个研究期间,研究中的平均体重在任何组中都没有统计学上的明显差异。(参见表7)。在整个研究期间,体重相对于第1天的百分比变化在任何组中也显示无统计学明显差异(参见表8)。
[0337]
表7.与第1天相比体重变化百分比总结。
[0338][0339]
表8.死亡率和发病率总结。
[0340][0341]
结论
[0342]
使用多粘菌素b在所有动物中产生轻度嗜酸性粒细胞增多症。施用试验品后,在研究第6周成功采集所有动物的腹腔液体。
[0343]
本实施例的结果表明用cardio油(30mg/kg i.p.,n=3;300mg/kg i.p.,n=3)以剂量依赖性方式明显抑制嗜酸性粒细胞趋化和化学动力活性。与亚油酸阴性对照相比,最大抑制(300mg)对趋化性为50.7%,对趋化因子为55.6%。用seacod(30mg/kg i.p.,n=3;300mg/kg i.p.,n=3)和亚油酸(100mg/kg i.p.,n=3)进行预处理不抑制嗜酸性粒细胞趋化和化学动力学活性。用阳性对照fevipiprant(5mg/kg i.p.,n=3;20mg/kg i.p.,n=3)进行预处理,也以剂量依赖性方式明显抑制嗜酸性粒细胞趋化和化学动力活性。与对照相比,对趋化作用的最大抑制率(20mg)为68.0%,对趋化因子为51.7%。在所有处理组中,与白三烯b4温育90分钟后嗜酸性粒细胞的存活力大于96%。
[0344]
实施例4
[0345]
在房尘螨(hom)提取物诱导的小鼠哮喘模型中,鲑鱼油的嗜酸性粒细胞调节特性
[0346]
本实施例展示了在屋尘螨(hdm)提取物诱导的鼠哮喘模型中,鲑鱼油(酶法提取的鲑鱼油,可从hofseth biocare asa商购)的嗜酸性粒细胞调节特性。为此,分别用生理盐水(ns)作载体对照,apolipoprotein a-iv(apoa-iv)用作阳性对照。研究涉及使用hdm提取物在小鼠中诱导哮喘状况并同时评价omego鲑鱼油(cardio软凝胶;20或60μg/动物)和apoa-iv(5μg/动物;作为阳性对照)对小鼠中嗜酸性粒细胞的调节。
[0347]
在治疗过程中没有观察到死亡率或发病率。所有组的任何动物均未观察到临床体征(signs)或症状(symptoms)。在整个研究期间,所有组中的动物在体重以及%体重变化方面没有显示任何统计学变化。
[0348]
在第1天,将所有20只小鼠麻醉并用在40μl pbs中的1μghdm蛋白鼻内敏化。从第7天至第11天,所有20只小鼠每天通过鼻内应用40μl pbs中的10μg hdm蛋白进行挑战。将小鼠随机分成4组,每组5只小鼠,用于从第7天至第14天的差异化治疗。第7天至第14天,第一组(g1)中的每只动物接受100μl ns;第二组(g2)中的每只动物接受100μl ns中的20μg cardio;第三组(g3)中的每只动物接受100μl ns中的60μg cardio;第四组(g4)中的每只动物接受100μl ns中的5μg apoa-iv。
[0349]
在第15天从所有20只小鼠收集支气管-肺泡灌洗(bal)液和脾,并通过流式细胞仪分析收集的样品的细胞性。如下表9中所总结,与g1相比,g3(60μg cardio/动物;p≤0.01)和g4(5μg apoa-iv/动物;p≤0.05)的bal液中的总细胞计数(嗜酸性粒细胞,肺泡巨噬细胞,淋巴细胞,单核细胞和中性粒细胞)明显减少。然而,与g1相比,仅在g3(60μg cardio/动物;p≤0.01)观察到bal液中嗜酸性粒细胞明显减少。此外,与g1相比,g3(60μg cardio/动物;p≤0.001)和g4(5μg apoa-iv/动物;p≤0.01)的脾脏组织中嗜酸性粒细胞的百分比明显降低和g4。bal液和脾脏样品分析显示,60μg cardio/动物的治疗有助于改善小鼠的气道嗜酸性粒细胞增多。
[0350]
表9.嗜酸性粒细胞增多分析总结
[0351][0352][0353]
结论
[0354]
使用hdm提取物在所有动物中创造哮喘状况。在给予试验品后,在研究的第15天从所有动物成功收集bal液。施用60μgcardio/动物能够减少鼠哮喘模型中的嗜酸性粒细胞增多病症,如bal液和脾的细胞性的结果所反映的。
[0355]
实施例5
[0356]
酶提取鲑鱼油的冬化及其对嗜酸性粒细胞凋亡的影响
[0357]
本实施例通过降低嗜酸性粒细胞效应器功能,比较了冬化对酶提取的鲑鱼油的抗炎功效的影响。在100ml玻璃烧杯中,放置80ml的鲑鱼油(酶提取的鲑鱼油,可从hofseth biocare asa商购)(在本文中也称为“omego”),冷却至8℃,并在4-8℃(冰箱)之间保存24小时。在烧杯底部沉淀出蜡状固体薄层(体积约10ml)。倾倒出10ml顶部液体油并收集用于如下所述的嗜酸性粒细胞凋亡测定。
[0358]
将过敏性人嗜酸性粒细胞置于rpmi 1640培养基中,该培养基补充有il-5(50pm),1%fbs和penstrep,同时加入上述制剂载体,100μg/ml omego和100μg/ml冬化omego。孵育18小时后取出等分试样,在pbs中洗涤两次,并重悬于结合缓冲液中。使用annexin v-fitc apoptosis detection kit i(sigma aldrich)对嗜酸性粒细胞进行染色,并立即通过流式细胞仪进行分析。每个样品采集1分钟,记录活细胞(膜联蛋白vneg)和凋亡细胞(膜联蛋白vpos)的百分比,如下表10所总结。
[0359]
表10.细胞凋亡试验总结
[0360]
[0361][0362]
结论
[0363]
如通过嗜酸性粒细胞的细胞凋亡增加所测量的,omego冬化实际上消除了嗜酸性粒细胞调节。
[0364]
除非另外明确指出,否则术语“一(a)”,“一个(an)”等是指一个或多个。
[0365]
在一些变型中,“约”是指本技术领域的技术人员容易知道的各个值的通常误差范围。本文中提到的“约”值或参数包含(和描述)针对值或参数本身的实施方式。例如,“约x”包含并描述“x”本身。在一些实施方式中,术语“约”当与测量结合使用或用于修饰值,单位,常数或值的范围时,是指+/-2%的变化。
[0366]
在一些变型中,本文中的两个值或参数“之间”包含(和描述)包含这两个值或参数本身的实施方式。例如,涉及“在x和y之间”的描述包含“x”和“y”本身的描述。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1