核酸配体偶联物及其用于向细胞递送的用途
核酸配体偶联物及其用于向细胞递送的用途
1.优先权声明
2.本技术依据35u.s.c.
§
119(e)要求2020年5月13日提交的美国临时申请号63/024,142的权益,其全部内容被通过引用并入本文。
技术领域
3.本发明涉及包含与核酸连接的配体的偶联产物。本发明还涉及将核酸递送至细胞并使用该偶联产物治疗疾病的方法。本发明还涉及增加细胞对核酸的摄取的方法,包括将核酸与配体偶联以形成本发明的偶联产物。
4.发明背景
5.使用传统方法阻断许多重要癌症靶标的困难促使发明人和其他人考虑使用rna干扰(rnai)作为治疗方法(pecot et al.,nat.rev.cancer 11:59(2011))。1998年rnai的发现(fire et al.,nature 391:806(1998))获得了2006年诺贝尔奖,揭示了双链rna(dsrna)可以结合细胞质内的mrna序列,且随后导致mrna被rna诱导的沉默复合体(risc)降解或被抑制翻译(pecot et al.,nat.rev.cancer 11:59(2011))。鉴于rnai能够有效沉默任何rna序列,使用“治疗性rnai”靶向“无成药性(undruggable)”靶标是高度可取的。发明人之前已经展示了rnai可用于靶向突变kras的概念验证(pecot et al.,mol.cancer ther.13:2876(2014))。
6.尽管rnai的使用具有巨大的潜力,但许多实际挑战阻碍了成功和有效递送用于癌症治疗的寡核苷酸的道路(pecot et al.,nat.rev.cancer 11:59(2011))。障碍包括由血清核酸外切酶和核酸内切酶引起的血管内降解、寡核苷酸快速清除、内体逃逸的需要以及避免免疫刺激。在过去几年中,可靶向的、生物相容的配体(例如,靶向去唾液酸糖蛋白受体(asgpr)的galnac)和当前最新的(state-of-the-art)化学修饰sirna(sir)的使用在绕过许多这些障碍方面取得了一些成功(foster et al.,mol.ther.26:708(2018);nair et al.,j.am.chem.soc.136:16958(2014))。鉴于所述的挑战,许多人已转向使用纳米颗粒载体将寡核苷酸递送至肿瘤,然而迄今为止尚未导致临床成功,且尚无fda批准的用于在癌症中递送纳米颗粒介导的寡核苷酸的疗法。
7.尽管本领域取得了进步,但本领域仍然需要改进的能够将核酸递送到细胞,如癌细胞的系统。因此,通过提供使用靶向配体将核酸递送至细胞的组合物和方法,本发明克服了技术上的缺陷。
8.发明概述
9.由于galnac偶联的化学优化的sir,如fda批准的靶向肝脏中的asgpr的givoshiran的引人注目的成功(sardh et al.,n.engl.j.med.380:549(2019)),发明人选择评估配体偶联方法是否可以靶向癌症并消除对纳米载体的需要。使用癌细胞系百科全书(ccle)数据集发现,表皮生长因子受体(egfr)在大多数上皮癌中高度表达。选择了ge11配体,其是一种被发现与egfr结合、但不诱导促有丝分裂信号传导的12个氨基酸的肽(li et al.,faseb j.19:1978(2005))。开发了一种高度可扩展、简便的ge11合成和点击化学法,使
用生物相容性聚乙二醇(peg)接头将ge11与sirna偶联。在来自不同癌症起源的两种细胞系(lu65-肺癌、hct 116-结肠癌)中(两者均表达egfr),与未偶联的sir相比,ge11-cy5-sirna迅速且大量地被内化到细胞中。当使用ge11-kras靶向sirna而不使用转染试剂时,也观察到大量rnai活性。sirna在两种细胞系中的摄取程度(在仅24小时内达到约>150-250倍的增幅)是引人注目的,并且考虑到使用被设计为靶向肝细胞的galnac-sirna时观察到的水平(约8倍增加)(nair et al.,j.am.chem.soc.136:16958(2014)),这远远超出了预期。鉴于寡核苷酸摄取到癌细胞中的程度,配体偶联的核酸递送在使用核酸治疗癌症方面具有真正的潜力。
10.因此,本发明的一个方面涉及一种偶联产物,其包含:
11.a)包含表皮生长因子受体(egfr)靶向部分的多肽;
12.b)接头;和
13.c)核酸。
14.本发明的另一方面涉及组合物,例如包含本发明的偶联产物的药物组合物。
15.本发明的又一方面涉及将核酸递送到细胞中的方法,该方法包括使细胞与有效量的本发明的偶联产物或组合物接触。
16.本发明的另一方面涉及治疗需要其的受试者中的疾病的方法,该方法包括对受试者施用治疗有效量的本发明的偶联产物或药物组合物,从而治疗疾病。
17.本发明的另一方面涉及增加细胞对核酸的摄取的方法,该方法包括将核酸通过接头与包含egfr靶向部分的多肽偶联以形成偶联产物,其中所述细胞表达egfr,并且其中相对于未与包含egfr靶向部分的多肽偶联的核酸,所述细胞对所述核酸的摄取增加。
18.本发明的这些和其他方面将在下面的发明描述中更详细地阐述。
19.附图简要说明
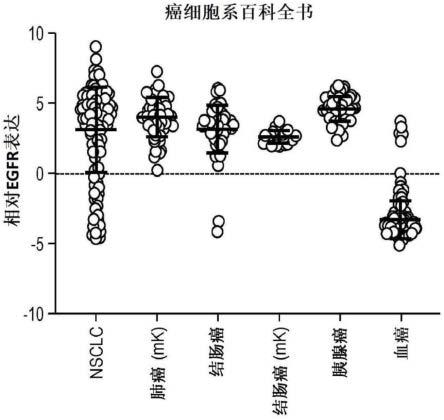
20.图1显示许多癌表达高水平的egfr。
21.图2显示经facs确认,lu65肺癌细胞系具有高egfr表达。
22.图3显示经facs确认,hct116结肠癌细胞系具有高egfr表达。
23.图4显示偶联产物的合成方案。
24.图5显示ge11-peg-kras seq3 sirna偶联产物的lc/ms确认。
25.图6显示ge11-peg-kras seq3 sirna偶联产物的lc/ms确认。
26.图7显示ge11偶联的cy5标记的sirna,其显示被显著地时间依赖性地自由摄取(无转染试剂)到两种不同的表达egfr的癌细胞(结肠癌和肺癌)中。
27.图8显示对于两种sirna,ge11偶联的kras沉默的sirna(seq2和seq3)在48小时时针对hct116(kras g13d突变体)结肠癌细胞提供了显著的kras沉默。未使用转染试剂。这表明ge11偶联的sirna可以被摄取入细胞中并有效沉默mrna。
28.图9显示在表达egfr的癌细胞(hct116结肠癌)中,ge11偶联的cy5标记的sirna通过受体介导的内吞作用机制进入细胞。先用gfp标记的报告质粒转染癌细胞,该报告质粒定位于早期(绿色,rab5a)和晚期(绿色,rab7a)核内体或溶酶体(绿色,lamp1)亚细胞结构。然后,在无转染试剂的情况下,在培养基中用ge11-sirna处理细胞4小时。然后用pbs清洗细胞三次,并且然后进行成像。cy5信号(蓝绿色)与早期和晚期核内体以及溶酶体共定位,表明它们通过受体介导的内吞作用机制进入细胞。
29.图10显示在表达egfr的癌细胞(hct116结肠癌)中,ge11偶联的cy5标记的sirna通过受体介导的内吞作用机制进入细胞。先用gfp标记的报告质粒转染癌细胞,该报告质粒定位于早期(绿色,rab5a)和晚期(绿色,rab7a)核内体或溶酶体(绿色,lamp1)亚细胞结构。然后,在无转染试剂的情况下,在培养基中用ge11-sirna处理细胞24小时。然后用pbs清洗细胞三次,并且然后进行成像。cy5信号(蓝绿色)与早期和晚期核内体以及溶酶体共定位,表明它们通过受体介导的内吞作用机制进入细胞。
30.图11a-11b显示hct116肿瘤(kras g13d)中kras被沉默的体内证据。建立大小约125mm3的hct116(kras g13d)肿瘤,然后用pbs或用通过所示接头与kras sirna序列偶联的egfr靶向配体(ge11)处理。所评估的接头使用与可裂解二硫键(spdp)或不可裂解(smcc或teg)柄偶联的己基氨基接头。(spdp:3(2-吡啶二硫代)-丙酸琥珀酰亚胺酯;smcc:反式4-(n-马来酰亚胺基甲基)环己烷-1-羧酸琥珀酰亚胺酯;teg:三甘醇)。用悬浮在无菌pbs中的ge11-sirna以5mg/kg(mpk)皮下注射处理小鼠。单次皮下注射溶于pbs的ge11-sirna(以200μl/小鼠注射)后,在第3天(d3)和第7天(d7)摘取肿瘤。分离肿瘤rna,并对kras和18s管家基因进行实时qpcr。在所示时间点发现肿瘤中kras高达50-70%被沉默。所示的每个组和时间点代表5个单独的肿瘤。
*
p<0.05,
***
p<0.01,
****
p<0.001。还给予小鼠5mpk或10mpk的一次性剂量(one-time dose)或5日10mpk剂量(5天内累积50mpk),且未发现可观察到的毒性或体重减轻。
31.发明详述
32.现在将参照附图描述本发明,附图中显示了本发明的优选实施方案。然而,本发明可以以不同的形式体现,而不应该被解释为局限于本文所述的实施方案。相反,提供这些实施方案是为了使本公开全面和完整,并将向本领域技术人员充分传达本发明的范围。
33.除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域的技术人员通常理解的含义相同的含义。本文描述本发明使用的术语仅仅是为了描述特定的实施方案,并不旨在限制本发明。本文提及的所有出版物、专利申请、专利和其他参考文献均通过引用以其整体并入。
34.核苷酸序列在本文中仅以单链呈现,5'到3'方向,从左到右,另外特别说明除外。按照37cfr
§
1.822和惯用法(established usage),本文中核苷酸和氨基酸以iupac-iub生物化学命名委员会推荐的方式表示,或(对于氨基酸)以单字母代码或三字母代码表示。例如,参见patentin用户手册,99-102(1990年11月)(美国专利与商标局)。
35.除非另有说明,本领域技术人员已知的标准方法可用于构建重组细小病毒和aav(raav)构建体、表达细小病毒rep和/或cap序列的包装载体以及瞬时和稳定转染的包装细胞。此类技术对于本领域技术人员而言是已知的。例如,参见sambrook et al.,molecular cloning:alaboratory manual第4版(cold spring harbor,ny,2012);ausubel et al.,current protocols in molecular biology(green publishing associates,inc.and john wiley&sons,inc.,new york)。
36.此外,本发明还考虑到,在本发明的一些实施方案中,可以排除或省略本文所述的任何特征或特征的组合。
37.为了进一步说明,例如,如果说明书指示特定的氨基酸可以选自a、g、i、l和/或v,则该语言还指示该氨基酸可以选自这些氨基酸的任何子集(例如,a、g或i或l;a、g,i或v;a
或g;仅l;等),如同本文明确阐述了每个此类子组合一样。此外,这种语言还指示一种或更多种特定氨基酸可以被放弃。例如,在特定的实施方案中,氨基酸不是a、g或i;不是a;不是g或v;等等,如同本文明确阐述了每个此类可能的放弃项一样。
38.定义
39.以下术语用于本文的描述和所附权利要求书中。
40.单数形式“一个/种(a,an)”也旨在包括复数形式,上下文另有明确说明除外。
41.此外,当指可测量的值如多核苷酸或多肽序列的长度量、剂量、时间、温度等时,本文所用的术语“约”意指包括指定量20%,10%、5%、1%、0.5%或甚至0.1%的变化。
42.也如本文使用的,“和/或”是指并包括一个或更多个相关所列项目的任一和所有可能的组合,而当以替代方案(“或”)解读时不组合。
43.如本文所用,过渡短语“主要由
……
组成”应被解释为包括所述及的材料或步骤“以及实质上不影响要求保护的发明的基本和新颖特征(例如核酸递送)的材料或步骤”。因此,本文使用的术语“主要由
……
组成”不应被解释为等同于“包括/包含”。
44.当应用于本发明的多核苷酸或多肽序列时,术语“主要由
……
组成”(和语法变体)表示由所述序列(例如,seq id no)和在所述序列的5’和/或3’或n端和/或c端上总共十个或更少(例如,1、2、3、4、5、6、7、8、9或10)的附加核苷酸或氨基酸(使得多核苷酸或多肽的功能没有实质性改变)组成的多核苷酸或多肽。十个或更少的附加核苷酸或氨基酸的总和包括两端附加核苷酸或氨基酸加在一起的总数。当应用于本发明的多核苷酸时,术语“实质性改变”是指与由所述序列组成的多核苷酸表达水平相比,修饰靶核酸表达的能力增加或减少至少约50%或更多。当应用于本发明的多肽时,术语“实质上改变”是指与由所述序列组成的多肽的活性相比,酶活性增加或降低至少约50%或更多。
45.术语“增强”或“增加”是指特定参数增加至少约1.25倍、1.5倍、2倍、3倍、4倍、5倍、6倍、8倍、10倍、12倍或甚至15倍。
46.本文使用的术语“抑制”或“减少”或其语法变体是指特定水平或活性的减少或减弱至少约15%、25%、35%、40%、50%、60%、75%、80%、90%、95%或更多。在特定的实施方案中,抑制或减少导致很少或基本上没有可检测到的活性(至多、不显著例如,小于约10%或甚至5%的量)。
47.如本文所用,术语“多肽”包括肽和蛋白质,另有说明除外。
48.如本文所用,“核酸”、“核苷酸序列”和“多核苷酸”可互换使用,且包括rna和dna,包括cdna、基因组dna、mrna、合成(例如,化学合成的)dna或rna以及rna和dna的嵌合体。术语多核苷酸、核苷酸序列或核酸是指核苷酸链,不考虑链长度。核酸可以是双链或单链的。在单链情况下,核酸可以是有义链或反义链。核酸可使用寡核苷酸类似物或衍生物(如肌苷或硫代磷酸酯核苷酸)合成。例如,这种寡核苷酸可用于制备具有改变的碱基配对能力或增加的对核酸酶抗性的核酸。本发明还提供了核酸,其是本发明的核酸、核苷酸序列或多核苷酸的互补序列(其可以完全互补或部分互补)。当合成产生dsrna时,不太常见的碱基,如肌苷、5-甲基胞嘧啶、6-甲基腺嘌呤、次黄嘌呤和其他碱基也可用于反义、dsrna和核糖酶配对。例如,含有尿苷和胞苷的c-5丙炔类似物的多核苷酸已经显示以高亲和力结合rna,并且是基因表达的有效反义抑制剂。也可以进行其他修饰,例如修饰磷酸二酯骨架或rna核糖糖基中的2'-羟基。
49.如本文所用,术语“序列同一性”具有本领域的标准含义。如本领域所知,许多不同的程序可用于鉴定多核苷酸或多肽是否与已知序列具有序列同一性或相似性。序列同一性或相似性可使用本领域已知的标准技术(包括但不限于smith&waterman,adv.appl.math.2:482(1981)的局部序列同一性算法)、通过needleman&wunsch,j.mol.biol.48:443(1970)的序列同一性比对算法、通过pearson&lipman,proc.natl.acad.sci.usa 85:2444(1988)的相似性搜索方法、通过计算机实施这些算法(威斯康星遗传软件包中的gap、bestfit、fasta和tfasta,genetics computer group,575science drive,madison,wi)、devereux et al.,nucl.acid res.12:387(1984)描述的最佳拟合序列程序、优选使用默认设置或通过检查确定。
50.有用算法的实例是pileup。pileup使用渐进的成对比对从一组相关序列中创建多序列比对。它还可以绘制一棵树,显示用于创建比对的聚类关系。pileup采用了feng&doolittle,j.mol.evol.35:351(1987)的渐进比对法的简化法;该方法类似于higgins&sharp,cabios 5:151(1989)所描述的方法。
51.有用算法的另一个实例是blast算法,在altschul et al.,j.mol.biol.215:403(1990)和karlin et al.,proc.natl.acad.sci.usa 90:5873(1993)中描述。一个特别有用的blast程序是wu-blast-2程序,其获自altschul etal.,meth.enzymol.,266:460(1996);blast.wustl/edu/blast/readme.html。wu-blast-2使用多个搜索参数,这些参数优选设置为默认值。这些参数是动态值,由程序本身根据特定序列的组成和正在搜索目的序列的特定数据库的组成来建立;但是,可以调整这些值以增加灵敏度。
52.另一个有用的算法是altschul et al.,nucleic acids res.25:3389(1997)报告的带空位的blast。
53.百分比氨基酸序列同一性值由匹配的相同残基数除以对齐区域中“较长”序列的残基总数确定。“较长的”序列是在对齐区域中具有最多实际残基的序列(wu-blast-2为最大化对齐得分而引入的缺口被忽略)。
54.以类似方式,核酸序列同一性百分比被定义为候选序列中与本文具体公开的多核苷酸中的核苷酸相同的核苷酸残基的百分比。
55.比对可包括在待比对的序列中引入空位。此外,对于含有比本文具体公开的多核苷酸更多或更少核苷酸的序列,应当理解,在一个实施方案中,序列同一性的百分比将基于相同核苷酸的数目相对于核苷酸总数来确定。因此,例如,在一个实施方案中,将使用较短序列中的核苷酸数来确定比本文具体公开的序列短的序列的序列同一性。在同一性百分比计算中,相对权重未分配给序列变异的各种表现(如插入、缺失、取代等)。
56.在一个实施方案中,只有相同得分为正(+1),并包括缺口在内的所有形式的序列变化被分配“0”值,其消除了对如下所述的用于序列相似性计算的加权尺度(weighted scale)或参数的需要。例如,可以通过将匹配的相同残基数除以比对区域中“较短的”序列的残基总数并乘以100来计算序列同一性百分比。“较长的”序列是在比对区域中具有最多实际残基的序列。
57.如本文所用,术语“基本上相同”或“对应于”表示两个核酸序列具有至少60%、70%、80%或90%的序列同一性。在一些实施方案中,两个核酸序列可以具有至少85%、90%、95%、96%、97%、98%、99%或100%的序列同一性。
58.如本文使用的,“分离的”多核苷酸(例如,“分离的dna”或“分离的rna”)是指与天然存在的生物体或病毒的至少一些其他组分分离或基本上不含这些组分的多核苷酸,例如细胞或病毒结构组分,或或通常发现的与该多核苷酸连接的其他多肽或核酸。
59.同样,“分离的”多肽是指与天然存在的生物体或病毒的至少一些其他成分分离或基本上不含这些组分的多肽,例如,细胞或病毒结构成分或或通常发现的与该多肽连接的其他多肽或核酸。
60.应用于多核苷酸的术语“片段”将被理解为意指相对于参考核酸或核苷酸序列长度被缩短的核苷酸序列,并且包含与参考核酸或核苷酸序列相同或几乎相同(例如,90%、92%、95%、98%、99%同一性)的连续核苷酸的核苷酸序列、主要由该核苷酸序列组成和/或由该核苷酸序列组成。在适当的情况下,根据本发明的这种核酸片段可以被包括在其作为组成部分的较大多核苷酸中。在一些实施方案中,这样的片段可以包含具有根据本发明的核酸或核苷酸序列的至少约8、10、12、15、20、25、30、35、40、45、50、75、100、150、200或更多个连续核苷酸的长度的寡核苷酸、主要由该寡核苷酸组成和/或由该寡核苷酸组成。
61.应用于多肽的术语“片段”将被理解为意指相对于参考多肽或氨基酸序列长度被缩短的氨基酸序列,并且包含与参考多肽或氨基酸序列相同或几乎相同(例如,90%、92%、95%、98%、99%同一性)的连续氨基酸的氨基酸序列、主要由该氨基酸序列组成和/或由氨基酸序列组成。在适当的情况下,根据本发明的这种多肽片段可以被包括在其作为组成部分的较大的多肽中。在一些实施方案中,这样的片段可以包含具有根据本发明的多肽或氨基酸序列的长度至少约4、6、8、10、12、15、20、25、30、35、40、45、50、75、100、150、200或更多个连续氨基酸的长度的肽、主要由该肽组成和/或由该肽组成。
[0062]“融合蛋白”是当编码两种(或更多种)自然界中未发现融合在一起的不同多肽的两种异源核苷酸序列或其片段在正确的翻译阅读框中融合在一起时产生的多肽。示例性融合多肽包括本发明的多肽(或其片段)与全部或部分谷胱甘肽-s-转移酶、麦芽糖结合蛋白或报告蛋白(例如,绿色荧光蛋白、β-葡萄糖醛酸酶、β-半乳糖苷酶、荧光素酶等)、血凝素、c-myc、flag表位等的融合。
[0063]
术语多核苷酸编码序列的“表达(express或expression)”意味着该序列被转录,并任选被翻译。通常,根据本发明,本发明编码序列的表达将导致本发明多肽的产生。完整表达的多肽或片段也可以在完整细胞中发挥作用,而无需纯化。
[0064]
如本文所用,术语“基因”是指能够用于产生mrna、反义rna、mirna等的核酸分子。基因也许能或也许不能被用于产生功能性蛋白质。基因可以包括编码区和非编码区(例如内含子、调控元件、启动子、增强子、终止序列和5’和3’非翻译区)。基因可以被“分离”,指的是实质上或基本上不含通常在其自然状态下与核酸相连接的成分的核酸。这些成分包括其他细胞材料、来自重组生产体系的培养基和/或化学合成核酸所使用的各种化学品。
[0065]
如本文所用,“互补”多核苷酸是那些能够根据标准watson-crick互补规则进行碱基配对的多核苷酸。具体而言,嘌呤将与嘧啶进行碱基配对,以形成鸟嘌呤与胞嘧啶(g:c)组合,且在dna的情况下腺嘌呤与胸腺嘧啶(a:t)配对,或在rna的情况下腺嘌呤与尿嘧啶(a:u)配对。例如,序列“a-g-t”与互补序列“t-c-a”结合。应当理解,两个多核苷酸即使彼此不完全互补,也可以彼此杂交,只要每个多核苷酸至少有一个区域与另一个基本上互补。
[0066]
如本文所用,术语“互补”或“互补性”是指多核苷酸在允许的盐和温度条件下通过
碱基配对的天然结合。两个单链分子之间的互补性可以是“部分的”,其中只有一些核苷酸结合,或者当单链分子之间存在完全互补性时,互补性可以是全部的。核酸链之间的互补程度对核酸链之间杂交的效率和强度具有显著影响。
[0067]
如本文所用,术语“基本上互补”或“部分互补”是指两个核酸序列的核苷酸的至少约50%、60%、70%、80%或90%是互补的。在一些实施方案中,两种核酸序列的核苷酸至少85%、90%、95%、96%、97%、98%、99%或更多可以是互补的。术语“基本上互补”或“部分互补”也可以指两个核酸序列能够在高严格条件下杂交,且这种条件在本领域是公知的。
[0068]
如本文所用,“异源的”是指来源于另一物种或来自相同物种或生物体但自其原始形式或主要在细胞中表达的形式被修饰的核酸序列。因此,来源于与核苷酸序列被引入的细胞不同的生物体或物种的核苷酸序列,对于该细胞及其后代来说是异源的。此外,异源核苷酸序列包括所来源和插入的天然原始细胞类型相同的核苷酸序列,但该核苷酸序列以非天然状态存在,例如不同的拷贝数,和/或受不同于自然界中发现的调控序列控制。
[0069]
如本文所用,术语“接触”、“引入”和“施用”可互换使用,且指将本发明的偶联产物或本发明的多核苷酸递送至细胞的过程,以抑制或改变或修饰靶基因的表达或细胞过程。偶联产物可以通过多种方式施用,包括但不限于细胞外引入到腔、胞间隙或引入到生物体的循环。
[0070]
在细胞或生物体的情况下,“引入”是指以使得核酸分子能够进入细胞内部的方式将该核酸分子呈递至生物体和/或细胞。当要引入一个以上的核酸分子时,这些核酸分子可以作为部分组装为一个多核苷酸或核酸构建体的一,或作为不同的多核苷酸或核酸构建体组装,并且可以位于相同或不同的核酸构建体上。因此,这些多核苷酸可以在单个转化事件中或在不同的转化事件中被引入细胞。因此,如本文所用,术语“转化”是指将异源核酸引入细胞。细胞的转化可以是稳定的或瞬时的。
[0071]
在多核苷酸的情况下,“瞬时转化”是指将多核苷酸引入细胞,而不整合到细胞的基因组中。
[0072]
在将多核苷酸引入细胞的情况下,“稳定地引入”或“被稳定地被引入”,意在将引入的多核苷酸稳定地并入到细胞的基因组中,并因此细胞被稳定地转染为具有该多核苷酸。
[0073]
本文所用的“稳定转化”或“稳定转化的”是指将核酸分子引入细胞并整合到细胞基因组中。因此,整合的核酸分子能够被其后代遗传,更具体地说,能够被连续多代的后代遗传。本文所用的“基因组”包括核基因组和线粒体基因组,且因此包括将核酸整合到例如线粒体基因组中。本文所用的稳定转化也可指保持在染色体外的转基因,例如,作为微型染色体。
[0074]
瞬时转化可通过例如酶联免疫吸附试验(elisa)或蛋白质印记法检测,其可检测由引入生物体的一种或更多种转基因编码的肽或多肽的存在。细胞的稳定转化可以通过例如细胞基因组dna的dna印迹杂交测定来检测,所述细胞基因组dna具有与导入生物体的转基因的核苷酸序列特异性杂交的核苷酸序列。细胞的稳定转化可以通过例如细胞rna的rna印迹杂交测定来检测,细胞rna具有与导入生物体的转基因的核苷酸序列特异性杂交的核酸序列。细胞的稳定转化也可以通过例如聚合酶链式反应(pcr)或本领域公知的其它扩增反应来检测,使用与转基因的靶序列杂交的特异性引物序列,导致转基因序列的扩增,其可
以根据标准方法来检测。转化也可以通过本领域公知的直接测序和/或杂交方案来检测。
[0075]
如本文所用,“转染试剂”是通过在细胞与核酸接触之前和/或细胞与核酸接触同时接触细胞,或在核酸接触细胞之前接触核酸来增强核酸向细胞中递送的任何化合物或分子。转染试剂不与核酸共价结合。
[0076]“治疗性多肽”或“治疗性核酸”是一种多肽或核酸,其可减轻或减少因细胞或受试者中的蛋白质或核酸缺乏、水平不足或过量或缺损而引起的症状。另外,“治疗性多肽”是以原本赋予受试者益处的多肽,例如抗癌作用或移植物存活性的改善。
[0077]
如本文所用,“rnai”或“rna干扰”是指由双链rna(dsrna)介导的序列特异性转录后基因沉默过程。如本文所用,“dsrna”是指部分或完全双链的rna。双链rna也称为小干扰rna(sirna)、小干扰核酸(sina)、microrna(mirna)等。在rnai过程中,将包含与靶基因的一部分互补的第一(反义)链和与第一反义链完全或部分互补的第二(有义)链的dsrna引入生物体。在引入生物体后,靶基因特异性dsrna被加工成相对较小的片段(sirna),且随后可分布在整个生物体内,导致在一代中具有可能与靶基因完全或部分缺失引起的表型非常相似的表型的功能丧失突变。
[0078]
microrna(mirna)是非蛋白质编码rna,通常长度在约18个至约25个核苷酸之间。这些mirna直接切割反式的靶转录物,负调控参与各种调控和发育途径的基因表达(bartel,cell 116:281-297(2004);zhang et al.,dev.biol.289:3-16(2006))。因此,mirna已被证明参与生长和发育的不同方面,以及信号转导和蛋白质降解。自从在植物中发现第一批mirna以来(reinhart et al.,genes dev.16:1616-1626(2002),park et al..curr.biol.12:1484-1495(2002)),已经鉴定出数百种。许多microrna基因(mir基因)已被鉴定并在数据库中为公众可得(mirbase;microrna.sanger.ac.uk/sequences)。美国专利公开号2005/0120415和2005/144669a1中也描述了mirna,其全部内容通过引用并入本文。
[0079]
编码mirna的基因产生长度为70bp至300bp的初级mirna(称为“pri-mirna”),其可以形成不完善的茎环结构。单个pri-mirna可包含一个至多个mirna前体。在动物中,通过rnasell酶drosha及其辅因子dgcr8/pasha,pri-mirna在细胞核中被加工成约65nt的更短发夹rna(pre-mirna)。然后,pre-mirna被输出到细胞质,在细胞质中被另一种rnaseiii酶dicer进一步处理,释放出约22nt大小的mirna/mirna
*
二聚体。有许多关于microrna生物合成和功能的综述,例如,参见bartel,cell 116:281-297(2004),murchison et al.,curr.opin.cell biol.16:223-229(2004)、dugas et al.,curr.opin.plant biol.7:512-520(2004)和kim,nature rev.mol.cell biol.6:376-385(2005)。
[0080]
如本文所用,当应用于多核苷酸或多肽序列时,术语“修饰的”是指由于一个或更多个缺失、添加、取代、化学修饰或其任意组合而与野生型序列不同的序列。
[0081]
如本文所用,“分离”或“纯化”(或语法等价词)病毒载体是指该病毒载体至少部分地与起始原料中的至少一些其他组分分离。
[0082]
术语“治疗(treat)”、“治疗(treating)”或“治疗(treatment of)”(及其语法变体)是指受试者病情的严重程度有所减轻,至少部分改善或稳定,和/或至少一种临床症状得到某种减轻、缓解、减少或稳定,和/或疾病或病症的进展有所延缓。
[0083]
术语“预防(prevent)”、“预防(preventing)”和“预防(prevention)”(及其语法变
体)指的是预防和/或延迟受试者中疾病、病症和/或临床症状的发作和/或降低相对于在没有本发明方法的情况下将发生的疾病、病症和/或临床症状发作的严重程度。预防可以是完全的,例如完全没有疾病、病症和/或临床症状。预防也可以是部分的,使得受试者中疾病、病症和/或临床症状的发生和/或发作的严重程度低于在没有本发明的情况下将发生的情况。
[0084]
本文所用的“治疗有效”或“治疗有效的”量是足以给受试者提供一些改善或益处的量。换句话说,“治疗有效”量是对受试者的至少一种临床症状提供某种缓解、减轻、减少或稳定的量。本领域技术人员应理解,只要向受试者提供一些益处,治疗效果不必是完全的或治愈性的。
[0085]
如本文所用,“预防有效”量是指足以预防和/或延缓受试者的疾病、病症和/或临床症状发作和/或减轻和/或延缓相对于在无本发明所述方法下所发生的受试者的疾病、病症和/或临床症状发作严重程度的量。本领域技术人员应理解,只要给受试者提供一些益处,预防水平就不必是完全的。
[0086]
偶联产物
[0087]
本发明的一个方面涉及偶联产物,其包含:
[0088]
a)包含表皮生长因子受体(egfr)靶向部分的多肽;
[0089]
b)接头;和
[0090]
c)核酸。
[0091]
包含egfr靶向部分的多肽可以是本领域已知或后来鉴定的任何靶向部分。在一些实施方案中,多肽包含十二肽ge11(yhwygytpqnvi(seq id no:1))的氨基酸序列或与其至少80%相同(例如与其至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性)的序列、主要由所述序列组成或由所述序列组成。ge11序列可以通过添加、缺失和/或取代的任何组合被修饰,并且可以包括天然存在的和非天然存在的氨基酸。
[0092]
可以对ge11序列或任何其他egfr靶向部分进行修饰,以提供用于制备偶联产物的反应位点。在一个实施方案中,将多肽修饰为在c-末端包含半胱氨酸残基。对于ge11,附加半胱氨酸残基形成序列yhwygytpqnvic(seq id no:2)。在一些实施方案中,多肽包含seq idno:2的氨基酸序列或与其至少80%相同(例如与其至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同)的序列、主要由所述序列组成或由所述序列组成。
[0093]
在一些实施方案中,egfr靶向部分可以是含碳硼烷的大环肽,如yin et al.,j.am.chem.soc.141:19193(2019)中所述的cbap5和cbap14,其全部内容通过引用并入本文。
[0094]
接头可以是任何适于共价或非共价地连接多肽和核酸的接头。在一些实施方案中,接头是药学上可接受的接头,例如但不限于聚乙二醇(peg)接头、可还原的二硫化物接头、酸不稳定肟接头、活性氧(ros)物质敏感的硼酸酯接头、肽接头或腙接头。在一些实施方案中,接头是与可裂解二硫键(例如,3-(2-吡啶基二硫基)-丙酸琥珀酰亚胺酯(spdp))或不可裂解的(例如,4-(n-马来酰亚胺基甲基)环己烷-1-羧酸琥珀酰亚胺酯(smcc)或三甘醇(teg))柄偶联的己基氨基接头。
[0095]
在一些实施方案中,接头可以包含聚乙二醇(peg)。在一些实施方案中,接头可以
包含二苯并环辛炔-peg4-马来酰亚胺、主要由二苯并环辛炔-peg4-马来酰亚胺组成或由二苯并环辛炔-peg4-马来酰亚胺组成。
[0096]
在一些实施方案中,多肽与接头共价结合,例如与半胱氨酸残基上的巯基共价结合。
[0097]
核酸可以是期望在体外或体内被引入细胞中的任何核酸。核酸可以是用于研究或治疗目的的核酸。核酸可以是可用于修饰(增加或减少)细胞中核酸或蛋白质水平的核酸。
[0098]
在一些实施方案中,核酸是dna、rna或dna和rna的杂合体。在一些实施方案中,核酸是双链或单链的。在单链情况下,核酸可以是有义链或反义链。
[0099]
核酸可以通过本领域已知的程序使用化学合成和酶连接反应来构建。例如,核酸可以使用天然存在的核苷酸或各种修饰的旨在增加分子的生物稳定性或增加核酸与靶核苷酸序列之间所形成双链的物理稳定性的核苷酸(例如可以使用硫代磷酸酯衍生物和吖啶取代的核苷酸)来化学合成。可用于生成核酸的修饰的核苷酸的实例包括但不限于:5-氟尿嘧啶、5-溴尿嘧啶、5-氯尿嘧啶、5-碘尿嘧啶、次黄嘌呤、黄嘌呤、4-乙酰胞嘧啶、5-(羧羟甲基)尿嘧啶、5-羧甲基氨基甲基-2-硫尿嘧啶、5-羧甲基氨基甲基尿嘧啶、二氢尿嘧啶、β-d-半乳糖q核苷、肌苷、n6-异戊烯基腺嘌呤、1-甲基鸟嘌呤、1-甲基肌苷、2,2-二甲基鸟嘌呤、2-甲基腺嘌呤、2-甲基鸟嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶,n6-腺嘌呤、7-甲基鸟嘌呤、5-甲基氨基甲基尿嘧啶、5-甲氧基氨基甲基-2-硫尿嘧啶、β-d-甘露糖q核苷、5'-甲氧基羧基甲基尿嘧啶、5-甲氧基尿嘧啶、2-甲硫基-n6-异戊烯基腺嘌呤、尿嘧啶-5-氧乙酸(v)、怀丁苷、假尿嘧啶、q核苷、2-硫胞嘧啶、5-甲基-2-硫尿嘧啶、2-硫尿嘧啶、4-硫尿嘧啶、5-甲基尿嘧啶、尿嘧啶-5-氧乙酸甲酯、尿嘧啶-5-氧乙酸(v)、5-甲基-2-硫尿嘧啶、3-(3-氨基-3-n-2-羧丙基)尿嘧啶、(acp3)w和2,6-二氨基嘌呤。或者,可以使用其中已克隆编码核酸的核酸的表达载体来产生核酸。
[0100]
核酸还可以包括核苷酸序列,其中至少一个或所有的核苷酸间桥接磷酸酯残基是修饰的磷酸酯,如膦酸甲酯、硫代膦酸甲酯、磷酸吗啉酯、磷酸哌嗪酯和氨基磷酸酯。例如,每一个或每隔一个核苷酸间桥接磷酸残基可以如所述进行修饰。在另一个非限制性实例中,核酸是核苷酸序列,其中至少一个或所有核苷酸含有2'低级烷基部分(例如,c1-c4、直链或支链、饱和或不饱和烷基,如甲基、乙基、乙烯基、丙基、1-丙烯基、2-丙烯基和异丙基)。在另一个实例中,一个或更多个核苷酸可以是2'-氟代核苷酸、2'-o-甲基核苷酸或锁核酸核苷酸。例如,每一个或每隔一个核苷酸可以如所述进行修饰。另见,furdon et al.,nucleic acids res.17:9193(1989);agrawal et al.,proc.natl.acad.sci.usa 87:1401(1990);baker et al.,nucleic acids res.18:3537(1990);sproat et al.,nucleic acids res.17:3373(1989);walder and walder,proc.natl.acad.sci.usa 85:5011(1988);其全部内容通过引用并入本文,以获得其制备多核苷酸分子,包括那些含有修饰的核苷酸碱基的多核苷酸分子的方法的指导。
[0101]
在某些实施方案中,核酸可选自由以下组成的组:sirna、microrna、shrna、反义核酸、核糖酶、杀伤trna、向导rna、长链非编码rna、反义mirna寡核苷酸(anti-mirna oligonucleotide)和质粒dna。
[0102]
在一个实施方案中,核酸是沉默kras的sirna或反义寡核苷酸,如美国专利号10,619,159或美国公开号2020/0248185中所述。
[0103]
在某些实施方案中,接头与核酸共价结合。可以对核酸进行修饰,以提供接头结合位点,例如包含叠氮基团作为结合位点。
[0104]
本发明的另一方面涉及包含本发明的偶联产物和载体的组合物。在某些实施方案中,组合物是包含本发明的偶联产物和药学上可接受载体的药物组合物。
[0105]
本发明的又一方面涉及增加细胞对核酸的摄取的方法,该方法包括将所述核酸通过接头与包含egfr靶向部分的多肽偶联以形成偶联产物,其中所述细胞表达egfr,并且其中相对于未与包含egfr靶向部分的多肽偶联的核酸,所述细胞对所述核酸的摄取增加。
[0106]
核酸、接头和egfr靶向部分可以是上述的任何一种。偶联物可以通过本领域已知的任何方法制备并可按上文和实例中所述的制备。
[0107]
使用方法
[0108]
本文提供了使用本发明的偶联物和/或组合物的多种方法。因此,本发明的一个方面涉及将核酸递送到细胞中的方法,该方法包括使细胞与有效量的本发明的偶联物或组合物接触。细胞可以是体外、离体或体内细胞。在一些实施方案中,细胞是癌细胞。在一些实施方案中,癌细胞选自由以下组成的组:非小细胞肺癌细胞、肺癌细胞、结肠癌细胞、胰腺癌细胞和血癌细胞。在某些实施方案中,细胞表达egfr,例如相对于其他细胞更高的egfr水平。在一个实施方案中,细胞是癌细胞,其表达相对于来自相同受试者的非癌细胞或相对于在一般人群中发现的egfr平均水平更高水平的egfr。
[0109]
在一些实施方案中,增加细胞摄取核酸的方法不包括使用与偶联物分离的转染试剂。
[0110]
本发明的另一方面涉及治疗需要其的受试者中的疾病的方法,该方法包括对受试者施用治疗有效量的本发明的偶联物或药物组合物,从而治疗疾病。疾病可以是其中病变细胞表达egfr的疾病,例如,相对于其他细胞更高水平的egfr。在一些实施方案中,疾病是癌症,例如癌症选自由以下组成的组:非小细胞肺癌、肺癌、结肠癌、胰腺癌和血癌。在一个实施方案中,癌症包含突变的人kras基因,该基因包含一种或更多种错义突变g12c、g12d、g12v和g13d。包含突变人kras基因(包含一种或更多种错义突变g12c、g12d、g12v和g13d)的癌症是这样的癌症,例如其内一个或更多个细胞表达突变kras基因的肿瘤。
[0111]
在一些实施方案中,治疗疾病的方法不包括使用与偶联物分离的转染试剂。
[0112]
在这些方面中每一个的一个实施方案中,受试者可以是已经被诊断患有疾病(例如癌症)的受试者。在另一个实施方案中,受试者可以是具有发展疾病(例如癌症)的风险的人(例如,由于遗传因素、吸烟、病毒感染、暴露于化学品等而易感)。在另一个实施方案中,受试者可以是已经被鉴定携带突变kras基因并且已经或尚未被诊断患有癌症的受试者。
[0113]
本发明的偶联物或组合物可以使用本领域已知的任何方法通过接触细胞而被递送至细胞。在一个实施方案中,对受试者直接施用本发明的偶联物或组合物。通常,将本发明的偶联物重悬在药学上可接受的载体(例如生理盐水)中,并口服、局部施用,或通过静脉内输注施用,或皮下注射、肌内、颅内、鞘内、腹膜内、直肠内、阴道内、鼻内、胃内、气管内或肺内施用。优选将其直接递送至疾病或病症的部位,例如肺、肠或胰腺。偶联物或植入物可以通过瘤内注射或注射到供养肿瘤的血管中而被递送至肿瘤。所需剂量取决于施用途径的选择;制剂的性质;患者疾病的性质;受试者的体型、体重、表面积、年龄和性别;正在施用的其他药物;和主治医师的判断。合适的剂量范围为0.01μg/kg至100.0μg/kg。鉴于各种施用
途径的效率不同,预计所需剂量差异很大。例如,预计口服施用比静脉注射施用需要更高的剂量(例如,2倍、3倍、4倍、6倍、8倍、10倍;20倍、50倍、100倍、150倍或更多倍)。这些剂量水平的变化可以使用标准经验程序进行优化调整,如本领域熟知的。施用可以是一次的或多次的。将抑制剂包封在合适的递送载体(例如,聚合物微粒或可植入装置)中可提高递送效率,特别是对于口服递送。
[0114]
本发明的偶联物或组合物可以任选地与其他治疗剂一起递送。另外的治疗剂可以与本发明的偶联物或组合物同时(concurrently)递送。如本文所用,词语“同时”表示在时间上足够接近以产生组合效果(即,同时可以是在同一时间(simultaneously),或者其可以是在彼此之前或之后的短时间周期内发生的两个或更多个事件)。在一个实施方案中,本发明的偶联物或组合物与用于治疗癌症的剂联合施用,例如:1)长春花生物碱类(例如,长春碱、长春新碱);2)表鬼臼毒素(例如,依托泊苷和替尼泊苷);3)抗生素类(例如,更生霉素(放线菌素d)、柔红霉素(道诺霉素;红比霉素)、多柔比星、博来霉素、普卡霉素(光辉霉素)和丝裂霉素(丝裂霉素c));4)酶(例如,l-天冬酰胺酶);5)生物反应调节剂(例如,干扰素-α);6)铂配位络合物(例如,顺铂和卡铂);7)蒽二酮类(例如,米托蒽醌);8)取代脲类(例如,羟基脲);9)甲基肼衍生物(例如,丙卡巴肼(n-甲基肼;mih);10)肾上腺皮质抑制剂(例如,米托坦(o,p'-ddd)和氨鲁米特);11)肾上腺皮质类固醇类(例如,泼尼松);12)孕酮类(例如,己酸羟孕酮、醋酸甲羟孕酮和醋酸甲地孕酮);13)雌激素类(例如,己烯雌酚和炔雌醇);14)抗雌激素药(例如,他莫昔芬);15)雄激素类(例如,丙酸睾酮和氟甲睾酮);16)抗雄激素药(例如,氟他胺)和17)促性腺激素释放激素类似物(例如,亮丙瑞林)。在另一个实施方案中,本发明的化合物与抗血管生成剂联合施用,例如,抗vegf抗体(例如,贝伐单抗(阿瓦斯汀)、兰尼单抗(lucentis)和其他血管生成促进剂(例如,bfgf、血管生成素-1)、抗α-v/β-3血管整合素抗体(例如,vitaxin)、血管抑素、内皮抑素、达肝素、abt-510、cngrc肽tnf-α偶联物、环磷酰胺、康普立停a4磷酸酯、二甲基黄原酮乙酸、多西他赛、来那度胺、恩扎妥林、紫杉醇、白蛋白结合型纳米微粒紫杉醇制剂(abraxane)、大豆异黄酮(genistein)、柠檬酸他莫昔芬、沙利度胺、adh-1(exherin)、ag-013736、amg-706、azd2171、甲苯磺酸索拉非尼、bms-582664、chir-265、帕唑帕尼、pi-88、瓦他拉尼碱、依维莫司、苏拉明、苹果酸舒尼替尼、xl184、zd6474、atn-161、西仑吉肽和塞来昔布或其任何组合。
[0115]
如本文所用,术语“癌症”是指任何良性或恶性的异常细胞生长。实例包括但不限于乳腺癌、前列腺癌、淋巴瘤、皮肤癌、胰腺癌、结肠癌、黑色素瘤、恶性黑色素瘤,卵巢癌、脑癌、原发性脑癌、头颈癌、胶质瘤、胶质母细胞瘤、肝癌、膀胱癌、非小细胞肺癌、头颈部癌、乳腺癌、卵巢癌、肺癌、小细胞肺癌、维尔姆斯氏瘤、宫颈癌、睾丸癌、膀胱癌、胰腺癌、胃癌、结肠癌、前列腺癌、泌尿生殖癌、甲状腺癌、食管癌、骨髓瘤、多发性骨髓瘤、肾上腺癌、肾细胞癌、子宫内膜癌、肾上腺皮质癌、恶性胰腺胰岛素瘤、恶性类癌、绒毛膜癌、蕈样肉芽肿、恶性高钙血症、宫颈增生、白血病、急性淋巴细胞白血病、慢性淋巴细胞白血病、急性髓性白血病、慢性髓性白血病、慢性粒细胞白血病、急性粒细胞白血病、毛细胞白血病、神经母细胞瘤、横纹肌肉瘤、卡波西肉瘤、真性红细胞增多症、特发性血小板增多症、霍奇金病、非霍奇金淋巴瘤、软组织肉瘤、骨肉瘤、原发性巨球蛋白血症和视网膜母细胞瘤。在一些实施方案中,癌症选自肿瘤形成癌的组。
[0116]
药物组合物
[0117]
本发明的又一方面涉及药物制剂和为实现上述所讨论的任何治疗效果(例如,治疗癌症)施用其的方法。药物制剂可以包括在药学上可接受的载体中的上述讨论的任一试剂。
[0118]“药学上可接受的”是指在生物学上或其他方面无害的材料,即该材料可以对受试者施用,而不会引起任何不想要的生物学效应,如毒性。
[0119]
本发明的制剂可以任选地包含药剂(medicinal agent)、药物(pharmaceutical agent)、载体、佐剂、分散剂、稀释剂等。
[0120]
本发明的偶联物或组合物可以按照已知的技术配制以在药物载体中施用。例如,参见remington,the science and practice of pharmacy(9
th ed.1995)。在根据本发明的药物制剂的制造中,偶联物(包括其生理上可接受的盐)通常与尤其是可接受的载体混合。载体可以是固体或液体,或两者都是,并且优选与偶联物或组合物一起配制成单位剂量制剂,例如片剂,其可以含有0.01%或0.5%至95%或99%(按重量计)的偶联物或组合物。可将一种或更多种偶联物或组合物掺入本发明的制剂中,其可通过任何公知的药学技术制备。
[0121]
本发明的又一方面是在体内治疗受试者的方法,其包括将包含在药学上可接受的载体中的本发明的偶联物或组合物的药物组合物施用于受试者,其中所述药物组合物以治疗有效量施用。可以通过本领域已知的施用化合物的任何方式将本发明的偶联物或组合物施用于需要其的人类受试者或动物。
[0122]
本发明制剂的非限制性实例包括那些适用于口服、直肠、口腔(例如舌下)、阴道、胃肠外(例如皮下、肌内包括骨骼肌、心肌、膈肌和平滑肌、皮内、静脉内、腹膜内)、局部(即皮肤和粘膜表面,包括气道表面)、鼻内、经皮、关节内、颅内、鞘内和吸入施用、通过门静脉内递送施用至肝脏以及直接器官注射(例如,注射到肝脏内、到肢体内、到脑或脊髓内以递送至中枢神经系统、注射到胰腺内或注射到肿瘤或肿瘤周围的组织内)。在任何给定的情况下,最合适的途径将取决于所治疗状况的性质和严重程度,以及正使用的特定偶联物的性质。在一些实施方案中,可能需要局部递送制剂以避免与全身施用相关的任何副作用。例如,局部施用可以通过在所需治疗部位直接注射,通过在所需治疗部位附近的部位静脉注射(例如,注射到为治疗部位供血的血管中)来完成。在一些实施方案中,制剂可以局部递送至缺血组织。在某些实施方案中,制剂可以是缓释制剂,例如,以缓释库的形式。
[0123]
对于注射,载体通常是液体,例如无菌无热原水、无热原磷酸盐缓冲液、抑菌水或cremophor el(basf,parsippany,n.j.)。对于其他施用方法,载体可以是固体或液体。
[0124]
对于口服施用,偶联物可以以固体剂型,例如胶囊、片剂和粉剂施用,或以液体剂型,例如酏剂、糖浆剂和悬浮剂施用。偶联物可与非活性成分和粉末状载体如葡萄糖、乳糖、蔗糖、甘露醇、淀粉、纤维素或纤维素衍生物、硬脂酸镁、硬脂酸、糖精钠、滑石、碳酸镁等一起包封在明胶胶囊中。可添加其他非活性成分以提供所需颜色、味道、稳定性、缓冲能力、分散性或其他已知所需特性,所述其他非活性成分的实例是红氧化铁、硅胶、十二烷基硫酸钠、二氧化钛、食用白色墨水等。类似的稀释剂可用于制备压制片剂。片剂和胶囊均可制成缓释产品,以在数小时内提供药物的连续释放。压制片剂可以是糖衣或薄膜包衣的,以掩盖任何令人不快的味道并保护片剂免受空气影响,或压制片剂可以是肠溶包衣的,以在胃肠道中选择性崩解。口服施用液体剂型可含有色素和调味剂,以增加患者的接受度。
[0125]
适用于口腔(舌下)施用的制剂包括在调味基质(通常是蔗糖和阿拉伯胶或黄蓍胶)中包含偶联物的含片(lozenge);以及在惰性基质例如明胶和甘油或蔗糖和阿拉伯胶中包含偶联物的锭剂(pastille)。
[0126]
适用于肠胃外施用的本发明的制剂包含偶联物的无菌水性和非水性注射溶液,该制剂优选与预期接受者的血液等渗。这些制剂可含有抗氧化剂、缓冲剂、抑菌剂和溶质,其使制剂与预期接受者的血液等渗。水性和非水性无菌悬浮液可包括悬浮剂和增稠剂。制剂可以在单位/剂量或多剂量容器中提供,例如,在密封的安瓿和小瓶中,并可储存在冻干条件下,其仅需要在使用前立即加入无菌液体载体,例如盐水或注射用水。
[0127]
临时注射溶液和悬浮液可以由前述种类的无菌粉剂、颗粒和片剂制备。例如,在本发明的一个方面,提供了一种包含本发明的偶联物的可注射、稳定、无菌的组合物,以单位剂量形式在密封容器中。偶联物或盐以冻干物的形式呈现,该冻干物能够与合适的药学上可接受的载体复溶以形成适于将其注射到受试者中的液体组合物。单位剂型通常包含约10mg至约10g的偶联物或盐。当偶联物或盐基本上不溶于水时,可以足量使用足量的药学上可接受的乳化剂来将偶联物或盐乳化在水性载体中。磷脂酰胆碱是这样一种有用的乳化剂。
[0128]
适用于直肠施用的制剂优选以单位剂量栓剂呈现。这些可以通过将偶联物与一种或更多种常规固体载体(例如可可脂)混合,然后将所得混合物成形来制备。
[0129]
适于向皮肤局部施用的制剂优选采取软膏、霜剂、洗剂、糊剂、凝胶、喷雾剂、气雾剂或油的形式。可以使用的载体包括凡士林、羊毛脂、聚乙二醇、醇、透皮促进剂及其两种或更多种的组合。
[0130]
适用于透皮施用的制剂可以呈现为适于长时间与接受者的表皮保持紧密接触的离散贴剂。适于透皮施用的制剂也可以通过离子电渗法递送(例如,参见tyle,pharm.res.3:318(1986)),并且通常采取偶联物的任选缓冲水溶液的形式。合适的制剂包含柠檬酸盐或bis/tris缓冲液(ph 6)或乙醇/水,并含有0.1m至0.2m的偶联物。
[0131]
或者,可将偶联物配制成用于经鼻施用或通过其他方式施用至受试者的肺部,例如,通过受试者吸入的包含偶联物的可吸入颗粒的气雾剂悬浮液施用。可吸入颗粒可以是液体或固体。术语“气雾剂”包括能够被吸入细支气管或鼻道的任何气载悬浮相。具体而言,气雾剂包括气载液滴悬浮液,可在计量吸入器或雾化器或弥雾机中产生。气雾剂还包括悬浮在空气或其他载气中的干粉组合物,其可以通过例如从吸入器装置吹入来递送。参见ganderton&jones,drug delivery to the respiratory tract,ellis horwood(1987);gonda(1990)critical reviews in therapeutic drug carrier systems 6:273-313;和raeburn et al.,j.pharmacol.toxicol.meth.27:143(1992)。如本领域技术人员所知,可以通过任何合适的方式,例如用压力驱动的气雾剂喷雾器或超声喷雾器,来生产包含偶联物的液体颗粒气雾剂。,参见例如美国专利号4,501,729。包含偶联物的固体颗粒气雾剂同样可以用任何固体颗粒药物气雾剂发生器通过制药领域已知的技术来生产。
[0132]
或者,人们可以以局部而非全身方式施用,例如以贮库或缓释制剂形式施用。
[0133]
此外,本发明提供了本文公开的偶联物及其盐的脂质体制剂。用于形成脂质体悬浮液的技术是本领域公知的。当偶联物或其盐为水溶性盐时,使用常规脂质体技术,可将其掺入脂质囊泡中。在这种情况下,由于偶联物或盐的水溶性,偶联物或盐将基本上被夹带在
脂质体的亲水中心或核心内。所用的脂质层可以是任何常规的组合物,并且可以含有胆固醇或可以不含胆固醇。当偶联物或感兴趣的盐为水不溶性时,再次采用常规的脂质体形成技术,可以将盐基本上夹带在形成脂质体结构的疏水脂质双层内。在任何一种情况下,所产生的脂质体可以通过使用标准超声和均质化技术来减小尺寸。
[0134]
可以将包含本文公开的偶联物或其盐的脂质体制剂冻干以产生冻干物,其可与药学上可接受的载体(如水)复溶以再生脂质体悬浮液。
[0135]
在水不溶性偶联物的情况下,可以例如在水基乳液中制备含有水不溶性偶联物的药物组合物。在这种情况下,组合物将含有足够量的药学上可接受的乳化剂以乳化所需量的偶联物。尤其有用的乳化剂包括磷脂酰胆碱和卵磷脂。
[0136]
在特定的实施方案中,将治疗有效量的偶联物施用于受试者,该术语如上文所定义。药物活性化合物的剂量可以通过本领域已知的方法来确定,参见例如remington's pharmaceutical sciences(maack publishing co.,easton,pa)。任何具体化合物的治疗有效剂量将因化合物和患者而异,并且将取决于患者的状况和递送途径。作为一般建议,约0.001mg/kg至约50mg/kg的剂量将具有治疗效力,所有重量均基于化合物的重量计算,包括使用盐的情况。较高水平的毒性问题可能将静脉注射剂量限制在较低水平,例如至多约10mg/kg,所有重量都基于化合物的重量计算,包括使用盐的情况。口服施用可采用约10mg/kg至50mg/kg的剂量。通常,肌内注射可采用约0.5mg/kg至5mg/kg的剂量。静脉内或口服施用的化合物的具体剂量分别为约1μmol/kg至50μmol/kg,且更具体地为约1μmol/kg至约22μmol/kg和约1μmol/kg至33μmol/kg。
[0137]
在本发明的特定实施方案中,可以以各种时间间隔(例如,每小时、每天、每周、每月等)采用一次以上的施用(例如,两次、三次、四次或更多次施用)以达到治疗效果。
[0138]
本发明可用于兽医和医学应用。合适的受试者包括禽类和哺乳动物,优选哺乳动物。本文使用的术语“禽类”包括但不限于鸡、鸭、鹅、鹌鹑、火鸡和野鸡。本文所用的术语“哺乳动物”包括但不限于人、牛、绵羊、山羊、马、猫、犬、兔类等。人类受试者包括新生儿、婴儿、青少年和成人。在其它实施方案中,受试者是疾病例如癌症的动物模型。在某些实施方案中,受试者患有疾病或有患病风险,例如癌症。
[0139]
以下实例并不旨在将权利要求的范围限制于本发明,而是旨在作为某些实施方案的示例。本领域技术人员想到的示例性方法的任何变化都将在本发明的范围内。如本领域技术人员将会理解的,要求保护的发明的每个方面都有若干实施方案和要素,并且此处预期了不同要素的所有组合,因此本文举例说明的具体组合不应解释为对所要求保护的发明的范围的限制。如果特定要素被移除或添加到组合中可用的要素组中,则该要素组将被解释为已纳入此类更改。
实施例1
[0140]
核酸偶联物的开发
[0141]
方法
[0142]
流式细胞术:为了进行egfr表达分析,将脱壁的lu65或hct116细胞在pbs中重悬为单细胞溶液。将荧光团偶联的egfr或对照igg抗体加入等份的细胞溶液中,并在冰上避光孵育30分钟。洗去细胞中多余的抗体。然后在流式细胞仪上运行样品,以检测荧光信号并鉴定
被抗体标记阳性的细胞的比例。
[0143]
为了评估游离sirna摄取,将荧光标记的sirna(未偶联或与ge11偶联)与lu65或hct116细胞孵育到指定的时间点。然后用pbs冲洗细胞以洗去多余的sirna,然后固定在2%多聚甲醛中。然后在流式细胞仪上运行样品,以检测荧光信号并鉴定摄取荧光sirna的细胞的比例。
[0144]
ge11合成和sirna偶联:采用固相肽合成法合成ge11(图4)。在肽链(ge11c)末端加入一个额外半胱氨酸氨基酸。c-末端半胱氨酸上的游离巯基与二苯并环辛炔(dbco)-peg4-马来酰亚胺试剂反应,以生成ge11c-dbco-peg4-马来酰亚胺偶联产物。进行无铜点击反应,使含dbco产物与叠氮偶联的sirna偶联,以生成最终ge11c-sirna偶联产物。然后通过rna clean&concentrator试剂盒运行产物,以去除多余的未偶联的ge11肽。
[0145]
液相色谱/质谱联用(lc/ms):通过lc/ms分析ge11偶联的sirna,以确认肽与sirna的成功偶联。lc/ms显示了所提交样品中存在的所有物质的质量大小。
[0146]
mrna表达分析:将hct116或lu65细胞与对照或偶联ge11的反义kras sirna按指定剂量孵育48小时。在48小时时,去除含有多余sirna的培养基,并在rna裂解缓冲液中裂解细胞。使用rna分离试剂盒从裂解样品中分离rna。然后使用nanodrop分光光度计定量rna,并将来自每个样品的等量rna上样到cdna合成反应中。使用针对kras的引物和将结果归一化的“管家”基因引物,通过定量pcr分析所得cdna。
[0147]
结果
[0148]
图1表明数百种实体瘤来源的癌细胞系的阳性egfr表达,强调了egfr介导癌症靶向的潜力。
[0149]
图2和图3显示了用egfr抗体(分别)染色肺癌lu65细胞系或结肠癌hct116细胞系导致荧光信号相对于用对照igg抗体染色的细胞右移(或增加)。这指示两种癌细胞系模型的高egfr阳性表达。
[0150]
在图5中,等于ge11质量(1642)、dbco-peg4-马来酰亚胺接头质量(674)和sirna反义链质量(6562)之和的质量产物(8878)的存在指示成功偶联的产物的存在。
[0151]
图6表明,当与ge11偶联时,相对于未偶联的荧光标记的sirna,表达egfr的癌细胞对荧光标记的sirna的摄取随时间显著增加。使用的sirna是靶向kras的seq2-dv22。这些数据表明,ge11肽的存在显著增强了sirna向癌细胞的递送。
[0152]
seq2-dv22
[0153]
有义链(seq id no:3)
[0154]
[mg]*[m]*[mc][mu][mc][mu][2flu][mg][2flg][2fla][2flu][ma][mu][mu][mc][mu][mc][mg][ma]
[0155]
反义链(seq id no:4)
[0156]
[mu[*[2flc]*[mg][ma][mg][2fla][ma][mu][ma||mu][mc][mc][ma][2fla][mg][2fla][mg][ma][mc]*[ma]*[mg]
[0157]
m-糖基上的2
′‑
o-甲基
[0158]
2fl-糖基上的2
′‑
氟
[0159]
*-核苷酸之间的硫代磷酸酯
[0160]
图7和图8表明用ge11偶联的sirna处理时靶基因表达的稳健敲除。使用的sirna是
靶向kras的seq2-dv22和seq3-dv22。由于未使用转染试剂,sirna进入细胞完全依赖于受体介导的摄取。这些数据提供了原理论证,即ge11偶联能够高效、有效地摄取sirna,该sirna被细胞内化时具有功能活性。
[0161]
seq3-dv22
[0162]
有义链(seq id no:5)
[0163]
[mc]*[ma]*[mg][mc][mu][ma][2fla][mu][2flu][2flc][2fla][mg][ma][ma][mu][mc][ma][mu][mu]
[0164]
反义链(seq id no:6)
[0165]
[ma]*[2fla]*[mu][mg][ma][2flu][mu][mc][mu][mg][ma][ma][mu][2flu][ma][2flg][mc][mu][mg]*[mu]*[ma]
[0166]
图9和图10表明在表达egfr的癌细胞(hct116结肠癌)中,ge11偶联的cy5标记的sirna通过受体介导的内吞作用机制进入细胞。使用的sirna是靶向kras的seq2-dv22。
[0167]
图11a-11b显示使用与ge11偶联的sirna进行基因沉默的体内证据。在小鼠中建立hct116(kras g13d)肿瘤,然后用pbs或用所示接头与kras sirna序列偶联的egfr靶向配体(ge11)(5mg/kg)处理。使用的sirna是靶向kras的d2-g13d-hi2f。我们发现在指示时间点肿瘤中的kras高达50%至70%被沉默。还给予小鼠一次性剂量5mg/kg或10mg/kg或5日10mg/kg剂量(5天内累积50mg/kg),而未发现可观察到的毒性或体重减轻。
[0168]
d2-g13d-hi2f
[0169]
有义链(seq id no:7)
[0170]
[2flg|*[mu]*[2fla][mg][2flu][mu][2flg][mg][2fla][2flg][2flc][mu][2flg][mg][2flu][mg][2fla||mc][2flg][mu][2fla]
[0171]
反义链(seq id no:8)
[0172]
[mu]*[2fla[*[mc][2flg][mu][2flc][ma][2flc][mc][2fla][mg][mc][mu][2flc][mc][2fla][ma][2flc][mu][2fla][mc]*[mc]*[ma[
[0173]
前述是对本发明的例示,且不应理解为对其的限制。本发明由以下权利要求限定,其中包括所述权利要求的等效方案。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1