冠状病毒感染的诊断、预防和治疗的制作方法
冠状病毒感染的诊断、预防和治疗
1.本技术要求2020年6月2日提交的gb 2008250.9的优先权,其内容和要素通过引用并入本文用于所有目的。
技术领域
2.本发明涉及冠状病毒肽,以及所述肽在诊断、治疗和预防冠状病毒感染中的应用。
背景技术:
3.冠状病毒是一组在哺乳动物和鸟类中引起疾病的相关的病毒。冠状病毒感染的症状在不同物种之间有所不同。例如,鸡的冠状病毒感染引起上呼吸道疾病,而牛和猪的冠状病毒感染倾向于引起腹泻。
4.在人类中,冠状病毒引起呼吸道感染。感染某些冠状病毒引起的疾病可以是温和的,如普通感冒。其他冠状病毒引起更严重和可能致命的疾病,如sars、mers和covid-19。
5.一些研究已经鉴定和表征了用于开发针对冠状病毒的疫苗的靶标(target)位点。例如,he等人进行了绘制sars冠状病毒的抗原位点的实验(1)。为了鉴定可能的候选疫苗,对sars的核衣壳蛋白进行了广泛的表征(2),并在所述蛋白中鉴定了优势t辅助细胞表位(3)。最近,根据以前的sars-cov免疫学研究已经鉴定了用于covid-19冠状病毒的潜在的疫苗靶标(4)。尽管如此,还没有市售可获得的预防或治疗人类冠状病毒感染的疫苗。用于确定人类个体中当前的和/或以前的冠状病毒感染的测试是有限的。由于控制冠状病毒感染的爆发依赖于涉及准确测试和/或有效疫苗接种的策略,因此提供疫苗和测试是非常需要的。
技术实现要素:
6.本发明涉及可以被用于诊断、预防或治疗人类中冠状病毒感染的冠状病毒衍生的肽。本发明人还鉴定了许多在不同冠状病毒之间是保守的并且由感染这些病毒的细胞上的mhc分子呈递的肽。疫苗组合物中包含一种或多种这些肽可以赋予针对一种或多种冠状病毒的保护能力,和/或治疗现存的冠状病毒感染的能力。每一种肽也可以被用于诊断冠状病毒感染是否存在,例如通过检测样品中能够与所述肽结合的分子(例如t细胞受体或抗体)是否存在。冠状病毒可以是例如与人类流行病(epidemic)或大流行病(pandemic)相关的冠状病毒。冠状病毒可以是例如人畜共患的冠状病毒。冠状病毒可以是例如betacoronavirus属的成员。冠状病毒可以是例如sarbecoronavirus亚属的成员。冠状病毒可以是例如sars冠状病毒或sars冠状病毒2。
7.因此,本发明提供了一种肽,所述肽包含seq id nos:1至34中的任何一个或其变体。
8.本发明还提供:
‑ꢀ
一种复合物,其包含与mhc分子结合的本发明的肽;
‑ꢀ
本发明的肽或复合物在确定个体中当前的或以前的冠状病毒感染是否存在的
方法中的应用;
‑ꢀ
本发明的肽或复合物在鉴定冠状病毒特异性t细胞的方法中的应用;
‑ꢀ
本发明的肽或复合物在鉴定冠状病毒特异性t细胞受体的方法中的应用;
‑ꢀ
一种t细胞,其包含能够与包含seq id nos: 1至34中的任何一个或其变体的肽结合的t细胞受体;
‑ꢀ
一种疫苗组合物,其包含本发明的肽,或者能够与t细胞受体结合的肽,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合;
‑ꢀ
一种疫苗组合物,其包含编码本发明的肽或能够与t细胞受体结合的肽的多核苷酸,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合;
‑ꢀ
一种预防或治疗冠状病毒感染的方法,其包含将本发明的疫苗组合物施用于感染了冠状病毒或有感染冠状病毒风险的个体;以及
‑ꢀ
用于预防或治疗个体中冠状病毒感染的方法的本发明的疫苗组合物。
附图说明
9.图1:实施例1的吸收光谱。
10.图2:实施例1的dls数据。
11.图3:a
ꢀ‑ꢀ
实施例1的hplc方法。b
ꢀ‑ꢀ
实施例1的hplc的结果。em009-064-01:没有任何肽的gnp为3.4%。em009-064-02:没有任何肽的gnp是0%。em009-064-03:没有任何肽的gnp是2.2%。
12.图4:实施例1的lc-ms肽定量。
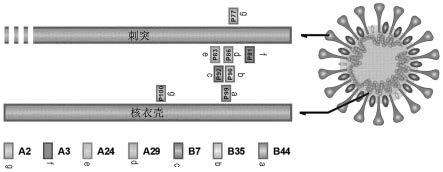
13.图5:显示实施例1中使用的肽的排列的示意图。
14.本发明的详细描述肽本发明提供一种包含seq id nos:1至34中的任何一个或其变体的肽。变体的定义详见下文。表1中列出了seq id nos: 1至34。
15.表1
ꢀ‑ꢀ
sars cov = sars冠状病毒。sars cov 2 = sars冠状病毒2。
16.为了鉴定seq id nos:1至34,已被证明在sars-cov中引起记忆t细胞反应的长肽序列被用来产生一系列长度为9至10个残基的短重叠肽。然后用mhcflurry处理这些序列来预测它们与各种hla等位基因的结合亲和力。选择亲和力小于或等于100 nm且与sars-cov2(ncbi登录号nc_045512)中的蛋白质有100%同一性的序列。
17.因此,本发明的肽能够与mhc i类分子结合。所述肽可以衍生自被感染的细胞内病毒蛋白质组的免疫蛋白体处理。所述肽可以是在一种或多种冠状病毒的表面上表达的肽,或在一种或多种冠状病毒内的细胞内表达的肽。冠状病毒可以是例如与人类流行病或大流行病相关的冠状病毒。冠状病毒可以是例如人畜共患的冠状病毒。冠状病毒可以是例如betacoronavirus属的成员。冠状病毒可以是例如sarbecoronavirus亚属的成员。冠状病毒可以是例如sars冠状病毒或sars冠状病毒2。肽可以是结构肽或功能肽,例如参与冠状病毒代谢或复制的肽。优选地,肽是内部的肽。优选地,肽在两种或更多种不同的冠状病毒或冠状病毒血清型之间是保守的。如果两种或更多种不同的冠状病毒或冠状病毒血清型中的每一个编码与肽有50%或以上(例如60%、70%、75%、80%、90%、95%、98%或99%)同源性的序列,则所述肽在两种或更多种不同的冠状病毒或冠状病毒血清型之间是保守的。
18.肽可以含有任何数量的氨基酸,即具有任何长度。通常,肽的长度为约8至约30、35或40个氨基酸,例如长度为约9至约29、约10至约28、约11至约27、约12至约26、约13至约25、约13至约24、约14至约23、约15至约22、约16至约21、约17至约20、或者约18至约29个氨基酸。肽的长度优选为9或10个氨基酸。肽可以是多肽。肽可以由seq id nos:1至34中的一个的氨基酸序列组成、或基本上由其组成。肽可以化学衍生自多肽冠状病毒抗原,例如通过蛋白酶水解切割。更典型地,可以使用本领域熟知的方法合成冠状病毒肽。
19.肽可以只包含seq id nos:1至34中的一个或其变体。替代地,肽可以包含以任何组合的seq id nos:1至34中的两个或更多个或其变体,例如三个或更多个、四个或更多个、
五个或更多个、六个或更多个、七个或更多个、八个或更多个、九个或更多个、十个或更多个、11个或更多个、12个或更多个、13个或更多个、14个或更多个、15个或更多个、16个或更多个、17个或更多个、18个或更多个、19个或更多个、20个或更多个、21个或更多个、22个或更多个、23个或更多个、24个或更多个、25个或更多个、26个或更多个、27个或更多个、28个或更多个、29个更多个、30个或更多个、31个或更多个、32个或更多个、或者33个或更多个。肽可以包含seq id nos:1至34中的全部或其变体。例如,肽可以包含seq id nos 21、1、19、28、2、27、16和14中的一个或多个。例如,肽可以包含seq id nos 21、1、19、28、2、27、16和14中的全部。
20.在某些实施方案中,肽可以包含seq id nos:9、24和25中的任何一个或多个。
21.hlriaghhl(seq id no:9)是基于sars-cov-1 m中的序列hlrmaghsl(seq id no:34)。
22.smwaliisv(seq id no:24)是基于sars-cov-1 pp1ab中的smwalvisv(seq id no: 31)序列。
23.tkaynvtqaf(seq id no:25)是基于sars-cov-1 n中的tkqynvtqaf(seq id no: 32)序列。
24.在不希望受任何特定理论约束的情况下,本发明人认为,取代有利地提供了对sars-cov-2改进的和特异性的检测。
25.肽可以包含seq id nos:1至34中的一个或多个的多个拷贝,例如两个或更多个,例如三个或更多个、四个或更多个、五个或更多个、六个或更多个、七个或更多个、八个或更多个、九个或更多个、十个或更多个。包含seq id nos:1至34中的一个或多个的多个拷贝或包含seq id nos 1至34中的一个或多个的肽的长度可以是约18至约250个氨基酸,例如约20、约30、约40或约50个氨基酸至约200、约150或约100个氨基酸。在所述肽中,seq id nos:1至34中的两个或更多个或seq id nos:1至34中的一个或多个的多个拷贝可以直接地连接到彼此,或者可以通过一个或多个,例如2至约20个氨基酸或约3至约10个氨基酸连接。在肽中,连接的氨基酸通常不包含在自然界中连接seq id nos:1至34中的两个或更多个的序列的确切氨基酸序列。
26.以及seq id nos:1至34中的任何一个或其变体,所述肽可以包含一个或多个cd8+ t细胞表位、一个或多个cd4+ t细胞表位和/或一个或多个b细胞表位。例如,所述肽可以包含两个或更多个(例如三个或更多个、四个或更多个、五个或更多个、十个或更多个、十五个或更多个或二十个或更多个)cd8+ t细胞表位。所述肽可以包含两个或更多个(例如三个或更多个、四个或更多个、五个或更多个、十个或更多个、十五个或更多个或二十个或更多个)cd4+ t细胞表位。所述肽可以包含两个或更多个(例如三个或更多个、四个或更多个、五个或更多个、十个或更多个、十五个或更多个或二十个或更多个)b细胞表位。
27.cd8+ t细胞表位优选是不包含seq id nos:1至34中的任何一个或其变体的cd8+ t细胞表位。例如,cd8+ t细胞表位可以是冠状病毒cd8+表位,即,由一种或多种冠状病毒表达并且能够(i)通过i类mhc分子呈递和(ii)通过cd8+ t细胞上存在的t细胞受体(tcr)识别的肽。替代地,cd8+ t细胞表位可以是一种或多种冠状病毒不表达的cd8+ t细胞表位。
28.cd4+ t细胞表位可以是例如冠状病毒cd4 +表位,即由一种或多种冠状病毒表达且能够(i)通过ii类mhc分子呈递和(ii)通过cd4+ t细胞上存在的t细胞受体(tcr)识别的
肽。替代地,cd4+ t细胞表位可以是一种或多种冠状病毒不表达的cd4+ t细胞表位。
29.b细胞表位可以例如是冠状病毒b细胞表位,即由一种或多种冠状病毒表达且能够通过b细胞上存在的b细胞受体(bcr)识别的肽。替代地,b细胞表位可以是一种或多种冠状病毒不表达的b细胞表位。
30.冠状病毒可以是例如与人类流行病或大流行病相关的冠状病毒。冠状病毒可以是例如人畜共患的冠状病毒。冠状病毒可以是例如betacoronavirus属的成员。冠状病毒可以是例如sarbecoronavirus亚属的成员。一种或多种冠状病毒可以包含例如sars冠状病毒和/或sars冠状病毒2。
31.术语“肽”不仅包括其中氨基酸残基通过肽(-co-nh-)键连接的分子,还包括其中肽键被逆转的分子。这种逆反(retro-inverso)模拟肽可以使用本领域已知的方法制备,例如meziere et al (1997) j. immunol.159, 3230-3237中描述的方法。该方法涉及制备含有涉及骨架的变化的伪肽,而不是侧链的方向。meziere等(1997)表明,至少对于mhc ii类和t辅助细胞应答,这些伪肽是有用的。含有nh-co键而不是co-nh肽键的逆反肽对蛋白质水解具有更强的抗性。
32.类似地,肽键可以被完全省略,条件是使用适合的连接部分保持氨基酸残基的碳原子之间的间隔;如果连接部分具有与肽键基本相同的电荷分布和基本相同的平面性,则是特别优选的。还应理解,肽可以方便地在其n-或c-末端被封闭,以帮助降低对外蛋白水解消化的易感性。例如,肽的n-末端氨基可以通过与羧酸反应来保护,肽的c-末端羧基可以通过与胺反应来保护。修饰的其他实施例包括糖基化和磷酸化。另一种可能的修饰是r或k的侧链胺上的氢可以被亚甲基取代(-nh2可以被修饰为-nh(me)或-n(me)2)。
33.术语“肽”还包括在体内增加或减少肽的半衰期的肽变体。根据本发明使用的能够增加肽的半衰期的类似物的实施例包括肽的类肽类似物、肽的d-氨基酸衍生物和肽-类肽杂合物。根据本发明使用的变体多肽的另一个实施方案包含多肽的d-氨基酸形式。使用d-氨基酸而不是l-氨基酸制备多肽,大大降低了这种试剂通过正常代谢过程的任何不希望的分解,减少了需要施用的试剂的量以及其施用频率。
34.变体如上所述,所述肽可以包含seq id nos:1至34中的任何一个的变体。例如,所述肽可以包含seq id nos: 1至34中的2个或更多个(例如3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、9个或更多个、10个或更多个、11个或更多个、12个或更多个、13个或更多个、14个或更多个、15个或更多个、16个或更多个、17个或更多个、18个或更多个、19个或更多个、20个或更多个、21个或更多个、22个或更多个、23个更多个、24个或更多个、25个或更多个、26个或更多个、27个或更多个、28个或更多个、29个或更多个、30个或更多个、31个或更多个、32个或更多个、或者33个或更多个)的变体。例如,所述肽可以包含seq id nos:1至34中的所有的变体。例如,所述肽可以包含seq id nos 21、1、19、28、2、27、16和14中的一个或多个的变体。例如,所述肽可以包含seq id nos 21、1、19、28、2、27、16和14中的所有的变体。
35.seq id nos:1至34中的任何一个的变体可以是与seq id nos:1至34中的任何一个区别不超过五个(例如不超过四个、不超过三个、不超过两个或不超过一个)氨基酸的序列。不超过五个氨基酸的差异中的每一个可以是相对于选自seq id nos: 1至34的相关序
列的氨基酸取代、缺失或插入。例如,所述氨基酸取代可以是保守的氨基酸取代。
36.优选地,seq id nos:1至34中的任何一个的变体可以是与seq id nos: 1至34中的任何一个区别不超过一个氨基酸的序列。例如,选自seq id nos:1至34的序列的变体可以相对于相关序列包含一个氨基酸取代、缺失或插入。例如,所述氨基酸取代可以是保守的氨基酸取代。
37.保守取代用相似化学结构、相似化学性质或相似侧链体积的其他氨基酸代替氨基酸。引入的氨基酸可能具有与其所代替的氨基酸相似的极性、亲水性、疏水性、碱性、酸性、中性或电荷。替代地,保守取代可以引入另一种芳香族或脂肪族的氨基酸代替预先存在的芳香族或脂肪族氨基酸。保守氨基酸变化是本领域公知的,并且可以根据下表2中定义的20种主要氨基酸的性质进行选择。当氨基酸具有相似的极性时,这也可以通过参考表3中氨基酸侧链的亲水尺度(hydropathy scale)来确定。
38.表2
ꢀ‑ꢀ
氨基酸的化学性质
丙氨酸(ala)脂肪族、疏水性、中性甲硫氨酸(met)疏水性、中性半胱氨酸(cys)极性、疏水性、中性天冬酰胺(asn)极性、亲水性、中性天冬氨酸(asp)极性、亲水性、带电荷(-)脯氨酸(pro)疏水性、中性谷氨酸(glu)极性、亲水性、带电荷(-)谷氨酰胺(gln)极性、亲水性、中性苯丙氨酸(phe)芳香族、疏水性、中性精氨酸(arg)极性、亲水性、带电荷(+)甘氨酸(gly)脂肪族、中性丝氨酸(ser)极性、亲水性、中性组氨酸(his)芳香族、极性、亲水性、带电荷(+)苏氨酸(thr)极性、亲水性、中性异亮氨酸(ile)脂肪族、疏水性、中性缬氨酸(val)脂肪族、疏水性、中性赖氨酸(lys)极性、亲水性、带电荷(+)色氨酸(trp)芳香族、疏水性、中性亮氨酸(leu)脂肪族、疏水性、中性酪氨酸(tyr)芳香族、极性、疏水性
表3
ꢀ‑ꢀ
亲水尺度
复合物本发明提供包含与mhc分子结合的本发明的肽的复合物。因此,所述复合物包含肽,所述肽包含与mhc分子结合的seq id nos:1至34中的任何一个或其变体、或由其组成。
39.肽:mhc结合是本领域熟知的。优选地,复合物中肽和的mhc分子之间的结合是非共价的。所述结合可以通过例如静电相互作用、氢键、范德瓦耳斯力和/或疏水作用来介导。
40.mhc分子可以是mhc 1类分子或mhc ii类分子。优选地,mhc分子是mhc i类分子。mhc i类分子可以是任何hla超型。例如,mhc i类分子可以是超型a2、a203/a2、a23、a24、a2403/a2、a2403/a24、a39、a3、a11、a30、a31、a32、a68、a69、b7、b8、b35、b37、b44、b48、b53、b60、b61、b62、b63、b72、b75、cw1或cw6。
41.所述复合物可以包含两种或更多种本发明的肽,以及两种或更多种mhc分子。例如,所述复合物可以包含三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)本发明的肽。所述复合物可以包含三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多
种)mhc分子。例如,复合物可以分别包含三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)本发明的肽,以及三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)mhc分子。所述复合物可以包含与mhc分子相同数量的本发明的肽。所述复合物可以包含与mhc分子数量不同数量的本发明的肽。例如,所述复合物可以包含四个mhc分子。所述复合物可以包含mhc四聚体或由其组成。例如,所述复合物可以包含十二个mhc分子。所述复合物可以包含mhc十二聚体或由其组成。
42.当复合物包含两种或更多种本发明的肽时,两种或更多种肽中的每一个可以是相同的。替代地,两种或更多种肽中的每一个可以是不同的。当复合物包含三种或更多种本发明的肽时,三种或更多种肽中的每一种可以是相同的。当复合物包含三种或更多种本发明的肽时,三种或更多种肽中的每一种可以是不同的。当复合物包含三种或更多种本发明的肽时,三种或更多种肽中的一些可以是相同的,并且三种或更多种肽中的一些可以是不同的。例如,复合物可以包含seq id nos 21、1、19、28、2、27、16和14中的两种或更多种。例如,复合物可以包含seq id nos 21、1、19、28、2、27、16和14中的全部。
43.当复合物包含两种或更多种mhc分子时,两种或更多种mhc分子中的每一个可以是相同的。替代地,两种或更多种mhc分子中的每一个可以是不同的。当复合物包含三种或更多种本发明的肽时,三种或更多种mhc分子中的每一种可以是相同的。当复合物包含三种或更多种本发明的肽时,三种或更多种mhc分子中的每一种可以是不同的。当复合物包含三种或更多种mhc分子时,三种或更多种mhc分子中的一些可以是相同的,并且三种或更多种mhc分子中的一些可以是不同的。
44.当复合物包含两种或更多种本发明的肽和两种或更多种mhc分子时,每一种肽可以与两种或更多种mhc分子中的一种结合。也就是说,复合物中包含的每一种肽可以与复合物中包含的一种mhc分子结合。优选地,复合物中包含的每一种肽与复合物中包含的不同mhc分子结合。也就是说,复合物中包含的每一种mhc分子优选地与复合物中包含的不超过一种肽结合。然而,所述复合物可以包含不与mhc分子结合的一种或多种本发明的肽。所述复合物可以包含不与本发明的肽结合的一种或多种mhc分子。
45.复合物中包含的一种或多种mhc分子可以相互连接。例如,复合物中的一种或多种mhc分子中的每一种可以被连接到骨架分子或纳米颗粒。复合物中包含的一种或多种mhc分子可以被连接到葡聚糖骨架。也就是说,复合物可以包含mhc葡聚糖或由其组成。将一种或多种mhc分子连接到葡聚糖骨架的机制是本领域已知的。任何数量的mhc分子都可以被连接到葡聚糖骨架。例如,一种或多种、两种或更多种、三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)本发明的肽和三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九
种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)mhc分子可以被连接到葡聚糖骨架。
46.复合物可以包含荧光团。荧光团在本领域是熟知的,包括fitc(异硫氰酸荧光素)、pe(藻红蛋白)和apc(别藻蓝蛋白)。复合物可以包含任何数量的荧光团。例如,复合物可以包含两种或更多种、三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)本发明的肽,以及三种或更多种(例如四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、或者20种或更多种)荧光团。当复合物包含多种荧光团时,复合物中包含的荧光团可以是相同的或不同的。当复合物包括骨架(例如葡聚糖骨架)时,荧光团优选连接到葡聚糖骨架。将荧光团连接到葡聚糖骨架上的机制是本领域已知的。
47.应用本发明的肽或复合物可以以多种方式利用,例如在下文所述的应用中。
48.确定当前的或以前的冠状病毒感染是否存在本发明提供了本发明的肽或复合物在确定个体中当前的或以前的冠状病毒感染是否存在的方法中的应用。
49.所述方法可以包含将肽或复合物与从个体获得的样品接触,并确定所述肽或复合物与样品中包含的分子之间是否存在结合。
50.所述样品可以是例如血液样品、血清样品、血浆样品、尿液样品、唾液样品、或者通过擦拭个体中存在的粘膜表面获得的样品。优选地,所述样品是血液样品、血清样品或血浆样品。
51.所述分子可以是具有免疫功能的分子。例如,所述分子可以被包含在先天免疫系统或适应性免疫系统中。优选地,所述分子具有适应性免疫的作用。所述分子可以是例如抗体或抗体片段。所述抗体或抗体片段可以在b细胞的表面上或被包含在b细胞中。所述抗体或抗体片段可以游离在样品中。所述分子可以是例如t细胞受体。所述t细胞受体可以是cd4+ t细胞受体。所述t细胞受体可以是cd8+ t细胞受体。所述t细胞受体可以在t细胞的表面上或被包含在t细胞中。所述t细胞可以是cd4+ t细胞。所述t细胞可以是cd8+ t细胞。
52.优选地,肽或复合物与分子之间的结合是非共价的。所述结合可以通过例如静电相互作用、氢键、范德瓦耳斯力和/或疏水作用来介导。检测肽或含肽复合物与分子之间结合的方法是本领域熟知的,包括例如酶联免疫吸附分析(elisa)、酶联免疫吸附点(elispot)和流式细胞仪。
53.结合的存在可以表明当前的或以前的冠状病毒感染的存在。结合的不存在可以表明当前的或以前的冠状病毒感染的不存在。
54.在当前的冠状病毒感染中,个体内可能存在冠状病毒颗粒或其组分(例如肽、蛋白质)。在当前的冠状病毒感染中,个体内可能存在对冠状病毒颗粒或其组分(例如肽、蛋白
质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。优选地,在当前的冠状病毒感染中,个体内存在(i)冠状病毒颗粒或其组分(例如肽、蛋白质)和(ii)对冠状病毒颗粒或其组分(例如蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。
55.在以前的冠状病毒感染中,个体内可能不存在冠状病毒颗粒或其组分(例如肽、蛋白质)。在以前的冠状病毒感染中,个体内可能存在对冠状病毒颗粒或其组分(例如肽、蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。优选地,在以前的冠状病毒感染中,个体内不存在冠状病毒颗粒或其组分(例如肽、蛋白质),并且个体内存在对冠状病毒颗粒或其组分(例如肽、蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。
56.冠状病毒可以是例如与人类流行病或大流行病相关的冠状病毒。冠状病毒可以是例如人畜共患的冠状病毒。冠状病毒可以是例如betacoronavirus属的成员。冠状病毒可以是例如sarbecoronavirus亚属的成员。冠状病毒可以是例如sars冠状病毒或sars冠状病毒2。
57.鉴定冠状病毒特异性t细胞本发明提供了本发明的肽或复合物在鉴定冠状病毒特异性t细胞的方法中的应用。所述方法可以包含将肽或复合物与从个体获得的样品接触,并确定所述肽或复合物与样品中包含的t细胞受体之间是否存在结合。
58.所述样品可以是例如血液样品、血清样品、血浆样品、尿液样品、唾液样品、或者通过擦拭个体中存在的粘膜表面获得的样品。优选地,所述样品是血液样品。
59.所述t细胞受体可以是cd4+ t细胞受体。所述t细胞受体可以是cd8+ t细胞受体。优选地,所述t细胞受体是cd8+ t细胞受体。
60.优选地,所述t细胞受体可以在t细胞的表面上或被包含在t细胞中。所述t细胞可以是cd4+ t细胞。所述t细胞可以是cd8+ t细胞。优选地,所述t细胞是cd8+ t细胞。
61.优选地,肽或复合物与t细胞受体之间的结合是非共价的。所述结合可以通过例如静电相互作用、氢键、范德瓦耳斯力和/或疏水作用来介导。检测肽或含肽复合物与t细胞受体之间结合的方法是本领域熟知的,包括例如酶联免疫吸附分析(elisa)、酶联免疫吸附点(elispot)和流式细胞仪。
62.结合的存在可以表明一种或多种冠状病毒特异性t细胞的存在。结合的不存在可以表明冠状病毒特异性t细胞的不存在。
63.所述个体可以是目前已经感染了冠状病毒。在当前的冠状病毒感染中,个体内可能存在冠状病毒颗粒或其组分(例如肽、蛋白质)。在当前的冠状病毒感染中,个体内可能存在对冠状病毒颗粒或其组分(例如肽、蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。优选地,在当前的冠状病毒感染中,个体内存在(i)冠状病毒颗粒或其组分(例如肽、蛋白质)和(ii)对冠状病毒颗粒或其组分(例如肽、蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。
64.所述个体可能以前感染过冠状病毒,但可能目前没有感染冠状病毒。在以前的冠状病毒感染中,个体内可能不存在冠状病毒颗粒或其组分(例如肽、蛋白质)。在以前的冠状病毒感染中,个体内可能存在对冠状病毒颗粒或其组分(例如肽、蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。优选地,在以前的冠状病毒感染中,个体内不存在冠状病毒颗粒或其组分(例如肽、蛋白质),并且个体内存在对冠状病毒颗粒或其组分(例如肽、
蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。因此,个体内可能不存在冠状病毒颗粒或其组分(例如肽、蛋白质),但是个体内可能存在对冠状病毒颗粒或其组分(例如肽、蛋白质)特异性的抗体、b细胞、cd8+ t细胞和/或cd4+ t细胞。
65.冠状病毒可以是例如与人类流行病或大流行病相关的冠状病毒。冠状病毒可以是例如人畜共患的冠状病毒。冠状病毒可以是例如betacoronavirus属的成员。冠状病毒可以是例如sarbecoronavirus亚属的成员。冠状病毒可以是例如sars冠状病毒或sars冠状病毒2。
66.鉴定冠状病毒特异性t细胞受体本发明提供了本发明的肽或复合物在鉴定冠状病毒特异性t细胞受体的方法中的应用。所述方法可以包含将肽或复合物与t细胞受体接触,并确定所述肽或复合物与t细胞受体之间是否存在结合。
67.所述t细胞受体可以是cd4+ t细胞受体。所述t细胞受体可以是cd8+ t细胞受体。优选地,所述t细胞受体是cd8+ t细胞受体。
68.所述t细胞受体可以在t细胞的表面上或被包含在t细胞中。所述t细胞可以是cd4+ t细胞。所述t细胞可以是cd8+ t细胞。优选地,所述t是cd8+ t细胞。
69.优选地,肽或复合物与t细胞受体之间的结合是非共价的。所述结合可以通过例如静电相互作用、氢键、范德瓦耳斯力和/或疏水作用来介导。检测肽或含肽复合物与t细胞受体之间结合的方法是本领域熟知的,包括例如酶联免疫吸附分析(elisa)、酶联免疫吸附点(elispot)和流式细胞仪。
70.结合的存在可以表明与肽或复合物接触的t细胞受体是冠状病毒特异性t细胞受体。结合的不存在可以表明与肽或复合物接触的t细胞受体不是冠状病毒特异性t细胞受体。
71.冠状病毒可以是例如与人类流行病或大流行病相关的冠状病毒。冠状病毒可以是例如人畜共患的冠状病毒。冠状病毒可以是例如betacoronavirus属的成员。冠状病毒可以是例如sarbecoronavirus亚属的成员。冠状病毒可以是例如sars冠状病毒或sars冠状病毒2。
72.t细胞本发明提供了一种包含t细胞受体的t细胞,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合。检测肽与t细胞受体之间结合的方法是本领域熟知的,包括例如酶联免疫吸附分析(elisa)、酶联免疫吸附点(elispot)和流式细胞仪。所述t细胞受体可以使用上述鉴定冠状病毒特异性t细胞受体的方法进行鉴定。
73.所述t细胞可以是分离的t细胞。
74.所述t细胞可以是cd4+ t细胞。所述t细胞受体可以是cd4+ t细胞受体。
75.所述t细胞可以是cd8+ t细胞。所述t细胞受体可以是cd8+ t细胞受体。优选地,所述t细胞是cd8+ t细胞。优选地,所述t细胞受体是cd8+ t细胞受体。
76.所述t细胞可以是表达嵌合抗原受体(car)的细胞。所述t细胞受体可以是car。
77.疫苗组合物本发明提供了一种疫苗组合物,其包含本发明的肽或能够与t细胞受体结合的肽,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合。变体的定
义见上文。所述疫苗组合物有许多益处,从下面的讨论中可以看出。关键的益处在此总结。
78.第一,所述疫苗组合物能够刺激针对冠状病毒的免疫反应。优选地,所述免疫反应是细胞免疫反应(例如cd8+ t细胞反应)。cd8+细胞毒性t淋巴细胞(ctls)通过其针对被感染的细胞的细胞毒性活性介导病毒清除。因此,刺激细胞免疫可以提供针对冠状病毒感染的有益防御。
79.第二,本发明人鉴定的肽在不同的冠状病毒(例如sars冠状病毒和sars冠状病毒2)之间是保守的,并且可以由感染了一种或多种所述病毒的细胞上的mhc分子呈递。疫苗组合物中包含此类保守的肽可以赋予针对(i)相关类型的病毒、(ii)多个种类的冠状病毒和/或(iii)特定种类的多个系或血清型的保护能力,即赋予交叉保护。病毒之间的100%同源性并不是赋予交叉保护需要的条件。相反,如果某些残基被保留在正确的位置中,在用与感染不同病毒的细胞中表达的cd8+ t细胞表位有例如大约50%或更多(例如60%、70%、75%、80%、90%、95%、98%或99%)同源性的序列进行免疫后,可以会产生交叉保护。因此,包含一种或多种包含seq id nos:1至34中的任何一种或其变体的肽、或者能够与能够与包含seq id nos:1至34中的任何一种或其变体的肽结合的t细胞受体结合的肽、或者相应的多核苷酸的疫苗组合物能够在表1中所列之外对多种现存的冠状病毒提供交叉保护。疫苗组合物中包含一种或多种保守得肽还可以赋予针对与冠状病毒基因组进化有关的新出现的冠状病毒株的保护能力。用这种方法,单一的冠状病毒疫苗组合物能够被用来赋予针对各种不同的冠状病毒的保护。这提供了控制冠状病毒感染传播的经济有效的方法。
80.第三,本发明人鉴定的不同肽能够与不同的hla超型结合。包含多种肽,每一种肽能够与不同的hla超型(或相应的多核苷酸)结合,从而使疫苗组合对具有不同hla类型的个体有效。用这种方法,单一的冠状病毒疫苗组合物能够被用于在很大一部分人群中赋予保护。这再次提供了控制冠状病毒感染传播的经济有效的方法。
81.第四,本发明的疫苗组合物中包含的冠状病毒肽可以被连接至纳米颗粒,例如金纳米颗粒。如下文更详细描述的,连接至纳米颗粒减少或消除了在疫苗组合物中包括佐剂的需要。连接至纳米颗粒也减少或消除了在疫苗组合物中包括病毒的需要。因此,本发明疫苗组合物在施用于个体时不太可能引起不利的临床效果。
82.所述疫苗组合物可以包含根据权利要求1的两种或更多种肽,每一种肽包含选自seq id nos: 1至34或其变体的不同的序列。每一种肽可以具有上述“肽”部分中列出的任何特性。例如,每一种肽可以包含选自seq id nos:1至34或其变体的多个序列,以及任选地一种或多种cd8+ t细胞表位、一种或多种cd4+ t细胞表位和/或一种或多种b细胞表位。在一方面,所述疫苗组合物可以包含三种或更多种、四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、20种或更多种、21种或更多种、22种或更多种、23种或更多种、24种或更多种、25种或更多种、26种或更多种、27种或更多种、28种或更多种、29种或更多种、30种或更多种、31种或更多种、32种或更多种、或者33种或更多种肽,每一种肽包含选自seq id nos: 1至34或其变体的不同的序列。所述疫苗组合物可以包含肽的任何组合。例如,该疫苗组合可以包含34种肽,每一种肽包含选自seq id nos:1至34或其变体的不同的序列。
83.所述疫苗组合物可以包含两种或更多种肽,每一种肽能够与不同的t细胞受体结
合,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合,其中每一种不同的t细胞受体能够与选自seq id nos:1至34或其变体的不同的序列结合。每一种肽可以具有上述“肽”部分中列出的任何特性。例如,所述疫苗组合物中包含的每一种肽可能能够与多种不同的t细胞受体结合,所述t细胞受体每一个能够与包含seq id nos:1至34中的任何一个或其变体的肽结合。所述疫苗可以包含一种或多种cd8+ t细胞表位、一种或多种cd4+ t细胞表位和/或一种或多种b细胞表位。在一方面,所述疫苗组合物可以包含三种或更多种、四种或更多种、五种或更多种、六种或更多种、七种或更多种、八种或更多种、九种或更多种、十种或更多种、11种或更多种、12种或更多种、13种或更多种、14种或更多种、15种或更多种、16种或更多种、17种或更多种、18种或更多种、19种或更多种、20种或更多种、21种或更多种、22种或更多种、23种或更多种、24种或更多种、25种或更多种、26种或更多种、27种或更多种、28种或更多种、29种或更多种、30种或更多种、31种或更多种、32种或更多种、或者33种或更多种肽,每一种肽能够与不同的t细胞受体结合,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合。所述疫苗组合可以包含肽的任何组合。例如,所述疫苗组合物可以包含34种肽,每一种肽能够与不同的t细胞受体结合,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合。
84.交叉保护本发明人鉴定的seq id nos:1至34是由多种冠状病毒表达的。因此,所述疫苗组合物可以引发针对一种以上冠状病毒(例如sars冠状病毒和sars冠状病毒2)的保护性免疫反应。换句话说,本发明的疫苗组合物可以引发针对一些不同的冠状病毒具有交叉保护的免疫反应。例如,不同的冠状病毒中的每一种可以是与人类流行病或大流行病相关的冠状病毒。例如,冠状病毒可以是人畜共患的冠状病毒。例如,冠状病毒可以是betacoronavirus属的成员。例如,冠状病毒可以是sarbecoronavirus亚属的成员。
85.通过接种包含与来自另一种病毒的序列具有100%同源性的表位的组合物而产生的免疫反应可以防止随后感染该病毒。通过接种包含与由另一种病毒编码的序列具有约50%或更多(例如60%、70%、75%、80%、90%、95%、98%或99%)同源性的表位的组合物而产生的免疫反应可以防止随后被该病毒感染。在某些情况下,保护作用与该表位和其他病毒编码序列之间某些残基的保守性有关。因此,用本发明的疫苗组合物免疫可以诱导针对表1中未提及的多种病毒(例如其他冠状病毒)的保护性免疫反应。
86.因此,本发明的疫苗组合物可以具有内在的交叉物种和/或交叉属功效,即是交叉保护性疫苗组合物。因此,单个本发明的冠状病毒疫苗组合物可以被用于赋予针对多种不同冠状病毒的保护。这提供了控制冠状病毒感染传播的经济有效的方法。
87.疫苗组合物中包含保守的肽可以赋予针对与冠状病毒基因组进化相关的新兴冠状病毒株的保护能力。这可能有助于冠状病毒感染的长期控制。
88.与hla超型的相互作用所述疫苗组合物可以包含至少两种肽,所述至少两种肽分别与不同的hla超型相互作用。在疫苗组合物中包括多种此类肽使得疫苗组合物能够在更大比例的被施用疫苗组合物的个体中引发免疫反应(例如cd8+ t细胞反应)。这是因为疫苗组合物应该能够在与疫苗组合物中所包含的肽中的一个相互作用的hla超型的所有个体中引发免疫反应。每个肽可以与a2、a203/a2、a23、a24、a2403/a2、a2403/a24、a39、a3、a11、a30、a31、a32、a68、a69、
b7、b8、b35、b37、b44、b48、b53、b60、b61、b62、b63、b72、b75、cw1或cw6或本领域已知的任何其他hla超型相互作用。肽的任何组合是可能的。
89.所述疫苗组合物可以包含至少一种肽,其与至少两种不同的hla超型相互作用。同样,这允许疫苗组合物在更大比例的施用了疫苗组合物的个体中引发免疫反应(例如cd8+ t细胞反应)。所述疫苗组合物可以包含至少两种、至少三种、至少四种、至少五种、至少十种、至少十五种、至少二十种、至少25种或至少30种肽,每一种与至少两种不同的hla亚型相互作用。每一种肽可以例如与至少两种、至少三种、至少四种、至少五种、至少六种、至少7种、至少8种、至少9种、至少10种、至少11种、至少12种、至少13种、至少14种或至少15种或不同的hla超型相互作用。每一种肽可以与来自a2、a2、a203/a2、a23、a24、a2403/a2、a2403/a24、a39、a3、a11、a30、a31、a32、a68、a69、b7、b8、b35、b37、b44、b48、b53、b60、b61、b62、b63、b72、b75、cw1和cw6或本领域已知的任何其他hla超型的以任何组合的两种或更多种相互作用。
90.优选地,所述疫苗组合物包含与a3、a11和a31相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:1和/或11的肽。例如,所述疫苗组合物可以包含包括seq id no:1的肽和包括seq id no:11的肽。
91.优选地,所述疫苗组合物包含与b7和b35相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:2的肽。
92.优选地,所述疫苗组合物包含与b72、a2和a203/a2相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:3的肽。
93.优选地,所述疫苗组合物包含与b72、b62和b75相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:4和/或15的肽。例如,所述疫苗组合物可以包含包括seq id no:4的肽和包括seq id no:15的肽。
94.优选地,所述疫苗组合物包含与a68、a11和a31相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:5和/或11的肽。例如,所述疫苗组合物可以包含包括seq id no:5的肽和包括seq id no:11的肽。
95.优选地,所述疫苗组合物包含与a203/a2和a2相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:3、8、13、14、21、24和/或26的肽。例如,所述疫苗组合物可以包含:包括seq id no:3的肽、包括seq id no:8的肽、包括seq id no:13的肽、包括seq id no:14的肽、包括seq id no:21的肽、包括seq id no:24的肽和包括seq id no:26的肽。
96.优选地,所述疫苗组合物包含与a2403/a2和a23相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:10的肽。
97.优选地,所述疫苗组合物包含与a11、a30、a3、a68和a31相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:11的肽。
98.优选地,所述疫苗组合物包含与a11、a30、a3和a68相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:12的肽。
99.优选地,所述疫苗组合物包含与b60、b48和b44相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:17的肽。
100.优选地,所述疫苗组合物包含与a68、b63和a203/a2相互作用的肽。在这种情况下,
例如,所述疫苗组合物可以包含包括seq id no:22的肽。
101.优选地,所述疫苗组合物包含与a2、a203/a2、a69和a32相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:24或seq id no:31的肽。
102.优选地,所述疫苗组合物包含与a2、a203/a2和a68相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:26的肽。
103.优选地,所述疫苗组合物包含与b35、b53、a29相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:27的肽。
104.优选地,所述疫苗组合物包含与b37、b60、b61、b44和b48相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:29的肽。
105.优选地,所述疫苗组合物包含与cw6和cw1相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:30的肽。
106.优选地,所述疫苗组合物包含与a30、b7、b8、b62和b72相互作用的肽。在这种情况下,例如,所述疫苗组合物可以包含包括seq id no:34的肽。
107.纳米颗粒肽、或者一个或多个肽可以被连接至纳米颗粒,例如在本发明的疫苗组合物中。所述疫苗组合物中进一步包含的任何其他肽也可以被连接至纳米颗粒。连接至纳米颗粒(例如金纳米颗粒)是有益的。
108.如上所述,肽连接至纳米颗粒(例如金纳米颗粒)减少或消除了在疫苗组合物中包括病毒或佐剂的需要。纳米颗粒可能包含免疫“危险信号”,有助于有效诱导对肽的免疫反应。纳米颗粒可以诱导强烈的免疫反应所需的树突状细胞(dc)活化和成熟。纳米颗粒可以包含非自身组分,该非自身组分改善了纳米颗粒的吸收,从而改善了诸如抗原呈递细胞等细胞对肽的吸收。因此,肽连接至纳米颗粒可以增强抗原呈递细胞刺激病毒特异性t和/或b细胞的能力。连接至纳米颗粒还促进了疫苗组合物通过皮下、皮内、透皮和口服/颊部途径的递送,从而提供了施用的灵活性。
109.纳米颗粒是尺寸在1到100纳米(nm)之间的颗粒,能够被用作固定配体的基质。在本发明的疫苗组合物中,纳米颗粒的平均直径或平均核(core)直径可以为1至100、20至90、30至80、40至70或50至60 nm。优选地,纳米颗粒的平均直径或平均核直径为5至40 nm,例如10至30 nm或20至32 nm。优选地,纳米颗粒的平均直径或平均核直径为5 nm。5至40 nm的平均直径或平均核直径促进纳米颗粒被吸收到胞质溶胶中。可以使用本领域众所周知的技术(例如透射电子显微镜)来测量平均直径或平均核直径。
110.适用于递送抗原(例如本发明的肽)的纳米颗粒是本领域已知的。用于生产此类纳米颗粒的方法也是已知的。
111.纳米颗粒可以例如是聚合物纳米颗粒、无机纳米颗粒、脂质体、免疫刺激复合物(iscom)、病毒样颗粒(vlp)或自组装蛋白。纳米颗粒优选为磷酸钙纳米颗粒、硅纳米颗粒或金纳米颗粒。
112.纳米颗粒可以是聚合物纳米颗粒。聚合物纳米颗粒可以包含一种或多种合成聚合物,例如聚(d,l-丙交酯-乙交酯)共聚物(plg)、聚(d,l-乳酸-乙醇酸)共聚物(plga)、聚(g-谷氨酸)(g-pga)m聚乙二醇(peg)或聚苯乙烯。聚合物纳米颗粒可以包含一种或多种天然聚合物,例如多糖,例如支链淀粉、藻酸盐、菊粉和壳聚糖。使用聚合物纳米颗粒可因可以包括
nm、或者约80至约90 nm。vlp有利地利用了进化出的病毒结构的力量,而自然地优化了它与免疫系统的相互作用。自然优化的纳米颗粒尺寸和重复的结构顺序意味着,即使在没有佐剂的情况下,vlp也会诱导有效的免疫反应。
120.纳米颗粒可以是自组装蛋白。例如,纳米颗粒可以包含铁蛋白。铁蛋白是一种可以自组装成近球形的10 nm结构的蛋白质。纳米颗粒可以包含主穹隆蛋白(mvp)。96个mvp单元可以自组装成桶形的穹隆纳米颗粒,尺寸约为40 nm宽和70 nm长。
121.纳米颗粒可以是磷酸钙(capo4)纳米颗粒。capo4纳米颗粒可以包含核,该核包含一个或多个(例如两个或更多个、10个或更多个、20个或更多个、50个或更多个、100个或更多个、200个或更多个、或者500个或更多个)capo4分子。capo4纳米颗粒及其生产方法是本领域已知的。例如,可以通过在恒定混合下以预定比例混合钙和磷酸盐的无机盐溶液来产生cap纳米颗粒的稳定的纳米悬浮液。
122.capo4纳米颗粒可以具有约80至约100 nm(例如约82至约98 nm、约84至约96 nm、约86至约94 nm或约88至约92 nm)的平均粒度(particle size)。在免疫细胞摄取和免疫反应方面,该粒度可能比其他较大粒度产生更好的性能。例如当在1个月、2个月、3个月、6个月、12个月、18个月、24个月、36个月或48个月的时期内测量时,粒度可以是稳定的(即没有显示出显著变化)。
123.capo4纳米颗粒能够与一种或多种抗原共同配制,所述抗原或吸附在纳米颗粒的表面上,或在颗粒合成过程中与capo4共沉淀。例如,可以通过以下方法将肽(例如本发明的肽)连接至capo4纳米颗粒:将肽溶解在dmso中(例如,浓度约为10 mg/ml),加至capo4纳米颗粒与n-乙酰氨基葡萄糖(glcnac)(例如在0.093 mol/l)和超纯水的悬浮液中,在室温下混合约4小时(例如1小时、2小时、3小时、5小时、6小时、7小时、8小时、9小时或10小时)。
124.所述疫苗组合物可以包含约0.15至约0.8%(例如0.2至约0.75%、0.25至约0.7%、0.3至约0.6%、0.35至约0.65%、0.4至约0.6%或0.45至约0.55%)的capo4纳米颗粒。优选地,疫苗组合物包含约0.3%的capo4纳米颗粒。
125.capo4纳米颗粒由于与人类硬组织(例如骨骼和牙齿)的化学相似性而具有高度的生物相容性。因此,有利地,capo4纳米颗粒在用于治疗应用时是无毒的。capo4纳米颗粒可通过肌肉内、皮下、口服或吸入途径安全施用。capo4纳米颗粒也很容易在商业上合成。此外,capo4纳米颗粒可能与抗原的缓慢释放有关,这可能会增强对连接于纳米颗粒的肽的免疫反应的诱导。capo4纳米颗粒既可以被用作佐剂,也可以被用作药物递送载体。
126.纳米颗粒可以是金纳米颗粒。金纳米颗粒是本领域已知的,并且特别描述于wo 2002/32404、wo 2006/037979、wo 2007/122388、wo 2007/015105和wo 2013/034726中。连接至每个肽的金纳米颗粒可以是在wo 2002/32404、wo 2006/037979、wo 2007/122388、wo 2007/015105和wo 2013/034726中的任何一个中描述的金纳米颗粒。
127.金纳米颗粒包括包含金(au)原子的核。核可以进一步包含一种或多种fe、cu或gd原子。核可以由金合金形成,例如au/fe、au/cu、au/gd、au/fe/cu、au/fe/gd或au/fe/cu/gd。核的原子总数可以是100至500个原子,例如150至450、200至400或250至350个原子。金纳米颗粒可以具有1至100、20至90、30至80、40至70或50至60 nm的平均直径。优选地,金纳米颗粒的平均直径为20至40 nm。
128.纳米颗粒可以包含包覆有α-半乳糖和/或β-glcnac的表面。例如,纳米颗粒可以包
含被α-半乳糖和/或β-glcnac钝化的表面。在这种情况下,纳米颗粒可以例如是包含核的纳米颗粒,所述核包括金属和/或半导体原子。例如,纳米颗粒可以是金纳米颗粒。β-glcnac是一种细菌病原体相关分子模式(pamp),能够激活抗原呈递细胞。以这种方式,包含被β-glcnac包覆或钝化的表面的纳米颗粒可以非特异性地刺激免疫反应。因此,包含seq id no:1至23所示的一个或多个cd8 + t细胞表位或其变体的黄病毒肽与这种纳米颗粒的连接可以改善由向个体施用本发明的疫苗组合物引发的免疫反应。
129.除肽以外的一种或多种配体可以被连接至纳米颗粒,其可以是上述纳米颗粒的任何类型。配体可以形成“冠状物(corona)”,可以部分或完全覆盖核的表面的层或涂层。冠状物可以被认为是围绕或部分围绕纳米颗粒核的有机层。冠状物可以提供或参与钝化纳米颗粒的核。因此,在某些情况下,冠状物可以是使核稳定的足够完整的涂层。冠状物可以促进本发明的纳米颗粒的溶解度(例如水溶性)。
130.纳米颗粒可以包含至少10个、至少20个、至少30个、至少40个或至少50个配体。配体可以包括一种或多种肽、蛋白质结构域、核酸分子、脂质基团、碳水化合物基团、阴离子基团或阳离子基团、糖脂和/或糖蛋白。碳水化合物基团可以是多糖、寡糖或单糖基团(例如葡萄糖)。一种或多种配体可以是非自身组分,由于其与致病组分的相似性,使得纳米颗粒更可能被抗原呈递细胞吸收。例如,一种或多种配体可以包含碳水化合物部分(例如细菌碳水化合物部分)、表面活性剂部分和/或谷胱甘肽部分。示例性配体包括巯基化葡萄糖、n-乙酰基葡糖胺(glcnac)、谷胱甘肽、2'-硫代乙基-β-d-吡喃葡萄糖苷和2'-硫代乙基-d-吡喃葡萄糖苷。优选的配体包括糖缀合物,其形成糖纳米颗粒。
131.接头可以促进配体与核的连接。接头可以包含巯基、烷基、二醇基或肽基。例如,接头可以包含c2-c15烷基和/或c2-c15二醇。接头可以包含能够共价连接至核的含硫基团、含氨基基团、含磷酸盐基团或含氧基团。替代地,配体可以例如通过配体中包含的含硫基团、含氨基基团、含磷酸盐基团或含氧基团直接连接至核。
132.连接至纳米颗粒所述肽可以在其n末端连接于纳米颗粒。通常,肽连接至纳米颗粒的核,但连接至冠状物或配体也是可能的。
133.所述肽可以例如通过使肽中的含硫基团、含氨基基团、含磷酸盐基团或含氧基团中的原子与纳米颗粒或其核中的原子共价键合而与纳米颗粒直接连接。
134.接头可以被用于将肽连接至纳米颗粒。接头可以包含能够共价连接至核中的原子的含硫基团、含氨基基团、含磷酸盐基团或含氧基团。例如,接头可以包含硫醇基、烷基、二醇基或肽基。
135.接头可以包含肽部分和非肽部分。肽部分可以包含序列x1x2z1,其中x1是选自a和g的氨基酸;x2是选自a和g的氨基酸;以及z1是选自y和f的氨基酸。肽部分可以包含序列aay或flaay(seq id no:44)。接头的肽部分可以与肽的n-末端连接。接头的非肽部分可以包含c2-c15烷基和/或c2-c15二醇,例如硫乙基(thioethyl group)或硫丙基(thiopropyl group)。
136.接头可以是(i)hs-(ch2)
2-conh-aay;(ii)hs-(ch2)
2-conh-laay(seq id no: 43);(iii)hs-(ch2)
3-conh-aay;(iv)hs-(ch2)
3-conh-flaay(seq id no:44);(v)hs-(ch2)
10-(ch2och2)
7-conh-aay;以及(vi)hs-(ch2)
10-(ch2och2)
7-conh-flaay(seq id no:
44)。在这种情况下,接头的非肽部分的硫醇基将接头连接至核。
137.用于将肽连接至纳米颗粒的其他合适的接头是本领域已知的,并且可以被本领域技术人员容易地鉴定和实施。
138.当疫苗组合物包含多于一种的肽时,两种或更多种(例如三种或更多种、四种或更多种、五种或更多种、十种或更多种或二十种或更多种)的肽可以连接至同一纳米颗粒。两种或更多种(例如三种或更多种、四种或更多种、五种或更多种、十种或更多种或二十种或更多种)的肽可以分别连接至不同的纳米颗粒。肽所连接的纳米颗粒可以是相同类型的纳米颗粒。例如,每一种肽可以连接至金纳米颗粒。每一种肽可以连接至capo4纳米颗粒。肽所连接的纳米颗粒可以是不同类型的纳米颗粒。例如,一种肽可以连接至金纳米颗粒,而另一种肽可以连接至capo4纳米颗粒。
139.多核苷酸疫苗本发明提供一种疫苗组合物,其包含编码根据权利要求1的肽或能够与t细胞受体结合的肽的多核苷酸,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合。
140.所述疫苗组合物可以包含编码两种或更多种本发明的肽的多核苷酸,每一种肽包含选自seq id nos:1至34或其变体的不同的序列。
141.所述疫苗组合物可以包含编码两种或更多种肽的多核苷酸,每一种肽能够与不同的t细胞受体结合,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合,其中每一种不同的t细胞受体能够与选自seq id nos:1至34或其变体的不同的序列结合。
142.所述疫苗组合物可以包含两种或更多种多核苷酸,每一种编码本发明的肽,其中每一种肽包含选自seq id nos:1至34或其变体的不同的序列。
143.所述疫苗组合物可以包含两种或更多种多核苷酸,每一种编码能够与t细胞受体结合的肽,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合,其中每一种肽能够与不同的t细胞受体结合,所述t细胞受体能够与包含seq id nos:1至34中的任何一个或其变体的肽结合,并且每一种不同的t细胞受体能够与选自seq id nos:1至34或其变体的不同的序列结合。
144.所述多核苷酸可以是dna。所述多核苷酸可以是rna。例如,所述多核苷酸可以是mrna。
145.药物、治疗方法和治疗用途本发明提供了一种预防或治疗冠状病毒感染的方法,所述方法包含将本发明的疫苗组合物施用于感染了冠状病毒或有感染冠状病毒风险的个体。本发明还提供了用于预防或治疗个体中冠状病毒感染的方法的本发明的疫苗组合物。
146.冠状病毒感染可以是例如与人类流行病或大流行病相关的冠状病毒感染。冠状病毒感染可以是例如人畜共患的冠状病毒感染。冠状病毒感染可以是例如betacoronavirus属的成员的感染。冠状病毒可以是例如sarbecoronavirus亚属的成员的感染。冠状病毒感染可以是例如sars冠状病毒感染或sars冠状病毒2感染。
147.疫苗组合物可以作为药物组合物提供。所述药物组合物优选包含药学上可接受的载体或稀释剂。可以使用任何合适的方法来配制所述药物组合物。使用标准的药学上可接
受的载体和/或赋形剂配制细胞,可以使用药学领域中的常规方法进行。制剂的确切性质将取决于几个因素,包括要施用的细胞和所需的施用途径。合适类型的制剂在remington's pharmaceutical sciences, 19th edition, mack publishing company, eastern pennsylvania, usa中有完整描述。
148.疫苗组合物或药物组合物可以通过任何途径施用。合适的途径包括但不限于静脉内、肌内、腹膜内、皮下、皮内、透皮和口服/颊途径。
149.组合物可以与生理上可接受的载体或稀释剂一起制备。通常,此类组合物被制备为肽和/或肽连接的纳米颗粒的液体悬浮液。可以将肽和/或肽连接的纳米颗粒与药学上可接受的并且与活性成分相容的赋形剂混合。合适的赋形剂例如是水、盐水、右旋糖、甘油等及其组合。
150.另外,如果需要,药物组合物可以包含少量的辅助物质,例如湿润剂或乳化剂和/或ph缓冲剂。
151.以与剂型相容的方式和治疗上有效的量施用肽或肽连接的纳米颗粒。施用量取决于要治疗的对象,要治疗的疾病以及对象的免疫系统的能力。所需施用的纳米颗粒的精确量可能取决于从业者的判断,并且可能是每个受试者所特有的。
152.可以将任何合适数量的肽或肽连接的纳米颗粒施用于对象。例如,患者的每千克可以施用至少或大约0.2
×
106、0.25
×
106、0.5
×
106、1.5
×
106、4.0
×
106或5.0
×
106的肽或肽连接的纳米颗粒。例如,可以施用至少或大约105、106、107、108、109个肽或肽连接的纳米颗粒。作为指导,要施用的肽或肽连接的纳米颗粒的数量可以为105至109个,优选为106至108个。
153.实施例1说明如下所述,冠状病毒肽被连接至金纳米颗粒。
154.选择了8种肽:p77、p81、p83、p86、p92、p96、p99和p100,如表4所示。
155.表4
肽序列seqidno蛋白质hla类型对应于p77aayrlnevaknl35sa2、a203/a2seqidno:21+n-末端aay(接头的肽部分)p81aayllnkhidayk36na3、a11、a31seqidno:1+n-末端aay(接头的肽部分)p83aayqfapsasaff37na24seqidno:19+n-末端aay(接头的肽部分)p86aayvtpsgtwlty38na29seqidno:28+n-末端aay接头的肽部分)p92aayapsasaffgm39nb7、b35seqidno:2+n-末端aay(接头的肽部分)p96aaytpsgtwlty40nb35、b53、a29seqidno:27+n-末端aay(接头的肽部分)p99aaymevtpsgtw41nb44seqidno:16+n-末端aay(接头的肽部分)p100aayllldrlnql42na2、a203/a2seqidno:14+n-末端aay(接头的肽部分)
本实验的目的是在4 mg au规模的测试gnp em009-062-01的基础上,为毒理学研究制备100 mg au规模的批次。总的肽装载从每个np 5eq开始(估计为每100 au原子/np),用于配体交换。
156.方法
计算表5关注8种肽的dmso溶液的制备。表5列出了假设多肽含量/纯度为90%的情况下,加入的dmso的称量出来的量和体积,以产生1 mm的库(stock)。肽定量是有问题的,虽然这些肽的肽纯度被引用,但没有给出"肽含量",这些肽的含量有时可以低至50%,因此我们使用90%作为估计值,然后再进行内部hplc定量。
157.表51 ml基础gnp重1.003 g,所以100 mg au =1.003*(100/3.193)=31.4 g,为了准确起见,基础颗粒被称重处理。采取的实际体积是基于以下计算:100 mg au = 505
ꢀµ
mole au = 5.05
ꢀµ
mole np,以5倍过量肽/np = 25.25
ꢀµ
mole总肽,但有8种肽,所以 = 3.16
ꢀµ
mole
每一种肽。
158.在层流净化罩(laf)中对肽进行称重和溶解,使用新鲜密封的瓶装dmso进行溶解。用hplc检测上述肽库。例如,对于p77,我们得到的auc(根据tyr或tryp残基在278 nm处的吸光度定义)面积为50.1,而不是预期的70。肽不是1 mm,而是0.716 mm,因此要得到3.16
ꢀµ
mole的p77,我们需要4.43 ml,如下表所示。一些肽库具有二硫化物肽。这些被忽略了,因为只有硫醇肽面积被定量。
159.用于配体交换的使用的8种肽的dmso溶液实际体积在下面的表6中给出。
160.表6步骤在50 ml无菌falcon管中称取31.4 g chemcon 基础gnp。将所有8种肽的dmso溶液一起加入250 ml的玻璃圆底烧瓶中。然后加入chemcon tox 基础gnp并短暂混合,对容器进行氮气冲洗并密封。该配体交换溶液混合物在300 rpm、30℃的水浴中保持搅拌3小时。
161.3小时后,将深棕色的gnp溶液浓缩在15 ml 10kda amicon管(x 8)中,然后用无菌“用于注射的水”清洗,所有的添加都在laf中进行(x5、4000 g,每次离心8分钟,amicon装置中dmso保持在15%以下)。将gnp溶液从amicon管中收集到12个1.5 ml的eppendorf管中,然后在17g下离心2分钟以去除任何聚集物。将每个eppendorf管的上清液合并,并通过两个0.2
ꢀµ
m的无菌nalgene注射器过滤器过滤(每个过滤器约5ml gnp溶液)。最终的无菌gnp溶液(em009-064-01)为10 ml,然后将其保存在4℃。从该最终的gnp溶液中取出200
ꢀµ
l,单独保存用于分析。
162.人们注意到,在amicon管膜上有一些gnp材料,并且在对主要产物以17 kg进行最
后硬旋2分钟后,在每个eppendorf管的底部发现了沉淀物。后来的调查显示,这些沉淀的gnp可以重新悬浮在0.2 m的碳酸盐缓冲液(cb ph 10.22)中。所有从amicon和eppendorf管中沉淀的gnp被重新悬浮在0.2 m碳酸盐缓冲液(ph 10.22)中,并浓缩在来自前一天的相同的8支amicon管中,然后用0.2 m cb再洗一次,接着用水清洗(x5,4000 g,每次离心8分钟)。在amicon管中几乎没有观察到gnp。以17 kg离心2分钟后(没有观察到沉淀),该gnp溶液(em009-064-02)为2.7 ml并被保存在4℃用于进一步分析。从下文可以看出,主要的无菌预处理的au产量为62.6%,其中24.9%以不溶性聚集物损失。为了溶解聚集的材料并大大增加产量,可以使用0.2 m的碳酸盐缓冲液(ph10.22)在水洗前冲洗。
163.em009-064-01:来自大毒理学批次的上清液gnp溶液。
164.em009-064-02:来自主要的毒理学批次的用0.2 m cb(ph 10.22)处理后的沉淀的gnp。
165.em009-064-03:em0090-64-01(50
ꢀµ
l)和02(13.52
ꢀµ
l)的试验混合物。
166.分析金测定表7显示了金测定的结果。
167.表7吸收光谱图1显示了chencontox base gnp、em009-064-01、em009-064-02和em009-064-03的吸收光谱。
168.在chemcon tox base gnp、em009-064-01、02和03批次中,在520 nm处没有看到质谱带。
169.dlsdls结果显示在图2中,并总结如下。
170.对于chemcontox base gnp,尺寸=3.77 nm(n = 3),sd =
ꢀ±
1.22 nm。对于em009-064-01,尺寸=6.08 nm(n = 3),sd =
ꢀ±ꢀ
2.62 nm。对于em009-064-02,尺寸 = 4.77 nm (n = 3),sd =
ꢀ±ꢀ
1.21 nm。对于em009-064-03,尺寸=4.75 nm (n = 3),sd =
ꢀ±ꢀ
1.05 nm。
171.纳米颗粒400 nm的hplc该方法概述于图3中。样品制备见下表8。
172.表8
对于每个批次,16
ꢀµ
g的au是在40
ꢀµ
l的水中。在hplc中,10
ꢀµ
l的该gnp溶液被注入到柱子中,这使得每个批次样品每次注入4
ꢀµ
g au。
173.hplc结果显示所有三个样品都有优秀的肽结合率(》96%)。em009-064-01没有任何肽的gnp是3.4%。em009-064-02没有任何肽的gnp是0%。em009-064-03:没有任何肽的gnp是2.2%。
174.lc-ms肽定量样品制备见下表9。
175.表9对于每个批次,25
ꢀµ
g的au与0.1 m tcep在40℃下孵育4小时,然后用dmso将其加满至100
ꢀµ
l。在lc-ms上,32
ꢀµ
l的gnp溶液被注入到柱中,这使得每个批次每次注入8
ꢀµ
g au。
176.结果显示在图4中。
177.表10显示了所有3个批次的单独的肽装载。
178.表10总结两个批次的颗粒尺寸都很好。然而,em009-064-01批次(上清液gnp溶液)比em009-064-02(用cb处理的沉淀gnp)的尺寸略大。在520 nm处,在三个批次中都没有观察到的质谱带。
179.整个gnp产物的hplc显示完全没有任何肽的最小的gnp《4%。em009-064-02 hplc色谱图中的大的单峰表明该批次具有更高的疏水性肽(p92和/或p100)的装载。可能这就是为
什么该批次在amicon清洗过程中从水溶液中沉淀。
180.em009-064-01:总的8条肽装载为4.2 eq(开始时为5 eq)。lc-ms显示p81和p77具有略高的装载,而p86和p83具有略低于预期的装载。
181.em009-064-02:总的8条肽装载为9.4eq(开始时为5 eq)。lc-ms显示p77和p83具有略低的装载,而p100具有非常高的装载,与其他肽相比几乎是双倍。p100是非常疏水的,如此高的装载,解释了为什么在em009-064-01纯化过程中,该批次从水洗中沉淀下来。然而,在用0.2 m cb洗涤后,该沉淀的gnp又能够再次被重新悬浮在水溶液中。该批次是在非无菌条件下溶解的,并且不打算与主要的em009-064-01产物混合。
182.em009-064-03:50
ꢀµ
l em009-064-01与13.52
ꢀµ
l em009-064-02混合。最终肽装载为4.89。p83装载仍然有点低,p100装载仍然很高,但是与em009-064-01和02批次相比,该混合的批次显示出更好的整体肽装载结果。
183.em009-064-01具有大约62.6 mg au,em009-064-02具有大约24.9 mg au。如果将两个批次组合在一起,将会得到87.5%金回收率。今后在amicon上进行最终的gnp纯化时,应使用0.2 m的cb来保持gnp在溶液中,以增加最终的黄金产量并提高肽比例/水平。
184.就产物数量而言,10 ml的材料以6.3 mg/ml au和1.34
ꢀµ
mole/ml的总肽含量(即13.4
ꢀµ
mole的总肽)提供超过1600个剂量的材料,每一种肽约1 nmole。
185.参考文献1. he y、zhou y、wu h、kou z、liu s、jiang s. mapping of antigenic sites on the nucleocapsid protein of the severe acute respiratory syndrome coronavirus. j clin microbiol. 2004 nov;42(11):5309-14. doi: 10.1128/jcm.42.11.5309-5314.2004.2. liu sj、leng ch、lien sp、et al. immunological characterizations of the nucleocapsid protein based sars vaccine candidates. vaccine. 2006;24(16):3100-3108. doi:10.1016/j.vaccine.2006.01.058.3. zhao j、huang q、wang w、zhang y、lv p、gao xm. identification and characterization of dominant helper t-cell epitopes in the nucleocapsid protein of severe acute respiratory syndrome coronavirus. j virol. 2007;81(11):6079-6088. doi:10.1128/jvi.02568-064. ahmed sf、quadeer aa、mckay mr. preliminary identification of potential vaccine targets for the covid-19 coronavirus (sars-cov-2) based on sars-cov immunological studies. viruses. 2020; 12(3):254. https://doi.org/10.3390/v12030254。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1