马赛替尼用于治疗阿尔茨海默病的制作方法
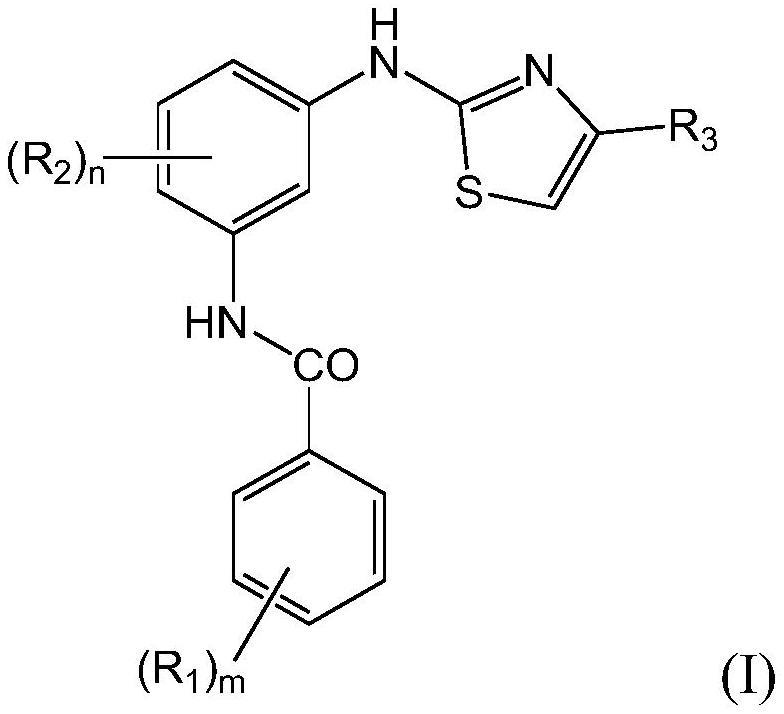
发明领域本发明涉及治疗有需要的患者的阿尔茨海默病(alzheimer’s disease),特别是治疗轻型阿尔茨海默病(less severe alzheimer’s disease)和/或早期阿尔茨海默病(early-stage alzheimer’s disease)或阿尔茨海默病性痴呆(alzheimer’s dementia)。
背景技术:
0、发明背景
1、阿尔茨海默病(ad)是老年人痴呆的最常见原因,尤其是在西方国家,据估计,该病估计占所有痴呆病例的约60%-70%。痴呆描述了一种以记忆障碍(dysmnesia)(即记忆障碍(memory disorder))、智力衰退、人格改变和行为异常为特征的综合征。这些症状最终导致社交和职业衰退。
2、阿尔茨海默病是一种不可逆转的神经退行性疾病,导致记忆和认知能力的致残性损害。阿尔茨海默病始于轻度认知问题,例如记忆丧失,最终发展到不再可能独立生活的阶段。患阿尔茨海默病的主要危险因素是年龄,其中65岁以后,患这种疾病的可能性大约每五年就会增加一倍。85岁及以上的所有个体中,约有三分之一可能患有阿尔茨海默病。家族史也会增加患这种疾病的风险,这可能归因于遗传或环境因素。
3、在大脑中观察到的阿尔茨海默病的两个组织病理学特征是在神经元之间形成的淀粉样斑(也称为神经炎斑或老年斑)和在神经元内形成的神经原纤维缠结。淀粉样斑是由淀粉样前体蛋白裂解产生的β-淀粉样肽的聚集引起的。神经原纤维缠结主要是由于磷酸化蛋白tau(τ)的异常积累造成的,该蛋白连接在一起形成细丝。淀粉样斑的沉积和神经原纤维缠结的形成被认为与该疾病的病因、发展和病程密切相关。
4、流行病学研究的荟萃分析表明,在美国和欧洲有500万至1000万人患有阿尔茨海默病。阿尔茨海默病已成为美国所有死亡病例的第六大原因,也是65岁以上美国人的第五大死亡原因。据估计,欧盟有超过300万痴呆患者,其中约70%患有阿尔茨海默病。据预测,到2050年,全球阿尔茨海默病患病率将翻两番,达到1亿多人,届时全球每85个人中就有1人患有该病。其中超过40%的病例属于需要像疗养院护理那样的高度关注的晚期阿尔茨海默病。
5、目前,批准的用于阿尔茨海默病的治疗由两种类型的药物组成:胆碱酯酶抑制剂(如多奈哌齐、利凡斯的明和加兰他敏(galantamine))和nmda(n-甲基-d-天冬氨酸)受体拮抗剂(美金刚(memantine))。胆碱酯酶抑制剂通过抑制突触间隙的乙酰胆碱酯酶来增加胆碱能传递。美金刚是一种电压依赖性、中等亲和力、非竞争性nmda受体拮抗剂。它调节病理性升高的谷氨酸补给水平的影响,病理性升高的谷氨酸补给水平可导致神经元功能障碍。目前批准的治疗已显示出对阿尔茨海默病的一些认知和非认知症状的功效。然而,它们的功效是有限的,并且可能会随着时间的推移而减弱。
6、因此,仍然需要针对阿尔茨海默病的有效治疗。具体地,仍然需要对轻型阿尔茨海默病和/或早期阿尔茨海默病或阿尔茨海默病性痴呆的有效治疗。
7、因此,本发明涉及2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物,其用于治疗有需要的患者、特别是本文定义的患有轻型阿尔茨海默病和/或早期阿尔茨海默病或阿尔茨海默病性痴呆的患者的阿尔茨海默病。
技术实现思路
1、本发明涉及马赛替尼或其药学上可接受的盐或溶剂化物,其用于治疗有需要的患者的阿尔茨海默病,其中在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前,该患有阿尔茨海默病的患者具有等于或大于、优选大于32的阿尔茨海默病合作研究-日常生活活动(adcs-adl)评分,和/或具有等于或大于13的简易精神状态检查(mmse)评分,和/或从诊断到用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始的时间等于或少于5年,和/或具有等于或小于40的阿尔茨海默病评定量表-认知分量表(adas-cog)评分。
2、在一个实施方案中,患有阿尔茨海默病的患者在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前具有等于或大于、优选大于32、35、38、39、41、47、50或55的adcs-adl评分。在一个实施方案中,患有阿尔茨海默病的患者在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前具有大于38或50的adcs-adl评分。在一个实施方案中,患有阿尔茨海默病的患者在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前具有大于39或55的adcs-adl评分。
3、在一个实施方案中,在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前,患有阿尔茨海默病的患者具有等于或大于13、14、15、16或17,优选等于或大于14的mmse评分。在一个实施方案中,患有阿尔茨海默病的患者在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前具有范围为21至25的mmse评分。
4、在一个实施方案中,患有阿尔茨海默病的患者从诊断到用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始的时间等于或少于5年、4年、3年或2年,优选等于或少于3年。
5、在一个实施方案中,患有阿尔茨海默病的患者在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前具有等于或小于40、35、32或25的adas-cog评分。在一个实施方案中,患有阿尔茨海默病的患者在用马赛替尼或其药学上可接受的盐或溶剂化物治疗开始之前具有等于或小于35的adas-cog评分。
6、在一个实施方案中,马赛替尼的药学上可接受的盐是甲磺酸马赛替尼。
7、在一个实施方案中,马赛替尼或其药学上可接受的盐或溶剂化物以范围为约1至约12mg/kg/天(mg每千克体重每天)的剂量施用,优选以约3mg/kg/天、4.5mg/kg/天或6mg/kg/天的剂量施用。在一个实施方案中,马赛替尼或其药学上可接受的盐或溶剂化物在至少12周期间以约4.5mg/kg/天的初始剂量施用,然后以约6mg/kg/天的剂量施用,每次剂量递增都受到毒性控制。在一个实施方案中,马赛替尼或其药学上可接受的盐或溶剂化物用于口服施用。在一个实施方案中,马赛替尼或其药学上可接受的盐或溶剂化物以每日两次摄入的形式施用。
8、在一个实施方案中,马赛替尼或其药学上可接受的盐或溶剂化物与至少一种另外的药物活性剂一起施用。在一个实施方案中,至少一种另外的药物活性剂选自多奈哌齐、利凡斯的明、加兰他敏和美金刚。
9、定义
10、在本发明中,下列术语具有以下含义:
11、-数字前的“约”包括所述数字值的正或负10%或更少。应当理解,术语“约”所指的值本身也是具体且优选地公开的。
12、-如本文所用,“基线”是指用本文所述的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物开始治疗之前的时间。在一个实施方案中,“基线”对应于用本文所述的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物治疗开始之前的状态。例如,在一个实施方案中,基线评分是在用本文所述的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物治疗开始之前的评分。在一个实施方案中,“基线”对应于用本文所述的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物治疗开始时的状态。例如,在一个实施方案中,基线评分是在用本文所述的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物治疗开始时的评分。
13、“药学上可接受的赋形剂”或“药学上可接受的载体”是指当施用于患者时不产生不利、过敏或其他不良反应的赋形剂或载体。它包括任何和所有溶剂,例如分散介质、包衣剂、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂。药学上可接受的赋形剂或载体是指任何类型的无毒固体、半固体或液体填充剂、稀释剂、包封材料或配制助剂。对于人类施用,制剂应符合诸如fda(美国食品和药物管理局)或ema(欧洲药品管理局)的监管机构要求的无菌性、热原性、一般安全性和纯度标准。
14、“患者”是指患有阿尔茨海默病的人类受试者。在一个实施方案中,患者正在等待接受、或正在接受医疗护理或者曾经是/正在是/将是医疗程序的对象,或者在被监测阿尔茨海默病的发展。
15、如本文所用,“ad患者”是指患有阿尔茨海默病(ad)的患者。
16、“阿尔茨海默病进展(ad进展)中的“进展”是指在病程中症状随着时间的推移逐渐恶化,特别是记忆损害和/或认知损害逐渐恶化。例如,可以使用阿尔茨海默病评定量表-认知分量表(adas-cog)、阿尔茨海默病合作研究-日常生活活动(adcs-adl)量表和/或简易精神状态检查(mmse)来评估ad进展。
17、如本文所用,“评分的进展(progression of score)”,例如adas-cog评分的进展、adcs-adl评分的进展或mmse评分的进展,是指用于评估患有阿尔茨海默病的患者的评分(例如adas-cog评分、adcs-adl评分或mmse评分)随时间推移的变化。随着疾病的进展,评分可以增加(即,adas-cog评分)或降低(即,adcs-adl评分或mmse评分)。评分的进展可用于评估治疗的功效。因此,在一个实施方案中,评分的进展对应于基线时(即,治疗开始之前)的评分与治疗一旦开始后的评分(在治疗开始后的特定时间点测量的)之间的差值。评分随着时间的推移不存在差值表明ad患者没有疾病进展且状态稳定。对于adas-cog评分,小幅增加(或给定时间点与基线之间的差值为正)表明疾病进展有限。因此,adas-cog评分的增加越小(即,正差值越小),ad患者越稳定。因此,与治疗前同一时间段内adas-cog评分的进展相比,adas-cog评分的较小增加表明疾病进展减慢。相反地,adas-cog评分的降低(或给定时间点与基线之间的差值为负)表明ad患者没有疾病进展且有所改善。对于adcs-adl评分和/或mmse评分,小幅降低(或给定时间点与基线之间的差值为负)表明疾病进展有限。因此,adcs-adl评分和/或mmse评分的降低越小(即,负差值越小),ad患者越稳定。因此,与治疗前相同时间段内adcs-adl评分和/或mmse评分的进展相比,adcs-adl评分和/或mmse评分的较小降低表明疾病进展减慢。相反地,adcs-adl评分和/或mmse评分(或给定时间点与基线之间的差值为正)的增加表明ad患者没有疾病进展并且有所改善。
18、“治疗有效量”或“治疗有效剂量”是指本文定义的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物的量或浓度,其目的是在对需要治疗的患者不引起显著的负面或不良副作用的情况下,预防、减少或减慢(减轻)ad患者的记忆损害和/或认知损害。在一个实施方案中,治疗有效量或治疗有效剂量的目的是在对需要治疗的患者不引起显著的负面或不良副作用的情况下,产生以下至少之一:
19、-减慢阿尔茨海默病的进展,这对应于adas-cog评分随时间推移的增加减慢、adas-cog评分随时间推移的稳定性或adas-cog评分随时间推移的降低;
20、-减慢阿尔茨海默病的进展,这对应于adcs-adl评分随时间推移的降低减慢、adcs-adl评分随时间推移的稳定性或adcs-adl评分随时间推移的增加;和/或
21、-减慢阿尔茨海默病的进展,这对应于mmse评分随时间推移的降低减慢、mmse评分随时间推移的稳定性或mmse评分随时间推移的增加。
22、“治疗”是指治疗性治疗、预防性(或阻止性)治疗或治疗性治疗和预防性(或阻止性)治疗两者,其中目的是预防、减少或减慢(减轻)需要治疗的患者的阿尔茨海默病的一种或多种症状或表现。在一个实施方案中,根据本技术的治疗的目的是预防、减少或减慢(减轻)需要治疗的ad患者的记忆损害和/或认知损害。在一个实施方案中,根据本技术的治疗的目的是实现至少以下之一:
23、
24、-减慢阿尔茨海默病的进展,这对应于adas-cog评分随时间推移的增加减慢、adas-cog评分随时间推移的稳定性或adas-cog评分随时间推移的降低;
25、-减慢阿尔茨海默病的进展,这对应于adcs-adl评分随时间推移的降低减慢、adcs-adl评分随时间推移的稳定性或adcs-adl评分随时间推移的增加;和/或
26、-减慢阿尔茨海默病的进展,这对应于mmse评分随时间推移的降低减慢、mmse评分随时间推移的稳定性或mmse评分随时间推移的增加。
27、如本文所用,“从诊断到治疗开始的时间”是指首次临床明确诊断阿尔茨海默病的日期(表示为日/月/年、月/年或年)与用本文所述的2-氨基芳基噻唑衍生物,特别是马赛替尼,或其药学上可接受的盐或溶剂化物治疗开始的日期(表示为日/月/年、月/年或年)之间的时间长度。在一个实施方案中,阿尔茨海默病的诊断基于dsm-iv标准(精神疾病诊断和统计手册,第四版(diagnostic and statistical manual of mental disorders,4thedition))和/或nincds-adrda标准(国家神经和交流障碍和中风研究所,以及阿尔茨海默病和相关疾病协会(national institute of neurological and communicativedisorders and stroke,and alzheimer's disease and related disordersassociation))。在一个实施方案中,如果日期被表达为月/年(即,如果缺少有关日期的信息),则该日被认为是该月的最后一天。在一个实施方案中,如果日期被表示为年(即,如果缺少关于日和月的信息),则该月份被认为是六月,而该日被认为是该月的最后一天,即六月的最后一天。
- 还没有人留言评论。精彩留言会获得点赞!