一种基于FPGA的组织氧代谢检测装置及方法
一种基于fpga的组织氧代谢检测装置及方法
技术领域
1.本发明涉及生物信息检测工程技术领域,尤其涉及一种基于fpga的组织氧代谢检测装置及方法。
背景技术:
2.脑卒中、冠心病、外周动脉疾病等心脑血管类疾病严重威胁着人类生命健康,如今虽然心脑血管类疾病的救治率逐年增高,但此类疾病的复发风险依然很高,组织氧代谢参数(如组织氧代谢率、组织氧饱和度、组织血流等)的便携式检测对提升治疗效果和避免复发具有重要的意义。耗氧量占全身20%左右的脑组织,其氧储备却仅可用十几秒钟,一旦出现脑缺血或者缺氧,脑组织存储的能量3分钟左右便会耗竭,5分钟左右大脑皮层神经细胞开始死亡,出现不可逆损伤。因此,唯有便携式的组织氧代谢检测才能有助于及时发现异常生理信号,特别是应用于对有氧代谢有很强依赖性的脑组织时,对检测装置便携式的要求更高。值得注意的是,组织氧代谢源于对组织氧饱和度、组织血流两种参数变化的检测,因此,组织氧代谢检测装置需满足组织氧饱和度、组织血流两种参数的检测。
3.扩散相关光谱(diffuse correlation spectroscopy,dcs)技术利用近红外光谱照射到组织表面,通过计算组织表面散射光斑的光强自相关函数(g2(τ)),推算组织中红细胞的运动状态,可实现组织血流的定量检测;根据修正的朗伯比尔定律,多波长dcs可实现组织氧饱和度的定量检测。相比于现有临床组织血流、组织氧饱和度检测技术,dcs技术解决了激光多普勒、核磁共振等技术存在辐射、实时性连续性差、仪器笨重成本高、操作难度大等问题,具有无创、实时、长时间连续检测、成本低、易操作等优势。然而,多波长dcs通过增加通道数的方式实现组织氧饱和度、组织血流两种参数的检测,即需要增加光源和探测器的数目,从而导致其检测装置复杂度、成本的升高;此外,如仍通过上位机对采集的多波长数据进行分析处理,必然会带来检测装置体积大、操作难等问题,难以实现组织氧代谢的便携式检测。
4.基于此,本发明提供一种基于fpga的组织氧代谢检测装置及方法,可实现对组织氧代谢参数的便携式无创检测。利用多波长dcs技术以时分方式将不同波长光源照射与被测组织表面,通过fpga处理模块实现下位机探测器信号的分析处理,由fpga处理模块替代传统上位机完成多波长数据处理的全过程,在降低装置体积和成本的同时,为临床组织氧代谢检测提供一种便捷式的无创检测装置与方法。
技术实现要素:
5.本发明提供一种基于fpga的组织氧代谢检测装置及方法,旨在以实现心脑血管类重大疾病的早期检测为目标,提供一种便捷式的组织氧代谢检测解决方案。该组织氧代谢检测装置利用多波长dcs技术可实现深层组织氧代谢长时间、连续、实时的无创检测;以时分方式实现不同波长切换,通过fpga处理模块实现下位机探测器信号的处理与传输,极大地降低了装置的体积和成本,兼顾采样时间和便捷性,操作方便;测量探头与受试者接触面
积小,新生儿、孕妇、重症患者均适用,检测要求低、操作方便。
6.详见下文描述:
7.一种基于fpga的组织氧代谢检测装置及方法,所述装置包括:光源模块、探测器模块、fpga处理模块、测量探头和显示模块。各模块具体组成如下:
8.(1)光源模块由激光器电源控制器和近红外波段不同波长的长相干激光器组成。其中,激光器电源控制器,用于时分方式控制不同波长激光器的开关;不同波长激光器与光源光纤耦合,不同波长光束以时分方式照射至被测组织表面。
9.(2)探测器模块为雪崩式光电二极管,用于接收经光源照射后被测组织体表面的散射光斑强度,与探测光纤耦合,记录光子数并转换为电脉冲信号输出。
10.(3)fpga处理模块用于接收并处理探测器输出的电脉冲信号,计算得到组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)的实时数据。
11.(4)测量探头用于固定光源光纤与探测光纤,使光源光纤与探测光纤垂直于被测组织表面,可依据光源光纤和探测光纤的探头距离大小获取不同深度的组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)。
12.(5)显示模块用于显示组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)的实时变化。
13.进一步地,本发明所述光源为近红外波段不同波长的长相干激光器,功率大于50mw,相干长度为10m以上,波长范围为650nm-950nm,中心波长可选择为685nm、785nm和830nm,经多模光纤传导。
14.进一步地,本发明所述光源光纤为多模光纤,芯径为50μm、62.5μm、100μm或以上。
15.进一步地,本发明所述探测光纤为单模光纤,芯径为5μm或9μm。
16.进一步地,本发明所述fpga处理模块替代上位机完成数据处理的全过程,首先利用探测器输出的电脉冲信号计算得到多波长的光强数据和光强归一化自相关(g2(τ))数据;然后,根据修正的朗伯比尔定律,利用多波长光强数据转换为组织氧饱和度,依据dcs理论,利用光强归一化自相关(g2(τ))数据转换为组织血流;最后,由组织氧饱和度、组织血流计算得到组织氧代谢率。
17.本发明的创新性在于将组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)的计算由fpga处理模块实现,相比于通过上位机将探测器输出的电脉冲信号计算得到组织氧代谢参数,fpga处理模块直接完成由电脉冲信号到组织氧代谢参数的变换,可有效减少组织氧代谢检测装置体积,降低装置成本,有助于实现组织氧代谢的便捷式无创检测。
18.有益效果
19.本发明提供一种基于fpga的组织氧代谢检测装置及方法,可实现对组织氧代谢参数的便携式无创检测。多波长dcs通过增加通道数的方式实现组织氧饱和度、组织血流两种参数的检测,即需要增加光源和探测器的数目,从而导致其检测装置复杂度、成本的升高;此外,如仍通过上位机对采集的多波长数据进行分析处理,必然会带来检测装置体积大、操作难等问题,难以实现组织氧代谢的便携式检测。为解决上述问题,本发明利用多波长dcs技术以时分方式将不同波长光源照射与被测组织表面,通过fpga处理模块实现下位机探测器信号的分析处理,关键在于由fpga处理模块替代传统上位机完成多波长数据处理的全过
程,在降低装置成本和体积的同时,为临床组织氧代谢检测提供一种便捷式的无创检测装置与方法。此外,该组织氧代谢检测装置采用光纤耦合测量探头,与受试者接触面积小,新生儿、孕妇、重症患者均适用,检测要求低、操作方便。
附图说明
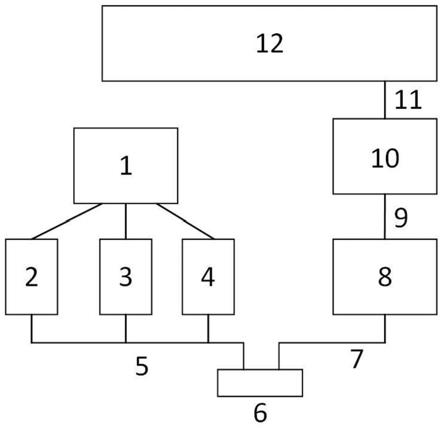
20.图1为基于fpga的组织氧代谢检测装置的系统示意图;
21.图2为基于fpga的组织氧代谢检测方法的流程图。
22.附图中,各标号所代表的部件列表如下:
23.1:激光器电源控制器
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2:激光器a
24.3:激光器b
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
4:激光器c
25.5:光源光纤
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
6:测量探头
26.7:探测光纤
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
8:探测器
27.9:第一数据线
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
10:fpga模块
28.11:第二数据线
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
12:显示模块
具体实施方式
29.为使本发明的目的、技术方案和优点更加清楚,以下结合具体实施例,并参照附图,对本发明实施方式作进一步地详细描述。
30.本发明提供一种基于fpga的组织氧代谢检测装置及方法,图1展示了本发明所述的一种基于fpga的组织氧代谢检测装置的系统示意图,该装置包括:
31.激光器电源控制器1,用于控制激光器a、激光器b和激光器c的开关,以时分方式实现不同光源的切换。
32.激光器a、激光器b和激光器c,其中心波长可在650nm-950nm之间进行选择,相干长度大于10m,功率大于50mw。本公开实施例中列举了激光器的中心波长为685nm、785nm和830nm,可根据实际需求选择其他波长,亦可以增加波长数目。
33.光源光纤5,用于将激光器光源的出射光经其传导后照射至被测组织体表面。
34.测量探头6,用于固定光源光纤5与探测光纤7,使其垂直于被测组织表面。
35.探测光纤7,用于将被测组织体表面的散射光斑传导至探测器8。
36.探测器8,用于接收经光源照射后被测组织体表面的散射光斑强度,记录光子数并转换为ttl电脉冲信号。
37.第一数据线9,用于探测器8与fpga处理模块10之间的数据传输。
38.fpga处理模块10,用于分析处理探测器输出的电脉冲信号,完成光强和光强归一化自相关(g2(τ))的计算,进一步计算组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)的实时数据。
39.第二数据线11,用于fpga处理模块10与显示模块12之间的数据传输。
40.显示模块12,用于实时显示组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)。
41.图2展示了本发明提供的一种基于fpga的组织氧代谢检测方法,利用图1所述装置可完成组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)的便携式无创检测。
42.具体步骤如下:
43.步骤一:测量探头固定于被测组织表面,确保光源光纤和探测光纤垂直入射与被测组织表面。
44.步骤二:为所述装置供电,保证激光器、探测器、显示模块等均已上电。打开激光器电源控制器开关,此时,将时分控制后的光束经光源光纤传导照射至所被测组织所需的位置点,雪崩式光电二极管通过测量探头探测被测组织表面的散射光斑强度,对该位置点处散射光子进行计数,并输出电脉冲信号。
45.步骤三:fpga处理模块接收步骤二中传输出的电脉冲信号并进行分析,处理得到不同波长下的光强和光强归一化自相关(g2(τ))数据。根据修正的朗伯比尔定律,利用多波长光强数据转换为组织氧饱和度;依据dcs理论,利用光强归一化自相关(g2(τ))数据转换为组织血流。然后,由组织氧饱和度和组织血流数据计算得到组织氧代谢率。至此,fpga处理模块已计算得到组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率),并将其数据传输至显示模块。
46.步骤四:显示模块接收得到的组织氧代谢参数(即,组织氧饱和度、组织血流、组织氧代谢率)并实时显示。
47.进一步,本发明所述一种基于fpga的组织氧代谢检测装置及方法,利用近红外光对组织血流变化的具体计算过程如下:
48.对于步骤三所得的电脉冲信号,即不同时刻的光强信号i(t),由fpga模块实现光强归一化自相关(g2(τ))计算,其公式为:
[0049][0050]
式中,i(t)代表t时刻探测的光强,τ为延迟时间,《》代表时间上取平均。
[0051]
db为布朗散射系数,依赖于相关函数g2(τ)的指数衰减率。
[0052]
血流因子(blood flow index,bfi)bfi≡αdb,其中α取值于0~1之间,代表运动的散射粒子占生物组织体内所有粒子的比例。
[0053]
血流(bf)与血流因子(bfi)的关系如下:
[0054]
bf=γbfi
[0055]
其中,bf为血流,单位为ml
·
100ml-1
·
min-1
;bfi为血流因子,单位为cm2/s;γ为比例常数,单位为(ml
·
100ml-1
·
min-1
)/(cm2/s)。
[0056]
相对血流(relative blood flow,rbf),即组织血流变化的计算公式如下:
[0057][0058]
其中,bf0与bfi0分别代表初始时刻的血流和血流因子。
[0059]
进一步,本发明所述一种基于fpga的组织氧代谢检测装置及方法,利用近红外光对组织氧饱和度变化的具体计算过程如下:
[0060]
对于步骤三所得的电脉冲信号,即不同时刻的不同波长的光强信号i(t),依据修正的朗伯比尔定律,由fpga模块实现含氧血红蛋白浓度和脱氧血红蛋白浓度变化计算公式如下:
[0061][0062]
其中,为氧合血红蛋白浓度变化,δc
hb
(t)为脱氧血红蛋白的浓度变化,分别代表氧合血红蛋白与脱氧血红蛋白在波长λ1和λ2下对应的摩尔消光系数,i(λ1,t)与i(λ1,t)分别代表在波长为λ1和λ2时刻为t时的光强,与分别代表波长λ1与λ2对应的路径差分因子。
[0063]
因此,组织氧饱和度的计算公式
[0064][0065]
可转换为:
[0066][0067]
式中,为氧合血红蛋白浓度,c
hb
为脱氧血红蛋白的浓度,与c
hb
(0)分别代表初始时刻(即t=0时)氧合血红蛋白浓度和脱氧血红蛋白的浓度。
[0068]
进一步,本发明所述一种基于fpga的组织氧代谢检测装置及方法,关于组织氧代谢率的计算,组织氧代谢率和相对氧摄取分数、组织血流之间的关系为:
[0069]
rmro2=roef
×
rbf
[0070]
式中,r代表相对变化量,即rmro2为相对氧代谢率,roef为相对氧摄取分数,rbf为相对血流。
[0071]
相对氧摄取分数roef为:
[0072][0073]
式中,sao2为动脉血氧饱和度,sao2(0)和sao2(t)分别代表初始时刻(即t=0时)和t时刻的动脉血氧饱和度,sto2(0)和sto2(t)分别代表初始时刻(即t=0时)和t时刻的组织氧饱和度。通常情况下,可假设:sao2=1,因此,相对氧摄取分数roef可表示为:
[0074][0075]
那么,可得相对组织氧代谢率(rmro2)为:
[0076][0077]
式中,sto2(0)和sto2(t)分别代表初始时刻(即t=0时)和t时刻的组织氧饱和度,rbf为相对血流。至此,式中变量均可通过测量计算得出。
[0078]
最后所应说明的是,虽然本发明参照当前的较佳实施方式进行了描述,但本领域的技术人员应能理解,上述较佳实施方式仅用来说明本发明,并非用来限定本发明的保护
范围,任何在本发明的精神和原则范围之内,所做的任何修饰、等效替换、改进等,均应包含在本发明的群里保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1