一种中草药贴剂的制作方法
1.本发明涉及药物领域,具体而言本发明涉及一种改善视力的中草药贴剂。
背景技术:
2.氧化应激的产生是由于机体受到内源性或外源性的伤害后,产生过多的自由基,释放出大量的活性氧自由基(ros)等氧化物质,而机体自身抗氧化的能力下降,不能清除蓄积过多的ros,致使氧化与抗氧化能力的失衡,机体的氧化反应远远超出抗氧化的清除能力。炎症因子参与炎症反应,其中,tnf-α和il-6是重要的炎症因子,tnf-α能激活中性粒细胞和淋巴细胞,使血管内皮细胞通透性增加,调节其他组织代谢活性并促使其他细胞因子的合成和释放,il-6能诱导b细胞分化和产生抗体,并诱导t细胞活化增殖、分化,参与机体的免疫应答,是炎性反应的促发剂等等。
3.氧化应激和炎症是导致多种疾病发生的重要因素,例如氧化应激会对眼睛造成损害,导致视力下降,尤其是对于青少年而言,由于学习压力大等因素,常常会用眼过度,氧化应激对眼睛造成损害会进一步加剧视力的减退,从而不利于青少年眼部的健康;再例如氧化应激和炎症导致皮肤疾病如皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹等等,严重影响患者的生活质量。然而,现有技术缺乏针对氧化应激和炎症治疗的有效药物,从而限制了氧化应激和炎症及其相关疾病的预防和治疗。
4.本领域需要开发一种有效治疗氧化应激和炎症及其相关疾病的药物。
技术实现要素:
5.本发明的目的在于提供一种有效治疗氧化应激和炎症及其相关疾病的中药材提取物。
6.本发明的第一方面提供了一种组合物,所述的组合物包括青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物和珍珠粉。
7.优选地,所述的提取物为干浸膏。
8.优选地,所述的提取物为干提取物。
9.优选地,所述的青葙子提取物包括醇水溶剂提取物。
10.优选地,所述的菊花提取物包括醇水溶剂提取物。
11.优选地,所述的山药提取物包括醇水溶剂提取物。
12.优选地,所述的车前子提取物包括醇水溶剂提取物。
13.优选地,所述的醇包括乙醇。
14.优选地,所述的醇水溶剂中,所述的醇的体积分数为50-70%,例如55-65%或60%。
15.优选地,所述的青葙子提取物通过以下方法制备:
16.将青葙子粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到青葙子提取物。
17.优选地,所述的菊花提取物通过以下方法制备:
18.将菊花粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到菊花提取物。
19.在本发明的一个优选例中,所述的枸杞子油通过以下方法制备:
20.将枸杞子油粉碎后,加入5-7重量倍的石油醚,38-42℃提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到枸杞子油。
21.优选地,所述的山药提取物通过以下方法制备:
22.将山药粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到山药提取物。
23.优选地,所述的车前子提取物通过以下方法制备:
24.将车前子粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到车前子提取物。
25.优选地,所述的珍珠粉通过以下方法制备:
26.将珍珠粉碎后,过1800-2200目筛,得到珍珠粉。
27.优选地,所述的珍珠粉通过以下方法制备:
28.将珍珠粉碎后,过2000目筛,得到珍珠粉。
29.优选地,所述的青葙子提取物的重量份为1-3重量份,较佳地1.5-2.5重量份,更佳地2重量份。
30.优选地,所述的菊花提取物的重量份为0.5-1.5重量份,较佳地0.8-1.2重量份,更佳地1重量份。
31.优选地,所述的枸杞子油的重量份为0.1-0.5重量份,较佳地0.2-0.4重量份,更佳地0.3重量份。
32.优选地,所述的山药提取物的重量份为0.08-0.5重量份,较佳地0.1-0.3重量份,更佳地0.2重量份。
33.优选地,所述的车前子提取物的重量份为0.1-0.5重量份,较佳地0.2-0.4重量份,更佳地0.3重量份。
34.优选地,所述的珍珠粉的重量份为0.01-0.05重量份,较佳地0.01-0.03重量份,更佳地0.02重量份。
35.优选地,所述的组合物包括:
36.组分用量(g)青葙子提取物1.5-2.5重量份菊花提取物0.8-1.2重量份枸杞子油0.2-0.4重量份山药提取物0.1-0.3重量份车前子提取物0.2-0.4重量份;和珍珠粉0.01-0.03重量份。
37.优选地,所述的组合物为药物组合物、食品组合物、保健品组合物或化妆品组合物。
38.优选地,所述的组合物还包括药学上、食品上、保健品上或化妆品上可接受的载
体。
39.优选地,所述组合物的剂型为口服制剂、注射制剂、外用制剂。
40.优选地,所述组合物的剂型为皮肤用贴剂。
41.优选地,所述皮肤用贴剂为脸部用皮肤贴剂、鼻部用皮肤贴剂、下肢用皮肤贴剂、上肢用皮肤贴剂、腹部用皮肤贴剂、胸部用皮肤贴剂或腰部用皮肤贴剂。
42.本发明第二方面,提供一种皮肤用贴剂,所述皮肤用贴剂包括如本发明第一方面所述的组合物。
43.优选地,所述的贴剂还包括压敏胶、增塑剂、保湿剂和经皮促渗剂中的一种或多种。
44.优选地,所述的经皮促渗剂包括氮酮。
45.优选地,所述的经皮促渗剂为2-4重量份,较佳地3重量份。
46.优选地,所述的增塑剂包括油酸单甘油酯。
47.优选地,所述的增塑剂为4-6重量份,较佳地5重量份。
48.优选地,所述的保湿剂包括甘油。
49.优选地,所述的保湿剂为4-6重量份,较佳地5重量份。
50.优选地,所述的压敏胶包括丙烯酸酯压敏胶。
51.优选地,所述的压敏胶为50-65重量份,较佳地60重量份。
52.优选地,所述皮肤用贴剂为脸部用皮肤贴剂、鼻部用皮肤贴剂、下肢用皮肤贴剂、上肢用皮肤贴剂、腹部用皮肤贴剂、胸部用皮肤贴剂或腰部用皮肤贴剂。
53.本发明第三方面,提供一种制备如本发明第二方面所述的皮肤用贴剂的方法,所述的方法包括:
54.将青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物、珍珠粉和乙醇充分混合后,加入丙烯酸酯压敏胶,在38-42℃下搅拌混合,加入氮酮、甘油和油酸单甘油酯,充分搅拌混合,静置脱气后,涂布于离型膜的表面,形成含药粘胶层,将含药粘胶层置于75-85℃烘箱中干燥后取出,压覆背衬层来贴附离型膜,得到皮肤用贴剂.
55.本发明第四方面,提供如一种如本发明第一方面所述的组合物或如本发明第二方面所述的皮肤用贴剂的用途,用于制备制剂,所述的组合物或制剂用于选自下组的一种或多种用途:(i)降低氧自由基(ros)水平;(ii)预防和/或治疗氧化应激;(iii)预防和/或治疗氧化应激引起的疾病;(iv)降低炎症因子水平;(v)预防和/或治疗炎症;和/或(vi)预防和/或治疗炎症引起的疾病。
56.优选地,所述的制剂为药物制剂、食品、保健品或化妆品。
57.优选地,所述的制剂还包括药学上、食品上、保健品上或化妆品上可接受的载体。
58.优选地,所述制剂为口服制剂、注射制剂、外用制剂。
59.优选地,所述制剂为皮肤用贴剂。
60.优选地,所述皮肤用贴剂为脸部用皮肤贴剂、鼻部用皮肤贴剂、下肢用皮肤贴剂、上肢用皮肤贴剂、腹部用皮肤贴剂、胸部用皮肤贴剂或腰部用皮肤贴剂。
61.优选地,所述的皮肤包括皮肤组织。
62.优选地,所述的氧化应激包括皮肤氧化应激。
63.优选地,所述的氧化应激包括活性氧自由基(ros)升高导致的氧化应激。
64.优选地,所述的ros包括皮肤ros。
65.优选地,所述的氧化应激包括糖尿病并发的氧化应激。
66.优选地,所述的炎症包括皮肤炎症。
67.优选地,所述的炎症包括炎症因子引起的炎症。
68.优选地,所述的炎症因子包括皮肤炎症因子。
69.优选地,所述的炎症包括糖尿病并发的炎症。
70.优选地,所述的炎症因子选自下组:肿瘤坏死因子-α、白介素6,或其组合。
71.优选地,所述的氧化应激引起的疾病包括氧化应激升高引起的疾病。
72.优选地,所述的氧化应激引起的疾病选自下组:视力减退、视力模糊、皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹,或其组合。
73.优选地,所述的炎症引起的疾病包括炎症因子升高引起的疾病。
74.优选地,所述的炎症引起的疾病选自下组:视力减退、视力模糊、皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹,或其组合。
75.优选地,所述的组合物或制剂还用于改善青少年视力。
76.本发明第五方面,提供一种(i)降低氧自由基(ros)水平;(ii)预防和/或治疗氧化应激;(iii)预防和/或治疗氧化应激引起的疾病;(iv)降低炎症因子水平;(v)预防和/或治疗炎症;和/或(vi)预防和/或治疗炎症引起的疾病的方法,给予所需对象施用如给予所需对象施用如本发明第一方面所述的组合物或如本发明第二方面所述的皮肤用贴剂。
77.优选地,所述的对象包括人或非人哺乳动物。
78.在本发明范围内中,本发明的上述各技术特征和在下文中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。
具体实施方式
79.本发明开发了一种中药材提取物,所述的中药材提取物包括青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物和珍珠粉,所述的中药材提取物能够用于降低氧自由基(ros)水平和炎症因子水平,以及预防和治疗与氧自由基(ros)和炎症因子相关的疾病例如视力减退、皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹等等。
80.术语
81.如本文所用,术语“包括”、“包含”与“含有”可互换使用,不仅包括开放式定义,还包括半封闭式、和封闭式定义。换言之,所述术语包括了“由
……
构成”、“基本上由
……
构成”。
82.如本文所用,术语“60%(v/v)乙醇水溶液”是指乙醇的体积分数为60%的乙醇水溶液,例如,60%的乙醇水溶液通过60ml无水乙醇+40ml水混合配制。
83.在本发明中,术语“预防”表示预防疾病和/或它的附随症状的发作或者保护对象免于获得疾病的方法。
84.本发明所述的“治疗”包括延缓和终止疾病的进展,或消除疾病,并不需要100%抑制、消灭和逆转,例如,与不存在本发明所述的提取物相比,本发明提取物将氧化应激和炎症减轻、抑制和/或降低了例如至少约10%、至少约50%、或至少约80%或完全根除。
85.在本发明中,青葙子为苋科植物青葙celosia argentea l.的干燥成熟种子。
86.在本发明中,菊花为菊科植物菊chrysanthemum morifolium ramat.的干燥头状花序。
87.在本发明中,枸杞子为茄科植物宁夏枸杞lycium barbarum l.的干燥成熟果实。
88.在本发明中,山药为薯蓣科植物薯蓣dioscorea opposita thunb.的干燥根茎。
89.在本发明中,车前子为车前科植物车前plantago asiatica l.或平车前plantago depressa willd.的干燥成熟种子。
90.在本发明中,珍珠为珍珠贝科动物马氏珍珠贝pteria martensii(dunker)等双壳类动物受刺激形成的珍珠。
91.组合物
92.本发明提供一种组合物,所述的组合物包括青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物和珍珠粉。
93.本发明所述的提取物可以为醇水溶剂提取物。
94.在本发明所述的醇水溶剂提取物中,所述的醇包括乙醇。
95.在本发明的一个优选例中,所述的醇水溶剂中,所述的醇的体积分数为50-70%,例如55-65%或60%。
96.在本发明的一个优选例中,所述的青葙子提取物通过以下方法制备:
97.将青葙子粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到青葙子提取物。
98.在本发明的一个优选例中,所述的菊花提取物通过以下方法制备:
99.将菊花粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到菊花提取物。
100.在本发明的一个优选例中,所述的枸杞子油通过以下方法制备:
101.将枸杞子油粉碎后,加入5-7重量倍的石油醚,38-42℃提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到枸杞子油。
102.在本发明的一个优选例中,所述的山药提取物通过以下方法制备:
103.将山药粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到山药提取物。
104.在本发明的一个优选例中,所述的车前子提取物通过以下方法制备:
105.将车前子粉碎后,加入5-7重量倍的58-62%(v/v)乙醇水溶液,加热回流提取3.8-4.2h后,过滤,得到提取液,经旋转蒸发、干燥后,得到车前子提取物。
106.在本发明的一个优选例中,所述的珍珠粉通过以下方法制备:
107.将珍珠粉碎后,过1800-2200目筛,得到珍珠粉。
108.优选地,所述的青葙子提取物的重量份为1-3重量份,较佳地1.5-2.5重量份,更佳地2重量份。
109.优选地,所述的菊花提取物的重量份为0.5-1.5重量份,较佳地0.8-1.2重量份,更佳地1重量份。
110.优选地,所述的枸杞子油的重量份为0.1-0.5重量份,较佳地0.2-0.4重量份,更佳地0.3重量份。
85℃烘箱中干燥后取出,压覆背衬层来贴附离型膜,得到皮肤用贴剂.
135.用途
136.本发明还提供一种本发明所述的组合物、或本发明所述的皮肤用贴剂的用途,用于制备制剂,所述的制剂用于选自下组的一种或多种用途:(i)降低氧自由基(ros)水平;(ii)预防和/或治疗氧化应激;(iii)预防和/或治疗氧化应激引起的疾病;(iv)降低炎症因子水平;(v)预防和/或治疗炎症;和/或(vi)预防和/或治疗炎症引起的疾病。
137.本发明所述的制剂可以为药物制剂、食品、保健品或化妆品。所述的制剂还可以包括药学上、食品上、保健品上或化妆品上可接受的载体。
138.在本发明的一个优选例中,所述制剂为口服制剂、注射制剂、外用制剂。例如所述制剂为皮肤用贴剂。
139.代表性地,所述皮肤用贴剂为脸部用皮肤贴剂、鼻部用皮肤贴剂、下肢用皮肤贴剂、上肢用皮肤贴剂、腹部用皮肤贴剂、胸部用皮肤贴剂或腰部用皮肤贴剂。
140.在本发明的一个优选例中,所述的皮肤包括皮肤组织。
141.优选地,所述的氧化应激包括皮肤氧化应激。
142.在本发明的一个优选例中,所述的氧化应激包括活性氧自由基(ros)升高导致的氧化应激。
143.优选地,所述的ros包括皮肤ros。
144.在本发明的一个优选例中,所述的氧化应激包括糖尿病并发的氧化应激。
145.在本发明的一个优选例中,所述的炎症包括皮肤炎症。
146.在本发明的一个优选例中,所述的炎症包括炎症因子引起的炎症。
147.在本发明的一个优选例中,所述的炎症因子包括皮肤炎症因子。
148.在本发明的一个优选例中,所述的炎症包括糖尿病并发的炎症。
149.优选地,所述的炎症因子选自下组:肿瘤坏死因子-α、白介素6,或其组合。
150.在本发明的一个优选例中,所述的氧化应激引起的疾病包括氧化应激升高引起的疾病。
151.代表性地,所述的氧化应激引起的疾病选自下组:视力减退、视力模糊、皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹,或其组合。
152.在本发明的一个优选例中,所述的炎症引起的疾病包括炎症因子升高引起的疾病。
153.代表性地,所述的炎症引起的疾病选自下组:视力减退、视力模糊、皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹,或其组合。
154.本发明的优异技术效果包括:
155.1、本发明开发一种中药材提取物,所述的中药材提取物包括青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物和珍珠粉,所述的中药材提取物能够用于降低氧自由基(ros)水平和炎症因子水平,以及预防和治疗与氧自由基(ros)和炎症因子相关的疾病例如视力减退、视力模糊、皮肤衰老、皮肤损伤、皮肤黄斑、皮肤溃疡、皮肤感染、皮肤瘙痒、皮肤感觉异常、皮疹等等。
156.2、本发明所述的中药材提取物能够制备成皮肤用贴剂,方便使用,安全性高,患者顺应性强。
157.3、本发明所述的中药材提取物安全性高,副作用性小,成药性高。
158.下面结合具体实施例,进一步阐述本发明。应理解,以下具体实施例以本技术方案为前提,给出了详细的实施方式和具体操作过程,但本发明的保护范围并不限于本实施例。
159.实施例1中药材提取物组合及其抗氧化和抗炎的研究
160.1、中药材提取物的制备
161.1.1青葙子提取物的制备
162.将青葙子粉碎后,加入6重量倍的60%(v/v)乙醇水溶液,加热回流提取4h后,过滤,得到提取液,经旋转蒸发、干燥后,得到青葙子提取物。
163.1.2菊花提取物的制备
164.将菊花粉碎后,加入6重量倍的60%(v/v)乙醇水溶液,加热回流提取4h后,过滤,得到提取液,经旋转蒸发、干燥后,得到菊花提取物。
165.1.3枸杞子油的制备
166.将枸杞子粉碎后,加入6重量倍的石油醚,40℃提取4h后,过滤,得到提取液,经旋转蒸发、干燥后,得到枸杞子油。
167.1.4山药提取物的制备
168.将山药粉碎后,加入6重量倍的60%(v/v)乙醇水溶液,加热回流提取4h后,过滤,得到提取液,经旋转蒸发、干燥后,得到山药提取物。
169.1.5车前子提取物的制备
170.将车前子粉碎后,加入6重量倍的60%(v/v)乙醇水溶液,加热回流提取4h后,过滤,得到提取液,经旋转蒸发、干燥后,得到车前子提取物。
171.1.6珍珠粉的制备
172.将珍珠粉碎后,过2000目筛,得到珍珠粉。
173.2、贴剂的制备
174.2.1提取物贴剂1
175.提取物贴剂1的处方如下表1所示:
176.表1提取物贴剂1的处方
177.组分用量(g)青葙子提取物4.0枸杞子油0.3山药提取物0.2车前子提取物0.3珍珠粉0.02氮酮3.0乙醇25.0甘油5.0油酸单甘油酯5.0丙烯酸酯压敏胶60.0
178.制备方法:
179.将青葙子提取物、枸杞子油、山药提取物、车前子提取物、珍珠粉和乙醇充分混合
后,加入丙烯酸酯压敏胶,在40℃下搅拌混合,加入氮酮、甘油和油酸单甘油酯,充分搅拌混合,静置脱气后,涂布于离型膜的表面,形成含药粘胶层,将含药粘胶层置于80℃烘箱中干燥20min后取出,压覆背衬层来贴附离型膜,得到提取物贴剂1。
180.采用测厚仪测定提取物贴剂1的厚度,贴剂经分切后得到每片含有青葙子提取物4mg/cm2的贴剂,每片贴剂的尺寸规格是为2
×
2cm2。
181.2.2提取物贴剂2
182.提取物贴剂2的处方如下表2所示:
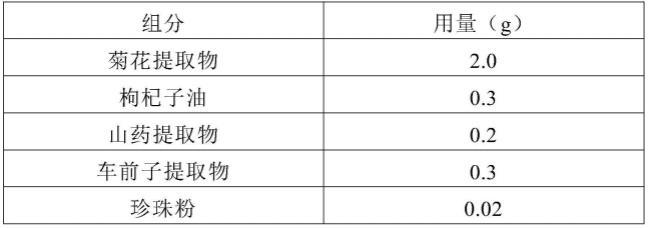
183.表2提取物贴剂2的处方
[0184][0185][0186]
制备方法:
[0187]
将菊花提取物、枸杞子油、山药提取物、车前子提取物、珍珠粉和乙醇充分混合后,加入丙烯酸酯压敏胶,在40℃下搅拌混合,加入氮酮、甘油和油酸单甘油酯,充分搅拌混合,静置脱气后,涂布于离型膜的表面,形成含药粘胶层,将含药粘胶层置于80℃烘箱中干燥20min后取出,压覆背衬层来贴附离型膜,得到提取物贴剂2。
[0188]
采用测厚仪测定提取物贴剂2的厚度,贴剂经分切后得到每片含有菊花提取物2mg/cm2的贴剂,每片贴剂的尺寸规格是为2
×
2cm2。
[0189]
2.3提取物贴剂3
[0190]
提取物贴剂3的处方如下表3所示:
[0191]
表3提取物贴剂3的处方
[0192]
组分用量(g)青葙子提取物2.0菊花提取物1.0枸杞子油0.3山药提取物0.2车前子提取物0.3珍珠粉0.02氮酮3.0乙醇25.0
甘油5.0油酸单甘油酯5.0丙烯酸酯压敏胶60.0
[0193]
制备方法:
[0194]
将青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物、珍珠粉和乙醇充分混合后,加入丙烯酸酯压敏胶,在40℃下搅拌混合,加入氮酮、甘油和油酸单甘油酯,充分搅拌混合,静置脱气后,涂布于离型膜的表面,形成含药粘胶层,将含药粘胶层置于80℃烘箱中干燥20min后取出,压覆背衬层来贴附离型膜,得到提取物贴剂3。
[0195]
采用测厚仪测定提取物贴剂3的厚度,贴剂经分切后得到每片含有青葙子提取物2mg/cm2和菊花提取物1mg/cm2的贴剂,每片贴剂的尺寸规格是为2
×
2cm2。
[0196]
2.4提取物贴剂4
[0197]
提取物贴剂4的处方如下表4所示:
[0198]
表4提取物贴剂4的处方
[0199]
组分用量(g)青葙子提取物0.5菊花提取物2.0枸杞子油0.3山药提取物0.2车前子提取物0.3珍珠粉0.02氮酮3.0乙醇25.0甘油5.0油酸单甘油酯5.0丙烯酸酯压敏胶60.0
[0200]
制备方法:
[0201]
将青葙子提取物、菊花提取物、枸杞子油、山药提取物、车前子提取物、珍珠粉和乙醇充分混合后,加入丙烯酸酯压敏胶,在40℃下搅拌混合,加入氮酮、甘油和油酸单甘油酯,充分搅拌混合,静置脱气后,涂布于离型膜的表面,形成含药粘胶层,将含药粘胶层置于80℃烘箱中干燥20min后取出,压覆背衬层来贴附离型膜,得到提取物贴剂4。
[0202]
采用测厚仪测定提取物贴剂4的厚度,贴剂经分切后得到每片含有青葙子提取物0.5mg/cm2和菊花提取物2mg/cm2的贴剂,每片贴剂的尺寸规格是为2
×
2cm2。
[0203]
2.5空白贴剂
[0204]
空白贴剂的处方如下表5所示:
[0205]
表5空白贴剂的处方
[0206]
组分用量(g)氮酮3.0乙醇25.0甘油5.0
油酸单甘油酯5.0丙烯酸酯压敏胶60.0
[0207]
制备方法:
[0208]
将乙醇和丙烯酸酯压敏胶混合后,在40℃下搅拌混合,加入氮酮、甘油和油酸单甘油酯,充分搅拌混合,静置脱气后,涂布于离型膜的表面,形成含药粘胶层,将含药粘胶层置于80℃烘箱中干燥20min后取出,压覆背衬层来贴附离型膜,得到空白贴剂。
[0209]
3、抗氧化和抗炎的研究
[0210]
3.1构建糖尿病大鼠模型
[0211]
通过将链脲佐菌素(stz)注射到正常健康雄性sd大鼠诱导糖尿病大鼠模型,诱导8天后,大鼠的血糖值维持在27.4
±
1.25mmol/l,显著高于正常大鼠的7.1
±
0.3mmol/l(p《0.05),且诱导的大鼠出现多饮、多食、多尿、体重降低、易激惹等糖尿病相关症状,表明成功构建糖尿病大鼠模型。
[0212]
3.2.实验方法
[0213]
将糖尿病大鼠随机分成模型组、实验组1、实验组2、实验组3和实验组4,每组各6只,并选择6只未经stz诱导的正常健康大鼠作为空白对照组。
[0214]
模型组、实验组1、实验组2、实验组3和实验组4的各组大鼠的同一背部皮肤部位给予1贴不同的贴剂,空白对照组的大鼠给予生理盐水(各组大鼠给药前,给药部位先经剔毛处理)),各组大鼠的给药如下:
[0215]
模型组:空白贴剂;
[0216]
实验组1:提取物贴剂1,其中,青葙子提取物的皮肤给药剂量为4mg/cm2;
[0217]
实验组2:提取物贴剂2,其中,菊花提取物的皮肤给药剂量为2mg/cm2;
[0218]
实验组3:提取物贴剂3,其中,青葙子提取物的皮肤给药剂量为2mg/cm2和菊花提取物的皮肤给药剂量为1mg/cm2;
[0219]
实验组4:提取物贴剂4,其中,青葙子提取物的皮肤给药剂量为0.5mg/cm2和菊花提取物的皮肤给药剂量为2mg/cm2;
[0220]
空白对照组:生理盐水。
[0221]
每天给药1次,连续给药14天后,取各组大鼠给药部位的皮肤组织,通过市售活性氧自由基(ros)检测试剂盒测定皮肤组织中的ros含量和通过elisa试剂盒测定皮肤组织中炎症因子tnf-α(肿瘤坏死因子-α)和il-6(白介素6)的表达。
[0222]
3.3实验结果
[0223]
3.3.1 ros含量测定
[0224]
各组大鼠皮肤组织中ros含量如表6所示:
[0225]
表6各组大鼠皮肤组织中ros含量(m
±
sd)
[0226]
组ros量(u/μg)空白对照组44.6
±
2.1模型组60.8
±
2.9实验组148.8
±
2.4**实验组253.7
±
2.5**实验组343.3
±
2.1**
实验组452.8
±
2.3*
[0227]
备注:与模型组比较,“*”为p<0.05,“**”为p<0.01。
[0228]
从表6中可以看出,模型组大鼠的皮肤组织中的ros含量显著高于空白对照组,表明糖尿病并发氧化应激。与模型组相比,中药材提取物能够降低皮肤组织中的ros含量,从而治疗糖尿病并发的氧化应激。
[0229]
3.3.2炎症因子的含量测定
[0230]
各组大鼠皮肤组织中的tnf-α(肿瘤坏死因子-α)和il-6(白介素6)的表达含量如表7所示:
[0231]
表7各组大鼠皮肤组织中ros含量(m
±
sd)
[0232]
组tnf-α(pg/μg)il-6(pg/μg)空白对照组17.5
±
1.164.2
±
3.1模型组28.7
±
1.3167.5
±
7.9实验组122.1
±
0.9**84.9
±
3.7*实验组224.9
±
1.2**113.2
±
5.3**实验组318.2
±
0.8**103.4
±
4.8*实验组424.3
±
1.0*107.9
±
5.2*
[0233]
备注:与模型组比较,“*”为p<0.05,“**”为p<0.01。
[0234]
从表7中可以看出,模型组大鼠的皮肤组织中的tnf-α和il-6含量显著高于空白对照组,表明糖尿病并发皮肤炎症。与模型组相比,中药材提取物能够降低皮肤组织中的tnf-α和il-6含量,从而治疗糖尿病并发的炎症。
[0235]
以上所述是本发明针对一种案例设计的实施方案,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下还可以作出若干改进,这些改进也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1